 |
|
||||||||||
|
Результаты регистрационных испытаний вакцины Эувакс В для профилактики гепатита В. Вакцина эуваксинструкция, хранение и показания к использованиюВ современном мире значительно возросли случаи заражения гепатитом В, что и поспособствовало разработке ряда лекарственных препаратов профилактического действия, среди которых присутствует и Эувакс вакцина. Эта вакцина представлена в виде высокоочищенных полипептидов (неинфекционного типа) поверхностного белка вируса гепатита В, которые подвергли адсорбированию на солях алюминия и консервированию тиомерсалом. Производитель вакцины – LG LifeScience, Франция, Корея. Цена варьируется в зависимости от города и страны. Показания и противопоказания к использованию Применение прививки Эувакс показано для предотвращения развития любого из подтипов вируса гепатита В у взрослых людей и детей в возрасте от 1 года.
Особенности воздействия препарата на беременных женщин не исследовались, поэтому доктора прописывают проведение вакцинации только в том случае, если положительные свойства препарата превышают отрицательные. Противопоказаний к выполнению прививки у матерей, кормящих грудью, не существует. Формы выпуска и особенности хранения Купить средство Эувакс можно в следующем виде:
Покупка вакцины возможна только в случае наличия специального медицинского рецепта, подписанного доктором, но в большинстве случаев медицинские учреждения сами занимаются закупками данного лекарственного средства. Эувакс необходимо хранить при температуре от 2 до 8 градусов. Использовать холодильник в качестве места хранения строго запрещено.  После того, как был вскрыт флакон, содержащий одну дозу вакцины, она больше не подлежит хранению. После того, как был вскрыт флакон, содержащий одну дозу вакцины, она больше не подлежит хранению.Флаконы, содержащие в себе несколько доз вакцины, могут храниться на протяжении 10 дней после вскрытия и только в том случае, если соблюдены такие условия:
Осуществлять забор каждой дозы препарата из флакона необходимо с помощью стерильного шприца.Препарат нужно сохранять в месте, недоступном для маленьких детей. Особенности проведения вакцинации Для препарата Эувакс инструкция по применению указывает на то, что перед введением препарата его нужно тщательно взболтать. Это объясняется тем, что в процессе хранения может возникнуть небольшой осадок. Средство Эувакс, согласно инструкции, вводят внутримышечно. Детям, входящим в возрастную группу менее трёх лет, введение осуществляется во внешнюю часть середины бедра, людям более старшего возраста препарат вводится в дельтовидную мышцу. Руководство к проведению вакцинации указывает на то, что, выполняя прививку, обязательно нужно убедиться, чтобы иголка не проникла в сосудистое русло. Строго запрещено осуществлять введение препарата в область ягодиц. Что касается дозировки препарата, то она определяется в зависимости от возраста пациента:
 Время проведения вакцинации напрямую зависит от того, входит ли человек в группу риска. Время проведения вакцинации напрямую зависит от того, входит ли человек в группу риска.Если человек не входит в группу риска, то прививку делают по следующее схеме:
Если же человек входит в группу риска, то и проведение вакцинации выполняется уже по другой схеме:
Отмечено, что Министерство здравоохранения считает, что выполнение ревакцинации является лишним, поскольку введение Эувакса гарантирует защиту от проникновения вируса гепатита В на срок около пятнадцати лет. Взаимодействие с другими препаратами и побочные эффекты Использование средства Эувакс, как и его аналогов Энджерикса и Имовакса, разрешено в один день с вакцинами, применяющимися для профилактики развития коклюша, столбняка, дифтерии, полиомиелита, паротита и кори. Обязательным условием в случае выполнения в один и тот же день нескольких профилактических прививок является введение вакцины в разные части тела. К тому же обязательно должны присутствовать разные шприцы. Что касается развития побочных эффектов, то выделяют следующие проявления:
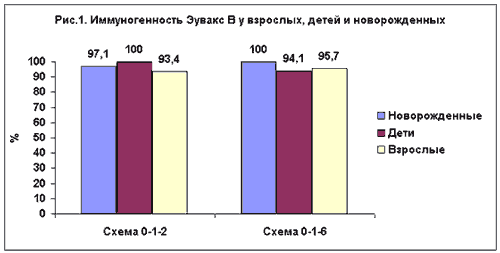
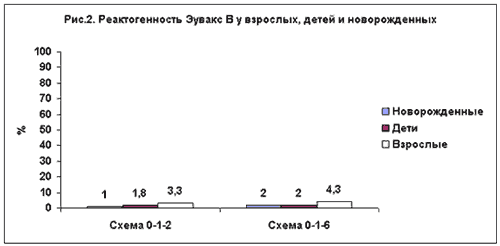
Согласно отзывам специалистов, за всё время применения препарата развития аллергических реакций не зафиксировано, присутствовало только 3 случая проявления повышенной чувствительности на компоненты препарата. Вирус гепатита В – это возбудитель, вызывающий заболевание, которое может нанести значительный вред печени, вплоть до развития цирроза и рака. Чтобы этого не допустить, следует заранее позаботиться о проведении вакцинации с помощью Эувакса или его аналогов. Рекомендуем прочитать: pechen1.ru Опыт применения вакцины Эувакс B для профилактики гепатита BОпыт применения вакцины "Эувакс B" для профилактики гепатита B С.Н. КузинНИИ вирусных препаратов им. О.Г. Анджапаридзе РАМН, Москва В России активная работа по широкой вакцинопрофилактике гепатита В (ГВ) началась в последние годы. В 1996 г. приказом Минздрава и Госкомсанэпиднадзора "О введении профилактических прививок против гепатита В" впервые вакцинация против ГВ была введена в национальный календарь прививок. К настоящему времени в России зарегистрированы несколько вакцин различных производителей, однако наибольшее распространение получили вакцины "Engerix B" фирмы "СмитКляйн Бичем" и "Эувакс В" фирмы "Авентис Пастер" (Франция). Последний препарат применяется в России уже два года, и в этой связи представляет большой интерес анализ первых итогов применения среди различных групп населения. Вакцина "Эувакс В" производится в Южной Корее компанией LG Chemical LTD наряду с группой фармацевтических препаратов, включая и другие вакцины. Фирма "Авентис Пастер" (Франция) является эксклюзивным дистрибьютором "Эувакс В" в России и на мировом рынке. Производство этой вакцины осуществляется в соответствии с международными нормами GMP (сертификат GMP от 06.11.1997, вакцина одобрена ВОЗ в марте 1998 года и июле 1999 года), кроме того, 29.04.1999 г. при регистрации в России ГИСК им. Л.А. Тарасевича и Бюро регистрации Минздрава РФ была также проведена сертификация производства. По результатам испытаний было выдано Регистрационное Удостоверение П-8-242-№011073 от 25.05.1999 г. "Эувакс В" - рекомбинантная вакцина против гепатита В, содержащая очищенный HBsAg вируса ГВ, продуцируемый дрожжевыми клетками Saccharomyces cerevisiae. Данная вакцина обеспечивает специфический иммунитет против известных вариантов вируса гепатита В (6 генотипов). "Эувакс В" выпускается в детской (1 доза содержит 10 мкг HBsAg) и взрослой (1 доза содержит 20 мкг HBsAg) дозировках. Наиболее распространенными схемами вакцинации являются 0-1-6 (для всех пациентов) и 0-1-2-12 (для лиц, входящих в группы риска). В соответствии с рекомендациями экспертов ВОЗ и Комитета по профилактике вирусных гепатитов (VHPB), ревакцинация после полного курса (три дозы) вакцины не требуется [1]. Вакцина "Эувакс В" помимо индивидуальной формы выпуска поставляется и в 10-дозовых флаконах. "Эувакс В" термостабильна: от +2 до +8°С - 3,5 года, при +25°С - 3 месяца, при +37°С - 1 месяц. В настоящее время в России реализовано около 1,5 млн. доз "Эувакс В", в странах СНГ - более 4 млн. доз, в мире - более 30 млн. доз. В связи с тем, что "Эувакс В" имеет относительно недолгую (с 1992 г.) историю применения для профилактики гепатита В в разных странах мира, представляет интерес обобщение и анализ имеющихся на настоящий момент данных по безопасности, иммунологической и профилактической эффективности данного препарата. Лабораторные и клинические регистрационные испытания вакцины "Эувакс В", проведенные Национальным Органом Контроля иммунобиологических препаратов - ГИСК им. Л.А. Тарасевича Минздрава РФ, продемонстрировали высокое качество препарата [2]. Поствакцинальных осложнений не было. Установлено, что местные поствакцинальные реакции (болезненность в месте инъекции) возникали у 3,1% привитых. Других проявлений местных реакций не отмечалось за весь период наблюдения. Частота появления анти-HBs после курса вакцинации по укороченной схеме (0-1-2 месяца) составила 92,9%. Различий в частоте сероконверсии между вакциной "Эувакс В" и референс-препаратом не выявлено. Средняя концентрация специфических антител составила 856,5 МЕ/л (протективная концентрация >10 МЕ/л). Важно отметить, что помимо России, в настоящее время вакцина "Эувакс В" зарегистрирована в 36 странах. Первый серьезный опыт применения вакцины "Эувакс В" приобретен в период 1995-1997 гг. в результате мультицентровых клинических испытаний, проведенных в нескольких медицинских колледжах Южной Кореи [3]. Испытания проводились по единой методике с участием двух возрастных групп: до 10 лет и старше. Группа до 10 лет была разделена на новорожденных и детей более старшего возраста. Использовали две схемы вакцинации: 0-1-2 и 0-1-6 месяцев. В результате проведенных исследований установлено:
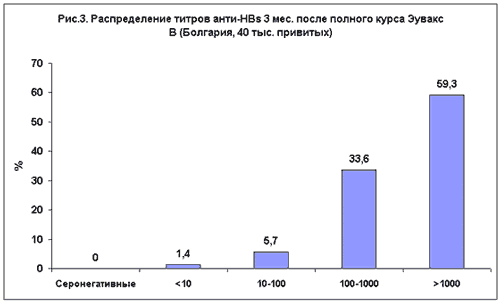
Первые опубликованные результаты широкомасштабного рутинного применения "Эувакс В" в детской дозировке - анализ реализованной программы массовой иммунизации новорожденных в период с июля 1998 по декабрь 1999 года в Болгарии [4]. В соответствии с этой программой было привито 40 тыс. детей по схеме 0-1-6 месяцев. Установлена безопасность и хорошая переносимость "Эувакс В". Небольшие местные, быстро проходящие реакции отмечены при активном выявлении у 1,5% детей. Иммунологическую эффективность оценивали в группе из 200 детей, отобранных по случайному признаку. Через 1-3 месяца после введения третьей дозы у всех детей выявлены анти-HBs антитела, причем у 98,6% с концентрацией более 10 МЕ/л (Рис.3). Авторами было сделано заключение, что вакцина "Эувакс В" в условиях массовой иммунизации безопасна, ареактогенна и обладает высокой иммунологической эффективностью.
Успешно применяется вакцина "Эувакс В" и в странах СНГ. Осуществляется широкомасштабная программа вакцинации в Казахстане [5].В рамках Национальной программы "Вирусные гепатиты в Республике Кыргызстан 1999-2010 гг." проведена вакцинация около 7000 новорожденных [6]. В Российской Федерации вакцина "Эувакс В" также получила широкое распространение. В настоящий момент она используется во многих субъектах РФ (г.Москва, Московская область, г.Санкт-Петербург, г.Пермь, г.Новосибирск, г.Оренбург, г.Рязань, г.Иркутск, г.Ростов-на-Дону и др.). Вакцину "Эувакс В" широко использует Министерство обороны РФ. Первые российские результаты применения вакцины "Эувакс В" были получены в Московской области, г.Подольск, где были привиты все школьники в возрасте 13 лет по схеме 0-1-6 детской дозой (10 мкг) [7]. Поствакцинальных осложнений не отмечено, зарегистрированные в единичных случаях поствакцинальные реакции были непродолжительными. Оценку напряженности поствакцинального иммунитета проводили в группе из 31 школьника через 1 месяц после окончания полного курса вакцинации. Поствакцинальные анти-HBs антитела обнаружены у всех детей, причем у 29 (93%) в концентрации, превышающей 1000 МЕ/л. Представляет большой интерес опыт массового применения вакцины "Эувакс В" в г. Москве, где в 2000 году были привиты школьники 7-х классов [8]., Всего провакцинировано 114 тысяч подростков по схеме 0-1-6 месяцев детской дозой (10 мкг). Охват составил 88,8%. В целом, по итогам трехкратной иммунизации частота поствакцинальных реакций составила 0,06%. Зафиксированы обычные местные (покраснение в месте введения препарата) и общие реакции (подъем температуры тела до 37,5°С). Необычных реакций и осложнений после проведения вакцинации не было. У 205 школьников, представляющих все территориальные округа г. Москвы (отобранных методом случайной выборки), была изучена напряженность поствакцинального иммунитета. Через 1 месяц после завершения полного курса наличие анти-HBs зафиксировано у 99,03% привитых (203 из 205). Только у одного подростка анти-HBs антитела определены в концентрации ниже протективной (10 МЕ/л). Важно констатировать, что очень высокая концентрация поствакцинальных антител - более 1000 МЕ/л отмечена у 80,3%. Реактогенность и иммунологическую активность вакцины "Эувакс В" среди медицинских работников изучали в г. Пермь [9]. Вакцинацию по схеме 0-1-6 в дозе 20 мкг проводили после предварительного скрининга медицинских работников на наличие HbsAg и анти-HBs. Реактогенность вакцины "Эувакс В" оценена как низкая. Все поствакцинальные реакции характеризовались малой интенсивностью и отмечены лишь у 3,6% лиц. Во всех случаях они проходили в течение 2-3 дней. Напряженность поствакцинального иммунитета оценивали трехкратно: через один месяц после первой вакцинации, через один месяц после второй и через две недели по окончании полного курса. Появление анти-HBs отмечено у 47,8% после первой вакцинации (у 34,7% в протективной концентрации), у 89,4% после второй вакцинации (у 76,3% в протективной концентрации) и после завершенного курса у всех вакцинированных, причем у 70,6% из них в высокой концентрации - превышающей 100 МЕ/л. Опыт применения вакцины "Эувакс В" в условиях крупного стационара Минобороны РФ интересен тем, что использованы различные схемы вакцинации, и проведена вакцинация с помощью комбинации вакцин "Эувакс В" и "Комбиотех" (Россия) [10]. Вакцинацию проводили среди медицинского персонала более 40 подразделений Военно-медицинской Академии г. Санкт-Петербурга. Применяли следующие схемы введения вакцин: 0-1-6 месяцев, 0-1-2, 0-1-3 и 0-1-18-22. По схеме 0-1-18-22 месяца для первых двух доз использовали вакцину производства "Комбиотех", для последующих - "Эувакс В". Всего в процессе реализации программы вакцинации привито более 2 тыс. человек. Поствакцинальные реакции отмечены у 0,51% по окончании полного курса вакцинации, при этом у 0,14% - местные реакции, у 0,37% - общие. Поствакцинальных осложнений не было. Констатирована высокая иммуногенность вакцины "Эувакс В": частота сероконверсии составила 94,5%, в том числе при применении схемы 0-1-6 месяцев - 97,1%, 0-1-2 месяца - 80,0%, 0-1-3 месяца - 95,7% и 0-1-18-22 месяца - 95,0%. Следует отметить, что высокая иммуногенность показана и в случае комбинации двух разных вакцин. Важно, что такая практика взаимозаменяемости вакцин против гепатита В допускается как международными, так и отечественными экспертами [11]. Обобщая имеющийся на данный момент в России опыт применения вакцины "Эувакс В" можно заключить, что данный препарат обладает низкой реактогенностью и высокой иммунологической эффективностью. В то же время, имели место сообщения Центра госсанэпиднадзора Красноярского края о случаях поствакцинальных реакций у медицинских работников, в результате чего была приостановлена реализация программы вакцинации. Министерством здравоохранения России было проведено эпидемиологическое расследование. По итогам всесторонней проверки были сделаны следующие выводы [12]: 1) образцы вакцины, поступившие на проверку в ГИСК им. Л.А. Тарасевича из 3 мест соответствуют требованиям нормативной документации, и дальнейшее использование этой серии вакцины "Эувакс В" разрешено; 2) отмечено незнание специалистами ЦГСЭН в Красноярском крае приказов Минздрава РФ и инструкции по применению данной вакцины. В целом, в настоящее время имеющиеся данные по опыту применения вакцины "Эувакс В", свидетельствуют о высоких показателях качества и эффективности, что позволяет рекомендовать ее для широко применения в практике здравоохранения. ЛИТЕРАТУРА medi.ru Эувакс В инструкция по применению, лечение, отзывы, показания, противопоказанияЭувакс ВРекомбинантная вакцина для профилактики гепатита ВЭувакс В представляет собой высокоочищенные неинфекционные полипептиды поверхностного белка (НВsAg) вируса гепатита В, адсорбированные на солях алюминия (используемых в качестве адъюванта) и консервированные тиомерсалом. Данный препарат, предназначенный для профилактики гепатита В, является рекомбинантной ДНК-вакциной и производится с помощью рекомбинантной ДНК технологии - продуцирование полипептидных фрагментов HBsAg в дрожжевых клетках Saсcharomyces cerevisiae. Вакцина удовлетворяет требованиям ВОЗ в отношении рекомбинантных вакцин для профилактики гепатита В. При производстве препарата не используются субстанции человеческого происхождения. ВНЕШНИЙ ВИД Эувакс В представляет собой беловатую, слабо опалесцирующую суспензию. СОСТАВ В 1,0 мл вакцины содержится: - Активный ингредиент: очищенный HBsAg.................................…………20 мкг - Адъювант: гель гидроокиси алюминия (по алюминию)......................…0,5 мг -Консервант: Тиомерсал…................0,01 в/о % - Эксципиенты: фосфат калия одноосновный, фосфат натрия двуосновный, хлористый натрий. ПОКАЗАНИЯ Специфическая иммунопрофилактика инфекции, вызываемой всеми известными подтипами вируса гепатита В. СХЕМА ПРИМЕНЕНИЯ Вакцина Эувакс В предназначена только для внутримышечного введения в область дельтовидной мышцы взрослым и детям старшего возраста и в переднебоковую поверхность бедра новорожденным и детям младшего возраста. - Детская доза (для новорожденных и детей до 15 лет включительно): 0,5 мл (10 мкг HBsAg). - Взрослая доза (для лиц с 16 лет): 1,0 мл (20 мкг HBsAg). Процесс иммунизации состоит из введения трех доз вакцины в соответствии со следующей схемой: - 1-я доза: выбранная дата; - 2-я доза: через 1 месяц после введения 1-й дозы; - 3-я доза: через 6 месяцев после введения 1-й дозы. Существует также альтернативная схема вакцинации: 1-я доза - выбранная дата, 2-я доза - через 1 месяц после введения 1-й дозы, 3-я доза - через 2 месяца после введения 1-й дозы, ревакцинация - через 12 месяцев после 3-й дозы первичной иммунизации. Данная схема может быть использована у некоторых групп населения: у новорожденных, матери которых инфицированы гепатитом В, у пациентов, инфицированных или с подозрением на инфицирование вирусом гепатита В, у лиц, отправляющихся в регионы с высоким уровнем заболеваемости. Введение дополнительных доз вакцины показано пациентам, находящимся на гемодиализе и с иммунодефицитами, поскольку у этой категории пациентов после первичной иммунизации защитные титры антител (> 10 МЕ/л) могут быть не индуцированы. ПРОТИВОПОКАЗАНИЯ Вакцина Эувакс В противопоказана пациентам с гиперчувствительностью к какому-либо ее компоненту (в том числе - к дрожжам) и пациентам с реакциями гиперчувствительности на предыдущее введение данной вакцины. ПРЕДОСТЕРЕЖЕНИЯ Общие предостережения: - Вакцинацию следует отложить у пациентов с прогрессирующим заболеванием, сопровождающимся повышением температуры тела. - У пациентов, страдающих рассеянным склерозом, сообщались отдельные неподтвержденные случаи обострения заболевания после вакцинации. Поэтому при вакцинации этих пациентов пользу от использования вакцины следует тщательно соизмерять с возможным риском обострения заболевания (см. Побочные реакции). - Иммунизация может быть неэффективна у лиц, находящихся в латентной или прогрессирующей стадии гепатита В. - При проведении вакцинации необходимо иметь в наличии медикаменты необходимые для оказания экстренной помощи в случае анафилактической реакции. Предупреждения по использованию: - Перед введением препарат следует хорошо взболтать, поскольку при хранении может образоваться небольшое количество осадка (белого цвета с прозрачной бесцветной надосадочной жидкостью). - Эувакс В не следует вводить в ягодичную область. Не следует вводить Эувакс В внутривенно. Беременность и лактация: - Влияние HBsAg на развитие плода не изучалось. Вместе с тем, как и в случае использования любой инактивированной вакцины, представляется маловероятной способность данного препарата оказывать побочное воздействие на эмбрион или плод. Тем не менее, вакцина Эувакс В должна использоваться у беременных только при наличии жизненных показаний. - Действие вакцины Эувакс В на грудных детей после вакцинации их матерей в специальных исследованиях не изучалось. Вместе с тем, не существует противопоказаний для использования данной вакцины у кормящих матерей. ПОБОЧНЫЕ РЕАКЦИИ Обычно отмечаются: - Местные реакции (покраснение, болезненность, припухание, уплотнение) самостоятельно проходящие в течение двух дней после вакцинации. Редко возможны: - Повышение температуры тела (выше 38,8°С). - Общие реакции (недомогание, утомляемость, головная боль, тошнота, рвота, головокружение, миалгия, артрит). - Кожная сыпь и преходящее повышение активности трансаминаз. Очень редко наблюдаются (без установления однозначной связи с вакцинацией): - Случаи полинейропатии, неврит зрительного нерва, паралич лицевого нерва, обострение рассеянного склероза, синдром Гийена-Барре, аллергические реакции немедленного типа. УСЛОВИЯ ХРАНЕНИЯ Не использовать по окончании срока годности, указанного на внешней упаковке. Хранить при температуре от +2°С до +8°С (в холодильнике). Не замораживать. СРОК ГОДНОСТИ 36 месяцев. ФОРМА ВЫПУСКА - 1 флакон, содержащий 0,5 мл вакцины; - 20 флаконов, содержащих по 0,5 мл вакцины в каждом; - 1 флакон, содержащий 1,0 мл вакцины; - 20 флаконов, содержащих по 1,0 мл вакцины в каждом; - 10 флаконов, содержащих по 5 мл вакцины в каждом; - 10 флаконов, содержащих по 10 мл вакцины в каждом. Дата создания документа: 02.06.1998 Пересмотрено:18.04.2001 Дистрибьютор: ПАСТЕР МЕРЬЕ КОННОТ КОРЕЯ 18th Fl. KANGNAM BLDG, 1321-1 SEOCHO-DONG, SEOCHO-KU SEOUL, 137-070, KOREA Производитель: LG Chem PHARMACEUTICAL DIV. 599, Yongjei-dong, Iksan-city, Chun Buk-do, 570-350, Korea Обо всех случаях необычных прививочных реакций следует информировать Национальные органы контроля медицинских иммунобиологических препаратов и Представительство фирмы "Авентис Пастер" (101000, Москва, Уланский пер., 5, тел. (095) 935 86 90) Приведённая выше информация по применению препарата представлена исключительно в ознакомительных целях и предназначена для специалистов. Полную официальную информацию о применении препарата, показаниях к применению на территории РФ читайте в инструкции по применению, находящейся в упаковке. Портал Academ-Clinic.RU не несёт ответственности за последствия, вызванные приёмом лекарственного средства без назначения врача. Не занимайтесь самолечением, не меняйте схему приёма, назначенную лечащим врачом! Пожалуйста, оцените статью, помогите сделать сайт лучше www.academ-clinic.ru Результаты регистрационных испытаний вакцины Эувакс В для профилактики гепатита ВТ.А. Бектимиров, М. А. Горбунов, Н. В. Шалунова, Л. И. ПавловаГосударственный НИИ стандартизации и контроля медицинских биологических препаратов им. Л.А.Тарасевича, Москва РЕЗУЛЬТАТЫ РЕГИСТРАЦИОННЫХ ИСПЫТАНИЙ ВАКЦИНЫ "Эувакс В" ДЛЯ ПРОФИЛАКТИКИ ВИРУСНОГО ГЕПАТИТА В Учитывая многообразие путей передачи гепатита В и огромное число источников этой инфекции (больные хроническими гепатитами, острыми формами инфекции и особенно носители HBsAg), наиболее перспективным средством профилактики этой инфекции является вакцинация. Вакцинация является единственным средством прерывания естественного механизма передачи вируса от матери-носительницы HBsAg к новорожденному ребенку. Кроме того, иммунизация против гепатита В обеспечивает защиту от заражения вирусом гепатита D. В настоящее время для профилактики гепатита В используются рекомбинантные дрожжевые вакцины, характеризующиеся слабой реактогенностью, полной безопасностью и выраженной протективной активностью. Вакцины против гепатита В даже при введении новорожденным в первые часы после рождения хорошо переносятся, обладая при этом выраженным защитным эффектом. При этом отсутствует интерференция с материнскими антителами или с пассивными" антителами, содержащимися в специфическом иммуноглобулине против гепатита В. Полностью отсутствует интерференция с другими вакцинами, и в том числе с вакцинами, входящими в календари профилактических прививок. В связи с этим вакцины против гепатита В можно применять в сочетании практически со всеми вакцинами. Опыт широкого использования вакцины против гепатита В во многих странах мира еще раз убедительно показал, что эффективное воздействие на снижение интенсивности эпидемического процесса гепатита В посредством иммунизации возможно только при правильно разработанной тактике и стратегии вакцинопрофилактики этой инфекции. Проводимая в течение многих лет вакцинация лиц только из так называемых групп высокого риска заражения (медицинских работников, наркоманов и т.п.) в таких странах как США, Франция, Германия и др. не обеспечила ожидаемого снижения заболеваемости гепатитом В и уровня носительства HBsAg в этих странах. Исходя из этого ВОЗ, обобщив многолетний опыт применения вакцины против гепатита В, рекомендовала в качестве наиболее эффективной меры специфической профилактики этой инфекции включение вакцинации в национальные календари прививок. В настоящее время более 80 стран Европы, Азии, Африки и Америки проводят сочетанную вакцинацию против гепатита В в рамках расширенной программы иммунизации (РПИ). Многолетний опыт применения вакцины против гепатита В в рамках национальных календарей профилактических прививок в ряде стран мира свидетельствует о том, что эта мера обеспечивает снижение заболеваемости гепатитом В и носительства вируса не только у детей и подростков, но и у взрослого населения в 10-20 раз. Полный курс вакцинации против гепатита В состоит из трех прививок, которые могут проводиться по двум схемам: так называемая "короткая" схема, при которой вакцинация проводится с месячным интервалом между прививками (0-1-2 мес.) и так называемая "классическая" схема иммунизации, при которой третья прививка проводится через 6 месяцев после первой (0-1-6 мес.). При использовании "короткой" схемы иммунизации (0-1-2 мес.) происходит быстрое нарастание антител, и поэтому ее рекомендуется использовать для экстренной профилактики гепатита В (новорожденные от матерей-носителей HBsAg) и в ургентных случаях возможного заражения вирусом ГВ при проведении оперативного вмешательства или других парентеральных манипуляций, а также при работе с кровью и ее препаратами. При "короткой" схеме иммунизации рекомендуется введение бустер-дозы вакцины через 12-14 месяцев, т.к. концентрация антител у привитых по схеме 0-1-2 мес. ниже, чем при применении "классической" схемы (0-1-6 мес.). Как правило, после полного курса иммунизации частота сероконверсий у лиц с защитным титром антител варьирует от 80 до 100%. Следует особо подчеркнуть, что только полный курс иммунизации обеспечивает защиту от заражения гепатитом В, т.к. две прививки вызывают образование антител лишь у 50-60% привитых. Продемонстрировано, что возможна взаимозаменяемость вакцин, изготовленных различными производителями. Так, если в начале иммунизации были использованы одна или две дозы одной вакцины, а завершен курс иммунизации вакциной другого производителя, то иммунный ответ был такой же, как и при использовании одного и того же препарата. Однако такой подход к иммунизации не должен быть рутинным. Им можно воспользоваться при иммунизации, в частности, детей-мигрантов в случаях, когда невозможно установить, какой вакциной прививался ребенок ранее. Длительность сохранения анти-HBs в сыворотке крови привитых зависит от величины титров антител, синтезируемых в процессе вакцинации, однако защита от развития клинически выраженной формы инфекции и формирования хронического носительства сохраняется в течение очень длительного периода времени даже после исчезновения антител. У иммунизированных людей с защитными титрами поствакцинальных антител отмечен быстрый иммунный ответ при введении бустерной дозы вакцины или при контакте с ВГВ даже спустя много лет после первичной иммунизации. Это указывает на длительное сохранение иммунологической памяти, предотвращающей развитие клинических форм ВГВ-инфекции или формирование хронического вирусоносительства. Исходя из этого, детям или взрослым с нормальным иммунным статусом вводить бустерные дозы вакцины нет никакой необходимости. В нашей стране зарегистрированы и разрешены к применению в практике здравоохранения отечественная вакцина против гепатита В, а также три вакцины зарубежных производств. Фирма "Пастер Мерье Коннот" (Франция) обратилась в ГИСК им. Л.А.Тарасевича с просьбой о возможности регистрации и использования в РФ дрожжевой рекомбинантной вакцины "Эувакс В" производства компании "LG Сhemical Ltd." (Республика Корея). Основными задачами данного исследования являлась оценка реактогенности и иммунологической активности вакцины "Эувакс В" с целью разрешения ее использования для профилактики гепатита В на территории РФ. Изучение реактогенности и иммунологической активности дрожжевой рекомбинантной вакцины "Эувакс В" против гепатита В проводилось в условиях контролируемого эпидемиологического опыта (полевые клинические испытания) при иммунизации взрослых лиц в возрасте 19-20 лет. Вакцина "Эувакс В" - высокоочищенный поверхностный антиген вируса гепатита В (HBsAg), адсорбированный на солях алюминия (адьювант) и консервированный тиомерсалом. Данный препарат является коммерческой рекомбинантной вакциной для профилактики гепатита В, полученной из HBsAg, продуцируемого дрожжевыми клетками с помощью рекомбинантной ДНК-технологии. Одна доза вакцины для вакцинации взрослых (1,0 мл) содержит 20 мкг антигена. Серии вакцины отконтролированы в специализированной лаборатории института по тестам, предусмотренным НТД на препарат и требованиями комитета экспертов ВОЗ по стандартизации биологических препаратов. В качестве референс-препарата была использована коммерческая вакцина против гепатита В, зарегистрированная в РФ. Иммунизации подлежали здоровые лица, не болевшие гепатитом В, не прививавшиеся против этой инфекции, не содержащие в крови маркеров гепатита В и не имеющие противопоказаний, предусмотренных инструкциями по применению обеих вакцин. От лиц, подлежащих вакцинации, получено письменное информированное согласие на проведение иммунизации. Вакцинацию проводили согласно инструкции по применению вакцин: внутримышечно в область дельтовидной мышцы трехкратно с интервалом в 1 месяц по схеме 0-1-2 мес. в дозе 1,0 мл (20 мкг). У всех лиц, подлежащих вакцинации (233 чел.), были исследованы сыворотки на наличие маркеров гепатита В. Из числа лиц, не имеющих в крови маркеров гепатита В (HBsAg, анти-HBs), методом случайно-выборочного распределения (единица выборки - 1 человек) были сформированы две группы: одна - численностью 91 человек - получила полный курс вакцинации вакциной "Эувакс В" (в дозе 1,0 мл), вторая - численностью 95 человек - получила референс-вакцину. За всеми привитыми с целью регистрации общих и местных постпрививочных реакций и осложнений было установлено медицинское наблюдение в течение 4-5 дней вплоть до полного их исчезновения. В структуре общих реакций подлежали учету температура тела, недомогание, головная боль, боль в правом подреберье, тошнота и другие симптомы. Из проявлений местных реакций учитывали болезненность, покраснение и припухлость в месте введения препаратов, возникновение инфильтратов, болезненность и увеличение регионарных лимфоузлов. Иммунологическую активность вакцин оценивали с помощью тест-системы ЗАО "Рош-Москва" (Россия) и тест-системы "Hepanostica", "Органон-техника" (Голландия) в сыворотках крови привитых, полученных из локтевой вены через 21-28 дней после полного курса иммунизации в ИФА. Всего было исследовано 168 сывороток, полученных от привитых вакцинами "Эувакс В" и референс-препаратом. Сыворотки крови были разлиты в ампулы, зашифрованы и сформированы в блоки. Иммунологическая активность сравниваемых вакцинных препаратов была охарактеризована по следующим показателям:
Все количественные показатели обрабатывали методом вариационной статистики. Достоверность различий определяли по Т-критерию Стьюдента-Фишера, при этом достоверными считали различия при р<0,05. Наблюдения за привитыми показали, что в 90-96% случаев как у привитых вакциной "Эувакс В", так и референс-вакциной не отмечалось повышения температуры на введение обеих вакцин против гепатита В. Слабо выраженные температурные реакции (37,1-37,5°С) регистрировались лишь у 3,1-10,0% привитых двумя сравниваемыми вакцинами (чаще на первое введение препаратов). Статистически значимых различий в частоте регистрации слабых температурных реакций среди привитых вакциной "Эувакс В" и референс-вакциной не отмечалось, при этом длительность температурных реакций не превышала 24 часов. Из местных реакций лишь у 1 привитого вакциной "Эувакс В" после второго введения препарата были зарегистрированы жалобы на болезненность при надавливании в месте введения вакцины (3,1%). Других проявлений местных реакций не отмечалось за весь период наблюдения ни у одного привитого сравниваемыми вакцинами. Таким образом, результаты изучения общих и местных постпрививочных реакций у привитых свидетельствуют о низкой реактогенности вакцины "Эувакс В". При определении иммунологической активности установлено, что после полного курса вакцинации против гепатита В по укороченной схеме иммунизации (0-1-2 мес.) у привитых вакциной "Эувакс В" уровень сероконверсий составил 92,9 ± 3,4%. Статистически значимых различий в уровне сероконверсий по сравнению с референс-вакциной не установлено (табл.). Одним из показателей, характеризующих иммуногенность вакцин против гепатита В, является величина титров специфических антител у привитых. При определении уровня антител с помощью тест-системы ЗАО "Рош-Москва" более чем у 50% привитых титры антител после полного курса вакцинации были выше 100 мМЕ/мл (титра длительной защиты). При использовании тест-системы "Hepanostica" выявлено, что даже при "короткой" схеме вакцинации титры антител в 70-85% случаев превышали 100 мМЕ/мл, а в 30-50% случаев - 500 мМЕ/мл и более. Сероконверсия и титры анти-HBs у привитых вакциной "Эувакс В" и референс-вакциной через 1 мес. после полного курса вакцинации (схема 0-1-2 мес., тест-система "Hepanostica") Таким образом, испытанная вакцина "Эувакс В" обладает выраженной иммунологической активностью при использовании по схеме 0-1-2 мес. Полученные нами результаты полностью согласуются с материалами полевых клинических испытаний вакцины "Эувакс В", представленными фирмой. Результаты проведенного лабораторного контроля и полевых клинических испытаний, свидетельствующие о низкой реактогенности и выраженной иммунологической активности дрожжевой рекомбинантной вакцины "Эувакс В", позволили рекомендовать ее для регистрации в Российской Федерации с целью использования для профилактики гепатита В. Представители Министерства здравоохранения России и Национального органа контроля медицинских иммунобиологических препаратов (ГИСК им. Л.А.Тарасевича) в соответствии с процедурой регистрации МИБП в Российской Федерации провели инспектирование производственных помещений и отдела биологического и технологического контроля качества вакцины против гепатита В компании "LG Chemical Ltd." (Республика Корея). Делегации была предоставлена полная возможность ознакомиться с условиями производства и контроля на соответствие их требованиям качественного производственного процесса (GMP). Инспектирование проводилось в городе Иксан, где размещены основные производственные подразделения, и в городе Тэджеон, где находятся научные подразделения и некоторые производственные отделы. Ознакомление с условиями производства показало их весьма высокий уровень. Несмотря на десятилетний срок эксплуатации производственных помещений и оборудования, они находятся в отличном состоянии. Конструкция помещений, размещение оборудования, обеспечивающие поточность технологического процесса, и особенно автоматизация и компьютеризация большинства этапов производства, а также электронный и компьютерный мониторинг производственных процессов позволяют, по мнению представителей России, отнести производство вакцины гепатита В компании "LG Chemical Ltd." к разряду наиболее современных производств МИБП. Следует также отметить, что микробиологический мониторинг производственных помещений обеспечивает гарантию асептических условий изготовления вакцин. Не оставляет также сомнения высокая компетентность персонала, который регулярно повышает свою квалификацию. В целом, фирма имеет тщательно предусмотренную систему гарантии качества (quality assurance), полностью удовлетворяющую требованиям GMP и контроля качества вакцины против гепатита В. Заслуживает полного одобрения работа отдела биологического и технологического контроля, который оснащен современной аппаратурой. Результаты тестирования позволили выдать фирме "LG Chemical Ltd." сертификат GMP на производство вакцины гепатита В. medi.ru инструкция по применению, аналоги, состав, показанияСамолечение может быть вредным для вашего здоровья.Необходимо проконсультироваться с врачом, а также ознакомиться с инструкцией перед применением. СоставСОСТАВ для формы выпуска 0,5 и 1,0 мл В 1,0 мл содержится: Активный ингредиент: очищенный HBsAg 20 мкг Адъювант: гель алюминия гидроксида (по алюминию) 0,5 мг Вспомогательные вещества: калия дигидрофосфат, натрия гидрофосфат, натрия хлорид, вода для инъекций. СОСТАВ для формы выпуска 5,0 и 10,0 мл В 1,0 мл содержится: Активный ингредиент: очищенный HBsAg 20 мкг Адъювант: гель алюминия гидроксида (по алюминию) 0,5 мг Консервант: Тиомерсал 0,01 в/о%. Вспомогательные вещества: калия дигидрофосфат, натрия гидрофосфат, натрия хлорид, вода для инъекций. Вакцина соответствует требованиям ВОЗ предъявляемым к рекомбинантным вакцииам для профилактики гепатита В. При производстве препарата не используются субстанции человеческого происхождения.ОписаниеБеловатая, гомогенная слабо опалесцирующая суспензия.ПротивопоказанияГиперчувствительность к пекарным дрожжам, а также к любому компоненту вакцины; аллергическая реакция, наблюдавшаяся при предыдущем введении препарата.Беременность и период лактации- Влияние HBsAg на развитие плода не изучалось. Вместе с тем, как и в случае использования любой инактивированной вирусной вакцины, представляется маловероятной способность данного препарата оказывать побочное воздействие на эмбрион или плод. Вакцина Эувакс В может использоваться у беременных только при высоком риске инфицирования вирусом гепатита В. - Действие вакцины Эувакс В на грудных детей после вакцинации их матерей в специальных исследованиях не изучалось. Противопоказаний для использования данной вакцины у кормящих матерей не существует.Способ применения и дозыПеред введением препарат следует хорошо взболтать, поскольку при хранении может образоваться небольшое количество осадка (белого цвета с прозрачной бесцветной над осад очной жидкостью). Вакцина Эувакс В предназначена только для внутримышечного введения. Не следует вводить Эувакс В в ягодичную область. При введении вакцины следует убедится, что игла не попала в сосудистое русло. -Детская доза (для новорожденных и детей до 15 лет включительно): 0,5 мл (10 мкг HBsAg). - Взрослая доза (для лиц с 16 лет): 1,0 мл (20 мкг HBsAg). Курс вакцинации состоит из введения трех доз вакцины в соответствии со следующей схемой: - 1 -я доза: выбранная дата 2- я доза: через 1 месяц после введения 1 -й дозы; - 3-я доза: через 6 месяцев после введения 1-й дозы. Для новорожденных, матери которых инфицированы вирусом гепатита В, а также для пациентов с подозрением на инфицирование вирусом гепатита В, и лиц, отправляющихся в регионы с высоким уровнем заболеваемости существует альтернативная схема вакцинации: 1-я доза - выбранная дата, 2-я доза - через 1 месяц после введения 1-й дозы, 3¬я доза - через 2 месяца после введения 1-й дозы, ревакцинация - через 12 месяцев после 1 -й дозы первичной иммунизации. ' Ревакцинация: ВОЗ нс рекомендуем проводить ревакцинацию, т.к. было показано, что вакцинация тремя дозами вакцины для профилактики гепатита В обеспечивает защиту па срок до 15 лет, кроме того, если защитный уровень антител в крови снижается но истечении этого времени, организм привитого человека остается способным обеспечить защитный уровень антител в ответ иа контакт с вирусом гепатита В. В тоже время ревакцинация может быть рекомендована программой вакцинации на региональном уровне. Введение дополнительных доз вакцины (в соответствии с возрастной дозировкой) может быть показано пациентам, находящимся на гемодиализе и с иммунодефицитами, поскольку у этой категории больных после первичной иммунизации защитные титры антител (>10 МЕ/л) могут быть не индуцированы.Побочное действиеОбычно отмечаются: - Местные реакции, такие как покраснение, болезненность и припухание; а также незначительное повышение температуры тела. Эти реакции проходят самостоятельно в течение двух дней после вакцинации. Редко отмечаются: - Повышение температуры тела (выше 38,8°С). - Общие реакции (недомогание, утомляемость, головная боль, тошнота, рвота, головокружение, миалгия, артрит). - Кожная сыпь. - Преходящее повышение активности трансаминаз. Очень редко наблюдаются (без установления однозначной связи с вакцинацией): - Случаи полинейропатии, неврит зрительного нерва, паралич лицевого нерва, обострение рассеянного склероза, синдром Гийена-Барре. необходимые для оказания экстренной помощи в случае а Учитывая теоретическую возможность развития аллергических реакций немедленного типа, при проведении вакцинации необходимо иметь в наличии медикаменты,Взаимодействие с другими лекарственными средствамиЭувакс В может применяться одновременно (в один день) с вакцинами для профилактики дифтерии, столбняка, коклюша, краснухи, кори, паротита или полиомиелита При этом препараты вводятся в разные участки тела с использованием разных шприцовОсобенности примененияУ пациентов с заболеванием, сопровождающимся повышением температуры тела, вакцинацию следует отложить до выздоровления. У пациентов, страдающих рассеянным склерозом, вакцинация, как и любая другая стимуляция иммунной системы, может вызвать обострение симптомов. Поэтому при вакцинации этих пациентов пользу от использования вакцины следует тщательно соизмерять с возможным риском обострения заболевания (см. Побочные реакции). Иммунизация может быть неэффективна у лиц, привитых в латентной или прогрессирующей стадии гепатита В.Форма выпускаПо 0,5 мл; 1,0 мл; 5,0 мл и 10,0 мл во флаконах. По 1, 10 или 20 флаконов по 0,5 мл или 1,0 мл с инструкцией по применению в картонной пачке. По 10 флаконов по 5,0 мл или 10,0 мл с инструкцией по применению в картонной пачке.Условия храненияПри температуре: от 2 до 8 °С. Не замораживать. Хранить в недоступном для детей месте.Срок годности3 года Не использовать после срока годности, указанного на упаковке.Эувакс В аналоги, синонимы и препараты группыСамолечение может быть вредным для вашего здоровья.Необходимо проконсультироваться с врачом, а также ознакомиться с инструкцией перед применением. apteka.103.by Эувакс В, рекомбинантная вакцина для профилактики гепатита В Суспензия для инъекций: инструкция, описание PharmPriceИнструкция по медицинскому применению лекарственного средства Эувакс В (Рекомбинантная вакцина для профилактики гепатита В)
Торговое название Эувакс В (Рекомбинантная вакцина для профилактики гепатита В)
Международное непатентованное название Нет
Лекарственная форма Суспензия для инъекций 0,5 мл, 1,0 мл, 5 мл, 10 мл
Состав Одна доза 0,5 мл (детская) и одна доза 1,0 мл содержит активное вещество- очищенный HBsAg 10 мкг и 20 мкг, вспомогательные вещества: гель алюминия гидроокиси 0,25 мг и0,5 мг, калия дигидрофосфат q.s., натрия гидрофосфат q.s., натрия хлорид 4,25мг 8,5 мг, вода для инъекций q.s. 5,0 мл и 10 мл вакцины содержат активное вещество - очищенный HBsAg 100 мкг и 200 мкг, вспомогательные вещества: гель алюминия гидроокиси 2,5 мг и5,0 мг, калия дигидрофосфат q.s., натрия гидрофосфат q.s., натрия хлорид 42,5мг и 85,0 мг, тимеросал 0,01% (вес/объем), вода для инъекций q.s.
Описание Дисперсионная суспензия
Фармакотерапевтическая группа Противогепатитные вакцины. Код АТС J07ВС01
Фармакологическе свойства Фармакокинетика Фармакокинетические исследования не проводились. Фармакодинамика Вакцина для профилактики вирусного гепатита В, представляетсобой очищенный поверхностный антиген,выделенный на основе генно-инженерной технологии дрожжей из культуры дрожжевыхклеток Saccharomyces cerevisiae, которые наследуют ген, кодирующийповерхностный антиген вируса гепатита В (HBV), производимый по технологиирекомбинантной ДНК. Эувакс В индуцируетобразование специфических гуморальных антител против поверхностного антигена вирусагепатита В (HBsAg) - анти-HBs антитела. Общепринято считать, что титр антител > 10 IU/мл.является защитным. Показано, что у новорожденных, детей и взрослых, относящихсяк группе риска, защитная эффективность составляет 95-100%. Средний геометрический титр постепенно повышается иполностью достигает защитного уровня после третьей вакцинации. При производстве вакцины не используются субстанциичеловеческого происхождения.
Показания к применению - профилактика вирусного гепатита В
Способ применения и дозы Рекомендуется вводить вакцину внутримышечно. Новорожденным и детям до 1 года, вводить в переднею-латеральнуючасть бедра, взрослым и детям старшего возраста – в область дельтовидной мышцы. Эувакс В не следует вводить в ягодичную область, из-за рискаповреждения седалищного нерва. Для новорожденных и детей до 16 лет разовая доза вакцинысоставляет 0,5 мл (10 мкг HBsAg). Для взрослых и детей старше 16 лет разовая доза составляет1,0 мл (20 мкг HBsAg). Процесс иммунизации состоит из введения трех доз вакцины в соответствиисо стандартной схемой: 1-я доза- выбранная дата, 2-я доза- через 1 месяц после введения 1-й дозы, 3-я доза- через 6 месяцев после введения 1-й дозы. Альтернативная (ускоренная) схема (0-1-2 мес.) – проводитсяс целью экстренной профилактики, детям, родившимся от матерей, инфицированныхвирусами гепатита В. Ревакцинацию проводят через 12 месяцев после 3-й дозыпервичной иммунизации. В зависимости от страны допускается применение и других схемиммунизации. Данная схема используется для экстренной профилактики, когдатребуется защита от гепатита В, например: новорожденных, матери которыхинфицированы гепатитом В, в случае контакта с вирусом (с кровью, половой,бытовой). Введение дополнительных доз вакцины показано пациентам,находящимся на гемодиализе из-за потери выработанных антител и симмунодефицитами, поскольку у этой категории пациентов после первичнойиммунизации защитные титры антител могут не достигнуть протективного уровня(> 10 МЕ/мл). Каждую дозу следует набирать стерильной иглой и шприцем пристрогом соблюдении правил асептики и антисептики во избежание загрязнениясодержимого флакона. Если время очередной прививки было пропущено, и всемаксимальные интервалы были также превышены, все остальные дозы вводятся собычными интервалами, невзирая на пропуск, хотя в данном случае дляподтверждения эффективности вакцинации по завершению курса прививок можетпотребоваться анализ концентрации антител.
Побочные действия Часто (≥1/10) - покраснение, болезненность, припухлость, уплотнение вместе инъекции, незначительное повышениетемпературы, самостоятельно проходящие в течение двух дней после вакцинации Редко (≥1/1000 и <1/100) - повышение температуры тела (выше 38,8°С) - недомогание, утомляемость, головная боль, головокружение - кожная сыпь - тошнота, рвота - миалгия, артрит - преходящее повышение активности трансаминаз Очень редко (<1/10 000). Однозначной связи с вакцинациейне установлено - полиневриты, неврит зрительного нерва, паралич лицевогонерва, обострение рассеянного склероза - синдром Гийена-Барре (1:200 000)
Противопоказания - гиперчувствительность на предыдущее введение вакцины, атак же к компонентам препарата, пекарским дрожжам и продуктам, содержащим их - повышение температура тела выше 37С - ОРВИ, грипп и другие острые инфекции - период обострения хронических заболеваний
Лекарственные взаимодействия Эффект Эувакса В снижает иммуносупрессивная терапия. ЭуваксаВ можно вводить одновременно с другими вакцинами: БЦЖ, АКДС, коревой, противполиомиелита. Разные инъекционные вакцины следует всегда вводить в разныеучастки.
Особые указания Введение Эувакса В пациентам, перенесшим инфекцию иобострение хронического заболевания, возможно через 2 месяца послевыздоровления. Пациентам с рассеянным склерозом, любая стимуляция иммуннойсистемы может вызвать обострение симптомов заболевания. Следовательно, длятакой группы пациентов введение вакцины назначают только в том случае, когдапредполагаемая польза превышает потенциальный риск обострения рассеянногосклероза. Вакцина не предотвратит развитие гепатита В, если иммунизация былапроведена у пациентов с латентной формой или в инкубационный период гепатита В. Пациентам с иммунодефицитами и лицам, находящимся на гемодиализе,может потребоваться введение дополнительных доз вакцины Эувакс В. Как и со всеми вводимыми вакцинами, следует иметь наготовенеобходимые лекарственные средства и оборудование для купирования возможнойанафилактической реакции на препарат после введения вакцины. Перед использованием, вакцину следует встряхнуть, так как вовремя хранения может образовываться белый осадок с прозрачной надосадочнойжидкостью. Вакцину не вводят в ягодичную область и внутривенно. Специфическим ограничением к применению вакцины (ввидувозможного понижения эффективности) может служить сильная недоношенность (вес< 1,5 кг). В таких случаях вакцинация обычно откладывается до моментадостижения ребенком веса 2 кг. Беременность и период лактации Влияние HBsAg на развитие плода не установлено. Однако, каки со всеми инактивированными вакцинами против вирусов, риск влияния на развитие плода считается незначительным. Применениевакцины Эувакс В в период беременности проводится только при наличии жизненныхпоказаний. Действие вакцины Эувакс В на грудных детей после вакцинацииих матерей в специальных исследованиях не изучалось. Вместе с тем, несуществует противопоказаний для использования данной вакцины у кормящихматерей. Особенности влияния лекарственного средства на способностьуправлять транспортным средством и потенциально опасными механизмами Не влияет.
Передозировка Не отмечена.
Форма выпуска и упаковка По 0,5 мл (детская доза) и 1,0 мл – в боросиликатномстеклянном флаконе вместимостью 3 мл, укупоренном резиновой пробкой c колпачкомтипа flip-off (алюминиевая основа с приложенной пластмассовой крышечкой). По 10флаконов вместе с инструкцией по медицинскому применению на государственном ирусском языках помещают в картонную пачку из картона По 5,0 мл (мультидоза) и 10,0 мл (мультидоза) в боросиликатномстеклянном флаконе вместимостью 10 мл и 20 мл, укупоренном резиновой пробкой cколпачком типа flip-off (алюминиевая основа с приложенной пластмассовойкрышечкой). По 5 флаконов вместе с инструкцией по медицинскому применению нагосударственном и русском языках помещают в картонную пачку.
Условия хранения Хранить при температуре от +2°С до +8°С. Не замораживать. После вскрытия флакона с одной дозой, вакцина хранению неподлежит. Многодозовые флаконы после вскрытия могут храниться ииспользоваться для последующих сессий иммунизации в течение 10 дней, в случаевыполнения следующих условий: Не истек срок годности. Вакцина хранилась при температуре от + 2 до + 8 ºC. Флаконы после открытия алюминиевого колпачка не погружалисьв воду или в другие растворы. Извлечение каждой дозы из флакона производилось стерильнымишприцем и иглой, с соблюдением строгих мер асептики для избежания контаминациисодержимого. Хранить в недоступном для детей месте!
Срок хранения 3 года Не применять препарат по истечении срока годности,указанного на упаковке.
Условия отпуска из аптек По рецепту
Производитель «LG Life Sciences Ltd», Корея. Упаковано ТОО «СП Глобал Фарм», Республика Казахстан, г. Алматы, ул.Джандосова 184«г», тел. 255-47-13, 229-57-55. Адрес организации принимающей на территории РеспубликиКазахстан претензии от потребителя по качеству продукции: ТОО «СП Глобал Фарм», Республика Казахстан г. Алматы, ул. Джандосова 184«г», тел. 255-47-13, 229-57-55. pharmprice.kz Эувакс В (Euvax B) | ООО «Сайлент 2000»
Эувакс В представляет собой беловатую, слабо опалесцирующую суспензию. СоставВ 1,0 мл вакцины содержится:Активный ингредиент: очищенный HBsAg 20 мкгАдъювант: гель гидроокиси алюминия (по алюминию) 0,5 мгКонсервант: Тиомерсал 0,01 в/о %Эксципиенты: фосфат калия одноосновный, фосфат натрия двуосновный, хлористый натрий. Показания: Специфическая иммунопрофилактика инфекции, вызываемой всеми известными подтипами вируса гепатита В. Схема примененияВакцина Эувакс В предназначена только для внутримышечного введения в область дельтовидной мышцы взрослым и детям старшего возраста и в переднебоковую поверхность бедра новорожденным и детям младшего возраста.Детская доза (для новорожденных и детей до 15 лет включительно): 0,5 мл (10 мкг HBsAg).Взрослая доза (для лиц с 16 лет): 1,0 мл (20 мкг HBsAg). Процесс иммунизации состоит из введения трех доз вакцины в соответствии со следующей схемой:1-я доза: выбранная дата;2-я доза: через 1 месяц после введения 1-й дозы;3-я доза: через 6 месяцев после введения 1-й дозы.Существует также альтернативная схема вакцинации: 1-я доза — выбранная дата, 2-я доза — через 1 месяц после введения 1-й дозы, 3-я доза — через 2 месяца после введения 1-й дозы, ревакцинация — через 12 месяцев после 3-й дозы первичной иммунизации. Данная схема может быть использована у некоторых групп населения: у новорожденных, матери которых инфицированы гепатитом В, у пациентов, инфицированных или с подозрением на инфицирование вирусом гепатита В, у лиц, отправляющихся в регионы с высоким уровнем заболеваемости.Введение дополнительных доз вакцины показано пациентам, находящимся на гемодиализе и с иммунодефицитами, поскольку у этой категории пациентов после первичной иммунизации защитные титры антител (> 10 МЕ/л) могут быть не индуцированы. ПротивопоказанияВакцина Эувакс В противопоказана пациентам с гиперчувствительностью к какому-либо ее компоненту (в том числе — к дрожжам) и пациентам с реакциями гиперчувствительности на предыдущее введение данной вакцины. ПредостереженияОбщие предостережения: Вакцинацию следует отложить у пациентов с прогрессирующим заболеванием, сопровождающимся повышением температуры тела.У пациентов, страдающих рассеянным склерозом, сообщались отдельные неподтвержденные случаи обострения заболевания после вакцинации. Поэтому при вакцинации этих пациентов пользу от использования вакцины следует тщательно соизмерять с возможным риском обострения заболевания (см. Побочные реакции).Иммунизация может быть неэффективна у лиц, находящихся в латентной или прогрессирующей стадии гепатита В.При проведении вакцинации необходимо иметь в наличии медикаменты необходимые для оказания экстренной помощи в случае анафилактической реакции. Предупреждения по использованию: Перед введением препарат следует хорошо взболтать, поскольку при хранении может образоваться небольшое количество осадка (белого цвета с прозрачной бесцветной надосадочной жидкостью).Эувакс В не следует вводить в ягодичную область. Не следует вводить Эувакс В внутривенно. Беременность и лактация:Влияние HBsAg на развитие плода не изучалось. Вместе с тем, как и в случае использования любой инактивированной вакцины, представляется маловероятной способность данного препарата оказывать побочное воздействие на эмбрион или плод. Тем не менее, вакцина Эувакс В должна использоваться у беременных только при наличии жизненных показаний.Действие вакцины Эувакс В на грудных детей после вакцинации их матерей в специальных исследованиях не изучалось. Вместе с тем, не существует противопоказаний для использования данной вакцины у кормящих матерей. Побочные реакцииОбычно отмечаются: Местные реакции (покраснение, болезненность, припухание, уплотнение) самостоятельно проходящие в течение двух дней после вакцинации.Редко возможны: Повышение температуры тела (выше 38,8°С).Общие реакции (недомогание, утомляемость, головная боль, тошнота, рвота, головокружение, миалгия, артрит).Кожная сыпь и преходящее повышение активности трансаминаз.Очень редко наблюдаются (без установления однозначной связи с вакцинацией):Случаи полинейропатии, неврит зрительного нерва, паралич лицевого нерва, обострение рассеянного склероза, синдром Гийена-Барре, аллергические реакции немедленного типа. Условия храненияНе использовать по окончании срока годности, указанного на внешней упаковке.Хранить при температуре от +2°С до +8°С (в холодильнике). Не замораживать.Срок годности — 36 месяцев slt2000.ru |
г.Самара, ул. Димитрова 131 [email protected] |
 |


 Эувакс В (Euvax B) — рекомбинантная вакцина для профилактики гепатита В, представляет собой высокоочищенные неинфекционные полипептиды поверхностного белка (НВsAg) вируса гепатита В, адсорбированные на солях алюминия (используемых в качестве адъюванта) и консервированные тиомерсалом. Данный препарат, предназначенный для профилактики гепатита В, является рекомбинантной ДНК-вакциной и производится с помощью рекомбинантной ДНК технологии — продуцирование полипептидных фрагментов HBsAg в дрожжевых клетках Saсcharomyces cerevisiae. Вакцина удовлетворяет требованиям ВОЗ в отношении рекомбинантных вакцин для профилактики гепатита В. При производстве препарата не используются субстанции человеческого происхождения.
Эувакс В (Euvax B) — рекомбинантная вакцина для профилактики гепатита В, представляет собой высокоочищенные неинфекционные полипептиды поверхностного белка (НВsAg) вируса гепатита В, адсорбированные на солях алюминия (используемых в качестве адъюванта) и консервированные тиомерсалом. Данный препарат, предназначенный для профилактики гепатита В, является рекомбинантной ДНК-вакциной и производится с помощью рекомбинантной ДНК технологии — продуцирование полипептидных фрагментов HBsAg в дрожжевых клетках Saсcharomyces cerevisiae. Вакцина удовлетворяет требованиям ВОЗ в отношении рекомбинантных вакцин для профилактики гепатита В. При производстве препарата не используются субстанции человеческого происхождения. 









