|
|
||||||||||
|
Хитрые актиномицеты. Антибиотики актиномицетыВажнейшие антибиотики, полученные из грибов и актиномицетов | Антибиотики группы пенициллина (природные и полусинтетические) наименее токсичны и обладают высоким эффектом действия. Пенициллин был выделен впервые в 1928 г. Флеммингом из зеленой плесени Penicillium notatum. Для клинического применения он был получен только в 1940 г. группой оксфордских ученых Флори, Чейном и Эбрахамом, а в 1942 г. — в Советском Союзе 3. В. Ермольевой. В настоящее время пенициллин получают из культур Penicillium chrysogenum в процессе их роста. Природные антибиотики представляют собой смесь различных пенициллинов (G, F, К, X), эффективность которых недостаточна. В промышленности препараты пенициллина получают с помощью направленного биосинтеза (биосинтетические пенициллины), добавляя в питательную среду, где культивируются пенициллиумы, различные вещества, используемые ими для синтеза антибиотиков. Наиболее активны из них бензилпенициллин (G) и феноксиметилпенициллин (V). Препараты пенициллина высокоактивны в отношении грамположительных (стафило-, стрепто- и пневмококки) и грамотрицательных (гонококки и менингококки) кокков. Действуют они также на бациллы сибирской язвы, клостридии и спирохеты. Особенно чувствительны к пенициллину возбудители сифилиса — бледные трепонемы. Пенициллин не оказывает действия на грамотрицательные бактерии семейства кишечных, микобактерии туберкулеза, риккетсии, вирусы, простейшие и грибы. Бензилпенициллии используют для парентерального введения в виде натриевой, калиевой или новокаиновой соли (новоциллин). Последний оказывает пролонгированное, т. е. продленное, действие: лечебная концентрация препарата в крови сохраняется 12 ч. Действие в течение 1—2 нед обеспечивает бензатинпенициллин (бициллин-1) и комбинированные препараты, состоящие из различных солей пенициллина (бициллин-3, бициллин-5). Эти препараты особенно эффективны при лечении сифилиса, ревматизма, осложнений после удаления миндалин. Феноксиметилпенициллин применяют внутрь, так как он устойчив к кислой среде желудка. Его используют в виде таблеток и гранул, из которых готовят суспензию.Механизм действия пенициллина в настоящее время хорошо изучен. Он тормозит последнюю стадию синтеза гликопептидов, составляющих основу клеточной стенки бактерий. Растущая клетка бактерий перестает синтезировать клеточную стенку и погибает. К пенициллину более чувствительны бактерии размножающиеся, чем находящиеся в покое. Пенициллин практически не токсичен для человека и животных, так как оболочки их клеток не содержат гликопептидов. Многие микроорганизмы, особенно стафилококки, приобретают устойчивость к пенициллину. Это связано с наличием у них фермента пенициллиназы, разрушающей пенициллин. Устойчивость грамотрицательных кишечных бактерий к пенициллину также является следствием наличия у них пенициллиназы. Хотя пенициллины малотоксичны, иногда они могут вызывать побочные реакции, связанные с повышенной чувствительностью больного к препарату. Эти реакции называются аллергическими. Они проявляются в виде сыпи-крапивницы, отеков век, губ, носа. У больных, повторно леченных пенициллином, может возникнуть анафилактический шок, который нередко заканчивается смертью. Однако он возникает крайне редко: 1 случай на миллион больных. При использовании больших, «ударных», доз пенициллина для лечения сифилиса или возвратного тифа могут наступить падение артериального давления, учащение сердцебиения и обморочное состояние. Подобная реакция развивается как следствие быстрого освобождения большого количества бактериальных токсинов при гибели возбудителей заболевания и токсичности этих продуктов для организма. Полусинтетические пенициллины — ампициллин, оксадиллин, метициллин, клоксациллин и карбенициллин — получают путем химического синтеза на основе 6-амино- пенициллановой кислоты (6-АПК), составляющей как бы ядро пенициллина. Ампициллин активен в отношении не только грамположительных, но и грамотрицательных микроорганизмов. Поэтому его наиболее широко применяют в клинике для лечения инфекционных заболеваний легких, мочеполовых и желчных путей, вызванных стрептококками, пневмококками, кишечной палочкой и протеем. Ампи¬циллин назначают в таблетках и капсулах. Внутримышечно и внутривенно его можно вводить в виде натриевой соли. Применение ампициллина иногда сопровожда¬ется тошнотой, рвотой. Оказывая губительное действие на кишечную микрофлору, он может вызывать явления дисбактериоза, сопровождающиеся поносом. Ампициллин, как и природные пенициллины, чувствителен к пенициллиназе и разрушается ею. Поэтому он оказывается неэффективным в отношении пенициллиназообразующих стафилококков. Карбенициллин по спектру антимикробного действия близок к ампициллину, но в отличие от других пенициллинов активен в отношении синегнойной палочки. Карбенициллин вводят парентерально, а при гнойных менингитах — ив спинномозговой канал. Препарат малотоксичен, но может вызвать аллергические реакции. Существует также комбинированный препарат ампициллина с оксациллином — ампиокс, который обычно назначают при тяжелом течении заболевания, если неизвестен возбудитель. Метициллин, оксациллин и клоксацйллин в отличие от ампициллина не разрушаются пенициллиназой и поэтому высоко эффективны при инфекциях, которые вызываются микробами, устойчивыми к пенициллину, особенно стафилококками. Оксациллин, кроме того, устойчив в кислой среде и его применяют внутрь. Эти препараты действуют на грамположигельную флору. Антибиотики широкого спектра действия эффективны в отношении микроорганизмов, принадлежащих к различным группам. К таким антибиотикам относят левомицетин, тетрациклины, аминогликозиды, полусинтетические пенициллины и полусинтетические цефалоспорины. Левомицетин (хлорамфеникол) выделен в 1947 г. из культуральной жидкости Streptomyces venezuelae. В настоящее время его получают с помощью химического синтеза. Левомицетин действует на грамположительные и грамотрицательные бактерии, риккетсии, некоторые крупные вирусы, например трахомы и орнитоза. К нему чувствительно большинство микробов, устойчивых к пенициллину, стрептомицину и сульфаниламидам. Левомицетин применяют при лечении брюшного тифа и паратифов, дизентерии, бруцеллеза, туляремии, коклюша, пневмонии, гонореи, сыпного тифа, трахомы, орнитоза и других инфекций. Левомицетин не действует на анаэробы, простейшие и микобактерии туберкулеза. Механизм действия связан с торможением процесса синтеза белка в клетке. Он нарушает равновесие в системе образования РНК- Левомицетин малотоксичен. Назначается в порошках и таблетках внутрь. В больших дозах при длительном применении может оказывать влияние на кроветворную систему.Синтомицин, действующим началом которого является левомицетин, вследствие его токсичности применяется в настоящее время только в виде линиментов и эмульсий для лечения гнойных заболеваний кожи и слизистых оболочек, при ожогах и трахоме. Тетрациклины объединяют группу антибиотиков, близких по химическому составу и биологическим свойствам. Первым был в 1945 г. выделен хлортетрациклин (ауреомицин, биомицин) из разнокультурной жидкости лучистого гриба Streptomyces aureofaciensа в 1949 г. — окситетрациклин (террамицин) из Str. rimosus, и в 1952 г. химическим путем получен тетрациклин. Teтpaциклины активны в отношении крупных вирусов и риккетсий, спирохет и простейших, грамположительных и грамотрицательных бактерий. Их используют при лечении пневмонии, дизентерии, бруцеллеза, туляремии, коклюша, гонореи, трахомы, сыпного тифа, амебной дизентерии. Лечебные дозы препаратов действуют бактериостатически, а более высокие — бактерицидно. Тетрациклины оказывают действие на синтез белка в клетке и функции рибосом. В больших дозах нарушают синтез гликопептидов клеточной стенки и проницаемость клеточных мембран. Тетрациклины исключают также из обмена веществ клетки металлы, необходимые для функционирования ферментов.Часто микроорганизмы приобретают устойчивость к тетрациклинам, которая бывает одновременно связана с устойчивостью к стрептомицину, левомицетину и сульфаниламидам. Такая приобретенная устойчивость может быть обусловлена наличием небольшой автономной хромосомы, лежащей в цитоплазме бактерий (R-фактор), которая может передаваться из одной микробной клетки в другую. Лекарственные формы применения тетрациклинов различны: таблетки, капсулы и суспензии, глазная мазь и свечи. Производные тетрациклина: гликоциклин предназначен для внутривенного и внутримышечного введения, а морфоциклин — только для внутривенного. При попадании под кожу он вызывает раздражение и образование инфильтрата. Существуют комбинированные формы тетрациклина с олеандомицином (олететрин), которые применяют в виде таблеток, и смесь олеандомицина с морфоциклином (олеморфоциклин), вводимая внутривенно. Окситетрациклин применяется внутрь в виде таблеток, в мазях, местно в присыпках и растворах. Окситетрациклин можно вводить внутримышечно. Полусинтетическое производное его — метациклин — принимают внутрь, так как он быстро всасывается и длительно сохраняется в крови. Хлортетрациклин для приема внутрь выпускается в виде таблеток и капсул. Побочное действие тетрациклинов связано с их губительным влиянием на микрофлору кишечника и особенно кишечную палочку. Гибель микроорганизмов, нормальных обитателей слизистых оболочек, приводит к размножению устойчивых к тетрациклинам дрожжеподобных грибов Candida, стафилококков и протея. В результате возникают дисбактериоз и такие тяжелые заболевания, как кандидамикозы, стафилококковые энтериты и гиповитаминозы. Эти осложнения можно предупредить при рациональном применении антибиотиков и одновременном употреблении противогрибкового препарата нистатина и витаминов. Поэтому выпускают препараты, являющиеся комбинациями тетрациклинов и витаминов: витациклин, витоксициклин и др. Аминогликозиды объединяют группу родственных препаратов, полученных из культуральной жидкости лучистых грибов — стрептомицет. К ним относят, помимо стрептомицина, неомицин, канамицин, мономицин (паромомицин) и гентамицин. Стрептомицины — антибиотики, которые образуют лучистые грибы из рода стрептомицет. Стрептомицин был выделен в конце 1943 г, Ваксманом. В 1946 г. из стрептомицина химическим путем получен дигидрострептомицин. Стрептомицин обладает широким спектром антибактериального действия и оказывает бактериостатическое и бактерицидное влияние на возбудителей чумы, туберкулеза, бруцеллеза, на шигелл и сальмонелл. В настоящее время его применяют преимущественно при лечении туберкулеза. Механизм действия стрептомицина связан с нарушением синтеза белка в клетке, так как он образует комплексы с ДНК и РНК клетки, препятствуя считыванию генетического кода. Стрептомицин нарушает также проницаемость клеточных мембран.Применение стрептомицина ограничено вследствие токсического действия на VIII пару черепных (слуховых) нервов. Это обусловливает нарушения функций слухового и вестибулярного аппарата: снижение и потерю слуха, пошатывание при ходьбе. При использовании стрептомицина микроорганизмы быстро приобретают устойчивость к нему. Некоторые микробы образуют даже стрептомицинзависимые формы, которые могут размножаться на питательных средах только при добавлении стрептомицина. Образованию устойчивых форм микобактерий туберкулеза препятствует назначение стрептомицина в сочетании с парааминосалициловой кислотой (ПАСК) и фтивазидом. Возможность практического применения аминогликозидов ограничена нейротоксическим и нефротоксическим действием препаратов. Канамицин наименее токсичен и вводится парентерально при лечении туберкулеза. Гентамицин широко используют при лечении заболеваний мочевыводящих путей и дыхательного тракта, вызванных грамотрицательными бактериями (кишечная палочка, протей), а также синегнойной палочкой. Парентеральное введение неомицин а запрещено. В случае приема внутрь аминогликозиды почти не всасываются и оказывают местное действие на микрофлору кишечника, поэтому их используют при заболеваниях желудочно-кишечного тракта, вызванных сальмонеллами, шигеллами, стафилококками, дизентерийной амебой (паромомицин, мономицин). Полусинтетические цефалоспорины получены химическим путем на основе 7-аминоцефалоспорановой кислоты (7-АЦК). Они обладают широким спектром действия в отношении как грамположительных, так и грамотрицательных бактерий: кокков, сибиреязвенных бацилл, клострвдий, коринебактерий, шигелл, сальмонелл, кишечной палочки. Эти антибиотики не действуют на синегнойную палочку, большинство штаммов протея, а также риккетсии, вирусы и простейшие. Цефалоспорины не разрушаются стафилококковой пенициллиназой и высокоактивны в отношении устойчивых к пенициллинам стафилококков. Наибольшее применение имеют цефалоридин (депорин) и цефалотин, которые вводятся в основном внутримышечно при инфекциях дыхательных и мочевыводящих путей, раневых инфекциях и инфицированных ожогах. Полусинтетические цефалоспорины малотоксичны и используются как антибиотики резерва. Антибиотики резерва применяют при лечении заболеваний, вызываемых устойчивыми к пенициллину грамположительными микробами, чаще стафилококками. К ним относят эритромицин, олеандомицин, выпускаемые за рубежом спирамицин и карбомицин, новобиоцин (альбомицин), ванкомицин и линкомицин. Для лечения туберкулеза используют также антибиотики резерва: флоримицин (БИОМИЦИН), циклосерин, канамицин, рифамицин и др. Противогрибковые антибиотики — нистатин (микостатин), леворин, трихомицин, амфотерицин В и микогептин — получены из культуральной жидкости различных видов стрептомицет. Гризеофульвин выделен из зеленой плесени Penicillium griseofulvum. Нистатин используют в таблетках, в виде мазей, свечей и глобулей для лечения кандидамикозов слизистых оболочек полости рта, влагалища, желудочно-кишечного тракта, мочеполовых органов и кожи. Механизм действия нистатина связан с нарушением проницаемости клеточных мембран патогенных грибов. Профилактическое применение нистатина рекомендуется при длительном приеме антибиотиков широкого спектра действия, особенно тетрациклинов, маленькими детьми, лицами пожилого возраста и ослабленными. В случаях применения больших доз нистатина иногда могут возникать тошнота, рвота и расстройство функции кишечника. Леворин назначают при кандидамикозах, аспергиллезе легких, а также при трихомониазе половых органов. Трихомицин обладает высокой активностью в отношении дрожжеподобных грибов Candida, а также трихомонад, некоторых трипаносом, лейшманий и спирохет, подавляет рост анаэробов — клостридий и стафилококков. Амфотерицин В — единственный препарат, эффективный при генерализованных микозах, таких, как гистоплазмоз, бластомикоз, криптококкоз и кандидасепсис. Препарат токсичен, и его применяют только по жизненным показаниям. Микогептин назначают внутрь при глубоких системных микозах: кокцидиоидозе, гистоплазмозе, аспергиллезе, кандидозе и др. Гризеофульвин используют при дерматомикозах человека: парше (фавус) волосистой части головы и гладкой кожи, трихофитии волос и кожи, микроспории, эпидермофитии, а также при фавусе и трихофитии лимфатических узлов и костей. При других грибковых заболеваниях он неэффективен. Противоопухолевые антибиотики оказывают выраженное цитотоксическое действие на опухолевые и быстрорастущие нормальные клетки организма, а также дают выраженный антимикробный эффект в отношении различных групп микроорганизмов. Как антибактериальные препараты они не применяются ввиду высокой токсичности. Большинство противоопухолевых антибиотиков образуется при биосинтезе различными видами стрептомицет. Механизм действия этих антибиотиков основан на влиянии их на синтез или метаболизм нуклеиновых кислот. Например, при действии брунеомицина наблюдаются прекращение синтеза и интенсивный распад ДНК, оливомицин подавляет синтез РНК на матрице ДНК, актиномицин и рубомицин подавляют ДНК-зависимый синтез РНК. К противоопухолевым относятся антибиотики группы актиномицинов (дактиномицин, хризомаллин, аурантин), группы ауреолевой кислоты (оливомицин, хромомицин), антрациклины (дауномицин, рубомицин) и стрептонигрины (брунеомицин), близкие по структуре к митомицину С.Противоопухолевые антибиотики применяют при различных формах злокачественных новообразований. | |||||||||||||||||||||||||||||
| Актиномицеты | |||||||
| Streptomyces sp. | |||||||
| промежуточные ранги
| |||||||
| Actinomycetales Buchanan, 1917 | |||||||
| Проверить информацию. Необходимо проверить точность фактов и достоверность сведений, изложенных в этой статье.На странице обсуждения должны быть пояснения. |
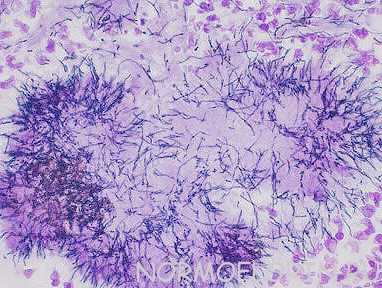
Актиномицеты (устар. лучистые грибки) — бактерии, имеющие способность к формированию на некоторых стадиях развития ветвящегося мицелия (некоторые исследователи, подчёркивая бактериальную природу актиномицетов, называют их аналог грибного мицелия тонкими нитями) диаметром 0,4—1,5 мкм, которая проявляется у них в оптимальных для существования условиях.
Имеют кислотоустойчивый (англ. acid fast) тип клеточной стенки, которая окрашивается по Граму как грамположительная, однако по структуре ближе к грамотрицательным. Характеризуются высоким (60—75 %) содержанием ГЦ пар в ДНК.Наиболее распространены в почве: в ней обнаруживаются представители почти всех родов актиномицетов. Актиномицеты обычно составляют четверть бактерий, вырастающих на традиционных средах при посевах их разведённых почвенных суспензий и 5—15 % прокариотной биомассы, определяемой с помощью люминесцентной микроскопии. Их экологическая роль заключается чаще всего в разложении сложных устойчивых субстратов; предположительно они участвуют в синтезе и разложении гумусовых веществ. Могут выступать симбионтами беспозвоночных и высших растений.
Строение
Косвенные данные позволят предположить у актиномицетов апикальный рост.
Дифференциация мицелия — процесс усложнения в процессе развития колонии актиномицета. Прежде всего она проявляется в делении на первичный (субстратный) и вторичный (воздушный) мицелий. Воздушный толще, он гидрофобен, содержит больше ДНК и ферментов, на поверхности его клеток имеются различные структуры (палочковидные, фиблиллы).
Мицелий с редкими перегородками, практически ценоцитный у спорообразующих, с частыми перегородками (септами) у форм, для которых мицелий распадается и близких к ним. Вегетативные клетки большинства форм делятся поперечными перегородками, Geodermatophilus и Dermatophilus — во взаимно перпендикулярных направлениях, некоторые актиномицеты содержат клетки с септами, проходящими в совершенно разных направлениях (спорангии Micromonospora, везикулы Frankia). Ветвление происходит по механизму почкования.
Часто дифференциация проявляется в образовании амицелиарных структур:
- коремии — тесное переплетение слившихся гиф, склеенных слизью с оксидами железа;
- агрегаты клеток;
- кристаллы вторичных метаболитов;
- «серные гранулы»;
- склероции — утолщённые гифы с вакуолями, заполненными липидами, может прорастать как спора;
- везикулы — инкапсулированные азотфиксирующие образования у Frankia.
В процессе старения цитоплазма клеток приобретает неравномерную электронную плотность, в ней перестают различаться рибосомы, граница нуклеоида расплывается, клеточная стенка становится тонкой и рыхлой, образуется микрокапсула. При автолизисе в цитоплазме образуются обширные светлые участки, нуклеоид распадается, в клеточной стенке образуются отверстия, клетка заполняется мембранными структурами, разрушающимися последними.
Жизненный цикл
Нокардиоформные актиномицеты редко образуют споры и размножаются преимущественно фрагментами быстро распадающегося мицелия. Актиномицеты, имеющие продолжительные мицелиальные стадии, различаются по типу спорообразования.
Спорообразование
По числу спор актиномицеты делят на моно- (например, Saccaromonospora, Micromonospora) олиго- (Actinomadura) и полиспоровые (Streptomyces), выделяя особо те, которые образуют спорангии. Спорообразование преимущественно экзогенное (Thermoactinomyces образует настоящие эндоспоры, однако в настоящее время этот род на основании хемотаксономических и генетических признаков, несмотря на выраженную мицелиальную стадию склонны относить к бациллам), реже псевдоэндогенное (Planomonospora, Dactylosporangium).
У Streptomyces и спорулирующих Actinomyces споры образуются в два этапа:
- Апикальный участок воздушной гифы отделяется септой, нуклеоид вытягивается.
- Почти одновременно клетка делится септами на участки, нуклеоид делится в тех же местах, клеточная стенка становится в 2 раза толще, споры округляются и их стенка становится в 7 раз толще стенки гифы.
У олигоспоровых септы закладываются базипитально. У монспоровых могут образовываться по механизму почкования.
Спорообразование вызывается т. н. фактором А (C13h32O4).
Прорастание споры
Прорастание происходит в следующие стадии:
- Инактивная спора гидрофобна, термоустойчива, не проявляет дыхательной активности
- Смачивающаяся активированная спора проявляет активность ферментов, начинается дыхание
- Спора набухает, начинается синтез РНК
- Выход 1—3 (реже 4) ростовых трубок, начинается синтез ДНК. Эта стадия необратима, остальные три — обратимы.
Образуют друзды — скопление переплетенных нитей с колбовидными утолщениями на концах.
Подвижность
Могут быть подвижны на стадии споры (актинопланы, Geodermatophilus и Dermatophilus), иногда подвижны части мицелия (эрсковия).
Экологические функции
Актиномицеты (особенно рода Micromonospora) обнаруживаются в водоёмах и их донных осадках, однако не решен вопрос о том являются ли они постоянными их обитателями или занесены из почвы, неизвестна также их роль в данных местообитаниях.
Почвы являются тем природным субстратом, откуда актиномицеты выделяются в наибольшем разнообразии. Однако большая часть биомассы актиномицетов представлена спорами, которые и дают колонии при учёте популяций в почве методом посева, лишь 1—4 % биомассы занимает мицелий[1]. Он обнаруживается в микрозонах с повышенным содержанием органического вещества.
Актиномицеты доминируют на поздних стадиях микробной сукцессии, когда создаются условия для использования труднодоступных субстратов. Активация актиномицетной микрофлоры происходит при внесении в почву крахмала, хитина, нефтепродуктов и т. д.. В то же время из-за медленного роста актиномицеты не способны конкурировать с немицелиальными бактериями за легкодоступные вещества. Возможно, что вторичные метаболиты (в особенности, меланоидные пигменты) играют какую-то роль в образовании гумуса.
Ценозообразующую роль актиномицеты играют в местах первичного почвообразования, находясь в этих условиях в ассоциации с водорослью. Эти ассоциации в лабораторных условиях формировали лишайникоподобный таллом (актинолишайник).
Актиномицеты (рода Streptomyces, Streptosporangium, Micromonospora, Actinomadura) являются постоянными обитателями кишечника дождевых червей, термитов и многих других беспозвоночных. Разрушая целлюлозу и другие биополимеры, они являются их симбионтами. Представители рода Frankia способны к азотфиксации и образованию клубеньков у небобовых растений (облепиха, ольха и др.). Есть патогенные формы, вызывающие актиномикоз. В организме человека обитают в ротовой полости, в кишечнике, в дыхательных путях, на коже, в зубном налете, в кариозных зубах, на миндалинах.
Отношение к факторам внешней среды
Большинство актиномицетов — аэробы, факультативные анаэробы присутствуют лишь среди актиномицетов с непродолжительной мицелиальной стадией. Здесь усматривается некоторая параллель с грибами, среди которых лишь немицелиальные дрожжи также способны жить в анаэробных условиях. Предполагается что менее эффективный анаэробный тип метаболизма успешен при большей относительной поверхности клеток, которая достигается фрагментацией мицелия.
Считается что актиномицеты более устойчивы к высушиванию чем немицелиальные бактерии, благодаря чему они доминируют в пустынных почвах. Лабораторное хранение почвенных образцов в условиях, не способствующих вегетативному росту прокариот увеличивает относительное содержание актиномицетов, учитываемое методом посева. Особенно долго способны сохраняться при высушивании склероции, образуемые родом Chainia. Показано что при aw=0,50 некоторые споры прорастают (р. Streptomyces, Micromonospora), однако образовавшийся мицелий не ветвится. При aw=0,86 прорастают споры практически всех актиномицетов, у некоторых мицелий ветвится, образуются микроколонии, оптимум достигается при aw=0,95.
Чаще всего актиномицеты нейтрофилы, однако некоторые роды ацидофильны или алкалофильны. Характерным свойством актиномицетов является ацидотолерантность, благодаря чему их доля в микробном комплексе лесных почв относительно высока. Отмечено что на кислой среде продлевается вегетативная стадия, на щелочной, напротив, ускоряется спорообразование.
Актиномицеты не требовательны к содержанию органического углерода в среде, многие из них способны расти на «голодном» агар-агаре. Представители рода Nocardia способны осуществлять хемосинтез, окисляя водород, метан и метанол. Широко среди актиномицетов распространена править] Биохимические особенности
Для актиномицетов отмечается наличие редких метаболических путей и ферментных систем. Например, для них характерен путь расщепления глюкозы Энтнера-Дудорова, встречается полифосфатгексокиназа (вместо обычной гексокиназы), существуют особенности в синтезе ряда аминокислот; во вторичном метаболизме им свойственен шикиматный путь синтеза ароматических соединений, включение цельных углеродных скелетов глюкозы во вторичные метаболиты, например, антибиотики.
Отличительной особенностью актиномицетов является способность к синтезу физиологически-активных веществ, антибиотиков, пигментов, пахучих соединений. Именно ими формируется специфический запах почвы и иногда воды (вещества геосмин, аргосмин, муцидон, 2-метил-изоборнеол). Актиномицеты являются активными продуцентами антибиотиков, образуя до половины известных науке.
Группы родов актиномицетов по 9 изданию определителя Берджи
Нокардиоформные актиномицеты
Аэробные организмы, имеющие в цикле развития мицелиальную стадию. Мицелий может распадаться на элементы, образуя цепочки, подобные спорангиям. Настоящих спор нет. Сюда относят род Nocardia, Rhodococcus, способный использовать углеводороды нефти, Promicromonospora, Actinobispora, Oerskovia и др.. деление на роды — по хемотипу клеточной стенки и другим хемотаксономическим признакам.
Роды с многогнездовыми спорангиями
Образующийся мицелий делится на отдельные кокковидные клетки, подвижные у Geodermatophilus и Dermatophilus и неподвижные у Frankia. Франкии — азотфиксирующие симбионты ольхи и других небобовых растений, образующие на их корнях клубеньки. Место обитания: почва, воды и кожа млекопитающих.
Актинопланы
В цикле развития имеют подвижную стадию и стадию образования развитого мицелия, разделенного перегородками. Сапротрофы и факультативные паразиты. Распространены в почве, лесной подстилке, животных останках и воде природных источников, часто развиваясь на пыльце попавших в неё растений. Разделяются на роды по типам спорангиев:
- Подвижные споры в спорангиях (Actinoplanes, Ampullariella, Dactylosporangium, Pilimelia)
- Неподвижные споры
- Одиночные (Micromonospora)
- В цепочках (Catellatospora)
Тип клеточной стенки II (содержит мезо-ДАПК и глицин).
Стрептомицеты и близкие роды
Образуют хорошо развитый воздушный мицелий, не распадающийся в процессе развития на отдельные клетки. Спорангии состоят из прямых или закрученных спиралью цепочек неподвижных спор. Обитают в почве, характеризуются сильной антибиотической и хитиноразлагающей активностью.
Тип клеточной стенки I (содержит L-ДАПК)
Мадуромицеты
Мицелий также не распадается на отдельные клетки. Споры только на воздушном мицелии в цепочках или спорангиях, как подвижные так и нет. Группа плохо изучена и требует ревизии. Образуют короткие цепочки спор (Actinomadura и др.), спорангии с неподвижными (Planomonospora) или подвижными спорами (Streptosporangium).
Типы клеточных стенок II—IV. В гидролизатах целых клеток обнаруживается мадуроза.
Термомоноспоры и близкие роды
Развитый мицелий, споры расположены одиночно, в цепочках или спорангиеподобных структурах. Тип клеточной стенки III (мезо-ДАПК, нет дифференцирующих сахаров).
Род Termoactynomyces
Термоактиномицеты образуют типичные эндоспоры и по этому признаку, а также по строению 16s рРНК должны быть отнесены к бациллам, однако образуют развитый мицелий. Термофилы, способные расти в диапазоне 40—48 градусов по Цельсию.
История изучения
В 1874 Ф. Кон в пробе из слёзного канала человека впервые обнаружил нитчатую бактерию, названную в честь врача, взявшего пробу Streptothrix foersteri. Поскольку родовое название Strepothrix уже было занято грибом, позднее бактерия была переименована в Streptomyces foersteri. В 1877 патолог Боллингер и ботаник Гарц исследовали опухоли (актиномикозные узлы) коров и обнаружили их возбудителя, которого из-за лучистого расположения нитей назвали лучистым грибком (Actinomyces). Это название вскоре стало собирательным для нескольких близких родов.
В 1884 немецкий врач Джеймс Израиль получил первую чистую культуру актиномицета (Actinomyces israelii). В дальнейшем было обнаружено множество патогенных форм (1888 — из ноги больного мадуровой болезнью человека Нокардом был выделен первый представитель рода Nocardia), в 1890—1892 Госпирини составил список родов актиномицетов.
В 1912—1916 стали появляться первые описания непатогенных актиномицетов, выделенных из обычных природных субстратов. В этот период свой вклад в развитие актиномицетологии внесли С. А. Ваксман, Краинский, Рудольф Лиске.
Новый этап развития науки начался в 1939, когда Красильников получил в нативном виде антибиотик мицетин, выделяемый стрептомицетами. В 1945 Ваксман, Шатц и Буги выделили стрептомицин. На актиномицеты оказалось обращено большое внимание, однако в основном развивались прикладные аспекты актиномицетологии, связанные с получением и применением антибиотиков. Тем не менее в это период также были получены сведения об экологии, биохимии, строении, циклах развития, которые в свою очередь позволили разработать принципы классификации актиномицетов.
С 1980-х-1990-х внимание переключилось на изучение экологических функций актиномицетов, их взаимоотношения в естественных условиях с животными, растениями и микроорганизмами. Происходит пересмотр систематики, связанный с получением данных о геноме актиномицетов.
Примечания
- ↑ Звягинцев Д. Г. Почва и микроорганизмы. — М.: 1987
Литература
- Зенова Г. М. Почвенные актиномицеты. — М.: Изд-во МГУ, 1992. — ISBN 5-211-02902-X
- Определитель бактерий Берджи. В 2-х т. Т. 2: Пер. с англ./Под ред. Дж. Хоула, Н. Крига, П. Снита, Дж. Стейли, С. Уилльямса. — М.: Мир, 1997. — 368 с., ил. — ISBN 5-03-003112-X
dic.academic.ru
г.Самара, ул. Димитрова 131 [email protected] |
 |