|
|
||||||||||
|
Эра антибиотиков закончилась. И что теперь? Конец антибиотикаКонец эры антибиотиков | SOFTMIXER
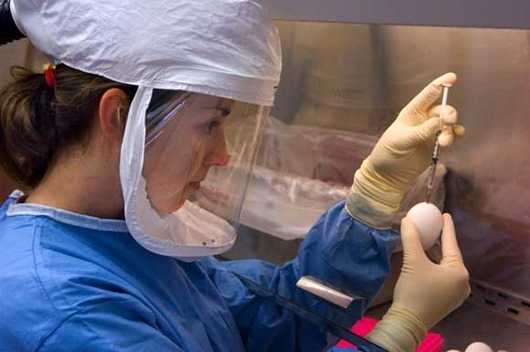
Когда Александр Флеминг в 1928 году, обнаружил в своей лаборатории стол, заражённый плесенью Penicillium notatum, он начал новую эру превосходства науки над природой. С тех пор антибиотики спасли миллионы жизней и избавили огромное количество людей от страданий. Но с самого начала этой эры учёным было известно, что ей придёт конец. Они просто не знали, когда именно… Сопротивляемость бактерий антибиотикам естественна и неизбежна. По воле случая у нескольких бактерий окажутся гены, способные защитить их от лекарств, они передадут эти гены дальше – и не только своему потомству, но иногда и соседям. Специалисты по вычислительной эпидемиологии наконец получают нужные данные и обрабатывают их для моделирования этого явления. Но никто не пытается использовать эти инструменты, чтобы предсказать конец эры антибиотиков – он уже наступил. Они концентрируются на том, чтобы понять, как скоро стойкие бактерии окажутся в большинстве и что доктора смогут с ними сделать – если это вообще возможно. В 2013 году тогдашний директор Центра по контролю и предотвращению заболеваний (CDC) Том Фриден сказал журналистам: «Если мы не будем вести себя осторожно, вскоре мы окажемся в постантибиотической эпохе». Сегодня, всего лишь четыре года спустя, это агентство утверждает, что мы в ней оказались.
«Мы говорим это потому, что появилась универсально стойкая бактерия», – говорит Джин Пател [Jean Patel], руководящая отделением CDC по стратегии и координации использования антибиотиков. «Люди умирают из-за отсутствия антибиотиков, способных лечить их инфекции – инфекции, которые не так давно было очень легко излечивать». В прошлом августе женщина возрастом за 70 попала в госпиталь в Рено, шт. Невада, с бактериальной инфекцией бедра. Бактерия принадлежала к классу особенно упорных микробов, известных, как карбапенем-устойчивые энтеробактерии (CRE). Но эту бактерию не брали ни карбапенемы, ни тетрациклин, ни колистин, и вообще никакой антибактериальный аппарат из 26-и имеющихся в продаже. Через несколько недель она умерла от септического шока. Для чиновников из области здравоохранения, к коим принадлежит и Пател, этот случай отмечает конец эры и начало новой. Вопрос в следующем: как быстро эта универсальная стойкость сможет распространиться? «Когда мы дойдём до ситуации, в которой инфекцию чаще будет невозможно вылечить, чем возможно? – говорит Пател. – Это будет очень сложно предсказать». Ей это точно известно, потому что она уже пыталась. В 2002 году первый стафилококк, устойчивый к ванкомицину, проявил себя у 40-летнего мужчины из Мичигана с хронической язвой ноги. Ситуация казалась весьма печальной: стафилококк – одна из самых распространённых инфекций у людей, а ванкомицин – самый распространённый антибиотик для его лечения. Кроме того, резистивный ген был расположен на плазмиде – свободно перемещающемся колечке ДНК, что позволяло ему легко передвигаться. Эпидемиологи из CDC работали совместно с микробиологами, такими, как Пател, над созданием модели, предсказывающей как далеко и как быстро он сможет распространиться. Пател не помнит точных цифр, но она вспоминает, что результаты получились пугающими. «Мы очень сильно озаботились этим вопросом», – говорит она.
К счастью, в данном случае модели ошиблись. С 2002 года было зафиксировано только 13 случаев появления стафилококка, устойчивого к ванкомицину, и все пациенты выжили. Такая ошибка весьма озадачила команды. Но в биологии иногда бывают такие сложности. «Я работала с этой бактерией в лабораториях, где она прекрасно растёт, но от человека к человеку, судя по всему, не распространяется», – говорит Пател. И хотя они ещё не знают, почему, одна из гипотез говорит о том, что появление этого резистентного гена не проходит для бактерии бесследно. Он сделал стафилококк невосприимчивым к его заклятому врагу, одновременно усложняя процесс выживания вне человеческого тела. Больничные правила, время года, география также могут влиять на распространение. Это похоже на попытки предсказания погоды. «Не получится сделать такие предсказания на бумаге или путём пристальных размышлений, – говорит Брюс Ли [Bruce Lee], исследователь общественного здравоохранения в институте Джона Хопкинса. Он работает с организациями, занимающимися здравоохранением в Чикаго и округе Ориндж, предсказывая наиболее вероятные пути распространения CRE – бактерий того типа, что убила женщину в Неваде – в случае их появления в больницах. В прошлом такие модели были основаны исключительно на математике – так Пател пыталась строить свои предсказания. Да, их уравнения были сложными, но не настолько, чтобы принять во внимание такие вещи, как человеческое поведение, биология бактерий и их взаимодействие с окружающей средой. „В нашей области люди всё больше начинают понимать, что для того, чтобы разобраться с распространением устойчивых к антибиотикам бактерий с достаточной степенью детализации, необходимо работать с моделями на основе данных, в которых можно просматривать миллионы различных сценариев – так, как это делают метеорологи“, – говорит Ли. В исследовании, опубликованном Ли в прошлом году, он описывает вероятность распространения CRE в 28 больницах и 74 частных лечебницах округа Ориндж. В этой модели у каждой виртуальной больницы было прописано количество коек, совпадающих с количеством коек в реальных учреждениях, а также вся информация по поводу связности учреждений.
В модели каждый пациент был вычислительной единицей, которая в любой определённый день либо переносит, либо не переносит CRE. Эти единицы двигались по экосистеме здравоохранения, взаимодействовали с врачами, медсёстрами, койками, стульями, дверьми по сотне миллионов раз, причём с каждой новой симуляцией эти параметры немного подстраивались. Он обнаружил, что без усиления мер по контролю, например, регулярной проверки пациентов на сопротивляемость и карантине переносчиков, CRE станет эндемическим заболеванием — постоянно присутствующим – практически во всех больницах округа Ориндж через десять лет. А после того, как CRE проникнет в систему здравоохранения, от него будет сложно избавиться. „Это как пытаться прогнать из дома термитов, – говорит Ли. – Как только они пробираются туда, где всё связано со всем, они становятся трудноизлечимой частью экосистемы“. Так что, если доктора смогут быстро идентифицировать людей, способных распространять CRE, он смогут хотя бы изолировать угрозу. Даже если самим пациентам они ничего предложить не сумеют. Пока хорошие новости заключаются в том, что единственные случаи передачи от человека к человеку на 100% стойкой бактерии происходят только в суперкомпьютере у Ли. В реальном мире таких случаев не зафиксировано. Но именно их и ищут Пател и CDC. Это и продвинет ситуацию на следующий уровень, говорит Пател. Чтобы держать руку на пульсе, в прошлом году агентство потратило $14,4 млн на создание сети из семи местных лабораторий, способных проводить генетическое тестирование бактериальных проб, взятых из больниц. Сейчас они претворяют в жизнь программу, которая когда-нибудь сможет связать все больницы в США с системой слежения CDC напрямую, чтобы автоматически отмечать каждое произошедшее в США событие, связанное со стойкими к антибиотикам бактериями, в реальном времени.
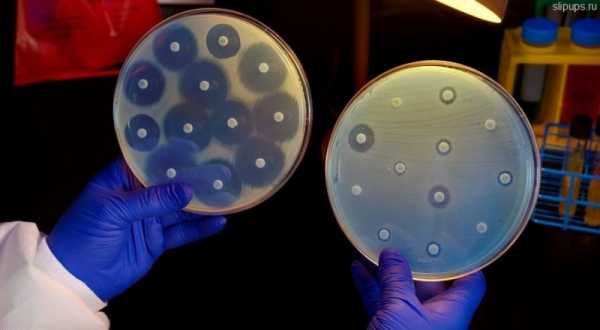
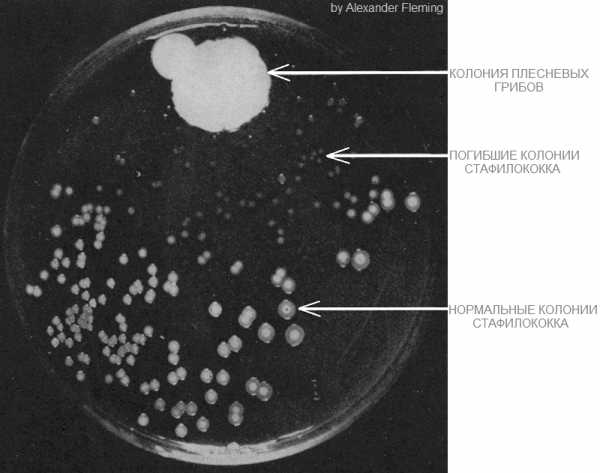
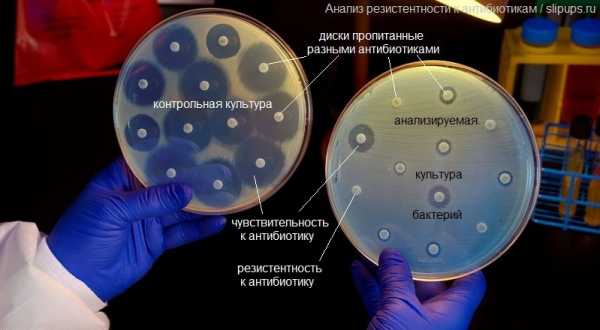
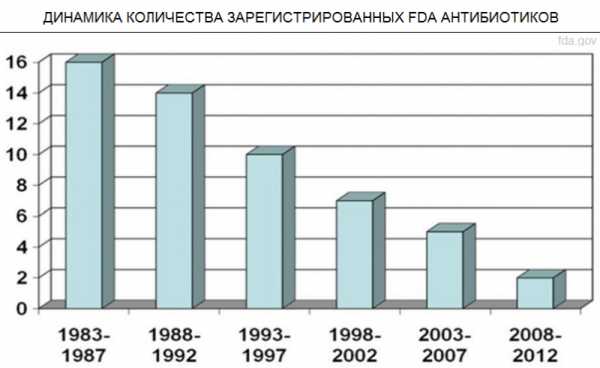
Параллельно Пател, и, с переменным успехом, остальной мир, следит за разработкой антибиотиков. В этой области тоже не всё гладко. На прошлой неделе Всемирная организация здравоохранения выпустила отчёт с анализом всех находящихся в разработке антибактериальных лекарств. Выводы мрачные: недостаточно лекарств, недостаточно инноваций. На каждое новое лекарство из 51 варианта уже можно найти заранее устойчивые к нему микроорганизмы. Исследователи, такие, как Пател и Ли, надеются, что их работа позволить минимизировать существующие угрозы, обнаружить новые по мере их появления, и дать фармакологическим компаниям время на разработку новых лекарств. Эра антибиотиков, возможно, и закончилась – но с наступающей новой эрой ещё многое можно сделать. link Похожие материалы:www.softmixer.com Эре антибиотиков приходит конец - Санкт-Петербург: статьиПривычные лекарства с каждым годом работают все хуже и хуже 14 июня 2017 в 18:48, просмотров: 1907О том, как не вернуться в «доантибиотическую эру», «МК» в Питере» рассказал Сергей Сидоренко, доктор медицинских наук, профессор кафедры микробиологии и микологии СЗГМУ им. Мечникова.  К 2050 году — 10 миллионов жертв — Сергей Валентинович, насколько ужасно было бы возвращение в «доантибиотическую эру»?— Мы забыли те времена, когда воспаление легких или гнойный фурункул на ноге были вполне «нормальными» причинами смерти человека. Менингит был однозначно приговором (сейчас нам удалось снизить смертность до 10 процентов). После появления антибиотиков начиная с 40-х годов смертность от инфекций в развитых странах сократилась в 10 раз. В 70-е годы нам казалось, что инфекции побеждены навсегда. О том, как жилось до их изобретения, забыли не только обыватели, но и сами врачи. К сожалению, в начале XXI века наступил так называемый кризис антибиотиков. Об этом говорят цифры — в среднем трех-пяти лет после начала массового употребления лекарства достаточно, чтобы микробы начали к нему адаптироваться. При этом с 2010 по 2015 год в практику было внедрено лишь два новых антибиотика. — Насколько плохи дела? Как быстро растет устойчивость бактерий к уже существующим лекарствам?— Уже сейчас ситуация хуже, чем семь лет назад. Врачи сталкиваются с этим каждый день. В случае легких инфекций врач может и не отдавать себе отчет, что все больший процент пациентов не реагирует на назначенный курс лечения и нужно менять один препарат на другой. Реаниматологи в больницах, наоборот, замечают, что несколько лет назад от перитонита умирало меньше людей, чем сейчас. Правительство Великобритании провело независимое исследование, чтобы спрогнозировать смертность от антибиотикорезистентности к 2050 году. Выяснилось, что если устойчивость к антибиотикам будет расти с той же скоростью, что и сейчас, то через 30 лет от «привыкших» к лекарствам микробов ежегодно будет умирать около 10 миллионов человек. Сейчас по той же причине в странах, где ведется подобный учет — в Европе и Америке, — умирает несколько десятков тысяч человек в год. Съездить в Индию за «супербактерией» — Какие микробы сегодня представляют особую опасность?— Есть так называемые супербактерии, которые устойчивы к карбапенемам. Так называется группа антибиотиков, которые до сегодняшнего дня считались «палочкой-выручалочкой» при самых тяжелых инфекциях. Но сейчас появились бактерии, ферменты которых устойчивы к этим препаратам. Самая большая беда в том, что в ближайшие 5–6 лет на рынке не появится антибиотиков, которые заменят карбапенемы. — Откуда взялась эта «супербактерия»? — Ее источником изначально является Индия. Там 40 процентов здорового населения носят ее в себе. Скорость распространения колоссальная. Трое из 57 туристов, посетивших Индию, возвращаются домой с этой бактерией в кишечнике. У них ничего не болит, и при счастливом стечении обстоятельств через 3–4 месяца она из кишечника уйдет. Но если в этот период у них случится, например, аппендицит, то их перспективы будут крайне сомнительны. В Россию импорт этих устойчивых бактерий происходит в больших объемах, но пока мы видим только верхушку айсберга. Новое поколение бактерий появляется за 10 минут, а антибиотиков — за 10 лет Проблеме антибиотикорезистентности бактерий была посвящена отдельная сессия на недавнем Петербургском международном экономическом форуме. Эксперты назвали сложившуюся ситуацию неравным боем. А виной всему — человеческая беспечность и жадность фермеров. Открытие пенициллина изменило эволюцию Ученые подсчитали: на Земле обитает примерно 10 в 30-й степени бактерий. За 3,5 миллиарда лет, что они живут на планете, эти существа приспособились к жизни практически во всех средах. — Открытие пенициллина стало огромным прорывом в борьбе с бактериями, но не решило проблему. Они обитают даже в вулканах, и уж тем более могут адаптироваться к антибиотикам. А человечество почивало на лаврах, мы решили, что уже все хорошо. И упустили время. Использование антибиотиков изменило эволюцию бактерий, — объяснил председатель комиссии по антимикробной резистентности Ассоциации британской фармпромышленности Джеймс Андерсон. — Проблема резистентности стала следствием нашей беспечности. Эта беспечность проявлялась по-разному. Так, в нашей стране до сих пор можно спокойно купить антибиотики в аптеке, хотя практически на всех упаковках подобных препаратов написано, что их следует отпускать только по рецепту врача. США в свое время затормозили разработки новых антибиотиков. Примерно 15 лет назад там были сильно ужесточены правила регистрации таких препаратов. — И тогда многие компании приостановили разработки антибиотиков. Им это было коммерчески невыгодно. А США — это около 40–50 процентов мирового рынка антибиотиков. И их действия оказали существенное влияние на процесс разработок по всему миру, — рассказал гендиректор одной из крупнейших российских фармкомпаний Василий Игнатьев. Сейчас, когда о проблеме резистентности заговорили на международном уровне, начали обсуждать ситуацию в ООН, правила, наоборот, смягчились. Разработки активизировались. Но, как заметил представитель крупной американской фармкомпании Стефен Бриггер Лунд, «для образования нового поколения бактерий требуется 10 минут, а на разработку нового антибиотика уходит 10 лет». Злоупотребляют все Ввязавшись в бой с бактериями, человечество начало его проигрывать из-за своих же ошибок. — Золотой век антибиотиков, в моем понимании, закончился в 1970-х. Сообщения об антибиотикорезистентности появились в 1940-х. А бурно об этом заговорили в 1980–1990-е, именно когда антибиотики начали массового использовать в сельском хозяйстве, — говорит замглавы Россельхознадзора Николай Власов. В конце XX века антибиотики стали очень активно применять не только для лечения скота, но и в качестве стимуляторов роста животных. В ответ бактерии начали еще быстрее приспосабливаться, причем как в организмах самих животных, так и в людях, которые получают антибиотики с мясом и прочими продуктами. — Да, бактерии приобретают устойчивость из-за неправильного применения препаратов в медицине, но еще больше этот эффект формируется и становится устойчивым в результате роста стимулирующего использования антибиотиков в сельском хозяйстве, — уверен Николай Власов. — Пока мы не поссорились с Европой и Америкой, у нас были десятки тысяч случаев в год, когда мы задерживали на границе грузы с превышающим допустимые нормы остаточным содержанием антибиотиков. Причем это были товары даже из Дании, которая, в моем понимании, образец правильного поведения. Но и там злоупотребляли. То есть это повсеместная проблема. Сейчас задерживаем и из Южной Америки. Власов также обратил внимание, что уже сейчас в США антибиотики применяются в сельском хозяйстве и для борьбы с болезнями растений, «а это еще более опасно, чем лечение животных». Надежда есть! — Способность бактерий приспосабливаться к антибиотикам обуславливается механизмами популяционной адаптации, которая заключается в последовательном, генетически запрограммированном повышении или понижении выработки определенного набора белков, — рассказал член-корреспондент РАН Алексей Тутельян. — Они как раз и позволяют бактериальной клетке выжить в неблагоприятной среде, в том числе и под воздействием антибиотиков, дезинсектантов, антисептиков. Эти белки сейчас рассматриваются учеными как потенциальные мишени, при создании нового типа препаратов, которые будут блокировать адаптационные возможности бактерий. Таким образом в ближайшее время, возможно, будет найдена альтернатива антибиотикам — препараты, которые станут не просто убивать бактерии, а лишат их главного оружия — возможности приспосабливаться. spb.mk.ru Эра антибиотиков закончилась. И что дальше? Когда Александр Флеминг вернулся из отпуска летом 1928 года, и обнаружил в своей лондонской лаборатории стол, заражённый плесенью Penicillium notatum, он начал новую эру превосходства науки над природой. С тех пор антибиотики, как открытые им лично, так и множество других, открытых благодаря его работам, спасли миллионы жизней и избавили огромное количество людей от страданий. Но с самого начала этой эры учёным было известно, что ей придёт конец. Они просто не знали, когда именно. Когда Александр Флеминг вернулся из отпуска летом 1928 года, и обнаружил в своей лондонской лаборатории стол, заражённый плесенью Penicillium notatum, он начал новую эру превосходства науки над природой. С тех пор антибиотики, как открытые им лично, так и множество других, открытых благодаря его работам, спасли миллионы жизней и избавили огромное количество людей от страданий. Но с самого начала этой эры учёным было известно, что ей придёт конец. Они просто не знали, когда именно.Сопротивляемость бактерий антибиотикам естественна и неизбежна. По воле случая у нескольких бактерий окажутся гены, способные защитить их от лекарств, они передадут эти гены дальше – и не только своему потомству, но иногда и соседям. Специалисты по вычислительной эпидемиологии наконец получают нужные данные и обрабатывают их для моделирования этого явления. Но никто не пытается использовать эти инструменты, чтобы предсказать конец эры антибиотиков – он уже наступил. Они концентрируются на том, чтобы понять, как скоро стойкие бактерии окажутся в большинстве и что доктора смогут с ними сделать – если это вообще возможно. В 2013 году тогдашний директор Центров по контролю и предотвращению заболеваний (CDC) Том Фриден сказал журналистам: «Если мы не будем вести себя осторожно, вскоре мы окажемся в постантибиотической эпохе». Сегодня, всего лишь четыре года спустя, это агентство утверждает, что мы в ней оказались. «Мы говорим это потому, что универсально стойкая бактерия появилась», – говорит Джин Пател [Jean Patel], руководящая отделением CDC по стратегии и координации использования антибиотиков. «Люди умирают из-за отсутствия антибиотиков, способных лечить их инфекции – инфекции, которые не так давно было очень легко излечивать». В прошлом августе женщина возрастом за 70 попала в госпиталь в Рено, шт. Невада, США, с бактериальной инфекцией бедра. Бактерия принадлежала к классу особенно упорных микробов, известных, как карбапенем-устойчивые энтеробактерии (CRE). Но эту бактерию не брали ни карбапенемы, ни тетрациклин, ни колистин, и вообще никакой антибактериальный аппарат из 26-и имеющихся в продаже. Через несколько недель она умерла от септического шока. Для чиновников из области здравоохранения, к коим принадлежит и Пател, этот случай отмечает конец эры и начало новой. Вопрос в следующем: как быстро эта универсальная стойкость сможет распространиться? «Когда мы дойдём до ситуации, в которой инфекцию чаще будет невозможно вылечить, чем возможно? – говорит Пател. – Это будет очень сложно предсказать». Ей это точно известно, потому что она уже пыталась. В 2002 году первый стафилококк, устойчивый к ванкомицину, проявил себя у 40-летнего мужчины из Мичигана с хронической язвой ноги. Ситуация казалась весьма печальной: стафилококк – одна из самых распространённых инфекций у людей, а ванкомицин – самый распространённый антибиотик для его лечения. Кроме того, резистивный ген был расположен на плазмиде – свободно перемещающемся колечке ДНК, что позволяло ему легко передвигаться. Эпидемиологи из CDC работали совместно с микробиологами, такими, как Пател, над созданием модели, предсказывающей как далеко и как быстро он сможет распространиться. Пател не помнит точных цифр, но она вспоминает, что результаты получились пугающими. «Мы очень сильно озаботились этим вопросом», – говорит она. К счастью, в данном случае модели ошиблись. С 2002 года было зафиксировано только 13 случаев появления стафилококка, устойчивого к ванкомицину, и все пациенты выжили. Такая ошибка весьма озадачила команды. Но в биологии иногда бывают такие сложности. «Я работала с этой бактерией в лабораториях, где она прекрасно растёт, но от человека к человеку, судя по всему, не распространяется», – говорит Пател. И хотя они ещё не знают, почему, одна из гипотез говорит о том, что появление этого резистентного гена не проходит для бактерии бесследно. Он сделал стафилококк невосприимчивым к его заклятому врагу, одновременно усложняя процесс выживания вне человеческого тела. Больничные правила, время года, география также могут влиять на распространение. Это похоже на попытки предсказания погоды. «Не получится сделать такие предсказания на бумаге или путём пристальных размышлений, – говорит Брюс Ли [Bruce Lee], исследователь общественного здравоохранения в институте Джона Хопкинса. Он работает с организациями, занимающимися здравоохранением в Чикаго и округе Ориндж, предсказывая наиболее вероятные пути распространения CRE – бактерий того типа, что убила женщину в Неваде – в случае их появления в больницах. В прошлом такие модели были основаны исключительно на математике – так Пател пыталась строить свои предсказания. Да, их уравнения были сложными, но не настолько, чтобы принять во внимание такие вещи, как человеческое поведение, биология бактерий и их взаимодействие с окружающей средой. „В нашей области люди всё больше начинают понимать, что для того, чтобы разобраться с распространением устойчивых к антибиотикам бактерий с достаточной степенью детализации, необходимо работать с моделями на основе данных, в которых можно просматривать миллионы различных сценариев – так, как это делают метеорологи“, – говорит Ли. В исследовании, опубликованном Ли в прошлом году, он описывает вероятность распространения CRE в 28 больницах и 74 частных лечебницах округа Ориндж. В этой модели у каждой виртуальной больницы было прописано количество коек, совпадающих с количеством коек в реальных учреждениях, а также вся информация по поводу связности учреждений. В модели каждый пациент был вычислительной единицей, которая в любой определённый день либо переносит, либо не переносит CRE. Эти единицы двигались по экосистеме здравоохранения, взаимодействовали с врачами, медсёстрами, койками, стульями, дверьми по сотне миллионов раз, причём с каждой новой симуляцией эти параметры немного подстраивались. Он обнаружил, что без усиления мер по контролю, например, регулярной проверки пациентов на сопротивляемость и карантине переносчиков, CRE станет эндемическим заболеванием — постоянно присутствующим – практически во всех больницах округа Ориндж через десять лет. А после того, как CRE проникнет в систему здравоохранения, от него будет сложно избавиться. „Это как пытаться прогнать из дома термитов, – говорит Ли. – Как только они пробираются туда, где всё связано со всем, они становятся трудноизлечимой частью экосистемы“. Так что, если доктора и сёстры смогут быстро идентифицировать людей, способных распространять CRE, он смогут хотя бы изолировать угрозу. Даже если самим пациентам они ничего предложить не сумеют. Пока хорошие новости заключаются в том, что единственные случаи передачи от человека к человеку на 100% стойкой бактерии происходят только в суперкомпьютере у Ли. В реальном мире таких случаев не зафиксировано. Но именно их и ищут Пател и CDC. Это и продвинет ситуацию на следующий уровень, говорит Пател. Чтобы держать руку на пульсе, в прошлом году агентство потратило $14,4 млн на создание сети из семи местных лабораторий, способных проводить генетическое тестирование бактериальных проб, взятых из больниц. Сейчас они претворяют в жизнь программу, которая когда-нибудь сможет связать все больницы в США с системой слежения CDC напрямую, чтобы автоматически отмечать каждое произошедшее в США событие, связанное со стойкими к антибиотикам бактериями, в реальном времени. Параллельно Пател, и, с переменным успехом, остальной мир, следит за разработкой антибиотиков. В этой области тоже не всё гладко. На прошлой неделе Всемирная организация здравоохранения выпустила отчёт с анализом всех находящихся в разработке антибактериальных лекарств. Выводы мрачные: недостаточно лекарств, недостаточно инноваций. На каждое новое лекарство из 51 варианта уже можно найти заранее устойчивые к нему микроорганизмы. Исследователи, такие, как Пател и Ли, надеются, что их работа позволить минимизировать существующие угрозы, обнаружить новые по мере их появления, и дать фармакологическим компаниям время на разработку новых лекарств. Эра антибиотиков, возможно, и закончилась – но с наступающей новой эрой ещё многое можно сделать. Материал из ВикипедииСэр Александр Флеминг (англ. Sir Alexander Fleming; 6 августа 1881, Дарвел[en] — 11 марта 1955, Лондон) — британский бактериолог. Открыл лизоцим (антибактериальный фермент, вырабатываемый человеческим организмом) и впервые выделил пенициллин из плесневых грибов Penicillium notatum[en] — исторически первый антибиотик.Оба открытия произошли в 1920-е годы и в большой степени случайно. Однажды, когда Флеминг был простужен, он посеял слизь из собственного носа на чашку Петри, в которой находились бактерии, и через несколько дней обнаружил, что в местах, куда была нанесена слизь, бактерии были уничтожены. Первая статья о лизоциме вышла в 1922 году. Беспорядок в лаборатории Флеминга ещё раз сослужил ему службу. В 1928 году он обнаружил, что на агаре в одной из чашек Петри с бактериями Staphylococcus aureus выросла колония плесневых грибов. Колонии бактерий вокруг плесневых грибов стали прозрачными из-за разрушения клеток. Флемингу удалось выделить активное вещество, разрушающее бактериальные клетки, — пенициллин, работа была опубликована в 1929 году. Флеминг не ожидал, что получить пенициллин в чистом виде будет настолько трудно. Его работу продолжили Говард Флори и Эрнст Борис Чейн, разработавшие методы очистки пенициллина. Массовое производство пенициллина было налажено во время Второй мировой войны. В 1945 году Флеминг, Флори и Чейн были удостоены Нобелевской премии в области физиологии и медицины. В сентябре 1945 накануне приезда во французскую столицу Александра Флеминга парижские газеты писали:«Для разгрома фашизма и освобождения Франции он сделал больше целых дивизий» В 1999 году журнал «Тайм» назвал Флеминга одним из ста самых важных людей XX века за его открытие пенициллина и сообщил:Это открытие изменит ход истории. Вещество, которое Флеминг назвал пенициллином, является очень активным противоинфекционным средством. После того, как возможности данного соединения были оценены по достоинству, пенициллин стал неотъемлемой частью любой методики лечения бактериальных инфекций. К середине века открытое Флемингом вещество широко вошло в производство фармацевтических препаратов, стал осуществляться его искусственный синтез, что помогло справляться с большинством древнейших заболеваний, таких как сифилис, гангрена и туберкулёз. russiahousenews.info Конец эры антибиотиков: почему супербактерии побеждаютglagolas — 27.10.2017 — Медицина Женщина в результате открытого перелома получила инфекцию бедренной кости и после безуспешной антибиотикотерапии умерла от септического шока. Патогеном оказалась представитель нормальной флоры человека - клебсиелла, устойчивая сразу ко всем 26 антибиотикам зарегистрированным в США.Ежегодно 23 000 человек в США, 25 000 в Европе и около 700 000 в мире погибает от бактериальных инфекций устойчивых к существующим антибиотикам. Прогнозируется, что через 30 лет смертность от супербактерий достигнет 10 млн. человек в год. На этом фоне сокращаются инвестиции в разработку новых антибиотиков. Сегодня расскажу о том, почему безобидные бактерии превращаются в агрессивные и устойчивые к лекарствам супербактерии, а разработка новых антибиотиков становится невыгодной. Случайное открытие антибиотиков Александр Флеминг знаменит непозволительной для бактериолога неряшливостью. В 1922 году уронив слизь из своего простуженного носа на культуру бактерий он наблюдал лизис колоний и так открыл фермент лизоцим. А в 1928 году случайно занес споры плесени в культуру стафилококка и обнаружил, что вокруг выросшего гриба все бактерии погибли: Флеминг догадался, что плесень синтезирует бактерицидное вещество с целью вытеснить конкурирующих за питательный субстрат бактерии. Выделенный из плесени пенициллин оказался эффективнее широко применяемых тогда хирургами наружных антисептиков. В отличие от антисептиков пенициллин можно вводить внутрь организма для борьбы с инфекцией в любых тканях и органах, а антибактериальная активность сохранялась даже после разведения препарата в 800 раз. Высокая активность мизерных доз позже была объяснена механизмом действия пенициллина. В отличие от антисептиков, которые лишь при высоких концентрациях разрушают клеточную стенку бактерии, пенициллин проникает внутрь клетки и прицельно блокирует синтез биополимера, необходимого для сборки клеточной стенки бактерии. Антибиотики - биологическое оружие в войне грибов и бактерий Однако вскоре Флеминг обнаружил, что если применить слишком низкую концентрацию пенициллина или вводить его короткое время, то выжившие колонии бактерий приобретают устойчивость к ранее эффективным дозам препарата. Позднее было установлено, что стафилококки имеют врожденную способность к синтезу фермента разрушающего пенициллин. Это своего рода антидот или противоракетная оборона, где вместо ракет противника - бактерицидное оружие грибов, а вместо противоракет - фермент расщепляющий бактерицид. Сегодня хорошо известно, что подобные противостояния происходят в природных условиях не только между грибами и бактериями, но даже между близкородственными видами одного рода бактерий. Ведь чем ближе родство, тем более одинакова ниша и субстрат, за которые нужно конкурировать. Например, прямо сейчас разные виды стафилококков ведут непрерывную борьбу за нишу на слизистых вашего рта, одновременно вырабатывая бактерицидные вещества и антидоты. Так что, если вам кажется, что только люди убивают друг друга в борьбе за территорию и ресурсы, посмотрите на этот снимок посева из полости рта здорового человека и представьте, какая резня идет сейчас у вас во рту: Однако в этой войне нет победителей и проигравших - миллионы лет эволюционного противостояния сотен видов микроорганизмов нашей микрофлоры обернулись балансом, который оказался бесценным приобретением для макроорганизма. Все ниши плотно заселены разношерстной флорой, где поголовье каждого вида строго ограничено бактерицидной активностью соседей, а также размерами ниши и иммунитетом макроорганизма. Например, вызывающий гнойные инфекции Золотистый стафилококк может без вреда для нашего организма иметь популяцию до 10 000 бактерий в мл. среды, а Клебсиелла пневмония, убившая пациентку в США, безобидно присутствует на коже или в кишечнике здорового человека, но не более 10 000 бактерий в грамме фекалий. Развитие резистентности к антибиотикам А теперь представьте, что будет, если одной из сторон гражданской войны в маленьком африканском государстве передать оружие массового уничтожения. В случае с бактериями таким оружием будет антибиотик, но не природный, а современный синтетический аналог, применяемый в больших дозах и не локально, а аналогично ковровой бомбардировке - санирующий весь организм целиком. В результате применения антибиотика видовое разнообразие быстро сократится за счет наиболее чувствительных к препарату видов бактерий. Освободившиеся ниши быстро заселятся видами способными активно синтезировать антидоты. Генетическое разнообразие представителей внутри одного вида тоже уменьшится - эволюционное преимущество получат колонии наиболее устойчивые к антибиотикам. Если антибиотик химически аналогичен бактерицидам каких-нибудь бактерий микрофлоры, то выжившие виды продолжат доминировать даже после отмены антибиотикотерапии. Таким образом применяя антибиотик мы неосознанно создаем положительный отбор наиболее резистентных штаммов. Поэтому бессистемное применение антибиотиков часто заканчивается хроническими инфекциями, обусловленными разрастанием условно-патогенной микрофлоры. Носитель таких бактерий будет распространять их среди членов семьи, родственников и знакомых, которые рано или поздно применят другие антибиотики, тем самым продолжив положительный естественный отбор, и монорезистентный штамм постепенно приобретет полирезистентность. Такие патогены медики называют супербактериями. Кроме того разные виды бактерий способны обмениваться между собой генами резистентности к антибиотикам с помощью горизонтального переноса внехромосомных генетических элементов (плазмиды): Опасно, если полирезистентными к антибиотикам становятся бактерии-анаэробы - способные к бескислородному метаболизму. В случае травмы они могут попасть в кровь и вызвать тяжелый сепсис, как это произошло в описанном выше клиническом случае, когда патоген глубоко проник в костную ткань. Пытаясь спасти женщину, врачи безуспешно применили 14 антибиотиков и еще 12 препаратов протестировали in vitro на культуре выделенной из очага инфекции, но и они оказались не эффективными. Еще более опасно, когда резистентность приобретают патогенные бактерии, например, возбудители дизентерии, сальмонеллезов и сибирской язвы. Несмотря на низкой распространенность данных инфекций, их возбудители могут легко приобрести резистентность к препаратам от представителей нормальной микрофлоры путем горизонтального переноса генов в составе плазмид. Кроме того часто источником опасных инфекций являются сельскохозяйственные животные, среди которых носительство антибиотикорезистентных бактерий распространено больше, чем среди людей. Это обусловлено тем фактом, что в животноводстве антибиотики пожизненно добавляются в корм с целью профилактики инфекций. Субтерапевтические дозировки не уничтожают бактерии, а лишь сдерживают их размножение. С другой стороны, еще Флеминг предупреждал, что применение низких концентраций антибиотиков ведут к снижению чувствительности бактерий к препарату. Группа ученых Гарварда поставила интересный эксперимент, наглядно демонстрирующий эволюцию резистентных штаммов под воздействием постепенно возрастающей концентрации антибиотика. Очень советую посмотреть короткое видео эксперимента тем, кто самостоятельно принимает антибиотики: Таким образом важно принимать антибиотик в терапевтических дозах и полным курсом в соответствии с рекомендациями врача. Метод оценки резистентности к антибиотикам в клинической практике Однако, если вызвавшая заболевание бактерия уже имеет резистентность к препарату, то даже длительный прием антибиотика в высоких дозах может оказаться бесполезным. В таких случаях требуется определение чувствительности патогена к препарату в лаборатории. Для этого на питательную среду одновременно с посевом бактерий укладываются бумажные диски, пропитанные различными антибиотиками. На фото слева - контрольная лабораторная культура (светло-желтая исчерченность на среде), а справа - культура той же бактерии, полученная у пациента из очага инфекции. Прозрачные кольца вокруг дисков означают отсутствие роста культуры и, следовательно, ее чувствительность к данному антибиотику. Если же прозрачное кольцо отсутствует, значит к данному антибиотику есть резистентность. Результаты такого обследования позволят назначить антибиотик узкого спектра действия и прицельно подавить патоген минимизировав ущерб для остальной микрофлоры. Однако выполнение данных анализов - дорогостоящая практика и требует нескольких дней для инкубации. Поэтому, чтобы не терять драгоценное время, врач зачастую назначает антибиотики, не дожидаясь результатов анализа на чувствительность возбудителя к препарату. В подавляющем большинстве случаев данный анализ вовсе не выполняется, а антибиотик назначается даже без выявления вида возбудителя. Такая тактика предполагает применение антибиотиков широкого спектра действия по принципу стрельбы пушкой по воробьям. В частном случае это может быть эффективно как с клинической, так и экономической точек зрения, но в долгосрочной перспективе и в масштабах человеческой популяции данная практика только усугубляет проблему антибиотикорезистентности. Разработка новых антибиотиков теряет рентабельность Разработка и испытания новых антибиотиков очень наукоемко и требует около $1 млрд. инвестиций на 10-12 лет до появления препарата в аптеках. При этом антибиотики применяются относительно короткими курсами, часто один или несколько раз за всю жизнь человека. Например, такие группы препаратов, как обезболивающие, жаропонижающие, гормональные - применяются гораздо шире и регулярнее, что делает их более привлекательными для инвесторов. В том числе эти факторы формируют нисходящий тренд внедрения в практику новых антибиотиков:
Дополнительные опасения у инвесторов вызваны распространением бактерий с резистентностью к антибиотикам последних поколений. Современные стандарты терапии вынуждают клиницистов воздержаться от широкого применения новых препаратов и использовать их в крайнем случае в качестве препаратов-резерва, что неизбежно снижает спрос и еще больше замедляет возврат инвестиций. Получается замкнутый круг, когда спровоцированная антибиотиками резистентность бактерий тормозит дальнейшее развитие отрасли в целом. Заключение Мой дед Степанов Донат умер от воспаления легких в 26 лет в сибирском поселке Яшкино. Ему не хватило несколько дней, чтобы дождаться отца, который вез из Москвы тогда еще дефицитный пенициллин. Спустя 30 лет в той же больнице и от той же болезни пенициллин спас мою недавно начавшуюся жизнь. Безусловно, открытие и внедрение в терапию антибиотиков совершило переворот в медицине. За 80 лет антибиотикотерапия позволила спасти миллионы жизней и наверняка увеличила среднюю продолжительность жизни человечества. Однако уже сегодня очевидна необходимость поиска новых решений снижающих зависимость медицины от антибиотиков. Я уже писал о пробиотиках, которые можно без вреда для здоровья самостоятельно принимать для профилактики рецидивирующих фарингитов, отитов, тонзиллитов, кариеса и галитоза. Также можно прочитать мой пост о бактериофагах, которые рассматриваются как альтернатива антибиотикам в борьбе с полирезистентными патогенами. Несмотря на какие-либо альтернативы не отказывайтесь от приема антибиотиков, назначенных врачом. Если терапия не приносит результатов, требуйте выполнения анализов на выявление возбудителя и определения чувствительности к антибиотику. Кроме того, следует помнить, что подавляющее большинство случаев ОРЗ вызвано вирусами, против которых антибиотики не действуют. О профилактике вирусных инфекций читайте мой пост про неэффективный витамин-С и противовирусную активность цинка. Анонс: в следующий раз расскажу о том, как бороться с акне без антибиотиков и гормональных препаратов. Чтобы не пропустить обновления - подписывайтесь на самый популярный блог о медицине! А если у вас нет аккаунта в ЖЖ, подписывайтесь на обновления в Фэйсбук, Вконтакте, Телеграм и Твиттер. Поделитесь информацией с друзьями, которые злоупотребляют приемом антибиотиков без назначения врача: yablor.ru Конец эры антибиотиков
Когда Александр Флеминг в 1928 году, обнаружил в своей лаборатории стол, заражённый плесенью Penicillium notatum, он начал новую эру превосходства науки над природой. С тех пор антибиотики спасли миллионы жизней и избавили огромное количество людей от страданий. Но с самого начала этой эры учёным было известно, что ей придёт конец. Они просто не знали, когда именно… Сопротивляемость бактерий антибиотикам естественна и неизбежна. По воле случая у нескольких бактерий окажутся гены, способные защитить их от лекарств, они передадут эти гены дальше – и не только своему потомству, но иногда и соседям. Специалисты по вычислительной эпидемиологии наконец получают нужные данные и обрабатывают их для моделирования этого явления. Но никто не пытается использовать эти инструменты, чтобы предсказать конец эры антибиотиков – он уже наступил. Они концентрируются на том, чтобы понять, как скоро стойкие бактерии окажутся в большинстве и что доктора смогут с ними сделать – если это вообще возможно. В 2013 году тогдашний директор Центра по контролю и предотвращению заболеваний (CDC) Том Фриден сказал журналистам: «Если мы не будем вести себя осторожно, вскоре мы окажемся в постантибиотической эпохе». Сегодня, всего лишь четыре года спустя, это агентство утверждает, что мы в ней оказались.
«Мы говорим это потому, что появилась универсально стойкая бактерия», – говорит Джин Пател [Jean Patel], руководящая отделением CDC по стратегии и координации использования антибиотиков. «Люди умирают из-за отсутствия антибиотиков, способных лечить их инфекции – инфекции, которые не так давно было очень легко излечивать». В прошлом августе женщина возрастом за 70 попала в госпиталь в Рено, шт. Невада, с бактериальной инфекцией бедра. Бактерия принадлежала к классу особенно упорных микробов, известных, как карбапенем-устойчивые энтеробактерии (CRE). Но эту бактерию не брали ни карбапенемы, ни тетрациклин, ни колистин, и вообще никакой антибактериальный аппарат из 26-и имеющихся в продаже. Через несколько недель она умерла от септического шока. Для чиновников из области здравоохранения, к коим принадлежит и Пател, этот случай отмечает конец эры и начало новой. Вопрос в следующем: как быстро эта универсальная стойкость сможет распространиться? «Когда мы дойдём до ситуации, в которой инфекцию чаще будет невозможно вылечить, чем возможно? – говорит Пател. – Это будет очень сложно предсказать». Ей это точно известно, потому что она уже пыталась. В 2002 году первый стафилококк, устойчивый к ванкомицину, проявил себя у 40-летнего мужчины из Мичигана с хронической язвой ноги. Ситуация казалась весьма печальной: стафилококк – одна из самых распространённых инфекций у людей, а ванкомицин – самый распространённый антибиотик для его лечения. Кроме того, резистивный ген был расположен на плазмиде – свободно перемещающемся колечке ДНК, что позволяло ему легко передвигаться. Эпидемиологи из CDC работали совместно с микробиологами, такими, как Пател, над созданием модели, предсказывающей как далеко и как быстро он сможет распространиться. Пател не помнит точных цифр, но она вспоминает, что результаты получились пугающими. «Мы очень сильно озаботились этим вопросом», – говорит она.
К счастью, в данном случае модели ошиблись. С 2002 года было зафиксировано только 13 случаев появления стафилококка, устойчивого к ванкомицину, и все пациенты выжили. Такая ошибка весьма озадачила команды. Но в биологии иногда бывают такие сложности. «Я работала с этой бактерией в лабораториях, где она прекрасно растёт, но от человека к человеку, судя по всему, не распространяется», – говорит Пател. И хотя они ещё не знают, почему, одна из гипотез говорит о том, что появление этого резистентного гена не проходит для бактерии бесследно. Он сделал стафилококк невосприимчивым к его заклятому врагу, одновременно усложняя процесс выживания вне человеческого тела. Больничные правила, время года, география также могут влиять на распространение. Это похоже на попытки предсказания погоды. «Не получится сделать такие предсказания на бумаге или путём пристальных размышлений, – говорит Брюс Ли [Bruce Lee], исследователь общественного здравоохранения в институте Джона Хопкинса. Он работает с организациями, занимающимися здравоохранением в Чикаго и округе Ориндж, предсказывая наиболее вероятные пути распространения CRE – бактерий того типа, что убила женщину в Неваде – в случае их появления в больницах. В прошлом такие модели были основаны исключительно на математике – так Пател пыталась строить свои предсказания. Да, их уравнения были сложными, но не настолько, чтобы принять во внимание такие вещи, как человеческое поведение, биология бактерий и их взаимодействие с окружающей средой. „В нашей области люди всё больше начинают понимать, что для того, чтобы разобраться с распространением устойчивых к антибиотикам бактерий с достаточной степенью детализации, необходимо работать с моделями на основе данных, в которых можно просматривать миллионы различных сценариев – так, как это делают метеорологи“, – говорит Ли. В исследовании, опубликованном Ли в прошлом году, он описывает вероятность распространения CRE в 28 больницах и 74 частных лечебницах округа Ориндж. В этой модели у каждой виртуальной больницы было прописано количество коек, совпадающих с количеством коек в реальных учреждениях, а также вся информация по поводу связности учреждений.
В модели каждый пациент был вычислительной единицей, которая в любой определённый день либо переносит, либо не переносит CRE. Эти единицы двигались по экосистеме здравоохранения, взаимодействовали с врачами, медсёстрами, койками, стульями, дверьми по сотне миллионов раз, причём с каждой новой симуляцией эти параметры немного подстраивались. Он обнаружил, что без усиления мер по контролю, например, регулярной проверки пациентов на сопротивляемость и карантине переносчиков, CRE станет эндемическим заболеванием — постоянно присутствующим – практически во всех больницах округа Ориндж через десять лет. А после того, как CRE проникнет в систему здравоохранения, от него будет сложно избавиться. „Это как пытаться прогнать из дома термитов, – говорит Ли. – Как только они пробираются туда, где всё связано со всем, они становятся трудноизлечимой частью экосистемы“. Так что, если доктора смогут быстро идентифицировать людей, способных распространять CRE, он смогут хотя бы изолировать угрозу. Даже если самим пациентам они ничего предложить не сумеют. Пока хорошие новости заключаются в том, что единственные случаи передачи от человека к человеку на 100% стойкой бактерии происходят только в суперкомпьютере у Ли. В реальном мире таких случаев не зафиксировано. Но именно их и ищут Пател и CDC. Это и продвинет ситуацию на следующий уровень, говорит Пател. Чтобы держать руку на пульсе, в прошлом году агентство потратило $14,4 млн на создание сети из семи местных лабораторий, способных проводить генетическое тестирование бактериальных проб, взятых из больниц. Сейчас они претворяют в жизнь программу, которая когда-нибудь сможет связать все больницы в США с системой слежения CDC напрямую, чтобы автоматически отмечать каждое произошедшее в США событие, связанное со стойкими к антибиотикам бактериями, в реальном времени.
Параллельно Пател, и, с переменным успехом, остальной мир, следит за разработкой антибиотиков. В этой области тоже не всё гладко. На прошлой неделе Всемирная организация здравоохранения выпустила отчёт с анализом всех находящихся в разработке антибактериальных лекарств. Выводы мрачные: недостаточно лекарств, недостаточно инноваций. На каждое новое лекарство из 51 варианта уже можно найти заранее устойчивые к нему микроорганизмы. Исследователи, такие, как Пател и Ли, надеются, что их работа позволить минимизировать существующие угрозы, обнаружить новые по мере их появления, и дать фармакологическим компаниям время на разработку новых лекарств. Эра антибиотиков, возможно, и закончилась – но с наступающей новой эрой ещё многое можно сделать. yaszdorov.ru Расплата за ошибки. Эра антибиотиков заканчивается — что дальше? | Здоровая жизнь | ЗдоровьеТолько в одном Евросоюзе устойчивость к противомикробным препаратам ежегодно уносит 25 тысяч человек, а экономические потери, связанные с расходами здравоохранения и потерей трудовых ресурсов, составляют более полутора миллиардов долларов. Цифры пугающие. Но ещё более страшными выглядят прогнозы специалистов, опубликованные в информационном бюллетене ВОЗ: к 2050 году убыль населения от устойчивости к антибиотикам составит около 50 млн человек в год. По чистой случайностиОткрытие антибиотиков произошло в 1928 году. Как-то вернувшись из отпуска в свою лабораторию, британский бактериолог Александр Флеминг обнаружил в термостатном шкафу забытую чашку Петри с колонией бактерий Staphylococcus aureus. Каково же было его изумление, когда он увидел, что часть из них погибла под воздействием образовавшейся там плесени! Позже учёный выяснил, что разрушающее действие на стафилококки оказали не сами плесневые грибы Penicillium notatum, а жидкость, выделяемая ими в ходе жизнедеятельности. Это активное вещество бактериолог назвал пенициллином. Через некоторое время коллеги Флеминга Говард Флори и Эрнст Борис Чейн разработали метод очистки пенициллина, за что все трое впоследствии были удостоены Нобелевской премии. В ходе исследований выяснилось, что пенициллин губителен не только для стафилококков, но и для дифтерийной и туберкулёзных палочек, стрептококков, пневмококков, гонококков и некоторых других микроорганизмов. Массовое производство пенициллина наладили в США в 1943 году. Так наступила эра антибиотиков. С помощью пенициллина начали успешно справляться с такими заболеваниями, как туберкулёз, сифилис, которые с древнейших времён считались неизлечимыми, а также успешно бороться с малярией, кишечными инфекциями, пневмонией, гнойными ранами, тяжёлыми заражениями крови, перитонитами. Однако окончательной победы антибиотики не принесли. Бактерии пошли в контрнаступление. Они оказались слишком живучими и сегодня всё легче приспосабливаются к новым условиям, меняя свой генетический код. Бич XXI века«Мир движется к постантибиотической эре, когда многие распространённые инфекционные заболевания могут вновь стать смертельными, — заявила генеральный директор ВОЗ Марагарет Чен на 136‑й сессии Исполнительного комитета ВОЗ в январе 2015 года. — В отсутствие эффективных антибиотиков выполнение некоторых из самых передовых мер вмешательства, которыми располагает современная медицина, таких как трансплантация органов, протезирование шейки бедра и тазобедренного сустава, химиотерапия онкологических заболеваний и оказание помощи недоношенным младенцам, может оказаться слишком опасным. Последствия этого можно кратко описать так: конец современной медицины в привычном для нас понимании. Врачи, занимающиеся ведением некоторых случаев туберкулёза и гонореи, уже оказались безоружными перед этими заболеваниями, поскольку даже препараты “последней надежды” неэффективны». Устойчивость микробов к антибиотикам стала сегодня одной из самых больших опасностей для здравоохранения во всём мире, её даже называют бичом XXI века. «Антибиотикорезистентность — одна из сложнейших проблем, которая стоит перед мировым здравоохранением. Мы знаем о ней уже 20 лет, и ВОЗ два года назад вынуждена была принять глобальный план действий по борьбе с устойчивостью к противомикробным препаратам, — сообщил специальный представитель ВОЗ в России Гайк Никогосян. — Вопрос о предотвращении антибиотикорезистентности был даже выдвинут на обсуждение Генеральной ассамблеи ООН, где политическую декларацию принимали на уровне глав государств и правительств. Это четвёртый случай, когда проблему пытаются решить в столь высоких инстанциях, что говорит о её размахе в мировом восприятии. Первые три касались ВИЧ/СПИДа, неинфекционных заболеваний и Эболы». Хуже не будет?В том, что антибиотики теряют свою эффективность, во многом виноваты сами люди. Антибиотики широко используют в животноводстве и птицеводстве, причём не только для лечения, но и для быстрого наращивания мышечной массы. Очень часто эта группа препаратов назначается по принципу «хуже не будет». "В некоторых регионах нашей страны в 70% случаев врачи прописывают антибиотики при простудных заболеваниях, вызванных вирусом", — признаётся замминистра здравоохранения Сергей Краевой. А вот данные исследования, организованного территориальным фондом ОМС Санкт-Петербурга: в питерских больницах врачи лишь в 15% случаев проясняют этиологию инфекции перед назначением антимикробной терапии взрослым пациентам, то есть в 85% случаев они действуют наобум, учитывая лишь симптомы, а в 69% — не соблюдают клинические рекомендации по назначению лекарств. Не лучше ситуация и с детьми: противомикробная нагрузка на организм новорождённых в петербургских больницах в 4 раза выше, чем в США. Скорее всего, похожая картина наблюдается по всей стране. Несмотря на формальный запрет безрецептурного отпуска антибиотиков, купить их у нас — не проблема. В 50% случаев в аптеках никто не спрашивает рецепт при их продаже. В результате, по данным исследований НИИ антимикробной химиотерапии Смоленской государственной медицинской академии, более 95% граждан, не имеющих медицинского образования, хранят их в домашних аптечках, причём число наименований колеблется от 1 до 11. Впрочем, мы не единственная страна, где доступ к антибиотикам де-факто остаётся свободным. По некоторым данным, за пределами Евросоюза, США и Канады от 19 до 100% всех антибиотиков приобретаются без рецепта врача. Ну а что сами больные, в руках которых оказываются противомикробные препараты? Недавно проведённое в России исследование показало, что каждый второй пациент не соблюдает график их приёма, прерывая лечение, как только почувствовал облегчение, либо уменьшая кратность приёма препарата. В ноябре 2016 года Всероссийский центр изучения общественного мнения (ВЦИОМ) представил результаты опроса родителей детей до 8 лет, который показал, что 23% мам иногда самостоятельно сокращают курс назначенных их детям антибиотиков, а 3% делают это всегда. А ведь подавление бактерий напрямую зависит от адекватной дозы антибиотиков. Альтернатива естьПотеря эффективности антибиотиков усугубляется и тем, что в разработке сегодня находится очень мало препаратов‑заменителей. «Новых антибиотиков практически нет. За последние годы не было создано ни одного нового класса антибиотиков, а те, что появились, представляют собой вариации уже существующих препаратов», — отмечает Гайк Никогосян. Такую позицию фармкомпаний можно понять: кому выгодно вкладывать миллионы долларов в создание лекарства, которое через 5–7 лет перестанет работать! Но существуют ли препараты, способные заменить антибиотики? Оказывается, да. Прежде всего речь идёт об известных всем вакцинах, запускающих управляемую иммунопрофилактику. Второе средство — бактериофаги. Это вирусы бактерий, состоящие из одной или двух цепей нуклеиновых кислот. Чаще всего они размножаются в клетках бактерий и вызывают их лизис. Бактериофаги — хорошо забытое старое. В этом году исполняется ровно 100 лет, как они были открыты канадским микробиологом Феликсом Д`Эррелем. Впрочем, ещё за 20 лет до открытия Д`Эрреля, в 1897 году, российский микробиолог Николай Гамалея впервые описал явление лизиса сибиреязвенной палочки под влиянием перевиваемого агента. В СССР бактериофаги начали применять против холеры, дизентерии, брюшного тифа ещё с 1930‑х годов. В годы войны с их помощью сдерживали эпидемии. Производятся они и сегодня в России, причём наша страна — одна из немногих, где бактериофаги зарегистрированы в качестве лекарственных средств. Поиск препаратов, способных заменить антибиотики, ведётся по всему миру. В разработках используются инновационные молекулярные подходы. Совсем недавно, например, в Университетском колледже Лондона разработали принципиально новый антибиотик, молекулы которого, присоединяясь к оболочке супербактерии, взламывают её защиту. Всем миромВ 2014 году ВОЗ приняла глобальный план действий по сдерживанию антимикробной резистентности, который содержит пять стратегических целей:
Руководствуясь этим планом, национальные министерства здравоохранения, в том числе и нашей страны, сформировали собственные дорожные карты преодоления антимикробной резистентности. Однако угроза столь велика, что здесь каждый должен включаться в борьбу. Тут есть над чем задуматься и врачам, и пациентам, и фармацевтам. www.aif.ru Эра антибиотиков закончилась. И что теперь? / Geektimes Когда Александр Флеминг вернулся из отпуска летом 1928 года, и обнаружил в своей лондонской лаборатории стол, заражённый плесенью Penicillium notatum, он начал новую эру превосходства науки над природой. С тех пор антибиотики, как открытые им лично, так и множество других, открытых благодаря его работам, спасли миллионы жизней и избавили огромное количество людей от страданий. Но с самого начала этой эры учёным было известно, что ей придёт конец. Они просто не знали, когда именно. Когда Александр Флеминг вернулся из отпуска летом 1928 года, и обнаружил в своей лондонской лаборатории стол, заражённый плесенью Penicillium notatum, он начал новую эру превосходства науки над природой. С тех пор антибиотики, как открытые им лично, так и множество других, открытых благодаря его работам, спасли миллионы жизней и избавили огромное количество людей от страданий. Но с самого начала этой эры учёным было известно, что ей придёт конец. Они просто не знали, когда именно.Сопротивляемость бактерий антибиотикам естественна и неизбежна. По воле случая у нескольких бактерий окажутся гены, способные защитить их от лекарств, они передадут эти гены дальше – и не только своему потомству, но иногда и соседям. Специалисты по вычислительной эпидемиологии наконец получают нужные данные и обрабатывают их для моделирования этого явления. Но никто не пытается использовать эти инструменты, чтобы предсказать конец эры антибиотиков – он уже наступил. Они концентрируются на том, чтобы понять, как скоро стойкие бактерии окажутся в большинстве и что доктора смогут с ними сделать – если это вообще возможно. В 2013 году тогдашний директор Центров по контролю и предотвращению заболеваний (CDC) Том Фриден сказал журналистам: «Если мы не будем вести себя осторожно, вскоре мы окажемся в постантибиотической эпохе». Сегодня, всего лишь четыре года спустя, это агентство утверждает, что мы в ней оказались. «Мы говорим это потому, что универсально стойкая бактерия появилась», – говорит Джин Пател [Jean Patel], руководящая отделением CDC по стратегии и координации использования антибиотиков. «Люди умирают из-за отсутствия антибиотиков, способных лечить их инфекции – инфекции, которые не так давно было очень легко излечивать». В прошлом августе женщина возрастом за 70 попала в госпиталь в Рено, шт. Невада, с бактериальной инфекцией бедра. Бактерия принадлежала к классу особенно упорных микробов, известных, как карбапенем-устойчивые энтеробактерии (CRE). Но эту бактерию не брали ни карбапенемы, ни тетрациклин, ни колистин, и вообще никакой антибактериальный аппарат из 26-и имеющихся в продаже. Через несколько недель она умерла от септического шока. Для чиновников из области здравоохранения, к коим принадлежит и Пател, этот случай отмечает конец эры и начало новой. Вопрос в следующем: как быстро эта универсальная стойкость сможет распространиться? «Когда мы дойдём до ситуации, в которой инфекцию чаще будет невозможно вылечить, чем возможно? – говорит Пател. – Это будет очень сложно предсказать». Ей это точно известно, потому что она уже пыталась. В 2002 году первый стафилококк, устойчивый к ванкомицину, проявил себя у 40-летнего мужчины из Мичигана с хронической язвой ноги. Ситуация казалась весьма печальной: стафилококк – одна из самых распространённых инфекций у людей, а ванкомицин – самый распространённый антибиотик для его лечения. Кроме того, резистивный ген был расположен на плазмиде – свободно перемещающемся колечке ДНК, что позволяло ему легко передвигаться. Эпидемиологи из CDC работали совместно с микробиологами, такими, как Пател, над созданием модели, предсказывающей как далеко и как быстро он сможет распространиться. Пател не помнит точных цифр, но она вспоминает, что результаты получились пугающими. «Мы очень сильно озаботились этим вопросом», – говорит она. К счастью, в данном случае модели ошиблись. С 2002 года было зафиксировано только 13 случаев появления стафилококка, устойчивого к ванкомицину, и все пациенты выжили. Такая ошибка весьма озадачила команды. Но в биологии иногда бывают такие сложности. «Я работала с этой бактерией в лабораториях, где она прекрасно растёт, но от человека к человеку, судя по всему, не распространяется», – говорит Пател. И хотя они ещё не знают, почему, одна из гипотез говорит о том, что появление этого резистентного гена не проходит для бактерии бесследно. Он сделал стафилококк невосприимчивым к его заклятому врагу, одновременно усложняя процесс выживания вне человеческого тела. Больничные правила, время года, география также могут влиять на распространение. Это похоже на попытки предсказания погоды. «Не получится сделать такие предсказания на бумаге или путём пристальных размышлений, – говорит Брюс Ли [Bruce Lee], исследователь общественного здравоохранения в институте Джона Хопкинса. Он работает с организациями, занимающимися здравоохранением в Чикаго и округе Ориндж, предсказывая наиболее вероятные пути распространения CRE – бактерий того типа, что убила женщину в Неваде – в случае их появления в больницах. В прошлом такие модели были основаны исключительно на математике – так Пател пыталась строить свои предсказания. Да, их уравнения были сложными, но не настолько, чтобы принять во внимание такие вещи, как человеческое поведение, биология бактерий и их взаимодействие с окружающей средой. „В нашей области люди всё больше начинают понимать, что для того, чтобы разобраться с распространением устойчивых к антибиотикам бактерий с достаточной степенью детализации, необходимо работать с моделями на основе данных, в которых можно просматривать миллионы различных сценариев – так, как это делают метеорологи“, – говорит Ли. В исследовании, опубликованном Ли в прошлом году, он описывает вероятность распространения CRE в 28 больницах и 74 частных лечебницах округа Ориндж. В этой модели у каждой виртуальной больницы было прописано количество коек, совпадающих с количеством коек в реальных учреждениях, а также вся информация по поводу связности учреждений. В модели каждый пациент был вычислительной единицей, которая в любой определённый день либо переносит, либо не переносит CRE. Эти единицы двигались по экосистеме здравоохранения, взаимодействовали с врачами, медсёстрами, койками, стульями, дверьми по сотне миллионов раз, причём с каждой новой симуляцией эти параметры немного подстраивались. Он обнаружил, что без усиления мер по контролю, например, регулярной проверки пациентов на сопротивляемость и карантине переносчиков, CRE станет эндемическим заболеванием — постоянно присутствующим – практически во всех больницах округа Ориндж через десять лет. А после того, как CRE проникнет в систему здравоохранения, от него будет сложно избавиться. „Это как пытаться прогнать из дома термитов, – говорит Ли. – Как только они пробираются туда, где всё связано со всем, они становятся трудноизлечимой частью экосистемы“. Так что, если доктора и сёстры смогут быстро идентифицировать людей, способных распространять CRE, он смогут хотя бы изолировать угрозу. Даже если самим пациентам они ничего предложить не сумеют. Пока хорошие новости заключаются в том, что единственные случаи передачи от человека к человеку на 100% стойкой бактерии происходят только в суперкомпьютере у Ли. В реальном мире таких случаев не зафиксировано. Но именно их и ищут Пател и CDC. Это и продвинет ситуацию на следующий уровень, говорит Пател. Чтобы держать руку на пульсе, в прошлом году агентство потратило $14,4 млн на создание сети из семи местных лабораторий, способных проводить генетическое тестирование бактериальных проб, взятых из больниц. Сейчас они претворяют в жизнь программу, которая когда-нибудь сможет связать все больницы в США с системой слежения CDC напрямую, чтобы автоматически отмечать каждое произошедшее в США событие, связанное со стойкими к антибиотикам бактериями, в реальном времени. Параллельно Пател, и, с переменным успехом, остальной мир, следит за разработкой антибиотиков. В этой области тоже не всё гладко. На прошлой неделе Всемирная организация здравоохранения выпустила отчёт с анализом всех находящихся в разработке антибактериальных лекарств. Выводы мрачные: недостаточно лекарств, недостаточно инноваций. На каждое новое лекарство из 51 варианта уже можно найти заранее устойчивые к нему микроорганизмы. Исследователи, такие, как Пател и Ли, надеются, что их работа позволить минимизировать существующие угрозы, обнаружить новые по мере их появления, и дать фармакологическим компаниям время на разработку новых лекарств. Эра антибиотиков, возможно, и закончилась – но с наступающей новой эрой ещё многое можно сделать. geektimes.ru |
г.Самара, ул. Димитрова 131 [email protected] |
 |