|
|
||||||||||
|
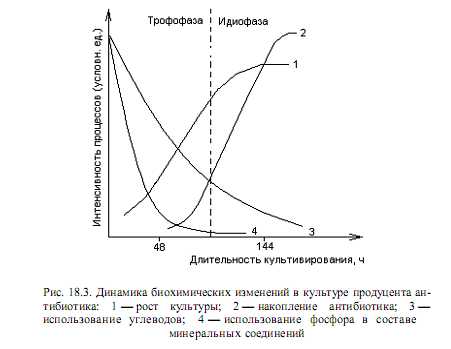
Закономерности биосинтеза антибиотиков. Этапы биосинтеза антибиотиков5.Биосинтез антибиотиков, его регуляция.Развитие м/о продуцента антибиотиков имеют 2х фазный характер: 1)трофофаза или фаза сбалансированного роста характеризуется тем, что в культуре продуцента происходит быстрое накопление биомассы, сопряженное с интенсивным потреблением компонентов субстрата – углерода, азота, фосфора, некоторые сниженные рН среды. Биосинтез не осуществляется в эту фазу. 2)идиофаза – фаза несбалансированного роста, характеризуется снижением общего кол-ва биомассы вследствие автолиза части клеток. Среда обогащена продуктами обмена автолиза, возрастает значение рН, синтезируются антибиотики. Принцип 2х фазности развития м/о продуцента антибиотика характерен для организмов, развивающихся в периодической культуре при использовании в качестве посевного материала молодые культуры или споры. У многих м/о продуктивность снижается в присутствии избытка углерода, особенно глюкозы – накопленным катоболитным репрессором, поэтому источник углерода необходимо добавлять в среду небольшими порциями, другой способ получения мутантов устойчив к катоболитной репрессии. Во многих случаях источник азота – фосфор. Также могут снизить образование антибиотиков, поскольку фосфат ингибирует транскрипцию некоторых генов синтеза антиб, поэтому необходимо контролировать концентрацию в течение всей ферментации или получать мутанты менее чувствительные к этим регуляторам процесса. Сами антиб как конечный продукт могут осуществлять регуляцию своего синтеза при помощи обратной связи. Данный способ позволяет контролировать процесс образования антиб, т.е стимулировать выделение в окружающую среду и т.о снижать его концентрацию в клетке (метод проницаемости мемраны). Поскольку антиб вторичные метаболиты, они синтезируются из первичных, поэтому необх наличие предшественников. У грибов р.пеницилиум аминоадипиновая к-та является предшественником биосинтеза лизина и пенициллина. Поскольку лизин явл конечным продуктом он ингибирует первый фермент своего синтеза, что сопровождается снижению кол-ва всех промежуточных продуктов, в том числе и адипиновой к-ты, след-но синтез пенициллина снижается. При внесении адипиновой к-ты в проц ферментации ингибирующий эффект лизина снижается и наоборот. Если высокое содерж лизина, в среде наблюдается ингибир пенициллин. Наряду с аминоадипиновой к-ой продуцент пенициллина мецифалоспарина нуждается в цистеине и валине. М/о культивируют глубинным способом в условиях аэрации и ист питания. Механизмы устойчивости к собств антиб связаны с инактивацией их в клетке, либо выделение их в окружающую среду, кроме того устойчивость обусловлена модификацией на генном уровне. 6.Механизмы биологического действия антибиотиков.По механизму действия антиб делят на следующие группы: 1)антиб, обладающие конкурентным действием в процессе метаболизма (пурамицин). 2)ингибирующие синтез клеточной стенки (пенициллины, цифалоспорины). 3)нарушающие ф-ии мембраны (грамицедин, трихомицин). 4)подавляющие синтез нуклеиновых к-т: а)синтез РНК (новобиоцин, неолицин), б)синтез ДНК (актиномицин, митомицин). 5)ингибиторы синтетических пуринов и перимединов (азосерин). 6)подавляет синтез белка (тетрациклин, хлоранфеникол). 7)ингибиторы дыхания (амномицин). 8)ингибиторы окислительного фосфорилирования (грамицидины). 9)обладают антиметаболитными сойствами (50 антиб, в их числе циклосирин). Антибиотики – это специфичный продукт жизнедеятельности организмов или их модификации, обладающие высокой физиологической активностью по отношению к определенным группам м/о (бактреии, грибы, микроводоросли, протозола), также к вирусам или к злокачественным опухолям, задерживая их рост или полностью подавляя их развитие. Спецефичность антибиотиков: 1)обладают высокой биологической активностью. 2)избирательностью биологического действия. Делят на 2 группы: 1)антиб узкого спектра действия (бензил пенициллин, новобиацин, гризиофульфин и т.д). 2)широкого спектра действия (тетрациклин, хлоранфеникол). Антиб могут накапливаться в клетке, могут выделятся во внешнюю среду, а могут то и др. Антиб – это конечный продукт метаболизма. Определенный м/о может синтезировать один или несколько антибиотиков. Антиб выступают в качестве фактора антоганизма, также выполняют функцию регуляторов ферментных систем. Ок 6 тыс антибиотических веществ природных и синтетических. studfiles.net Закономерности биосинтеза антибиотиков
Антибиотики относятся к вторичным метаболитам — низкомолекулярным веществам, функции которых несущественны для роста чистых культур. Вторичные метаболиты (антибиотики, алкалоиды, гормоны роста растений, токсины) производятся представителями ограниченного числа таксономических групп. В отличие от первичных метаболитов, вторичные имеют более сложное химическое строение и образуются, как правило, в ходе длинных метаболических путей. Известно, что образование антибиотиков делает их продуцентов более конкурентоспособными и является мощным фактором в борьбе организмов за существование. Однако это не единственная роль антибиотиков: недавно обнаружено, что данные вещества осуществляют функцию контроля и регуляции процессов метаболизма, выполняя роль специфических эффекторов, контролирующих активность ряда ферментных систем. Кроме этого, существует точка зрения, согласно которой антибиотики могут служить клеточными компонентами, в виде которых клетка избавляется от накопившихся в ней по тем или иным причинам в избытке метаболитов и восстановительных эквивалентов. Биосинтез большинства вторичных метаболитов, в том числе антибиотиков, обычно осуществляется на определенной стадии развития микроорганизма, в условиях торможения основных процессов анаболизма—биосинтеза нуклеиновых кислот, белка, липидов, полисахаридов. Различают две принципиально различные стадии развития популяции продуцентов антибиотиков. Первая, носящая название трофофаза или фаза сбалансированного роста, характеризуется интенсивным синтезом соединений, требующихся для роста клеток, что сопровождается быстрым потреблением основных питательных компонентов среды. Эта фаза соответствует фазе логарифмического роста периодической культуры микроорганизмов. После исчерпания некоторых ингредиентов среды (в первую очередь, углерода, азота, молекулярного кислорода) и накопления продуктов метаболизма наступает вторая фаза (идиофаза, или фаза несбалансированного роста). Идиофаза отличается заметным торможением или прекращением роста микробной популяции, что соответствует переходу в стационарную фазу роста периодической культуры. Здесь начинают преобладать протеолитические процессы, происходит автолитический распад клеток. Именно в идиофазе многие микроорганизмы начинают синтезировать вторичные метаболиты, к числу которых относятся и антибиотики. Описанные закономерности можно отобразить графически (рис. 18.3).
В большинстве случаев максимум накопления антибиотика в культуральной жидкости наступает после максимума накопления биомассы. Это объясняется тем, что синтез ферментов, ответственных за образование антибиотиков, подавлен (репрессирован) во время трофофазы. Биосинтез антибиотиков — наследственно закрепленное свойство организмов. Гены, ответственные за эти процессы, могут располагаться на хромосомах (нуклеоидах у прокариот), а также на плазмидах. Регуляция процесса синтеза антибиотика осуществляется разными способами: чаще в ходе катаболитной репрессии, с помощью репрессии синтеза ферментов конечным продуктом, а также при аллостерическом ингибировании антибиотиком активности ключевых ферментов своего биосинтеза. При этом важными компонентами среды, оказывающими влияние на биосинтез антибиотиков, являются глюкоза, а также фосфат. Как правило, избыток этих веществ отрицательно сказывается на образовании антибиотиков. Антибиотическая продуктивность организма отражает количество антибиотика (в мкг или в единицах), образованное единицей массы (обычно 1 мг) сухих клеток микроорганизма-продуцента в единицу времени (обычно за 1 ч). Этот параметр зависит, в первую очередь, от вида микроорганизма, фазы роста клеток, состава среды, условий культивирования. Препараты антибиотиков характеризуются разной степенью чистоты и, соответственно, активности, которая выражается в количестве единиц антибиотической активности (ЕД), содержащихся в 1 мг или 1 мл препарата. За единицу антибиотической активности принимают минимальное количество чистого вещества антибиотика, способное подавить развитие определенного числа клеток стандартного штамма микроорганизма (тест-микроба) в единице объема культуральной жидкости. Например, 1 ЕД стрептомицина эквивалентна 1 мкг чистого основания этого вещества, 1 ЕД пенициллина соответствует 0,6 мкг натриевой соли бензилпенициллина. При этом в качестве тест-микроба для стрептомицина используется E.coli, а для пенициллина — Staphylococcus aureus.
Похожие статьи:poznayka.org 4. Проанализируйте возможность успешного сочетания биосинтеза, оргсинтеза и биотрансформации на примере получения беталактамных антибиотиков. ОтветБиосинтез - это синтез природных органических соединений в живых организмах. Процессы биосинтеза играют важную роль во всех живых клетках. С точки зрения биотехнологии биосинтез рассматривается как промышленное получение биологически активных соединений (антибиотиков, гормонов, витаминов, аминокислот и т.д.) с участием живых организмов. Антибиотики – низкомолекулярные (менее 2000 г/моль) вещества природного или полусинтетического происхождения. Оказывают подавляющее действие на рост и размножение бактерий и при этом относительно мало или вовсе не повреждающие клетки макроорганизма. Продуцентами антибиотиков являются грибы, актиномицеты, бактерии. Антибиотики – вторичные метаболиты, органические соединения, не требующиеся культуре клеток для роста. Биотехнологическое производство -лактамного антибиотика бензилпенициллина основано на промышленном культивировании плесневого гриба Penicillium chrysogenum. Ферментацию ведут в две стадии при температуре 22-26 оС, при рН среды от 5,0 до 7,5 при интенсивной аэрации среды. На второй стадии в среду добавляют фенилуксусную кислоту как предшественник бензилпенициллина. В течении 4 суток количество бензилпенициллина достигает максимума и ферментацию прекращают. Бензилпенициллин (пенициллин G, от слова «gold») – «золотой» стандарт антибиотика. При ферментативном гидролизе бензилпенициллина образуется 6-аминопенициллановая кислота (6-АПК), исходная структура, «core-structure» для синтеза новых антибиотиков. На основе 6-АПК было получено более 40000 полусинтетических пенициллинов. В промышленности 6-АПК получают путем гидролиза бензилпенициллина при участии штаммов бактерий с высоким содержанием пенициллиназы, или используют иммобилизованную пенициллиназу. Примером успешного сочетания биосинтеза, оргсинтеза и биотрансформации может служить получение полусинтетического антибиотика ампициллина. Первая стадия - гидролиз бензилпенициллина и получение 6-АПК осуществляется при участии пенициллинацилазы мутанта Kluyvera citrophila. Далее в ферментер вносят мутант Pseudomonas melanogenum и метиловый эфир фенилглицина. Условия процесса изменяют таким образом, чтобы они способствовали образованию ампициллина. В роли катализатора выступает пенициллинацилаза, образуемая Pseudomonas melanogenum, которая не способна в этих условиях гидролизовать или синтезировать бензилпенициллин. В ходе этого двухстадийного процесса образуется только ампициллин (рис. 1, 2).
Рис. 1. Получение 6-АПК из бензилпенициллина
Рис. 2. Получение ампициллина из метилового эфира фенилглицина и 6-АПК В качестве примера органического синтеза можно рассматривать химический синтез радикалов, которые используются для получения различных антибиотиков пенициллинового ряда из 6-АПК. Биотрансформация – это методы генетической инженерии, которые позволяют получить высокопродуктивные биотехнологические штаммы. Традиционно это введение определенного гена в плазмиду, а затем получение генетически модифицированных продуцентов с полезными свойствами. К современным методам биотрансформации можно отнести error-prone PCR (использование не полностью подходящего праймера для получения точечных направленных мутаций в амплифицированном гене) и DNA shuffling (разрезание ДНК на фрагменты 50-100 п.н., а затем проведение ПЦР без праймера, так что эти фрагменты сами служат праймерами). Методы DNA shuffling и error-prone PCR позволяют получить гибриды или химерные формы организмов, обладающие уникальными свойствами. studfiles.net Антибиотики биосинтез - Справочник химика 21Гетероциклические ядра составляют основу для построения многочисленных гомологических рядов, содержащих углеводородные остатки в виде боковых цепей, а также всевозможные функциональные группы. К гетероциклическим соединениям относятся, кроме упомянутых, также многие другие важные природные вещества. Это, например, алкалоиды — азотсодержащие растительные физиологически активные вещества. Среди них есть и сильные яды (стрихнин, никотин), и важные лекарственные препараты (хинин, резерпин). Гетероциклические ядра составляют основу многих антибиотиков, например пенициллина, тетрациклина витаминов. (витамины группы В п др.). Пуриновые и пиримидиновые основания входят в состав нуклеиновых кислот — материальных носителей наследственности, играющих важнейшую роль в процессах биосинтеза белков. [c.340]Наиболее важным продуцентом стрептомицина, используемым для промышленного производства этого антибиотика, является Streptomy es griseus. Биосинтез протекает при 26—28° с использованием питательной [c.715] С каждым годом все большее число разнообразных процессов микробиологического синтеза реализуется в промышленных условиях, Промышленная биотехнология становится новым перспективным направлением, открывающим необозримые горизонты использования продуктов биосинтеза микроорганизмов в народном хозяйстве. Увеличивается число биохимических заводов и комбинатов по производству уже освоенной продукции микробиологического синтеза — ферментных препаратов, витаминов, кормовых антибиотиков, аминокислот, микробиологических препаратов для борьбы с вредителями растений, кормовых дрожжей и др. Широким фронтом ведутся исследования по получению и технологии производства новых биологически активных препаратов, разрабатываемых с использованием современных достижений молекулярной генетики и генной инженерии. К перспективным задачам промышленной биотехнологии относится также реализация микробиологических процессов, направленных на решение энергетической проблемы, в том числе производство биогаза, топливного этанола, метана, топливного водорода с помощью фотосинтезирующих микроорганизмов и др. [c.3] Антибиотики широко используют в качестве молекулярных инструментов при исследовании фундаментальных проблем биологии, таких, как расшифровка тончайших механизмов биосинтеза белка, нуклеиновых кислот и структуры клеточных стенок бактерий, создание моделей транспорта ионов через биологические мембраны и др. [c.64] Методы получения антибиотиков путем химического синтеза чрезвычайно сложны и не могут конкурировать с их биосинтезом методами биотехнологии. Существует несколько способов получения как природных, так и полусинтетических антибиотиков. Направленный биосинтез антибиотиков осуществляется путем прямой ферментации микроорганизма — продуцента с подходящим [c.64] Большое значение для биосинтеза антибиотика имеет подбор рационального состава питательных сред, которые определяются в соответствии со штаммом продуцента. У каждого штамма потребность в источниках питания неодинакова, поэтому состав питательных сред не может быть постоянным для всех продуцентов. [c.413] Тетрациклины — антибиотики широкого спектра действия. Они активны в отношении грам-отрицательных и грам-положительных бактерий, риккет-сий, некоторых крупных вирусов и простейших. Они устойчивы к действию различного рода гидролаз, к ним медленнее развивается резистентность микроорганизмов. К их недостаткам следует отнести различные побочные эффекты. Механизм антимикробного действия тетрациклинов основан на ингибировании ими биосинтеза белка микробной клетки. [c.304] Антибиотики—вещества, образуемые микроорганизмами или получаемые из других природных источников, обладающие антибактериальным, антивирусным и противоопухолевым действием. Они вмешиваются в обмен белков, нуклеиновых кислот и в энергетические процессы пораженных организмов и клеток, избирательно воздействуя на определенные молекулярные механизмы. Так, в биосинтезе белка (о поименованных ниже этапах биосинтеза белка см. гл. VII) пуромицин высвобождает недостроенные полипептиды, тетрацик-лины подавляют присоединение аминоацил-тРНК к рибосоме, хлорамфеникол (левомицетин)—пептидилтрансферазную реакцию в ней, эритромицин блокирует перемещение рибосомы по информационной РНК, стрептомицин искажает считывание кода белкового синтеза. В биосинтезе нуклеиновых кислот (терминологию см. в гл. VI) противораковые и антибактериальные антибиотики (актиномицины, митомицин, новобицин, рифамицин и др.) подавляют процессы репликации и транскрипции. На энергетические процессы в клетке воздействуют антимицин (подавляет перенос электронов в цитохромной системе), ОЛИГОМИ1ЩН (подавляет сопряжение окисления с фосфорилированием) и другие антибиотики. Биосинтез гликопротеинов клеточных стенок бактерий приостанавливается под действием пенициллинов и D-циклосерина проницаемость клеточных мембран нарушается грамицидинами, нистатином и многими другими антибиотиками. [c.175] L-ИЗОЛЕЙЦИН (L-a-aминo- -мeтилвaлepиaнoвaя к-та) С2НзСН(СНэ)СН(МН2)СООН, крист. [а] 4-40,3° (конц. 4 г Б 100 мл 6 н. НС1) рК СООН и NHs соотв. 2,32 и 9,76 ограниченно раств. в воде и сп., не раств. в эф. Незаменимая аминокислота, входит в состав белков. Пептидные связи, образованные И., плохо гидролизуются нз-за пространств, затруднений. Биосинтез — из треонина. Остаток алло-И. содержится в молекулах нек-рых антибиотиков. [c.210] Из гидролизатов можно получать пищевую глюкозу, техническую ксилозу, ксилит, сорбит, глицерин, этиленгликоль, фурфурол, этиловый и бутиловый спирты, ацетон, белково-витаминные дрожжи и другие ценные продукты. Наиболее перспективным направлением переработки моноз является каталитическое превращение их в полупродукты для органического синтеза, а также биосинтез белковых веществ, витаминов и антибиотиков. Из лигнина получают фенолы, ацетат кальция, активированный уголь, бензол, толуол наполнители для каучуков. [c.75] Химиков интересует ход реакций образования в организмах природных продуктов из простейших органических соединений. Поэтому такие процессы интенсивно исследовались и в ряде случаев хорошо известны (например, способ образования, или биосинтеза, изопреноидов или некоторых антибиотиков). [c.179] Биосинтез гликопептида стенки проходит через несколько этапов, включаюш их образование полисахаридных цепей, нараш ивание на них пептидных разветвлений и в заключение — сшивание этих пептидов пентагли-циновыми мостиками. Ряд антибиотиков блокирует определенные стадии этого процесса, что в итоге приводит к нарушению биосинтеза стенки и, следовательно, к появлению нежизнеспособных бактериальных клеток после деления. Так, бацитрацин и ванкомицин ингибируют биосинтез полисахаридных цепей гликопептида, а пенициллин угнетает заключительный этап — образование пентаглициновых сшивок. Гликопептид рассматриваемого типа — обитая основа клеточной стенки самых разнообразных бактерий в то же время подобные структуры отсутствуют в клетках животных организмов. Отсюда становятся понятными причины широты антибактериального спектра таких антибиотиков, с одной стороны, и их исключительно низкая токсичность для животных, с другой. [c.151] Высокая ценность антибиотиков и необходимость производства их в больших масштабах привели к созданию антибиотической промышленности, отличной от химической, основанной на биосинтезе, с поддержанием стерильности, интенсивной аэрации и контролируемой температуры в течение всего процесса ферментации. Явилась необходимость в селекции высокопроизводительных штаммов микроорганизмов — продуцентов антибиотиков для их очистки понадобилось создание экстракционного оборудования, аппаратуры для промышленной ионообменной хроматографии и др. [c.687] Добавление в питательную среду а-аминоадипиновой кислоты предотвращает ингибирующий эффект лизина и активирует биосинтез пенициллина в отсутствие лизина. Кроме ретроингибирования биосинтез многих антибиотиков тормозится высокими концентрациями своих же антибиотиков. Следует отметить, что в процессе эволюции микроорганизмы выработали механизмы защиты от действия собственных антибиотиков. Эта проблема успешно решается [c.68] Производственное получение антибиотиков, как правило, осуществляется путем биосинтеза и имеет много об щих стадий, основными из которых являются подбор высокопроизводительных штаммов и питательных сред процесс биосинтеза выделение антибиотика из культуральной жидкости иг его очистка [c.413] Дополнение 12-А. Биосинтез стрептомицина, т. 2, стр, 332 Дополнение 15-А. Антибиотики рифамиции и рифампицин, т. 3, стр. 208 [c.380] Интенсивность биосинтеза того или другого антибиотика-, зависит в первую очередь от свойств штамма продуцента. Природные штаммы в большинстве своем малоактивны и не могут использоваться для промышленных целей. Поэтому после отбора наиболее активного природного штамма продуцента антибиотика для повышения его продуктивности применяют различные приемы и методы, основанные на законах генетики. [c.413] Витамин В12 в настоящее время получается главным образом из естественных источников (отходы производства антибиотиков, биосинтез Ас. ргор1оп1сит, а также извлечение концентратов из активного ила водоочистительных стаиций — для целей животноводства и птицеводства). [c.206] Биосинтез антибиотиков, как и любых других вторичных метаболитов, возрастает в фазе замедленного роста клеточной популяции (конец трофофазы) и достигает максимума в стационарной фазе (идиофазе). Считают, что в конце трофофазы изменяется энзиматический статус клеток, появляются индукторы вторичного метаболизма, освобождающие гены вторичного метаболизма из-под влияния катаболитной репрессии. Поэтому любые механизмы, тормозящие клеточную пролиферацию и активный рост, стрессовые ситуации, активируют процесс образования антибиотиков. [c.67] Аминокислоты — структурные единицы белков. Природные аминокислоты вовлечены в биосинтез ферментов, ряда гормонов, витаминов, антибиотиков, алкалоидов, токсинов и других азотсодержащей соединений (пурины, пиримидины, гем и пр.). В организме животаого практически половина белковых аминокислот не синтезируется. Они назьтаются незаменимыми аминокислотами и должны поступать в организм с пищей. Недостаток каждой из этих аминокислот в пищевом или кормовом рационе приводит к, нарушенЁйб обмена веществ, замедлению роста и развития. Сведения о ежедневной потребности человека в незаменимых аминокислотах представлены в табл. 3.2. [c.40] См. лит. при ст. Каучуки синтетические. ИЗОПРЕНОИДЫ, природные соед., рассматриваемые как продукты превращ. изопрена, напр, его полимеризации, циклизации, окисления (на самом деле путь биосинтеза И. иной). К И. относятся терпены и их производные, стерины, стероиды, каучук натуральный, гуттаперча и др. Нек-рые И.— структурные фрагменты антибиотиков, витаминов, гормонов животных. [c.212] Огромные успехи исследований механизмов кодирования наследственной информации и биосинтеза белка, ферментативного катализа и регулирования активности ферментов, действия антибиотиков и гормонов, всей той области изучения живого, которую принято называть молекулярной биологией, приучили всех к мысли о том, что в структурах молекул жизни положение буквально каждого атома строго обусловлено и подчинено выполнению предназначенных для этих молекул биологических функций. Именно в атом смысле принято обычно говорить о специфичности биополимеров, прочно ассоциировавшейся в сознании исследователей с однозначным соответствием между структурой и выполняемой функцией. При таком комплексе стр>траспределения различных моносахаридных остатков по цепи. И, тем не менее, накапливающийся материал по сложному и высоко специализированному функционированию углевод ных полимеров в живых системах убеждает в том, что и в этой области возможен и необходим перевод функций- нальных свойств биополимеров на язык молекулярных структур, т. е. применим основной принцип молекулярной) [c.162] В издании рассмотрены все основные классы природных соединений, для которых приведены кпассификации, особенности молекулярной структуры, таблицы типичных представителей, схемы характерных химических реакций, значимые медико-биологические свойства, пути биосинтеза, природные источники При создании книги использована оригинальная литература по 2000 год вкпючительно Содержание книги отражено в 13 главах Введение, Простейшие бифункциональные природные соединения. Углеводы, Аминокислоты, пептиды и белки. Липиды жирные кислоты и их производные, Изопреноиды-1, Изопреноиды-И, от сесквитерпенов до политерпенов. Фенольные соединения. Алкалоиды и порфирины. Витамины и коферменты, Антибиотики, Разные группы природных соединений, Металло-знзимы, Предметный указатель [c.2] Другое важное свойство антрахинонов определяется энергетикой их граничных молекулярных орбиталей это эффективные электроноакцепторы, что позволяет им образовывать комплексы переноса заряда, а в сочетании с планарностью трициклического фрагмента — образовывать такие комплексы с парами Уотсона-Крика в структурах ДНК. Другими словами, антрациклиновые антибиотики могут интерка-лировать двойную спираль ДНК и тем самым ингибировать их биосинтез — на этом основано противоопухолевое действие данного класса препаратов. [c.306] Принципы получения вторичных метаболитов основаны на особенностях их образования клетками микроорганизмов. Биосинтез вторичных метаболитов фазоспецифичен и происходит по завершении стадии роста, в и 1 иофазе, благодаря чему их еще называют идиолитами (см. с. 32). Среди вторичных метаболитов ведущее место по объему производства занимают антибиотики. [c.61] Антибиотики, нашедшие широкое применение в медицине (пенициллины, цефалоспорины, циклосерин и нек-рые др.), блокируют отдельные стадии биосинтеза П. отсутствием П. в клетках эукариот (все организмы, за исключением бактерий и синезеленых водорослей) объясняется избирательность этнх антибиотиков по отношению к бактериальным клеткам. Бактерицидное действие фермента лизоцима обусловлено расщеплением углеводных цепей П. путем гидролиза гликозидных связей остатков Ы-ацетил-О-мурамовой к-ты. [c.468] Другой способ получения антибиотиков состоит в использовании для их биосинтеза блокированных мутантов, у которых отсутствует (блокировано) определенное звено в цепи реакций, веду-ищх к синтезу антибиотика. Блокированные мутанты не способны образовывать нужный антибиотик. Используя низкую субстратную специфичность ферментов вторичного метаболизма и вводя аналоги предшественников антибиотика, последние переводят в аналоги самого антибиотика в ходе процесса, известного как мутационный биосрштез, или мутасинтез [c.65] Т.-антибиотики ншрокого спектра действия. Они активны в отношении грам1юложит. и грамотрицат. бактерий. Механизм антибактериального действия Т. основан на подавлении ими биосинтеза белка микробной клетки. [c.559] Первоначально витамин В12 получали исключительно из природного сырья, но из 1 т печени можно было вьщелить всего лишь 15 мг витамина. Единственный способ его получения в настояшее время — микробиологический синтез. Обнаружение витамина в качестве побочного продукта при производстве антибиотиков в значительной степени стимулировало поиск организмов-проду-центов витамина и изучение путей его образования. Однако механизмы регуляции биосинтеза витамина В до настоящего времени полностью не расшифрованы. Известно, что при высоких концентрациях витамин полностью репрессирует синтез ключевых ферментов своего новообразования. [c.55] В Советском Союзе получение витамина В12 сочетается с производством антибиотика стрептомицина, поскольку для того и другого продуцентом является один и тот же актиномицет (лучистый гриб) — Streptomy es griseus. Изменяя технологические условия, можно направить процесс биосинтеза либо в сторону выхода витамина В12 (прибавление в питательную среду солей кобальта), либо в сторону выхода стрептомицина. [c.407] chem21.info |
г.Самара, ул. Димитрова 131 [email protected] |
 |