|
|
||||||||||
|
О группах антибиотиков, их видах и совместимости. 18 групп антибиотиков18.Микробный антагонизм.— угнетение роста одного микроба другим, одна из форм взаимоотношений между микроорганизмами в ассоциациях. Антагонистические свойства присущи многим почвенным споровым и гнилостным бактериям, актиномицетам, грибам (базидальным, сумчатым и др.). Механизм антагонистического действия микробов может быть связан с различными причинами: образованием токсических продуктов метаболизма, антибиотиков. Антибиотики-разновидность химиотерапевтических препаратов,содержащие специфические вещества,образуемые клеткой в процессе жизнедеятельности.Являются продуктами метаболизма многих микро-в,высших растений. Для производства природных антибиотиков используют штаммы бактерий,грибов,ко-е засевают в питательный субстрат,далее экстрагируют,очищают,концентрируют,проверяют на безвредность и активность.За единицу активности принимают минимально кол-о антибиотика, кот-е задерживает рост стандартного штамма определенного вида. 19.Классификация антибиотиков.По спектру биологи-о дей-я: Узкого спектра действия(нистатин,леворин) Широкого спектра действия(тетрациклины,левомицетин) По биоллогич-у происх-ю: Из микроорганизмов Из высших растений Из клеток животных. По химическому строению: Беталактамиды(пенициллины,цефалоспорины) Тетрациклин и его полусинтетические производства. Макролиды Левомицетин Полиеновые антибиотики. 20.Механизмы действия различных групп антибиотиков.1.Ингибирующий синтез клеточной стенки(пенициллины,цефалоспорины) 2.Нарушающие функции цитоплазматической мембраны(полиеновые антиб-и,полимиксины) 3.Ингибирующие синтез белков на рибосомах(тетрациклины,левомицетин) 4.Угнетающие синтез нуклеиновых кислот(рифампицин). 21.Методы определения чувствительности бактерий к антиб-м.Метод дисков-на чашку Петри с плотной питательной средой засеивают взвесь изучаемой культуры микроба. На засеянную поверхность агара помещают и слегка прижимают бумажные диски,пропитанные антиб-и.Диски накладывают на равном расстоянии друг от друга.Чашки выдерживают при 37 градусов 16-18 часов,учитывают результаты путем измерения зон задержки роста микробов вокруг дисков,включая диаметр самого диска. Зона 10 мм-устойчивый,11-15мм-малоус-й, 15-25мм- чувствительный и выше- высокочувтвительный. Метод серийных разведений. Им определ-т минимальную концентрацию антибиотиков. Вначале готовят основной раствор,содержащий ряд последовательных двойных разведений в питательной среде. Далее к каждому разведению добавляют смыв суточной агаровой культуры испытуемого микроор-а.Результаты учитывают после инкубации при 37 градусах в течении 18-20 часов. Минимальную концентрацию антибиотика определяют по последней пробирке с прозрачным бульоном при наличии интенсивного роста в контроле. 22.Механизмы возникновения антибиотикорезистентности.В основе механизма распространения генов антибиотикорезистентности между бактериями лежит обмен плазмидами и конъюгативными транспозонами. В эволюции антибиотикорезистентности плазмиды и конъюгативные транспозоны выполняют функцию генетических платформ, на которых посредством рекомбинационных систем бактерий происходит сборка и сортировка генов антибиотикорезистентности, включенных в транспозоны, интегроны, генные кассеты и инсерционные криптические последовательности. К настоящему времени известно не менее четырех биохимических механизмов, отвечающих за развития у бактерий антибиотикорезистентности: детоксикация антибиотика; уменьшение проницаемости стенки микроорганизма для антибиотиков и/или выкачивание его из клетки; структурные изменения в молекулах, являющихся мишенями для антибиотиков; продукция альтернативных мишеней для антибиотиков. Высокие уровни антибиотикорезистентности у грамотрицательных бактерий обусловлены их способностью детоксицировать антибиотики в периплазматическом пространстве. В клеточной стенке грамположительных бактерий периплазматическое пространство отсутствует, поэтому механизмы их детоксикационной резистентности к антибиотикам менее эффективны, чем у грамотрицательных бактерий. Целесообразно расширить круг исследуемых проблем, связанных с распространением антибиотикорезистентных патогенных микроорганизмов в клинике, включив в него процессы накопления и обмена генов антибиотикорезистентности среди бактерий в природных экосистемах. Антибиотики следует применять только по показаниям, когда заболевание вызвано микроорганизмами, в отношении которых существуют эффективные препараты. Для их подбора необходимо до назначения лечения взять у больного материал для исследования, выделить чистую культуру возбудителя и определить его чувствительность к антибиотикам. Чувствительность к антибиотикам, или антибиотикограмму, определяют с помощью методов разведения и диффузии (к ним относится метод бумажных дисков). Методы разведения являются более чувствительными: с их помощью выясняют, какой антибиотик эффективен по отношению к данному микроорганизму, и определяют его необходимое количество . минимальную подавляющую концентрацию (МПК). Фармакологический принцип. При назначении антибиотика необходимо определить правильную дозировку препарата. studfiles.net 15. Группы антибиотиков, ингибирующих синтез рнк.1. Ансамицины. 2. Гризеофульвин 16. Механизмы развития резистентности микроорганизмов к антибиотикам.Приобретенная резистентность формируется при модификации детерминант природной чувствительности: А) Снижение проницаемости внешних структур микроорганизма к АБ (либо с прекращением поступления АБ в клетку МБ, либо с усилением процессов выведения АБ из клетки; характерен для тетрациклинов, аминогликозидов) Б) Маскировка или модификация мишени действия АБ: ü хромосомная резистентность к бета-лактамам в результате модификации пенициллинсвязывающего белка ü резистенстность к аминогликозидам в результате утраты или повреждения L-белков 30S-субъединицы бактериальной рибосомы и др. В) Индукция экспрессии или появление новых форм ферментов биотрансформации АБ (бета-лактамазы для пенициллинов; аминогликозидтрансферазы, ацетилтрансферазы, фосфортрансферазы, нуклеотидилтрансферазы для аминогликозидов) Г) Переход на коллатеральные метаболические пути (замена ПАБК фолиевой кислотой при применении сульфаниламидов) 17. Приобретение устойчивости бактерий к антибиотикам, причины. Осуществляется на генетическом уровне за счет мутаций собственной бактериальной хромосомы, генов, принесенных бактериофагами. На БХ уровне это проявляется за счет механизмов резистентности: 1. модификации мишеней действия препаратов 2. ферментативная инактивация 3. активное выведение препарата из микробной клетки 4. снижение проницаемости внешних структур клетки. Основные механизмы приобретения устойчивости штаммов МО в макроорганизме: 1. возбудитель теряет чувствительность к АБ в процессе лечения 2. получение резистентного штамма извне 3. селекционное давление (в ходе лечения погибает возбудитель, размножаются другие бактерии) 4. сочетание нескольких механизмов развития устойчивости. Возможно наличие природной устойчивости МО к определенной группе АБ. 18. Осложнения антибиотикотерапии со стороны макроорганизма. 1. Действие на иммунитет: -аллергические реакции -подавление отдельных звеньев иммунитета 2. Дисбактериоз 3. Токсические реакции (гепато- и нефротоксические действия) 19.Методы изучения чувствительности бактерий к антибиотикам.Определение чувствительности бактерий к АБ. 1. Метод дисков -посев газоном -диски с разными АБ - (37°С 24-48 ч) зона задержки роста определяется по диаметру. 2. Метод серийных разведений 1:100 1:200 1:400 ... +контроль (без АБ) Устанавливается оптимальная концентрация АБ. -Чувствительные МО (рост МО подавляется при использовании обычных доз препарата.) -МО умеренной устойчивости (рост МО подавляется при использовании максимальных доз препарата.) -Устойчивые МО (рот не подавляется препаратом). 20.Стерилизация. Методы стерилизации. Предстерилизационная очистка — механическое удаление инородного материала с обеззараживаемой поверхности. Стерилизация — полное уничтожение МО. а) тепловая -сухим жаром -паром под давлением -текучим паром -дробная стерилизация -тиндализация (дробная с низкими температурами) б) лучевая (гамма излучение) в) химическая (спирты, перекись водорода, йод) г) газовая (окиси этилена и формальдегида при 60-80°С) Контроль стерилизации: -физические методы -химический контроль -биологический контроль. 21.Дезинфекция. Дезинфекция — физический или химический процесс, в результате которого уничтожаются все МО, кроме спор бактерий. -тепловая -УФ облучение -химическая. Для дезинфекции применяют: - альдегиды (глутаральдегид, формальдегид) - кислородсодержащие препараты (перекись водорода) - хлорактивные соединения (хлорная известь, хлорамин) - соединения йода (йодофоры) - спирты (этиловый и изопропиловый) - ПАВ - фенилсодержащие препараты. 22.Понятие об асептике и антисептике. Асептика — комплекс мер для предупреждения попадания возбудителя инфекции в рану или органы больного. Антисептика — совокупность мер для уничтожения микробов. -физическая антисептика -механическая антисептика -химическая антисептика. Антисептики: а) галоиды (препараты йода, хлора) б) перекись водорода в) кислоты и их соли, щелочи, спирты, альдегиды г) детергенты д) производные нитрофурана е) фенол и его производные ё) красители ж) соединения тяжелых металлов -биологическая антисептика. studfiles.net Группы антибиотиков: классификация, применение, побочный эффектКаждый слышал о существовании и предназначении антибиотиков, но не все знают, какие существуют группы антибиотиков и в чем их принципиальное различие. Тем не менее, эта информация является важной для понимания тех или иных предписаний врача и становится ключевой при выборе препарата для лечения. Об основных группах антибиотиков и различиях между ними речь пойдет далее. Антибиотики – это группа лекарственных препаратов, которые направлены на борьбу с болезнетворными микроорганизмами – бактериями. В зависимости от происхождения антибиотические препараты можно разделить на природные, полусинтетические и синтетические. При этом, строго говоря, название «антибиотик» присваивается только первой группе препаратов, т.е. натурального происхождения. Полусинтетические и синтетические антибиотики принято называть антибактериальными препаратами, хотя между этими терминами нет принципиальной разницы. Противомикробные лекарства получают из различных живых организмов: тканей рыб и животных, растений, плесневых грибов. В зависимости от мишеней воздействия различают антибактериальные, противогрибковые и противоопухолевые противомикробные лекарства. Несмотря на то, что в начале статьи было упомянуто о том, что антибиотики главным образом рассматриваются как препараты для борьбы с бактериями, такие группы лекарств также существуют под этим названием. В зависимости от направленности действия на бактерии выделяют антибиотические лекарства широкого и узкого спектров действия. Препараты широкого спектра действия эффективно воздействуют против многих видов организмов, тогда как антибиотики узкого спектра действия разработаны для борьбы с конкретным возбудителем заболевания. По типу воздействия на бактерии выделяют бактериостатические и бактерицидные типы антибиотических лекарств. Бактериостатические антибиотики препятствуют делению и росту бактерий, после чего выжившие микроорганизмы уничтожаются иммунной системой человека. Бактерицидные же препараты повреждают оболочку бактерий, напрямую разрушая их, из-за чего гибнут не только патогенные, но и симбиотически существующие в организме человека бактерии. Классификация антибиотиков по химическому составуНа данный момент антибиотики разных групп различают именно по принципу химической структуры. Самыми ранними из открытых антибиотиков являются пенициллины, которые впервые были получены из плесневых грибков. На сегодняшний день существует несколько поколений пенициллинов, последние из которых, полученные полусинтетическим методом, устойчивы к воздействию мутировавших бактерий и с меньшей вероятностью воспринимаются организмом человека как аллерген. Вторая группа антибиотиков – цефалоспорины, которых на данный момент насчитывается 4 поколения. Эти антибиотики оказывают бактерицидное действие и используются главным образом для лечения половых инфекций, инфекций кожи и слизистых в ЛОР-практике. Преимуществом этой группы антибиотических лекарств является их доступность для использования во время беременности, т.к. они не оказывают вредного воздействия на плод. Следующая группа препаратов – макролиды. Эти антибактериальные лекарства обладают бактериостатическим эффектом, избирательны в действии на различные бактерии. Кроме того, преимуществом препаратов является возможность применения их в течение краткого курса, минимальная токсичность и возможность возникновения аллергических реакций. Тетрациклины – еще одна широкая группа антибиотических лекарств, включающая в себя препараты природного и синтетического происхождения. Эти лекарства используются для лечения тяжелых бактериальных и гнойных воспалений. Наиболее эффективным считается применение тетрациклинов в виде мазей, т.к. при системном воздействии бактерии начинают быстро приспосабливаться к препарату. Аминогликозиды – препараты, которые используются против грамотрицательных аэробных бактерий. Несмотря на высокую эффективность этих препаратов, они используются в медицинской практике довольно редко из-за своей высокой токсичности и агрессивного бактерицидного эффекта, который повреждает естественную микрофлору организма. Существуют и другие виды групп антибиотических препаратов, представители которых также используются в медицинской практике. Кроме того, выделяют особые группы препаратов для лечения туберкулеза, грибковых заболеваний, опухолей, проказы. Некоторые существующие антибиотики являются по своему составу комбинированными, за счет чего относятся к отдельной категории препаратов. Другие классификации антибиотиковРаспределение антибиотиков по группам возможно и по другим основаниям. Например, антибиотики делятся по способу применения на пероральные, инъекционные и местные. Пероральные препараты принимаются в виде таблеток, капсул, сиропов, порошков и растворов через рот. Большинство классов и поколений антибиотиков имеют препараты в этой форме выпуска. Она удобна для приема пациентами, не требует специальных навыков и условий, и в большинстве случаев эффективно доставляет лекарство для борьбы с системной инфекцией. Инъекционный метод введения антибиотических препаратов имеет преимущество перед пероральным в плане скорости всасывания лекарства и достижения терапевтического эффекта. Кроме того, при этом способе введения лекарства не страдает кишечная микрофлора, что особенно важно для ослабленных пациентов. Однако внутримышечные и внутривенные инъекции должны выполняться только профессионально подготовленным медицинским персоналом в стерильных условиях, т.к. подготовка антибиотиков к введению требует специальных навыков. Местный способ введения – это капли и мази, которые применяются при локализованных инфекциях. Такой способ применения позволяет избежать повышения общей чувствительности микроорганизмов к антибиотикам и воздействовать непосредственно на очаг заболевания, что уменьшает токсические эффекты и повышает эффективность лечения. Путь введения лекарства зависит не только от доступной формы выпуска, но и от вида заболевания, состояния пациента. Его должен определить врач на основании анализа многих факторов, центральными из которых являются локализация очага инфекции. Кроме того, варьирование различных способов введения позволяет увеличить совместимость различных препаратов между собой. С лекарственным взаимодействием приходится считаться при хронических заболеваниях у пациента и при присоединении вторичных заболеваний во время бактериальной инфекции. Подбор антибиотиковКак уже было упомянуто ранее, противобактериальные средства чаще всего эффективны против ограниченной группы патогенной микрофлоры. Помимо этого, именно подбор антибиотиков узкого спектра действия наиболее эффективен в лечении инфекционных заболеваний, т.к. он минимально изменяет природный иммунитет организма. Именно поэтому назначать антибиотики может только специалист. Прежде всего, врач на приеме может приблизительно определить тип возбудителя в зависимости от локализации очага поражения. Например, можно разделить грамположительные и грамотрицательные бактерии, которые имеют различные места локализации и характерные проявления. Это уже дает основания для определения чувствительности к антибиотикам определенной группы в конкретном случае заболевания. Наиболее информативно способствует назначению верного препарата результат лабораторных анализов. Для его проведения у пациента берут субстрат (мочу, кровь, слизь и т.д. в зависимости от места поражения) и производят посев бактериальной флоры с целью выявить ее количественный, качественный состав, а также то, насколько чувствительные бактерии в конкретном штамме к тем или иным видам препаратов. Если при инфицировании было обнаружено несколько групп возбудителей, то для каждого из них идет подбор антибиотиков по группам, проверяется совместимость препаратов между собой, или же назначается препарат широкого спектра действия, который был бы эффективен против всех обнаруженных возбудителей. Важно понимать, что назначение врача для приема антибиотических средств необходимо еще и по той причине, что бактериальное и вирусное заболевание легко спутать по внешним признакам человеку без медицинского образования, и, тем более, без лабораторных анализов. Тем не менее, антибиотики неэффективны против вирусных возбудителей и в случае их применения могут только усугубить обстановку, снизив местный иммунитет организма. Особенности применения антибиотиковПомимо уже означенной важности приема антибиотических средств только по назначению лечащего врача, антибиотические лекарства имеют и другие особенности, которые необходимо знать и соблюдать для эффективного и безопасного лечения. Например, необходимо знать о том, что большинство антибиотиков обладают тератогенным действием, поэтому при прохождении антибактериального лечения необходимо воздерживаться от наступления беременности во избежание ее осложнений и появления врожденных уродств у плода. Антибиотические лекарства на ранних сроках беременности должны применяться только в тех случаях, когда заболевание угрожает жизни матери или сохранению плода с большей степенью вероятности, чем применение токсичных препаратов. Кроме того, необходимо иметь в виду, что подавляющее большинство препаратов негативно сказываются на состоянии печени. Поэтому больным с печеночной недостаточностью лечение системными антибиотическими лекарствами назначают только в случаях крайней необходимости, под присмотром врача в стационаре. Здоровым же людям, во избежание наступления проблем с этим органом, следует избегать приема алкоголя на протяжение всего курса лечения, а также соблюдать диету, обеспечивающую минимальную нагрузку на печень. Следует иметь в виду, что некоторые антибиотические средства не совместимы с отдельными продуктами питания (как, например, употребление молочных продуктов снижает эффективность перорального введения тетрациклинов). Возможные побочные эффекты антибиотиковНесмотря на безусловную пользу антибиотических средств в лечении инфекционных заболеваний, они имеют свои побочные эффекты. Прежде всего, это токсический эффект, который практически неизбежен для ослабленного болезнью организма, и тем более при длительном приеме антибиотических препаратов. Это уже упомянутые проблемы с печенью у взрослых, и ототоксичный эффект (снижение слуха, особенно у детей и развивающегося плода), и замедление роста костной ткани у детей. При индивидуальной непереносимости компонентов препарата токсический эффект проявляется даже при употреблении минимальных доз препарата. Из-за влияния антибиотических препаратов на полезные для организма человека бактерии, у пациентов на фоне приема лекарств могут возникнуть симптомы дисбактериоза – различные кишечные и желудочные расстройства, которые могут продолжаться довольно длительное время, если во время курса препаратов или сразу по его завершении не принимать специальные лекарства для восстановления флоры ЖКТ. Часто встречаются и аллергические реакции на антибиотические препараты. Они зачастую возникают потому, что организм, подвергшись угнетению иммунитета сперва из-за болезни, а затем и из-за гибели естественной флоры, начинает из последних сил агрессивно реагировать на любое постороннее вмешательство, за которое и принимает компоненты лекарства. Аллергические реакции могут проявляться различным образом от относительно безобидной крапивницы и заканчивая тяжелыми отеками и удушьем. Таким образом, нельзя отрицать пользу антибиотиков для сохранения здоровья человечества. Однако, учитывая имеющееся разнообразие групп этих препаратов, следует доверить ориентировку среди них профессионалу – лечащему врачу, для достижения максимального эффекта от лечения при минимальных побочных эффектах для организма человека. proantibiotik.ru Все, что вам нужно знать про антибиотики. Часть 3. Досье на популярные группы
Здравствуйте, дорогие друзья! Сегодня мы с вами завершим разбор наиболее популярных групп антибиотиков. Напомню, что пока мы с вами поговорили только о пенициллинах и цефалоспоринах. Постараюсь не растекаться мыслью по древу и быть краткой, чтобы вы у меня тут не заснули. Ведь откровенно говоря, как написала одна моя читательница в комментариях, тема-то скуууучная… Но я сильно надеюсь, что вы победите сон и дочитаете статью до конца. Хотя бы потому, что я для вас очень старалась. :-) А если дочитаете, то я уверена, что вы возьмете из нашего сегодняшнего разговора что-то полезное для себя. Это вам поможет при случае просветить и вразумить любителей «палить из пушки по воробьям» и выпрашивать у вас антибиотики. Ну что же, приступим. Группа аминогликозидов
Аминогликозиды были выделены из лучистых грибков рода Actinomyces в 1944 году. Родоначальником этой группы является стрептомицин. Существует 3 поколения аминогликозидов:
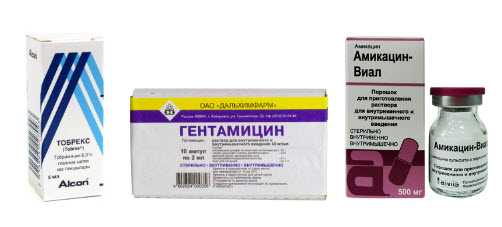
Стрептомицин чаще всего применяли в лечении туберкулеза, но туберкулезная палочка к нему быстро адаптировалась, и честно говоря, не знаю, применяют ли его сейчас. Канамицин в этом плане оказался более стойким. А вот к неомицину резистентность микробов практически не развивается. Поэтому он до сих пор широко используется в некоторых средствах для местного применения: Полижинакс, Тержинан, Флуцинар Н, Пимафукорт, Анауран, Полидекса, Макситрол и др. Гентамицин. Резистентность к нему развивается медленно. Он применяется не только парентерально, но, подобно неомицину, входит в состав ряда наружных средств, таких как: Целестодерм-В с гарамицином, Гаразон, Акридерм ГК, Тридерм и др. К тобрамицину микробы еще не сумели приспособиться. Помните, в состав какого средства он входит? Правильно! :-) В состав глазных капель Тобрекс. Препарат третьего поколения Амикацин когда-то произвел фурор в клинической практике. Его назначали при тяжелых инфекционных заболеваниях: он очень хорошо работал там, где его «коллеги» оказывались бессильны. Но ввиду токсичности Амикацина, его применение ограничено. Механизм действияАминогликозиды оказывают бактерицидное действие: они угнетают синтез белка – основного строительного материала бактериальной клетки, и она гибнет. На каких возбудителей они действуют?Наибольшую активность они проявляют в отношении грамотрицательных бактерий: кишечной палочки, протея, клебсиеллы, действуют на возбудителей туберкулеза, чумы, бруцеллеза, туляремии, на синегнойную палочку, менингококк. Как они ведут себя в организме?При приеме внутрь они практически не всасываются, поэтому применяются парентерально, кроме неомицина, который оказался самым токсичным для слухового нерва. По этой причине его используют только в наружных средствах. И только на неповрежденные поверхности, иначе он попадет в системный кровоток и может вызвать побочные эффекты. Основные показания к применению аминогликозидов
Побочные эффектыПомню, были времена, когда Гентамицин назначали направо-налево всем подряд, включая новорожденных. А между тем, антибиотики этой группы очень токсичны. Они ототоксичны, то есть повреждают слуховой и вестибулярный аппараты, вызывая снижение слуха или даже полную и необратимую его потерю, нарушение координации движений, головокружение. Они нефротоксичны, т.е. оказывают повреждающее действие на почки, особенно часто у пожилых, если применяются длительно и в высоких дозах. К счастью, после отмены препарата, функция почек в большинстве случаев восстанавливается. Они могут вызвать нервно-мышечную блокаду вплоть до полного паралича дыхательных мышц. Беременные, кормящие, дети, пожилыеБеременным аминогликозиды назначаются только в крайнем случае, так как они могут оказывать нефротоксическое действие на плод и вызывать врожденную глухоту. Кормящим – осторожно, поскольку эти средства проникают в грудное молоко, и нарушают кишечную микрофлору малыша. Детям – только при непереносимости других антибиотиков или в случае чувствительности возбудителя только к этой группе, так как они вызывают угнетение нервной системы: ступор, вялость и даже кому. Пожилым они назначаются только по жизненным показаниям: у большинства людей преклонного возраста почки работают уже не так, как хотелось бы. Группа макролидов
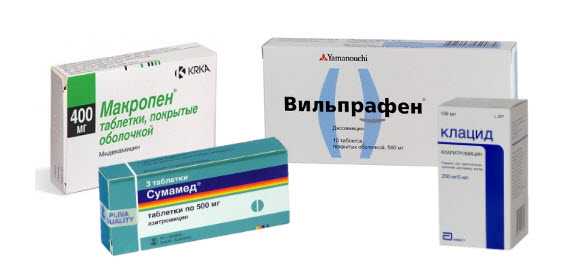
Макролиды – любимая многими врачами группа препаратов. Родоначальником группы является эритромицин, выделенный в 1952 году из почвенного грибка с труднопроизносимым названием Streptomyces erythreus. В химической формуле макролидов может содержаться 14, 15 или 16 атомов углерода, и чаще всего макролиды подразделяют не по поколениям, а вот так:
Преимущества макролидов
Пару слов об особенностях некоторых макролидов. Эритромицин – сейчас не знаю, а когда-то его особенно любили назначать при заболеваниях горла (ангина, фарингит). Из группы макролидов он чаще других (в 30-40% случаев) вызывает побочные эффекты и прежде всего, боли в животе, тошноту, рвоту, диарею, так как усиливает перистальтику желудочно-кишечного тракта. У пожилых его применение приводит к снижению слуха (!) Принимать его следует за час до еды, так как пища уменьшает его биодоступность. Кларитромицин – в отличие от других макролидов, проявляет высокую активность в отношении Helicobacter pylori, который, как считают, является виновником язвенной болезни. Так что он включен в схемы эрадикации, т.е. уничтожения этой микробины. Побочные эффекты дает в 16% случаев. Его можно принимать независимо от приема пищи. Азитромицин отличается короткими схемами приема (1-3 дня). Побочные эффекты вызывает в 9% случаев (чаще всего, диспепсические расстройства). Лечебная концентрация сохраняется 5-7 дней после приема последней дозы. Механизм антибактериального действия макролидовМакролиды, как и предыдущая группа, тоже подавляют синтез белков в бактериальной клетке, но действуют они бактериостатически. Хотя в высоких концентрациях оказывают бактерицидное действие. Правда, микробы пытаются адаптироваться и к макролидам. Одни из них вырабатывают ферменты, которые мешают связыванию антибиотика с рибосомами бактериальной клетки, где происходит синтез белка. Другие без зазрения совести выпроваживают антибиотик из своего дома с помощью транспортных белков. И, тем не менее, резистентность микробов к ним пока считается невысокой. На каких возбудителей действуют?Они активны в отношении грамположительных кокков (стафилококков, стрептококков, пневмококков), действуют на возбудителей коклюша, дифтерии, токсоплазмоза, но самая главная их особенность – способность проникать внутрь клетки, где любят обустраивать себе жилье хламидии, микоплазмы и некоторые др. микроорганизмы. Мало какие антибиотики могут этим похвастаться. А поскольку выше упомянутые инфекции чрезвычайно распространены среди сексуально активных слоев населения, то не зарастет народная тропа в аптеку жертв внутриклеточных оккупантов с внушительным списком препаратов наперевес. :-) Как они ведут себя в организме?В целом макролиды хорошо всасываются в желудочно-кишечном тракте, но на их всасывание влияет прием пищи. Он значительно уменьшает биодоступность эритромицина, в меньшей степени – азитромицина, рокситромицина и мидекамицина и практически не влияет на биодоступность кларитромицина, спирамицина и джозамицина. Основные показания к применению
Наиболее частые побочные эффекты
В инструкциях вы увидите огромный список побочных, которые я здесь перечислять не буду. Среди них есть и серьезные. Но все-таки, сколько публикаций я не встречала, большинство докторов сходится во мнении, что это наиболее безопасная группа. А вы как считаете, друзья? Беременные, кормящие, дети, пожилыеБеременным – назначают, взвесив все «за» и «против», если нет альтернативы (кроме рокситромицина, который противопоказан). Только Джозамицин (Вильпрафен) разрешен. Кормящим – макролиды проникают в грудное молоко, поэтому лучше воздержаться. Джозамицин разрешен. Детям – применяются в возрастных дозировках и соответствующих формах выпуска. Пожилым – без особенностей. Чаще, чем у молодых, встречается нарушение функции печени. А при использовании эритромицина – снижение слуха. Важно! Антациды уменьшают всасывание макролидов, особенно азитромицина. Группа тетрациклинов
К этой группе относятся тетрациклин и доксициклин. Эти средства очень токсичны, вызывают массу побочных эффектов, хотя и действуют на «миллион» всяких-разных микробов, включая внутриклеточные и экзотические. Механизм действияДействуют бактериостатически, подавляя синтез белка в микробной клетке. На кого действуют?Активны в отношении стафилококков, стрептококков, гонококков, клебсиел, возбудителей сальмонеллеза, дизентерии, хламидийной инфекции, сифилиса, а доксициклин плюс к этому действует на микроорганизмы, вызывающие туляремию, холеру, бруцеллез, лихорадку Ку и много других инфекций. Как они ведут себя в организме?Безобразно! :-) Наверное, нет ни одной системы в теле человека, которую не затронули бы антибиотики этой группы. Сам тетрациклин всасывается в ЖКТ примерно на 60-80%, а доксициклин – на все 100. Основные показания к применениюЯ даже затрудняюсь выделить наиболее частые инфекции, при которых врачи назначают тетрациклины, и прежде всего, доксициклин:
Побочные эффекты:
Как видите, побочных много, и очень серьезных, поэтому НИКОГДА не рекомендуйте тетрациклины самостоятельно. Как, впрочем, и антибиотики других групп. Беременные, кормящие, дети, пожилыеБеременным и кормящим – противопоказаны. Детям –с 8 лет. Тетрациклины замедляют рост костей у детей, необратимо изменяют цвет зубов на желтый или светло-коричневый. Пожилым – противопоказаны при тяжелых нарушения функции печени. Важно! Доксициклин снижает эффективность эстрогенсодержащих пероральных контрацептивов – во лечения этим препаратом необходимо использовать альтернативные средства контрацепции. Антациды уменьшают всасывание тетрациклинов, поэтому между их приемами нужно делать перерыв 1-3 часа. Для профилактики изъязвления желудочно-кишечного тракта доксициклин принимают в дневные часы с большим количеством жидкости, лучше во время еды. Учитывая, что тетрациклины вызывают фотосенсибилизацию, пребывание на солнце следует ограничить во время лечения доксициклином и в течение 4-5 дней после него. Предупреждайте об этом покупателя! А лучше предложите ему на этот период солнцезащитные средства. Напомню вам, что фотосенсибилизация – это повышенная чувствительность кожи к действию ультрафиолетовых лучей. Она может проявиться либо тяжелым солнечным ожогом с покраснением и образованием пузырей, либо коричневыми пятнами на открытых участках тела. Группа линкозамидов |
||||||||||||||||||||||||||||||||||||
г.Самара, ул. Димитрова 131 [email protected] |
 |