|
|
||||||||||
|
4. Меры предосторожности при интратекальном введении антибиотиков. Эндолюмбальное введение антибиотиковЭффективность эндолюмбального введения антибиотиков - Заболевания центральной нервной системы - Некоторые особенности применения антибиотиков в клинике - Рациональная антибиотикотерапияОтносительно целесообразности и эффективности эндолюмбального введения антибиотиков в настоящее время нет единого мнения. При строгом соблюдении техники введения (не быстрее 1 мл раствора в минуту) и ограничении доз и кратности введения (эндолюмбально рекомендуют вводить антибиотики не более 3 раз) эффективность эндолюмбального введения антибиотика связана с быстрым созданием бактерицидной концентрации антибиотика в ликворе и длительностью ее сохранения. Терапевтическая концентрация (0,25 —0,08 ЕД/мл) в ликворе после однократного введения бензилпенициллина обнаруживается в течение 12 ч, стрептомицина—24—36 ч. Имеются данные, что эндолюмбальное введение антибиотиков значительно улучшает течение процесса как в ранней, так и в поздней стадии болезни. При менингитах пневмококковой и стафилококковой этиологии вводят бензилпенициллин эндолюмбально (в виде натриевой соли). При выделении устойчивых стафилококков назначают метициллин или оксациллин. При менингитах, вызванных гемофильной палочкой, применяют эндолюмбально стрептомицин или ампициллин. При менингококковом менингите эндолюмбальное введение антибиотиков не показано. Бензилпенициллин эндолюмбально применяют в следующих дозах: новорожденным—2500 ЕД, грудным детям — 2500—5000 ЕД, детям до 4 лет —5000 ЕД, от 4 до 14 лет —5000—8000 ЕД, взрослым — 10 000 ЕД (при данной дозе через 12 ч в ликворе обнаруживается концентрация 0,25—0,08 ЕД/мл). Метициллин взрослым вводят в дозе 25 мг. Стрептомицин эндолюмбально назначают в виде хлоркальциевого комплекса, новорожденным в дозе 8—10 мг, детям до 2 лет—10—15 мг, до 4 лет—20—35 мг, до 10 лет—35—50 мг, взрослым—50—75 мг. Ампициллин детям вводят в дозе 5—10 мг, взрослым—10—20 мг. Ориентировочные дозы антибиотиков, наиболее часто применяемых при лечении менингитов, приведены в таблице ниже. Ориентировочные схемы антибиотикотерапии при бактериальных менингитах (внутривенное, внутримышечное введение)
При этом необходимо учитывать, что предлагаемые схемы антибиотикотерапии могут корректироваться в зависимости от индивидуальных особенностей течения заболевания, свойств возбудителя и др. «Рациональная антибиотикотерапия»,С.М.Навашин, И.П.Фомина Смотрите также на тему:www.medvyvod.ru Интратекальное введение лекарственных препаратов - НеврологияИнтратекальное введение (эндолюмбальное введение) обозначает доставку вещества в подоболочечное пространство (от лат. teka - оболочка), т.е. субарахноидально, после прокола твердой мозговой оболочки. В нейрохирургической практике при выполнении лекарственных блокад анестетик и кортикостероидные препараты могут вводиться в эпидуральное пространство, т.е. между твердой оболочкой спинного мозга и желтой связкой.Основными преимуществами интратекального введения являются [1] возможность создания максимальных концентраций лекарственного вещества в мозговой ткани и цереброспинальной жидкости (ЦСЖ), а также [2] введение препаратов, не проникающих через гематоэнцефалический барьер. В ряде случаев введение лекарственного средства в концевую цистерну позволяет [3] уменьшить его дозу и [4] снизить его системное токсическое воздействие. К недостаткам метода можно отнести [1] относительно сложную методику введения фармакологических средств, [2] риск перепадов интракраниального давления и [3] невозможность введения эмульсий и суспензий. При соблюдении техники выполнения люмбальной пункции (ЛП) вероятность повреждения мозговой ткани минимальна. Одним из основных показаний для введения антибактериальных препаратов в ЦСЖ методом пунктирования люмбального пространства является бактериальный менингит. Такая процедура показана при отсутствии клинического и лабораторного улучшения состояния больного в течение 72 ч после начала парентерального введения антибиотиков. Существует точка зрения, что данный временной промежуток должен быть меньше, и отсутствие санации ЦСЖ на фоне проводимого лечения в течение 24 - 48 ч - достаточное основание для интратекальной противомикробной терапии. Показаниями для этого вида лечения являются вентрикулит (воспаление эпендимы желудочков мозга, обычно развивающееся в результате ее инфекционного поражения), поздно начатое лечение и рецидив менингита или менингоэнцефалита, особенно у больных с иммунодефицитом. Основные группы антибиотиков, используемых для введения в ЦСЖ с учетом наиболее вероятной природы возбудителей и их резистентности к препаратам данной группы. В настоящее время при бактериальном поражении ЦНС в концевую цистерну вводятся аминогликозиды (амикацин, гентамицин, тобрамицин), ванкомицин, полимиксин, диоксидин. Коррекция этиотропного лечения, как правило, проводится после получения результатов бактериологического исследования. В случае курсового введения антибиотиков показанием для отмены данной манипуляции являются [1] появление признаков токсического воздействия препарата (снижение содержания белка в ЦСЖ ниже 1 г/л) и [2] наступление лимфоцитарной санации ЦСЖ (кроме туберкулезного поражения ЦНС). Необходимо помнить о недопустимости введения в ликворное пространство калиевой соли пенициллина и колистина (полимиксин Е) - это может привести к летальному исходу прямо во время процедуры.Также необходимо помнить, что введение антибиотика в эндолюмбальное пространство не заменяет этиотропной терапии, получаемой больным парентерально. Кроме того, необходимо учитывать такие факторы, как аллергологический анамнез, спектр выделенных штаммов патогенных микроорганизмов и их чувствительность к антибиотикам, фармакокинетические и фармакодинамические особенности конкретных препаратов, их сочетаемость и синергизм с препаратами, в том числе антибактериальными, получаемыми больным в виде базисной терапии. Перед выполнением ЛП врач должен понимать степень выраженности у больного отека головного мозга, о котором можно судить по данным нейровизуализации и офтальмоскопии. При выраженном отеке введение препаратов в концевую цистерну малоэффективно, а выведение ЦСЖ может привести к повреждению головного мозга в результате его вклинения в большое затылочное отверстие. Другим показанием для эндолюмбального применения лекарственных средств является грибковый менингит (криптококковый, кандидозный, гистоплазмоидный, кокцидиоидомикозный), в этом случае вводится амфотерицин В (читывая его относительно высокое нефротоксическое действие, встречающееся у 80% больных, целесообразно применение липосомального варианта - амбизом, обладающего меньшей токсичностью). При туберкулезном поражении ЦНС возможно интратекальное введение изониазида) При наличии у пациента таких нейроонкологических заболеваний, как менингеальный карциноматоз, нейролейкоз, лепто-менингеальная лимфома и некоторые злокачественные опухоли ЦНС, в том числе метастазы рака, интратекально вводятся цитостатики. В ряде исследований была показана эффективность и безопасность интратекального введения церебролизина в остром периоде инфаркта мозга. Установлено достоверно более быстрое и значительное развитие регресса неврологического дефицита у больных, получавших такой вид лечения, по сравнению с пациентами, перенесшими ишемический инсульт, которым данный препарат в подоболочечное пространство не вводился. Имеется опыт введения в ликворное пространство озоно-кислородной смеси и биологического регулятора гипофиза эпиталамина при лечении черепно-мозговой травмы (ЧМТ). Эффективность такой методики доказана в исследованиях, основанных на данных лабораторного анализа ЦСЖ, нейроофтальмологических методов, нейрокартирования и вызванных потенциалов. В нейрохирургической практике при лечении люмбо-сакральных радикулопатий со стойким выраженным болевым синдромом применяется эпидуральное введение кортикостероидов (бетаметазона, триамциналона диацетата или метилпреднизолона ацетата). Для уменьшения спастичности, сопровождающей некоторые заболевания ЦСЖ, интратекально, через установленный в концевой цистерне катетер с помощью специальной помпы вводят баклофен, выпускаемый для такого применения в специальной инъекционной форме по 1 и 5 мл под торговым названием лиорезал интратекальный. читайте также статью «Оценка эффективности длительной интратекальной терапии резистентных болевых синдро-мов» Зеелигер А., Мельник Н.Ю., Центр патологии позвоночника и противоболевой терапии, клиника «ЛИНКС ФОМ РЕЙН», Кельн (Український нейрохірургічний журнал, №2, 2008) [читать] После прокола твердой мозговой оболочки необходимо оценить проходимость субдурального пространства путем проведения ликвородинамических проб. Это особенно важно в случае наличия у пациента опухолевого или метастатического поражения спинного мозга или его оболочек. При наличии блока ликворопроводящих путей вводимый препарат не поступит интракраниально, а его миелотоксическое действие может повыситься из-за невозможности распределения в ЦСЖ. Методика введения лекарственных средств в субарахноидальное пространство состоит в следующем: разовую дозу вводимого препарата разводят в 2 - 3 мл изотонического (0,9%) раствора натрия хлорида. После выполнения ЛП на уровне L3 - S1 (игла прокалывает кожу, гиподерму, межостистые и желтые связки отростков позвонков и твердую оболочку мозга) канюлю шприца вставляют в павильон пункционной иглы, набирают в шприц до 5 - 6 мл ЦСЖ и медленно вводят 2 - 3 мл содержимого шприца. Затем вновь наполняют шприц ЦСЖ до 5 мл и медленно вводят все содержимое шприца. После манипуляции пункционную иглу извлекают. Если состояние больного позволяет, то ему показано нахождение в постели с приподнятым ножным концом в течение 30 мин. Необходимо помнить, что попадание в субарахноидальное пространство инородных субстанций (воздух, контрастные вещества, анестетики, химиотерапевтические препараты, антибактериальные средства) может вызвать средней степени или выраженную менингеальную реакцию. Она проявляется плеоцитозом до 1000 клеток в 1 мкл, повышением содержания белка при нормальном содержании глюкозы и стерильном посеве ЦСЖ. В большинстве случаев это состояние быстро регрессирует, но иногда может привести к арахноидиту, радикулиту или миелиту. Частота таких осложнений неизвестна. подробнее в статье «Интратекальное введение лекарственных препаратов» И.А. Лебедев, Е.В. Левитина, А.К. Акимжанова, О.А. Рахманина, Т.Э. Шторк; ГБОУ ВПО «Тюменский государственный медицинский университет», Тюмень, Россия; Государственный медицинский университет, Семей, Казахстан (Журнал неврологии и психиатрии, №10, 2016) [читать]laesus-de-liro.livejournal.com Эндолюмбальное введение препарата «Меркацин» в комплексном лечении гнойного менингита.Эндолюмбальное введение препарата «Меркацин» в комплексном лечении гнойного менингита. Эндолюмбальное введение препарата «Меркацин» в комплексном лечении гнойного менингита. Старцев О.Ю. заведующий неврологическим отделением Бендерской городской больницыМищенко А.В. врач реаниматолог Бендерской городской больницы Несмотря на достигнутый прогресс в понимании этиологии и патогенеза, применение современных антибактериальных препаратов, лечение гнойных менингитов остаётся сложной задачей. Основными факторами, осложняющими лечение гнойных менингитов, являются развитие заболевания у пожилых, ослабленных больных, у пациентов с иммунодефицитом, наличие среди возбудителей менингита устойчивых к обычно используемым антибиотикам штаммов. Обязательным условием успешного лечения гнойного менингита является немедленное, после установления диагноза, начало адекватной антибиотикотерапии и создание терапевтической концентрации антибиотика в очаге воспаления. В отделение реанимации БЦГБ поступила больная Б. 57 лет, в крайне тяжёлом состоянии. Сознание угнетено, оценка по шкале Glasgow 8 баллов. Отмечались умеренно выраженные менингеальные симптомы, тахикардия (90-108 ударов в минуту), тахипноэ (20-22 в минуту), субфебрильная температура. Из анамнеза известно, что больная накануне в течение 5 дней – «лечила правое ухо» в домашних условиях. Сразу же при госпитализации была проведена диагностическая люмбальная пункция. Цереброспинальная жидкость желтоватого цвета, мутная, из иглы вытекает струёй, цитоз 2235 клеток в 1 мкл., 78% - нейтрофилов, 22% - лимфоцитов, белок – 3,5 г/л, глюкоза – 4,3 ммоль/л, реакция Нонне-Апельта ++. Тяжесть состояния усугублялась развитием декомпенсации сахарного диабета, кетоацидозом (сахар крови 15 ммоль/л, ацетон в моче +++). Был выставлен диагноз: вторичный гнойный менингит неуточнённой этиологии. Для эмпирической антибактериальной терапии нами была выбрана комбинация препаратов Меркацин (аминогликозид III поколения – амикацин, компании World Medicine) и Цефтазидим (цефалоспорин III поколения). Учитывая, что уровень концентрации цефтазидима и амикацина в ликворе составляет 20-40 и 30% соответственно было решено внутривенное введение антибиотиков в максимальных суточных дозах дополнить эндолюмбальным введением МЕРКАЦИНА, которое проводилось в течение трёх дней, начиная со второго дня лечение. Доза меркацина составляла 125 мг препарата растворённого в 5 мл физиологического раствора для эндолюмбального введения, предварительно извлекалось 5 мл цереброспинальной жидкости. Параллельно проводилась дезинтоксикационная, противоотёчная, противовоспалительная терапия и инсулинотерапия. Таким образом, за четыре дня комбинированного (внутривенного и эндолюмбального) введения Меркацина и Цефтазидима произошла санация цереброспинальной жидкости. Выводы: Эндолюмбальное введение препарата Меркацин в дозировке 125 мг эффективно в схеме эмпирической антибактериальной терапии у тяжёлых реанимационных больных с вторичным гнойным менингитом неуточнённой этиологии. Таблица 1. Динамика анализа Цереброспинальной жидкости.
Опубликовано в Вестнике Министерства здравоохранения и социальной защиты ПМР №1 2009г. worldmedicine.md 6.3.6. Профилактика и лечение внутричерепных нагноений.Посттравматические и послеоперационные менингиты - частое осложнение черепно-мозговой травмы и экстренных нейрохирургических вмешательств (до 30% по данным разных авторов). Обычным способом лечения является парентеральное применение антимикробных средств, в том числе и путем внутриартериального введения. Неудовлетворительные результаты этих методов лечения, несмотря на энтузиазм отдельных авторов, объясняются рядом причин. В результате отсутствия точной информации о проницаемости ГЭБ для антибактериальных препаратов нельзя судить достоверно о том, достаточна ли концентрация антибиотиков в ликворе и ткани мозга при их внутривенном введении для подавления роста микроорганизмов. Возможность достижения более высоких концентраций антимикробных средств при внутриартериальном пути введения также не доказана, так как для преодоления препаратом ГЭБ принципиально важной является длительность экспозиции лекарства. Сомнительно, что 5-10 сек, в течение которых препарат проходит через мозг при введении в сонную артерию, достаточно для проникновения антибиотика в церебральную ткань. Десятилетие назад при лечении посттравматического менингита стандартная схема антибактериального лечения предусматривала применение бензилпенициллина. Мы тоже ранее применяли при посттравматическом менингите внутривенные инъекции бензилпенициллина в больших дозах (до 36-40 млн ЕД) в расчете на достижение достаточной концентрации антибиотика в спинномозговой жидкости. Однако в настоящее время, в связи с практически полной резистентностью микрофлоры к пенициллину, мы считаем использование этой схемы лечения нецелесообразным. Есть еще один существенный фактор. Для достижения эффекта антибиотика важно проникновение его не просто в мозг, а в гнойный очаг. Последний представляет собой скопление гнойного ликвора, которое не всегда хорошо дренируется в другие отделы ликворных пространств. Указанные соображения послужили причиной разработки принципиально новой концепции лечения гнойных менингитов. Два основополагающих положения этой концепции:•интратекальное введение химиотерапевтических средств,•дренирование и выведение гнойного ликвора (ликвораферез). Обязательным условием дренирования ликворных пространств и интратекального введения антибиотиков является отсутствие аксиальной дислокации головного мозга, определяемой по неврологическим признакам и данным КТ. Необходимо подчеркнуть важность контроля неврологического статуса, так как появление дислокационной симптоматики служит показанием для прекращения выведения ликвора и требует эндолюмбального введения больших доз физиологического раствора для профилактики вклинения мозга. При начальных признаках менингита достаточно введения антимикробного препарата эндолюмбально один-два раза в сутки путем люмбальной пункции. При нарастающих проявлениях внутричерепного нагноения мы прибегаем к дренированию люмбального канала. Люмбальный дренаж устанавливают под местной анестезией в типичном для люмбальной пункции месте – между II и III поясничными позвонками. Лучше использовать не прямую иглу, а изогнутую на дистальном конце, называемую иглой Туохи (рис. 6.26). Срез иглы направляют к голове больного и по методике Сельдингера вводят катетер. Необходимоприменять только катетеры большого диаметра (внутренний диаметр не менее 1,4 мм), чтобы предупредить их обструкцию гнойным ликвором. Мы также рекомендуем использовать жесткие полиэтиленовые катетеры, которые не деформируются при их проведении через плотную желтую связку. После катетеризации люмбального канала к катетеру присоединяют удлинительную трубку (обычно от стерильной системы для инфузионной терапии) и размещают вдоль спины в краниальном направлении. Возле головы больного располагают стерильную закрытую емкость для сбора ликвора (рис. 6.27). Антибиотики вводят эпизодически через резиновую вставку рядом с катетером. Дренаж пережимают, выводят от 3 до 10 мл ликвора с последующим замещением выведенного объема физиологическим раствором, имеющим температуру тела больного и содержащего антибактериальный препарат. Через 30 минут дренаж открывают и устанавливают на пассивный отток. При отсутствии побочных реакций, возникновении судорог и резких вегетативных проявлений (тахипноэ, тахикардии, артериальной гипертензии), эту манипуляцию повторяют 4-6 раз в сутки. Признаками эффективности люмбального дренирования является снижение воспалительного цитоза ликвора и других проявлений менингита. При неэффективности лечения производят смену антибактериального препарата или рассматривают вопрос о дренировании других ликворных пространств. Подозрение на вентрикулит служит показанием к наружному дренированию желудочков. Интратекально применяются антибиотики, исходя из характера и чувствительности микрофлоры. При возникновении менингита экстренность ситуации не позволяет ждать результатов посева ликвора, поэтому при интратекальном назначении антимикробных препаратов мы предлагаем учитывать данные мониторинга флоры конкретного отделения реанимации. Смену антибиотиков производят только при их неэффективности в течение 3-4 дней. Данные литературы позволяют ориентироваться только на использование устаревших антибактериальных препаратов, к которым утеряна чувствительность микрофлоры. В связи с этим по жизненным показаниям мы используем современные антибиотики. Расчет дозы препарата производят следующим образом. Объем ликвора составляет 150 мл, что в 30 раз меньше объема циркулирующей крови. Исходя из этого, максимальную суточную дозу препарата уменьшают в 30 раз, а начальную дозу препарата снижают в 100 раз. Так как этиологическими агентами, вызывающими менингит, являются нозокомиальные микроорганизмы, то для интратекального введения выбирают такие антибактериальные препараты, которые «перекрывают» как Грамположительные (стафилококк и энтерококк), так и Грамотрицательные бактерии (синегнойную и кишечную палочки, клебсиеллу, акинетобактер). Применяемые в нашей практике интратекально разовые дозы антимикробных препаратов, показавшие свою высокую эффективность: амикацин 50-100 мг, таривид (офлоксацин) 10-20 мг, максипим 50-100 мг, фортум 50-100 мг, меронем 10-20 мг. При торпидном течении менингита и недостаточной эффективности антибиотиков дозы препаратов по витальным показаниям повышают в 1,5-2 раза или комбинируют с введением ванкомицина (2,5-5 мг) или диоксидина (5-10 мг). Алгоритм лечения посттравматического менингита представлен в таблице 12.
Побочные явления при эндолюмбальном введении антимикробных средств отмечены нами у четырех больных, что составляет менее 0,15%. В пяти случаях у этих больных при введении в спинномозговой канал антибиотиков мы наблюдали судорожный приступ. Следует отметить, что подобное осложнение может отмечаться и при широко используемом эндолюмбальном введении натриевой соли бензилпенициллина. Редкость таких осложнений не позволяет разработать необходимые меры профилактики. Однако у нас сложилось впечатление, что побочные эффекты при эндолюмбальном введении антибиотиков не наблюдаются при выраженном менингите. Судорожные проявления мы наблюдали у пациентов, выздоравливающих от менингита, с нормализующимся анализом ликвора. В двух случаях отмечено появление нижней параплегии на фоне эндолюмбального введения диоксидина. В обоих случаях менингит был излечен, у одного пациента движения восстановились через месяц, у другого параплегия сохранялась через 3 месяца наблюдения. Мы не смогли связать это осложнение только с побочным эффектом диоксидина, так как возможной причиной мог быть слипчивый процесс в оболочках спинного мозга. В любом случае необходим контроль над состоянием двигательных функций нижних конечностей при эндолюмбальном применении антибиотиков и антисептиков. В нашей практике люмбальные дренажи удаляют при цитозе ликвора менее 100 лейкоцитов в 1 мл. Введение антибиотиков прекращают при цитозе менее 50 лейкоцитов в 1 мл. Использование интратекального введения антибиотиков в сочетании с дренированием ликворных пространств позволило за 5 лет снизить летальность в отделении нейрохирургической реанимации НИИ скорой помощи им. Н.В. Склифосовского от посттравматического и послеоперационного менингита с 90 до 10%. Появился даже морфологический термин – «леченый менингит». Смысл этого термина в том, что пациент, перенесший менингит, может в последующем погибнуть от иных причин. При патологоанатомическом исследовании макроскопических признаков менингита не выявляется, и только микроскопически можно обнаружить помутнение мозговых оболочек, свидетельствующее о перенесенном их воспалении. Мы отдаем себе отчет, что полученные данные нуждаются в проверке в рамках проспективного рандомизированного исследования. Однако высокая эффективность терапии ставит под сомнение этичность проведения данного исследования, в котором группой сравнения должны быть пациенты без интратекального введения препаратов и поэтому заведомо обреченные на летальный исход. К сожалению, эндолюмбальное введение препаратов не позволяет достичь эффекта при нарушении сообщения гнойного очага с ликворной системой. Такая ситуация наблюдается при долго сохраняющемся вентрикулите, локальном менингоэнцефалите. Летальность при данных состояниях очень высокая (70-80%). Исход болезни фактически зависит от того, удастся ли хирургическим путем достичь дренирования очага и создать возможность подведения антибиотиков и антисептиков к месту воспаления. www.reancenter.ru 4. Меры предосторожности при интратекальном введении антибиотикова. Перед введением каждой дозы измеряют концентрацию антибиотика в СМЖ, чтобы избежать его избыточного накопления. б. После каждой пункции исследуют СМЖ, чтобы своевременно выявить блокаду ликворопроводящих путей (выраженное увеличение концентрации белка), ятрогенное инфицирование (цитоз) или химический менингит (увеличение числа лейкоцитов, преимущественно нейтрофилов, и концентрации белка). в. При блокаде ликворопроводящих путей, иногда возникающей при менингите, антибиотики могут не поступать в очаги инфекции. Проходимость ликворопроводящих путей определяют с помощью введения в желудочек радиоактивного коллоида. У больных с несообщающейся гидроцефалией может потребоваться комбинированное эндолюмбальное и внутрижелудочковое (через дренажный катетер) введение антибиотиков. 5. Показания.Интратекальная терапия обычно применяется, если при в/в введении антибиотиков не достигается бактерицидная концентрация в СМЖ. Показания к интратекальному введению четко не определены; ясно, однако, что к нему следует прибегать только в редких случаях. а. Менингиты, вызываемые грамотрицательными бактериями 1) Если возбудитель чувствителен кампициллинуили цефалоспоринам третьего поколения, то бактерицидной концентрации этих препаратов в СМЖ можно достичь с помощью в/в введения. Опыт показывает, что данные антибиотики можно применять в качестве монотерапии против большинства чувствительных возбудителей. Однако Pseudomonas spp., Serratia spp., Acinetobacter spp. и некоторые виды Proteus spp. обычно устойчивы к этим антибиотикам. Поэтому при подозрении на одну из этих инфекций целесообразно в качестве эмпирической терапии использовать комбинированное в/в и интратекальное введение аминогликозидов. 2) Если микроорганизм устойчив кампициллинуи цефалоспоринам или лечение неэффективно, то рекомендуется комбинирование в/в и интратекального введения аминогликозидов в сочетании с одним из пенициллинов широкого спектра действия. 3) Показания к введению аминогликозидов через резервуар Оммайя не определены. Если нет уверенности в преимуществе внутрижелудочкового введения, лечение лучше начинать с эндолюмбального введения, а к внутрижелудочковому прибегать только в следующих случаях: а) При высокой устойчивости возбудителя (определяется по МБК антибиотика). б) При неэффективности эндолюмбального введения. в) При блокаде ликворопроводящих путей, препятствующей распространению эндолюмбально вводимых препаратов в субарахноидальные цистерны основания мозга. б. Стафилококковый менингит. Для лечения менингита, вызванного пенициллиназапродуцирующими штаммами Staphylococcus aureus, в субарахноидальное пространство вводятбацитрацинв дозе 5000—10 000 МЕ. Однако такая терапия показана только по жизненным показаниям в отсутствие эффекта от в/в введения высоких дозоксациллинаилинафциллина. Методика введения та же, что и для аминогликозидов. в. Энтерококковый менингит(возбудитель — Streptococcus faecalis) встречается редко, в основном у новорожденных, после хирургических вмешательств или при инфекционном эндокардите. Несмотря на чувствительность возбудителя кампициллинуin vitro, необходимо комбинированное лечение пенициллинами и аминогликозидами в дозах, используемых при тяжелых инфекциях. Назначаютбензилпенициллинигентамицинв/в, а при неэффективности — дополнительногентамицининтратекально. Д. Кортикостероидная терапия 1. Дети. Дексаметазон(0,15 мг/кг в/в каждые 6 ч в течение первых 4 сут антибиотикотерапии) снижает риск нарушения слуха и других неврологических осложнений у детей с бактериальным менингитом. Поэтому многие рекомендуют применять кортикостероиды во всех случаях бактериального менингита у детей с нормальным иммунитетом. Кортикостероиды тем эффективнее, чем раньше они назначены. 2. Взрослые.Некоторые рекомендуют всегда назначать кортикостероиды в противовоспалительных дозах (40—80 мг/сутпреднизонаили другой препарат в эквивалентной дозе) при бактериальном менингите у взрослых с нормальным иммунитетом. Однако контролируемые испытания такого лечения не проводились. 3. Высокие дозы кортикостероидов применяют при отеке мозга, вызванном тяжелым менингитом (см.гл. 8, п. I.З.1). 4. Поддерживающие дозы кортикостероидов назначают при подозрении на кровоизлияние в надпочечники (см.гл. 8, п. I.Б.1.а.2). Е. Профилактическое лечение лиц, находившихся в контакте с больными 1. Показания. Менингококковая инфекция распространяется воздушно-капельным путем. Больные заразны в течение первых суток лечения антибиотиками. Вероятность менингококковых заболеваний у членов семьи больного — примерно 3:1000, остальные становятся носителями и могут заражать других чувствительных к возбудителю лиц. В связи с этим профилактическая антибиотикотерапия рекомендуется: а. Членам семьи. б. Детям и персоналу дошкольных учреждений в. Медицинским работникам, проводившим СЛР. studfiles.net Лечение отогенных внутричерепных осложнений и отогенного сепсисаОсновным патогенетическим принципом лечения внутричерепных отогенных осложнений является элиминация гнойного очага в ухе. Целью лечения отогенных внутричерепных осложнений являются улучшение общего состояния больного, исчезновение имеющейся неврологической симптоматики. Для достижения данных целей независимо от тяжести состояния пациента необходимо дренирование инфекционного очага и проведение адекватной интенсивной антибактериальной терапии. Показания к госпитализацииПоказаниями для госпитализации являются наличие в анамнезе острых или хронических заболевании ушей, появление на фоне острого или обострении хронического гнойного среднего отита, судорог, психических расстройств, жалоб на головную боль, тошноту, рвоту, повышение температуры, выявление менингеальных симптомов. Больные с подозрением на внутричерепные осложнения нуждаются в срочной госпитализации в специализированное лечебное учреждение, а при подтверждении диагноза подлежат неотложному хирургическому лечению. Немедикаментоэное лечениеВ последние годы при лечении отогенных внутричерепных осложнений применяются следующие виды немедикаментозного лечения:
Медикаментезное лечение отогенных внутричерепных осложнений и отогенного сепсисаОдним из важных аспектов послеоперационного лечения больных с отогенными внутричерепными осложнениями является комплексная интенсивная медикаментозная терапия. Медикаментозное лечение отогенных внутричерепных осложнений включает, прежде всего, применение антибиотиков. Антибактериальная терапия должна начинаться с больших доз антибиотиков и проводится с использованием всех основных путей введения лекарственных средств (внутривенно - с целью создания максимальной концентрации антибиотика в крови; внутримышечно - для обеспечения поддерживающего антибактериального эффекта). Наиболее эффективно региональное введение антибиотиков в ликворные пути или артериальную систему головного мозга. Пациентам с гнойно-воспалительными поражениями головного мозга обычно оказывается ургентная помощь, и до начала антибактериальной терапии невозможно определить конкретных возбудителей инфекции. Поэтому выбор эмпирической антибактериальной терапии должен основываться на знании наиболее вероятных возбудителей и данных об антибиотикорезистентности в регионе При назначении антибактериальной терапии пациенту с внутричерепным осложнением отогенной природы необходимо учитывать как активность данного лекарственного средства в отношении предполагаемых возбудителей (особенно устойчивости к действию бета-лактамаз), так и его способность проникать через гематоэнцефалический барьер. Бактериальный посев и пробу на чувствительность к антибиотикам необходимо провести как можно скорее. Однако до получения результатов бактериологического исследования должна быть назначена эмпирическая терапия, включающая введение двух-трех антибиотиков одновременно. Высокоэффективная схема лечения, включающая два антибиотика, одним из которых может быть полусинтетический пенициллин или цефалоспорин II поколения, вторым - антибиотик аминогликозидной группы. Антибиотики вводятся в максимальных терапевтических концентрациях. После получения результатов бактериологического исследования спинномозговой жидкости и идентификации возбудителя может быть назначена целенаправленная терапия. При использовании в качестве основного антибиотика бензилпенициллина применяется его натриевая соль в дозе 30-50 млн ЕД/сут с равномерным распределением на 6-8 приёмом. Следует отметить, что пенициллин до настоящего времени не утратил своего терапевтического значения при многих инфекциях. Приходится учитывать и тот факт, что это один из наиболее дешёвых антибиотиков. В зависимости от эффекта эта терапия продолжается в течение 3-5 сут с последующим переходом на поддерживающие дозы - 12-18 млн ЕД/сут. Среди полусинтетических пенициллинов широкого спектра действия, устойчивых к бета-лактамазам. Наиболее известны комбинации амоксициллин + клавулановая кислота и ампициллин + сульбактам, которые также обладают антианаэробной активностью. Если среди возбудителей идентифицированы или предполагаются анаэробы, в комбинации с антистафилококковым пенициллином (оксациллин) применяют метронидазол внутривенно. Такое сочетание широко используется, и неоднократно подтвердило свою высокую эффективность при оказании ургентной помощи самым тяжёлым больным с гнойно-септическими осложнениями головного мозга. Вполне удовлетворительный клинический эффект, подтверждённый бактериологическими исследованиями, достигается также у больных с тяжёлыми внутричерепными осложнениями при использовании цефалоспоринов III-IV поколения. В настоящее время широко применяются такие препараты, как цефтриаксон, цефотаксим, цефтазидим. относящиеся к III поколению цефалоспоринов. В частности, цефтазидим, применяемый парентерально по 1-2 г через каждые 8-12 ч, является препаратом выбора при синегнойной инфекции. Цефалоспорин IV поколения цефепим, характеризующийся широким спектром действия, может быть использован для лечения пациентов с нейтропенией и ослабленным иммунитетом. Цефалоспорины редко комбинируют с другими антибиотиками, однако возможны сочетания с аминогликозидами, метронидазолом. Гликопептиды представляют практически единственную группу антибиотиков, сохраняющих высокую активность в отношении резистентных к другим антибиотикам стафилококков и энтерококков. Ванкомицин также показан при неэффективности или непереносимости пенициллинов или цефалоспоринов. Следует отметить, что ванкомицин должен быть отнесён в группу резерва и использоваться лишь в ситуациях, когда другие антибиотики оказываются неэффективными. Наряду с различными видами микроорганизмов в последнее время причиной тяжёлых гнойно-воспалительных поражений уха и внутричерепных отогенных осложнений в ряде случаев являются разнообразные грибы (чаще наблюдается аспергиллёз, кандидоз, пенициллиноз и др.). Среди противогрибковых препаратов наиболее целесообразно использование триазолов (кетоконазол, флуконазол, итраконазол). В отдельных случаях возможно применение амфотерицима В. Интракаротидное введение антибиотиков осуществляется путём пункции общей сонной артерии либо посредством введённого в общую сонную артерию стандартного сосудистого катетера. Наиболее удобным и безопасным является проведение катетера в сонную артерию через поверхностную височную артерию. Доза антибиотика, вводимого в сонную артерию, составляет 0,5-1,0 г, препарат назначается два раза в сутки. При катетеризации общей сонной артерии осуществляется непрерывное введение антибиотика с помощью аппарата для введения лекарственных веществ, суточная доза препарата может достигать 2 г. суточное количество инфузионного раствора составляет 1-1,5 л/сут. Основой инфузатов является раствор Рингера-Локка или 0,9% раствор натрия хлорида с добавлением в него гепарина, ингибиторов белкового распада, спазмолитиков. Эндолюмбальное введение антибиотиков проводят 1-2 раза в сутки. Препаратами выбора для этих целей являются цефалоспорины, аминогликозиды в дозе 50-100 мг. Выведение 10-15 мл спинномозговой жидкости при проведении люмбальных пункций также является важным элементом санации ликворных путей. Ускорение санации спинномозговой жидкости достигается проведением ликворосорбции. Для большинства случаев менингитов, обусловленных грамотрицательными бактериями, требуется 10-14 дневное лечение после того, как посевы спинномозговой жидкости становятся стерильными. Для стафилококкового менингита длительность терапии составляет обычно 14-21 день. Особенности антибиотикотерапии при лечении абсцессов головного мозгаВыбор антибиотиков для лечения бактериального абсцесса зависит от большого количества факторов, наиболее важным из которых является вид возбудителя. В связи с этим ещё до назначения антибактериальных средств необходимо сделать посев содержимого абсцесса. Другими факторами являются способность антибиотиков проникать в полость абсцесса, его бактерицидные или бактериостатические свойства и спектр действия. До выделения возбудителя антибиотики назначаются против наиболее вероятных инфекционных агентов. Если источником является хронический гнойный средний отит, то должна предполагаться смешанная аэробная и анаэробная инфекция, а в схему лечения необходимо включать антибиотики широкого спектра действия. В данном случае возможно назначение метронидазола (будет перекрывать анаэробные микроорганизмы), который превосходно проникает в полость абсцесса, и бензилпенициллина для действия на грамположительные бактерии (хотя половина выделяемых в настоящее время возбудителей резистентны к нему). В связи с этим рекомендуются устойчивые к бета-лактамазам полусинтетические пенициллины или ванкомицин. У ослабленных и предварительно леченных больных необходимо назначение антибактериальных средств, воздействующих на грамотрицательные бактерии. Длительное использование антибиотиков в стадии ограниченного энцефалита позволяет достигнуть успехов в лечении заболевания. Хорошие результаты лечения достигнуты у больных с небольшими абсцессами (средний диаметр 2,1 см), особенно когда известен источник инфекции. При множественных абсцессах антибиотики могут использоваться в качестве единственного вида лечения для образований менее 2,5 см в диаметре при условии получения культуры возбудителя хотя бы из одного абсцесса. Для промывания полости абсцесса используется 0,9% раствор хлористого натрия с включением в него антибиотиков широкого спектра действия, не обладающих эпилептогенной активностью, из расчёта 0,5 г на 500 мл раствора; протеолитических ферментов: ингибиторов белкового распада. Лечение множественных абсцессовНеотложное хирургическое вмешательство необходимо проводить при множественных абсцессах, превышающих 2,5 см в диаметре или вызывающих заметный масс-эффект. Если все абсцессы менее 2,5 см в диаметре и не вызывают масс-эффект, осуществляют аспирацию содержимого наибольшего абсцесса для микробиологического исследования. От применения антибиотиков необходимо воздержатся до тех пор, пока не будет получен материал для культивирования. До получения результатов посева используют антибиотики широкого спектра действия, а затем применяют антибактериальные препараты в соответствии с результатами идентификации возбудителя в течение минимум 6-8 нед, а у ослабленных пациентов в течение более чем 1 года. Таким образом, в настоящее время имеется значительное количество разнообразных антибактериальных препаратов, раздельное или комбинированное применение которых позволяет перекрыть весь спектр возможных возбудителей при тяжёлых инфекционных поражениях ЛОР-органов. Назначая терапию, врач обязан учитывать тяжесть заболевания, особенности предполагаемого возбудителя, возможность существования и развития в процессе лечения резистентности к используемому препарату Проведение этиотропной антибактериальной терапии необходимо сочетать с активным патогенетическим и симптоматическим лечением. При отогенных хирургических осложнениях проводят дегидратационную и дезинтоксикационную терапию. Внутривенно вводят следующие препараты: маннитол 30-60 г в 300 мл 0,9% раствора натрия хлорида 1 раз в сутки, фуросемид 2-4 мл в сутки: магния сульфат 10 мл; декстроза 20 мл и натрия хлорид 15-30 мл; метенамин 3-5 мл; гидроксиметилхиноксилиндиоксид - 300 мг; гемодез - 250-400 мл; аскорбиновая кислота - 5-10 мл; глюкокортикоиды (преднизолон, гидрокортизон). Кроме того, подкожно и внутримышечно вводят антигистаминные препараты и витамины группы В, внутривенно - пентоксифиллин 200-300 мг. В качестве симптоматической терапии по показаниям назначают сердечные гликозиды, аналептики и анальгетики. При психомоторном возбуждении внутривенно вводят диазепам 2-4 мл. При тромбозе сигмовидного синуса и отогенном сепсисе назначают антикоагулянты, в основном гепарин натрия (от 10000 до 40 000-80 000 ЕД в сутки). Лечение антикоагулянтами проводят под контролем времени свёртывания крови или уровня протромбина крови. Антикоагулянтная терапия способствует вымыванию из микроциркуляторных депо микроорганизмов и обеспечивает проникновение антибиотиков в самые отдалённые участки сосудистого русла. Также применяют протеолитические ферменты (внутримышечно). Поскольку у данных больных иммунная система испытывает значительные нагрузки и функционирует в условиях, близких к критическим, особое внимание следует уделять иммунной терапии как пассивной, так и активной (антистафилококковая плазма, антистафилококковый иммуноглобулин, иммунокорректоры органического, неорганического и растительного происхождения и др.). При интенсивной терапии больных с отогенными внутричерепными осложнениями необходимо учитывать биохимические показатели гомеостаза и корригировать их. Хирургическое лечениеХирургическое лечение - ведущий метод лечения отогенных внутричерепных осложнений. Целью хирургического вмешательства является устранение первичного гнойно-воспалительного очага среднего или внутреннего уха. Данный результат может быть достигнут путём широкого обнажения твёрдой мозговой оболочки и при необходимости пунктирования мозга или мозжечка, вскрытия или дренирования абсцесса. Операции при отогенных внутричерепных осложнениях изложены в отдельной главе. Дальнейшее ведениеДальнейшее ведение больных, перенёсших отогенные внутричерепные осложнения, заключается в динамическом наблюдении оториноларинголога и невролога. В связи с высокой частотой эпилептического синдрома в остром периоде заболевания и после оперативного лечения всем больным с субдуральными эмпиемами в течение года после операции назначают противосудорожные препараты. ПрогнозОдин из наиболее важных факторов, определяющих исход, - предоперационный неврологический статус. Смертность колеблется от 0 до 21% у больных, находящихся в ясном сознании, до 60% у больных с признаками дислокации и до 89% у больных в коме. Каждый врач в процессе лечения больного острым или хроническим гнойным средним отитом должен помнить а возможности возникновения внутричерепных осложнений и при подозрении на них незамедлительно направить больного в отоларингологический стационар. Благоприятный исход отогенных внутричерепных осложнений зависит от своевременной диагностики, хирургического вмешательства на пораженном ухе, срочной элиминации интракраниального очага, применения комплекса чувствительных данной флоре антибиотиков, а также других лекарственных средств в соответствующих дозах и от правильного ведении больного н послеоперационном периоде. При синусогенном сепсисе прогноз в подавляющем большинстве случаев благоприятен. Летальность составляет 2-4%. При выраженном снижении резистентности и изменении реактивности организма могут наблюдаться молниеносные формы сепсиса. Прогноз при них неблагоприятный. ilive.com.ua / педиатры / педиатры / статьи меркацин / Эндолюмбальное введение препарата «Меркацин» в комплексном лечении гнойного менингитаМеркацин Эндолюмбальное введение препарата «Меркацин» в комплексном лечении гнойного менингита. Старцев О.Ю. заведующий неврологическим отделением Бендерской городской больницы Мищенко А.В. врач реаниматолог Бендерской городской больницы Несмотря на достигнутый прогресс в понимании этиологии и патогенеза, применение современных антибактериальных препаратов, лечение гнойных менингитов остаётся сложной задачей. Основными факторами, осложняющими лечение гнойных менингитов, являются развитие заболевания у пожилых, ослабленных больных, у пациентов с иммунодефицитом, наличие среди возбудителей менингита устойчивых к обычно используемым антибиотикам штаммов. Обязательным условием успешного лечения гнойного менингита является немедленное, после установления диагноза, начало адекватной антибиотикотерапии и создание терапевтической концентрации антибиотика в очаге воспаления. В отделение реанимации БЦГБ поступила больная Б. 57 лет, в крайне тяжёлом состоянии. Сознание угнетено, оценка по шкале Glasgow 8 баллов. Отмечались умеренно выраженные менингеальные симптомы, тахикардия (90-108 ударов в минуту), тахипноэ (20-22 в минуту), субфебрильная температура. Из анамнеза известно, что больная накануне в течение 5 дней – «лечила правое ухо» в домашних условиях. Сразу же при госпитализации была проведена диагностическая люмбальная пункция. Цереброспинальная жидкость желтоватого цвета, мутная, из иглы вытекает струёй, цитоз 2235 клеток в 1 мкл., 78% - нейтрофилов, 22% - лимфоцитов, белок – 3,5 г/л, глюкоза – 4,3 ммоль/л, реакция Нонне-Апельта ++. Тяжесть состояния усугублялась развитием декомпенсации сахарного диабета, кетоацидозом (сахар крови 15 ммоль/л, ацетон в моче +++). Был выставлен диагноз: вторичный гнойный менингит неуточнённой этиологии. Для эмпирической антибактериальной терапии нами была выбрана комбинация препаратов Меркацин (аминогликозид III поколения – амикацин, компании World Medicine) и Цефтазидим (цефалоспорин III поколения). Учитывая, что уровень концентрации цефтазидима и амикацина в ликворе составляет 20-40 и 30% соответственно было решено внутривенное введение антибиотиков в максимальных суточных дозах дополнить эндолюмбальным введением МЕРКАЦИНА, которое проводилось в течение трёх дней, начиная со второго дня лечение. Доза меркацина составляла 125 мг препарата растворённого в 5 мл физиологического раствора для эндолюмбального введения, предварительно извлекалось 5 мл цереброспинальной жидкости. Параллельно проводилась дезинтоксикационная, противоотёчная, противовоспалительная терапия и инсулинотерапия. Таким образом, за четыре дня комбинированного (внутривенного и эндолюмбального) введения Меркацина и Цефтазидима произошла санация цереброспинальной жидкости. Выводы: Эндолюмбальное введение препарата Меркацин в дозировке 125 мг эффективно в схеме эмпирической антибактериальной терапии у тяжёлых реанимационных больных с вторичным гнойным менингитом неуточнённой этиологии. Таблица 1. Динамика анализа Цереброспинальной жидкости.
Опубликовано в Вестнике Министерства здравоохранения и социальной защиты ПМР №1 2009г. studfiles.net |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
г.Самара, ул. Димитрова 131 [email protected] |
 |

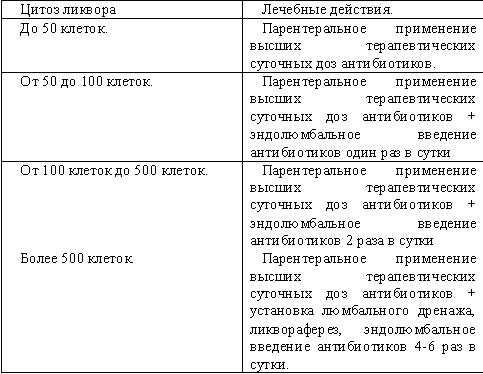 Табл.12. Алгоритм антибиотикотерапии менингита
Табл.12. Алгоритм антибиотикотерапии менингита