|
|
||||||||||
|
Классические принципы рациональной антибиотикотерапии:. Рациональная комбинация антибиотиковКомбинированное применение антибиотиков - Med24info.comВ настоящее время комбинированное применение антибиотиков является преобладающим в терапии бактериальных инфекций. Известно, что при комбинированном использовании антибиотиков могут возникнуть:
Таким образом, 1-ю группу можно комбинировать со 2-й и 3-й. Исключение: комбинация карбенициллина с аминог- ликозидами. Комбинация 2-й и 3-й групп является нежелательной. Допустима комбинация 2-х антибиотиков из одной группы. Нельзя комбинировать 2 аминогликозидных антибиотика, из-за увеличения риска побочных эффектов. Антагонистами являются пенициллины и цефалос- порины с тетрациклинами и хлорамфениколом. Ашта- гонистами являются макролиды и хлорамфеникол. Примеры рациональных комбинаций:
гиперчувствительности на пенициллин (анафилаксия) не должны получать цефалоспорины (альтернатива включает азтреонат, хинолоны, сульфаниламиды или ванкомицин).
диарея: все антибиотики), и при этом должен осуществляться контроль за развитием инфекции.
www.med24info.com Комбинированная антибиотикотерапия — SportWiki энциклопедияКомбинированная антимикробная терапия[править]Комбинированная антимикробная терапия применяется по строгим показаниям. При выборе комбинации препаратов необходимо учитывать возможные взаимодействия между ними, влияющие как на микро-, так и на макроорганизм. Препараты, действующие на разные мишени, могут усиливать или ослаблять антимикробную активность друг друга. Побочное действие комбинации антимикробных средств слагается из побочных эффектов отдельных препаратов, а иногда и превышает простую сумму их побочных эффектов. Например, ванкомицин сам по себе не оказывает выраженного нефротоксического действия, но, по некоторым данным, усугубляет нефротоксичность аминогликозидов (Farberand Moelle-ring, 1983). Оценка взаимодействия антимикробных средств[править]Существует два способа оценки взаимодействия антимикробных средств. В первом случае микроорганизмы высевают на жидкие питательные среды, содержащие разные сочетания последовательных двукратных разведений двух исследуемых препаратов, и инкубируют в течение 18—24 ч. Затем определяют МПК каждого антибиотика в отдельности и в присутствии другого препарата. Если МПК комбинации антибиотиков составляет не более 25% МПК каждого препарата в отдельности, антибиотики действуют синергично. Синергизм может быть обусловлен повышением чувствительности микроорганизма к одному препарату под действием другого. Если МПК комбинации антибиотиков равна половине МПК каждого из них в отдельности, это означает, что препараты действуют независимо друг от друга, а их эффект суммируется (аддитивное действие). Если МПК комбинации антибиотиков меньше, чем МПК каждого из них в отдельности, препараты действуют антагонистически (то есть ослабляют действие друг друга). При сравнении всех (а не только одинаковых) комбинаций двукратных разведений антибиотиков можно построить так называемые изоболы (рис. 43.2). Если антибиотики действуют синергично, изобола представляет собой вогнутую кривую, если аддитивно — прямую линию, если антагонистически — выпуклую кривую. Для каждой точки изоболы можно рассчитать индекс МПК — сумму концентраций, выраженных в долях МПК. Для двух антимикробных средств А и Б его рассчитывают следующим образом: Индекс МПК = МПК А в присутствии Б/МПКА+МПК Б в присутствии А/МПКБ В случае аддитивного действия индекс МПК равен единице, при синергизме он меньше 1, при антагонизме — больше. К сожалению, с помощью этого метода нельзя выявить синергичный бактерицидный эффект, так как определяются не МБК, а МПК. Другой способ оценки взаимодействия препаратов заключается в построении кривых, описывающих динамику гибели микроорганизмов. Культуру микроорганизмов инкубируют в присутствии обоих антимикробных средств и каждого из препаратов в отдельности. Для оценки числа выживших микроорганизмов ее периодически пересевают. О синергизме говорят в том случае, если число бактерий в среде, содержащей комбинацию препаратов, как минимум в 100 раз меньше, чем в среде, содержащей наиболее активный из препаратов. Если число бактерий различается менее чем в 100 раз, говорят об индифферентном действии. Если же число бактерий в присутствии комбинации антимикробных средств больше, чем в присутствии наиболее активного из них, препараты действуют антагонистично.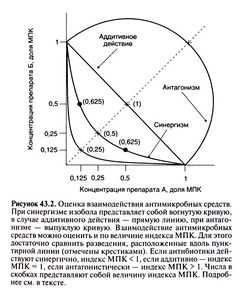 Рисунок 43.2. Оценка взаимодействия антимикробных средств. Рисунок 43.2. Оценка взаимодействия антимикробных средств. В 1952 г. Джавиц и Ганнисон предложили простой способ оценки взаимодействия антимикробных средств, основанный на их свойствах (Jawetz and Gunnison, 1952). Авторы заметили, что бактериостатические антибиотики (например, тетрациклины, эритромицин, хлорамфеникол) часто действуют антагонистично по отношению к бактерицидным препаратам (таким, как β-лактамные антибиотики, ванкомицин, аминогликозиды), поскольку первые подавляют деление бактериальных клеток и синтез белка, необходимые для реализации действия большинства бактерицидных антибиотиков. С другой стороны, два бактерицидных препарата обычно действуют синергично. Так, препараты, подавляющие синтез клеточной стенки, и аминогликозиды проявляют синергизм в отношении многих видов бактерий. Исключение составляет рифампицин. Будучи бактерицидным препаратом, он индифферентно или даже антагонистически взаимодействует с другими бактерицидными антибиотиками in vitro. Клиническое значение этого явления не установлено, поскольку in vivo комбинации с рифампицином эффективны. Показания к комбинированной антимикробной терапии[править]Назначение нескольких антимикробных средств оправдано в следующих случаях: 1) при эмпирической терапии (возбудитель не известен), 2) при лечении смешанных инфекций, 3) при необходимости усилить антимикробное действие в отношении определенного возбудителя, 4) в целях предупреждения лекарственной устойчивости. Эмпирическая терапия[править]Это самый частый повод для назначения комбинации антимикробных средств. Чтобы правильно подобрать лечение, необходимо знать особенности инфекции, ее наиболее вероятных возбудителей, а также антимикробные спектры препаратов, которые могут применяться в данной ситуации. Если состояние больного тяжелое, антимикробная терапия должна быть направлена против всех возможных возбудителей. Для этого часто приходится назначать несколько препаратов. Например, при внебольничной пневмонии используют цефуроксим в сочетании с макролидами: первый активен в отношении грамотрицательных бактерий, а вторые — в отношении возбудителей атипичных пневмоний, например Mycoplasma pneumoniae. Но такое лечение не должно быть слишком длительным. В нем нет необходимости, если возбудитель уточнен или выяснилось, что инфекция вообще отсутствует. Комбинированная терапия недешева, увеличивает риск побочных эффектов, способствует развитию суперинфекции и отбору полирезистентных штаммов. Неоправданное применение комбинации антимикробных средств бывает обусловлено тем, что врачи начинают лечение до взятия материала на посев или же, получив данные о возбудителе и его чувствительности, не меняют схему лечения. Конечно, отказаться от терапии, доказавшей свою эффективность, может быть трудно. Тем не менее нужно всегда стремиться назначать препарат с наиболее узким спектром действия и минимальными побочными эффектами. Лечение смешанных инфекций. Комбинированная антимикробная терапия показана при смешанной инфекции, возбудители которой чувствительны к разным антимикробным средствам. Например, абсцессы брюшной полости, печени и головного мозга, а также инфекции половых органов часто бывают вызваны смешанной аэробной и анаэробной микрофлорой. Усиление действия антимикробных средств[править]Совместное применение нескольких антимикробных средств может значительно усиливать их действие, хотя преимущества комбинированного лечения перед монотерапией доказаны лишь для небольшого числа инфекций. Наиболее убедительные доказательства получены для энтерококкового эндокардита (Wilson et al., 1995). In vitro пенициллины оказывают на Enterococcus faecalis и Enterococcus faecium лишь бактериостатическое действие, а в комбинации со стрептомицином или с гентамицином — бактерицидное. Причем после монотерапии пенициллинами рецидивы возникают намного чаше, чем после комбинированной терапии. In vitro пенициллины действуют синергично со стрептомицином или гентамицином и в отношении зеленящих стрептококков. В экспериментах на животных комбинация этих препаратов быстрее уничтожала возбудителей в вегетациях на клапанах по сравнению с монотерапией пенициллинами. Поданным клинических исследований, при стрептококковом эндокардите двухнедельная комбинированная терапия столь же эффективна, как и четырехнедельная монотерапия пенициллинами. Кроме того, пенициллины и аминогликозиды проявляют синергизм в отношении Staphylococcus aureus (как in vitro, так и в экспериментальных моделях in vivo). Например, у некоторых больных с инфекционным эндокардитом трехстворчатого клапана, вызванным Staphylococcus aureus, эффективна двухнедельная терапия тобрамицином или гентамицином (в низких дозах) в сочетании с нафциллином, хотя обычно таким больным назначают монотерапию нафциллином в течение 4—6 нед (Chambers etaL, 1988). Комбинация β-лактамных антибиотиков и аминогликозидов рекомендуется при инфекциях, вызванных Pseudomonas aeruginosa. In vitro β-лактамные антибиотики, активные в отношении псевдомонад, и аминогликозиды действуют синергично в отношении большинства штаммов Pseudomonas aeruginosa. В экспериментах на животных комбинированная терапия тоже оказалась эффективнее, чем монотерапия указанными препаратами. В некоторых, хотя далеко не во всех, клинических испытаниях (Hilfetal., 1989; Vidal etal., 19%; Leibovici et al., 1997) сочетание β-лакгамных антибиотиков с аминогликозидами увеличивало выживаемость при тяжелых псевдомонадных инфекциях. Комбинированную терапию рекомендуется применять и при инфекциях, вызванных другими грамотрицательными палочками. Однако ее преимущества перед монотерапией во многих случаях остаются недоказанными (Ваглеге, 1992; Rybak and McGrath, 1996). Синергизм сульфаниламидов и ингибиторов дигидрофолатредуктазы (например, триметоприма) обусловлен блокадой последовательных этапов синтеза фолиевой кислоты. Комбинированный препарат триметоприм/сульфаметоксазол активен в отношении микроорганизмов, устойчивых к сульфаниламидам. Его успешно применяют при инфекциях мочевых путей, пневмоцистной пневмонии, брюшном тифе, дизентерии и не которых инфекциях, вызванных устойчивыми к ампициллину штаммами Haemophilus influenzae. По данным исследований in vitro и экспериментов на животных, фторцитозин и амфотерицин В действуют синергично в отношении Cryptococcus neoformans. При криптококковом менингите в отсутствие ВИЧ-инфекции фторцитозин позволяет снизить дозу амфотерицина В и сократить продолжительность лечения с 10 до 6 нед; риск побочных эффектов при этом снижается, а эффективность лечения остается прежней (Bennett et al., 1979). Кроме того, при криптококковом менингите на фоне СПИДа эта комбинация позволяет быстрее добиться стерильности СМЖ, чем монотерапия амфотерицином В (van der Horst etal., 1997). Предупреждение лекарственной устойчивости[править]Комбинированная терапия препятствует отбору штаммов, устойчивых к одному из препаратов. Если частота появления мутантов, устойчивых к одному антимикробному средству, составляет, например, 10~7, а к другому — 10~6, то вероятность одновременного возникновения обеих мутаций равна произведению этих частот, то есть 10~13. Чтобы это событие произошло, число микроорганизмов должно быть на несколько порядков больше, чем обычно бывает при инфекциях. Предупреждение лекарственной устойчивости лежит в основе комбинированной терапии туберкулеза. При монотерапии микобактерии туберкулеза часто приобретают устойчивость к препарату, а одновременное назначение двух и более противотуберкулезных средств существенно повышает шансы на успех лечения. Другим примером служит лечение стафилококковых инфекций (например, эндокардита протезированных клапанов и остеомиелита) рифампицином. Добавление второго препарата позволяет избежать появления устойчивых к рифампицину штаммов стафилококков (Zim-merli et al., 1998). С той же целью комбинированную терапию назначают и при инфекции, вызванной Helicobacter pylori (Taylor et al., 1997). В отношении прочих инфекций убедительных данных о том, что комбинированная терапия предотвращает возникновение лекарственной устойчивости, нет. Недостатки комбинированной терапии[править]К ним относятся повышение риска побочных эффектов, появление полирезистентных штаммов и высокая стоимость. Кроме того, как уже было отмечено, бактериостатические и бактерицидные препараты могут действовать антагонистично. Клиническое значение антагонизма антимикробных средств остается неясным. Хотя in vitro он наблюдается довольно часто, in vivo случаи антагонизма редки. Наиболее яркий пример такого антагонизма—лечение пневмококкового менингита. В 1951 г. Леппер и Даулинг заметили, что при лечении пневмококкового менингита пенициллином летальность составила 21%, а при одновременном назначении хпортетрациклина она увеличилась до 79% (Lepper and Dowling, 1951). Позднее эти данные были подтвержаены другими исследователями, обнаружившими увеличение летальности бактериального менингита у детей с 4,3 до 10,5% при комбинированной терапии ампициллином, хлорамфениколом и стрептомицином по сравнению с монотерапией ампициллином (Mathies at al., 1967). Антагонизм возникает только в том случае, если оба препарата активны в отношении данного микроорганизма, и в большинстве случаев не играет сколько-нибудь заметной роли. Несмотря на то что комбинация бактериостатического и бактерицидного препарата обычно дает лишь бактериостатический эффект, лечение в большинстве случаев все равно будет успешным благодаря действию защитных механизмов. Если же эти механизмы не срабатывают и для излечения инфекции необходимо бактерицидное действие (например, при менингите, эндокардите, у больных с нейтропенией при инфекциях, вызванных грамотрицательными бактериями), эффективность антимикробной терапии снижается. sportwiki.to Лекция. Антибиотики - 1.docЛекция. Антибиотикискачать (83.5 kb.)Доступные файлы (1):содержание1.docРеклама MarketGid: АНТИБИОТИКИНаиболее распространенные ошибки применения:
^ - в - лактамиды - аминогликозиды - фосфомицин - ристомицин - полимиксин - фторхинолоны - Ко – тримоксазолы - рифампицин Бактериостатики: - левомицетин - тетрациклин - линкомицин - клиндамицин - макролиды - сульфаниламиды В некоторых случаях это разделение условно: в – лактамиды эффективно действуют на делящуюся клетку, т.е. в начале инфекции. Чем ниже МПК, тем чувствительнее микроорганизм. ^ (и здесь нужно разрабатывать экспресс-методы диагностики). Когда же эта манипуляция необходима?
(!) Контроль над забором материала, чтобы не обсеменить извне. Чтобы АБ действовал, в очаге необходимо создание 3 МПК. В эксперименте: если в крови 10 МПК, то эффект +++ 7 МПК ++ 5 МПК + 3 МПК +/- А способность накапливаться в очаге зависит от АБ. АБ всасываются в ЖКТ и делятся на 3 группы:
Нельзя запивать лекарственные препараты тонизирующими напитками, т.к. резко нарушается всасывание за счет связывания с железом. Поэтому нежелательно запивать и соками. У многих АБ есть тропность к различным органам и тканям. Например, при менингите метронидазол на 100% проникает в СМЖ, и на 60% - левомицетин. Костные АБ: тетрациклины, фузидин, линкомицин. В бронхиальном секрете накапливаются: эритромицин, триметоприл. В желчевыводящих путях: эритромицин, тетрациклин. В мочевыводящих путях: пенициллины и ! гентамицин !, чье выведение с мочой длится долго после отмены, вплоть до 10 дней. Иногда приходится вводить АБ местно в очаг. ^ 1. Сильно кумулируют – аминогликозиды - полимиксины - естественные тетрациклины - ристомицин 2. Умеренно кумулируют: в – лактамиды 3. Мало кумулируют: - доксициклин - левомицетин - фузидин [Эти препараты сильно кумулируются у пациентов с заболеваниями печени]. (!) Каким органом АБ выводятся, тот орган и повреждают. (!) Обычно переоценку эффективности АБ – терапии проводят через 2 – 4 дня, и если АБ через 2 дня не действует, то необходим тщательный анализ. При хроническом процессе сроки переоценки – 1 неделя. Осложнения АБ – терапии
Лекарственная аллергия (в т.ч. 60% - пенициллиновый ряд) (!) Необходим учет возможности перекрестной аллергии - у пенициллинов – 100%, пенициллины с цефалоспоринами – 15%, сульфаниламиды, противомикробные и противодиабетические, фуросемид и бисептол, новокаин и новокаиновая соль пенициллина. (!) Необходим учет аллергического антибактериального анамнеза: не забывать о возможности сенсибилизации не только антибиотиками, но и пищей (в ней могут быть АБ), плесенью, эпидермофитией. Токсическое действие антибиотиков
[Аминогликозиды плохо проникают в мокроту при парентеральном введении] Дисбактериоз Нужно выбрать препараты, не попадающие в кишечник, например, амоксициллин всасывается в верхних отделах ЖКТ, ампициллин доходит до нижних отделов. Лучше амоксициллин, или ампициллин с носителем (проходит печень, затем активно освобождается). Бифидум-бактерин – хорошо, устойчив к АБ. (!) Закончили АБ-терапию, бак. Препараты должны еще 1 неделю вводиться. Можно молочные продукты – не молоко (!),а также Вит. PP. ^ – не усилить эффект, а расширить спектр действия. - пенициллины + тетрациклины = нельзя - АБ снижают эффект других препаратов (противоэпилептических, оральных контрацептивов) - Индукторы микросомальных ферментов повышают гепатотоксичность гепатотоксичных средств: - фенобарбитал + тетрациклин, эритромицин. - теопек (эуфиллин) + эритромицин = гепатотоксичное действие - фторхинолоны (ципролет) - карбенициллин не действует на синегнойную палочку Перед забором мокроты:
Дисковый метод чувствительности к АБ жид. сред. Клиренс креатинина (КК) – биохимический показатель, характеризует функцию почек. КК = M тела * (180 – возраст) / К * 8 в N = 80 – 120 … ^
Цефалоспорины. I, II, III поколение не активны в отношении энтерококков. I поколения – цефалотин - ГР + кокки - цефазолин (кефзол) - ГР- кокки - цефалексин - кишечная палочка, анаэробы II поколения – цефамандол - ГР+ кокки - цефалоксин - ГР - флора больше III поколения – (!) клафоран (цефотаксим) - цефтазидим - ГР - флора - (!) цефаперазол (фортум) - синегнойная палочка - лонгацеф (цефабит) - госпитальные штаммы - антабусоподобный эффект – нельзя совмещать с алкоголем (коллапс) IV поколения – кейтен - действует на энтерококк Карбапинемы
ГР- кокки (гоно-, менингококки) ГР- флора (кишечная палочка, протей, сальмонеллы, шигеллы, синегнойная палочка) Парентеральное и капельное ведение. Показания:
Тиенам восстанавливает чувствительность микрофлоры к другим антибиотикам, как и ципрофлоксацин. Побочные явления: флебиты, диспепсические расстройства, дисбактериоз. Рациональная комбинация Задачи:
- аддиция (суммация)
бактериостатик + бактериостатик = чаще суммация Любопытно, но в 2% случаев комбинация ампициллина и гентамицина при действии на протей дает антагонизм. Желательно комбинировать АБ в следующих случаях (Померанцев):
- цефалоспорины + аминогликозиды - макролиды + тетрациклины ^
- ампициллин + гепарин - АБ + гепарин - ампициллин + р-р глюкозы, стабилизированный HCl - пенициллины + аминогликозиды = нельзя в одном шприце - ампициллин + линкомицин 2. Фармакокинетическое. - рифампицин + контрацептивы + противодиабетические препараты + антиконвульсанты + антикоагулянты = ослабляется действие - линкомицин + - фторхинолоны + метилксантин = кумуляция ксантином - клиндамицин +
ФОРТУМ (цефтазидим) – бактерицидный препарат выбора при тяжелых инфекциях
При госпитальных инфекциях:
Взрослым: в/м или в/в от 1 до 6 г/сут, внутрибрюшинно от 125 до 250 мг на 2 л диализной жидкости МАНДОЛ (цефамандол нафат, cefamandol nafat) – цефалоспориновый антибиотик широкого спектра действия - с улучшенной активностью как в ГР-отриц.,так и в ГР-полож. пределах - также в пределах аэробных и анаэробных смешанных инфекций - никакой метаболизации не происходит - терапевтические концентрации в плевре, в синовиальной жидкости, в желчи, в костях - очень хорошая переносимость - хорошо комбинируется с аминогликозидами Показания:
Доза 0,5 – 2гр на каждые 4 – 8 часов, в зависимости от рода и степени тяжести инфекции. Для жизнеопасных инфекций рекомендуется доза 12 г/сут. КЕФЗОЛ (цефазолин, Cephazolin)
НЕБЦИН (тобрамицина сульфат, Tobramicin sulfat)
РЕФЛИН (Cefazolin) Пред- и послеоперационная хирургическая профилактика:
gendocs.ru Побочное действие антибиотиков. Рациональное комбинирование антибактериальных средств.Побочные эффекты антибиотиков, обусловленные их аллергенным действием. а) аллергические реакции: -лихорадка -ангионевротический отек -сывороточная болезнь -полиартрит -системная красная волчанка -анафилактический шок б) кожные реакции: -кореподобная сыпь, геморрагическая сыпь (пурпура) -крапивница -узловатая и мультиформная эритема -эксфолиативный или контактный дерматит в) ротовая полость: -сухость, жжение, болезненность -зуд ротовой полости и языка -стоматит, острый глоссит, хейлоз, черный или коричневый налет на языке г) ЖКТ: тошнота, рвота, диарея Побочные эффекты и осложнения антибиотикотерапии, связанные с фармакодинамическим действием: а) нервная система: -поражение VIII пары черепно-мозговых нервов -парестезия -нарушение сна или эмоционального статуса -периферический неврит -психозы или судороги -угнетение дыхания б) кровь: -эозинофилия (сенсибилизация к любому АБ) -апластическая или гемолитическая анемия -тромбоцитопения -лейкопения -гиперкалиемия, гипернатриемия, гипокалиемический алкалоз в) выделительная система: -гематурия, кристаллурия, нарушение оттока мочи -острый тубулярный некроз, нефротоксичность г) ЖКТ: желтуха, гепатит, стеаторея Побочные эффекты и осложнения антибиотикотерапии, связанные с химиотерапевтическим действием: а) дисбактериоз – развивается при применении АБ широкого спектра действия, сопровождается подавлением, изменением спектра микрофлоры кишечника, колонизацией кишечника патогенной микрофлорой. Проявления: псевдомембранозный колит, энтероколиты, кандидоз (оральный, фарингеальный, ректальный, перианальный) б) иммунодепрессия в) реакции обострения (реакция Яриша-Герсгеймера): бактериолиз, эндотоксиновый шок.
Показания для комбинированной антибиотикотерапии. · лечение тяжелых больных с подозрением на инфекцию неизвестного происхождения · предупреждение развития резистентных штаммов в некоторых клинических ситуациях · расширение спектра противомикробной активности (терапия микст-инфекций) · усиление противомикробного эффекты при тяжелых состояниях · снижение токсичности отдельных АБ Принципы комбинированной антибиотикотерапии. 1. Нельзя комбинировать бактерицидные и бактериостатические АБ. 2. Нельзя совместно использовать АБ со сходными побочными эффектами. 3. Не рекомендуется использовать одновременно более двух-трех АБ 4. Комбинированная антибиотикотерапия должна быть удобна для пациента и по возможности экономически выгодна. 79. Сульфаниламидные препараты. Синтетические противомикробные средства. Классификация сульфаниламидных препаратов для по локализации и продолжительностидействия: · Сульфаниламиды системного действия: а) короткого действия (Т1/2 < 10 ч): сульфаниламид (стрептоцид), сульфадимидин (сульфадимезин), сульфаэтидол (этазол). б) средней продолжительности действия (Т1/2= 10-24 ч): сульфадиазин. в) длительного действия (Т1/2= 24-48 ч.): сульфаметоксипиридазин, сульфадиметоксин, сульфадоксин г) cверхдлительного действия (Т1/2 >60 ч.): сульфален. · Сульфаниламиды, действующие в просвете ЖКТ: фталилсульфатиазол (фталазол), сульфасалазин. · Сульфаниламиды для местного применения: сульфацетамид, сульфадиазин серебра.
Бактериостатический эффект сульфаниламидов основан на структурном сходстве с парааминобензойной кислотой (ПАБК), которая необходима для жизнедеятельности микроорганизмов. Изначально были чувствительны многие грамположительные и грамотрицательные кокки, грамотрицательные палочки (Е.соli, P.mirabilis и др.), однако в настоящее время они приобрели устойчивость. Сульфаниламиды сохраняют активность против нокардий, токсоплазм, малярийных плазмодиев. Природная устойчивость характерна для энтерококков, синегнойной палочки и анаэробов. Хорошо всасываются в ЖКТ (кроме неабсорбируемых), особенно при приеме натощак в измельченном виде. Хорошо распределяются в организме, проникают через ГЭБ (лучше всех сульфазин). Наибольшую концентрацию в крови создают препараты короткой и средней продолжительности действия. Метаболизируются в печени. Выводятся с мочой и желчью. Показания: -Нокардиоз. -Токсоплазмоз (чаще сульфадиазин в сочетании с пириметамином). -Тропическая малярия, устойчивая к хлорохину (в сочетании с пириметамином). Противопоказания: -Возраст до 2 месяцев, так как сульфаниламиды вытесняют билирубин из связи с белками плазмы и могут вызывать ядерную желтуху (исключение - врожденный токсоплазмоз). -Тяжёлые нарушения функции печени. -Почечная недостаточность. Побочное действие: 1. Нефротоксичность двух типов: а) кристаллурия при кислой реакции мочи б) нефрит гиперчувствительной природы 2. Диспепсические явления (тошнота, рвота, диарея) 3. Кожные реакции (сыпь, эксфолиативный дерматит) 4. Неврологические реакции 5. Гипотиреоидизм 6. Нарушения гемопоэза (анемия, лейкопения) 7. Гепатотоксичность Для предупреждения кристаллурии больные при приеме сульфаниламидных препаратов должны получать обильное щелочное питье. По антимикробной активности сульфаниламиды значительно уступают антибиотикам, поэтому сфера их применения довольно ограничена. Их назначают главным образом при непереносимости антибиотиков или развитии к ним привыкания. Нередко сульфаниламиды комбинируют с некоторыми антибиотиками. СУЛЬФАДИМИДИН (Sulfadimidinum). Сульфаниламид короткого действия. Активен в отношении грамположительных и грамотрицательных кокков, Escherichia coli, Shigella spp., Klebsiella spp., Vibrio cholerae, Clostridium paraperfringens, Bacillus anthracis, Corynebacterium diphtheriae, Yersinia pestis, Chlamydophila (Chlamydia) spp., Actinomyces israelii, Toxoplasma gondii. Быстро всасывается из ЖКТ (преимущественно в тонкой кишке), на 75–86% связывается с белками плазмы. Хорошо проникает в ткани (в т.ч. в легкие, ликвор), быстро выводится из организма, T1/2 — 5–7 ч; элиминация осуществляется преимущественно почками. Показания: Инфекционно-воспалительные заболевания, вызванные чувствительной микрофлорой: тонзиллит, бронхит, пневмония, гайморит, отит, воспалительные заболевания желче- и мочевыводящих путей, раневая инфекция, гонорея, рожа, дизентерия, токсоплазмоз, нокардиоз. Противопоказания: Гиперчувствительность. Ограничения к применению: Заболевания кроветворной системы, нарушения функции почек, гипербилирубинемия у детей (из-за опасности развития билирубиновой энцефалопатии), дефицит глюкозо-6-фосфатдегидрогеназы (из-за опасности развития гемолитического криза), порфирия, азотемия, беременность, кормление грудью. Побочные действия: Тошнота, рвота, кристаллурия, лейкопения, агранулоцитоз, аллергические реакции. Сульфадимидин, как и другие сульфаниламидные препараты, часто применяют вместе с антибиотиками. СУЛЬФАДИАЗИН. Антибактериальное средство широкого спектра действия, производное сульфаниламида. Средней продолжительности действия. Сульфадиазин активен в отношении Staphyloccocus spp., Escherichia coli, Proteus spp., Klebsiella spp. К сульфадиазину также чувствительны некоторые виды грибов. Показания: Профилактика и лечение инфекционно-воспалительных заболеваний, вызванных чувствительными к сульфадиазину микроорганизмами: при ожогах, пролежнях, глубоких ранах. Противопоказания: Беременность, повышенная чувствительность к сульфадиазину. Не применяют у новорожденных. Побочные действия: Местные реакции: чувство жжения, зуд. При длительном применении препарата на больших поверхностях концентрация сульфадиазина в сыворотке крови может достигнуть пороговых величин и привести к развитию лейкопении. СУЛЬФАДИМЕТОКСИН (Sulfadimethoxinum). Относится к группе сульфаниламидных препаратов длительного действия. Эффективен в отношении грамположительных и грамотрицательных бактерий: действует на пневмококки, стрептококки, стафилококки, кишечную палочку, палочку клебсиеллы (палочку Фридлендера), возбудителей дизентерии; менее активен в отношении протея; активен в отношении вируса трахомы, не действует на штаммы бактерий, устойчивые к другим сульфаниламидным препаратам. Показания: Инфекционно-воспалительные заболевания, вызванные чувствительными к сульфадиметоксину микроорганизмами, в т.ч. ангина, гайморит, отит, бронхит, дизентерия, воспалительные заболевания желчевыводящих и мочевыводящих путей, рожистое воспаление, раневые инфекции, трахома. Противопоказания: Повышенная чувствительность к сульфаниламидам, угнетение костномозгового кроветворения, почечная и/или печеночная недостаточность, хроническая сердечная недостаточность, врожденный дефицит глюкозо-6-фосфатдегидрогеназы, порфирия, азотемия, беременность. Сульфадиметоксин снижает эффективность бактерицидных антибиотиков, действующих только на делящиеся микроорганизмы (в т.ч. пенициллины, цефалоспорины). Побочные действия: Со стороны ЦНС: возможна головная боль. Со стороны пищеварительной системы: диспептические симптомы, тошнота, рвота, холестатический гепатит. Аллергические реакции: кожные высыпания, лекарственная лихорадка. Со стороны системы кроветворения: редко - лейкопения, агранулоцитоз. КО-ТРИМОКСАЗОЛ. Ко-тримоксазол — комбинированный антибактериальный препарат группы сульфаниламидов. Ко-тримоксазол - химиотерапевтическое средство с широким спектром бактерицидного действия, обусловленного блокированием биосинтеза фолатов в микробных клетках: сульфаметоксазол нарушает синтез дигидрофолиевой кислоты, а триметаприм препятствует превращению дигидрофолиевой кислоты в тетрагидрофолиевую. Активность препарата проявляется в отношении почти всех групп микроорганизмов: грамотрицательных — Salmonella spp., Shigella spp., Neisseria spp., B. proteus vulg., Vibrio cholerae, Jersinia spp., Escherichia coli, Corinebacterium; грамположительных — Staphylococcus spp. и др. К препарату чувствительны также хламидии, актиномицеты, клебсиеллы. Важное клиническое значение имеет активность ко-тримоксазола против пневмоцист Pneumocystis carinii, важного возбудителя пневмоцистной пневмонии у ослабленных, иммунодефицитных больных, особенно больных СПИДом. При приеме внутрь оба компонента препарата полностью всасываются из желудочно-кишечного тракта. Основной путь элиминации — почки. Показания: Инфекции дыхательных путей (бронхит, пневмония, абсцесс легкого, эмпиема плевры, отит, синусит), менингит, абсцесс головного мозга, мочеполовой системы (пиелонефрит, уретрит, сальпингит, простатит), в том числе гонорейной природы, желудочно-кишечных (дизентерия, холера, брюшной тиф, паратиф, диарея), кожи и мягких тканей (пиодермия, фурункулез и др). Противопоказания: Повышенная чувствительность к триметоприму и/или сульфаниламидам, беременность, новорожденные до 6 недель жизни, тяжелые кардиальные, печеночные, почечные и гематологические заболевания, дефицит глюкозо-6-фосфатдегидрогеназы. Побочные действия: Со стороны органов желудочно-кишечного тракта — диспепсия, тошнота, рвота, анорексия, редко — холестатический и некротический гепатиты, повышение уровня трансаминаз и билирубина, псевдо-мембранозный энтероколит, панкреатит, стоматит, глоссит. Со стороны органов кровотворения — агранулоцитоз, апластическая анемия, тромбоцитопения, гемолитическая анемия, мегалобластическая анемия, гипотромбинемия, метгемоглобинемия, эозинофилия. Со стороны мочевыделительной системы — кристаллургия, почечная недостаточность, интерстициальный нефрит, повышение уровня креатина плазмы. Токсическая нефропатия с олигоурией и анурией. Аллергические реакции — крапивница, сыпь, токсический эпидермиальный некролиз (синдром Лайелла), синдром Стивена-Джонсона, аллергический миокардит, мультиформная эритема, эксфолиативный дерматит, отек Квинке, зуд, покраснение склер, повышение температуры тела. Прочие — гиперкалиемия, гипонатриемия, асептический менингит, периферический неврит, головная боль, депрессия, артралгия, миалгия, слабость, фотосенсибилизация Передозировка. Симптомы — анорексия, тошнота, рвота, слабость, боли в животе, головная боль, сонливость, гематурия, кристаллурия, помутнение сознания,смерть. Принимаемые меры: отмена препарата, промывание желудка (не позднее 2 часов после приема чрезмерной дозы), обильное питье, форсированный диурез, прием фолината кальция (5-10 мг/сут), при необходимости гемодиализ. ФТАТИЛСУЛЬФАТИАЗОЛ (ФТАЛАЗОЛ) (Phthalazolum). Относится к группе сульфаниламидов, дейстфующих в просвете ЖКТ. Фталазол медленно всасывается из желудочно-кишечного тракта. Основная масса препарата при введении внутрь задерживается в кишечнике, где постепенно происходит отщепление активной (сульфаниламидной) части молекулы. Создающейся при этом высокой концентрацией сульфаниламида в кишечнике в сочетании с активностью препарата в отношении кишечной флоры, объясняют его большую эффективность при кишечных инфекциях. Фталазол малотоксичен; побочных явлений обычно не вызывает. Применяют при дизентерии (острой и хронической в стадии обострения), колитах, гастроэнтеритах, а также при оперативных вмешательствах на кишечнике для предупреждения гнойных осложнений. Лечение фталазолом при необходимости сочетают с назначением антибиотиков. Целесообразно одновременно с фталазолом назначать также хорошо всасывающиеся сульфаниламидные препараты (сульфадимезин, этазол, этазол-натрий и др.). СУЛЬФАЦЕТАМИД (СУЛЬФАЦИЛ-НАТРИЙ). Сульфаниламид для местного применения. Препарат эффективен при стрептококковых, гонококковых, пневмококковых и коли-бациллярных инфекциях. Хорошая растворимость в воде позволяет использовать препарат для инъекций; растворы закапывают также в коньюнктивальный мешок. Для инъекций применяют сульфацетамид при пневмониях, гнойных трахеобронхитах, инфекциях мочеполовых путей и других инфекционных заболеваниях. Вводят внутривенно медленно (в течение не менее 5 мин). В глазной практике сульфацил-натрий применяют в виде растворов и мази при конъюнктивитах, блефаритах, гнойных язвах роговицы и других инфекционных заболеваниях глаз. Препарат эффективен при гонорейных заболеваниях глаз у новорожденных и взрослых. Сульфацетамид можно применять для лечения инфицированных ран. Раневые поверхности припудривают порошком. Препарат обычно хорошо переносится. Иногда, особенно при использовании более концентрированных растворов, наблюдается раздражение тканей; в этих случаях назначают растворы меньшей концентрации. Сульфацетамид противопоказан при наличии в анамнезе данных о токсикоаллергических реакциях на сульфаниламиды. Внутривенное введение противопоказано при тяжелых заболеваниях кроветворной системы и уремии. СУЛЬФАСАЛАЗИН. Сульфаниламид для местного применения. Препарат оказывает антибактериальное действие в отношении диплококков, стрептококков, гонококков, кишечной палочки. Особенностью препарата является то, что он оказывает выраженный лечебный эффект у больных неспецифическим язвенным колитом. Механизм этого действия изучен не полностью. Определенную роль играет способность препарата накапливаться в соединительной ткани (в том числе в ткани кишечника) и постепенно отделять 5 - аминосалициловую кислоту и сульфапиридин, обладающие противовоспалительным и антибактериальным свойствами. Этот же механизм действия, по-видимому, лежит в основе терапевтической эффективности при неспецифическом язвенном колите. Основным показанием к применению салазосульфапиридина является неспецифический язвенный колит. Назначают внутрь. Салазосульфапиридин эффективен также при легкой и средне-тяжелой формах болезни Крона (гранулематозный колит). В последнее время салазосульфапиридин (сульфасалазин) стали применять в качестве базисного средства при лечении ревматоидного артрита, используя наличие у препарата иммунокорригирующих свойств. При лечении салазосульфапиридином могут возникнуть тошнота, рвота, головная боль, головокружение. В случае развития аллергических реакций (кожные высыпания, лекарственная лихорадка), лейкопении применение препарата следует прекратить. Препарат противопоказан при наличии в анамнезе выраженных токсико-аллергических реакций на сульфаниламиды. Лечение надо проводить под тщательным врачебным наблюдением; необходимо систематически контролировать картину крови. Таблетки рекомендуется принимать через равные промежутки времени после еды, обильно запивать 1 - 2 % раствором натрия гидрокарбоната. Препарат выделяется с мочой и при щелочной (но не кислой) реакции окрашивает ее в желто-оранжевый цвет.
megalektsii.ru Классические принципы рациональной антибиотикотерапии:
В последние годы классические принципы антибиотикотерапии существенно дополнены. Появилось понятие – алгоритм антибактериальной терапии хирургических инфекций. В основном это касается так называемой эмпирической терапии (назначение антибиотика когда ещё не высеян штамм микроорганизмов и не определена чувствительность). При эмпирической терапии существует 2 принципа: принцип максимального спектра и принцип разумной достаточности. Принцип максимального спектра– назначение антибиотиков максимального спектра действия и наибольшей эффективности для обеспечения наибольшей вероятности уничтожения микроорганизмов – возбудителей заболевания. В то же время высока вероятность формирования резистентных штаммов микроорганизмов и неэффективности применения в последующем курсов других антибиотиков. Принцип разумной достаточности– назначение не самого сильного и не самого широкого спектра действия препарата, но достаточно эффективного в отношении предпологаемого возбудителя. Вероятность достижения клинического эффекта весьма высока и в то же время менее вероятна селекция резистентности, а в резерве остаются более мощные современные препараты. Выбор подхода и сочетание этих двух принципов индивидуальны и зависят от степени тяжести инфекции, состояния пациента, вирулентности микроорганизма. При тяжёлых инфекциях при эмпирической терапии целесообразно назначать либо комбинацию антибиотиков первой очереди (например полусинтетический пенициллин - ампициллин и аминогликозид – гентамицин) или проводить монотерапию антибиотиком второй очереди (цефалоспорины 2-го или 3-го поколения, реже современные макролиды). Лишь при особо тяжёлых инфекциях и неэффективности других препаратов используют антибиотики резерва – фторхинолоны и карбопенемы. При этиотропной терапии выбор препарата определяется результатом микробиологического исследования (выделение возбудителя и его чувствительности к антибиотикам). В современной хирургии доказана высокая эффективность так называемой ступенчатой терапии – раннего перехода с парентерального введения антибиотиков на пероральные формы препаратов той же группы, или близких по спектру действия. studfiles.net |
г.Самара, ул. Димитрова 131 [email protected] |
 |