 |
|
||||||||||
|
Вирус, убивающий младенцев. Что такое РСВ-инфекция. Вакцина от рс инфекцииВакцина от РСВ-инфекцииКаждый год в мире госпитализируются миллионы детей с заболеваниями легких, вызванными респираторно-синцитиальным вирусом (РСВ), и до 160 тыс. детей погибает в результате развития вызванных им тяжелых пневмоний. В десятку научных прорывов 2013 г. по версии «Science» попали исследования в области структурной молекулярной биологии, целью которых является создание профилактической вакцины от этого вирусного заболевания. Через полтора года исследователи планируют получить препарат, пригодный для клинических испытаний В России каждый год регистрируется 25—31 млн случаев инфекций дыхательных путей, а еще около 10 млн остаются, судя по всему, неучтенными, потому что в случаях «легкой простуды» больные к врачу обычно не обращаются. Этот самый массовый тип заболеваний вызывается преимущественно вирусами из семейств пикорнавирусов (риновирусами и энтеровирусами), парамиксовирусов, коронавирусов, аденовирусов, парвовирусов, а также бактериями.
Нужно отметить, что именно вирусы являются непосредственной причиной более 70 % всех респираторных инфекций, а бактерии нередко продолжают начатое вирусами дело, становясь причинами вторичных, уже бактериальных инфекций. При этом единственной вирусной респираторной инфекцией, против которой разработаны вакцины, остается пока вирус гриппа. Судя же по данным медицинской статистики, главной причиной острых респираторных инфекций являются риновирусы. Но так как они вызывают заболевания с относительно легким протеканием и продолжительностью не более 2—5 дней, то их просто терпят как небольшое, пусть и неизбежное, зло. Да и серотипов этих вирусов существует множество, поэтому затраты на соответствующую вакцину будут весьма значительными, а защититься от всех просто невозможно. Среди остальных вирусов, вызывающих ОРВИ, выделяется респираторно-синцитиальный вирус (РСВ). У взрослых и детей старшего возраста он вызывает поражения дыхательного тракта, проявляющиеся ринофарингитом, бронхитом и пневмонией, но особенно опасен он для детей младшего возраста, у которых поражение вирусом нижних дыхательных путей может заканчиваться летальным исходом. Сейчас в профилактических целях для детей с высоким риском заражения РСВ используют препарат «Palivizumab», созданный на основе моноклональных антител – белков-иммуноглобулинов, способных связываться только с одним антигеном инфекционного агента (в данном случае – с участком вирусного F-белка, который способствует слиянию оболочки вируса с мембраной клеткой). Однако для профилактики заболевания этот препарат должен использоваться неоднократно, при том что цена его высока.
С помощью подходов структурной биологии исследователям удалось детально изучить особенности процесса слияния вируса с клетками в течение инфекционного процесса и обнаружить наиболее «уязвимый» участок на молекуле F-белка (Cohen et al., 2013). В результате был создан модифицированный аналог этого белка, который может служить в качестве мощного иммуногена, основного ингредиента профилактической вакцины. И действительно, введение этого белка лабораторным животным стимулировало выработку в их организмах сильнодействующих антител, намного более эффективных, чем «Palivizumab». Результаты этих исследований дают основания надеяться, что вакцина против РСВ будет в ближайшее время разработана и внедрена в практику, в том числе и у нас в стране. Ведь, к примеру, в том же Новосибирске, по данным Е. И. Сергеевой из ГНЦ вирусологии, и биотехнологии «Вектор» (Кольцово, Новосибирская обл.), респираторно-синцитиальный вирус вызывает, до 7 % всех заболеваний ОРВИ. В заключение отметим, что за последнее десятилетие стали известны еще два новых типа возбудителей ОРВИ: метапневмовирусы и бокавирусы. Так, среди детей, госпитализированных в стационары Москвы за период 2003—2009 гг. с тяжелыми респираторными заболеваниями, свыше четверти было инфицировано именно этими вирусами (Козулина, 2010). При этом наиболее восприимчивыми к метапневмовирусу оказались дети грудного возраста, а к бокавирусу – двух первых лет жизни. Очевидно, эти два возбудителя ОРВИ наравне с респираторно-синцитиальным вирусом должны стать объектом интенсивных исследований, направленных на создание безопасных и эффективных профилактических вакцин. scfh.ru Респираторно-синцитиальная инфекция - причины, симптомы, диагностика и лечение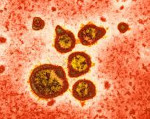 Респираторно-синцитиальная инфекция – заболевание вирусной этиологии, характеризующееся воспалением нижних отделов дыхательных путей, умеренным катаральным и интоксикационным синдромом. Клинические проявления респираторно-синцитиальной инфекции включают субфебрильную температуру, познабливание, слабость, упорный сухой, приступообразный кашель, экспираторную одышку. Диагноз респираторно-синцитиальной инфекции подтверждается путем выделения вируса из смывов носоглотки и серологической диагностики. Лечение, как правило, амбулаторное, препаратами интерферона, отхаркивающими и муколитическими средствами.  Респираторно-синцитиальная инфекция (РС-инфекция) – ОРВИ, протекающая с преимущественным поражением нижних дыхательных путей в виде бронхита, бронхиолита и интерстициальной пневмонии. Название заболевания отражает место размножения вируса в организме (респираторный тракт) и цитопатогенные эффекты, вызываемые в культуре клеток образование обширных синцитиальных полей (слияния клеток). В структуре различных ОРВИ на долю респираторно-синцитиальной инфекции приходится 15-20% всех случаев. Наиболее уязвимы перед лицом инфекции дети первого года жизни и раннего возраста. В связи с этим особое внимание респираторно-синцитиальной инфекции уделяется со стороны педиатрии. Причины респираторно-синцитиальной инфекцииРеспираторно-синцитиальный вирус принадлежит к роду Pneumovirus, семейству Paramyxoviridae. Вирионы имеют округлую или нитевидную форму, диаметр 120-200 нм, липопротеидную оболочку. Отличительной особенностью РС-вируса служит отсутствие в оболочке гемагглютинина и нейраминидазы. Во внешней среде вирус быстро инактивируется при нагревании и использовании дезинфицирующих средств, однако хорошо переносит низкие температуры и может до нескольких часов сохраняться в капельках слизи. Респираторно-синцитиальная инфекция относится к вирусным болезням с воздушно-капельным путем передачи. Вирус способны распространять как больные люди, так и его носители. Для респираторно-синцитиальной инфекции характерны семейные и коллективные вспышки; регистрируются случаи внутрибольничной инфекции, особенно в педиатрических стационарах. Распространенность инфекции повсеместная и круглогодичная с вспышками заболеваемости в зимне-весеннее время. Наибольшая восприимчивость к респираторно-синцитиальной инфекции отмечается среди недоношенных, детей в возрасте от 4-5 месяцев до 3-х лет. Как правило, в раннем возрасте большая часть детей переболевает респираторно-синцитиальной инфекцией. Ввиду нестойкости приобретенного иммунитета нередки повторные случаи возникновения РС-инфекции, которая на фоне остаточного иммунитета протекает в более стертой форме. Однако при полном исчезновении из организма специфических секреторных антител (IgA) вновь может развиться манифестная форма респираторно-синцитиальной инфекции. Патогенез РС-инфекции сходен с механизмом развития гриппа и парагриппа и связан с тропностью вирусов к эпителию дыхательных путей. Входными воротами служит респираторный тракт; первичное размножение вируса происходит в цитоплазме эпителиальных клеток носоглотки, однако патологический процесс может быстро распространяться на мелкие бронхи и бронхиолы. При этом происходит гиперплазия пораженных клеток, образование псевдогигантских клеток и симпластов. Клеточные изменения сопровождаются явлениями гиперсекреции, сужением просвета бронхиол и их закупоркой густой слизью, лейкоцитами, лимфоцитами и слущенным эпителием. Это приводит к нарушению дренажной функции бронхов, образованию мелкоочаговых ателектазов, эмфиземы легочной ткани, нарушению газообмена. Дальнейшее развитие респираторно-синцитиальной инфекции определяется степенью дыхательной недостаточности и присоединением бактериальной флоры. Симптомы респираторно-синцитиальной инфекцииВ зависимости от преимущественной заинтересованности тех или иных отделов респираторного тракта, РС-инфекция может протекать в форме назофарингита, бронхита, бронхиолита или пневмонии. Обычно первые симптомы респираторно-синцитиальной инфекции появляются спустя 3-7 дней после заражения. Развитие заболевания постепенное: в первые дни беспокоят субфебрилитет, познабливание, умеренная головная боль, скудные серозно-слизистые выделения из носа. В некоторых случаях появляются признаки конъюнктивита, инъекция сосудов склер. Характерным симптомом респираторно-синцитиальной инфекции служит упорный сухой кашель. В случае присоединения пневмонии температура повышается до 38-39 °С, нарастают явления интоксикации. Возникает тахипноэ, боли за грудиной, иногда - приступы удушья. Кашель становится продуктивным, приступообразным с отделением густой, вязкой мокроты в конце приступа. При тяжелой форме респираторно-синцитиальной инфекции нарастают признаки дыхательной недостаточности, возникает одышка экспираторного типа, развивается цианоз губ и акроцианоз. В некоторых случаях РС-инфекция протекает с явлениями обструктивного бронхита и ложного крупа. Длительность течения легких форм РС-инфекции составляет неделю, средне-тяжелых - 2-3 недели. Из наслаивающихся бактериальных осложнений чаще всего возникают средний отит, синусит, пневмония. Наиболее тяжело респираторно-синцитиальная инфекция протекает у детей первого года жизни. При этом отмечается высокая лихорадка, возбуждение, судорожный синдром, постоянный кашель, рвота, кашицеобразный или жидкий стул. Летальные исходы регистрируются в 0,5% случаев. Диагностика и лечение респираторно-синцитиальной инфекцииОснованием для предполагаемого диагноза «респираторно-синцитиальная инфекция» может служить характерная клиническая картина, напряженная эпидемиологическая ситуация и массовая вспышка заболевания, особенно среди детей. На рентгенограмме легких выявляется понижение прозрачности легочных полей, усиление и тяжистость бронхососудистого рисунка, мелкоочаговые воспалительные тени, участки ателектазов и эмфиземы. Специфическое лабораторное подтверждение респираторно-синцитиальной инфекции осуществляется с помощью выделения РС-вируса из носоглотки на культуре ткани и определения нарастания титра антител в парных сыворотках (РН, РСК и РНГА). При проведении дифференциальной диагностики исключаются грипп, парагрипп, риновирусная инфекция, аденовирусная инфекция, легионеллез, орнитоз, коклюш, микоплазменная, хламидийная и бактериальная пневмония. Лечение легких и среднетяжелых случаев респираторно-синцитиальной инфекции проводится амбулаторно; детям первого года жизни и пациентам с осложненным течением заболевания необходима госпитализация. В остром периоде показаны постельный режим, полноценная щадящая диета, кислородотерапия, щелочные ингаляции. Назначаются препараты противовирусного действия (акридонуксусная кислота, умифеновир, кагоцел), отхаркивающие средства и бронхолитики, при наличии обструктивного синдрома – глюкокортикоиды. При развитии бактериальных осложнений назначаются антибиотики. Прогноз и профилактика респираторно-синцитиальной инфекцииВ большинстве случаев прогноз благоприятный; в госпитализации нуждаются около 2% пациентов. Летальные исходы возможны среди недоношенных и новорожденных, детей с врожденными пороками сердца, легких, иммунодефицитом. Перенесенный в раннем детстве бронхиолит, связанный с респираторно-синцитиальной инфекцией, является фактором риска развития бронхиальной астмы у детей в будущем. Профилактические мероприятия направлены на предупреждение внутрибольничных и коллективных вспышек респираторно-синцитиальной инфекции путем изоляции больных, дезинфекции и частого проветривания помещений. Вакцина против респираторно-синцитиальной инфекции находится на стадии разработки; в качестве меры специфической иммунопрофилактики может применяться иммуноглобулин против РС-вируса. www.krasotaimedicina.ru Эпидемия респираторно-синцитиальной инфекции. Вакцина против болезни АльцгеймераПередачу ведет из Нью-Йорка Евгений Муслин. Эпидемия респираторно-синцитиальной инфекции, вакцина против болезни Альцгеймера, а также последние медицинские новости - вот темы передачи. Евгений Муслин: Хотя хорошо известно, что острые инфекции дыхательных путей вызываются не только вирусами гриппа, но и многими другими возбудителями, в общественном сознании прочно укоренилось представление о том, что эпидемии так называемых простудных заболеваний - это всегда "грипп". Но вот недавно Центр по контролю за заболеваемостью в Атланте объявил о развитии в США эпидемии, вызванной совсем другим вирусным агентом, так называемым респираторно-синцитиальным вирусом. Мы попросили профессора Даниила Голубева прокомментировать это сообщение. Даниил Голубев: Действительно, термином "грипп" называют огромную группу заболеваний, вызываемых чуть ли не сотней разных возбудителей, кстати, не только вирусов, но и некоторых бактерий, а также микоплазм и даже грибков. Ну, а если говорить о вирусах, то помимо трех серотипов вируса - А, В и С, острые респираторные заболевания (так называемые ОРЗ) вызываются четырьмя серотипами парагриппозных вирусов, более чем 20 серотипами аденовирусов, и вот респираторно-синцитиальным (РС) вирусом, распространением которого озабочен сейчас главный федеральный центр США по контрою и профилактике инфекций в Атланте (СиДиСи). Евгений Муслин: Почему-то никогда до этого года не приходилось слышать специальных сообщений о каких-то других эпидемий респираторных заболеваний, кроме тех, которые вызываются вирусом гриппа. По-видимому, нынешнее сообщение СиДиСи связано с особо широким распространением этого респираторно-синцитиального вируса? Даниил Голубев: Да, дело обстоит именно так. СиДиСи отмечает повсеместное распространение РС-инфекции в разных районах США, а также в Канаде и Северной Мексике, и учитывая, то, что эта инфекция поражает самых маленьких детей, как и то, что против нее нет на вооружении никаких вакцин - ситуация вызывает немалую тревогу. Евгений Муслин: Расскажите пожалуйста поподробнее об этой инфекции? Даниил Голубев: Возбудитель респираторно-синцитиальной инфекции (РС-вирус) входит в семейство так называемых парамиксовирусов, которые хотя и родственны, но в то же время существенно отличны от ортомиксовирусов, включающих в себя вирусы гриппа - А,В и С. В семейство парамиксовирусов, помимо РС-вируса, входят также возбудители кори, эпидемического паротита (свинки), парагриппа. Но РС-вирус существенно отличен и от них, и по своей структуре, и по целому ряду свойств. Главным "оружием" РС-вируса является так называемый "белок слияния", распложенный на поверхности вирусной частицы. Связываясь с поверхностными мембранам атакуемых клеток этот белок обусловливает их слияние и образование многоядерных симпластов - синцитиев. Отсюда и название вируса - "респираторно-синцитиальный". РС-вирус - бесспорно, респираторный вирус, то есть микроорганизм, поражающий дыхательные пути (респираторный тракт) но в отличие от других подобных возбудителей "объектом его нападения" являются не верхние, а нижние дыхательные пути - трахеи, бронхи и легкие. Особенно часто поражает РС-вирус новорожденных и детей в возрасте до трех лет, вызывая у них бронхиты, бронхиолиты и пневмонии, протекающие очень тяжело, а иногда завершающиеся летальным исходом. Заболевания, как правило, возникают не изолированно, а в виде вспышек, иногда достаточно обширных. Евгений Муслин: Как часто такие вспышки возникают? Даниил Голубев: В отличие от других респираторных вирусных инфекций, в частности, гриппа, вспышки РС-инфекции разной интенсивности возникают ежегодно в зимний сезон, поражая сотни и тысячи детей. Как отметил представитель СиДиСи доктор Дэвид Шей, в прошлом году заболеваемость РС-инфекцией начала регистрироваться в конце октября и продолжала регистрироваться вплоть до марта. Новый подъем заболеваемости начался ранней осенью этого года в южных штатах, а затем последовало повсеместное распространение инфекции. Особенно обширные вспышки возникают среди детей, госпитализированных в лечебных учреждениях, что и стало причиной особой озабоченности СиДиСи. Евгений Муслин: А как протекает у детей РС-вирусная инфекция? Даниил Голубев: Большинство симптомов аналогичны тем, которые характеризуют другие респираторные инфекции: повышение температуры, обильное отделяемое из носа, кашель, но в тяжелых случаях могут возникать тяжелая одышка и даже приступы удушья. По данным доктора Шея, до 500 маленьких детей ежегодно погибает в США в результате пневмоний, возникающих под влиянием РС-вируса. Кроме того, СиДиСи отмечает, что в этом году отмечено немало случаев РС-инфекции среди пожилых и престарелых американцев. Евгений Муслин: Как же надо бороться с этой тяжелой респираторной инфекцией? Даниил Голубев: К сожалению, арсенал лечебных и профилактических средств при РС-инфекции крайне невелик. Как известно, антибиотики на вирусы не действуют, но при первых же признаках пневмонии антибиотики необходимо немедленно применять, поскольку в этом случае к вирусам присоединяются разнообразные бактерии. Для лечения неосложненных пневмонией случаев остаются только симптоматические средства... Очень печально, что не существует никаких вакцин для предупреждения РС-инфекции у маленьких детей. И это несмотря на то, что активные попытки подготовить такие вакцины предпринимались уже в 60-е - 70-е годы - и в США, и в бывшем СССР. В США была подготовлена "убитая" РС-вакцина, то есть, взвесь вирусных частиц, инактивированных разными физическими воздействиями и неспособными поэтому вызвать заражение. Как известно, именно такой принцип положен в основу приготовления других вакцин, успешно применяемых в практике здравоохранения, в частности, вакцин против гриппа, которыми ежегодно прививаются десятки миллионов американцев. К сожалению, убитая вакцина против РС-инфекции оказалась не только неэффективной, но и реактогенной, вызывавшей парадоксальную аллергическую реакцию, что, конечно, сделало ее непригодной для внедрения в практику. Не получила положительного развития и попытка подготовить эффективную живую вакцину против РС-вирусной инфекции, предпринятая в те же годы в Академии Медицинских Наук СССР профессором А.А. Смородинцевым, хотя им же были успешно опробованы живые вакцины против полиомиелита и подготовлены оригинальные варианты живых вакцин против кори, свинки, гриппа, краснухи, клещевого и комариного энцефалитов. РС-вирус оказался самым крепким орешком. Евгений Муслин: Ну и как же предупредить заражение РС-вирусом? Даниил Голубев: Рекомендации по этому поводу выглядят довольно странно, но я повторю то, что говорится в рекомендациях СиДиСи: нужно... часто мыть руки, тщательно мыть посуду и не пользоваться общими чашками, стаканами и другой посудой... Дело в том, что хотя РС-вирус - респираторный, то есть передаваемый по воздуху с капельками слюны так же, как вирусы гриппа и других ОРЗ, этот возбудитель достаточно устойчив и может сохранить свою заразительность в течение достаточно длительного времени, находясь на поверхности кожи рук или на посуде. Поэтому немудреный лозунг: "Мойте часто и тщательно свои руки"! - как это ни кажется странным, на сегодня вполне определенный и эффективный метод предупреждения РС-инфекции. Лилия Шукаева: Из Торонтского университета в Канаде поступило сенсационное сообщение о разработке эффективной вакцины против тяжелейшего неврологического заболевания - болезни Альцгеймера, причем клинические испытания этой вакцины на людях могут быть начаты уже в ближайшее время. Как сообщают исследователи, эта вакцина предотвращает и лечит необратимую до сих пор потерю памяти, являющуюся одним из главных симптомов прогрессирующего старческого слабоумия, характерного для этой болезни. Сообщение о новой вакцине опубликовано в старейшем научном журнале "Nature" - "Природа". При болезни Альцгеймера, от которой страдают миллионы людей во всем мире, причем количество больных по причине старения населения все увеличивается, в мозгу у больных накапливаются токсические биохимические соединения - амилоиды, образующие так называемые амилоидные бляшки. Эти бляшки повреждают нервные клетки, что, согласно современным научным представлениям, и является причиной болезни Альцгеймера. Исследователи уже ранее доказали, что эти бляшки можно разрушить, впрыскивая подопытным мышам особую вакцину, приготовленную из амилоидных пептидов. Однако, даже такое разрушение бляшек до сих пор никогда не приводило к улучшению мозговых функций. Свои эксперименты канадские исследователи проводили на мышах, в мозгу у которых наблюдались амилоидные бляшки, и которые страдали от симптомов, аналогичных симптомам людей с болезнью Альцгеймера. Этим мышам и вводилась вакцина, приготовленная из амилоидных пептидов. Наблюдения показали, что новая вакцина предотвращает дальнейшее образование бляшек, очищает мозговые ткани и устраняет симптомы, характерные для болезни Альцгеймера. Видимо, такое действие вакцины объясняется стимулированием иммунной системы, атакующей амилоидные бляшки. Руководитель торонтского исследования доктор Кристофер Джанус заявил на пресс-конференции: "Наши результаты также показывают, что медикаментозное лечение, направленное на блокирование дальнейшего образования вредных пептидов у больных и на очистку мозговой ткани хорошо сочетается с вакцинированием. В будущем, видимо, наиболее перспективным окажется именно такое комбинированное лечение". Канадские исследователи считают, что их работа окончательно доказывает, что болезнь Альцгеймера вызывается именно амилоидными пептидами. По словам другого участника исследовательской группы доктора Дэвида Уэствея, в развитии болезни Альцгеймера, вполне возможно, играют роль и другие факторы, но первопричина заболевания несомненно связана с амилоидными пептидами. По его мнению, введение новой вакцины может стать ключевым элементом в ликвидации симптомов альцгеймеровского слабоумия, будь оно частично вызвано даже генетическими, или какими-либо другими факторами. Следующим шагом, как считают канадские исследователи, должны стать предварительные испытания, проводимые фармацевтическими фирмами, которые должны показать безопасность новой вакцины, после чего можно будет приступить к более широким экспериментам по уточнению ее терапевтической эффективности. Клинические испытания на людях могут начаться в течение ближайших нескольких месяцев. Британская альцгеймеровская ассоциация в Лондоне дала высокую оценку канадскому исследованию. "Если результаты, полученные на животных, полностью подтвердятся на людях, - сказал представитель Ассоциации, -то это будет означать серьезную возможность лечения и даже предотвращения миллионов случаев старческого слабоумия". Медицинские новости. Евгений Муслин: Медики-исследователи Вашингтонского университета под руководством доктора Даниэла Гольдберга разрабатывают сейчас метод, позволяющий предотвратить распространение малярийной инфекции в организме человека, укушенного инфицированным малярийным комаром. Ученые считают возможным как бы поймать инфекционные малярийные частички в ловушку и удерживать их до тех пор, пока они распадутся и перестанут представлять собой опасность. Этого можно добиться, считают исследователи, предотвратив выплескивание этих частичек из защитной оболочки. А для этого нужно блокировать энзим - протеазу. Сейчас от малярии во всем мире страдают примерно 500 миллионов человек, и 2 миллиона детей ежегодно умирают от этой болезни. Малярийные паразиты - одноклеточные плазмодии, сначала инфицируют красные кровяные шарики. Проникнув в такой шарик, они закутываются в особую защитную оболочку, так называемую паразитофорную вакуольную мембрану и начинают в ней размножаться. Через некоторое время оболочка лопается, и паразиты попадают в кровеносную систему. Доктор Гольдберг и его коллеги пробовали воздействовать на культуры инфицированных кровяных шариков особым препаратом, так называемым Е 64, и убедились, что этот препарат, блокируя действие некоторых энзимов, противодействует разрушению оболочки, сдерживающей распространение малярийных плазмодиев. Однако, при понижении концентрации Е 64 паразиты вновь угрожают заражением организму. Надежная изоляция паразитов - считает доктор Гольдберг, принципиально вполне достижима, но для этого необходимы некоторые дополнительные исследования. Работа доктора Гольдберга и его коллег опубликована в Трудах Американской Национальный Академии Наук. Сейчас 90 процентов смертей от малярии приходится на Африку, причем две трети жертв - это дети. Малярия - сегодня самая распространенная тропическая болезнь, и в охватываемых ей зонах проживает более 40 процентов человечества. Гавайские исследователи пришли к выводу, что систематическое потребление соевых продуктов в подростковом возрасте на 50 процентов снижает в будущем у взрослых женщин опасность заболеть раком груди. Связь между соевыми продуктами и профилактикой рака медики отмечали уже давно, но в данном случае эксперименты впервые были начаты еще у подростков. Дело в том, что соя содержит много изофлавонов, которых почти нет в других растениях, а женщины с высоким содержанием этих веществ в организме очень редко болеют раком молочной железы. Исследование, о котором идет речь, было обнародовано в середине декабря в Гонолулу, на Международном химическом конгрессе. Руководитель исследования профессор Адриан Франке подчеркнул, что диета - это, видимо, не единственный фактор, играющий защитную роль. Так, у японок, проживающих в Японии, риск рака груди исключительно мал, и он остается почти таким же ничтожным в случае переезда в Америку. Для их же детей риск увеличивается и сравнивается с показателями остального американского населения, а для их внучек он еще выше. Пока еще неизвестно, в чем тут дело - отметил профессор Франке. По его мнению, причина в сочетании диеты с характером трудовой деятельности и с другими психо-социальными факторами. Сегодня медики во всем мире насчитывают уже 30 рождений детей с использованием замороженной мужской спермы, либо замороженных женских яйцеклеток. Такая техника помогает бороться с бесплодием. Но вот примерно месяц назад в Сингапуре, в Томсоновском медицинском центре, впервые родились близнецы, для которых медики использовали, так сказать, полностью замороженное сырье - и замороженную сперму, и замороженные яйцеклетки. Как заявил на пресс-конференции доктор Ченг Ли Чанг, разработавший соответствующую методику, теперь врачи получили возможность помогать семьям, в которых оба супруга страдают от проблем, чреватых бесплодием. В данном случае, как пояснил доктор Ченг, в сперме отца почти не было сперматозоидов, а у матери овуляция, то есть, выход яйцеклеток в полость тела, происходила только под воздействием гормональных лекарств. Поэтому врачам пришлось сначала извлечь порцию спермы из яичек мужа, после чего в результате четырехчасовых усилий им удалось обнаружить в ней всего 8 пригодных для использования сперматозоидов, которые и были заморожены впрок. Затем у жены были извлечены и также заморожены несколько женских яйцеклеток. После оттаивания и оплодотворения в пробирке зародыши были имплантированы будущей матери, которая и родила близнецов. Вся описанная процедура заняла 16 месяцев и стоила супругам около 12 тысяч долларов. Применяемая техника пока исключительно сложна и необходимы дополнительные исследования, прежде, чем она получит более широкое клиническое применение. Основная сложность связана с тем, что женские яйцеклетки, в отличие от мужской спермы, очень трудно замораживать, так как они продолжают свое развитие, а содержащийся в них генетический материал весьма чувствителен к внешним воздействиям и может быть легко поврежден. В 1827-м году один молодой немецкий дирижер отправился в Вену проведать умирающего Бетховена и на другой день после смерти великого композитора отрезал у него небольшой пучок волос, чтобы сохранить их на память. А в октябре 2000-го года волоски из этого пучка были помещены в электронный ускоритель, синхротрон Аргоннской национальной лаборатории, чтобы подвернуться тщательному химическому анализу. Анализ показал исключительно высокое содержание свинца, чем видимо и объясняются пожизненные страдания Бетховена из-за прогрессирующего ухудшения слуха, его постоянно беспокойное состояние и сама преждевременная смерть. Проводили анализ американские физики Кен Кемнер, Дерек Манчини и Франческо Де-Карло, разрабатывавшие новые более чувствительные методы рентгеновского исследования с помощью мощных источников фотоновых пучков. В частности, они сравнивали данные анализа бетховеновских волос с данными, получаемыми при аналогичном анализе волос с известным содержанием свинца. Оказалось, что содержание свинца у Бетховена примерно в 100 раз превышало нормальный уровень. Соответственно он страдал от постоянных желудочных болей, повышенной раздражительности и тяжелых депрессий - все это известные сегодня симптомы свинцового отравления. Сейчас физики проводят в Аргоннской национальной лаборатории дополнительные исследования, надеясь определить источники бетховеновского свинцового отравления. Возможно, свинец попадал в его организм из минеральной воды, которую он в изобилии пил на водных курортах, где часто лечился.ю или из посуды для приготовления и хранения пищи, или, наконец, из вин, хранившихся в кувшинах с внутренней оболочкой из свинца, как это было принято в Европе в начале XIX века. В сотрудничестве с медиками из Исследовательского института здравоохранения в Нэпервилле - штат Иллинойс, аргоннские физики пытались найти в бетховеновских волосах ртуть, поскольку ртутные препараты использовались в те времена для лечения сифилиса, от которого, по мнению некоторых исследователей, страдал композитор, и искали следы наркотиков. Но ни ртути, ни наркотиков найти не удалось - Бетховен, видимо, избегал опиумного обезболивания даже во время своего долгого и мучительного умирания, чтобы сохранить полную ясность духа для музыки, над которой он продолжал работать до своего последнего дня.www.svoboda.org Вирус, убивающий младенцев. Что такое РСВ-инфекция | Здоровье ребенка | Здоровье
Необычная простудаРеспираторно-синцитиальная инфекция, несмотря на малознакомое название, встречается достаточно часто. Ею могут переболеть и дети, и взрослые во время сезона простуд – то есть с октября по май – наравне с другими вирусными инфекциями: ОРВИ, парагриппом, гриппом, аденовирусной… Но если клинические проявления гриппа, например, – высокая температура и поражение слизистой оболочки верхних дыхательных путей, то при РСВ происходит поражение нижних отделов с частым развитием бронхита, бронхиолита и пневмонией у детей первых двух лет жизни. В США ежегодно регистрируется 125 тысяч госпитализаций по поводу РСВ. В России статистики нет, но, учитывая, что у нас населения в два раза меньше, можно предположить 50–60 тысяч ежегодных случаев заболевания РСВ. Погибают от РСВ 250 тысяч детей в мире ежегодно.Бронхиальное дерево в этом возрасте еще не развито, просвет бронхов небольшой. Под воздействием РС-вируса происходит отек слизистой оболочки бронхов, вырабатывается избыточное количество густой мокроты, которая скапливается и перекрывает просвет. Если взрослый человек или ребенок постарше могут откашляться, то совсем маленьким детям это не под силу из-за особенностей анатомического строения дыхательных путей. У малыша развивается дыхательная недостаточность – учащается дыхание, кожа становится бледной или с синевой. Врачи в этом случае ставят диагноз «бронхиолит» или «обструктивный бронхит». Иногда дыхательная недостаточность настолько тяжелая, что требуется проведение искусственной вентиляции легких. В результате эта нестрашная для взрослых инфекция настолько тяжело протекает у малышей, что, как правило, их приходится госпитализировать. Кто болеет чащеПо поводу РСВ ходит немало слухов. Один из них – что мальчики болеют чаще девочек. Да, это так, но этот факт не имеет никакого значения для профилактики и лечения заболевания. Другой миф – что этой болезни подвержены дети из семей с социально низким статусом. На самом деле инфицирование не зависит от уровня достатка семьи. А вот что РСВ‑инфекция чаще диагностируется в многодетных семьях – правда. Инфекция всегда там, где много контактов между детьми. Собственно РСВ может подхватить и единственный ребенок в семье, которого регулярно водят в садик, развивающие кружки, на детские спектакли. Угроза жизниДля некоторых групп детей РС-инфекция может угрожать жизни. Это в первую очередь дети первых двух лет, особенно недоношенные, рожденные раньше 32‑й недели беременности, у которых наблюдается незрелость дыхательных путей и легких. Также в группу риска входят дети с кардиомиопатиями, врожденными пороками сердца, с избыточным кровотоком в легких или с пороками сердца, сопровождающимися синюшностью (цианозом) кожи. Многие специалисты относят к группе риска детей с синдромом Дауна, врожденными аномалиями легких, нейромышечной патологией. Всем этим ребятишкам для профилактики РС-инфекции необходима сезонная иммунизация. Она пассивная, то есть вводится не ослабленный или убитый возбудитель, как при других прививках, а уже готовые антитела, которые и будут защищать организм от РС-вируса. Использование антител к РС-вирусу в качестве средства профилактики заболевания за многие годы доказало свою эффективность. Но к сожалению, эта вакцина не входит в национальный календарь прививок, поэтому каждый регион прививает своих детей в силу возможностей за счет местного бюджета. По сути, профилактика РС‑инфекции является новой технологией для отечественного здравоохранения и требует поиска дополнительных путей финансирования. Потому что для детей группы риска это единственно возможная защита. Хотя, безусловно, в вопросах профилактики не следует пренебрегать и соблюдением банальных мер предосторожности: ограничить контакты ребенка в сезон простуд, выполнять правила личной гигиены. Последнее касается всех членов семьи. Смотрите также: Парвовирусная инфекция: малоизвестный детский вирус → www.aif.ru Респираторный синцитиальный вирусРеспираторно-синцитиальный вирус и иммунитет человека. Иммунный ответ при РС-вирусной инфекции.В пато- и иммуногенезе при респираторно-синцитиальных (PC) заразах человека и крупного скота имеется громадное сходство. Заболевание протекает наиболее не легко у детей и телят в возрасте 1—3 мес на фоне материнских антител. Инфицирование сопровождается возникновением в респираторном тракте противовирусных антител, которыми владел к IgM, IgA и IgG.
Ускоренная их продукция отмечается при повторном заражении либо иммунизации. На поверхности эпителиальных клеток верхних дыхательных путей при РС-инфекции идентифицированы антитела всех изотипов, но в основном IgA. Но не распознано корреляции между уровнем вирусспецифических IgA и приживляемостью вируса в носоглотке. Ключевая роль клеточного иммунитета как фактора защиты от респираторно-синцитиальной инфекции была доказана экспериментально. Перенос мышиных донорских иммунных Т-лимфоцитов зараженным мышам с нарушенным клеточным иммунитетом давал предупреждение развитие инфекции. Вирусспецифические Тц-лимфоциты разрушают клетки-мишени, инфицированные гомологичным и гетерологичным (А и В) вариантами РС-вируса. Значительный вклад в предотвращение болезни и выздоровление от PC-инфекции вносят клеточные механизмы, опосредованные специфическими антителами. Инфицированные вирусом моноциты лизируются лимфоцитами в присутствии иммунной сыворотки. Лишь живой PC-вирус и рекомбинантный вирус вакцины, экспрессиру-ющий белок F PC-вируса, индуцировали образование вирусспецифических Т-лимфоцитов у мышей. Инактивированный PC-вирус либо его гликопротеины F и G таким действием не владели. Главным антигеном-мишенью для Тц-лимфоцитов являлся F-белок и в меньшей степени белок G РС-вируса. В молозиве рожениц и молоке кормящих иммунных матерей IgA были адресованы по большей части к F белку вируса. Полученные информацию о серьёзной роли Т-лимфоцитов в элиминации вируса из организма, говорят о том, что разрабатываемые вакцины с целью достижения надежной защиты должны индуцировать у привитых индивидумов формирование Т-клеточного иммунитета. Более того, оказалось, что нуклеопротеид PC-вируса распознается лучше Т-клетками-эффекторами, чем поверхностный G-гликопротеин. Эти данные в целом согласуются с данными, взятыми в следствии изучений механизма антигенного распознавания при гриппозной инфекции, в то время, когда внутренние вирусные антигены являются основными структурами, распознаваемыми Тц-лимфоцитами. При PC-инфекции имеет место антителозависимая клеточная цитотоксичность, в которой основной мишенью есть F-белок вируса, экспрессируемый на поверхности инфицированных клеток. Эта иммунологическая реакция занимает важное место в защите организма и его выздоровлении от РС-инфекции. Вирусные инфекции различаются между собой выраженностью гуморального и клеточного иммунитета, участием параиммунных механизмов защиты. При острых вирусных заразах возбудитель достаточно быстро исчезает из организма. При большинстве вирусных заболеваний господствует гуморальный иммунитет. Роль клеточного иммунитета велика при ряде зараз, вызываемых оболочечными вирусами (оспа, герпес, ретровирусные инфекции и др.), особенно в то время, когда они передаются из клетки в клетку. Вируснейтрализующие антитела не найдены при африканской чуме свиней и алеутской болезни норок. Коронавирусы перитонита кошек и инфекционного бронхита кур смогут длительно персистировать при наличии громадного количества противовирусных антител. Многие вирусные инфекции. поражающие органы дыхания и пищеварения, относятся к локальным заразам, потому, что клетки, выстилающие слизистые оболочки этих органов, являются не только входными воротами инфекции, но и основным местом репликации вирусов. В этом случае основная роль в защите принадлежит гуморальным и клеточным факторам местного иммунитета. Для защиты организма от вирусов, вызывающих заболевание методом переноса возбудителя через кровоток к органам-мишеням, основное значение имеют сывороточные нейтрализующие антитела и системный клеточно-опосредованный иммунитет. Как мы знаем, что возбудители большинства вирусных зараз попадают в организм через слизистые оболочки, исходя из этого изучение механизмов местного иммунитета получает особенную актуальность.  Аппликацию живых вакцин на слизистые оболочки при ряде зараз (полиомиелит, трансмиссивный гастроэнтерит, ротавирусная заболевание свиней и др.) возможно разглядывать как наиболее естественный контакт организма с вирусом, закрепившийся эволюционно и обусловливающий стремительное развитие местной и общей защитных реакций. Потому, что иммунный статус слизистых оболочек определяется главным образом локальным образованием специфических антител и Тц-лимфоцитов, разработка и совершенствование средств специфической профилактики многих болезней (особенно желудочно-кишечных и респираторных) должны вестись с учетом этих изюминок. Данное требование полностью относится и к лактогенному иммунитету новорожденных. Иммунизация животных через слизистые покровы живыми вакцинами во многих случаях оказалась более действенной если сравнивать с парентеральной иммунизацией. Исходя из этого для выраженного местного иммунитета нужно разрабатывать в основном живые вакцины и соответствующие методы их применения. Инактивированные вакцины для местной иммунизации фактически не созданы. Изучения по созданию адъювантов для таких вакцин лишь начинаются. Создание выраженного местного иммунитета при парентеральной иммунизации теоретически быть может, но для этого, по-видимому, потребуется создание инактивированных препаратов с высокой антигенной активностью. Учитывая взаимосвязь механизмов системного и местного иммунитета, перспективным представляется сочетание местной и парентеральной иммунизации, и комбинированное применение живых и инактивированных вакцин.
Последовательное использование живой. а после этого инактивированной вакцины против полиомиелита было рекомендовано в Соединенных Штатах вместо трёхкратного введения живой вакцины. Живая вакцина весьма редко приводит к паралитическому полиомиелиту у вакцинированных и контактировавших с ними людей. Инактивированную вакцину применяли для предотвращения редких случаев инфицирования центральной нервной системы, вызванных живой вакциной. Живую вакцину применяли для увеличения иммунитета слизистой оболочке желудочно-кишечного тракта и создания популяционного иммунитета. На сегодня в Соединенных Штатах рекомендовано применять лишь инактивированную вакцину. Одновременное интаназальное использование живой вакцины и парентеральное введение инактивированной вакцины применяют при иммунизации людей против гриппа А. Первая стимулирует образование иммунитета слизистой оболочке респираторного тракта, вторая — системный иммунитет.  Иммунизация живой вакциной с последующей бустеризацией инактивированной вакциной оказалась нужной против Венесуэльского энцефалита. Репликативно-дефектная вакцина против вируса несложного герпеса 2 (HSV-2) при комбинированном введении на слизистую и парентерально создавала хорошую защиту. Сочетанное применение разных вакцинных препаратов, схем и способов их применения может содействовать стимуляции многих компонентов иммунной системы, тем самым повышая защитный эффект. При профилактике массовых вирусных болезней КРС (ИРТ, ВД и ПГ-3) прекрасные результаты взяты в случае сочетанного применения живых, а после этого инаткивированных комбинированных вакцин. Иммунизация против вирусов в ранний период жизни воображает особую проблему. Одной из обстоятельств есть недостаточная возрастная иммунокомпетентность организма в ранний период жизни. Иммунная система в поздний эмбриональный и начальный неонатальный период ещё не сформирована и не закончена полная структурная организация вторичных иммунных органов.  Другой обстоятельством есть подавление иммунного ответа на вакцинацию нейтрализующими материнскими антителами. Подавляющего действия материнских антител в случае с живыми вакцинами возможно избежать, используя их орально либо на слизистые оболочки. К примеру, вакцинный штамм полиовируса по окончании орального введения вакцины хорошо размножается в кишечнике, приводя к выраженному иммунитету. tpk-eti.ru |
г.Самара, ул. Димитрова 131 [email protected] |
 |



 Наш эксперт – заведующий отделением аритмологии Научно-исследовательского клинического института педиатрии ГБОУ ВПО «Российский национальный исследовательский университет имени Н. Н. Пирогова» Минздрава России, вице-президент Ассоциации детских кардиологов России Игорь Ковалев.
Наш эксперт – заведующий отделением аритмологии Научно-исследовательского клинического института педиатрии ГБОУ ВПО «Российский национальный исследовательский университет имени Н. Н. Пирогова» Минздрава России, вице-президент Ассоциации детских кардиологов России Игорь Ковалев.








