|
|
||||||||||
|
Антибиотики для животных. Ветеринария совместимость антибиотиковАнтибиотики для животных - ВетеринарияАнтибиотики для животных — наиболее часто назначаемый класс препаратов в ветеринарной медицине. По возможности их выбор должен основываться на результатах посева культуры и выявления чувствительности к ним. При выборе препарата надо обращать внимание на особые характеристики желудочно-кишечного тракта и анатомии животных. К безопасным антибиотикам для животных всех видов относят энрофлоксацин, ципрофлоксацин и комбинацию триметоприм/сульфаниламид. Побочные эффекты от применения антибиотиков у животных Токсичность, вызываемая антибиотиками у животных может быть результатом прямого или косвенного воздействия лекарственного средства. Как и у кроликов, у грызунов наиболее важный механизм токсичности антибиотиков развивается вследствие нарушения функции нормальной кишечной флоры. Виды животных с преимущественно грамположительной кишечной флорой, например шиншиллы, морские свинки и хомяки, подвергаются более высокому риску. Мыши, песчанки и крысы менее восприимчивы к антибиотико-ассоциированной энтеротоксемии. Хотя при пероральном введении антибиотиков для животных наблюдается значительная частота возникновения осложнений, токсические эффекты возможны также при парентеральном применении препаратов, которые выделяются в активной форме в желчь. У восприимчивых видов животных антибиотики со спектром влияния, ограниченным грамположительными бактериями, нарушают нормальную кишечную флору и создают условия для активного размножения грамотрицательных бактерий и клостридий. К наиболее распространенным видам бактерий. которые размножаются и вызывают нарушения, относят Clostridium difficile, С. spiroforme, С. perfringens и Escherichia coli, заболеваемость ими зависит от вида животного и используемого антибиотика. Размножение этих бактерий приводит к изменению pH в просвете кишечника и увеличению производства летучих жирных кислот. Последние препятствуют дальнейшему росту нормальной кишечной флоры и создают условия для выработки токсинов Clostridium spp. Эти токсины уничтожают эпителий слизистой оболочки, вызывая воспаление, диарею и возможные системные заболевания. Клостридиальная энтеротоксемия может сформироваться уже в течение 3 дней после введения одной дозы антибиотика.
Доза антибиотиков для животных
К классам антибиотиков для животных, прием которых может вызвать смерть ( в частности хомяков, морских свинок), относят бета-лактамы (амоксициллин, ампициллин и пенициллин), макролиды (эритромицин, тилозин, спирамицин), линкозамиды (клиндамицин, линкомицин) и специфические антибиотики бацитрацин, ванкомицин. Тетрациклины (тетрациклин, хлортетрациклин, окситетрациклин) и цефалоспорины тоже могут приводить к развитию энтеротоксемии у этих видов. Хлорамфеникол, как правило, является «безопасным» антибиотиком для грызунов, при введении в высоких дозах (300 мг/кг) может вызвать энтеротоксемию у хомяков. Лечение антибиотик-ассоциированной энтеротоксемии включает в себя поддерживающую терапию, подавление аномального роста бактерий (антибиотиками) и восстановление кишечной флоры (пробиотиками или скармливанием свежих фекалий от здоровых животных). Использование колестирамина, ионообменной смолы помогает абсорбировать токсины. Этим самым облегчается действие клинических признаков у кроликов, и, похоже, подобный эффект отмечается и у грызунов. Чтобы избежать возникновения антибиотик-ассоциированной энтеротоксемии, необходимо предварительно тщательно выбирать антибиотик для животных. Несмотря на то, что морские свинки, шиншиллы и хомяки более восприимчивы к ним, антибиотик-ассоциированная диарея может развиться у всех видов животных. Об этом осложнении должны знать владельцы, они должны наблюдать за домашними животными, прекратить дачу антибиотиков в случае развития диареи и все время лечения. Даже при использовании «безопасных» антибиотиков для животных рекомендуют использовать пробиотики Lactobacillus во время лечения и в течение 5-7 дней после прекращения антибиотикотерапии. Антибиотики (и некоторые сопутствующие лекарственные средства) могут также оказать прямое токсическое воздействие на животных. Например, стрептомицин и прокаин токсичны для мышей, хомяков и морских свинок, нитрофурантоин вызывает невропатологию у крыс, а песчанки не переносят стрептомицина и дигидрострептомицина. Есть также отдельные сообщения о токсичности метронидазола при лечении у шиншилл, в результате чего развивается заболевание вестибулярного аппарата или печеночная недостаточность. Морские свинки и шиншиллы весьма восприимчивы к ототоксическому эффекту хлорамфеникола и аминогликозидов при применении их в дозах, превышающих рекомендуемые.
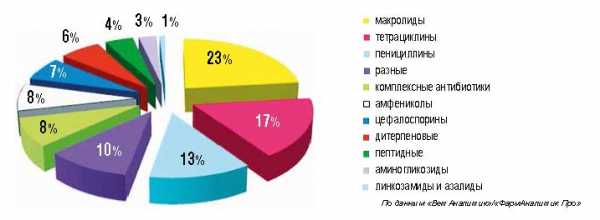
Полезно:surgeryzone.net Обзор ветеринарных антибиотиков группы макролидов15.01.2018Обзор ветеринарных антибиотиков группы макролидовРоссийский рынок противобактериальных средств — второй по величине в ветеринарной фармацевтике. Антибиотические лекарственные средства занимают его основной сектор. На сегодняшний день в ветеринарии применяется широкий диапазон лекарственных соединений как для лечения, так и для профилактики заболеваний и стимулирования роста животных. Отсутствие жесткого регулирования оборота антибиотиков в лечебных целях обеспечивает высокий уровень предложения и конкуренции. Импортозамещение: перспективы и реальность Несмотря на экономический кризис, интерес российских животноводов и птицеводов к зарубежной продукции растёт. По данным «ВетАналитик»/«ФармАналитик Про», в 2016 г. импорт антибиотиков составил 82,2 млн USD (7,65 млн упаковок), что на 2% в стоимостном и на 4,6% в натуральном выражении больше, чем в 2015 г. Всего с 2011 по 2016 гг. рынок импортных препаратов вырос на 6% в стоимостном и на 25% — в натуральном выражении. По данным Frost&Sullivan, более 50% кормовых и ветеринарных антибиотиков приходится на зарубежные препараты. По данным «ВетАналитик»/«ФармАналитик Про», более 86% продающихся в свободном обращении антибиотиков (без учёта госзакупок) производится за рубежом. Антибиотические препараты для животных включают в себя следующие группы: азолиды, аминогликозиды, амфениколы, дитерпеновые, линкозамиды, комплексные антибиотики, макролиды, пенициллины, пептидные, разные (бацитрацин цинка, флавофосфолипол, авиламицин), тетрациклины, цефалоспорины. В стоимостном выражении наибольшую долю рынка ветеринарных антибиотиков занимают препараты на основе макролидов, тетрациклинов, пенициллинов. По статистическим данным шестого отчета ESVAC (2016), тетрациклины и пенициллины являются наиболее используемыми антибиотиками и составляют 33,4 и 25,5% соответственно. Третье место занимают сульфаниламины и триметоприм (12,6%), четвертое — макролиды (7,5%).
Импорт антибиотиков для животных в 2016 г. в стоимостном выражении (USD) По данным «ВетАналитик»/«ФармАналитик Про» В настоящее время в России есть собственные производители антибиотиков, способные выпускать препараты в объеме, необходимом для импортозамещения. По данным «ВетАналитик»/«ФармАналитик Про», импорт субстанций антибиотиков в 2015–2016 гг. вырос на 36% в стоимостном и на 52% — в натуральном выражении (тоннах), что говорит об ослаблении зависимости от ряда зарубежных препаратов в последние годы. Развитие отечественного рынка в основном идет по пути создания дженериков, тогда как зарубежные компании активно внедряют инновации. Ряд отечественных компаний успешно поставляют продукцию в другие страны и уже сертифицированы по системе GMP, однако на своем рынке они находятся в среде с высокой конкуренцией и потому вынуждены импортировать значительную часть продукции. Рыночная экономика диктует условия, которые на данном этапе развития российским производителям сложно выполнить. Очевидно, что российским предприятиям необходимы значительные вложения в область науки и синтеза новых молекул, а также в развитие собственного производства субстанций дженериков, и это требует поддержки государства в форме дотаций и налоговых льгот. Разрешить нельзя, отменить В ноябре 2017 г. совместно с ВОЗ и Всемирной организацией охраны здоровья животных (МЭБ) была проведена всемирная Неделя правильного использования антибиотиков. В рамках мероприятия экспертами был сделан ряд заявлений. Во-первых, необходимо, чтобы противобактериальные препараты ответственно использовались во всех отраслях и применялись только тогда, когда это действительно нужно. Так как в животноводстве противомикробные препараты применяются в значительных объемах, очень важно сосредоточить внимание на совершенствовании методов санитарно-эпидемического контроля, а также на повышении иммунитета скота. В распространении резистентной микрофлоры огромную роль играет ненадлежащая очистка сточных вод. Во-вторых, полное исключение противомикробных препаратов из ветеринарной медицины не является решением проблемы. Эксперты предупреждают, что это создаст вакуум, в котором инфекционные заболевания могут стремительно распространяться, пагубно сказываясь на животноводстве и растениеводстве и угрожая общественному здоровью. Согласно концепции МЭБ, применение противомикробных препаратов в нелечебных целях, например в качестве стимуляторов роста, должно быть минимизировано. При этом отношение к кормовым антибиотикам в развитых странах двоякое. В США кормовые антибиотики были запрещены только в 2017 г., тогда как в странах ЕС полный запрет действует уже более 10 лет (при этом применение препарата Тилозина в кормовых целях было запрещено в ЕС еще в 1999 г.). По данным компании Alltech, около 50 стран либо уже запретили, либо находятся в процессе реализации запрета на использование антибиотиков для стимулирования роста животных. В России кормовые антибиотики в настоящее время не регистрируются. По мнению Эйдан Коннолли, вице-президента по инновациям компании Alltech, «при снижении потребления антибиотиков ожидаемые результаты могут оказаться не лучшими. Фермы, которые ввели соответствующие изменения, сообщают, что продуктивность снижается не сразу, а в течение долгого времени. Например, при выращивании птицы в течение трех лет после исключения антибиотиков продуктивность не менялась, но на четвертый год показатели ухудшились. Аналогичные тенденции зафиксированы и у других видов животных. В таких случаях трудно обратить вспять устоявшиеся тенденции. Поиск естественной замены антибиотика — вот единственная альтернатива». Потребление антибиотиков можно значительно сократить, включая в рационы подкислители и пробиотики. Причиной возникновения резистентности бактерий к антибиотикам могут стать поддельные и некачественные препараты, последствия применения которых предугадать невозможно. Важной профилактической мерой является определение возбудителей, циркулирующих в каждом конкретном хозяйстве, и их чувствительности к антибиотикам. В отношении выбора химиотерапевтических препаратов нужно соблюдать рекомендуемую дозу и кратность применения. В появлении опасных штаммов бактерий часто виновны сотрудники хозяйств, нарушающие правила зоогигиены и кормления животных. Устойчивость бактерий к тем или иным химическим веществам является типичной приспособительной реакцией и может возникнуть при любом подавляющем воздействии условий среды на популяцию микроорганизмов. Нерациональное применение в кормлении оксида цинка, сульфата меди, использование питьевой воды с повышенной жесткостью также могут привести к мутациям условно-патогенных и патогенных бактерий. К сожалению, на сегодняшний день не существует альтернативы антибиотикам в лечении инфекционных болезней, поэтому важно установить единые для всех стран принципы рационального использования антибиотиков в медицине, в том числе ветеринарной. Следуя рекомендациям «Европейского стратегического плана действий по проблеме устойчивости к антибиотикам», утвержденного на 61-й сессии Европейского регионального комитета ВОЗ (документ EUR/RC61/14), необходимо создание интегрированных систем надзора за устойчивостью к антибиотикам (в отношении человека, животных и пищевых продуктов), а также государственного контроля за использованием антибиотиков у сельскохозяйственных животных. Такой подход является оптимальным в свете современных представлений об эпидемиологии инфекционных заболеваний. Механизмы государственного регулирования оборота антибиотиков широко применяются в развитых странах. Например, в Швеции, Дании, Норвегии, Нидерландах, Канаде, США терапевтические антибиотики применяются согласно рецепту для каждого конкретного животного, статистика об их использовании поступает в органы власти. Макролиды — ведущий сегмент рынка антибиотиков Антибиотики группы макролидов применяются с лечебными и лечебно-профилактическими целями. Некоторые противобактериальные средства на основе макролидов
Лекарственные препараты на основе макролидов выпускаются в форме инъекционных и оральных растворов, таблеток, в виде гранул и порошков для премиксов. Также потребителям доступны лекарства в форме ветеринарных субстанций. Макролиды хорошо накапливаются в тканях, обладают бактериостатическим эффектом, воздействуют на рибосомальный аппарат бактериальных клеток. Среди них есть препараты как природного происхождения, так и полусинтетические. Одно из основных мест по объему производства, широте показаний и эффективности применения занимают антибиотик тилозин (устойчивое однокислотное основание) и его соли — тилозин тартрат и тилозин фосфат. Тилозин разработан для сугубо ветеринарного применения и впервые выделен из культуры гриба в 1955 г. Препараты тилозина и его солей активны в отношении большинства патогенных микроорганизмов (Staphylococcus spp., Streptococcus Spp., Clostridium spp., Pasterella spp., Mycopasma spp., Brachyspira hyodysenteriae, Chlamydia spp., Spirocheta spp.), наиболее часто применяются для лечения болезней свиней (дизентерии, гастроэнтероколиты), птицы (при респираторном микоплазмозе, инфекционном синусите, колибактериозе, пастререллезе, аэросаккулите и некоторых других заболеваниях). Эти антибиотики вносятся с кормом или водой (в зависимости от рекомендаций производителя), а также инъекционно. Из организма эти активные вещества выводятся преимущественно в неизменном виде и частично в виде метаболитов с мочой и фекалиями, но способны накапливаться в яйцах. При внутримышечном применении препараты тилозина резорбируются быстро и достигают максимальных концентраций в тканях уже через 1 час после введения. Терапевтический уровень антибиотика сохраняется в организме в течение 20–24 часов. Выводится из организма преимущественно с мочой и желчным секретом, у лактирующих животных — и с молоком, у самцов — со спермой. По степени воздействия на организм препараты на основе тилозина относятся к малоопасным веществам. Они не применяются курам-несушкам, а также вместе с другими антибиотиками (в том числе с пенициллином, цефалоспорином, линкомицином, другими макролидами). При назначении антибиотиков на основе тилозина необходимо строго соблюдать установленные дозы добавок и период их применения, так как существует риск возникновения резистентности патогенных микроорганизмов. Механизм возникновения устойчивости патогенов к макролидам различен: это может быть мутация одного гена или сразу нескольких, в том числе способных инактивировать и другие антибиотики. Например, может возникнуть резистентность бактерий не только к макролидам, но и к пенициллинам, цефалоспоринам, аминогликозидам. Тилмикозин — антибиотик группы макролидов, обладающий широким спектром бактериального действия в отношении Staphylococcus spp., Streptococcus Spp., Pasterella spp., Haemophilus spp., Mycopasma spp., а также Corynebacterium pyogenes и Actinomyces pyogenes. Назначается телятам, поросятам, цыплятам-бройлерам и племенной птице при пастереллезе, актиномикозе, микоплазмозе. Запрещено применение курам-несушкам, а также взрослым жвачным животным. Тулатромицин — полусинтетический антибиотик подкласса триамелидов, оказывающий бактериостатическое действие на грамположительные (Streptococcus spp., Staphylococcus spp. (включая штаммы, продуцирующие бета-лактамазы), Corynebacterium pyogenes и др.) и грамотрицательные бактерии (Pasteurella haemolytica, Pasteurella multocida, Haemophilus somnus), а также на Mycoplasma hyopneumoniae, Mycoplasma bovis, Actinobacillus pleuropneumoniae, которые вызывают заболевания дыхательных путей у крупного рогатого скота и свиней. Тулатромицин быстро резорбцируется и медленно выводится из организма. Максимальная концентрация антибиотика в крови регистрируется уже через 30 минут после введения. Наиболее высокая концентрация препарата достигается в легких, печени, почках. Антибиотик применяют крупному рогатому скоту и свиньям для профилактики и лечения бактериальных инфекций органов дыхания (пневмонии, бронхопневмонии) и при других инфекционных заболеваниях, вызываемых микроорганизмами, чувствительными к тулатромицину. Препарат не следует смешивать в одном шприце с другими лекарственными средствами и не рекомендуется назначать одновременно с другими макролидами или линкозамидами. Убой свиней на мясо разрешается не ранее чем через 30 суток, а мясо в месте введения препарата можно использовать не ранее чем через 68 суток после последнего применения препарата. Убой крупного рогатого скота на мясо разрешается не ранее чем через 30 суток. Молоко в пищу людям следует использовать не ранее чем через 60 суток после применения препарата. Тилвалозина тартрат активен в отношении грамположительных и некоторых грамотрицательных микроорганизмов, в том числе Mycoplasma hiopneumonia, Brachyspira hyodysenteriae, Lawsonia intracellularis, Brachyspira hyodysenteriae. При оральном применении тилвалозина тартрат всасывается в желудочно-кишечном тракте и проникает в большинство органов и тканей. Терапевтическая концентрация антибиотика в крови животных достигается через 1–3 часа и сохраняется в течение 15–18 часов. Тилвалозин выводится из организма животных преимущественно в неизменном виде и в виде метаболитов, в основном с фекалиями и в меньших количествах — с мочой. Спирамицин — 16-членный макролид. Благодаря особой структуре этот антибиотик обеспечивает более стойкое связывание с рибосомами бактерий, чем 14-членные макролиды, поэтому обеспечивает более длительное действие и создает высокую концентрацию в тканях. По некоторым данным, микрофлора, устойчивая к 14-членным макролидам, сохраняет чувствительность к спирамицину. Антибиотик активно применяется как ветеринарии, так и медицине. Тилдипирозин — первый в мире трехосновной 16-членный макролид. При внутримышечном введении период полувыведения его составляет 4,4 суток. Это вещество способно хорошо накапливаться в легких, плазме и бронхиальной жидкости, сохраняя эффект при лечении респираторных заболеваний свиней до 14 суток. Антибиотик воздействует на Actinobacillus pleuropneumoniae, Pasteurella multocida, Bordetella bronchiseptica, Haemophilus parasuis — возбудителей респираторных заболеваний свиней. На основе тилдипирозина компанией MSD производится препарат Зупрево. Конкурентным преимуществом препарата является однократное применение, а период ожидания по мясу составляет всего 9 дней. Гамитромицин — 15-членный полусинтетический макролид, обладающий бактерицидным и бактериостатическим эффектом. Период полувыведения препарата составляет не менее 2 суток, максимальная концентрация в плазме достигается уже через 30–60 минут. Гамитромицин назначается крупному рогатому скоту и свиньям для профилактики респираторных заболеваний, вызванных Mycoplasma bovis, Mannheimia haemolytica, Pasteurella multocida, Haemophilus parasuis, Bordetella bronchiseptica. На его основе производится препарат Зактран (производитель Merial, с 2017 г. Boehringer Ingelheim). На основе макролидов также производятся комбинированные препараты. Противобактериальный Флоритил производства «Асконт+» — первый препарат, сочетающий макролид и феникол в инъекционной форме, обеспечивающий синергидное действие против грамположительной, грамотрицательной и смешанной микрофлоры. Российский препарат Дизпаркол («Агрофарм») производится на основе левомицитина, метронидазола, тилозина и назначается для лечения колибактериоза и сальмонеллеза поросят и телят, а также дизентерии поросят. Лекарственное средство для лечения эндометритов коров Эндометрамаг-Т (производитель «Мосагроген») производится на основе тилозина тартрата, пропранолола гидрохлорида. Слабой стороной применения тилозина является узкий диапазон рабочей pH среды (от 7,5 до 8,5), что сильно снижает его активность в слабокислой среде кишечника, а плохая проникающая способность затрудняет преодоление полисахаридных пленок на пути к клеткам микоплазмы. Ученые выяснили, что совместное использование фосфомицина с тилозином позволяет повысить терапевтическую эффективность последнего (препарат для птицы Фосбак Плюс Т от «МедпроВет»). В настоящее время в ветеринарную практику российских специалистов внедрено более 40 препаратов на основе макролидов. Среди них есть как оригинальные молекулы, так и дженерики. Производители ветеринарных макролидов: S.P. Veterinaria, Huvepharma, Ceva, Elanco, Interchemie Werken, Phibro, Zoetis, MSD, Livisto, Merial (часть компании Boehringer Ingelheim), а также NITA-FARM, «Ветбиохим», «ВИК – здоровье животных», «АВЗ С-П», «Асконт+», «Мосагроген» и др. Количество показов: 709 Автор: В.Лавренова, маркетолог издательства «Сельскохозяйственные технологи» Источник: "Ценовик" Январь 2018www.tsenovik.ru Совместимость лекарственных средств
Совместимость лекарственных средств
При медикаментозном лечении часто используют сочетания лекарственных средств для усиления действия одного препарата другим, ограничения дозы каждого из них, ослабления побочных эффектов; при полисиндромных проявлениях заболевания — для воздействия на ряд механизмов патогенеза, корригирования возникших сдвигов, облегчения всех имеющихся жалоб; при наличии нескольких заболеваний — для одновременного лечения каждого из них. Поскольку известны побочные эффекты, свойственные тем или другим лечебным препаратам, существует возможность профилактики этих нежелательных последствий лечения путем назначения защитных препаратов: лечение глюкокортикоидами следует проводить под защитой антибиотиков, антацидов, анаболических средств; противомикробные антибиотики ввиду опасности развития дисбактериоза сочетать с нистатином или другими противогрибковыми препаратами. Успехи дифференцированной фармакотерапии все более увеличивают перечень возможных и желательных направлений лечения. Но терапевтическая активность угрожает обернуться полипрагмазией с ее многочисленными опасностями, наиболее очевидной из которых является несовместимость препаратов.
Различают три рода несовместимости лекарственных прописей: физическую (или физико-химическую), химическую и фармакологическую. К числу физических несовместимостей относят те, которые зависят от разной степени растворимости препаратов, коагуляции коллоидных систем и расслоения эмульсий, отсыревания и расплавления порошков, адсорбционных явлений.
Образование осадка при совмещении алкалоидных препаратов (в 1% растворе) с другими лекарственными веществами
Химическая несовместимость возникает в результате реакций, которые происходят при соединении растворов в одном объеме. Они предотвращаются раздельным введением препаратов.
Несовместимые сочетания препаратов
Значительно многообразнее и сложнее варианты фармакологической несовместимости, обусловленной взаимодействием аффектов лекарств при одновременном их применении.
Сведения по поводу физической и химической несовместимости включены в рецептурные справочники, бюллетени, таблицы. Прописи контролируют при оформлении рецептов в аптеках. Тем не менее в повседневной практике из-за недостаточной осведомленности врачей и медицинского персонала нередко допускаются отклонения от утвержденных рекомендаций с отрицательными последствиями для больного.
При одновременном приеме больным нескольких таблеток возможна не только их фармакологическая несовместимость, но и химическое взаимодействие в желудочно-кишечном тракте в условиях, когда пищеварительные соки и иные ингредиенты химуса становятся биологическими катализаторами возникающих реакций.
Фармакологическая несовместимость имеет различные причины и формы. Антагонистическая (или абсолютная) несовместимость возможна в тех случаях, когда препараты имеют разнонаправленное влияние на процессы, протекающие в клетке, ткани, органе или целом организме, и эффект одного подавляется эффектом другого. Этот вид несовместимости с успехом используется при лечении отравлений, когда препарат вводят в качестве антидота: например, атропин при отравлении ингибиторами холинэстеразы, фосфорорганическими веществами, мухомором (мускарин), пилокарпином; наоборот, пилокарпин, прозерин, физостигмин — при отравлении атропином.
Несовместимость возникает и между синергистами в связи с тем, что непропорционально возрастает опасность передозировки или умножения побочного действия. Одновременное назначение β-адреноблокатора, дигоксина и резерпина вызывает брадикардию, нарушения проводимости, угрожает развитием аритмий; введение строфантина на фоне лечения другими препаратами сердечных гликозидов может вызвать асистолию или фибрилляцию желудочков сердца; применение аминогликозидов канамицина, гентамицина, неомицина на фоне стрептомицина приводит к поражению VIII пары черепных нервов, безвозвратной потере слуха, иногда к развитию почечной недостаточности (относительная несовместимость, сходная с эффектом передозировки).
Фармакокинетическая несовместимость возникает в связи с теми изменениями, которые один из препаратов вносит в условия всасывания, выведения или циркуляции в организме другого (других) препарата.
Назначение мочегонных петли нефрона (фуросемид, урегит) отрицательно сказывается на терапии аминогликозидами: быстрее снижается их концентрация в крови и в тканях, возрастает нефротоксический эффект. Наоборот, стрептомицин, нарушая механизм секреции пенициллина канальцевым эпителием, удлиняет сроки его терапевтической концентрации в крови (благоприятное фармакокинетическое потенцирование).
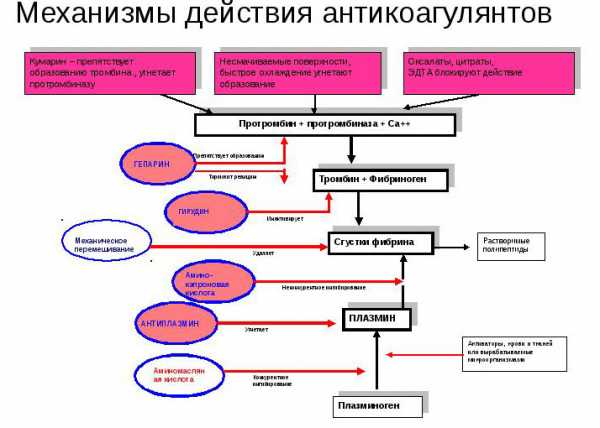
Выделяют также метаболическую (всегда дозозависимую, относительную) несовместимость лекарств, которая изучена на примере сочетанного применения фенобарбитала и антикоагулянтов: фенобарбитал способствует ускоренному метаболизму последних и резкому ослаблений их действия.
В других случаях в основе метаболической несовместимости лежат угнетение процессов разрушения лекарственного вещества, снижение клиренса, повышение концентрации в плазме крови, сопровождающиеся развитием признаков передозировки. Так, ингибиторы моноаминоксидазы (ипразид, ниаламид) тормозят метаболизм катехоламинов, тирамина, серотонина, вызывая гипертензивные реакции.
Классификация антибактериальных средств (по Manten- Wisse)
Большую остроту приобрела проблема сочетанной антибактериальной терапии. Получены, в том числе полусинтетически, десятки тысяч антибиотиков, различающихся по своим лечебным характеристикам. Показания к сочетанной противомикробной терапии определяются многими соображениями: 1.возможностью повышения терапевтической эффективности; 2.расширением спектра антибактериального действия при неуточненном возбудителе; 3.уменьшением побочного действия по сравнению с адекватной монотерапией; 4.снижением опасности возникновения резистентных штаммов микробов.
Однако при применении одновременно двух или нескольких препаратов возможны четыре формы взаимодействия: индифференция, суммарное действие, потенцирование и антагонизм.
Индифференция состоит в том, что один препарат не оказывает отчетливого влияния на антибактериальное действие другого.
Суммарное (или аддитивное) действие имеет место тогда, когда результат является суммой монотерапевтических эффектов. Если степень антибактериальной активности сочетания препаратов оказывается большей, чем суммарное действие компонентов, говорят о потенцировании (или синергизме). Но нередко эффект комплексного применения антибиотиков оказывается меньшим, чем одного из ингредиентов: имеет место антагонизм действия препаратов. Одновременное применение антибиотиков, между которыми возможен антагонизм, является прямой ошибкой врача.
Уже в 50-е годы был сформулирован принцип сочетания антибиотиков в зависимости от типа их действия на возбудителя — бактерицидного или бактериостатического (см. классификацию). При сочетании антибиотиков, оказывающих бактерицидное действие, как правило, достигается эффект синергизма или аддитивное действие. Сочетание бактериостатических антибиотиков ведет к аддитивному действию или индифференции.
Сочетание же бактерицидных антибиотиков с бактериостатическими препаратами чаще всего нежелательно. Летальность от менингококкового сепсиса у детей при попытках единовременного применения пенициллина и левомицетина возрастала по сравнению с результатами, получаемыми при лечении тем или другим из этих препаратов в отдельности.
Если микроорганизм более чувствителен к компоненту с бактериостатическим действием, может появиться синергизм, но когда он чувствителен к бактерицидному действию, как правило, наступает антагонизм, бактериостатический препарат снижает эффективность бактерицидного. И в венерологии, и при лечении острых пневмоний одновременное применение сульфаниламидов и пенициллина сопровождалось неблагоприятными результатами по сравнению с эффектом, полученным при энергичном лечении одними пенициллинами: «обрывающего» действия при применении бактерицидного антибиотика (абортивное течение пневмонии при раннем назначении пенициллина) не наступает.
При моноинфекциях сочетанное лечение антибиотиками редко бывает обоснованным, при смешанных заражениях оно может быть ценным, но только если соблюдаются условия рационального сочетания антибиотиков и учтены все показания и противопоказания.
К настоящему времени установлено, что ни широкий спектр активности антибиотика, ни мегадозы, ни комбинации антибиотиков или последовательная замена одних другими проблемы успешного лечения бактериальных заболеваний не решают, пока за этим скрывается попытка лечить вслепую, методом проб и ошибок. Необходимо точное, прицельное, узконаправленное лечение на основе определения видовой и индивидуальной чувствительности возбудителя к лечебному агенту, надежной и своевременной этиологической диагностики заболевания.
Антибиотики не следует без необходимости совмещать с жаропонижающими, снотворными, глюкокортикоидными препаратами (это противоречит рекомендации применять глюкокортикоиды «под защитой» антибиотиков, что находит объяснение в приоритетном значении в одних случаях задач антибактериальной, в других — глюкокортикоидной терапии).
Хорошо изученная на моделях антибиотиков проблема сочетанного лечения касается и других разделов химиотерапии внутренних болезней. С одной стороны, приобретает все большее значение полихимиотерапия. Она необходима при онкологических заболеваниях, гемобластозах, где отход от комплексной программы чаще всего означает нарушение системы лечения, срыв лекарственно-обусловленной ремиссии и гибель больного. Тщательно разрабатывается комплексный подход к терапии хронических заболеваний. С другой стороны, нарастает необходимость все более настойчивой борьбы со случайными, произвольными комбинациями фармакологических препаратов. Смертельно опасным считают одновременное применение морфина и анаприлина, но последствия зависят от суммарной дозы и ее адекватности состоянию больного. Избегают назначения анаприлина одновременно с изоптином (верапамилом), анаприлина с ингибиторами моноаминоксидазы, релаксантов на фоне приема хинидина. Просчеты в применении медикаментозной терапии, несмотря на попытки ее индивидуализации, а часто именно из-за некритичного варьирования приводят к многочисленным осложнениям.
В США за 10 лет (1961—1970) госпитализировано в связи с осложнениями медикаментозного лечения 15 млн человек, экономические потери превысили таковые от инфекционных заболеваний.
Тем не менее лучшие из сложных, многокомпонентных лекарственных прописей не без оснований получили распространение и апробированы лечебной практикой. Они характеризуются сбалансированностью ингредиентов, и их «упрощение» не всегда бывает безвозмездным. К числу таких препаратов относятся, например, применяемые при бронхиальной астме солутан, теофедрин, антастман, в гастроэнтерологии — викалин и слабительные коктейли, в гепатологии — Лив 52 и эссенциале.
Монотерапия даже наиболее современными препаратами часто оказывается лишь первой ступенью лечения. Ей на смену затем приходит более эффективное всесторонне рассчитанное комплексное лечение больного. Иногда эта комплексность достигается включением физиотерапевтических и иных немедикаментозных средств лечения, но чаще в первую очередь речь идет о комбинации фармакологических препаратов. Широкое распространение получила система ступенчатого подхода к лечению больных с прогрессирующими формами артериальной гипертензии. На смену монотерапии, которую в свое время предпочитали проводить салуретиками тиазидового ряда, а ныне варьируют в зависимости от особенностей процесса (мочегонные с включением калийсберегающих, препараты раувольфии, β-адреноблокаторы, клофелин, антагонисты кальция), затем приходит политерапия. Закономерным является процесс разработки стандартизованных полиингредиентных рецептур. К числу таких прописей относились депрессии, разработанный к 1960 г. А. Л. Мясниковым, и более современные формы — адельфан, бринердин, триампур и др. Следует различать комплексные препараты, включающие набор тех или иных ингредиентов преимущественно с целью восполнения возникающего в организме дефицита или заместительной терапии, и сочетанное применение фармакодинамически активных препаратов. К числу первых относятся инфузионные растворы сложного электролитного состава, поливитаминные и полиаминокислотные рецептуры. К числу вторых — сложные рецептуры синергично действующих препаратов. Рациональный подбор комплексного препарата во втором случае значительно сложнее, но и прописи первого рода требуют строгого соблюдения оптимальных соотношений (табл. 5). При поддерживающем, длительном лечении значение приобретают развитие толерантности к тому или иному/препарату, снижение его эффективности. Наряду с другими методами преодоления этого феномена (прерывистый курс, ритм приемов) большое значение имеет правильное использование политерапии.
Фармакологическая несовместимость витаминов при длительном их введении в повышенных дозах
Для проведения поддерживающей терапии создаются специальные лекарственные формы, отвечающие ряду условий, в том числе комплексные, обладающие достаточной длительностью действия, допускающие прием в течение дня одной таблетки. Иногда полиингредиентные таблетки делают по необходимости многослойными (мексаза, панзинорм).
Одна из задач создания официальных комплексных фармакологических форм — предупреждение произвольного, ограниченного лишь прямыми противопоказаниями использования случайных комплексов лекарств. Конечный результат полипрагмазии всегда отличается от ожидаемой суммы искомых эффектов, поскольку многообразны формы взаимодействия этих эффектов в организме и труднопредсказуемы побочные действия.
Крайняя сложность учета всех сторон взаимодействия медикаментов вынуждает придерживаться апробированных, выверенных сочетаний. Заслуженное распространение получают поэтому такие оправдавшие себя прописи, как капли Вотчала, 4-компонентная схема лечения нефрита по Киндкайдт Смит (Kindcaid Smith), фиксированные программы в гематологии, обычно обозначаемые буквенными или цифровыми аббревиатурами (ЦВАМП, «7 + 3» и др.).
Импровизация в составлении индивидуальных схем лечения больного, произвольный выбор сочетаний лекарств не позволяют предотвратить неожиданных осложнений терапевтического вмешательства, нередко создают фармакологическую какофонию.
Не только сочетание отдельных медикаментов между собой, но даже их взаимодействие с рядом широко распространенных пищевых продуктов требует осведомленного учета. Применение мочегонных тиазидового ряда вынуждает обогащать диету солями калия, прием тетрациклина — воздерживаться, от молока и молочных продуктов, а также фруктов, так как содержащийся в них кальций образует с этим антибиотиком нерастворимые комплексы. При назначении ингибиторов моноаминоксидазы (ниаламида, нуредала) из рациона питания исключают сыр, сливки, пиво, вино, так как содержащиеся в них амины (тирании) при подавлении МАО оказывают выраженное гипертензивное действие («сырный синдром»).
В геронтологической практике применяют более осторожные, уменьшенные дозы многих медикаментов. Ряд препаратов, например дизопирамид из числа антиаритмических средств, переносится пожилыми лицами особенно плохо. Но в связи с нередким наличием у престарелых нескольких заболеваний, по поводу которых может проводиться поддерживающее лечение, встает и другая проблема: выбор наиболее необходимых направлений лечения, а при возникновении острого заболевания — оценка целесообразности продолжения поддерживающей терапии или временного ее прекращения на период проведения актуального лечения по поводу интеркуррентной болезни. Между тем в практике чаще происходит нечто прямо противоположное: при врачебном осмотре, тем более при стационарном обследовании, выявляется весь комплекс имеющихся у пациента нарушений и заболеваний, и лечащий врач, не умея определить разумные приоритеты, начинает лечение по всем обнаружившимся линиям. Терапевту способствуют в этом консультанты других медицинских специальностей, у каждого из которых могут оказаться достаточные основания для назначения лечения. Фармакологическое вмешательство происходит нарастающим итогом, несбалансированно. За один прием такой пациент получает из рук медицинской сестры 10—15 и более таблеток. Результат такой полипрагмазии можно предвидеть только в том смысле, что отрицательные последствия ее более вероятны, чем искомые.
Повышенная осторожность необходима при лечении детей, беременных женщин, а также при включении в комплекс внутривенных, капельных, внутримышечных и иных парентеральных введений. russiannurse.ru Антибиотики | Лечи зубкиВсе антибиотики по механизму действия подразделяют на 2 категории, обладающие Бактерицидным И Бактериостатическим Эффектом. К первой категории относятся препараты, способные убивать микроорганизмы: пенициллины, цефалоспорииы, аминогликозиды и другие. Препараты второй категории тормозят развитие и размножение микроорганизмов: левомицетин, тетрациклин, эритромицин и другие. В настоящее время в отечественной медицине используется до 30 различных групп антибиотиков, включающих до 200 препаратов. В табл. 4 приведены основные современные антибактериальные препараты, используемые в последние годы в России. Для рационального построения антимикробной терапии необходимы сведения о характере возбудителей инфекции и чувствительности их к отдельным препаратам. Недостаток "классического метода" - исследования очень трудоемкие и занимают довольно много времени (результаты могут быть получены лишь через 2 суток), хотя метод дает наиболее достоверную информацию. Ускоренные методы определения чувствительности менее точны, но позволяют получить ответ через 8-18 часов. Бактериоскопия мазков из раны, окрашенных по Граму, позволяет определить групповую принадлежность микробов и на этом Таблица 4 Современные препараты Для Лечения гнойной инфекции (Страчунский Л. С. и соавт., 2002)
Основании быстро подобрать антибиотик (табл. 5). Для экспресс-диагностики анаэробной неклостридиальной инфекции (АНИ), наряду с бактериоскопией раневого отделяемого, используют метод газовой хроматографии, основанный на выявлении специфических продуктов метаболизма анаэробных микроорганизмов (летучие жирные кислоты). Все более широкое применение получает метод микробиологи - Таблица 5 Ориентировочная схема выбора антимикробных препаратов по результатам бактериоскопии мазка из клинического материала
Ческой диагностики АНИ, предложенный П. И. Бучиным и соавт. (1993), который подробно изложен в следующей главе. Наименее достоверна ориентация на клиническую картину и локализацию патологического процесса, хотя и сбрасывать их со счетов не следует. Так, например, при наличии внешних признаков синегнойной инфекции показаны карбенициллин, один из современных аминогликозидов (тобрамицин и др.), местно - полимиксин; препараты II ряда: азло-циллин (ципрофлоксан), цефтазидим (фортум), цефоперазон (цефо-бид), имипенем или современные хинолоны (таривид и др.). При гнойно-воспалительных заболеваниях мягких тканей лица и шеи в патологическом процессе преимущественно участвуют стафилококки, стрептококки, неклостридиальные анаэробы. Ориентировочный выбор антибактериальных средств, основанный на этом принципе, проводят с помощью данных, представленных в табл. 5. В связи с полиэтиологичностью современных видов гнойной инфекции, резистентностью многих штаммов часто приходится применять комбинацию антибактериальных средств. К показаниям для проведения комбинированной химиотерапии относятся: - эмпирическое лечение гнойных инфекционных осложнений и заболеваний неизвестной этиологии; - смешанный характер гнойной инфекции с участием различных микробных групп; - тяжелые гнойно-септические осложнения и заболевания, вызываемые полирезистентными возбудителями (медиастинит, сепсис и др.). По возможности назначают парные сочетания, так как большее число препаратов резко увеличивает частоту побочных эффектов и нередко оказывает нежелательное действие. Некоторые сведения о совместимости отдельных препаратов представлены в табл. 6. При лечении локализованных форм инфекции в большинстве случаев обходятся без антибиотиков либо назначают короткий курс (до 4 дней). Иногда ограничиваются пероральным приемом таблетиро-ванных препаратов - феноксиметилпенициллина, оксациллина натриевой соли, диклоксациллина, ампициллина, карфециллина, доксицик-лина и других либо прибегают к локальному введению антибиотиков в смеси с раствором местного анестетика в виде "коротких блоков". Антибактериальную терапию сепсиса начинают сразу же после установления диагноза, не дожидаясь результатов лабораторных исследований. При этом избирают максимальные дозы препаратов широкого спектра действия, активных в отношении и грамположительных, и грамотрицательных микробов, например, современные аминоглико-зиды в сочетании с цефалоспоринами Ш-ГУ поколений либо с азло-циллином ШТУ поколений или назначают цефалоспорины и азлоцил-лин. Если сепсис развивается после ранений и операций в челюстно-лицевой области при возможном наличии в ране неклостридиальных анаэробов, то к цефалоспоринам или современным аминогликозидам следует добавлять метронидазол либо клиндамицин, линкомицина гидрохлорид. В преодолении устойчивости возбудителей гнойной инфекции к антибиотикам основным принципом является назначение их по строгим показаниям. Второй принцип состоит в том, что целенаправлен
ное применение химиопрепарата узкого спектра действия более предпочтительно, чем лекарственного средства, обладающего широким спектром (при условии одинаковой их эффективности в отношении выделенного возбудителя). Третье условие предполагает непрерывное расширение арсенала антибактериальных средств за счет постоянного внедрения в клиническую практику все новых препаратов, к которым госпитальные штаммы не успевают выработать устойчивости. При этом местное применение антибиотиков, особенно способствующее генерации устойчивых штаммов, следует сводить к минимуму, продиктованному строгими показаниями. Рекомендуется временное прекращение (на 6-12 месяцев) профилактического использования того или иного антибиотика с одновременным значительным ограничением его применения для лечебных целей. За это время происходит многократное снижение процента возбудителей, устойчивых к конкретному препарату. Немаловажное значение в борьбе с распространением антиби-отико-резистентных штаммов принадлежит традиционным мероприятиям по сохранению строгого противоэпидемического режима работы в хирургических стационарах. При выборе дозы антибактериальных средств следует учитывать состояние внутренних органов, в особенности выполняющих экскреторную функцию. При угнетении функциональной активности печени, почек применение даже среднетерапевтических доз может создавать в организме больного опасные уровни химиопрепаратов. Поскольку печень обеспечивает в основном выведение рифампицина, левоми-цетина, мономицина, эритромицина, при наличии признаков нарушения ее функции лучше отказаться от применения перечисленных препаратов. Почки принимают участие в элиминации большинства антибиотиков - пенициллинов, цефалоспоринов, аминогликозидов и других. Поэтому сниженная функция почек, наиболее точно определяемая по клиренсу эндогенного креатинина, либо проявления нефроток-сического действия препаратов (гематурия, альбуминурия, цилиндру-рия) должны служить поводом к уменьшению дозировок, увеличению интервалов между отдельными инъекциями. Существующие схемы не всегда обеспечивают оптимальные режимы для введения антибиотиков, и для расчета безопасных доз иногда приходится определять концентрацию химиопрепаратов непосредственно в крови. Из-за возможности быстро создавать ударные концентрации антибиотиков в организме оптимальным путем для профилактики и лечения признано внутривенное их введение. Весьма эффективно местное введение препарата, при котором очень высокие его концентрации создаются непосредственно в очагах потенциальной инфекции. Перспективным признан эндолимфатический путь введения антимикробных препаратов в грудной лимфатический сосуд; применяемая методика позволяет создать концентрацию лекарственного средства, превышающую в несколько раз минимальную подавляющую для большинства возбудителей гнойной инфекции. В лимфатический сосуд вводят 1/2 суточной дозы; вторую половину применяют в виде внутривенных, внутримышечных инъекций; ежедневные однократные введения осуществляются в течение 2-8 суток. Однако широкому использованию этой методики, весьма эффективной в борьбе с гнойной инфекцией, препятствуют технические сложности, связанные с катетеризацией лимфатических сосудов.
Приводим современную схему применения антибактериальных препаратов для профилактики и лечения гнойной стоматологической инфекции (табл. 7). Похожие записи:lechizubki.ru |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
г.Самара, ул. Димитрова 131 [email protected] |
 |