|
|
||||||||||
|
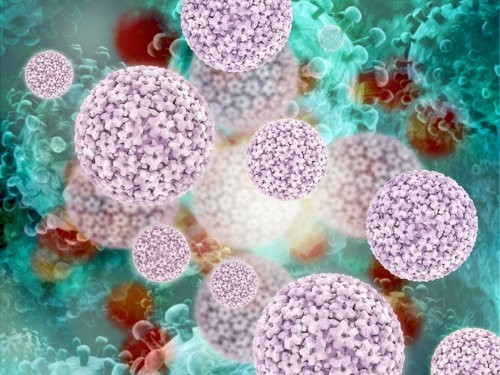
Ученые утверждают: найдена универсальная вакцина против рака. Вакцина против раканайдена универсальная вакцина против ракаИсследователи нашли способ убедить иммунную систему организма атаковать опухоли, и это практически не вызывает побочных эффектов.
Ученые сделали очень большой шаг на пути к созданию универсальной вакцины против рака, которая заставит иммунную систему атаковать опухоли организма, как если бы они были вирусами. Международная группа исследователей описала в журнале Nature, что они взяли куски генетического кода РНК рака, положили их в крошечные наночастицы жира, а затем ввели смесь в кровь трех пациентов, которые находились на последних стадиях заболевания. Иммунная система пациентов стала производить Т-клетки, которые предназначались для атаки раковых клеток. Также эта вакцина была эффективна при борьбе с агрессивно растущей опухолью у мышей. Об этом рассказали ученые под руководством профессора Угур Сахин из Университета Иоганна Гутенберга в Германии. «[Такие] вакцины недороги в производстве, и практически любой антиген опухоли [белок, атакуемый иммунной системой] может быть закодированы с помощью РНК», — написали они. «Таким образом, подход нанодисперсной РНК иммунотерапии может рассматриваться в качестве универсально применимой вакцины нового класса для иммунотерапии рака». В исследовании говорится о трех пациентах, которые получили низкую дозу вакцины. Целью этого эксперимента не было проверить, насколько хорошо сработала вакцина. Несмотря на то, что казалось, что иммунная система пациентов реагирует, нет никаких доказательств, что их опухоль в результате ушла. У одного пациента с подозрением на рак лимфоузлов опухоль стала меньше после того, как он получил вакцину. Другой пациент, чья опухоль была удалена хирургическим путем, после вакцинации прожил без рака семь месяцев. Третий пациент имел восемь опухолей, которые распространились от начального рака кожи в его легкие. Эти опухоли оставались клинически «стабильными» после того, как была введена вакцина. Вакцина, которую использовали целый ряд различных кусочков РНК, активировала дендритные клетки, которые выбирают мишени для атаки иммунной системой организма. На это последовал решительный ответ от «убийцы» Т-клетки, которая обычно разбирается с инфекциями. Иммунотерапия рака в настоящее время вызывает значительный ажиотаж в медицинских кругах. Она уже используется для лечения некоторых видов рака у ряда пациентов, находящихся в ремиссии более 10 лет после лечения. В то время как традиционное лечение некоторых форм рака может привести к полному излечению, рак легких, меланома и некоторые опухоли мозга и шеи остаются трудно излечимыми. Возможность ввести эффективную вакцину в кровь пациента была бы значительным шагом вперед. Вакцина вызывает только лишь гриппоподобные побочные эффекты в отличие от тяжелых последствий, вызванных химиотерапией. Профессор Алан Мелчер из Института исследований рака, сказал: «Иммунотерапия рака является быстро развивающейся и воодушевляющей областью. Это новое исследование на мышах и небольшом количестве пациентов показывает, что иммунный ответ против рака может быть спровоцирован вакциной нового типа». Хотя исследование очень интересное, оно еще далеко от того, чтобы доказать на 100% свою эффективность для пациентов. «В частности, существует неопределенность в том, будет ли терапевтический эффект, который мы видели в исследовании на мышах, также достигнут у людей. Также есть практическая проблема производства наночастиц для широкого клинического применения». Доктор Хелен Риппон, глава Международной ассоциации изучения рака, сказала: «Мы знаем, что иммунная система имеет большой потенциал, чтобы ею манипулировать и активировать на борьбу с раковыми клетками, поэтому мы финансируем исследования в этой области уже 15 лет». «Это новые захватывающие результаты, которые вселяют надежду, что РНК-наночастицы смогут сделать это». Она описала реакцию иммунного ответа у трех пациентов как «положительную» и отметила, что рак кожи на последней стадии «крайне сложно вылечить». «Однако, нужны исследования с участием большего числа людей с различными типами рака и в течение длительных периодов времени, прежде чем мы могли бы сказать, что мы обнаружили «универсальную вакцину против рака». Но это исследование является весьма позитивным шагом вперед в достижении этой глобальной цели», — сказала она. Оригинал публикации: «Independent» newvz.ru Прививки против рака шейки маткиФактор рискаТочные причины, из-за которых развивается болезнь, не установлены. Но существует ряд факторов, которые способны повлиять на возникновение опухоли. Главным из этих факторов является вирус папилломы человека (ВПЧ). В большинстве случаев вирус передаётся половым путём. Большая вероятность им заразиться у лиц с неконтролируемым количеством половых партнёров и незащищенных половых актов.  Вид вакцины ВПЧ в себе имеет большое количество разных вирусов, некоторые из них считаются наиболее активными по отношению к развитию онкологического процесса. Вот для этих видов и была разработана прививка от папилломы и рака шейки матки соответственно. Виды вакцинНа данный момент разработано два вида препарата, которые запатентованы и применяются для вакцинации — это Гардасил и Церварикс. В ближайшем будущем планируется ввести эти препараты в календарь обязательной вакцинации. Проблема подобных профилактических целей заключается в стоимости подобной прививки. Средняя цена для одного пациента составляет в пределах 500 долларов. Помимо этого препараты имеют значимые недоработки и недостатки. Механизм действияВакцина от рака шейки матки работает по следующему принципу, препарат состоит из частиц вируса, точнее его оболочки без него самого. Попадая в организм, он не заражает его, а вырабатывает иммунные, защитные функции, которые помогают справиться с вирусом, если он настоящий попадёт вовнутрь организма человека. Вакцинация проводится в течение полугода в три этапа. Первый укол выполняется в любой выбранный день, второй через два месяца и третий спустя пол года после первой вакцинации. Гардасил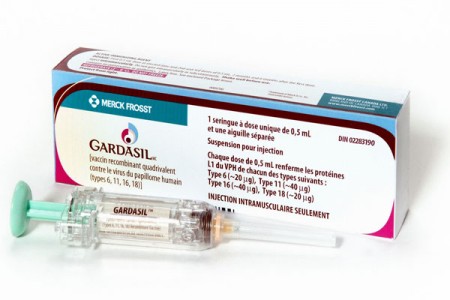 Фото препарата Препарат активен против четырёх видов вируса: 6, 11, 16 и 18. Показан препарат девушкам и молодым женщинам в возрасте от 9 до 26 лет в целях профилактики развития ВПЧ представленных типов, а также для недопущения развития предраковых дисплазий и генитальных кондилом. Противопоказания медикамент имеет следующие:
Противопоказаний к применению в период лактации и беременности не указано, но и также сказано, что исследований на женщинах этой группы не проводилось, лишь на животных. Поэтому целесообразность применения в этот период остаётся под вопросом. Из побочных явлений выделяют следующие:
За и против примененияПрививка против рака шейки матки препаратом гардасил имеет свои явные недостатки, заключаются они в следующем. Если всё же у женщины будет выявлен рак шейки матки, бездейственность средства всегда можно списать на оставшееся огромное количество типов вируса папилломы, помимо 6,11, 16 и 18, которые указаны в перечне воздействия. Также медикамент может таить в себе серьёзную опасность для здоровья. Связано такое утверждение с составом средства, его компонентами являются:
Накопления этих компонентов в организме способно привести к различным нарушениям, например, таким как: снижение почечной или печеночной функции;
Еще один важный момент в применении вакцины заключается отсутствие данных о здоровье детей рождённых от женщин привитых гардасилом. Однозначным преимуществом вакцинации является шанс предупредить развития серьёзной патологии, но, к сожалению, полностью обезопасить женщину медикамент не может. ЦервариксВторой популярный медикамент, использующийся для вакцинации — это церварикс. Действие вакцины направлено на блокировку ВПЧ 16 и 18 типов.  Вакцинация рака шейки матки Показания к применению:
Побочные явления возможны следующие:
Важно! Также как и гардасил, церваркс имеет в своём составе вредные компоненты, такие как алюминий, хлорид натрия и бура, негативное воздействие которых было описано. Также важно отметить, что исследования эффективности и наличия побочных эффектов проверялись лишь фирмами производителями препаратов. Поэтому прививка от рака шейки матки последствия может иметь не всегда предсказуемые, этот факт следует учитывать перед вакцинацией. Также заявленная возрастная аудитория составляет 9-26 лет, хотя на самом деле исследования проводились на женщинах возрастом от 15 до 26. То есть, прививка для девочек от рака шейки матки в возрасте от 9 до 14 лет, может оказаться не безопасной.  Возрастной барьер для вакцинации Говорить о пользе и вреде той или иной вакцины можно много, но выбор в её применении или отказе от прививки остаётся за женщиной. Вакцинация от опухоли шейки матки еще не столь популярна в странах СНГ и за счёт этого существует опаска у пациентов к её применению. Также неизвестно, как поведет себя препарат в организме через 20-30 лет, так как исследованиям медикаментов этой группы не более 6 лет. А инъекция делается совсем в молодом возрасте, как правило, ещё не рожавшим девушкам. Выбор остаётся только за вами! Видео: когда нужно делать прививку от рака шейки матки?Будьте здоровы! onkolog-24.ru Вакцины от рака: предотвратить, побороть, обнадежить - МедНовостиПри упоминании слова «вакцина» большинство людей сразу думает о кори, ветряной оспе или гриппе. В этих вакцинах для вызова иммунного ответа организма используются ослабленные, убитые микроорганизмы или типичные для них молекулы. После попадания вакцины в организм иммунная система учится реагировать на подобный «раздражитель» в режиме тренировки, запоминает патоген и при столкновении с реальной инфекцией быстро побеждает. Часть противораковых вакцин работает по похожему принципу, только бороться приходится уже со своими клетками. Ученые давно разрабатывают вакцины, которые могли бы предупредить либо вылечить рак. Одни из первых опытов принадлежали Уильяму Коли с его «токсинами». Иммунотерапия рака — лечение опухолей с помощью антител — одно из самых перспективных направлений в терапии рака, сложившееся несколько десятков лет назад. Но первые опыты задействования иммунитета в борьбе с раком гораздо старше. «МедНовости» проследили историю иммунотерапии от Средневековья до разработки современных препаратов. Продолжение следует. Другие пытались вызвать ответ иммунной системы на опухоли, используя БЦЖ — бациллу Кальметта-Герена (Bacille Calmette-Guérin, BCG) для профилактики туберкулеза. Это живая аттенюированная вакцина с богатым составом, и было бы удивительно, если бы она не оказывала сильного воздействия на иммунную систему в целом. Однако с 1935 года большинство попыток лечения ею рака показали неутешительный результат. Несмотря на это, при обработке данных всех опубликованных докладов, стало ясно, что, если БЦЖ вводили в самом раннем возрасте или вакцинация обеспечивала мощную защиту от туберкулеза, — то вакцина предотвращала лейкемию. Читайте еще: Сотрудники Калифорнийского университета в Сан-Франциско сообщили, что вакцина против гемофильной инфекции типа В, защищающая от бактериального менингита, снижает риск развития самого распространенного у детей типа рака крови — острого лимфобластного лейкоза. Профилактические вакцины от ракаНебольшая часть онкологий вызвана вирусами. Поэтому вакцины, защищающие от этих вирусов, могут использоваться и как противораковые. Они нацелены не на раковые клетки, а именно на инфекцию.
Вирус папилломы человека. Фото: Shutterstock. С 1970-х годов стало ясно, что вирус папилломы человека (ВПЧ, или HPV) может привести к малигнизации клеток. Этой проблемой занимался Харальд цур Хаузен (Harald zur Hausen) и его коллеги. В 2001 году в интервью он заявил, что перспективы вакцин против рака многообещающие: «Сейчас по всему миру 10 миллионов случаев рака в год. В будущем должна появиться возможность предотвратить 1,25 млн из них с помощью вакцинации». ВПЧ — самая распространенная вирусная инфекция половых путей. Всего известно более 100 типов этого вируса, и как минимум 13 из них могут привести к онкологии. Его связывают с раком шейки матки, ануса, влагалища, пениса и некоторыми другими. Сейчас есть две одобренных профилактических вакцины против нескольких типов ВПЧ: Гардасил (одобрена FDA в 2006 году) и Церварикс (одобрен в 2009 году). Обе включают в себя вирусоподобную частицу рекомбинантного белка капсида L1. Совещательный комитет по иммунизационной практике США (The Advisory Committee on Immunization Practices of the US CDC) рекомендует рутинные прививки девочкам и мальчикам в 11-12 лет, но можно привить ребенка с 9 лет. Те, кто не был привит в раннем возрасте, могут привиться и позже. К сожалению, противораковые прививки от ВПЧ единственные в своем роде. Например, у пациентов с хроническим вирусом гепатита В (ВГВ, или HBV) повышается риск рака печени. Но вакцины против ВГВ пока не разработано. Помимо этого, большинство видов онкозаболеваний не вызвано вирусами. Врачи пока не уверены, можно ли и для них создать превентивные вакцины. Некоторые разработки уже есть, но они находятся на ранних стадиях, и о результатах говорить пока рано. Кроме того, как считается, даже при успехе до внедрения в рутинную клиническую практику пройдет много времени. Вакцины, борющиеся с ракомЦель вакцин от рака отличается и от обычных, и от профилактических противоопухолевых, борющихся с вирусами. Прививка такой смеси должна показать иммунной системе, как побороть уже существующую болезнь. К сожалению, подавляющее большинство таких разработок находится на различных стадиях клинических испытаний и еще не применяется широко. Из-за этого вылечивание рака простой прививкой все еще остается делом будущего. Исследователи используют несколько стратегий действия вакцины. Первая опция — это вакцины с раковыми клетками. Клетки опухоли, удаленной во время операции, изменяют в лабораторных условиях и вводят пациенту. Иммунные клетки реагируют не только на вколотую вакцину с убитыми раковыми клетками, но и на похожие — то есть, на раковые клетки, оставшиеся в организме. Если вакцина вводится тому же пациенту, у которого вырезали опухоль, ее называют «аутологичной». Если же «донор» и реципиент раковых клеток — разные люди, то это аллогенная вакцина. Исследователи из университета Томаса Джефферсона (Thomas Jefferson University) в 2014 году проводили клинические испытания подобной вакцины на 12 пациентах с рецидивирующей глиобластомой. Раковые клетки участников обрабатывали в лаборатории препаратом AS-ODN, который выключает рецептор IGF-R1. Было показано, что этот рецептор стимулирует рост и метастазирование опухоли, а его блокировка может привести к ее самоуничтожению. У половины пациентов был выявлен иммунный ответ на вакцину. Ученые объясняют это тем, что у остальных иммунитет мог быть ослаблен предшествующей химиотерапией. Следующий этап клинических испытаний проводится в 2015 году. Второй тип — это вакцины с антигенами. Для стимуляции иммунной системы в них используются не целые раковые клетки, а один или несколько антигенов, белков либо пептидов. Эти вакцины делают не для конкретного пациента, а против определенного типа рака. Читайте еще: О процессе разработки терапевтической вакцины от меланомы (рака кожи) и результатах ее испытания «МедНовостям» рассказал профессор, доктор наук, заведующий лабораторией генетических основ клеточных технологий Института общей генетики РАН Сергей Киселев. В Америке же в 2014 году проводили исследования по безопасности вакцины против рака груди. Разработка ученых из школы медицины университета Вашингтона (Washington University School of Medicine) «натаскивает» белые клетки крови на маммаглобин-А. Этот белок экспрессируется практически исключительно в молочной железе, и в 40-80% опухолей его уровень аномально высок. У половины из 14 женщин с метастатическим раком молочной железы и высокой концентрацией маммаглобина-А рак не прогрессировал в течение года после вакцинирования (в контрольной группе таких исходов было значимо меньше). Побочные эффекты были незначительными. Исследования планируется продолжить.
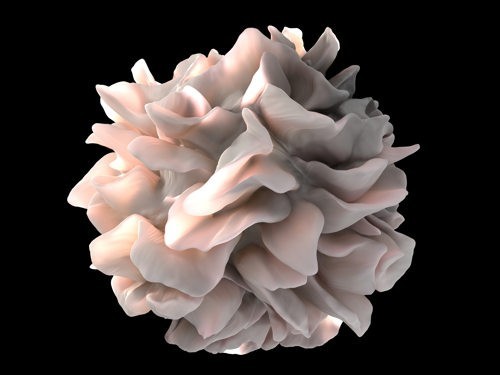
Уильям Гилландерс, Университет Томаса Джефферсона. Фото: Robert Boston / Washington University School of Medicine Одна из стратегий — генные вакцины. Их нельзя отнести к отдельному типу, но для их создания нужны векторы — нуклеотидные последовательности, которые вставляют в чужой геном. Таким образом, используя собственный ферментный аппарат клетки-мишени, ученые заставляют ее производить нужный белок. Для этого часто используют фрагменты ДНК вирусов, бактерий, дрожжевых клеток. Использование таких вакцин позволяет не только заставить клетку производить дополнительные опухолевые антигены, но и вызвать усиление иммунного ответа, поскольку генный материал взят от, например, бактерии. Вдобавок, их производство проще и дешевле. Уже было проведено клиническое исследование II фазы Prostvac-V/F в конце 2014 года для пациентов с раком простаты, устойчивым к гормональной терапии. Prostvac-V основан на вирусе коровьей оспы и модифицирован так, чтобы производить ПСА (простатспецифический антиген) и три других белка, заметных для иммунной системы (триада костимулирующих молекул — TRICOM). Prostvac-F же делают из вируса оспы кур. Он содержит тот же генетический материал, но вводится несколько раз. Наконец, самые успешные, пожалуй, — это вакцины с использованием дендритных клеток. Эти клетки помогают иммунной системе «увидеть» опухоль. Они разрушают раковые клетки и выставляют на своей поверхности их «кусочки». Т-клетки распознают антигены и начинают иммунную реакцию против содержащих их клеток.
Дентритная клетка. Фото: National Institutes of Health / Wikimedia Sipuleucel-Т (Provenge) для лечения рака предстательной железы единственная получила одобрение FDA. Она используется для тех пациентов, кому не помогает гормональная терапия. Принцип ее действия таков: клетки иммунной системы выделяют из крови пациента и преобразовывают их в дендритные клетки, обрабатывая их специальной смесью молекул. Кроме того, новоявленным дендритным клеткам предъявляют простатическую кислую фосфатазу (РАР). Затем их несколько раз внутривенно вводят обратно пациенту, чем и вызывают ответ организма на опухоль. Несмотря на то, что вакцина не лечит рак простаты, она продлевает пациенту жизнь в среднем на несколько месяцев. Активно исследуются и другие вакцины с дендритными клетками. Nature Reviews Cancer пишут, что в этом году Митчелл, Батич (Mitchell, Batich) и коллеги показали, что ответ на вакцину у больных с глиобластомой может быть усилен за счет пре-кондиционирования с Td анатоксином (столбняк/дифтерия — tetanus/diphtheria), антигеном, вызывающим сильную реакцию организма. ПерспективыС совершенствованием научной техники и накоплением знаний оказалось, что иммунная система гораздо сложнее, чем предполагалось, и раковые клетки «хитрее» в маскировке. Но, несмотря на это, появляется все больше удачных разработок вакцин от рака. Все большее предпочтение отдается персонализированным вакцинам — нацеленным на мутации конкретного пациента. Так, недавно американские ученые сообщали об успешных клинических испытаниях вакцины против меланомы. Читайте еще: Проведены первые клинические испытания персонализированных вакцин против меланомы. Сделанные с учетом индивидуальных мутаций пациентов вакцины вызвали сильный ответ иммунной системы. Прогресс не стоит на месте. Например, ученые создали трехмерную самособирающуюся конструкцию для «обучения» иммунных клеток. В опыте на мышах в поры конструкции загрузили опухолевые белки, которые надо было предьявить иммунной системе, и потом получили мощный ответ организма. Сами ученые возлагают на вакцины большие надежды. «В последние годы исследователи и общественность начали осознавать роль, которую иммунная система играет в профилактике и лечении рака», — говорит Крейг Хупер (Craig Hooper), профессор Департамента биологии рака Университета Томаса Джефферсона (Thomas Jefferson University). Эстебан Селис (Esteban Celis), профессор иммунологической программы центра Моффитта (Moffitt's Immunology Program), считает, что такие вакцины — хорошая альтернатива традиционным методам лечения, приводящим к серьезным побочным эффектам и часто бесполезным на поздних стадиях болезни. В 2013 году вакцины от рака возглавили десятку научных прорывов. Иммунотерапия онкологических заболеваний возглавила рейтинг наиболее значительных научных достижений 2013 года, составленный журналом Science и опубликованный в его номере от 20 декабря. В топ-10 также вошли еще семь открытий в области медицины, генетики и биологии. medportal.ru Вакцина против рака. Методика лечения рака В. А. БритоваВакцина против рака.Методика лечения рака В. А. Бритова Известный паразитолог Василий Александрович Бритов долгие годы занимался изучением трихинеллеза. Основываясь на фактических данных, он обнаружил, что в регионах, где население питается мясом диких животных или сырым мясом, уровень заболевания раком ниже. Пытаясь выяснить причину этого, он пришел к выводу, что вероятным фактором, предотвращающим возникновение заболевания, является высокий уровень заражения населения этих регионов трихинеллезом. Медицина считает это заболевание одним из самых тяжелых паразитарных поражений. Трихинеллы (или трихины) - это мелкие (до 4,5 мм) круглые черви. Взрослые особи паразитируют в кишечнике, а личинки - в мышцах пораженного организма. В мясе личинки трихинелл окружены капсулой, которая образована клетками хозяина. При поедании такого мяса в кишечнике человека личинки выходят из капсул и в течение 3 суток достигают половой зрелости. Оплодотворенные самки прикрепляются головой к слизистой оболочке кишечника. Выделяют они не яйца, а сразу личинки. В кишечнике человека личинки пронизывают его стенку, выходят в лимфатические сосуды, а оттуда - в кровеносную систему. По сосудам они разносятся по всему организму, и через несколько дней (от 3 до 9) начинают оседать в мышцах. Чаще всего поражаются диафрагма, межреберные мышцы, мышцы гортани и языка, шея, глазные мышцы, мочеиспускательный канал и пищевод, а также мышцы ног. Личинки трихин выделяют вещества, разрушающие пораженные ими ткани. Развивается активный воспалительный процесс. Организм человека начинает защищаться: вокруг личинки образуется капсула, которая защищает организм человека от паразита, но в то же время способствует нормальному существованию личинок. Стенки капсулы прорастают кровеносными сосудами и нервными окончаниями. С кровью паразит получает от организма человека необходимые ему питательные вещества и кислород, а сам выводит в кровь вредные продукты жизнедеятельности, которые вызывают аллергическую реакцию и отравляют весь организм. Примерно через полгода стенки капсулы пропитываются известью, но личинки долго еще остаются живыми.Лечится заболевание трудно и долго, оно опасно своими осложнениями, которые нередко приводят к смерти. В. А. Бритов выяснил, что, попадая в кишечник, трихинеллы начинают оказывать мощное воздействие на иммунную систему человека. Таким образом происходит как бы вакцинация, и в дальнейшем человек уже не болеет раком. Ученый разработал и вакцину против рака, которая служит не только для профилактики, но и помогает в лечении рака. Основной принцип ее действия - резкое увеличение защитных сил организма.Для вакцины против рака он использует специальную "породу" трихинелл, не обладающую вредным действием на организм. Кроме того, по прошествии определенного времени, когда воздействие трихинелл поспособствовало усилению иммунитета, он избавляет организм от них с помощью противопаразитарной терапии. Это происходит до того, как трихинеллы разнесутся по организму и проникнут в мышечные ткани. Таким образом, человек не заболевает трихинеллезом. В. А. Бритов занимался этой темой несколько десятилетий и даже является держателем патента на свое изобретение. Но его метод лечения не признан медициной: онкологи и паразитологи относятся к нему крайне отрицательно.На данный момент вакцина против рака используется только в частном порядке, а разговоры о дополнительных исследованиях и тем более внедрении ее в практику даже не ведутся.Хочу предостеречь тех, кто решит самостоятельно экспериментировать с трихинеллезом, пытаясь съесть мясо дикого животного. Как утверждает автор методики, его вакцина не имеет ничего общего с подобной самодеятельностью: она разработана на основе многолетних исследований. Заболевание же трихинеллезом не менее опасно, чем злокачественная опухоль, и тот факт, что жители отдаленных районов, зараженные трихинеллами, не болеют раком, не значит, что они не умирают от трихинеллеза. Далее - Причина рака - трихомонадыСмотрите - Алкоголь и рак Роль сна для больного ракомИнтересная статья: Цветочная пыльца — незаменимый продукт для онкологических больныхВернуться в Меню раздела В заключении видео о том, что рак излечим и кто мешает спасению миллионов людей. www.rakynet.ru Вакцина против рака » Oncoclub
Вакцина против опухолей: мифы, реальность и будущее Регулярно появляющиеся в СМИ сообщения о создании долгожданной профилактической вакцины, способной предотвратить появление раковых опухолей, всегда вызывают огромный интерес у населения и специалистов. Насколько их надежды оправданы, могут сказать только представители ведущих онкологических учреждений России, коллективы которых занимаются этой проблемой уже не одно десятилетие. Medportal.ru публикует интервью, которое дал «Медицинской газете» заместитель директора Российского онкологического научного центра им. Н.Н.Блохина РАМН по научной работе, директор НИИ экспериментальной диагностики и терапии опухолей, заслуженный деятель науки и техники РФ, профессор Анатолий Барышников. — Анатолий Юрьевич, как вы оцениваете причину появления подобных сообщений? — К сожалению, в последние годы возрос ажиотаж вокруг вопроса об антираковых вакцинах. Само их появление связано с ослаблением в годы перестройки контроля со стороны Фармкомитета и Минздрава России за использованием всевозможных новых методов лечения. Хотя в 2000 году министр здравоохранения Ю.Шевченко и издал приказ «О лекарственных средствах», где был четко регламентирован порядок изучения, испытания и клинического применения новых препаратов. Возможно из-за того, что положения указанного документа не были доведены до широкой аудитории, может быть, по иным причинам, но различные специалисты, чаще даже не врачи, а, скажем, ветеринары или лица, совсем далекие от медицины, решают заработать деньги на человеческом горе. Начинают заниматься «производством» противоопухолевых вакцин. Откройте любую страницу в «желтой» прессе и найдетеодно-два объявления о «лечении рака» и т.п. Мы не успеваем срывать подобные листки-призывы со стен онкоцентра. Больше того, был и у нас такой доктор, который якобы изобрел противораковую вакцину. После того как эту его деятельность запретили у нас, он уехал в США. Там сначала лечил своей вакциной собак, но после неудач и запрета вернулся назад. А мы еще долгое время получали оттуда письма возмущенных владельцев собак, что вакцина не помогла их питомцам, и они погибли. — Возможно ли создание противораковых вакцин в принципе? — Этим во всем мире занимаются уже более 30 лет. Но тут необходимо провести деление вакцин на два типа. Первые, классические, которые используются для профилактики, к примеру, инфекционных заболеваний: гриппа, коклюша, дифтерии и т.д. Они изготовляются из ослабленных организмов, и годы их применения показали, что они имеют право на существование, предохраняя человека от инфекций. Противораковые же вакцины совершенно иного типа, они не для профилактики, а скорее для лечения опухоли. Создается иммунный ответ, который если и не вылечит, то, по крайней мере, предотвратит развитие метастазов, остаточной болезни. Ведь как бы тщательно ни удалили опухоль, всегда остаются клетки, из которых рак способен возродиться. Теоретически эти клетки можно убить с помощью иммуноответа. Противоопухолевая вакцина как раз и направлена на усиление иммунного ответа. Разработкой таких вакцин против рака, как я сказал, занимаются уже давно, но наиболее сильный всплеск активности исследователей произошел после 1974 года, в рамках советско-американского соглашения. У нас лидером был лауреат Государственной премии СССР профессор Георгий Свет-Молдавский, который вместе с академиком АМН СССР Николаем Трапезниковым очень активно испытывал эти вакцины в клинике. В 1975 году была опубликована первая в мировой истории статья о создании вакцины против рака молочной железы. Но, как видим, прошло уже почти 30 лет, а воз и ныне там. За это время появилась лишь одна вакцина американского ученого Мертона, которую FDA разрешило к клиническому применению. Она создана на основе определенного штамма БЦЖ и используется в мировой практике при лечении рака мочевого пузыря. При инстилляции мочевого пузыря ослабленными бактериями развивается иммунный ответ и опухоль лечится. Но это единственный пример. Все другие работы крупнейших мировых центров в течение прошедших десятилетий оказались безуспешными. Поэтому просто смешно слышать, чтокакие-то маленькие частные компании объявляют, что они создали вакцину, особенно — для профилактики рака. — Если это возможно, когда же такую создадут? — Именно для профилактики — лет через 10-20, а то и через 50. Ведь нужны огромные исследования, большие популяции людей из группы риска. Необходимо будет показать, что такая вакцина способна эффективно блокировать развитие опухоли. Сейчас же речь идет лишь о лечении больных с помощь вакцин. В этом плане существует три «излюбленные» онкологами локализации рака: кожи (меланома), почки и толстой кишки. Эти опухоли плохо лечатся другими методами, они доступны для наблюдения, а самое главное и страшное — они очень быстро метастазируют. В течение двух лет видно, что если появились метастазы, то неизбежен летальный исход, а если их нет, значит, человека вылечили. — Значит, применение вакцин в таких нозологиях связано с быстрой оценкой эффективности? — Да, и все онкоучреждения, разрабатывающие лечебные вакцины, в первую очередь проверяют их при подобных заболеваниях. — А чем занимаются сотрудники Российского онкоцентра РАМН им. Н.Н.Блохина и других российских медучреждений этого профиля? — Если раньше мы искали вирусы, которые вызывают опухоли у животных, и с их помощью пытались создать иммунный ответ для профилактики рака, то сейчас от этого отказались. Наши исследования показали: если из 10 подопытных мышей у 5 вследствие иммунного ответа опухоль рассасывается, то у других 5 она стимулируется. Страшно, что в 50% случаев, применяя вакцины, можно лишь усилить рост опухоли. По отношению к человеку такие методы недопустимы. А причину, те интимные механизмы, которые вызывают рост опухоли, установить не удавалось. Сегодня появились новые технологии, и вновь возрос интерес к созданию профилактических вакцин. С помощью генной инженерии создаем белок, который отличается от находящегося в организме и способен усилить противоопухолевый иммунный ответ. И у нас в онкоцентре, и в других российских и зарубежных онкоучреждениях сейчас ведутся работы по нескольким перспективным направлениям. Первое — берут ген мини-антител и ген энтеротоксина А или В, соединяют и помещают в плазмиду, затем вводят в организм животного, и продуцируется белок. Последний своей малой частью моноклонального антитела способен соединиться с опухолью, а ген энтеротоксина может вызвать иммунный ответ и привлечь иммунокомпетентные клетки, которые убьют опухоль. Белок, связанный с опухолью, становится чужеродным, развивается иммунный ответ, который ведет к гибели опухоли. Такие эксперименты уже идут и у нас, и за рубежом, пока на животных. Но это очень перспективное направление, и можно ожидать, что действительно будут получены белки, отличные от существующих в организме. Кроме того, можно изменить белок, ввести его в опухоль, что повысит его антигенность и приведет к гибели раковых клеток. Другой вид вакцины, над созданием которой сегодня работают исследователи, — дендритная. Сначала обнаружили дендритные клетки в виде отростков, способных захватывать различные микробы, опухолевые клетки, переваривать их до пептидов, а затем вместе с антигенами гистосовместимости приставляют к иммунным клеткам. Те, в свою очередь, начинают развивать иммунный ответ и это, в конечном счете, убивает опухоль. Таких клеток мало. Но появилась технология, позволяющая выращивать сотни миллионов этих клеток в пробирке, «обучать» их — показывать, что есть опухолевый антиген, и вводить больному. Уже есть хороший клинический эффект. Больные, которые, казалось бы, должны умереть в течение года, живут, и мы их вакцинируем постоянно, поскольку пока не знаем, когда нужно остановиться. Этот метод очень перспективен, и работа здесь продолжается. Еще один тип генно-инженерной вакцины разработан академиком РАН Георгием Георгиевым, директором Института биологии гена РАН. Он и его ученики обнаружили новый ген, усиливающий иммунный ответ. Он вводится в опухолевые клетки, которые затем облучают и, в свою очередь, вводят больному подкожно или внутрикожно. Начинает работать «фабрика» по продуцированию белка, усиливающего местный иммунный ответ. Убиваются опухолевые клетки (даже те, в которых не было гена). Направление очень перспективное, подобные работы ведутся и за рубежом, но там используют другие гены. — А вы лично верите в создание эффективных противораковых вакцин? — Безусловно. С помощью современных методов генной инженерии, молекулярной биологии можно создать вакцину, способную показать организму наличие опухоли, которую необходимо распознать и убить. Это вполне реально. Но это будет лечебная, лекарственная вакцина. Для создания же профилактической вакцины, по моему мнению, пока в науке предпосылок нет. Путь предстоит долгий, поскольку даже при испытаниях на животных еще нет положительных результатов. Весь мир ищет, но… Кроме того, я хочу сказать, все, что публикуется в «желтой» прессе, — это реклама для привлечения пациентов. В случаях излечения нет четких доказательств, что у больного была опухоль, а не воспаление и т.п. Люди хотят заработать. И все, что исходит не из академических институтов, не из учреждений, подконтрольных Минздравсоцразвития России, — это шарлатанство.
Источник: www.medportal.ru «Медицинская газета» 3 сентября 2004 г Если вам понравилось добавьте + www.oncoclub.eu Иммунотерапия и вакцина против ракаЗащитная система (иммунная система) расходует большую часть своей силы на разделение здоровых клеток и «чужих» клеток. Для того, чтобы это было возможным, иммунная система использует контрольные точки на клеточном уровне. Для активации защитной системы необходимо, чтобы молекулы, оказывающие влияние на контрольные точки, были в активной или пассивной позиции. Лекарства, которые призваны активизировать защитную систему и сумели открыть новую эру в лечении рака после 2012 года, называются иммунотерапией. Целью иммунотерапии в лечении онкологических заболеваний служит стимулировать иммунную систему для сражения с раком, укрепление и восстановление иммунной системы. Иммунотерапевтические препараты, несмотря на то, что являются сравнительно новыми, путем активизации иммунной системы, опираются на довольно старые теории лечения рака, и на самом деле иммунотерапия – это первый нехирургический метод лечения рака, который был открыт еще до появления химиотерапии и радиотерапии. В ходе работ, которые проводятся в области лечения онкологических заболеваний уже на протяжении примерно 100 лет, ученые сконцентрировались на изучении методов, способных напрямую убивать раковые клетки. Считалось, что один из самых важных механизмов собственной защиты организма - иммунная система (защитная система) – обладает недостаточной силой, и полагали, что недостаточность иммунной системы провоцирует укрепление раковых клеток. Два конца нашей иммунной системы, которая есть в нашем организме, подобны острому лезвию ножа. При чрезмерной и бесконтрольной работе возникают различные заболевания, которые развиваются, разрушая различные органы – данный феномен мы можем назвать избыточной активностью иммунной системы. При недостаточной работе иммунной системы мы становимся подвержены различным инфекциям, также могут возникать такие негативные проявления, как склонность к развитию рака.
126 лет назад нью-йоркский хирург Вильям Коли обнаружил, что тяжело больной пациент с онкологическим заболеванием на продвинутой стадии заразился инфекций, после чего последовала высокая температура, а затем вдруг рак стал регрессировать. Он предположил, что бактериальная инфекция, которой заразился больной, каким-то образом сыграла роль в уменьшении раковой опухоли, после чего он искусственным образом ввел живую бактерию другому больному. Это испытание привело к успеху, и больной прожил еще 26 лет, умерев не из-за онкологического заболевания. Коли подумал, что он близок на пути к открытию. Он продолжал проводить исследования и использовать бактерии. Коли и другие доктора, работавшие в той же области, вылечили более 1000 больных таким методом. Токсины Коли, при которых вызывается острая инфекция с повышением температуры для лечения рака, получили название прививки от рака на основе смешенных бактерий. Коли добился успеха при первом опыте, но последующие испытания не всегда заканчивались также благополучно. Никто не знал, почему токсины Коли, то есть - почему острая инфекция, которая сопровождается температурой, помогали в борьбе против рака и почему они иногда не помогали. Даже и сам Коли не мог дать этому никаких объяснений. Затем стало ясно, что токсины Коли образуют острую инфекцию с повышением температуры, активируя тем самым иммунную систему и запуская различные механизмы в организме человека. Так и в современной иммунотерапии развиваются похожие, но различные механизмы. В 1900 годах была разработана радиотерапия, затем химиотерапия, и интерес к токсинам Коли оставил в тени ранее открытые методы. До тех пор, пока в 1990-х годах не возник профессор Джеймс Эллисон, питавший надежду разработать лекарство, задействующее иммунную систему в борьбе против рака. Внимание Эллисона привлекла специальная биологическая молекула, которая называется CTLA-4. В работе, которую провел Эллисон и его коллеги, удалось доказать, что данная молекула, расположенная на самых важных клетках иммунной системы, именуемых Т-клетками, тормозит активность клеток Т (ингибирует их действие), и препятствует иммунной системе распознавать рак. Было известно, что Т клетки играют критическую, ключевую роль в регулировании агрессии (способности нападения) иммунной системы. Он заинтересовался тем, поможет ли устранение такого препятствия в лечении онкологического заболевания, и приступил к испытаниям над крысами, больными раком. В статье, опубликованной в 1996 году, Джим Эллисон, Макси Краммел и Дана Лич продемонстрировали, что у крыс, у которых активация молекулы CTLA-4 предотвращалась посредством специального антитела, рост опухоли удалось остановить. Это исследование стало источником воодушевления для разработки лекарств, открывающих новую эпоху в лечении онкологии, которые известны как регуляторы контрольной точки иммунной системы (checkpoint regulators). После такого прогресса «Ипилимумаб» (на рынке известен под названием «Ервой»), представляющее собой антитело, предотвращающее действие молекулы CTLA-4, продемонстрировало положительный эффект для больных злокачественной меланомой – видом рака, который считается в высшей степени агрессивным видом рака кожи продвинутой (4) стадии, и помогло спасти жизнь тысячам пациентов.
После такого важного поворота развития ученые начали поиск других способов, способных активировать иммунную систему через контрольные точки, и проводить испытания с молекулами на различных видах рака. Исследования, которые проводились в начале 2000 годов, показали, что рак, для того, чтобы скрыться от иммунной системы, использует, помимо CTLA-4, также поверхностные молекулы клетки под названием PD-1 и PD-L1. Молекула PD-1 находится только на поверхности клеток иммунной системы, и при прикреплении к собственным стимулирующим молекулам (ligand) клетки иммунной системы косвенно влияют на ослабление иммунной системы, приводя ее в пассивный вид. Сегодня используетсят 2 иммунотерапевтических препарата, которые препятствуют соединение PD-1 к собственным стимулирующим молекулам: «Ниволумаб» (продается на рынке под названием «Опдиво») и «Пембролизумаб» (продается на рынке под названием «Кейтруда»). Молекула PD-L1 – это симулирующая молекула протеиновой структуры, которая расположена одновременно и на поверхности клеток иммунной системы, и на поверхности раковых клеток, и при соединении к рецептору PD-1 (приемник) приводит клетки иммунной системы в пассивное состояние. Было установлено, что опухоли, у которых имеется большое количество молекул PD-L1 на поверхности клеток – их принято называть опухоли с позитивным PD-L1 – имеют более агрессивную структуру, при этом иммунотерапевтические препараты являются более эффективными в борьбе именно с такими видами рака. Единственным лекарственным препаратом, препятствующим соединение молекулы PD-L1 к PD-1, и получившим разрешение на использование в настоящее время, является «Атезолизумаб» (продается на рынке под названием «Тецентрик»).
Масштабы использования иммунотерапевтических препаратов в лечении онкологических заболеваний растут с каждым днем. Иммунотерапевтические оекарства, являющиеся регуляторами контрольных точек иммунной системы, получили разрешение на применение при следующих видах рака (по порядку):
При слове «вакцина» большинству из нас приходят на умпрививки, которые используются для защиты здоровья человека от различных инфекционных заболеваний. На сегодняшний день вакцины от краснухи, ветрянки, столбняка, гриппа и гепатита спасли жизнь миллионам людей. В этих прививках используются ослабленные или убитые вирусы (некоторые бактерии) для того, чтобы активировать иммунную систему. Таким образом, организм приобретает иммунитет против вредных микроорганизмов, не сталкиваясь с ними. Многие вакцины против рака работают подобным образом, они учат иммунную систему человека реагировать и нападать на раковые клетки. Вакцины против рака принято делить на две группы: защитные и лечебные. Ниже будут подробно рассмотрены обе эти группы вакцин. В нашей статье мы расскажем о двух лечебных вакцинах, получивших международное признание и разрешение от Американского агентства по контролю за пищевыми продуктами и лекарственными препаратами (FDA). Вакцина против рака предстательной железы Sipuleucel-T (Provenge) Несмотря на то, что при раке предстательной железы, распространившемся по организму, за счет гормоно подавляющей терапии (тестостерон) обеспечивается контроль в течение долгих лет, все же у больных наблюдается возобновление заболевания в результате увеличения уровня ПСА или развития новых очагов заболевания. Такие случаи мы можем назвать «рак предстательной железы с устойчивостью к гормонам». Иммунотерапевтическое лечение рака предстательной железы призвано подключаться в данную группу больных. Spiluecel-T (Provenge) – это первая разработанная вакцина против рака. Spileucel-T – это вакцина, разработанная в результате пятнадцатилетних исследований, получившая утверждение от Американского агентства по контролю за пищевыми продуктами и лекарственными препаратами (FDA). Данная вакцина, разработанная против рака предстательной железы, внесла положительный вклад в общую выживаемость в 4 месяца в ходе проведенных исследований, и в 2010 году получила разрешение от Американского агентства по контролю за пищевыми продуктами и лекарственными препаратами (FDA). Каким образом вводится вакцина Sipuleucel-T? Вакцина создается индивидуально для каждого человека. Сначала забирается кровь из организма пациента, далее посредством специальных аппаратов из крови выделяются белые кровяные тельца (сражающиеся клетки нашей иммунной системы), оставшуюся кровь вводят пациенту обратно (процедура лейкафереза). Белые кровяные тельца, называемые отделенными дентритными клетками, в лабораторной среде начинают стимулироваться посредством специфического антигена простаты – белка рака предстательной железы (РАР) и факторов роста иммунных клеток (GM-CSF). Можно использовать после подготовки, спустя три дня. Вакцина вводится с перерывом в две недели, всего три раза. Кому подходит лечение посредством вакцин? Лечение вакциной подходит больным раком предстательной железы на продвинутой стадии, с распространением в организме, с устойчивостью к гормональному лечению. Несмотря на то, что в ходе проведенных исследований наблюдалось преимущество с точки зрения выживаемости, все же нельзя говорить о том, что в данном случае вакцина является панацеей. После лечения может не наблюдаться снижения уровня специфического антигена простаты (ПСА). Вакцина против злокачественного меланомного рака кожи Talimogene Laherparepvec (IMLYGIC) В этой вакцине используются генетические модифицированные вирусы, на получила утверждение от Американского агентства по контролю за пищевыми продуктами и лекарственными препаратами (FDA) 25 октября 2015 года. Вакцина разрешается к использованию в местном (локальном) лечении повреждений ткани при меланоме, распространившейся в лимфатическом узле, под кожей или на коже, которую невозможно удалить во время операции и которая возобновилась после проведения первого хирургического вмешательства. В вакцинах использованы генетически модифицированные вирусы (ниже представлена подробная информация об онколитических вирусных вакцинах). Вакцина против меланомы под названием Talimogene laherparepvec вводится непосредственно меланомную внутрь опухоли, которая возобновилась и которую невозможно удалить хирургическим способом. В исследовании данной вакцины, получившей утверждение от Американского агентства по контролю за пищевыми продуктами и лекарственными препаратами (FDA), приняло участие 436 больных меланомой. Одной группе этих больных вводилась вакцина Imlygic, другой группе был применен колоно-стимулирующий фактор granulocyte-macrophage (GM-CSF). В результате у 16% тех, кому применялась вакцина Imlygic, наблюдалось значительное уменьшение в повреждении кожи и лимфатического узла, при этом тех же результатов у другой группы (GM-CSF) удалось достичь лишь в объеме 2%. Вместе с тем, при talimogene laherparepvec не удалось добиться увеличения выживаемости или значительной регрессии при меланоме, распространенной в мозг, кости, печень, легкие или в другие органы. Дальнейшая информация для тех, кто интересуется наукой: все разновидности иммунотерапии, которая используется при онкологических заболеваниях, и другие прививки от рака 1. Активаторы иммунной системы, не свойственные заболеванию Первым вдохновением для современной иммунотерапии явились токсины Коли, и ученые нацелились на увеличение ответной реакции иммунной системы на различные виды патогенов и рака. В результате такого рода практик была получена ответная реакция со стороны иммунной системы, не присущая заболеванию (неспецифическая), которое необходимо было вылечить. Такие неспецифические иммунотерапии до сих пор помогают нам в лечении некоторых видов рака. Вакцина BCG Первым иммунотерапевтическим лекарством стало BCG (Bacillus Calmette-Guerin) – ослабленная форма бактерии, которая приводит к возникновению туберкулеза (БЦЖ). На протяжении 20 лет вакцина БЦЖ использовалась в качестве вакцины против туберкулеза. К 1990 году после десятилетних испытаний данной вакцины при многих видах рака было получено разрешение на использованием только при раке мочевого пузыря, и в настоящее время это является основным лечением данного вида рака. Цитокины Цитокины представляют собой молекулы, которые используются при взаимодействии клеток иммунной системы между собой. Они используются в качестве иммунотерапевтических препаратов (неспецифических), не свойственных заболеванию. Они играют роль в распознавании опухоли со стороны иммунной системы. Наиболее известные факторы нейкроза опухоли -(TNFα) и İnterferon alfa (IFNα),- способствуя остановке роста и самоуничтожению клеток, напрямую воздействуют на раковые клетки. İnterLökin-2 (IL-2) и GM-CSF активизируют природные уничтожающие клетки иммунной системы (природный убийца = NK), клетки T и дентрические клетки. Среди этих молекул, IL-2 используется при злокачественной меланоме и при раке почек. INFα используется при меланоме, хронической миелоцитозной меланоме, при волосатоклеточном лейкозе, при фолликулярной лимфоне не-Ходжкина, и при саркоме Капоши. Адъюванты Адъюванты также являются неспецифическими иммунными стимуляторами, и часто используются вместе с вакцинами для того, чтобы создать более мощную ответную реакцию иммунной системы. Часто используемые адъюванты являются продуктами бактерий молекул и агонистами TLR (Toll-like receptor). Кроме того, GM-CSF, стимулирующий дентрические клетки, являющийся одним из важных элементов иммунной системы, часто используется в качестве адъюванта вакцины от рака.2. Иммунотерапия с помощью антител Иммунотерапевтические препараты, о которых уже упоминалось выше, как правило, стимулируют клетки иммунной системы, не нацеливаясь при этом на определенный антиген (специфическая молекула белка). В этом разделе мы рассмотрим иммунотерапевтические препараты, которые называются «специфической иммунотерапией» за то, что они нацеливаются именно на определенный антиген. Моноклональные антитела Антитела представляют собой белки, которые производятся иммунной системой, задачей которых является наша защита от патогенных и раковых клеток. Начиная с 1970-х годов эти очищенные молекулы высокой избирательности, способные образовываться в лабораторной среде, принято называть «моноклональными антителами». Область применения моноклональных антител довольно широка.
Герцептин (название действующего вещества: «Трастузумаб») является одним из моноклональных антител, которые были впервые использованы в области онкологии, он сумел изменить историю лечения рака груди. В 25-30% случаев рака груди на поверхности клеток объем рецептора HER2 превышает норму, при этом данный рецептор отвечает за контроль роста и размножения клеток. Герцептин предотвращает активностьэтого важного рецептора роста, и убивает клетку. Моноклональные антитела нацелены на специфические объекты, поэтому они обладают довольно низкими проявлениями побочных действий. Вместе с тем, эти лекарства в большинстве случаев не могут обеспечить полное лечение (курс). Со временем может развиться устойчивость к этилам. Биспецифические антитела «Биспицефические антитела», являющиеся новой формой терапии с антителами, представляют собой молекулы, запрограммированные на две разные цели посредством генетической инженерии. Это протеины, которые образуются путем соединения друг с другом двух различных с физической точки зрения моноклональных антител. Самой распространенной формой биспицефических антител являются продукты генетической инженерии, которые известны под названием биспицефических T-cell engagers (BITEs), способных с одной стороны прикрепляться к Т-клетке, с другой стороны к раковой клетке. Примером BITE, получившим утверждение от Американского агентства по контролю за пищевыми продуктами и лекарственными препаратами (FDA), служит препарат под названием «Блинатумомаб», который используется в лечении В-клеточной лейкемии. Это лекарство прикрепляется с одной стороны к CD3, расположенной на поверхности Т клетки, и с другой стороны к молекулам под названием CD19, расположенным на поверхности опухолевой клетки. 3. Вакцины против рака Основной причиной утраты жизни при онкологическом заболевании является «оккупация» другой ткани и органов раковыми клетками. Это явление называется метастазами. Согласно последним проведенным исследованиям, было установлено, что метастазы ответственны за 90 процентов смертей в результате онкологии. Отсутствие желаемого успеха в лечении, которое применяется при онкологического заболевании с метастазами, то есть при четвертой стадии, а также появление последствий в виде ряда побочных явлений подтолкнуло ученых специалистов к разработке новых методов лечения рака. За последние годы вакцины против рака приобрели большую популярность, и большое количество фирм сосредоточилось на исследованиях в данной связи., Итак, вакцины против рака можно разделить на две группы. Это:
С 1900-х годов стало известно, что вирусы приводят к развитию рака. Согласно последнему отчету, опубликованному Всемирной организацией здравоохранения, 15 процентов рака, которые возникают по всему миру, связаны с вирусами. Большинство видов рака, связанных с вирусами, наблюдается в мало развитых и в развивающихся странах. Причиной тому служит не регулярное выполнение программы вакцинации и не соблюдение необходимых правил гигиены. Главным определением, которое используется для таких вирусов, служит «онковирусы». Клетки онковирусов инфицируют, то есть проникают внутрь органов и приобретают контроль над клетками. Это свойство они используются для того, чтобы размножаться. Насколько известно, в наших клетках существует ДНК, контролирующая основные процессы. Вирусы присоединяются к ДНК клеток, в которые они вводят собственную генетическую информацию. Клетки с нарушенным геном, начинают бесконтрольно делиться и размножаться. В результате развивается рак. Как будет рассмотрено далее, некоторые вирусы тормозят активность генов, подавляющих опухоль, и некоторые вирусы добавляют онкогены к клеткам (гены, провоцирующие рост клеток). Вирусы, являющиеся причиной возникновения рака, которые удалось установить на сегодняшний день, и виды рака представлены ниже.
В 2006 году вакцины под названием Gardasil и Cervarix, стали поставляться на рынок, получив утверждение от Американского агентства по контролю за пищевыми продуктами и лекарственными препаратами (FDA) в 2006 году, и благодаря ним в организме человека начинает вырабатываться иммунитет против вируса HPV. Вакцину Gardasil рекомендуют применять до периода полового созревания и в начале ведения активной половой жизни. Не следует забывать, что для тех, кто уже инфицировался, эти вакцины не будут обладать защитным, то есть профилактическим действием. Вакцина Gardasil получила утверждение более, чем в 120 странах. Вакцины против рака шейки матки в нашей стране также доступны в продаже. В ходе последних проведенных исследований было установлено, что в странах, в которых выполняется программа вакцинации, частота возникновения рака шейки матки снижена. b. Терапевтические прививки от рака (обладающие лечебным действием) Прививки от рака, разработанные с целью лечения, образуют крепкий иммунитет против раковых клеток, или нацелены на убийство раковой клетки с вирусом, созданным посредством генетических технологий. Защитные вакцины формируют иммунитет от вирусов, вызывающих рак, именуемых «онковирусами». Одним из основных принципов работы вакцин от рака, разработанных с целью лечения, является устранение раковых клеток, с использованием «вирусов». Вирусы, которые используются при разработке данных вакцин, называются онколитическим вирусами. Слово «онколитический» обозначает «уничтожающий опухоль». С этой целью вирусы нацеливаются только на раковую клетку и уничтожают ее. Когда созданный при помощи генетических техник вирус проникает в здоровую клетку, он не наносит ей никакого вреда. Но в раковых клетках, проникая внутрь, вирус начинает размножаться, вызывает взрыв раковой клетки и приводит в итоге к ее гибели. В последнее время в области лечения онкологических заболеваний было разработано большое количество вакцин с онколитическим вирусом. Большинство из них в настоящее время находится на стадии разработки и клинических исследований, и в рутинную практику они до сих пор не введены. Отсутствует какая-либо одна вакцина с онколитическим вирусом, которая была бы разработана для всех видов рака. Ниже вы можете узнать про вакцины с онколитическими вирусами, над которыми до сих пор продолжаются клинические исследования, и которые в ближайшее время ожидают получить разрешение для использование. Talimogene laherparepvec (T-VEC, OncoVEX): Вакцина получила утверждение от Американского агентства по контролю за пищевыми продуктами и лекарственными препаратами (FDA) для лечения меланомного рака кожи.
Разновидности лечебных вакцин против рака:
Вакцины против опухолевых клеток могут выполняться из собственных опухолевых клеток больного, Такого рода вакцины являются индивидуальными, и называются «Отологическими» вакцинами. Для того, чтобы можно было сделать вакцину, не каждое время может быть подходящим для того, чтобы взять раковые клетки у больного в достаточном количестве. Поэтому вакцины могут также выполняться и посредством опухолевых клеток разных больных, у которых обнаружен одинаковый тип раковой опухоли. Такого рода вакцины называются «Аллогенными». Вакцины на основе дендритных клеток Дендритные клетки представляют собой вид белых кровяных телец. Основной функцией служит активация иммунной системы, обеспечивающей борьбу организма против инфекции, вырабатывая антиген. Дендритные вакцины получаются путем смешивания раковых клеток с дендритными клетками в лабораторной среде. Дендритные клетки, которые активируются посредством дендритов, принадлежащих раковым клеткам, возвращаются больному и помогают иммунной системе распознавать раковые клетки и уничтожать их. Вакцины на основе дендритных клеток являются индивидуальными. Вакцины ДНК Действие антираковых вакцин начинается снижаться со временем. Причиной тому служит возвращение иммунной системы к прежнему режиму работы со временем. В исследованиях, проведенных в последнее время, было установлено, что вакцины, содержащие ДНК, в течение более длительного времени активируют иммунную систему организма. Это связано с тем, что обеспечивается постоянная выработка антигена. Насколько известно, механизмом управления клеток является ДНК. ДНК в раковых клетках содержит генетическую информацию, которая производится белками (антигенами) раковых клеток. Эти части ДНК содержат более одного антигена, дающего возможность для создания вакцины. ДНК, содержащая генетическую информацию антигенов рака, вводятся больному в лабораторной среде. Клетки встраиваются в структуру этого ДНК, образуют антигены, присущие раковой клетке, и, активируя иммунную систему, обеспечивают нацеливание на раковые клетки. Вакцины на основе антигенов Вакцины на основе антигенов нацелены на активацию иммунной системы, используя части протеинов или определенные протеины на поверхности раковых клеток. В то же время раковые антигены смешиваются с молекулами, обеспечивающими более эффективную работу вакцины. Эти молекулы называются адъювантными. Адъюванты помогают организму распознавать чужеродные клетки и образовывать реакцию иммунной системы. В качестве примера адъюванта можно назвать цитокины (интерлокин 2). CimaVax-EGF известна под названием «кубинская вакцина», она также относится к данному классу вакцин. В этой вакцине больному вводится молекула под названием EGF (антиген), которая обогащается адъювантами. Целью является создание иммунной реакции через клетки, дающие антиген больному, и через клетки В, образующие антитела. EGF соединяется к собственному рецептору (EGFR), который в большом количеству находится на поверхности определенных раковых клеток. Ученые стараются соединить EGF антител, которые провоцируются в результате вакцины, и предотвратить распространение сигнала роста и размножения от рецептора EGFR в раковой клетке.
Некоторые вакцины на основе антигенов обеспечивают только иммунную реакцию против определенного вида рака. Исследования, которые проводились в последние годы, были сосредоточены на сборе в одной вакцине несколько антигенов и на более быстром распознавании иммунной системой этих антигенов. Вакцины на основе анти-идиотипов Антитела анти-идиотипов – это антитела, которые были произведены для имитации определенного антигена. Некоторые антигены, характерные для определенного вида рака, расположенные на поверхности раковой клетки (например, гликолипиды), не могут распознаваться иммунной системой. Для того, чтобы иммунная система смогла распознать эти структуры, в настоящее время проводятся испытания, направленные на то, чтобы разработать антираковые вакцины в лабораторной среде на основе антител анти-идиотипов, которые могут имитировать эти структуры. Эти вакцины обеспечивают выработку антител в организме человека против раковых клеток. Другими словами, вакцина оказывает воздействие в качестве антигенов раковой клетки. При инъекции вакцины, обеспечивается распознавание иммунной системой антигенов, расположенных на раковой клетке.
Научная критика на вакцины, произведенные на Кубе Здесь необходимо особо отметить, что вакцины CimaVax и Vaxira не обещают непременного лечения рака легких. Производители вакцины ставят на этом особый акцент.
Будьте здоровы и счастливы...Профессор Д-р Мустафа Оздоган Информация, представленная в данной статье, предназначена только для информационных целей, для диагностики и лечения обязательно обратитесь к врачу. www.oncotrust.ru |
г.Самара, ул. Димитрова 131 [email protected] |
 |