|
|
||||||||||
|
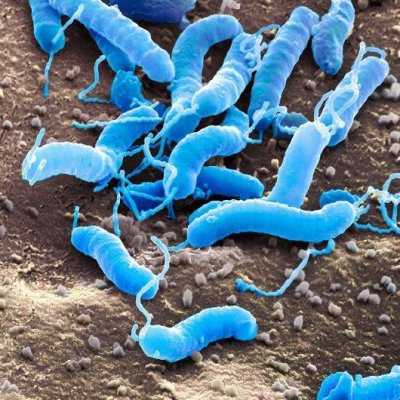
Развитие у микроорганизмов устойчивости к антибиотикам. Возникновению устойчивости микрофлоры к антибиотику способствуетРазвитие у микроорганизмов устойчивости к антибиотикамДанные о появлении устойчивых к аптибиотикам микроорганизмов у животных, леченных антибиотиками, очень разноречивы. В. И. Ежов изучал штаммы пастерелл от птицы в 12 хозяйствах Краснодарского края, где с лечебной целью длительно применяли тетрациклиновые антибиотики. Ни в одном случае он не обнаружил появления устойчивых рас. Такие же результаты получены при изучении 209 штаммов пастерелл в других хозяйствах, где тетрациклиновые препараты применяли с лечебно-профилактической целью в течение 1—5 месяцев. А. X. Саркисов и Е. Т. Тришкина за последние 10 лет изучили антибиотикоустойчивость у 2285 различных патогенных микроорганизмов (возбудители рожи свиней, пуллороза цыплят, пастереллеза птиц, сальмонеллеза свиней, телят и птиц и др.), выделенных у разных животных, и не установили сколько-нибудь закономерно разврвающейся устойчивости их к антибиотикам. В. А. Фортушиый, И. Н. Гладенко и И. И. Шмидов обращают внимание на то, что в хозяйствах Украинской ССР они часто встречались с явлениями развития антибиотикорезистентности кишечной палочки, сальмонелл и др. Например, при лечении свиней, больных паратифом, стрептомицином устойчивость выделяемых возбудителей болезни к нему все время возрастала: через 5 дней с начала лечения для угнетения роста пастерелл требовалось 10—59,5 мкг/мл стрептомицина, через 15 дней — уже 58,5—117 мкг/мл, через 25 дней — 58,5— 234 мкг/мл, а через 2 месяца— 117—936 мкг/мл. На возможность появления устойчивости у патогенных возбудителей в хозяйственных условиях указывают также Н. И. Леонов, Л. С. Каврук и др. Такие же противоречивые данные о развитии у микробов аптибиотикоустойчивости имеются и в иностранной литературе. Г. Мантель и X. Кампельмахер отрицают возможность быстрого развития такой устойчивости у микробов в хозяйствах, а К. Ремси, С. Эдверс и некоторые другие ученые приводят четкие доказательства ее появления. Все это затрудняет ориентацию практических работников. Однако возможность образования рас микробов, устойчивых к отдельным антибиотикам, доказана в лабораторных условиях й в медицинской практике. Ее не отрицают и те исследователи, которые не обнаружили устойчивых микробов в хозяйствах, где применяют антибиотики. Все дело заключается в том, что антибиотикоустойчивость развивается неодинаково у возбудителей разного вида при различных условиях антмбиотикотерапии. Развитие устойчивости у микроорганизмов обусловлено ослаблением или незначительным нарушением жизненно важных процессов метаболизма и поддержанием этих биохимических процессов на уровне, позволяющем сохранить жизнь микроорганизма. Наиболее часто в основе развития устойчивости лежит ослабление синтеза микробного белка вследствие деформации некоторой части матриц или изменения отдельных свойств каких-то аминокислот в разных биохимических реакциях. Так как в любой клетке пластический белок может образовываться несколькими путями, то при нарушении основных путей совершенствуются резервные, которые неуязвимы для данного антибиотика. Нередко устойчивость развивается вследствие того, что в ответ на введенный антибиотик в клетке постепенно создаются условия, повышающие способность клетки разрушать вещества. Антибиотик разрушается настолько быстро, что даже в больших дозах он уже не успевает оказать противомикробное влияние. Иногда в ответ на частичное разрушение антибиотиками отдельных ферментов в клетке увеличивается производство их в десятки и даже сотни раз. В таких случаях антибиотик действует слабо или совсем не действует. В отдельных условиях при умеренном неблагоприятном влиянии антибиотиков в микробной клетке резко ослабевает резорбция их, а иногда и адсорбция оболочкой микроба. Одной из важных форм резистентности микробов к антибиотикам служит природная устойчивость того или иного процента микроорганизмов к антибиотику. В различных условиях она колеблется от 0,01 до 20% и выше. В таких случаях антибиотик не влияет на более стойкие особи микробов. Более того, о« в той или иной мере улучшает условия для их размножения. В результате через некоторое время после лечения у животных обнаруживают рецидив болезни, но уже вызванный возбудителем, устойчивым к антибиотику. В практике следует больше уделять внимания антибиотикоустойчивости микробов, так как она развивается не только при неправильном использовании этих веществ, а и под воздействием отдельных аминокислот, при недостатке некоторых витаминов и др. Чтобы предупредить возникновение и развитие антибиотикоустойчивости, нужно применять антибиотики строго по показаниям и только в самых необходимых случаях, точно определять рациональные дозы и срок лечения, доводить начатое лечение до конца и не отменять его, несмотря на видимое улучшение в состоянии больного. Кроме того, чтобы избежать появления антибиотикоустойчивых рас микробов, нужно в каждом хозяйстве применять для лечения несколько антибиотиков с разным механизмом действия. Для комбинированной терапии нужно подбирать препараты также с различным механизмом действия, н обязательно синергисты. Полезно одновременно с антибиотиками назначать) нитрофурановые препараты, висмутовые, йодистые, сульфаниламиды и др. Для быстрого излечения больного животного и препятствия возникновению устойчивых микроорганизмов необходимо, кроме назначения антибиотика стимулировать макроорганизм введением неспецифических (кофеин, гемотерапия и др.) и специфических (вакцины, сыворотки) средств. В хозяйстве, где существует инфекция, целесообразно изучить уровень антибиотикоустойчивости, темпы и динамику ее нарастания, а также продолжительность сохранения. Это особенно важно проводить там, где антибиотики широко применяли с лечебной и профилактической целями при колмбактериозе, паратифе молодняка, пуллорозе цыплят, паратифе водоплавающей птицы, мастите коров и некоторых других болезнях. Повышение устойчивости микроорганизмов к антибиотикам безусловно неблагоприятное явление, если оно касается возбудителей болезней. Но это же явление будет иметь совсем другое значение, если оно касается физиологической микрофлоры животных. Повышение устойчивости физиологической микрофлоры ценно потому, что исключает нарушение ее функции при длительном применении антибиотиков для ускорения роста животных. Кроме того, как это было указано нами еще в 1957 г., от малых доз антибиотиков повышается резистентность физиологической микрофлоры к большому количеству ядов, токсинов и патогенных микробов, попадающих в организм животного. В некоторых условиях возможно образование зависимости микробов от антибиотиков, то есть создается такое состояние, когда микробы не могут развиваться без антибиотиков. Это явление бывает при культивировании микроорганизмов в средах, содержащих небольшие количества препарата (в 10—1000 раз меньше средней бактериостатической). Установлено, что зависимость быстрее. развивается к тем же антибиотикам, что и резистентность. В экспериментах доказана возможность образования зависимости и у экспериментальных животных, но в широкой практике при назначении антибиотиков как стимуляторов роста животных зависимость не обнаружена. Если вы нашли ошибку, пожалуйста, выделите фрагмент текста и нажмите Ctrl+Enter. www.activestudy.info Антибиотикорезистентность: механизмы и пути ее преодоленияМеханизмы антибиотикорезистентностиВ последнее время антибиотикорезистентность стала проблемой номер один в фармакологической промышленности, занимающейся разработкой противомикробных препаратов. Все дело в том, что она свойственная практически всем известным разновидностям бактерий, в связи с чем терапия антибиотиками становится все менее эффективной. Такие распространенные патогенные микроорганизмы, как стафилококки, кишечная и синегнойная палочка, протеи имеют устойчивые штаммы, которые распространены более своих предков, подверженных воздействию антибиотиков. Резистентность к различным группам антибиотиков, и даже к отдельным препаратам, развивается по-разному. Старые добрые пенициллины и тетрациклины, а также более новые разработки в виде цефалоспоринов и аминогликозидов характеризуются медленным развитием антибиотикорезистентности, параллельно с эти снижается и их терапевтический эффект. Чего нельзя сказать о таких препаратах, действующим веществом которых является стрептомицин, эритромицин, римфампицин и линкомицин. Резистентность к этим препаратам развивается стремительным темпом, в связи с чем назначение приходится менять даже в течение курса лечения, не дожидаясь его окончания. То же самое касается препаратов олеандомицина и фузидина. Все это дает основание предположить, что механизмы развития антибиотикорезистентности к различным препаратам значительно отличаются. Попробуем разобраться, какие свойства бактерий (природные или приобретенные) не позволяют антибиотикам производить их иррадикацию, как это задумано изначально. Для начала определимся с тем, что резистентность у бактерии может быть природной (защитные функции, дарованные ей изначально) и приобретенной, о которой мы говорили выше. До сих пор мы в основном говорили об истинной антибиотикорезистентности, связанной с особенностями микроорганизма, а не с некорректным выбором или назначением препарата ( в этом случае речь идет о ложной антибиотикорезистентности). Каждое живое существо, включая простейших, имеет свое неповторимое строение и некоторые свойства, позволяющие ему выживать. Все это закладывается генетически и передается из поколения в поколение. Природная резистентность к конкретным действующим веществам антибиотиков также заложена генетически. Причем у разных видов бактерий резистентность направлена на определенный вид препаратов, с чем и связана разработка различных групп антибиотиков, воздействующих на отдельно взятый вид бактерий. Факторы, которые обуславливают природную резистентность, могут быть различными. Например, структура белковой оболочки микроорганизма может быть такова, что антибиотику не под силу с ним справиться. А ведь антибиотикам под силу повлиять лишь на белковую молекулу, разрушая ее и вызывая гибель микроорганизма. Разработка эффективных антибиотиков подразумевает учет строения белков бактерий, против которых направлено действие препарата. Например, антибиотикорезистентность стафилококков в отношении аминогликозидов связана с тем, что последние не могут проникнуть сквозь микробную оболочку. Вся поверхность микроба покрыта рецепторами, с отдельными видами которых и связываются АМП. Малое количество подходящих рецепторов или их полное отсутствие приводят к тому, что связывания не происходит, а значит и антибактериальный эффект отсутствует. Среди прочих рецепторов есть и такие, которые для антибиотика служат своеобразным маячком, сигнализирующим о местоположении бактерии. Отсутствие таких рецепторов позволяет микроорганизму скрываться от опасности в виде АМП, что является своеобразной маскировкой. У некоторых микроорганизмов есть природная способность активно выводить АМП из клетки. Такая способность называется эффлюксом и она характеризует резистентность синегнойной палочки в отношении карбапенемов. Биохимический механизм антибиотикорезистентностиКроме перечисленных выше природных механизмов развития антибиотикорезистентности существует еще один, связанный не со строением бактериальной клетки, а с ее функционалом. Дело в том, что в организме бактерии могут вырабатываться ферменты, способные оказывать негативное действие на молекулы активного вещества АМП и снижать его эффективность. Бактерии при взаимодействии с таким антибиотиком тоже страдают, их действие заметно ослабляется, что создает видимость излечения от инфекции. Тем не менее, пациент остается носителем бактериальной инфекции еще некоторое время после так называемого «выздоровления». В этом случае мы имеем дело с модификацией антибиотика, в результате чего он становится неактивным в отношении данного вида бактерий. Ферменты, вырабатываемые разными видами бактерий, могут отличаться. Для стафилококков характерен синтез бета-лактамазы, провоцирующей разрыв лактемного кольца антибиотиков пенициллинового ряда. Выработкой ацетилтрансферазы можно объяснить устойчивость к хлорамфениколу граммотрицательных бактерий и т.д. Приобретенная антибиотикорезистентностьБактериям, как и другим организмам, не чужда эволюция. В ответ на «военные» действия в их отношении, микроорганизмы могут изменять свою структуру или начать синтезировать такое количество ферментного вещества, которое способно не только снижать эффективность препарата, но и разрушать его полностью. Например, активная выработка аланинтрансферазы делает «Циклосерин» неэффективным в отношении бактерий, продуцирующих ее в больших количествах. Антибиотикорезистентность может развиваться и вследствие модификации в структуре клетки белка, являющегося одновременно и ее рецептором, с которым должен связываться АМП. Т.е. данный вид белка может отсутствовать в бактериальной хромосоме или изменить свои свойства, в результате чего связь между бактерией и антибиотиком становится невозможной. Например, утрата или видоизменение пенициллинсвязывающего белка становится причиной нечувствительности к пенициллинам и цефалоспоринам. В результате развития и активации защитных функций у бактерий, ранее подверженных разрушительному действию определенного вида антибиотикив, изменяется проницаемость клеточной мембраны. Это может быть осуществлено за счет уменьшения каналов, по которым действующие вещества АМП могут проникнуть внутрь клетки. Именно эти свойством обусловлена нечувствительность стрептококков к бета-лактамным антибиотикам. Антибиотики способны влиять на клеточный метаболизм бактерий. В ответ на это некоторые микроорганизмы научились обходиться без химический реакций, на которые воздействует антибиотик, что также является отдельным механизмом развития антибиотикорезистентности, который требует постоянного контроля. Иногда бактерии идут на определенную хитрость. Путем присоединения к плотной субстанции они объединяются в сообщества, именуемые биопленкой. В рамках сообщества они являются менее чувствительными к антибиотикам и могут спокойно переносить дозировки, убийственные для отдельно взятой бактерии, обитающей вне «коллектива». Еще один вариант – это объединение микроорганизмов в группы на поверхности полужидкой среды. Даже после деления клеток часть бактериальной «семьи» остается внутри «группировки», не поддающейся влиянию антибиотиков. Гены антибиотикорезистентностиСуществуют понятия генетической и негенетической лекарственной резистентности. С последней мы имеем дело, когда рассматриваем бактерии с неактивным метаболизмом, не склонные к размножению в обычных условиях. У таких бактерий может вырабатываться антибиотикорезистентность к определенным видам препаратов, тем не менее, их потомству эта способность не передается, поскольку она не заложена генетически. Это свойственно патогенным микроорганизмам, вызывающим туберкулез. Человек может заразиться и не подозревать о болезни долгие годы, пока его иммунитет в силу каких-то причин не даст сбой. Этой является толчком к размножению микобактерий и прогрессированию болезни. Но для лечения туберкулеза используются все те же препараты, вед бактериальное потомство по-прежнему остается чувствительным к ним. Точно так же обстоит дело и с утратой белка в составе клеточной стенки микроорганизмов. Вспомним, опять же о бактериях, чувствительных к пенициллину. Пенициллины тормозят синтез белка, служащего для построения клеточной оболочки. Под воздействием АМП пенициллинового ряда микроорганизмы могут утрачивать стенку клеток, строительным материалом которой является пенициллинсвязывающий белок. Такие бактерии становятся резистентными к пенициллинам и цефалоспоринам, которым теперь не с чем связываться. Это явление временное, не связанное с мутацией генов и передачей видоизмененного гена по наследству. С появлением клеточной стенки, свойственной предыдущим популяциям, антибиотикорезистентность у таких бактерий исчезает. О генетической антибиотикорезистентности говорят, когда изменения в клетках и метаболизме внутри них происходят на уровне генов. Мутации генов могут вызывать изменения в структуре клеточной мембраны, провоцировать выработку ферментов, защищающих бактерии от антибиотиков, а также изменять количество и свойства рецепторов бактериальной клетки. Здесь существует 2 пути развития событий: хромосомный и внехромосомный. Если происходит мутация гена на том участке хромосомы, который отвечает за чувствительность к антибиотикам, говорят о хромосомной антибиотикорезистентности. Сама по себе такая мутация возникает крайне редко, обычно ее вызывает действие лекарств, но опять-таки не всегда. Контролировать это процесс очень сложно. Хромосомные мутации могут передаваться из поколения в поколение, постепенно формируя определенные штаммы (разновидности) бактерий, устойчивых к тому или иному антибиотику. Виновниками внехромосомной резистентности к антибиотикам становятся генетические элементы, существующие вне хромосом и называемые плазмидами. Именно эти элементы содержат гены, ответственные за выработку ферментов и проницаемость бактериальной стенки. Антибиотикорезистентность чаще всего является результатом горизонтального переноса генов, когда одни бактерии передают некоторые гены другим, не являющимся их потомками. Но иногда можно наблюдать и несвязанные точечные мутации в геноме патогена (размер 1 в 108 за один процесс копирования ДНК материнской клетки, что наблюдается при репликации хромосом). Так осенью 2015 года ученые из Китая описали ген MCR-1, обнаруженный в свином мясе и кишечнике свиней. Особенностью этого гена является возможность его передачи другим организмам. Спустя некоторое время этот же ген был найден не только в Китае, но и в других странах (США, Англия, Малайзия, страны Европы). Гены антибиотикорезистентности способны стимулировать выработку ферментов, которые ранее не вырабатывались в организме бактерий. Например, фермент NDM-1(металло-бета-лактамаза 1), обнаруженный у бактерий Klebsiella pneumoniae в 2008 году. Сначала он был обнаружен у бактерий родом из Индии. Но в последующие годы фермент, обеспечивающий антибиотикорезистентность относительно большинства АМП, был выявлен у микроорганизмов и в других странах (Великобритания, Пакистан, США, Япония, Канада). Патогенные микроорганизмы могут проявлять устойчивость как по отношению к определенным препаратам или группам антибиотиков, так и относительно различных групп препаратов. Существует такое понятие, как перекрестная антибиотикорезистентность, когда микроорганизмы становятся нечувствительными к препаратам со сходным химическим строением или механизмом воздействия на бактерии. Антибиотикорезистентность стафилококковСтафилококковая инфекция считается одной из самых распространенных среди внебольничных инфекций. Впрочем, даже в условиях стационара на поверхностях различных объектов можно обнаружить порядка 45 различных штаммов стафилококка. Это говорит о том, что борьба с этой инфекцией является чуть ли не первоочередной задачей медработников. Трудность выполнения этой задачи заключается в том, что большинство штаммов наиболее патогенных стафилококков Staphylococcus epidermidis и Staphylococcus aureus являются резистентными ко многим видам антибиотиков. И количество таких штаммов растет с каждым годом. Способность стафилококков к множественным генетическим мутациям в зависимости от условий обитания делает их практически неуязвимыми. Мутации передаются потомкам и в краткие сроки появляются целые генерации устойчивых к антимикробным препаратам инфекционных возбудителей из рода стафилококков. Самая большая проблема – это метициллинорезистентные штаммы, которые являются устойчивыми не только к бета-лактамам (β-лактамным антибиотикам: определенные подгруппы пенициллинов, цефалоспоринов, карбапенемов и монобактамов), но и другим видам АМП: тетрациклинам, макролидам, линкозамидам, аминогликозидам, фторхинолонам, хлорамфениколу. Продолжительное время уничтожить инфекцию можно было только при помощи гликопептидов. В настоящее время проблема антибиотикорезистентности таких штаммов стафилококка решается посредством нового вида АМП – оксазолидинонов, ярким представителем которых является линезолид. ilive.com.ua Судьба антибиотиков | Журнал Популярная МеханикаС появлением антибиотиков человечеству стало казаться, что многие болезни отступили навсегда. Но увы, вскоре оказалось, что бактерии быстро вырабатывают устойчивость к этим препаратам. Ученые разрабатывали все новые антибиотики, но и к ним микроорганизмы рано или поздно приспосабливались. Кто же победит в этой неумолимой гонке вооружений — люди или микробы? Александр Чубенко 1 сентября 2016 19:30 Доклад генерального директора ВОЗ Маргарет Чен «Устойчивость к противомикробным препаратам в Европейском союзе и в мире» на прошедшей в 2012 году в Копенгагене конференции «Борьба с устойчивостью к противомикробным препаратам — время действовать» произвел эффект разорвавшейся бомбы. Хотя скорее это было похоже на вскрытие давно назревшего нарыва: то, что микробы быстро приобретают устойчивость к антибиотикам, Александр Флеминг заметил еще до того, как во время Второй мировой войны началось промышленное производство пенициллина. Несколько десятков лет после появления пенициллина фармакологи продолжали разрабатывать новые антибиотики, врачи — успешно их применять, и к концу 1970-х казалось, что инфекционным болезням скоро настанет конец… но конец настал оптимистичным прогнозам. Тем более что активная разработка более эффективных модификаций известных классов антибиотиков по многим, в том числе финансовым причинам в последние десятилетия постепенно сокращалась. А последний новый класс — фторхинолоны — появился в 1980 году. Да и их с тех пор только модифицировали и совершенствовали. Рост числа устойчивых штаммов специалисты обсуждали и 20, и 30 лет назад, но в подавляющем большинстве случаев в узкоспециализированных научных журналах. В 2001 году, когда стало окончательно ясно, что фармпромышленность проигрывает в гонке с патогенами, ВОЗ обнародовала Глобальную стратегию по сдерживанию кризиса резистентности к противомикробным препаратам. Но призыв срочно приступить к решению проблемы совпал с терактами 11 сентября и письмами со спорами сибирской язвы, переключившими внимание общественности и правительств на борьбу с терроризмом. Только после конференции в Копенгагене в СМИ наконец началась паника. И хотя в популярных статьях ужасы грядущего конца света часто сильно преувеличивают, шумиха вокруг наступления постантибиотиковой эры пошла на пользу разработчикам антимикробных средств: о проблеме задумались не только специалисты, но и грантодатели, и фармкомпании. Самые опасныеВ опубликованном осенью 2013 года Центрами по контролю и профилактике заболеваний США (CDC) докладе «Угроза устойчивости к антибиотикам в Соединенных Штатах» (Antibiotic resistance threats in the United States, 2013) перечислено около 15 наиболее опасных и распространенных штаммов и групп «супермикробов», распределенных по трем степеням угрозы здоровью населения. К первой группе — микробов, «представляющих наибольшую угрозу и требующих немедленного реагирования» — авторы отнесли возбудителей псевдомембранозного колита и гонореи, а также энтеробактерии. Устойчивость по наследству Гены устойчивости можно получить с помощью вертикального переноса — по наследству от родительской клетки, горизонтального — в результате конъюгации — своеобразного полового процесса, при котором бактерии соединяются участками клеточных стенок и обмениваются генами, или с помощью бактериофагов, которые, разбегаясь из убитой бактерии, могут вместе со своими генами прихватить участок микробной ДНК, передать ее следующей зараженной бактерии и погибнуть под действием бактериального иммунитета. Как развивается антибиотикорезистентность: 1. Из множества бактерий хотя бы несколько оказываются устойчивыми к применяемому антибиотику. 2. Антибиотики уничтожают чувствительных к ним виновников болезни и нарушают состав полезной микрофлоры, защищающей организм от инфекций. 3. В результате выжившим патогенным бактериям становится легче плодиться и размножаться. 4. Часть из них передает гены, обеспечивающие антибиотикорезистентность, другим бактериям, на которых данный антибиотик при повторном применении не подействует. Clostridium difficile, возбудитель псевдомембранозного колита. После курса лечения антибиотиками от любой другой болезни и вызванного им подавления нормальной микрофлоры эта инфекция может проявиться во всем диапазоне кишечных расстройств, от относительно безопасной диареи до перфорации кишки. В 2000 году появился особенно заразный штамм клостридии, устойчивый к фторхинолоновым антибиотикам. Ежегодные потери от этой инфекции в США, по последним данным, около 250 000 заболевших, миллиард долларов на их лечение и 14 000 умерших. Энтеробактерии (бактерии рода Klebsiella и патогенные штаммы кишечной палочки), устойчивые к наиболее сильнодействующим антибиотикам — карбапенемам. В год — 9000 случаев, 600 смертей. Neisseria gonorrhoeae. Реальное число заболевших гонореей в США специалисты оценивают примерно в 820 000 в год — почти в три раза больше, чем по официальной статистике. Распространенность самолечения и нелеченных из-за бессимптомного течения болезни случаев ускорили рост числа штаммов гонококка, устойчивых к одному или нескольким антибиотикам (сейчас их — уже 30%). В 2009 году в Японии был выявлен устойчивый к последней надежде венерологов — цефалоспоринам — штамм H041. Пока он не получил широкого распространения, но если так пойдет и дальше… А оно, несомненно, так и пойдет, и без принятия срочных мер самые пессимистичные прогнозы о «мире без антибиотиков» могут стать реальностью. Ко второй группе супербактерий, «представляющих серьезную угрозу», авторы доклада отнесли устойчивые к флуконазолу дрожжеподобные грибы рода Candida (в том числе вид Candida albicans, известный многим если не по латинскому названию, то по русскому слову «молочница») и 11 бактерий, в том числе самый известный из супермикробов — метициллинрезистентный золотистый стафилококк (MRSA). На его долю приходится от 30 до 60% госпитальных инфекций, причем не в Африке, а в развитых странах, где его эволюцию подстегивали особенно активно. Около трети заболевших умирают даже при самом адекватном лечении. Красивое имя Staphylococcus aureus получил в честь формы колоний при выращивании в культуре («staphyle» — «гроздь винограда», кокки — бактерии округлой формы), а золотистый он потому, что, в отличие от большинства бактерий, от природы бесцветных, окрашен в желто-оранжевый цвет за счет пигмента стафилоксантина. Этот условно-патогенный микроорганизм присутствует на коже и слизистых оболочках 20% населения и, пока с хозяином все в порядке, никак не проявляет своей зловредной сущности. Но при нарушенном иммунитете, попадании в царапины и раны или в кровяное русло (например, с инъекцией или капельницей) он может вызвать множество болезней, начиная с кожных инфекций и заканчивая смертельно опасными заболеваниями, от некротического воспаления легких до менингита. А пищевые продукты, в которых размножился S. aureus, могут привести к пищевому отравлению вплоть до инфекционно-токсического шока. До появления антибиотиков смертность от стафилококковых инфекций в крови или внутренних органах доходила до 90%. После появления пенициллина она начала снижаться, но к 1950 году устойчивость к пенициллину выработали 40% больничных штаммов, а к 1960-му — уже 80%. Некоторое время врачам удалось продержаться за счет новых модификаций антибиотиков того же класса бета-лактамов, но буквально через несколько месяцев и на них коварный микроб начинал вырабатывать гены лактамаз с соответствующей резьбой. Название «метициллинрезистентный» ввели, когда стало ясно, что госпитальные штаммы S. aureus начали сопротивляться самому новому на тот момент (1959) представителю бета-лактамов — метициллину. На это микробам потребовалось всего два года: о первом случае выявления MRSA сообщили в 1961-м. Но примерно до 1990 года заболевания, вызванные MRSA, оставались редкостью, и метициллин продолжали применять, тем более что действующие на MRSA антибиотики других классов (например, гликопептиды или аминогликозиды) имеют слишком много побочных эффектов и/или неудобны в применении (предусматривают только внутривенное введение и постоянный контроль состава крови во избежание передозировки). Некоторое время последней линией обороны был ванкомицин — антибиотик из группы гликопептидов, но уже появились штаммы, устойчивые и к нему. Примерно так же развивается лекарственная устойчивость и у микробов, отнесенных CDC к третьему классу опасности (два штамма стрептококков, устойчивых к эритромицину и клиндамицину, и штамм золотистого стафилококка, устойчивый к ванкомицину). К сожалению, нет никаких оснований надеяться на то, что следующий список супермикробов станет короче. Кто виноват?Врачи продолжают прописывать антибиотики без необходимости — и по инерции, и для страховки от обвинений в бездействии. Там, где антибиотики можно купить без рецепта, пациенты часто принимают их по собственному разумению. В результате около 70% антибиотиков применяется без достаточных оснований (в том числе при вирусных инфекциях, хотя единственный эффект от такого «лечения» — появление штаммов бактерий, устойчивых к данному антибиотику). И даже если антибиотики назначены по показаниям, больше половины пациентов забывают вовремя их принимать и/или заканчивают лечение раньше положенного срока (Флеминг и об этом говорил как о самом эффективном способе выработать у бактерий резистентность к пенициллину). Огромный вклад в искусственный отбор устойчивых штаммов внесли животноводы: в Северной Америке и в Европе (до введения ЕЭС запрета на применение антибиотиков для профилактики болезней и в качестве стимуляторов роста) половина производства противомикробных препаратов работала на сельское хозяйство. Результат — не только нечувствительные к антибиотикам инфекции, которые могут передаваться людям (например, сальмонеллез), но и множество других видов микробов (в том числе патогенных для человека), которые встретились с устойчивыми штаммами в природе и получили от них гены устойчивости. www.popmech.ru Устойчивость микроорганизмов к антибиотикамИстория человечества по данным различных археологических исследований насчитывает от десятков тысяч до 2 млн. лет. Организм человека на протяжении всей истории находился в сложных природных условиях, одной из составляющих которых является микробиологический мир. На сегодняшний день мы продолжаем существовать в среде, наполненной невидимыми организмами, общее количество которых на земном шаре в сотни тысяч раз превышает численность людей нашей планеты. Агрессивность внешней среды, в которой эволюционировал и развивался человек как биологический и социальный вид, предопределяла постоянные повреждения целости человеческого организма, а миграция людей сопровождалась более широким распространением инфекционных заболеваний. Выживание человеческого организма как биологического вида было невозможно без наличия естественных механизмов защиты от инфекций. В условиях отсутствия медицинской науки процесс выживания зависел только от исхода борьбы между возбудителем (микроорганизмом) болезни и организмом хозяина (человеком). Во многих случаях результат этой борьбы был не в пользу человека. Но наиболее важным шагом в борьбе с гнойными заболеваниями стало открытие в середине прошлого века химических соединений, которые могут уничтожать микроорганизмы внутри человеческого организма - антибиотиков: в 1928 году шотландский бактериолог Александр Флеминг заметил бактерицидное действие плесени, а через 12 лет англичанин Хоуард У. Флори установил, что введение вещества, которое производится плесенью, позволяет спасти зараженных в эксперименте животных. В 1945 году Флемингу, Чейни и Флори была присуждена Нобелевская премия за открытие пенициллина. Чашу весов в борьбе между микроорганизмами и человеческим организмом начали склоняться в пользу человека. Казалось, что путь в более 2000 лет завершился полной и безоговорочной победой. Но уже через 16 лет - в 1961 году - появилось первое сообщение о метициллинрезистентном золотистом стафилококке (МRSА), в 1967 году в Австралии была обнаружена первая резистентная к пенициллину бактерия рода Streptococcus pneumoniae. Распространение резистентности стало увеличиваться катастрофическими темпами: уже в 1963 году человечество пережило первую вспышку антибиотикорезистентной инфекции. В конце 60-х годов ХХ века МRSА распространился во всех странах Европы, в 70-х годах - в США, а в 80-х годах данный возбудитель оказывался во всех странах мира. В начале XXI века были обнаружены Внегоспитальные штаммы МRSА. В 1997 году в Японии и США были впервые зарегистрированы ванкомицинрезистентные штаммы золотистого стафилококка (VRSА-штаммы).
Способствующие распространению МRSА-инфекции факторыПациенты стационаров - основной источник, но основным механизмом переноса инфекции является медицинский персонал. Как кратковременное, так и длительное лечение антибиотиками неинфицированного МRSА пациента также создает благоприятный фон. Другие факторы включают:
На современном этапе отмечается рост инфекций, связанных с внегоспитальными штаммами МRSА. В отличие от госпитальных штаммов, внегоспитальные не являются мультирезистентными.
Ванкомицинрезистентные энтерококки (ВРЭ)Наиболее распространенными представителями этой группы антибиотикорезистентных штаммов является E.faecalis и E.faecium. Некоторые штаммы данных микроорганизмов резистентны ко всем известным антибиотикам. Впервые ванкомицинрезистентные энтерококки описаны в 1988 году, а уже в 2010 году штаммы указанных микроорганизмов зарегистрированы на всех континентах. Одной из причин быстрого распространения ВРЭ в Европе стало добавление в комбикорм гликопептида авопарцина. Факторами, которые создают благоприятный фон являются применение таких антибиотиков, как ванкомицин, цефалоспорины, имипенем и антианаэробные препараты. Основным путем инфицирования является фекально-оральный. В отличие от МRSА, при борьбе с ВРЭ важное значение имеет изоляция пациента. Другими факторами являются соблюдение правил личной гигиены и ограничение применения антибиотиков.
Мультирезистентные грамотрицательные палочки (МРГП)Большинство представителей данной группы относятся к микрофлоре кишечника (кишечная палочка, клебсиеллы, синегнойная палочка, ацинетобактер и др.). Представители МРГП преимущественно оказываются в отделениях неонатологии и интенсивной терапии, а также в отделениях, где проводится лечение болезней мочевыделительной системы. Мультирезистентные штаммы МРГП преимущественно проявляют в странах Южной и Восточной Европы. Инфицирование происходит через контакт с загрязненной средой (в т.ч. через руки персонала). Поскольку представители МРГП относятся к группе микроорганизмов, которые обычно заселяют организм человека, то основным фактором появления МРГП является нерациональное применение антибиотиков. Наиболее опасными пациентами считаются больные с диареей и раневой инфекцией.
Современные тенденции развития резистентности к антибиотикамНа современном этапе отмечается изменение основных типов возбудителей антибиотикорезистентных инфекций как в стационарах, так и в популяциях. Возбудители МRSА постепенно вышли за пределы стационаров и распространились во внегоспитальной сфере, заняв ведущее место среди внегоспитальных инфекций, вызванных антибиотикорезистентными микроорганизмами. В то же время среди госпитальных инфекций основными полирезистентными возбудителями стали Acinetobacter и отдельные штаммы Klebsiella и Pseudomonas. Новые возбудители госпитальных инфекций имеют принципиально иные механизмы развития и распространения резистентности, в частности появление резистентности МRSА к фторхинолонам: фторхинолоны как в монотерапии, так и в комбинации с другими препаратами рассматривались как эффективная альтернативная схема лечения МRSА. Рост резистентности к антибиотикам стал причиной появления явления, обозначенного термином "внутрибольничная инфекция" (ВБИ). К примеру, по материалам Национальной системы контроля внутрибольничных инфекций США частота ВБИ среди пациентов стационара составляет 5,7%; ежегодно в США от ВБИ страдает около 2 млн. пациентов, из них - 90000 - умирает; за последние 10 лет летальность от ВБИ выросла в 7 раз; расходы на лечение 1 пациента с ВБИ растут в 5-6 раз и составляют около 4.5 млрд. долларов. Проникновение полирезистентных микроорганизмов во внегоспитальную сферу создает проблему выбора антибиотиков для стартовой эмпирической терапии гнойно-септического заболевания: и сегодня, и в отдаленной перспективе эмпирическая стартовая антибиотикотерапия будет оставаться единственным методом в начале лечения любого гнойно-септического заболевания. В основу эмпирической антибиотикотерапии положены данные по естественной чувствительности микроорганизмов к определенному антибактериальному препарату. Однако распространение резистентных микроорганизмов не только в условиях стационара, но и в отдельных популяциях значительно усложняет решение данного вопроса, поскольку требует создания бактериальных паспортов популяций (регионов). Большое значение имеет отсутствие в отечественных научных источниках доступной информации по проблеме резистентности для практикующих врачей: как следствие, большинство врачей не только не знакомо с проблемой роста антибиотикорезистентности, но даже не представляет опасности, обусловленной этим явлением. medlibera.ru medlibera.ru |
г.Самара, ул. Димитрова 131 [email protected] |
 |



 Не только бактерии Устойчивость к противомикробным препаратам развивается и у патогенных грибков, паразитов и вирусов. Но главная проблема грозящего медицине кризиса — это антибиотикорезистентные штаммы бактерий, и прежде всего — госпитальные инфекции.
Не только бактерии Устойчивость к противомикробным препаратам развивается и у патогенных грибков, паразитов и вирусов. Но главная проблема грозящего медицине кризиса — это антибиотикорезистентные штаммы бактерий, и прежде всего — госпитальные инфекции.  Найти и уничтожить Изящное решение разработано группой Мэтью Чана в Наньянском технологическом университете (Сингапур). Обычную кишечную палочку ученые превратили в оружие против Pseudomonas aeruginosa — синегнойной палочки, частой причины больничных инфекций. В геном «бактерии-бомбы» ввели четырехступенчатую конструкцию. Первая синтезирует белки-индикаторы, которые связываются с сигнальными молекулами, обеспечивающими «чувство кворума» синегнойной палочке и другим микробам-коллективистам, образующим скопления-биопленки, связанные молекулами ДНК. Получившийся комплекс запускает сразу три реакции: синтез антимикробного пептида микроцина S, фермента ДНКазы-I, разрушающей биопленку (оба соединения выделяются в окружающую среду через клеточную мембрану), и комплекса белков, обеспечивающих движение кишечных палочек в направлении большей концентрации «молекул кворума». В результате разрушаются и патогены, образующие биопленку, и отделяющиеся от нее микробы. Как и методика выращивания «в клетке» некультивируемых бактерий, этот метод является принципиально новой платформой, позволяющей создавать новые противомикробные средства. Антибактериальная бомба: 1. Кишечная палочка выделяет белки-индикаторы, которые демаскируют синегнойную палочку. 2. «Бомба» выделяет вещества, убивающие синегнойную палочку и разрушающие биопленку: происходит «взрыв». 3. Осколки бомбы (кишечная палочка) двигаются в направлении противника, и цикл начинается снова.
Найти и уничтожить Изящное решение разработано группой Мэтью Чана в Наньянском технологическом университете (Сингапур). Обычную кишечную палочку ученые превратили в оружие против Pseudomonas aeruginosa — синегнойной палочки, частой причины больничных инфекций. В геном «бактерии-бомбы» ввели четырехступенчатую конструкцию. Первая синтезирует белки-индикаторы, которые связываются с сигнальными молекулами, обеспечивающими «чувство кворума» синегнойной палочке и другим микробам-коллективистам, образующим скопления-биопленки, связанные молекулами ДНК. Получившийся комплекс запускает сразу три реакции: синтез антимикробного пептида микроцина S, фермента ДНКазы-I, разрушающей биопленку (оба соединения выделяются в окружающую среду через клеточную мембрану), и комплекса белков, обеспечивающих движение кишечных палочек в направлении большей концентрации «молекул кворума». В результате разрушаются и патогены, образующие биопленку, и отделяющиеся от нее микробы. Как и методика выращивания «в клетке» некультивируемых бактерий, этот метод является принципиально новой платформой, позволяющей создавать новые противомикробные средства. Антибактериальная бомба: 1. Кишечная палочка выделяет белки-индикаторы, которые демаскируют синегнойную палочку. 2. «Бомба» выделяет вещества, убивающие синегнойную палочку и разрушающие биопленку: происходит «взрыв». 3. Осколки бомбы (кишечная палочка) двигаются в направлении противника, и цикл начинается снова.