|
|
||||||||||
|
/ Реактогенность и безопасность поликомпонентной вакцины(ВП-4) при профилактике острых респираторных заболеваний у дошкольников. / оценка научной публикации. Вп 4 вакцинаВакцина поликомпонентная ВП–4 — КиберПедияВ состав вакцины поликомпонентной ВП–4 (Россия) входят лизаты Staphylococcus aureus, Proteus vulgaris, Klebsiella pneumoniae, Echerichia coli. Для получения препарата использованы оригинальные штаммы возбудителей, обладающие высокой иммуногенностью, слабыми сенсибилизирующими свойствами и широкой перекрестной активностью антигенов в отношении возбудителей заболеваний респираторного тракта. В опытах in vitro было показано, что при заражении мышей Klebsiella pneumoniae выживает 95% мышей, вакцинированных ВП–4, и погибает 100% мышей контрольной группы. двукратное подкожное введение ВП–4 вызывает выработку специфических антител ко всем компонентам вакцины и увеличение уровня IgG в крови. В опытах in vitro показано значительное увеличение синтеза ИЛ–1 и ИЛ–2 и пролиферации лимфоцитов в селезенке вакцинированных мышей [16]. ВП–4 может применяться подкожно или назально–оральным методом. Применение ВП–4 при хроническом бронхите после антибактериальной терапии привело к ускорению выздоровления, улучшению состояния больных, снижению числа рецидивов. При этом отмечалось увеличение титра специфических антител и повышение функциональной активности Т–лимфоцитов [16]. Отмечается положительный эффект применения ВП–4 при смешанной форме бронхиальной астмы у взрослых и детей, причем со стороны иммунологических показателей отмечали усиление фагоцитоза, увеличение CD4+, CD8+, CD16+–клеток, сывороточного IgA при изначально сниженных показателях, уровень сывороточного IgE не повышался. Клинически отмечалось снижение частоты приступов затрудненного дыхания, числа рецидивов и тяжести заболеваний респираторного тракта [16]. Ликопид Ликопид – N–ацетил–глюкозаминил–N–ацетил–мурамил–дипептид (Россия) – синтезирован в 1977 г. [18,19]. Главной мишенью ликопида в организме человека являются клетки моноцитарно–макрофагального звена иммунной системы. Под влиянием ликопида усиливается поглощение и киллинг микроорганизмов; стимулируются цитотоксические свойства макрофагов по отношению к бактериальным и вирус–инфицированным клеткам; усиливается синтез цитокинов: ИЛ–1, ФНО–a, ГМ–КСФ, b–интерферона и др., что, в свою очередь, оказывает стимулирующее действие на продукцию антител и пролиферацию Т– и В–лимфоцитов [17]. Проведенные клинические испытания показали, что применение ликопида перспективно при гнойных послеоперационных осложнениях, папилломатозе, псориазе, хроническом бронхите. Назначение препарата приводит к увеличению длительности ремиссий, уменьшению частоты рецидивов. Наиболее эффективно применять препарат в фазу ремиссии с профилактической целью [10,17]. По нашим данным, применение ликопида в дозе 1мг в течение 10 дней у длительно и часто болеющих детей не оказывает стимулирующего влияния на показатели крови (иммунорегуляторный индекс, CD3+, CD8+, CD19+ –клетки), но стимулирует активность макрофагов. Повышение уровня IgA в слюне наблюдалось у всех больных. Показания к назначению: длительно и часто болеющие дети, хронический фарингит, хронический тонзилит, хронический бронхит. В остром периоде – на фоне или после окончания базисной терапии; с профилактической целью – без предшествующей базисной терапии. Проведенные исследования [11] высеваемости микрофлоры из зева у детей дошкольных учреждений г. Москвы в 2000 г. показывают, что наиболее часто высевается стафилококк, в частности Staphylococcus aureus. При этом два и более возбудителя были выделены у 16,3%, а монокультура – у 60,3% обследованных детей. Только 52,8–88,7% выделенных из зева штаммов стафилококка и 45,5–63,8% штаммов стрептококка были чувствительны к различным антибиотикам. Представленные данные подтверждают целесообразность введения бактериальных иммуномодуляторов в комплексное лечение повторных инфекций носоглотки и респираторного тракта. Таким образом, бактериальные иммуномодуляторы могут назначаться в остром периоде на фоне базисной терапии, а также с профилактической целью. Все препараты оказывают влияние на систему местного иммунитета носоглотки и респираторного тракта, повышают уровень IgA в слюне. Ряд препаратов обладают системным действием на показатели периферической крови. Список литературы Вы можете найти на сайте http://www.rmj.ru
cyberpedia.su Диссертация на тему «Динамика показателей системного и местного иммунитета у пациентов с бронхолегочными заболеваниями при применении поликомпонентной вакцины :ВП-4» автореферат по специальности ВАК 14.00.36 - Аллергология и иммулология1. Абатуров А.Е., Абатуров Ан. Е./ Нозоспецифические особенности динамики иммунологических показателей у детей раннего возраста больных острыми респираторными вирусными инфекциями различной этиологии.// ЖМЭИ.-1989.-№6.-с.70-74 2. Агальцова С.И. Иммунологические и морфологические проявления местного и системного иммунитета при пероральной иммунизации корпускулярной коклюшной вакциной: Автореф. дис. канд. мед. на-ук.-М., 1990.-24 с. 3. Адо А.Д., Булатов П.К. Клинико-физиологические основы классификации бронхиальной астмы. -М., 1969.-206 с. 4. Аллергия, иммунитет и патология внутренних органов: Сборник научных трудов./-Рязань.-1995.-с.26 5. Артемова О.П. Сравнительная оценка гуморального звена местного иммунитета у больных с хроническими неспецифическими заболеваниями легких и некоторые способы его коррекции: Автореф. дис. канд. мед. наук.-М., 1995.-23 с. 6. Ашмарин И.П., Воробьев A.A. Статистические методы в микробио-логии.-М., 1961.-180 с. 7. Балаболкин И.И., Степушина М.А., Егорова Н.Б., и др./ Использование поликомпонентной бактериальной вакцины ВП-4 в лечении бронхиальной астмы у детей.// Int. J. on immunorehabilitation.-1998.-№10.-с.158-164 8. Балаболкин И.И., Степушина M.A., Краснопрошина Л.И. и др./ Эффективность поликомпонентной бактериальной вакцины ВП-4 при бронхиальной астме у детей.// Педиатрия.-1998.-№4.-с.29-33 9. Бейли Н. Статистические методы в биологии.: Пер. с англ./Под ред. Налимова В.В.-М.: «Мир»,1959.-271 с. 10. Беляков И.М./ Иммунная система слизистых./ Иммунология,-1997.-№4.-с. 7-13 11. Бредфорд Хилл А. Основы медицинской статистики: Пер. с англ./Под ред. Меркова А.М.-М.: «Гос. Издательство мед. литературы», 1958.-306 с. 12. Волгарева Г.М., Голгеев Ю.Д., Егорова Н.Б., и др./ Исследование мутагенности новой поликомпонентной вакцины из антигенов Klebsiella pneumoniae, Staphylococcus aureus, Proteus vulgaris и Escherichia coli.// ЖМЭИ.-1991.-№6.-с.50-52 13. Воробьев А.А., Осипов В.И./ Роль проницаемости мембран слизистой желудочно-кишечного тракта для микроорганизмов и их антигенов в механизме пероральной вакцинации.// ЖМЭИ.-1971.-№4.-с.60-64 14. Воробьев А.А., Лебединский В.А. Массовые способы иммунизации.-М.: «Медицина», 1977.-c.255 15. Воробьев А.А., Осипов В.И., Лебединский В.А./ Современное представление о проникновении макромолекулярных антигенов и микроорганизмов через слизистые оболочки и в клетки животных.// Успехи современной биологии.- 1979.-т.88.-№2(5).-с. 226-240 16. Галкина О.В., Алешина Л.А., Басек Т.С., и др. / Особенности имму-ноглобулинового профиля бронхоальвеолярной жидкости при патологии дыхательного тракта.// Медицинская иммунология,-1999.-Т.1.-№3-4.-с.34-35 17. Гервазиева В.Б., Петрова Т.И./ Экология и аллергические заболевания у детей.// Аллергология и иммунология.-2000.-т.1.-№1.-с. 101-108 18. Гублер Е.В. Вычислительные методы анализа и распознавания патологических процессов.-Л. «Медицина», 1978.—290 с. 19. Егорова Н.Б., Мансурова Н.Л., Ефремова В.Н. и др./ Экспериментальное изучение иммуногенности монопрепарата антигенного комплекса клебсиеллы пневмонии его ассоциаций с антигенами стафилококка, протея и кишечной палочки.// ЖМЭИ.-1984.-№1.-с.35-38 20. Егорова Н.Б., Ефремова В.Н., Курбатова Е.А., Кузьмина Л.А./ Итоги экспериментального и клинического изучения поликомпонентной вакцины из антигенов условно патогенных микроорганизмов.// ЖМЭИ-1997.-№6.-с.96-101 21. Иммуномодуляторы: Сборник научных трудов/ НИИВС им. И.И. Мечникова АМН СССР.-М.:-1987-198 с. 22. Иммунохимическая диагностика гаммапатий: Метод, рекомендации/ МНИИЭМ им. Г.М. Габричевского МЗ РФ; Подгот. Чернохвостова Е.В., Герман.Г.П. Москва, 1984.- 51 с. 23. Иммунологические методы./Под ред. Г. Фримеля.-М.: «Медицина», 1987.-C.73-89 24. Исследование иммуноглобулинов и других белков в секретах человека: Метод, рекомендации/ МНИИЭМ им. Г.М. Габричевского МЗ РФ; Подгот. Чернохвостова Е.В. и др. Москва, 1987.- 33 с. 25. Каральник Б.В. Эритроцитарные диагностикумы.-М.: «Медицина», 1976 26. Каральник Б.В./ Варианты реакции агглютинации: настоящее и будущее.// ЖМЭИ.-1989.-№8.-с.84-89 27. Касаткин В.Н., Михайлова Н.В., Румянцев А.Г./ Результаты трехлетнего катамнеза у часто болеющих детей.// Педиатрия.-1998.-№2.-с.43-46 28. Комарова Л.Г., Алексеева О.П. Новые представления о функции слюнных желез в организме (клинико-биохимический аспект). -Н.Новгород:,1994.-96 с. 29. Краснов М.В., Ботвиньева В.В. Иммунологическая реактивность детей.- Чебоксары: Изд-во Чуваш. Ун-та, 1993.-104 с. 30. Краснопрошина Л.И., Алексеева И.А., Соколов Я.А., Грачева A.M./ Радиоиммунологический метод определения антименингококковых секреторных антител IgA-класса в слюне человека.// ЖМЭИ.-1991.-№2.-с.51-54 31. Курбатова Е.А., Егорова Н.Б., Киселева Б.С./ Протективная активность бесклеточной клебсиеллезной вакцины в отношении различных сероваров Klebsiella pheumoniae.// ЖМЭИ.-1984.-№8.-с.80-83 32. Курбатова Е.А./ Разработка поликомпонентной вакцины из антигенов условно-патогенных микроорганизмов (экспериментальное и клинико-иммунологическое исследование): Дисс. д. мед. наук: 14.00.36 и 03.00.07.- Защищена 25.12.97.- М., 1997.-313 с. 33. Левина Л.А. Мигунов В.Н., Зайцева Е.В., и др./ Противоэшерихиоз-ные антитела в сыворотке крови неиммунизированных доноров и препаратах иммуноглобулина человека.// ЖМЭИ.-1995.-№ 1.-е.62-66 34. Мартынов Ю.В., Девяткина Н.П., Маринин И.Ю., Спирихина Л.В./ Определение менингококковых антител в слюне здоровых людей.// ЖМЭИ.-1991 .-№9.-с.З 5-37 35. Николаенко В.Н. Сдвиги в системе иммунекомпетентных клеток у людей, иммунизированных различными вакцинными препаратами: Дисс. канд. мед. наук: 14.00.36.- М.,1990.-179 с. 36. Новиков Д.К., Новикова В.И. Оценка иммунного статуса.-М.; Вит.: «Витязь», 1996.-282 с. 37. Осипова Г.Л./ Иммунотерапия поликомпонентной вакциной больных с хроническими обструктивными заболеваниями легких: Дисс. канд. мед. наук: 14.00.36.- Защищена 16.09.93.- М.,1993.-94 с. 38. Оценка иммунологического статуса человека: Метод, рекомендации/ МОЛГМИ им. Н.И. Пирогова МЗ РСФСР; Подгот. Чередеев А.Н. и др.- Москва, 1980.-31 с. 39. Петров Р.В., Хаитов P.M., Пинегин Б.В./ Иммунодиагностика имму-нодефицитов.//Иммунология.-1997.-№4.-с. 4-7о 40. Першин Б.Б., Кузьмин С.Н., Кочкуркин В.Н., и др./ Реакции местного иммунитета у пловцов сборной страны.//ЖМЭИ.-1996.-№1.-с.53-57 41. Покровская Е.Е., Камальдинова Э.Г., Иванова В.В., Шварцман Я.С./ Местный и общий гуморальный иммунитет при респираторно-синцитиальной инфекции.// Иммунология.-1992.-№2.-с.21-23 42. Польнер A.A., Кузин И.И., Ермолин Г.А., и др./ Иммуноглобулины бронхиального секрета при бронхиальной астме и хроническом бронхите.// Совет. Медицина.-1984.-№6.-с.36-39 43. Прокопенко В.Д. Особенности лабораторной диагностики и клинического течения основных форм вторичной иммунологической недостаточности: Автореф. дис. докт. мед наук.-М., 1996.- 44 с. 44. Райкис Б.Н., Ракитина E.JL, Титаренко А.И., Щербакова Б.В./ Использование иммунокорректоров бактериального происхождения в терапии часто болеющих детей Ставропольского края.// Тез. докл. 2-го съезда по иммунореабилитации.- Эйлат, Израиль.-1998.-28 с. 45. Ройт А./ Основы иммунологии. -М.: Мир, 1991.-252 с. 46. Смирнова Г.И., Коровина H.A., Захарова И.Н./ Применение рибому-нила у детей с хронической бронхо-легочной патологией.// Материалы Всероссийской научной конференции «Аллергические болезни у детей».-1996.-е. 115 47. Современные аспекты изучения иммунологической безвредности и эффективности вакцин: Сборник научных трудов./ МНИИЭМ им. Г.Н. Габричевского.-М.- с. 44-64 48. Сокуренко С.И., Караулов A.B./ Иммунотерапия хронических об-структивных заболеваний легких.// В кн: Успехи клинической иммунологии и аллергологии. Под ред. Караулова А.В.-М.: «Лекарства и пищевые добавки»,-2000.-е. 91-123 49. Справочник по функциональной диагностике в педиатрии./ Под. ред. Ю.Е. Вельтищева, Н.С. Кисляк; М.: Медицина, 1979.-624 с. 50. Степушина М.А./ Эффективность поликомпонентной бактериальной вакцины (ВП-4) при бронхиальной астме у детей: Дисс. канд. мед. наук: 14.00.36 и 14.00.09.- Защищена 28.01.97.-М.,1997.-94 с. 51. Студеникин М.Я., Соколова Т.С. Аллергические болезни у детей. -М.: Медицина, 1986.-288 с. 52. Тотолян A.A./ Современные подходы к диагностике иммунопатологических состояний.// Медицинская иммунология.-1999.-т. 1.-№ 1-2.-с.75-108 53. Уланова М.А., Горелова Ж.Ю., Резник И.Б., и др./ Влияние бронхо-мунала на заболеваемость острыми респираторными инфекциями и иммунологические показатели у детей раннего возраста.// Пульмонология.- 1992.-Приложение 1 .-с.49-52 54. Урбах В.Ю. Биометрические методы.-М.: «Наука», 1964.-415 с. 55. Федорцов К.К. Стандартизация иммунологических методов и их применение для для изучения иммунологической реактивности человека в экстремальных условиях: Дисс. канд. мед. наук: 14.00.36.-М, 1994.-120с. 56. Федосеева В.Н., Порядин Г.В., Ковальчук Л.В., и др./ Руководство по иммунологическим и аллергологическим методам в гигиенических исследованиях.-М: Промедэк, 1993.-320 с. 57. Федько Н. А., Бодрова И.В., Щербакова Б.В./ Клинико-иммунологи-ческие показатели при частых респираторных заболеваниях у детей и возможности иммунокоррегирующей терапии.// Тез. докл. 2-ой Конгресс педиатров России.- Москва.-1998.-118 с. 58. Федько H.A., Щербакова Б.В./ Эффективность использования препарата ВП-4 в терапии у часто болеющих детей.// Депонированная ст. в ГЦНМБ.-Москва.-1999.-21 с. 59. Хаитов P.M., Пинегин Б.В., Истамов Х.И./ Экологическая иммунология. -М.: ВНИРО, 1995.-220 с. 60. Хорошилова H.B. Клинико-иммунологическая оценка эффективности применения рибомунила и низкоинтенсивной лазерной терапии у больных хроническим бронхитом: Автореф. дис. канд. мед. наук.- М.-1993 .-с. 17 61. Чередеев А.Н., Ковальчук Л.В./ Концептуальные проблемы оценки иммунного статуса человека.// ЖМЭИ.-1990.-№11.-С.90-95 62. Чучалин А.Г. Иммунокоррекция в пульмонологии.-М., 1989.-е.84-90 63. Чучалин А.Г., Егорова Н.Б., Ефремова В.Н., и др./ Иммунотерапия поликомпонентной вакциной в пульмонологической практике.// Пульмонология,-1991 .-№4.-с. 14-20 64. Чучалин А.Г., Осипова Г.Л., Егорова Н.Б., и др./ Контролируемые исследования по эффективности поликомпонентной вакцины при иммунотерапии у больных с хроническими обструктивными заболеваниями органов дыхания.// Пульмонология.-1995.-№2.-с.55-61 65. Чучалин А.Г., Балаболкин И.И., Егорова Н.Б., и др./ Иммунотерапия бронхиальной астмы поликомпонентной вакциной при назально-оральном введении.// ЖМЭИ.-1997.-№3.-с.84-88 66. Шарапов C.B., Плиско Л.Ф./ Физико-иммунологическая характеристика отделяемого бронхов при бронхиальной астме.// Иммунология.-1992.-№4.-с.39-42 67. Шварцман Я.С., Хазенсон Л.Б. Местный иммунитет.-Л.^Медицина», 1978.-224 с. 68. Щербакова Б.В./ Эффективность использования поликомпонентной вакцины ВП-4 в терапии у часто болеющих детей: Дисс. канд. мед. наук: 14.00.36,- Защищена 16.09.99.-М.,1999.-128 с. 69. Энциклопедия клинических лабораторных тестов./ под ред. Н. Тица.-М.: Лабинформ.-1997 70. Alurkar V., Kamat R./ Immunomodulatory properties of porins of some members of the family Enterobacteriaceae.// Infect. Immun.-1990.-v.65.-№6.-p.23 82-23 88 71. Atkinson J.C./ The role of salivary measurements in the diagnosis of salivary autoimmune diseases.// Annal of the N.-Y. Acad. Of Sciences.-1995.-v.694.-p.238-251 72. Bellanti J.A., Zeligs B.J./ Current concepts of immune investigation in children with respiratory diseases.// Respiration-1994.-v.61.-№l.-p.3-7 73. Bergemann R./ Preventiv treatment of chronic bronchitis: a meta-analysis of clinical trials with bacterial extract (OM-85 BV) and a cost-effectiveness analysis.//Mon. chest dis.-1994.-v.49.-№4.-p.302-307 74. Bergmann K.-C., Johurent K., Noack K./ Stimulation of paraspecific defence mechanisms in the respiratory tract by inchalation of a bacterial ly-sate.// Prax. Klin. Pneumol.-1985.-v.39.-№4.-p. 127-129 75. Bergmann K.-C., Waldman R.H./ Stimulation of secretory antibody following oral administration of antigen.// Rev. Resp. Dis.-1988.-v.10.-p.939-950 76. Boackle R.J./ The partial isolation and function of salivary factors which interact with the complement system: a possible role in mucosal immunity.// Adv. Exp. Med. Biol.-1978.-v.107.-p.411-421 77. Bosch A., Lucena F., et al./ Bacterial immunostimulant (Broncho-Vaxom) versus levamisole on the humural immune responses in mice.// J. of Immu-nogfarmacology.-1983.-v.5.-p. 107-116 78. Brandtzaeg P./ Molecular and cellular aspects of the secretory immunoglobulin system.// APMIS-1995.-v. 103 .-№ 1 .-p. 1 -19 79. Brown T.I./ Immunity at mucosal surfaces.// Adv. Dent. Res.-1996.-v.10,-№l.-p.62-65 80. Burrel R./ Immunomodulation by bacterial endotoxin.// Crit. Rev. Microbiol.- 1990,-v. 17.-p. 189-208 81. Canh P. Quan, Berneman A,, Pires R., et al,/ Natural polyreactive secretory immunoglobulin A autoantibodies as a possible barrier to infection in humans.// Infec. and Immun. -1997.-v.65.-№10.-p.3997-4004 82. Caille J./ Treitment des infection des bronches par vaccination et desensi-bilisation par nasale.// Gas. Med. Fr.-1969.-v.76.-p.25 83. Chretien J et al./ Acute respiratory infections in children: a global public-health problem.//N. Engl. J. med.-1984.-v.310.-p.982-984 84. Clancy R./ Oral vaccine: to exploit contemporary knowledge of mucosal immunology.// Third annual vaccines: New technologies & applications.-1995.-p.l-4 85. Clot J., Andary M./ Immunostimulation induced by a lyophilized bacterial lysate. Broncho-Vaxom: an in vitro study of specific and non-specific responses.// Med. Hyg.-1980.-v.38.-p.2776-2782 86. Collet J.-P., Ducruet T., Kramer M.S., et al./ Stimulation of nonspecific immunity to reduce the risk of . recurrent infections in children attending day-care centers.// Pediatr. Ifect. Dis.-1993.-v.l2.-p.648-652 87. Collet J.P., Boissel J.P./ OM-85 BV: Primary versus secondery prevention.// Respiration.-1994.-v.61 .-p.20-23 88. Clements M.L., Betts R.F., Tierney E.L., Murphy B.R./ Resistence of adults to challenge with influenza A wild-type virus after receiving live or inactivated virus vaccine.// J. Clin. Microbiology.-1986.-v.23.-p. 73-76 89. Cvoriscec B./ Oral immunotherapy of chronic bronchitis: a double-blind placebo-controlled multicentre study.// Respiration-1989.-v.55.-p.l29-135 90. Czerkinsky C., Prince S.J., Michalek S.M. et. al./ IgA antibody-producing cells in peripheral blood after antigen ingestion: evidence for a commonmucosal immune sistem in humans.// Proc. Natl. Acad. Sci.-1987.-v.84.-p.2449-2453 91. Djuric O., Michailovic-Vucinic V., Stojcic V.// Effect of Broncho-Vaxom on clinical and immunological parameters in patients with chronic obstructive bronchitis. A double-blind, placebo-controlled study.// Int. J. Immunotherapy.- 1989.-v.3 .-p. 139-143 92. Drummond P.D., Hewson-Bower B./ Increased psychosocial stress and decreased mucosal immunity in children with recurrent upper respiratory tract infections.// J. Psychosom. Res.-1997.-v.43.-№3.-p.271-278 93. Emmerich B., Emslander H.P., Milatovic D., et al./ Effects of a bacterial extract on local immunity of the lung in patients with chronic bronchitis.// Lung.-1990.-p.726-731 94. Epstein M.M., Baumgarten A./ The usefulness of routine screening for salivary secretory component.// J. Allergy Clin. Immunol.-1991.-v.88.-№9.-p.356-360 95. Fiocci A., Arancio R., Cinquepaulei P., et al./ Recurrent respiratory infections in childhood: expirence with a bacterial ribosomes (immucytal).// J. of Int. Med. Res.-1990.-v. 18.-p.50-60 96. Fox P.C./ Salivary monitoring in oral diseases.// Annal of the N.-Y. Acad. Of Sciences.-1995.-v.694.-p.235-237 97. Garibaldi R.A./ Epidemiology of communiti-acquired respiratory tract infections in adults.// Am. J. med.-1985.-v.78.-6B.-p.32-37 98. Gleeson M., Cripps A.W., Clancy R.L./ Modifiers of the human mucosal immune system.// Immunol. Cell Biol.-1995.-v.73.-№5.-p.397-404 99. Gleeson M., Cripps A.W., Clancy R.L., et al./ The significance of transient mucosal IgA deficiency on the development of asthma and atopy in children.//Adv. Exp. Med. Biol.-1995.-v.371B.-p.861-864 100. Gluck U./ Intranasal virosomal influenza vaccine produces strong immune response./ J. of virology.-1999.-v.73.-p.7780-7786 101. Gorse G.J., Otto E.E., Powers D.S. et al./ Induction of mucosal antibodies by live attenuated and inactivated influenza virus vaccines in the chronically ill elderly.// J. Infect. Disease.-1996,-v.l73.-p.285-290 102. Grimwood K., Lund J.C., Coulson B.S., at al./ Comparison of serum and mucosal antibody responses following severe acute rotavirus gastroenteritis in young children.// J. Clin. Microbiol.-1988.-v.26.-№4.-p.732-738 103. Hewson-Bower B., Drummond P.D./ Secretory immunoglobulin A increases during relaxation in children with and without recurrent upper respiratory tract infections.// J. Dev. Dehav pediatr.-1996.-v.l7.-№5.-p.311-316 104. Holmgren G., Czerkinsky C., Lycky N., Svennerholm A.-M./ Mucosal immunity: implications for vaccine development.// Immunobiol.-1992.-v.l84.-p. 157-179 105. Holmgren G., Czerkinsky C., Lycky N., Svennerholm A.-M./ Strategies for the induction of immune responses at mucosal surfaces making use of cholera toxin B subunit as immunogen carrier and adjuvant.// Am. J. Trop. Med. Hyg.-1994.-v.50.-№5.-p. 42-54 106. Holmgren G., Svennerholm A.-M./ Bacterial enteric infections and vaccine development.// Gast. Clin. N. Am.-1992.-v.21.-p. 283-302 107. Immunobiology of the tonsils and adenoids: Handbook of mucosal immunology./ Edited by Ogra P.L., Mestecky J., Lamm M.E., et. al.-San Diego: Academic Press Inc,-1994.-p.625-640 108. Kauppi M., Escola J./ Anti-capsular polysaccharide antibody concentration in saliva after immunization with Haemophilus influenzae type b conJugate vaccines.// Pediatr. Infect. Dis. -1995.-v.l4.-№4.-p.286-294 109. Kraehenbugl J.-P., Neutra M.R./ Molecular and cellular basis of immune protection of mucosal surfaces.// Physiol.-1992.-v.72.-p. 853-879 110. Kraehenbugl J.-P., Neutra M.R./ Transepithelial transport and mucosal defence: secretion IgA.// Trends cell biol.-1992.-№2.-p.l70-174 111. Kugler J., Hess M., Haake D./ What accounts for the interindividual variability of slgA concentration in saliva?// Annal of the N.-Y. Acad. Of Sciences.-1995.-v.694.-p.296-298 112. Lusuardi M., Capelli A., Donner C.F./ Lung immune defences after stimulation of gut-associated lymphoid tissue with OM-85 BV: a doudle-blind study in patients with chronic bronchitis.// Eur. Respir. Rev. -1996.-v.36.-№6.-p. 182-185 113. Maestroni G.M., Losa G.A./ Clinical and immunological affects of an orally administrated bacterial extract.// J. int. immunofarmacol.-1984.-v.6.-p.111-117 114. Madore D.V., Johnson-Kraines C.L., Rothstein E.P., et al./ Kinetic of antibody response to Haemophilus influenzae type b vaccines.// Cur. Med. Res. and Opinion.-1999.-v.15.-№2.-p. 105-112 115. Mancini G., Nacb D.K., Heremans J.S./ Further studies on single radial immunodiffusion. Quantitative analysis of related and unrelated antigens. // Immunochem.-1970.- v.7.-p. 261-264 116. Mauel J./ Macrophage activation by OM-85.// Respiration-1992.-v.59.-№3.-p.l4-18 117. McDermott M.R., Bienenstock J./ Evidence for a common mucosal immunologic system. I. Migration of B immunoblasts into intestinal, respiratory and genital tissues.// J. Immunol.-1979.-v.122.-p. 1892-1898 118. McGhee J.R., Kiyono H., Michalek S.M., Mestecky J./ Enteric immuni-zacion reveals a T cell network for IgA responses and suggests that humans possess a common mucosal immune system.// A. Van Leuwenhoek.-1987.-v.53.-p.537-543 119. McGhee J.R., Mestecky J., Dertzbaugh M.T., et. al./ The mucosal immune system: from fundamental concepts to vaccine development.// Vaccine.- 1992.-№10.-p.75-88 120. McGhee J.R., Kiyono H./ New perspectives to vaccine development: mucosal immunity to infections.//Infect. Agents Dis.-1993.- №2.-p.55-73 121. Mestecky J./ The common mucosal immune system and current strategies for induction of immune responses in external secretions.// J. Clin. Immun.-1987.-№7.-p.265-276 122. Mestecky J., McGhee J.R./ Immunoglobulin A (IgA): Molecular and cellular interactions involved in IgA biosynthesis and immune response.// Advances in Immunology. -1987.-№40.-p. 153-245 123. Michel F.B., Dussoud d"Hinterland, Bousquet J., et al./ Immunostimulation by a ribosomal vaccine associated with a bacterial cell wall adjuvant.// Infec. and Immun. -1978.-v.20.-p.760-769 124. Moro I., Komiyama K., Kusama K., et al./ Molecular aspects of secretory IgA (s-IgA) in gut- associated lymphoid tissues.// Nippon. Rinsho.-1996.-v.54.-№4.-p.l 155-1161 125. Mucosal immunity to viruses: Handbook of mucosal immunology./ Edited by Ogra P.L., Mestecky J., Lamm M.E., et. al.-San Diego: Academic Press Inc,-1994.-p.333-343 126. Mucosal immunoglobulins: Handbook of mucosal immunology./ Edited by Ogra P.L., Mestecky J., Lamm M.E., et. al.-San Diego: Academic Press Inc,-1994.-p. 79-97 127. Navazesh M./ Methods of collecting saliva.// Annal of the N.-Y. Acad. Of Sciences.-1995.-v.694.-p.72-77 128. Neutra M.R., Pringault E., Kraehenbugl J.-P./ Antigen sampling across epithelial barriers and induction of mucosal immune responses./ Annual Rev. Immunol.-1996,-v. 14.-p.275-300 129. Nuesslein T.G./ The concentrations of secretory immunoglobulin A and specific slgA antibodies in the saliva of school children.// Adv. Exp. Med. Biol.-1995.-v.371B.-p.l 167-1171 130. Oggiano N., Giralamo F., et al./ Polyvalent oral bacterial vaccine in recurrent respiratory infections.// Minevra. Pediat.-1985.-v.37.-№19.-p.741-745 131. Orcel B./ Oral immunization with bacterial extracts for protection against acute bronchitis in elderly institutionalized patients with chronic bronchitis.//Eur. Respir. J.-1994.-№7.-p. 446-452 132. Ozek J., Truszczynski M./ Mucosal immunity with implications for use in developing a new generation of vaccines.// Postepy Hig. Med. Dosw. -1995 .-v.49.-№4.-p.469-486 133. Palma-Carlos A., Palma-Carlos M./ Immunomodulation with bacterial extracts in respiratory diseases.// Lung.-1990.-v.l68.-p.732-773 134. Paupe J./ Immunotherapy with an oral bacterial extract (OM-85 BV) for upper respiratory infections.// Respiration-1991.-v.58.-p.150-154 135. Percival R.S., Marsh P.D., Challacombe S.J./ Age-related changes in salivary antibodies to commensal oral and gut biota.// Oral microbiol. Immunol." 1997.-v. 12.-№ 1 .-p.57-63 136. Pietz K., Haas J., Wurster U./ Protein composition, IgG, and IgA analysis in the saliva of patients with multiple sclerosis.// Annal of the N.-Y. Acad, of Sciences.-1995.-v.694.-p.305-307 137. Puigdollers J.M., Serna G.R., Del Rey I.H., et al./ Immunoglobulin production in man stimulated by an orally administered bacterial lysate.// Respiration.- 1980.-v.40.-p. 142-149 138. Rico-Mrendez F.G., Massey-Reynaud L.F., Rendron L., et al./ Measurement of slgA in patients with chronic stable bronchitis.// Rev. Allerg. Mex.-1997.-v.44.-№ 1 .-p.4-7 139. Scotti L., Biondelli G., Borzanni M./ The use of polyvalent oral bacterial vaccine for reccurent respiratory infections in children.// Minerva pediat.-1987.-v.35.-№7.-p.251-256 140. Staats H.F., Jackson R.J., Marinaro M., et. al./ Mucosal immunity to infection with implications for vaccine development.// Immunology.-1994.-№6.-p.572-583 141. Stein-Streilein J., Frazier J.-L., Gross C.N., Hart D.A./ Splenic influence on the development of a local pulmonary immune response.// Infec. and Immun. -1979.-v.24.-№ 1 .-p. 139-144 142. Tarlo S., Broder J., Spence L.A./ A prospective study of respiratory infection in adult asthmatics and their normal spouses.// Clin. Allergy.-1979.-v.9.-№3.-p.293-301 143. Taubman M.A., Smith D.J./ Significance of salivary antibody in dental diseases.// Annal of the N.-Y. Acad, of Sciences.-1995.-v.694.-p.203-215 144. Tomasi T.B./ Mucosal immunity: the origin and migration patterns of cell in the secretory system.// J. Allergy Clin. Immunol.-1980.-v65.-№l.-p. 12-19 145. Toy L.S., Mayer L./ Basic and clinical overview of the mucosal immune system.// Semin Gastrointest Dis.-1996.-v.7.-№l.-p.2-l 1 146. Vissink A., Panders A.K., Nauta J.M. et al./ Applicability of saliva as a diagnostic fluid in Sjogren's syndrome.// Annal of the N.-Y. Acad. Of Sci-ences.-1995.-v.694.-p.325-329 147. Watanabe N., Kato H., Mogi G./ Induction of antigen-specific IgA-forming cells in the upper respiratory mucosa.// Ann. Otol. Rhinol. Laryn-gol.-1989.-v.98.-№7.-p.523-529 148. Wienholt M.G., Erbling M.C., Bennetts R.W. et al./ Detection of antibodies to Helicobacter pylori using oral fluid specimens.// Annal of the N.Y. Acad. Of Sciences.-1995.-v.694.-p.340-342 149. Wu H.Y., Russel M.W./ Nasal lymphoid tissue intranasal immunization and compartmentalization of the common mucosal immune system.// Immunol. Res.-1997,-v. 16.-№2.-p. 187-201 150. Wybran J., Libin M., Schandene L./ Activation of natural killer cells and cytokine production in humans by bacterial extracts (OM-85 BV).//Lung.-1990; Suppl.:720-725 www.dissercat.com Применение бактериальной терапевтической вакцины Иммуновак-ВП4 в лечении поллинозов - Терапевтический архив №03 2018Резюме Углубленное изучение функции и структуры лимфоидной ткани желудочно-кишечного тракта и дыхательных путей открывает широкие возможности для применения мукозальных вакцин с целью повышения иммунитета к различным инфекционным агентам. Одним из таких препаратов является вакцина Иммуновак-ВП4, содержащая патоген-ассоциированные молекулярные структуры (PAMPs) микроорганизмов. Их представляют антигены Klebsiella pneumoniae, Proteus vulgaris, Escherichia coli, Staphylococcus aureus. Обнаруженная во многих исследованиях и экспериментах способность вакцины индуцировать врожденный иммунитет дает возможности для профилактики и лечения как инфекционных, так и аллергических заболеваний, поскольку способствует переключению Th3 иммунного ответа на Th2. Цель исследования заключалась в изучении эффективности комплексного использования бактериальной терапевтической вакцины Иммуновак-ВП4 и аллерген-специфической иммунной терапии (АСИТ) при поллинозе у детей и взрослых.Материалы и методы. Бактериальную терапевтическую вакцину Иммуновак-ВП4 применяли ежегодно, назальным и оральным введением у пациентов до начала курса АСИТ стандартизованными водно-солевыми растворами аллергенов.Результаты. Применение бактериальной терапевтической вакцины Иммуновак-ВП4 до начала курса АСИТ способствовало снижению частоты острых респираторных инфекций в 8,5 раза по сравнению с группой контроля. Клиническая эффективность комплексного лечения по результатам анкетирования пациентов через 7 лет после начала терапии составила 90%. Отмечены достоверное снижение IgG4 к причинно-значимым аллергенам, общего иммнуноглобулина E (IgE) и тенденция к уменьшению IgE. Заключение. Использование бактериальной терапевтической вакцины Иммуновак-ВП4, являющейся естественным лигандом толл-подобных рецепторов в сочетании с АСИТ, представляется эффективным и перспективным направлением при лечении аллергических заболеваний.Ключевые слова: поллиноз, PAMPs, аллерген-специфическая иммунотерапия, бактериальные вакцины, Иммуновак-ВП4, десенсибилизация.https:// doi.org/10.26442/terarkh301890316-20 Application of bacterial therapeutic vaccine Immunovac-VP4 in the treatment of pollinosisM.P. KOSTINOV1,2, A.M. PODDUBIKOVA1, O.O. MAGARSHAK1, A.V. PODDUBIKOV1 1FGBNU I.I. Mechnikov Research Institute of Vaccines and Sera, Laboratory vaccination and immunotherapy of allergic diseases, Moscow, Russia; 2I.M. Sechenov First Moscow State Medical University, Moscow, RussiaSummary In-depth study of the function and structure of the lymphoid tissue of the gastrointestinal tract and respiratory tract opens wide opportunities for the use of mucosal vaccines to improve immunity to various infectious agents. One such drug is The immunovac-VP4 vaccine containing pathogen-associated molecular structures (PAMSs) of microorganisms. They are the antigens of Klebsiella pneumoniae, Proteus vulgaris, Escherichia coli, Staphylococcus aureus. Discovered in many studies and experiments, the ability of the vaccine to induce innate immunity provides opportunities for prevention and treatment of both infections and allergic diseases, because it promotes the switching of Th3 immune response to Th2. The aim of the study was to study the effectiveness of the complex use of bacterial therapeutic vaccine Immunovac-VP4 and allergen-specific immune therapy (ASIT) in pollinosis in children and adults.Materials and methods. Bacterial therapeutic vaccine Immunovac-VP4 was used annually, nasal and oral administration in patients before the course of ASIT standardized aqueous-salt solutions of allergens.Results. The therapeutic application of bacterial vaccines, Immunoac-ВП4 before the course ASIT has helped to reduce the frequency of acute respiratory infections in 8,5 times in comparison with the control group. Clinical efficacy of complex treatment according to the results of the survey of patients in 7 years after the start of therapy was 90%. There was a significant decrease In IgG4 to causally significant allergens, General immnunoglobulin E (IgE) and a tendency to decrease IgE. Conclusion. The use of bacterial therapeutic vaccine Immunovac-VP4, which is a natural ligand of toll-like receptors in combination with ASIT, seems to be an effective and promising direction in the treatment of allergic diseases.Keywords: pollinosis, PAMPs, allergen-specific immunotherapy, bacterial vaccines, Immunovac-VP4, desensitization.
Распространенность поллинозов в различных странах и регионах, по результатам исследований, проведенных ISAAC, колеблется от 2,9 до 54,1%. Распространенность поллинозов в структуре аллергических заболеваний достигает 24% [1]. Исследования, проведенные сторонниками «гигиенической» гипотезы указывают на географические, связанные с уровнем урбанизации и сапиентации, различия в распространенности аллергических заболеваний. Единственным патогенетическим способом лечения поллинозов до настоящего времени является аллерген-специфическая иммунная терапия (АСИТ), поскольку она способна изменить тип иммунного ответа с Th3 на Th2, снизить уровни специфических иммуноглобулинов E (IgE) [2–8]. Эффективность АСИТ, которая применяется более 100 лет, не вызывает сомнений. Однако успешное проведение курсов АСИТ прерывается рецидивирующими респираторными инфекциями и их осложнениями [9, 10]. Индукция периферической Т-клеточной толерантности и формирование регуляторных Т-клеток являются ключевыми механизмами АСИТ. СD4+, CD25+ регуляторные клетки, индуцированные интерлейкином-10 (ИЛ-10) и TGF-β, способны индуцировать первый тип регуляторных Т-клеток и, возможно, способны предупредить развитие аллергических заболеваний, а также играют важную роль в успешности АСИТ. Механизмами такого действия являются: подавление различных провоспалительных клеток, таких как эозинофилы, тучные клетки, базофилы, развитие толерантности к аллергену с прямым или косвенным вовлечением T-регуляторных клеток, формирование противоспалительных антител (АТ), особенно IgG4, индуцированных ИЛ-10 [11]. Включение в терапию поллинозов при АСИТ патоген-ассоциированных молекулярных структур (pathogen-associated molecular patterns – PAMPs) с целью предотвращения острых респираторных инфекций (ОРИ) и повышения эффективности АСИТ является наиболее перспективным [12, 13]. Одним из таких препаратов является поликомпонентная вакцина Иммуновак-ВП4, имеющая в своем составе липополисахарид, пептидогликан, тейхоевую кислоту, белковые антигены клеточных стенок (производства ФГУП «НПО «Микроген» Минздрава РФ). При использовании Иммуновак-ВП4 формируется невосприимчивость к ОРИ посредством активации системы врожденного иммунитета [14, 15]. Особое место в этих механизмах имеет липополисахарид грамотрицательных бактерий [16]. Показана способность PAMPs, входящих в состав вакцины Иммуновак-ВП4, индуцировать иммунитет, формировать невосприимчивость к ОРИ, снижать частоту обострений хронических заболеваний и способствовать переключению с Th3- на Th2-тип иммунного ответа [17].Цель исследования заключалась в изучении эффективности комплексного использования бактериальной терапевтической вакцины Иммуновак-ВП4 и АСИТ при поллинозе у детей и взрослых. Материалы и методы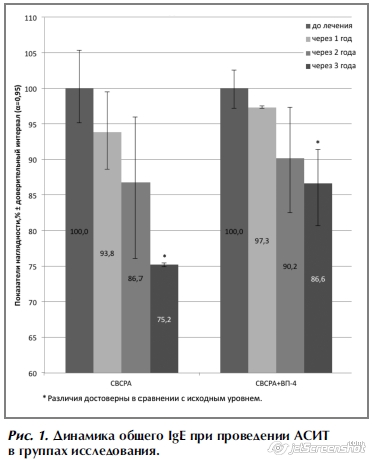 В исследовании принимали участие 69 человек в возрасте от 5 до 40 лет, при этом большинство (59) дети и подростки до 18 лет. Всем участникам исследования проводили подкожным введением АСИТ поллинозов стандарными водно-солевыми растворимыми аллергенами (СВСРА) в сочетании с вакциной Иммуновак-ВП4. Исследование проведено на базе поликлиники №1 Управления делами Президента и консультативного центра при ФГБНУ НИИВС им. И.И. Мечникова. Пациентов разделили на 2 группы случайным образом. В первую вошли 22 человека, которым проводили АСИТ с ежегодно предшествовавшим ему курсом вакцинации Иммуновак-ВП4. Контрольная группа из 47 человек проходили лечение СВСРА. Всем пациентам АСИТ проводилась впервые в период ремиссии, вне сезона пыления. В состав вакцины Иммуновак-ВП4 входят PAMPs 4 условно-патогенных бактерий: Klebsiella pneumоniae, Proteus vulgaris, Escherichia coli и Staphylococcus aureus. Препарат применяли назальным и оральным способом по схеме перед началом курсов АСИТ [20]. У 55% больных поллиноз протекал как сезонный риноконъюнктивит, у 20% – в виде бронхиальной астмы легкого и среднего течения и у 25% выявлено сочетание этих двух нозологий. Длительность заболевания варьировала от 2 до 10 лет. Диагноз «поллиноз» ставили на основании данных анамнеза, клинической картины и результатов лабораторных исследований. Всем больным проводили скарификационные кожные пробы с СВСРА, цитологию слизистой оболочки носа, исследовали функцию внешнего дыхания (ФВД), определяли уровни IgE, специфических IgE и IgG4 методом иммуноферментного анализа (ИФА). Проводили анкетирование включенных в исследование пациентов до начала и после завершения каждого из трех курсов АСИТ. Анкета содержала вопросы, касающиеся степени выраженности симптомов аллергического заболевания, дозировки и кратности приема противоаллергических препаратов, частоты ОРИ до начала и в период лечения [21]. В исследовании принимали участие 69 человек в возрасте от 5 до 40 лет, при этом большинство (59) дети и подростки до 18 лет. Всем участникам исследования проводили подкожным введением АСИТ поллинозов стандарными водно-солевыми растворимыми аллергенами (СВСРА) в сочетании с вакциной Иммуновак-ВП4. Исследование проведено на базе поликлиники №1 Управления делами Президента и консультативного центра при ФГБНУ НИИВС им. И.И. Мечникова. Пациентов разделили на 2 группы случайным образом. В первую вошли 22 человека, которым проводили АСИТ с ежегодно предшествовавшим ему курсом вакцинации Иммуновак-ВП4. Контрольная группа из 47 человек проходили лечение СВСРА. Всем пациентам АСИТ проводилась впервые в период ремиссии, вне сезона пыления. В состав вакцины Иммуновак-ВП4 входят PAMPs 4 условно-патогенных бактерий: Klebsiella pneumоniae, Proteus vulgaris, Escherichia coli и Staphylococcus aureus. Препарат применяли назальным и оральным способом по схеме перед началом курсов АСИТ [20]. У 55% больных поллиноз протекал как сезонный риноконъюнктивит, у 20% – в виде бронхиальной астмы легкого и среднего течения и у 25% выявлено сочетание этих двух нозологий. Длительность заболевания варьировала от 2 до 10 лет. Диагноз «поллиноз» ставили на основании данных анамнеза, клинической картины и результатов лабораторных исследований. Всем больным проводили скарификационные кожные пробы с СВСРА, цитологию слизистой оболочки носа, исследовали функцию внешнего дыхания (ФВД), определяли уровни IgE, специфических IgE и IgG4 методом иммуноферментного анализа (ИФА). Проводили анкетирование включенных в исследование пациентов до начала и после завершения каждого из трех курсов АСИТ. Анкета содержала вопросы, касающиеся степени выраженности симптомов аллергического заболевания, дозировки и кратности приема противоаллергических препаратов, частоты ОРИ до начала и в период лечения [21].РезультатыПо окончании первого курса АСИТ у всех пациентов регистрировали снижение интенсивности клинических проявлений поллиноза, уменьшение объема паллиативного лечения. На рис.1 представлена динамика сывороточного общего IgЕ. Данные представлены в показателях наглядности, исходный уровень антител принимали за 100%. Представленные данные свидетельствуют о постепенном снижении количества IgE во всех группах получавших АСИТ. После третьего года терапии снижение общего IgE было статистически достоверным. Наиболее выраженное уменьшение содержания IgE наблюдали в группе пациентов, у которых АСИТ сочеталась с вакциной Иммуновак-ВП4.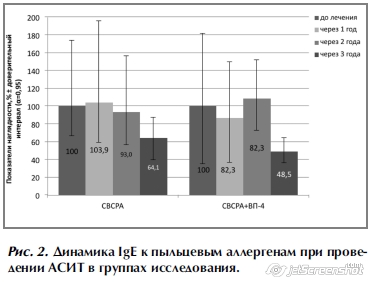 На рис. 2 представлена динамика уровней IgЕ-антител к пыльцевым аллергенам в показателях наглядности. В виду большого колебания индивидуальных данных, по результатам исследования можно свидетельствовать лишь о тенденции в изменении уровней специфических IgE в годовой динамике. При этом в обеих группах можно отметить тенденцию к снижению уровней специфического IgE после третьего года проведения АСИТ. В группе пациентов, получавших Иммуновак-ВП4, снижение оказалось статистически достоверным по отношению к уровням предыдущего года. Также следует отметить усреднение этого показателя, которое стало особенно выраженным по окончании терапии. Включение Иммуновак-ВП4 в курс АСИТ привело к изменению в профиле IgG4-антител у пациентов после окончания первого года АСИТ в этой группе (рис. 3). Количество антител относительно исходного уровня возросло на 84,4% (в группе сравнения на 36,2%). Однако после второго курса лечения количество IgG4-антител снизилось до 61,6% от исходного (в группе сравнения до 83,4%). После третьего года АСИТ количество IgG4-антител в группе пациентов, получавших Иммуновак-ВП4, снизилось до 47,5%, тогда как в контрольной группе практически вернулось к исходному уровню. Во время проведения АСИТ регистрировали сопутствующую заболеваемость ОРИ. В первой группе пациентов заболеваемость составила 4,5%. При этом в группе сравнения заболеваемость составляла 38,3%. Следует отметить, что в ранее проведенном исследовании с одновременным использованием АСИТ На рис. 2 представлена динамика уровней IgЕ-антител к пыльцевым аллергенам в показателях наглядности. В виду большого колебания индивидуальных данных, по результатам исследования можно свидетельствовать лишь о тенденции в изменении уровней специфических IgE в годовой динамике. При этом в обеих группах можно отметить тенденцию к снижению уровней специфического IgE после третьего года проведения АСИТ. В группе пациентов, получавших Иммуновак-ВП4, снижение оказалось статистически достоверным по отношению к уровням предыдущего года. Также следует отметить усреднение этого показателя, которое стало особенно выраженным по окончании терапии. Включение Иммуновак-ВП4 в курс АСИТ привело к изменению в профиле IgG4-антител у пациентов после окончания первого года АСИТ в этой группе (рис. 3). Количество антител относительно исходного уровня возросло на 84,4% (в группе сравнения на 36,2%). Однако после второго курса лечения количество IgG4-антител снизилось до 61,6% от исходного (в группе сравнения до 83,4%). После третьего года АСИТ количество IgG4-антител в группе пациентов, получавших Иммуновак-ВП4, снизилось до 47,5%, тогда как в контрольной группе практически вернулось к исходному уровню. Во время проведения АСИТ регистрировали сопутствующую заболеваемость ОРИ. В первой группе пациентов заболеваемость составила 4,5%. При этом в группе сравнения заболеваемость составляла 38,3%. Следует отметить, что в ранее проведенном исследовании с одновременным использованием АСИТ  и вакцины Иммуновак-ВП4 не обнаружено клинических эффектов, наблюдаемых при превентивном назначении вакцины Иммуновак-ВП4. В группе из 25 больных поллинозом при использовании АСИТ с параллельным курсом Иммуновак-ВП4 заболеваемость ОРИ составила 32%, т.е. оказалась сопоставима с заболеваемостью, регистрируемой нами в группе сравнения. Результаты анкетирования пациентов свидетельствуют о высоком клиническом эффекте АСИТ по завершению 3-летнего курса лечения, который характеризовался сокращением количества эпизодов ОРИ, их продолжительности, тяжести и объема лекарственной терапии. При этом включение вакцины Иммуновак-ВП4 в схему лечения привело к повышению клинической эффективности АСИТ в среднем на 15% по сравнению с группой контроля. Большой интерес представляют результаты отсроченного анкетирования спустя 7 лет после начала АСИТ (рис. 4). Все больные отмечали снижение тяжести симптомов поллиноза. В случае проведения АСИТ с предварительным использованием вакцины Иммуновак-ВП4 эффективность лечения по результатам анкетирования через 7 лет достигала в среднем 90% против 65% у больных, получавших только АСИТ. Можно предположить, что назначение Иммуновак-ВП4 у пациентов с поллинозом увеличивает потенциал иммунологических механизмов АСИТ с восстановлением патологических сдвигов и достижением более продолжительной клинической ремиссии заболевания [22]. и вакцины Иммуновак-ВП4 не обнаружено клинических эффектов, наблюдаемых при превентивном назначении вакцины Иммуновак-ВП4. В группе из 25 больных поллинозом при использовании АСИТ с параллельным курсом Иммуновак-ВП4 заболеваемость ОРИ составила 32%, т.е. оказалась сопоставима с заболеваемостью, регистрируемой нами в группе сравнения. Результаты анкетирования пациентов свидетельствуют о высоком клиническом эффекте АСИТ по завершению 3-летнего курса лечения, который характеризовался сокращением количества эпизодов ОРИ, их продолжительности, тяжести и объема лекарственной терапии. При этом включение вакцины Иммуновак-ВП4 в схему лечения привело к повышению клинической эффективности АСИТ в среднем на 15% по сравнению с группой контроля. Большой интерес представляют результаты отсроченного анкетирования спустя 7 лет после начала АСИТ (рис. 4). Все больные отмечали снижение тяжести симптомов поллиноза. В случае проведения АСИТ с предварительным использованием вакцины Иммуновак-ВП4 эффективность лечения по результатам анкетирования через 7 лет достигала в среднем 90% против 65% у больных, получавших только АСИТ. Можно предположить, что назначение Иммуновак-ВП4 у пациентов с поллинозом увеличивает потенциал иммунологических механизмов АСИТ с восстановлением патологических сдвигов и достижением более продолжительной клинической ремиссии заболевания [22].ОбсуждениеПолученные результаты исследования свидетельствуют о высокой эффективности применения вакцины Иммуновак-ВП4 в клинической практике АСИТ поллинозов. Способность PAMPs регулировать врожденный и адаптивный иммунный ответ, переключать с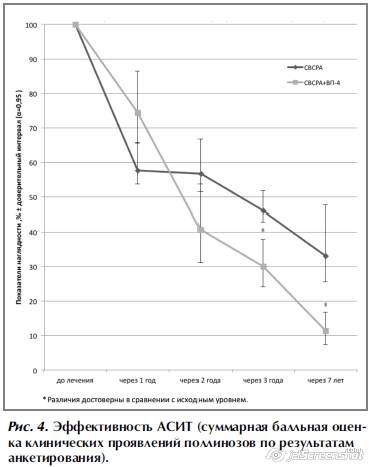 Th3-ответа на Th2-ответ, дает возможность рассматривать их как патогенетические средства, обладающие адъювантными и аддитивными свойствами, как новые лекарственные средства для иммунотерапии, в том числе аллергических заболеваний. Свидетельством эффективности комплексного применения препаратов является уменьшение сезонного роста специфических для аллергенов сывороточных уровней IgE. Во второй группе, где применялось комбинированное лечение, отмечали более низкую (в 8,5 раза) частоту ОРИ в период проведения АСИТ по сравнению с контрольной группой. Результаты исследования подтверждают, что препарат Иммуновак-ВП4 имеет высокую эффективность при лечении поллинозов в случае назначения его до начала АСИТ. Эти результаты можно объяснить двойственным эффектом Иммуновак-ВП4 при аллергических заболеваниях, как препарата, содержащего PAMPs. Первоначально показано, что липополисахариды (ЛПС) увеличивают синтез IgE in vitro, но в последствии in vivo установлено, что ЛПС ингибируют выработку аллерген-специфических IgE в том случае, когда вводится перед сенсибилизацией [16]. Известно, что доза ЛПС и период введения могут являться критическими факторами, определяющими эффекты TLR4 лигандов на проявления аллергического ответа. В эксперименте низкие аспирационные дозы ЛПС усиливают Th3-ответ на антиген сенсибилизации и на эозинофильное воспаление, тогда как высокие дозы ЛПС взывают Th2-ответ без эозинофильного воспаления в легких [23]. Помимо эффектов влияния TLR4, в настоящее время имеются данные о модуляции Th3-типа аллергического ответа в отношении еще трех рецепторов: TLR2, TLR7 и TLR9. Th3-ответа на Th2-ответ, дает возможность рассматривать их как патогенетические средства, обладающие адъювантными и аддитивными свойствами, как новые лекарственные средства для иммунотерапии, в том числе аллергических заболеваний. Свидетельством эффективности комплексного применения препаратов является уменьшение сезонного роста специфических для аллергенов сывороточных уровней IgE. Во второй группе, где применялось комбинированное лечение, отмечали более низкую (в 8,5 раза) частоту ОРИ в период проведения АСИТ по сравнению с контрольной группой. Результаты исследования подтверждают, что препарат Иммуновак-ВП4 имеет высокую эффективность при лечении поллинозов в случае назначения его до начала АСИТ. Эти результаты можно объяснить двойственным эффектом Иммуновак-ВП4 при аллергических заболеваниях, как препарата, содержащего PAMPs. Первоначально показано, что липополисахариды (ЛПС) увеличивают синтез IgE in vitro, но в последствии in vivo установлено, что ЛПС ингибируют выработку аллерген-специфических IgE в том случае, когда вводится перед сенсибилизацией [16]. Известно, что доза ЛПС и период введения могут являться критическими факторами, определяющими эффекты TLR4 лигандов на проявления аллергического ответа. В эксперименте низкие аспирационные дозы ЛПС усиливают Th3-ответ на антиген сенсибилизации и на эозинофильное воспаление, тогда как высокие дозы ЛПС взывают Th2-ответ без эозинофильного воспаления в легких [23]. Помимо эффектов влияния TLR4, в настоящее время имеются данные о модуляции Th3-типа аллергического ответа в отношении еще трех рецепторов: TLR2, TLR7 и TLR9.Заключение«Гигиеническая гипотеза», имеющая в своей основе географические различия распространенности аллергических заболеваний, указывает на влияние внешних факторов на этот процесс [24]. Считают, что улучшение гигиенических условий, урбанизация, вакцинация, использование антибиотиков для контроля инфекций в раннем возрасте лишают иммунную систему новорожденного экспозиции бактериальных аллергенов, необходимой для стимуляции T1-лимфоцитов, что приводит к доминированию в иммунном ответе T2-лимфоцитов. Атопические аллергические заболевания характеризуются иммунопатологическим доминированием Th3-лимфоцитов. «Гигиеническая гипотеза» имеет очевидное значение в профилактике аллергических заболеваний, поскольку указывает на то, что увеличение контакта с микроорганизмами в раннем возрасте может играть важную роль в уменьшении распространенности атопических заболеваний. С этой позиции препарат ВП-4 можно рассматривать как превентивное средство – вакцину – источник бактериальных антигенов для лиц, находящихся в условиях высокого риска развития атопических заболеваний. Эффекты вакцины ВП-4 и ее безопасность в отношении развития аутоиммунных заболеваний, аллергических, инфекционных заболеваний почек, кожи, герпетических инфекций хорошо изучены [25–27]. Являясь природным комплексом, содержащим лиганды для различных TLR [11,15], ВП-4 имеет преимущества природного ЛПС по части обеспечения Th2/Th3-баланса перед разрабатываемыми препаратами, дериватами ЛПС. Использование естественных и синтетических лигандов TLR является перспективой для развития новых иммунотерапевтических стратегий при лечении аллергических заболеваний. В дальнейшем считаем необходимым определить препараты и дозы, оптимальные для профилактики или лечения аллергии, изучить возможность объединения агонистов TLR с антигенами для АСИТ, установить их соотношение и пути введения.Авторы заявляют об отсутствии конфликта интересов. Сведения об авторах: Костинов Михаил Петрович – д.м.н., проф., зав. лабораторией вакцинопрофилактики и иммунотерапии аллергических заболеваний ФГБНУ НИИВС им. И.И. МечниковаМагаршак Ольга Олеговна – к.м.н., с.н.с. лаборатории вакцинопрофилактики и иммунотерапии аллергических заболеваний ФГБНУ НИИВС им. И.И. МечниковаПоддубиков Александр Владимирович – к.м.н., зав. лабораторией микробиологии ФГБНУ НИИВС им. И.И. Мечникова Контактная информация: Поддубикова Анна Михайловна – м.н.с. лаборатории микробиологии ФГБНУ НИИВС им. И.И. Мечникова, e-mail: [email protected]; тел.: +7(910)416-16-22 Список исп. литературыСкрыть список 1. РАДАР. Аллергический ринит у детей: рекомендации и алгоритм при детском аллергическом рините. – М.: Оригинал-макет; 2015:80. Ссылка активна на 30.05.2016. [RADAR. Allergic rhinitis at children: recommendations and algorithm at children's allergic rhinitis. Moscow: Dummy;2015:80. (In Russ.)]. Accessed 30.05.2016. http://new.mosgorzdrav.ru/uploads/imperavi/ru-RU/029_2015.pdf 2. Jacobsen L, Wahn U, Bilo MB. Allergen-specific immunotherapy provides immediate, long-term and preventive clinical effects in children and adults: the effects of immunotherapy can be categorised by level of benefit - the centenary of allergen specific subcutaneous immunotherapy. Clinical and Translational Allergy 2012;2:8. doi:org/10.1186/2045-7022-2-8 3. Аллергия у детей: от теории - к практике. Под ред. Л.С. Намазовой-Барановой. М.: Союз педиатров России. 2010-2011:668. [An allergy at children: from the theory - to practice. Under the editorship of L.S. Namazova-Baranova. M.: Union of pediatricians of Russia. 2010-2011:668. (In Russ.)]. 4. Павлова К.С., Курбачева О.М. Патогенетическая терапия аллергических заболеваний: возможности АСИТ в России. Эффективная фармакотерапия. Аллергология и иммунология. 2012;2. [Pavlova KS, Kurbachev OM. Patogeneticheskaya therapy of allergic diseases: possibilities of ASIT in Russia. Effective pharmacotherapy. Allergology and immunology. 2012; 2. (In Russ.)]. http://elibrary.ru/download/ 59185464.pdf Accessed 16.05.2016 http://elibrary.ru/download/ 59185464.pdf. Ссылка активна на 16.05.2016 5. Вишнева Е.А, Намазова-Баранова Л.С., Алексеева А.А., Эфендиева К.Е, Левина Ю.Г, Томилова А.Ю. и др. Аллерген-специфическая иммунотерапия у детей. Стандартизация подходов к оценке эффективности. Педиатрическая фармакология. 2015;12(2):173-179. [Vishneva EA, Namazova-Baranova LS, Alekseeva AA, Efendiyeva KE, Levina YuG, Tomilova AYu et al. Allergenspetsifichesky immunotherapy at children. Standardization of approaches to to efficiency assessment. Pediatric pharmacology. 2015;12(2):173-179. (In Russ.)]. doi.org/10.15690/ pf.v12i2.1280 6. Wesley BА et al. Mechanisms of allergen-specific immunotherapy. J Allergy Clin Immunol. 2013;131:1288-96. doi.org/10.1186%2Fs40413-015-0063-2 7. Shamji MH, Durham SR. Mechanisms of immunotherapy to aeroallergens. Clin. Exp. Allergy. 2011;4:1235-1246. doi:10.1111/j.1365-222.2011.03804.x 8. Scadding G, Durham S. Mechanisms of sublingual immunotherapy. J. Asthma. 2009;46:322-334. doi:10.1080/02770900902785729 9. Бочарова К.А. Профилактика рецидивирующих респираторных инфекций у пациентов с бронхиальной астмой. Научный результат. 2015;3:36-42. [Bocharova KA. Prevention of recurrent respiratory infections at patients with bronchial asthma. Scientific result. 2015;3:36-42. (In Russ.)]. doi:10.18413/2313-8955-2015-1-3-36-42 10. Булгакова В.А., Балаболкин И.И. Применение иммунофармакопрепаратов при бронхиальной астме у детей. Медицинский совет. 2008;1-2:61-66. [Bulgakova VA, Balabolkin II. Application of immunofarmakopreparat at bronchial asthma at children. Medical council. 2008;1-2:61-66. (In Russ.)]. http://elibrary.ru/download/60561501.pdf ссылка доступна на 18.05.16 11. Егорова Н.Б., Ахматова Н.К., Курбатова Е.А. и др. Клеточные и молекулярные основы антимикробного мукозального иммунитета. Москва: ООО «ИПП КУНА»; 2013. [Egorova NB, Akhmatova NK, Kurbatova EA et al. Cellular and molecular bases of antimicrobic mukozalny immunity. Moscow: JSC IPP KUNA; 2013. (In Russ.)]. 12. Алексеева А.А., Левина Ю.Г., Торшхоева Р.М. и др. Клинический пример использования рибосомального комплекса в терапии часто болеющего ребенка. Вопросы современной педиатрии. 2011;2;10:211-215. [Alekseeva AA, Levina JG, Torshkhoyeva RM et al. Clinical example of the use of ribosomal complex therapy of frequently ill child. Issues of modern Pediatrics. 2011;2;10:211-215. (In Russ.)] http://elibrary.ru/download/10539376.pdf Ссылка доступна на18.05.16 13. Егорова Н.Б., Курбатова Е.А., Грубер И.М. и др. Новый тип вакцин с комбинацией агонистов toll-подобных рецепторов-tlrs 1/2, 4,5/6, 9. Журнал микробиологии, эпидемиологии и иммунологии. 2011;4:40-46. [Egorova NB, Kurbatova EA, Gruber IM et al. New type of vaccines with a combination of agonists of toll-like receptors-tlrs 1/2, 4,5/6, 9. Journal of Microbiology, epidemiology and immunology. 2011;4:40-46. (In Russ.)]. http://elibrary.ru/item.asp?id=23087760 Ссылка доступна на 18.05.16 14. Булгакова В.А., Балоболкин И.И. Иммунофармакотерапия детей с аллергическими болезнями. Педиатрическая фармакология. 2006;3:22-28. [Bulgakova VA, Balobolkin II. Immunopharmacotherapy children with allergic diseases. Pediatric Pharmacology. 2006;3:22-28. (In Russ.)] http://elibrary.ru/download/60470864.pdf Accessed 18.05.16 15. Ахматова Н.К., Киселевский М.В. Врожденный иммунитет: противоопухолевый и противоинфекционный. М.: Практическая медицина; 2008:256. [Akhmatova NK, Kisielewski MV. Innate immunity: anti-tumor and anti-infective; M.; Practical Medicine; 2008:256. (In Russ.)] http://preview.medprint.ru/978-5-98811-111-5.pdf Accessed 18.05.16 16. Tulic MK, Fiset PO, Manoukian JJ et al. Role of Toll-like receptor 4 in protection by bacterial lipopolysaccharide in the nasal mucosa of atopic children but not adults. Lancet. 2004; 363:1689-97 doi:10.1111/j.1365-2249.2006.03296.x 17. Егорова Н.Б., Курбатова Е.А. Иммунотерапевтическая концепция использования микробных антигенов при атопии и патологии, ассоциированной с условно-патогенной микрофлорой (на примере поликомпонентной вакцины Иммуновак-ВП4). Медицинская иммунология. 2008; 10 (1): 13-20. [Yegorova NB, Kurbatova EA. Immunotherapeutic concept of using microbial antigens in atopy and pathology associated with pathogenic microflora (for example, Immunovac-VP4 multicomponent vaccines). Medical immunology. 2008; 10 (1): 13-20. (In Russ.)] doi: http://dx.doi.org/10.15789/1563-0625-2008-1-13-20 18. Burks W, Calderon МА, Casale Т, Сох L, Demoly Р, Jutel М, Nelson Н, Akdis Cezmi А. Update оп allergy immunotherapy: American Academy of Allergy, Asthma & Immunology/European Academy of Allergy and Clinical Immunology/PRACTALL consensus report. Allergy Clin Immunol. 2013; 131: 1288-96. doi: 10.1186/1939-4551-7-23 19. Гущин И.С., Курбачева О.М. Аллергия и аллерген-специфическая иммунотерапия. М.: Фармарус Принт Медиа, 2010; 228: 16. [Gushchin JS, Kurbacheva OM. Allergy and allergenspetsificheskye immunotherapy. M.: Farmarus Print Media. 2010; 228:16. (In Russ.)]. 20. Семенов Б.Ф., Егорова Н.Б., Семенова И.Б., Курбатова Е.А. Терапевтические вакцины. Российские медицинские вести. 2000; 5; 3: 26-32. [Semenov BF, Egorova NB, Semenova IB, Kurbatova EA. Therapeutic vaccines. Russian medical vesti. 2000; 5; 3: 26-32. (In Russ.)]. http://elibrary.ru/item.asp?id=23038332 Accessed 18.05.16 21. Ильина Н.И., Павлова К.С. Повышая доступность качественного и современного лечения аллергических заболеваний. Лечащий врач. 2012;3: 97. [Ilyina NI, Pavlova KS. By increasing the availability of high-quality and modern treatment of allergic diseases. Attending vrach. 2012; 3: 97. (In Russ.)]. http://www.lvrach.ru/2012/03/ 15435385/ Accessed 18.05.16 22. Allergen-specific immunotherapy provides immediate, long-term and preventive clinical effects in children and adults: the effects of immunotherapy can be categorised by level of benefit - the centenary of allergen specific subcutaneous immunotherapy. Clinical and Translational Allergy. 2012; 2:8. doi: 10.1186/2045-7022-2-8 23. Eisenbarth SC, Piggott DA, Huleatt JW et al. Lipopolysaccharide-enhanced, toll-like receptor 4-dependent T helper cell type 2 responses to inhaled antigen. J Exp Med. 2002;196:1645-1651. doi: 10.1084/jem. 20021340 24. Ненашева Н.М. Атопическая бронхиальная астма: роль аллерген- специфической иммунотерапии. Российский аллергологический журнал. 2015;6:54-67. [Nenashev NM. Atopic asthma: the role of allergen specific immunotherapy. Russian journal Allergy. 2015;6:54-67. (In Russ.)]. Http://elibrary.ru/item.asp?id=25475435 Ссылка доступна на 18.05.16 25. Егорова Н.Б., Семенов Б.Ф., Курбатова Е.А. Динамика аутоантител у пожилых людей в процессе вакцинации грипполом и поликомпонентной вакциной ВП-4. Журнал микробиологии, эпидемиологии и иммунобиологии. 2002;5;29-35. [Egorova NB, Semenov BF, Kurbatova EA. Dynamics of autoantibodies in elderly people in the process of vaccination Grippol and multicomponent vaccine VP-4. Journal of Microbiology, Epidemiology and immunobiologii. 2002;5;29-35. (In Russ.)]. http://rusalljournal.ru/raj-6-2015/n-m-nenasheva-atopicheskaya-bronxialnaya-astma-rol-allergen-specificheskoj-immunoterapii54-67/ Accessed 18.05.16 26. Костинов М.П. Иммунокоррекция в педиатрии. Практическое руководство для врачей. М.: Медицина для всех, 1997: 111. [ Kostinov MP. Immunocorrection in pediatrics. A practical guide for doctors. M.: Medicine for all, 1997: 111.(In Russ.)]. http://elibrary.ru/item.asp?id= 20264263 27. Клинико-иммунологическая эффективность иммунобиологических препаратов. Справочник. М.П. Костинов, Н.А. Озерецковский, ред. М.: Миклош, 2004: 256. [Clinical and immunological efficacy of immunobiological preparations. Directory. M. P. Kostinov, N.А. Ozeretskovsky, ed., Moscow: Miklosh, 2004: 256. (In Russ.)]. http://elibrary.ru/item.asp?id=23053132 28. Костинов М.П. Иммунокоррекция в педиатрии. Практическое руководство для врачей. Издание 2-е доп. М.: Медицина для всех, 2001: 240 с. [Kostinov MP. Immunocorrection in pediatrics. A practical guide for doctors. Edition 2 nd ext. M.: Medicine for all, 2001: 240 s. (In Russ.)]. http://elibrary.ru/item.asp?id=20264263 Поступила 24.05.2017 con-med.ru оценка научной публикацииРеактогенность и безопасность поликомпонентной вакцины(ВП-4) при профилактике острых респираторных заболеваний у дошкольников. Оценка научной публикации Дизайн Данное исследование является экспериментальным (рандомизированное полевое контролируемое испытание), аналитическим, выборочным, научным (исследование специально организуется для получения новых данных), проспективным, одномоментным (поперечным) так как изучается заболеваемость за ограниченный отрезок времени. Название Название статьи достаточно информативно, кратко, которое полностью отражает тему статьи. Отношения между компонентами названия полностью понятны и являются терминологически точными. В названии нет ненужного многословия и «балласта». Название статьи построено достаточно грамотно: все слова согласованны друг с другом и связаны по смыслу, в названии нет грамматических и орфографических ошибок. Абстракт Является информативным, то есть содержит информацию о том, что было проделано и каким образом. Абстракт структурированный, так как включают в очень сжатом виде все основные разделы статьи. В абстракте имеется цель проведения данного исследования, что было проделано, что установлено и сделано заключение. Цифровые данные представлены в абстракте там, где это необходимо (определения числа участников в данном исследовании, схема применения). Абстракт написан очень понятно, прописаны основные моменты статьи и сделано заключение. Лишней информации нет. Объем абстракта полностью охватывает содержание всей статьи. Во введении представлена информация о составе вакцины ВП – 4, установленном эффекте ВП- 4 пи терапии хронических рецидивирующих заболеваний дыхательного тракта. Достаточно подробна описана цель данного исследования. Читателя может заинтересовать то, что после проведения курса вакцинотерапии заболеваемость респираторными заболеваниями (ОРЗ) снижалась в 2,9 раза. Данная информация способствует привлечению и удержанию внимания гипотетического читателя. Материалы и методы В данной работе представлены и проанализированы результаты профилактики ОРЗ поликомпонентной вакциной в 4 детских дошкольных учреждений (ДДУ) Северо–восточного округа Москвы при детской поликлинике №55 в соответствии с разрешением Комитета здравоохранения от 17.10.99 и с согласия родителей. Численность опытной группы составляла 168 детей в возрасте от 2,6 до 6 лет. В группу сравнения вошли 120 детей из тех же ДДУ того же возраста. Вакцинацию проводили с 25.01.99 по 25.02.99 в период пика эпидемии гриппа и на фоне резкого подъема заболеваемости ОРЗ. Для проведения профилактики применяли вакцину поликомпонентную высушенную во флаконах по 4 мг (1 пероральная доза), разрешенную к применению в практике здравоохранения приказом МЗ РФ от17.11.93. Схема проведения ВП – 4 состояла из 3 назальных и 6 – 9 пероральных введений с интервалом 3 – 4 дня. Длительность курса 26±4 дня. Формат стать удобен читателю. Из- за отсутствия рисунков и таблиц статья выглядит незавершенной (например: можно добавить таблицу со схемой применения). Статистическую обработку данных проводили с помощью критерия t Стьюдента. При анализе результатов было установлено, что заболеваемость детей ОРЗ была одинаково высокой в опытный и контрольной группах, составляя 33,3 ±3,6 и 31,7±4,2% соответственно (p>0,05).Число эпизодов заболеваний на 1 ребенка – 0,34 и 0,35 соответственно, средняя длительность 1 эпизода болезни в сравниваемых группах различий не имели (p>0,05). В этот же период была изучена частота появления заболеваний, нередко осложняющих течение гриппа и ОРЗ и склонных к рецидивирующему течению (бронхит, отит, и др.), а также аллергических и соматических заболеваний. Оказалось, что введение вакцины не увеличивало число этих заболеваний в опытной группе по сравнению с контрольной. Результаты проведенного исследования представлены наглядно, в виде таблиц, при анализе которых, читатель понимает и не теряет нить рассуждений. Цифровые значения, представленные в работе, полностью согласуются между собой. Этот раздел посвящен обсуждению результатов исследования и тому, как их надо понимать и интерпретировать. В этом разделе дается четкий ответ на цель исследования – оценка реактогенности и безопасности поликомпонентной вакцины, примененной для профилактики ОРЗ у детей, а так же ее влияния на появление вакциноиндуцированных аллергических реакций, латентно протекающих процессов и уровня заболеваемости ОРЗ. Ответ на вопрос исследования дается далеко не в самом начале. К концу статьи возникает полное ощущение завершенности и получения ответов на все вопросы. В статье, в основном, представлены факты, мнения авторов нет. Кафедра эпидемиологии Оценка научной публикации «Реактогенность и безопасность поликомпонентной вакцины (ВП – 4) при профилактике острых респираторных заболеваний у дошкольников» Выполнила: студентка 5 курса Преподаватель: Полибин Р.В. г. Москва 2010 г. studfiles.net |
г.Самара, ул. Димитрова 131 [email protected] |
 |