|
|
||||||||||
|
Индивидуальная вакцина от меланомы вызывает мощный иммунный ответ. Вакцина от меланомыВакцина от меланомы работает, но стоит очень дорого - МедНовостиНовый класс персонализированных противораковых вакцин, адаптированных к опухолям отдельных пациентов, задержал развитие болезни в двух независимых клинических испытаниях. Nature опубликовал одновременно два разных исследования от двух независимых команд, испытывавших персонализированные вакцины, лечащие или по крайней мере предохраняющие от рецидива меланомы на поздних, практически неизлечимых стадиях болезни. Одна вакцина была разработана в американском Институте Dana Farber (Dana-Farber Institute), а другая — частной немецкой биотехнологической фирмой BioNTech, которая использует так называемый РНК-мессенджер, чтобы воспроизвести код для создания своих «терапевтических» белков. Вакцина, разработанная в Dana Farber, работает с неоантигенами, специфичными для для опухоли конкретного человека. Антигены — это молекулы, которые отображаются на поверхности клеток и стимулируют иммунную систему. Неоантигены являются молекулами на поверхностях клеток, которые продуцируются мутациями ДНК, которые присутствуют в раковых клетках, но отсутствуют в нормальных клетках. что делает неоантигены идеальными мишенями для иммунной терапии против рака, говорят ученыеВакцины, используемые в исследовании фазы I, содержали до 20 неоантигенов, полученных из опухоли конкретного пациента. Вакцины вводили пациентам для тренировки собственной иммунной системы для распознавания этих неоантигенов с целью стимулирования иммунной системы к уничтожению раковых клеток, на поверхности которых они находились. Подход BioNTech заключается в работе с эпитопами, частями макромолекулы антигена, которые непосредственно являются мишенью для иммунных клеток. В чем заключается уникальность новой вакцины? Предыдущие методы иммунотерапии, такие как препараты ингибитора контрольной точки, также вызывают иммунные реакции против неоантигенов рака, но не имеют такой высокой специфичности. Они могут вызывать реакции иммунной системы организма против нормальных тканевых антигенов, приводя к тому, что иммунная система атакует нормальные ткани. Исследователи обнаружили, что персональная вакцина вызвала целенаправленный ответ Т-клеток на несколько неоантигенов опухолей, помимо того, что обычно наблюдается в ответ на существующие виды иммунотерапии. Ученые из Dana-Farber Institute and Broad Institute вводили вакцину шести пациентам с меланомой, опухоли которых были удалены хирургическим путем, и которые были подвержены высокому риску рецидива. Вакцинация была начата через 18 недель после операции. При медиане 25 месяцев после вакцинации у четырех из шести пациентов не было обнаружено доказательств рецидива рака. У двух других пациентов, с метастазами в легкие, болезнь возобновилась после вакцинации. В этот момент они начали лечение препаратом пембролизумаб, который ингибирует иммунную контрольную точку PD-1. Оба пациента получили полное разрушение опухолей в результате курса лечения и увеличение количества специфических Т-клеток, готовых бороться с опухолями в случае рецидива. Вторая, неоэпитопная вакцина, тоже привела к вполне вдохновляющим результатам: иммунный ответ возник у всех пациентов, т-клетки убивали опухолевые клетки, ориентируясь на специфические маркеры-эпитопы. У двоих пациентов был достигнут эффект стабильной выживаемости без роста опухоли. Еще у двух пациентов с метастатической болезнью иммунный ответ был серьезный иммунный ответ, у одного, правда, наблюдался потом рецидив. Третий продемонстрировал полный иммунный ответ в сочетании с иммунотерапевтической блокадой PD1. Результаты исследования показывают, что персонализированная неоантигенная вакцина может потенциально преодолеть два основных препятствия в терапии рака. Одним из них является гетерогенность опухолей: тот факт, что они состоят из клеток с множеством различных признаков, часто позволяет злокачественным опухолям уклоняться от препаратов, нацеленных на злокачественные клетки, имеющие одну и ту же определенную генетическую аномалию. Вакцина, поскольку она содержит много разных неоантигенов из опухоли, нацелена на разные генетические аномалии опухолевых клеток. Этот метод демонстрируют большую перспективу в лечении рака, который обычно развивает устойчивость к моно-препаратам. Второе препятствие при раке состоит в том, чтобы генерировать иммунный ответ, резко сфокусированный только на раковых клетках, избегая при этом атаки на нормальные клетки и ткани. Обе вакцины были запрограммированы атаковать только специфические антигены или их части — эпитопы, и поэтому имели очень скромные побочные эффекты. Несмотря на десятилетия попыток разработать эффективные вакцины против рака, они в основном не смогли создать мощные противоопухолевые иммунные ответы. Авторы нового исследования говорят, что это было связано с тем, что все эти вакцины, как правило, были созданы на основе опухолевых антигенов, которые были слишком похожи на антигены нормальных клеток. В результате организм вырабатывал более слабый иммунный ответ, чтобы избежать атаки на нормальные клетки (процесс, называемый иммунной толерантностью). Поскольку новые вакцины изготавливают по «индивидуальному проекту» для каждого пациента, используя антигены, созданные мутациями, уникальными для рака именно этого конкретного пациента, и присутствуют только на раковых клетках, процесса иммунной толерантности удается избежать. Что дальше? Roche, крупнейший в мире производитель лекарств от рака, уже сделал ставку на технологию BioNTech после подписания в сентябре прошлого года контракта стоимостью 310 миллионов долларов, что позволит ему протестировать немецкую вакцину с помощью препарата для иммунотерапии Tecentriq. Соучредитель и главный исполнительный директор BioNTech Угур Сахин(Ugur Sahin) сообщил, что комбинированные испытания с использованием препарата Roche против различных видов рака должны были начаться уже в конце этого года. Конкурирующая биотехнологическая фирма Neon Therapeutics, которая была создана для проведения исследований в США, начала тестирование своей персонализированной вакцины из неоантигена в сочетании с препаратом Opdivo от Bristol-Myer's в прошлом году. Сколько стоит супер-вакцина? Уже применяющиеся новые препараты, такие как Opdivo и Tecentriq, значительно усиливают иммунную систему организма и тем самым серьезно улучшают шансы на выживание больных с меланомой, но цена курса лечения составляет более 150 000 долларов в год. Сахин признал, что такая высокая стоимость вакцины сначала будет неизбежной, но, возможно, со временем ее цена может быть уменьшена за счет увеличения масштаба и автоматизации производства. «В среднесрочной и долгосрочной перспективе стоимость вакцины должна заметно снизиться. Это индивидуальный метод лечения, но это универсальный процесс», — сказал он. «На данный момент мы находимся на очень ранней стадии, но в долгосрочной перспективе этот новый метод вакцинации может коренным образом изменить подход к лечению онкологических заболеваний». Корнелиус Мелиеф (Cornelius Melief)из Медицинского центра Лейденского университета (Leiden University Medical Center), который не участвовал ни в одном из исследований, подтвердил, что исследование его немецких и американских коллег полностью доказало огромный потенциал неоантигенных вакцин. «Контролируемые рандомизированные клинические испытания фазы II с большим количеством участников теперь необходимы для определения эффективности этих вакцин у пациентов с любым типом рака, который имеет достаточные мутации для обеспечения достаточных целей неоантигена для такого подхода», — сказал он. medportal.ru Индивидуальная вакцина от меланомы вызывает мощный иммунный ответПо предварительным данным первого клинического исследования на людях, проведенного в Washington University School of Medicine, индивидуальные вакцины от меланомы могут быть использованы для получения мощного иммунного ответа против мутаций в опухолях пациентов.
Изготовленная индивидуальная вакцина, которая была дана трем пациентам с развитой меланомой, привела к увеличению числа и разнообразия борющихся с раком Т-клеток, отвечающих на развитие опухоли. Это открытие усиливает иммунотерапию, стратегию лечения, которая помогает иммунной системе обнаруживать и уничтожать раковые клетки. Исследование было опубликовано 2 апреля 2015 года в специальном выпуске Science Express, посвященном иммунологии и иммунотерапии рака. Вакцины от рака были разработаны методом первого секвенирования генома опухолей пациентов и образцов его здоровых тканей для выявления мутировавших белков под названием неоантигены, уникальных для раковых клеток. После этого, используя компьютерные алгоритмы и лабораторные тесты, исследователи смогли предсказать и проверить, какие из этих неоантигенов могут, скорее всего, вызвать сильный иммунный ответ, и которые можно включить в вакцину. Вакцины были введены пациентам с меланомой, которым ранее была проведена операция по удалению опухолей, но у которых рак метастазировал в лимфатические узлы, что является показателем рецидива этого смертельного заболевания. Данные об иммунном ответе, обнаруженном у первых трех пациентов, были опубликованы в статье. Если дополнительное тестирование у большего количества пациентов покажет, что вакцина эффективна, в будущем она может быть дана пациентам в послеоперационном периоде для стимуляции иммунной системы, чтобы она атаковала раковые клетки и предупреждала рецидивы. «Это исследование показывает, что индивидуально созданные вакцины могут вызвать очень сильный иммунный ответ, — говорит автор Геральд Линнет, онколог Вашингтонского университета, ведущий клинические исследования в Siteman Cancer Center иBarnes-Jewish Hospital. -Опухолевые антигены мы вводим в вакцину, провоцируя сильный ответ среди Т-клеток, киллеров иммунной системы, отвечающих за уничтожение опухолей. Наши результаты предварительные, но мы думаем, что вакцины имеют терапевтический потенциал, основанный на ширине и разнообразии ответа Т-клеток». Однако ученые предупреждают, что еще слишком рано говорить, будут ли вакцины эффективны в долгосрочной перспективе. Исследование было проведено для оценки безопасности их использования и иммунного ответа. Ни один из пациентов не испытал какого-либо побочного эффекта. Более ранние попытки применения вакцин были направлены на нормальные белки, обычно повышенные в случае рака. Эти же белки также находятся в здоровых клетках, что затрудняет стимуляцию иммунного ответа. Новый подход, разработанный командой ученых из Вашингтонского университета, соединяет знания раковой геномики с иммунотерапией опухоли. «Подход, который мы описали, фундаментально отличается от обычного обнаружения мутаций, которое направлено на идентификацию мутировавших генов, управляющих развитием рака. Вместо этого, мы ищем уникальный набор мутировавших белков в опухоли пациента, которые могли бы быть распознаны иммунной системой, как чужеродные», — говорит соавтор Элейн Мардис, соруководитель Mc Donnell Genome Institute в Вашингтонском университете. Меланома известна тем, что имеет большое количество генетических мутаций, вызванных воздействием ультрафиолетового излучения. Образцы биопсии меланомы обычно несут 500 и более мутировавших генов. Используя алгоритмы прогнозирования, исследователи сузили поиск кандидатов для вакцины путем идентификации неоантигенов, которые не только были обнаружены в опухоли пациента, но также распознаны иммунной системой больного, как чужеродные. Биохимическая проверка экспрессии неоантигенов на поверхности раковых клеток была произведена в сотрудничестве с группой Вильяма Хильдебранда в Университете Oklahoma Health Sciences Center . Это обеспечило необходимую уверенность в том, что вакцина будет стимулировать самые эффективные Т-клетки для борьбы с меланомой. «Вы можете представить, что неоантиген – это флаг на каждой раковой клетке, — говорит автор Беатриз Каррено. – Каждая меланома у больного может иметь сотни разных флагов. Выбирая неоантигены для создания вакцины, мы смогли идентифицировать флаги на раковых клетках пациентов. Тогда мы создали индивидуальные вакцины к избранным флагам для каждой опухоли». Беатриз Каррено и ее коллеги выбрали набор из семи уникальных неоантигенов для каждой вакцины и использовали специализированные иммунные клетки (дендритические клетки), полученные от пациентов, для введения этих неоантигенов в иммунную систему. Дендритические клетки играют важную роль в иммунном ответе организма, стимулируя Т-клетки уничтожать опухоль. После инфузии вакцины, кровь больных была обследована каждую неделю на протяжении 4 месяцев. Анализируя образцы крови, исследователи смогли обнаружить, что у каждого пациента сформировался иммунный ответ на специфичные неоантигены из их вакцин. Вакцины также стимулировали выработку различных клонов Т-клеток, направленных против неоантигенов. Ученые предполагают, что этот подход может быть также использован для активации Т-клеток и нацеливание их на клетки при других злокачественных новообразованиях с высоким уровнем мутаций, таких, как рак легких, мочевого пузыря, прямой и ободочной кишки. «Наша команда разработала новую стратегию проведения индивидуальной иммунотерапии рака, — говорит Геральд Линнет. – Много исследователей имели гипотезы, что можно использовать неоантигены для широкой активации человеческой иммунной системы, но мы не были уверенны в этом до сегодняшнего дня. У нас по-прежнему много работы, но это важный первый шаг, который открывает двери к индивидуальному лечению рака, основанному на иммунотерапии». farmamir.ru Иммунитет против меланомы. Учёные нашли новый способ бороться с раком | Здоровая жизнь | ЗдоровьеОднако в последнее время, благодаря открытиям немецких, швейцарских и американских ученых, найдены новые подходы для борьбы с этим заболеванием. Загадки меланоцитовЭта опухоль развивается из клеток меланоцитов, которые у здорового человека придают коже смуглый оттенок или образуют загар. В начале своего развития меланома похожа на крупную родинку, и только опытный глаз отличит более темные сегменты внутри нее. А позже, когда уже образовались метастазы, злокачественная меланома не поддается обычным препаратам против рака. Из каждых четырех смертей от рака кожи три вызваны меланомой. Число людей, заболевших этим видом рака, растет год от года – за последние 15 лет их стало в два раза больше. Характер этой опухоли по-прежнему до конца неясен даже для специалистов. Ведь меланоциты, пигментные клетки кожи, которые участвуют в образовании загара и родинок, ведут себя спокойно у большинства людей. И лишь у небольшого процента других вырываются из-под контроля и разрастаются, давая начало опухоли. Почему это происходит? Вероятно, все зависит от генетики, которая определяет тип кожи и чувствительность к ультрафиолетовым лучам. Светлокожие люди, рыжие, с веснушками заболевают чаще, чем те, у кого смуглая кожа. Обладатели множества родимых пятен подвергаются большему риску. Часто заболевают дети, для которых любой перегрев на солнце оборачивается солнечным ожогом. Казалось бы, ясно, что развитие опухоли «подталкивают»ы ультрафиолетовые лучи. Но почему-то она образуется на участках тела, которые редко подвергаются солнечному облучению, например, на коже стоп или на половых органах. И наконец, почему с каждым годом больных с черным раком кожи становится все больше? Ведь солнце как светило испокон веков, так и светит. Конечно, бывают годы солнечной активности, но от этого напрямую заболеваемость меланомой не зависит. Сенсация в МаннгеймеЛаборатория профессора Дирка Шадендорфа входит в состав клиники Маннгеймского университета. На нескольких пациентах-добровольцах ее сотрудниками был испытан новый метод иммунотерапии, разработанный совместно со швейцарскими учеными. Врачи наблюдали шестнадцать пациентов, страдающих злокачественной меланомой. Распространение агрессивной опухоли у больных и образование метастазов не смогли остановить ни хирургическое лечение, ни химиотерапия, ни радиационное облучение. Надежд на выздоровление не было. И вдруг сработала новая методика: у четырех пациентов опухоли и метастазы уменьшились частично, у двух – исчезли полностью. Немецкий онкологический центр и клиника при Маннгеймском университете немедленно предоставили в распоряжение лаборатории самое современное оборудование, онкологическую амбулаторию и несколько коек в Маннгеймской клинике для лечения больных раком кожи. Исследования стали проводить на добровольцах не только с меланомой, но и с прогрессирующей лимфомой кожи, плоскоклеточным раком на запущенной стадии. Было испытано десять экспериментальных методов лечения. Принцип всех этих методик один – помочь иммунной системе пациента более активно бороться против раковых клеток. Для этого иммунные клетки пациента ориентируют на уничтожение клеток меланомы, предварительно обрабатывая антигенами опухолевых клеток, которые становятся маркерами опухолевого процесса в организме больного. Одновременно дают сигнал наиболее активным иммунным клеткам, Т-лимфоцитам, уничтожить злокачественные клетки. Происходит тренировка клеток-защитников. Чтобы навести Т-лимфоциты пациента «на след» раковых клеток в организме, исследователи размножают иммунные клетки крови пациента, добавляя различные вещества, стимулирующие их рост. Затем они бросают клеткам крови антигены раковых клеток «для поедания». После этого «натренированные» иммунные клетки вводятся в лимфатические узлы больного. Лимфатические сосуды разносят их по всему организму, привлекая другие клетки-защитники. Получается что-то вроде вакцинации. Такая прививка позволяет избавиться даже от метастазов меланомы. В лаборатории профессора Стивена Розенберга из Национального онкологического института США в Мериленде применили эту методику и добились хороших результатов у нескольких пациентов. В лаборатории Шадендорфа пытаются выяснить, как возникает рак кожи, чтобы найти другие методы борьбы с ним. Доктор биологии Моника Керн считает, что необходимо прежде всего найти ответ на вопрос: почему клетки меланомы не поддаются лечению лекарствами, обычно применяемыми при раке? Она обнаружила, что в клетках меланомы есть гены, которые позволяют им сопротивляться химическим лекарствам. Ученые надеются, что такое сопротивление можно подавить с помощью медикаментов или генной терапии. Группа сотрудников из 16 человек исследуют дальнейшие возможности активизации иммунной системы пациента. Чем легче распознаются раковые клетки в организме, тем быстрее можно их уничтожить. Поэтому ученые пытаются найти как можно больше маркеров‑антигенов, которыми помечены раковые клетки. Сегодня известно уже более 20 раковых антигенов меланомы, и чем больше их будет обнаружено, тем успешнее можно будет бороться с опухолевыми клетками. Надежда остаетсяВ Германии создана совместная американо-немецкая лаборатория, которая занимается разработкой нового метода лечения меланомы и клиническими испытаниями. Большинство пациентов с раком кожи, которые лечатся здесь, в возрасте от 40 до 50 лет. Самому пожилому – 75‑лет. Восемь лет назад он обнаружил на подошве стопы темное пятно величиной с ноготь, которое время от времени кровоточило. Были проведены две операции, затем наступил период «затишья», а после пошли метастазы в виде узелков на икре, дальше – в области паха. Пациент был направлен в Мангейм, где ему стали делать подкожные инъекции в бедро с интервалом в 14 дней. Кроме усталости и появляющейся время от времени головной боли, неприятных ощущений у него не возникает. Сегодня не редкость и те, кто заболел злокачественной меланомой уже в 20 лет. Врачи считают, что это связано с гормональными нарушениями, которые возникают при перемещении людей в другие климатические зоны, особенно из северных областей – в южные. Сегодня люди стали более мобильны, легко меняют место жительства, и в этом есть свои плюсы, но какая-то доля роста заболеваемости меланомой, по-видимому, связана с этими изменениями образа жизни. Всего в клинической совместной лаборатории лечатся около 500 больных. Сначала им рекомендуют классический метод лечения, и лишь когда он не помогает, принимают в клинику. Еще не ясно, будет ли «вакцинация» против рака кожи широко применяться в больницах. Сначала нужно получить ответы на многие вопросы. И первый из них: почему лечение действует на одних пациентов, а на других – нет? Вопрос этот еще ждет своего ответа. Смотрите также:www.aif.ru Вакцинация против меланомы — Медицинский вестник
Меланома называется еще «черным раком» и по праву относится к наиболее опасным разновидностям злокачественных опухолей, в большом количестве случаев заканчивающимся летальным исходом. Но совсем недавно сразу в нескольких научных лабораториях в разных концах мира были сделаны открытия, которые могут положить начало успешной борьбе человечества с меланомой.
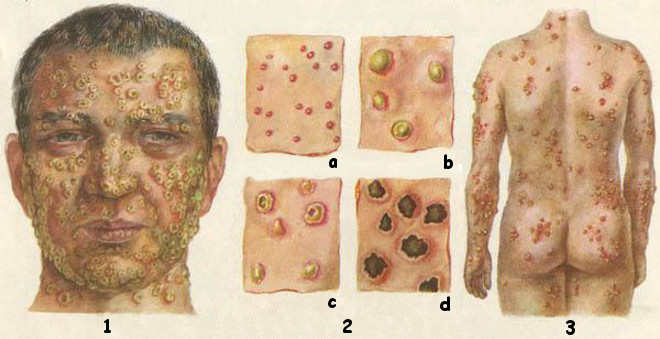
Уникальная опухоль Основу меланомы составляют клетки меланоциты, именно в них вырабатывается пигмент меланин, который придает коже привлекательный бронзовый цвет. На первых стадиях развития меланома напоминает достаточно большую родинку, и лишь профессионал сможет увидеть в ней более темные включения. На стадии формирования метастазов меланому нельзя контролировать с помощью стандартной химиотерапии.
Из 4 человек, умерших от рака, 3 болели меланомой. Количество пациентов, приходящих с этим заболеванием к врачам увеличивается ежегодно и за последние полтора десятка лет оно увеличилось вдвое.
Даже онкологи, специализирующиеся по меланоме, до конца не знают все об этом виде рака. У подавляющего количества людей меланоциты существуют всю жизнь и никак не дают о себе знать. А у некоторых они перерождаются и формируют злокачественное новообразование.
По мнению специалистов, существует наследственная предрасположенность к меланоме, определяющая особый тип кожи, а также особую реакцию на ультрафиолет. Наиболее подвержены этому заболеванию рыжие, люди со светлой кожей, а также те, у кого много веснушек.
Чем больше на теле родимых пятен, тем выше вероятность развития заболевания. Это заболевание поражает не только взрослых, но и малышей, началом заболевания в таком случае выступает ожог ультрафиолетом.
Вроде бы толчком к развитию заболевания является облучение солнечными лучами. Но загадка в том, что в большинстве своем меланома формируется на закрытых участках тела, которые почти никогда не облучаются солнцем, например, в паху или на ступнях. И еще один вопрос: почему количество больных растет ежегодно? Дневное светило озаряет нашу планету не одно тысячелетие. Причем замечено, что не существует корреляции между уровнем активности солнца и количеством вновь заболевших.
Открытие совершено В лаборатории при Маннгеймском университете было сделано открытие, которое поможет ответить на некоторые вопросы о загадочной опухоли. В эксперименте участвовали пациенты с меланомой, на которых испытывали новое иммунное лекарство.
16 больных проходили лечение. У всех них заболевание было уже на неизлечимой стадии, все методы были испробованы: и радиотерапия, и операция, и химиотерапия. Ни у одного из них не было шанса на излечение. После прохождения лечения в клинике при Маннгеймском университете у 4 участников частично пропали метастазы, опухоль уменьшилась, а у 2 и вовсе пропали.
Как только были получены такие ошеломляющие результаты, лаборатория получила режим наибольшего благоприятствования, финансирование и новое оборудование. Кроме этого, разрешено было лечить пациентов в онкологической клинике при их согласии.
В экспериментах стали участвовать пациенты не только меланомой, а также и с прогрессирующей формой лимфомы, а также тяжелыми степенями плоскоклеточного рака дермы. В лаборатории исследовали эффективность 10 методик терапии. Все они основаны на том, чтобы активизировать защитные силы самого организма против злокачественных клеток. Пациент получает препараты, которые «нацеливают» иммунные тельца на злокачественных пришельцев. В клетки опухоли вводят особые антигены, притягивающие иммунных агентов. А «тяжелая артиллерия» иммунитета – Т-лимфоциты получают команду полностью уничтожить врага. Таким образом, иммунная система учится распознавать чужеродные клетки и уничтожать их.
Для того чтобы указать Т-лимфоцитам мишень, у пациента изымается некоторое количество иммунных клеток из крови и в лаборатории в них добавляют стимуляторы роста иммунных телец. После чего в пробу крови запускают антигены злокачественных тканей, которые заглатываются лимфоцитами. Это своего рода тренировка иммунитета. После нее уже наученные лимфоциты вливаются в лимфоузлы пациента. С током лимфы они попадают в самые отдаленные участки тела и там передают свой «опыт» появившимся вновь клеткам. Методика несколько напоминает вакцинацию.
Подобная «вакцина» помогает устранить даже метастазы опухоли. Методика апробирована и в Национальном онкологическом институте США, где уже полностью излечены несколько больных.
В клинике Шадендорфа ученые работают над вопросом появления рака кожи. Исследователи полагают, что выяснив механизм озлокачествления клеток, можно будет ближе подобраться к лечению опухолей. Очень беспокоит их вопрос о том, почему же из всех видов рака именно меланома не реагирует на химиотерапию? Уже выявлены некоторые гены, присутствующие в клетках опухолей, помогающие им противостоять препаратам. Исследователи считают, что с этими летками можно будет пытаться разобраться, используя генную инженерию.
Штат лаборатории составляют 16 сотрудников, которые трудятся над усилением иммунного ответа организма человека на появление злокачественных клеток. Необходимо, чтобы иммунитет быстро и легко выявлял эти клетки. Тогда и подавлять их он будет достаточно оперативно. В связи с этим пока ученые бьются над выявлением маркеров для внедрения их в злокачественные клетки. На сегодняшний день определено больше двух десятков антигенов, которые можно использовать в качестве маркеров.
Наука идет вперед Ученые из США и Германии объединили свои усилия в борьбе против меланомы. Они создают принципиально новую методику лечения болезни. Уже проходят клинические испытания эти методики. В эксперименте участвуют пациенты в возрасте 40 – 50 лет, но встречаются и семидесятилетние. Один из пациентов старшего возраста 7 лет назад заметил на ступне темное плоское образование диаметром два сантиметра. Иногда оно выделяло кровь. Пациент перенес два хирургических вмешательства, после чего заболевание вроде бы затухло, но через некоторое время по ногам до паха пошли метастазы.
Тогда больного отправили в Мангейм. Здесь он получал подкожные уколы в область бедра с промежутками в две недели. Самые тяжелые побочные эффекты этой терапии – некоторая вялость и головная боль, которая проходит сама собой.
Современные онкологи не удивляются даже, обнаруживая меланому у двадцатилетних молодых людей. В таком возрасте причина заболевания скрывается в гормональных расстройствах, развивающихся на фоне резкой перемены климата при переездах. Наиболее опасен переезд из более холодных регионов в более теплые. Современный мир предполагает частые передвижения, это очень удобно. Но вероятно, резкая смена климата тоже играет свою роль в развитии злокачественной меланомы.
Сегодня в лаборатории Мангейма пятьсот пациентов. Но первым делом они проходят все стадии обычной терапии. И лишь в том случае, когда она не эффективна, используют инновации.
Пока непонятно – войдет ли «прививка» от рака в широко используемые методы лечения. Перед тем как рекомендовать ее для широкого использования, необходимо более детально изучить методику и ее дальние последствия. Самый же главный вопрос в том, что одни пациенты излечиваются полностью, другие же вовсе не отвечают на эту методику. Это очень важный вопрос, пока еще остающийся нерешенным.
clinic-virtus.com Вакцина от меланомы работает, но стоит очень дорого
Новый класс персонализированных противораковых вакцин, адаптированных к опухолям отдельных пациентов, задержал развитие болезни в двух независимых клинических испытаниях. Nature опубликовал одновременно два разных исследования от двух независимых команд, испытывавших персонализированные вакцины, лечащие или по крайней мере предохраняющие от рецидива меланомы на поздних, практически неизлечимых стадиях болезни. Одна вакцина была разработана в американском Институте Dana Farber (Dana-Farber Institute), а другая — частной немецкой биотехнологической фирмой BioNTech, которая использует так называемый РНК-мессенджер, чтобы воспроизвести код для создания своих «терапевтических» белков. Вакцина, разработанная в Dana Farber, работает с неоантигенами, специфичными для для опухоли конкретного человека. Антигены — это молекулы, которые отображаются на поверхностиклетоки стимулируют иммунную систему.Неоантигены являются молекулами на поверхностях клеток, которые продуцируются мутациями ДНК, которые присутствуют враковых клетках,но отсутствуют внормальных клетках. что делает неоантигены идеальными мишенями для иммунной терапии против рака, говорят ученыеВакцины, используемые в исследовании фазы I, содержали до 20 неоантигенов, полученных из опухоли конкретного пациента.Вакцины вводили пациентам для тренировки собственной иммунной системы для распознавания этих неоантигенов с целью стимулирования иммунной системы к уничтожению раковых клеток, на поверхности которых они находились. Подход BioNTech заключается в работе с эпитопами, частями макромолекулы антигена, которые непосредственно являются мишенью для иммунных клеток. В чем заключается уникальность новой вакцины? Предыдущие методы иммунотерапии, такие как препараты ингибитора контрольной точки, также вызывают иммунные реакции против неоантигенов рака, но не имеют такой высокой специфичности.Они могут вызывать реакции иммунной системы организма против нормальных тканевых антигенов, приводя к тому, что иммунная система атакует нормальные ткани.Исследователи обнаружили, что персональная вакцина вызвала целенаправленныйответТ-клеток на несколько неоантигенов опухолей, помимо того, что обычно наблюдается в ответ на существующие виды иммунотерапии. Ученые из Dana-Farber Institute and Broad Institute вводили вакцину шести пациентам с меланомой, опухоли которых были удалены хирургическим путем, и которые были подвержены высокому риску рецидива.Вакцинация была начата через 18 недель после операции.При медиане 25 месяцев после вакцинации у четырех из шести пациентов не было обнаружено доказательств рецидива рака.У двух других пациентов, с метастазами в легкие, болезнь возобновилась после вакцинации.В этот момент они начали лечение препаратом пембролизумаб, который ингибирует иммунную контрольную точку PD-1.Оба пациента получили полное разрушение опухолей в результате курса лечения и увеличение количества специфических Т-клеток, готовых бороться с опухолями в случае рецидива. Вторая, неоэпитопная вакцина, тоже привела к вполне вдохновляющим результатам: иммунный ответ возник у всех пациентов, т-клетки убивали опухолевые клетки, ориентируясь на специфические маркеры-эпитопы. У двоих пациентов был достигнут эффект стабильной выживаемости без роста опухоли. Еще у двух пациентов с метастатической болезнью иммунный ответ был серьезный иммунный ответ, у одного, правда, наблюдался потом рецидив. Третий продемонстрировал полный иммунный ответ в сочетании с иммунотерапевтической блокадой PD1. Результаты исследования показывают, что персонализированная неоантигенная вакцина может потенциально преодолеть два основных препятствия в терапии рака. Одним из них является гетерогенность опухолей: тот факт, что они состоят из клеток с множеством различных признаков, часто позволяет злокачественным опухолям уклоняться от препаратов, нацеленных на злокачественные клетки, имеющие одну и ту же определенную генетическую аномалию.Вакцина, поскольку она содержит много разных неоантигенов из опухоли, нацелена на разные генетические аномалииопухолевых клеток. Этот метод демонстрируют большую перспективу в лечении рака, который обычно развивает устойчивость к моно-препаратам. Второе препятствие при раке состоит в том, чтобы генерировать иммунный ответ, резко сфокусированный только на раковых клетках, избегая при этом атаки на нормальные клетки и ткани. Обе вакцины были запрограммированы атаковать только специфические антигены или их части — эпитопы, и поэтому имели очень скромные побочные эффекты. Несмотря на десятилетия попыток разработать эффективные вакцины против рака, они в основном не смогли создать мощные противоопухолевые иммунные ответы.Авторы нового исследования говорят, что это было связано с тем, что все эти вакцины, как правило, были созданы на основе опухолевых антигенов, которые были слишком похожи на антигены нормальных клеток. В результате организм вырабатывал более слабый иммунный ответ, чтобы избежать атаки на нормальные клетки (процесс, называемый иммунной толерантностью).Поскольку новые вакцины изготавливают по «индивидуальному проекту» для каждого пациента, используя антигены, созданные мутациями, уникальными для рака именно этого конкретного пациента, и присутствуют только на раковых клетках, процесса иммунной толерантности удается избежать. Что дальше? Roche, крупнейший в мире производитель лекарств от рака, уже сделал ставку на технологию BioNTech после подписания в сентябре прошлого года контракта стоимостью 310 миллионов долларов, что позволит ему протестировать немецкую вакцину с помощью препарата для иммунотерапии Tecentriq. Соучредитель и главный исполнительный директор BioNTech Угур Сахин(Ugur Sahin) сообщил, что комбинированные испытания с использованием препарата Roche против различных видов рака должны были начаться уже в конце этого года. Конкурирующая биотехнологическая фирма Neon Therapeutics, которая была создана для проведения исследований в США, начала тестирование своей персонализированной вакцины из неоантигена в сочетании с препаратом Opdivo от Bristol-Myer's в прошлом году. Сколько стоит супер-вакцина? Уже применяющиеся новые препараты, такие как Opdivo и Tecentriq, значительно усиливают иммунную систему организма и тем самым серьезно улучшают шансы на выживание больных с меланомой, но цена курса лечения составляет более 150 000 долларов в год. Сахин признал, что такая высокая стоимость вакцины сначала будет неизбежной, но, возможно, со временем ее цена может быть уменьшена за счет увеличения масштаба и автоматизации производства. «В среднесрочной и долгосрочной перспективе стоимость вакцины должна заметно снизиться. Это индивидуальный метод лечения, но это универсальный процесс», — сказал он.«На данный момент мы находимся на очень ранней стадии, но в долгосрочной перспективе этот новый метод вакцинации может коренным образом изменить подход к лечению онкологических заболеваний». Корнелиус Мелиеф (Cornelius Melief)из Медицинского центра Лейденского университета (Leiden University Medical Center), который не участвовал ни в одном из исследований, подтвердил, что исследование его немецких и американских коллег полностью доказало огромный потенциал неоантигенных вакцин. «Контролируемые рандомизированные клинические испытания фазы II с большим количеством участников теперь необходимы для определения эффективности этих вакцин у пациентов с любым типом рака, который имеет достаточные мутации для обеспечения достаточных целей неоантигена для такого подхода», — сказал он. griskomed.ru Вакцины от меланомы - vechnayamolodost.ruДве персонализированные вакцины против меланомы успешно испытаны на людях «Чердак» Две исследовательские группы из разных стран провели клинические исследования индивидуальных вакцин против меланомы, подтвердившие их эффективность и безопасность. Меланома – опухоль высокой степени злокачественности, при которой пигментные клетки кожи под воздействием различных факторов перерождаются в злокачественные. Один из таких факторов – генетические мутации, которые нарушают процессы деления клеток, вызывая их аномальный рост, или препятствуют их естественному самоуничтожению. Чаще всего для возникновения меланомы требуется 4−6 разных генетических мутаций, но существуют такие гены, в которых достаточно всего лишь одной. Меланома с трудом поддается традиционному лечению, но восприимчива к иммунотерапии – введению в организм пациента моноклональных антител к раковым клеткам. Следующий шаг в лечении меланомы – внедрение персональных вакцин, которые создадут у пациента иммунитет конкретно к его опухоли. Команда ученых из Института раковых исследований Dana-Farber, женской больницы Бригэма и Гарвардской медицинской школы (США) провела клиническое исследование персонализированной вакцины против опухолевого антигена. Вакцина разрабатывалась индивидуально для каждого участника исследования. Ученые секвенировали геном опухоли каждого пациента, выявляли свойственный только ей набор мутаций и создавали вакцину, направленную против клеток этой конкретной опухоли. Комплекс мутаций, свойственных только этой опухоли, называется мутаном. Мутаном заставляет клетки опухоли вырабатывать чужеродные для организма белки. Этих белков нет в здоровых тканях, поэтому их наличие в составе вакцины вызывает высокий иммунный ответ. В организме рецепиента вырабатываются Т-лимфоциты, которые атакуют опухолевые клетки, содержащие эти белки-антигены. Это помогает уничтожать клетки первичной опухоли и предотвратить метастазирование и рецидивы. В исследовании участвовали шесть пациентов. После вакцинации у четырех испытуемых в течение 25 месяцев не было рецидивов. У двоих пациентов с рецидивирующей опухолью, которые после вакцинации также получали лечение иммунологическим препаратом, наблюдалась полная регрессия опухоли и увеличение числа специфичных к антигенам опухоли Т-лимфоцитов. Австрийско-немецкая группа ученых применила индивидуальные нео-эпитопные вакцины к пациентам с меланомой III и IV стадии. Ученые определили индивидуальные для опухоли каждого пациента мутаномы и разработали вакцины, специфичные для эпитопов каждого из них. (Эпитоп – участок молекулы белка-антигена, который связывается с антителами.) В этом исследовании были выделены 125 типов мутаций, тогда как вакцина, которую тестировали американцы, работает против 20. Все пациенты прошли курс из 20 вакцинаций, который они перенесли без серьезных побочных эффектов. У всех участников исследования в ответ на применение вакцин выработались Т-лимфоциты, работающие против клеток опухоли. В целом у участников создался иммунитет к 60% из 125 выявленных мутаций, причем у каждого пациента появились Т-клетки против как минимум трех мутаций. Общее число случаев метастазирования у пациентов существенно снизилось, повысились сроки выживаемости без прогрессирования болезни. По мнению авторов работы, поливалентные нео-эпитопные вакцины могут предотвратить рецидив меланомы у пациентов из группы высокого риска как в монотерапии, так и в комбинации с препаратами моноклональных антител. Оба исследования показали высокую эффективность и безопасность индивидуальных вакцин против меланомы, созданных на базе анализа мутаций конкретных опухолей пациентов. Оба исследования опубликованы в журнале Nature: Ott et al., An immunogenic personal neoantigen vaccine for patients with melanoma; Sahin et al., Personalized RNA mutanome vaccines mobilize poly-specific therapeutic immunity against cancer. Портал «Вечная молодость» http://vechnayamolodost.ru 06.07.2017 www.vechnayamolodost.ru Вакцина от меланомы — WNSЕжегодно в странах Европы регистрируется 321 000 случаев заболевания раком молочной железы. Примерно 40% больных умирают. На ранних стадиях этот недуг не доставляет беспокойства, а при диагностике на позднем этапе почти не поддается лечению. Российские ученые проводят клинические испытания методики профилактики онкологических заболеваний.
В конце августа 2004 года канадские исследователи из медицинского центра университета McGill и университета McMaster обнаружили ген beta 1‑integrin, отвечающий за возникновение рака молочной железы. Этот ген, как было доказано на экспериментах с мышами, инициирует рост и развитие раковой опухоли. Данные, полученные исследователями, показывают, что блокирование этого гена позволяет остановить развитие опухоли у мышей. Следующий шаг – создание терапевтических средств для блокирования гена в организме человека.
«Мыши – это наше все»
Член-корреспондент Российской академии медицинских наук профессор Сергей Северин считает, что если клинические испытания подтвердят результаты экспериментов на животных, то открытие позволит создать принципиально новые методики лечения рака молочной железы. Сергей Северин является научным руководителем компании «Русские биотехнологии». Как и канадские коллеги, он занимается изучением и диагностикой раковых заболеваний. «В России 42% женщин приходят в клинику на поздних стадиях заболевания из-за низкой информированности о симптомах, страха узнать правду и попыток самолечения, – говорит Сергей Северин. – Для снижения риска необходимо развивать раннюю диагностику рака. Одним из безопасных методов профилактики может стать метод ксеновакцинации (вакцинации клетками животных. – Прим. «Ко») с применением полиакриламидного геля». Первую вакцинацию провел Эдвард Дженнер в 1796 году. В организм человека вводились возбудители коровьей оспы. Болезнь протекала в легкой форме, а у выздоровевшего вырабатывался иммунитет. Сегодня большинство вакцин, применяемых для профилактики бактериальных и вирусных заболеваний, готовятся на основе сыворотки крови различных животных. Однако до сих пор не удавалось создать вакцину против раковых заболеваний. Когда в организм человека попадают раковые клетки животного, например клетки меланомы мыши, иммунная система начинает активно вырабатывать антитела. Они уничтожают чужие клетки, а заодно и раковые клетки человека (в строении раковых клеток человека и животных есть аналогичные генетические нарушения). При этом возникает настолько мощный иммунный ответ, что все введенные клетки разрушаются за очень короткий срок. В результате иммунная система не успевает запомнить зараженные клетки и быстро прекращает вырабатывать необходимые антитела. Над созданием «долгоиграющей» вакцины против рака работают в медицинских центрах десятков стран. Например, в Австралии (наиболее интересные результаты достигнуты в Newcastle Mater Hospital, Queensland Institute of Medical Research) создано шесть вакцин, одна из которых заявлена к клиническим испытаниям.
Капсула под кожей
В России решение проблемы было найдено почти случайно, причем в другой сфере – пластической хирургии. Врач Алексей Котелевиц, практикующий хирург в Центре репродукции человека Минздрава РФ предложил провести на мышах испытания разных видов полиакриламидных гелей с целью подтверждения их безопасности.В это же время доктор химических наук заведующий лабораторией НИИ резиновых и латексных изделий Владислав Лопатин создал разновидность полиакриламидного геля, который при подкожном введении не растекается. В ходе экспериментов было обнаружено, что это вещество через два месяца после подкожного введения образует соединительно-тканевую капсулу, пронизанную кровеносными сосудами. Гель, используемый в эксперименте, уже запатентован в России под названием «Витагель».Сейчас идет процесс его регистрации за рубежом. На уникальные свойства «Витагеля» обратил внимание Сергей Северин, который и предложил использовать его для ксеновакцинации от некоторых видов онкологических заболеваний. Механизм получения вакцины следующий: чужеродные клетки с мышиной меланомой помещаются внутрь гелевой капсулы. Оболочка защищает биологический материал, не позволяя клеткам иммунной системы организма человека проникать внутрь. При этом клетки трансплантанта сохраняют активность, сигнализируя о своем присутствии в организме, в течение нескольких месяцев. Человеческий организм, распознав «чужаков», начинает активно вырабатывать антитела. Но иммунная система не может уничтожить клетки, которые находятся под защитой гелевой капсулы. Нескольких месяцев «борьбы» вполне хватает для того, чтобы Т-лимфоциты крови запомнили генетическое нарушение, вызывающее раковое заболевание. Такие антитела начинают вырабатываться постоянно, и человеческий организм становится невосприимчивым к данному виду онкологического заболевания.
Второй круг
Сегодня препарат, созданный компанией «Русские биотехнологии», проходит вторую стадию клинических испытаний. Доклинические тесты на животных и первая фаза под названием «Клиническое исследование переносимости метода ксеногенной вакцинации у больных метастатической меланомой» закончились успешно. Подтверждена безопасность препарата, выявлены возможные противопоказания и побочные эффекты. С начала этого года и до конца 2005-го будет проводиться вторая стадия клинических испытаний в трех российских научных центрах: Московском научно-исследовательском онкологическом институте, НИИ онкологии им. Петрова (Санкт-Петербург) и Российском научном центре рентгенорадиологии Министерства здравоохранения РФ. В испытаниях, во время которых проверяется эффективность методики, участвуют более ста добровольцев. Финансово-промышленная группа «Промышленные инвесторы» вложила $2 млн в разработку этой методики вакцинации. В ближайшие пять лет компания готова потратить на проект, который реализуют «Русские биотехнологии», еще $5 млн. Председатель совета директоров группы «Промышленные инвесторы» Сергей Генералов убежден, что компания получит прибыль от внедрения данного метода лечения рака. «Как только у нас будут убедительные результаты клинических испытаний, мы выйдем на биржу, пригласим других инвесторов», – сказал Генералов на презентации проекта. Оппоненты этого метода сомневаются в принципиальной возможности создания противораковой вакцины. Ведь она может спровоцировать сильную реакцию иммунной системы здорового человека. Результат такой прививки будет предсказуемым только в том случае, если для каждого пациента вакцину подбирать индивидуально.
webnewsite.ru |
г.Самара, ул. Димитрова 131 [email protected] |
 |

 Беатриз Каррено и Мишель Беккер-Хапак вводят индивидуальную вакцину от меланомы в инфузионный пакет, после чего она будет введена пациенту внутривенно.
Беатриз Каррено и Мишель Беккер-Хапак вводят индивидуальную вакцину от меланомы в инфузионный пакет, после чего она будет введена пациенту внутривенно. Вместо предисловия
Вместо предисловия