 |
|
||||||||||
|
новости интернета и современных технологий. Когда выйдет вакцина от вич для полного излечения на 2018 годНадежда уже есть, вакцины пока нетКак пишет «The Telegraph», мужчина из Британии, возможно, станет вторым человеком в мире, которого удалось излечить от ВИЧ-инфекции. Это один из 50 пациентов, которые участвовали в исследовании новой стратегии, направленной на излечение от ВИЧ, разработанной учеными из пяти Британских университетов. Изучаемая схема работает в два этапа. Сначала вакцина помогает организму распознать и уничтожить инфицированные ВИЧ клетки. На втором этапе препарат Вориностат активирует спящие клетки (вирусные резервуары), после чего они также могут быть обнаружены и уничтожены иммунной системой. После завершения запланированного курса, вирус в крови пациента не обнаруживался. Это с одной стороны может быть результатом применяемой стратегии, а с другой – результатом применения АРТ. Ученые планируют получить окончательные результаты исследования к 2018 году. ВИЧ трудно излечить так как его мишенью является именно иммунная система. ВИЧ встраивается в ДНК Т-лимфоцитов, после чего они не только перестают распознавать его, но и становятся фабрикой для его воспроизведения. Существующее лечение (антиретровирусная терапия) тормозит процесс размножения вируса, но не может обнаружить и воздействовать на спящие Т-клетки (резервуары). В Великобритании более 100000 человек живет с ВИЧ. Из них около 17% не знают, что они инфицированы. Пациент, о котором идет речь, сказал: «Было бы здорово если бы лекарство было найдено. В моем последнем анализе, который я сдавал пару недель назад, вирус обнаружен не был. Я принимал участие в исследовании, чтобы помочь другим и себе. Это было бы грандиозным достижением если бы после стольких лет что-то было бы найдено чтобы излечить людей от этой болезни. Тот факт, что я являюсь частью этого, просто невероятен». Профессор Сара Фидлер из Имперского колледжа Лондона, добавила: "Эта стратегия специально разработана, чтобы очистить организм от всех форм ВИЧ, в том числе и спящих. Это сработало в лаборатории и есть вероятность, что это будет работать и у людей. Но мы все еще достаточно далеки от какой-либо фактической терапии. Мы продолжим лабораторные тесты в течение следующих пяти лет. В настоящее время мы не рекомендуем прекращать АРТ. А в будущем – это зависит от результатов, которые мы получим. Мы планируем исследовать это». Только один человек в мире был излечен от ВИЧ. Это Тимоти Браун, известный как Берлинский пациент, который перенес операцию по пересадке стволовых клеток от человека с естественным иммунитетом к ВИЧ в 2008 году. Комментарии экспертовМедицинский директор компании Gilead Андрей Поляков: – Про исследование и первого "излеченного" от ВИЧ-инфекции пациента (кстати первым был и останется "берлинский" пациент, которому пересадили костный мозг от донора с Дельта 32 мутацией) сведений для анализа и комментариев крайне мало. Скорее всего речь идёт об использовании метода "kick and kill" или "shock and kill". Этот подход изучается уже несколько лет на животных и начались первые этапы изучения безопасности и эффективности у человека. Основной принцип этого подхода – активация клеток иммунной системы, находящихся в латентном состоянии и содержащих генетический материал ВИЧ в виде интегрированной в геном клетки провирусной ДНК. Достичь полной элиминации ВИЧ с помощью стандартной АРТ не удаётся именно из-за наличия "спящих" клеток, которые могут находиться в таком состоянии очень долго. В качестве активаторов этих клеток уже несколько лет изучают ингибиторы гистон деацитилазы (HDAC inhibitors). Препараты этого класса продемонстрировали эффективность на животных моделях. Изучение этих препаратов у ВИЧ-позитивных пациентов началось также несколько лет назад. Препараты этого класса ингибируют фермент гистон деацитилазу, функция которого тормозить процессы считывания информации с клеточной ДНК и синтеза белков в клетке. При блокировании данного фермента клетки активируются и запускается репликация вируса, что приводит к быстрой гибели клетки. В присутствии антиретровирусных препаратов вирус не может инфицировать новые клетки, а ингибиторы HDAC позволяют ускорить гибель всех клеток, служащих резервуаром ВИЧ и, таким образом, полностью избавить организм от вируса. В настоящее время, скорее всего, идёт подбор дозировок препаратов, которые позволят эффективно активировать латентные клетки и при этом быть минимально токсичными для других клеток. подбираются препараты, которые лучше проникают именно в латентные лимфоциты. Изучаются также препараты других классов и иммуно-терапевтические вакцины, помогающие клеткам естественным киллерам (NK) распознавать инфицированные клетки и уничтожать их. Возможно в статье речь идёт об одном из таких исследований, где одновременно используется иммуно-терапевтическая вакцина и селективный ингибитор HDAC вориностат. По ранее полученным результатам и обнадёживающим данным из представленного исследования можно судить, что вероятность получения терапии, позволяющей излечить ВИЧ-инфекцию уже довольно высока. Заместитель главного врача по медицинской части Московского областного центра по борьбе со СПИДом, д.м.н. Григорий Каминский: – Главная мечта любого ВИЧ-позитивного пациента – получить полное излечение. Английские ученые применили принципиально новый подход, основанный на иммунологическом распозновании и "выталкивающей" терапии. Очевидно, что необходимо сравнение конкурентных стратегий, оттачивание терапии. Но прорыв сделан. Профессор Имперского колледжа Лондона Сара Фидлер считает, что на это потребуется 5 лет. Понравилась статья или у вас другое мнение? Напишите на нашем форуме. spid.center ВИЧ-инфекцию и рак можно будет вылечить!Диабетикам не придется пить сахароснижающие препараты или колоть инсулин, а больным лейкозом – проходить химиотерапию. Открытие 2017 года дарят надежду «безнадежным» больным.У ВИЧ-инфицированных появилась надежда на выздоровление. Специалисты из Национального института здоровья США и одной из самых известных фармацевтических компаний мира усовершенствовали природные антитела, которые выделяет организм в ответ на атаку вируса, объединив их в одно соединение, которое уничтожает… 99% штаммов вируса иммунодефицита! Опробовали ее на обезьянах — 24 приматам ввели соединение, после чего вирус, ни один из подопытных не заразился. Испытывать его на людях начнут в 2018 году. Исследователи попытаются выяснить, можно ли таким образом предотвратить инфекции или даже вылечить ее. 2017 год ознаменовался многими другими удивительными открытиями.Например, ученые впервые эффективно применили систему редактирования генома CRISPR/Cas9 (способ удаления нуклеотидных последовательностей в цепочке ДНК). Биолог Дэвид Лю из Института Броуда, который объединяет Гарвардский и Массачусетский технологический институт, убежден: применять старую версию — то же самое, что удалять бородавки с помощью мачете. Обычный CRISPR вырезает большие куски ДНК. Усовершенствованный, который разработал Лю и его команда, «работает» деликатно, с отдельными буквами генетического кода. Риск появления побочных эффектов и при редактировании опасных мутаций — сведен к минимуму. Больных раком вскоре смогут лечить с помощью генной терапии. В июне на заседании коллегии FDA (Управление продовольствия и медикаментов США) выступал один из ученых, занимающийся разработкой новых методик лечения онкозаболеваний. Вдруг его речь прервала 12-летняя девочка. Держа отца за руку, она подошла к трибуне. В зале воцарилась тишина. Подросток не произнесла ни слова — лишь умоляюще смотрела в глаза ученого. Это сыграло свою роль — FDA согласовало первую в историю генетическую терапию рака (CAR-T-терапию). Из крови пациента получают лимфоциты, генетически модифицируют их и возвращают в кровь, а те берутся делать то, чему их научили, — уничтожать злокачественные клетки. Неизлечимо больная Эмили Уайтхед стала первым ребенком в мире, которая испытала на себе революционный метод лечения рака. После того, как ей ввели «натренированные» клетки иммунной системы, которые отвечают за приобретенный иммунитет, у девочки начался «цитокиновый шторм». Если бы CAR-T-терапия не действовала быстро, ответ организма убил бы пациентку. Сейчас ребенок здоров, а FDA утвердила два вида генетической терапии онкопатологий.
В 2017 году ученые достигли значительных результатов в изучении стволовых клеток, которые можно превратить в клетки любых тканей организма, эпителий или нейроны. В частности, ученые выяснили, что в пульпе сохраняются стволовые клетки. А это означает, что в скором будущем не придется ставить коронки и тратиться на импланты. Молочные и постоянные зубы (те, что по каким-то причинам придется вырвать) можно будет сдавать специалистам на хранение, а при необходимости из этого биоматериала можно будет вырастить новые зубы, которые, в отличие от имплантов, точно не выпадут. Стволовыми клетками, установили исследователи, можно лечить лейкоз (рак крови). Эта болезнь поражает костный мозг — основной орган, который отвечает за кроветворение. Традиционное лечение предусматривает химио- и лучевую терапию, но в 2017 году врачи из Лондонской клиники заявили, что им удалось вылечить от лейкоза двух детей. Ученые отобрали у пациентов стволовые клетки и генетически модифицировали их, превратив в такие, что способны атаковать злокачественные клетки. Исследователи из Школы медицины Вашингтонского университета и Гарвардского университета выделили стволовые клетки из кожи больных сахарным диабетом 1-го типа и превратили их в клетки, которые продуцируют… инсулин! При этой болезни поджелудочная вообще не вырабатывает этого гормона, поэтому пациенты вынуждены регулярно вводить его с помощью шприца и иглы (в желудке инсулин разрушается, поэтому в форме таблеток его не выпускают). Инновационную терапию внедрять в клиническую практику пока не планируют, однако ученые предполагают, что много пациентов с этим диагнозом имеют все шансы дожить до того дня, когда смогут контролировать уровень глюкозы без сахароснижающих препаратов и ежедневных утомительных инъекций. В 2018 году стартует новый проект — ученые попробуют оживить мозг у 20 умерших, причиной смерти которых стала травма этого органа. Деятельность нервной системы попытаются восстановить с помощью стволовых клеток. Конечно, покойники не воскреснут. Задача, которую ставят перед собой ученые, – разработать новые методы лечения пациентов, находящихся в вегетативном состоянии (в которых бьется сердце, дышат, переваривают пищу и испражняются, но не реагируют на внешние раздражители), и больных, страдающих от дегенеративных заболеваний и неуклонно теряют нейроны. Также исследователи попытаются вырастить мини-мозг и проследить, как на него влияют разные болезни, например, инфицирования вирусом Зика. 1838.xn--p1ai Можно ли сделать вакцину против ВИЧ?
С помощью ступенчатой вакцинации иммунную систему хотят научить вырабатывать редкий тип антител, эффективно нейтрализующих ВИЧ. По данным Всемирной организации здравоохранения, в 2016 году с ВИЧ во всем мире жили 36,7 миллионов человек, 1,8 миллиона заразилось, а 1 миллион умер от развившегося СПИДа. Лекарства, которое полностью уничтожало бы ВИЧ, пока не существует. Антиретровирусные препараты, которые инфицированные люди вынуждены принимать пожизненно, сдерживают размножение вируса, но целиком его истребить не могут. Дело в том, что когда ВИЧ проникает в клетку, он встраивается в ДНК, где становится недосягаемым для лекарств и невидимым для иммунной системы. Там он может тихо «отсиживаться» и не приступать к размножению, пока не настанет безопасный момент. Известен лишь один случай полного излечения от ВИЧ. Тимоти Браун, прославившийся как «берлинский пациент», в 2007 году перенес трансплантацию костного мозга (напомним, что именно костный мозг – резервуар иммунных клеток) от донора, который обладал естественной устойчивостью к ВИЧ. (Донор был из 1% тех счастливчиков, у которых на клетках нет рецептора, с помощью которого ВИЧ в них попадает.) С первого дня после трансплантации пациент прекратил принимать антиретровирусные препараты и больше к ним не возвращался, и в дальнейшем вирус у него так и не смогли найти ни в какой форме. К сожалению, случай с Тимоти Брауном остается исключением. У других пациентов полного избавления от вируса не случалось, к тому же замещение зараженной иммунной системы с помощью трансплантации от донора – очень сложная и рискованная процедура. С ВИЧ также можно бороться методами генной терапии. У инфицированного человека забирают Т-клетки из крови и редактируют их геном: с помощью технологии CRISPR/Cas9 (о которой мы неоднократно писали) удаляют ген того самого рецептора, которого нет у людей с естественной устойчивостью к ВИЧ. Как несложно догадаться, на деле в этом направлении все обстоит гораздо сложнее, чем на словах, и пока что о молекулярно-генетическом лекарстве от ВИЧ говорить рано. Но, как известно, предотвратить болезнь лучше, чем ее лечить – иными словами, против ВИЧ хорошо бы иметь вакцину. Однако, как и в случае с лекарством, 30 лет поисков вакцины против него не увенчались успехом. При вакцинировании иммунитет должен запомнить характерные молекулярные признаки вируса. Но вирусы легко мутируют, а ВИЧ мутирует особенно быстро – из-за того, что фермент, который он использует для копирования своей генетической информации, допускает много ошибок.
В течение года с момента инфицирования популяция ВИЧ может достичь такого же генетического разнообразия, какого достигает за то же время вирус гриппа в масштабе всего мира. Поэтому новая вакцина от гриппа у нас – каждый год, а вакцины от ВИЧ нету вовсе. По этой же причине организм не в состоянии победить ВИЧ самостоятельно. Иммунная система не поспевает за изменчивостью вируса: пока она изобретает антитела против одних генетических вариантов, уже вовсю плодятся другие, против которых антитела не работают. Но сравнительно недавно надежда на создание вакцины появилась вновь, когда исследователи открыли особый тип антител – нейтрализующие антитела широкого спектра действия. Они сильно мутированы (изменены) по сравнению с обычными антителами и направлены против консервативных участков вируса (то есть таких, которые слабее всего изменяются от поколения к поколению). В исследованиях последних лет было установлено, что они способны нейтрализовать до 98% всех генетических вариантов ВИЧ. Иммунная система в какой-то момент сама начинает стабильно вырабатывать такие антитела, но этот момент наступает через несколько лет после заражения – слишком поздно. Сотрудники Института аллергии и иммунологии в Ла-Холья и Института Скриппса разработали стратегию вакцинации, которая учит иммунную систему вырабатывать антитела широкого спектра быстро. Чтобы понять, что именно тут имеется в виду, нужно представлять, как вообще иммунные клетки начинают синтезировать антитела против патогена. Антитела производят В-лимфоциты. При этом сами они могут взаимодействовать с чужеродными молекулами, в том числе и с вирусными белками. У нас постоянно появляются В-клетки с самыми разными рецепторами для распознавания чужаков, так что для любого вируса обязательно найдутся В-клетки, которые схватят его молекулы. Вирусный материал В-клетки поглощают, преобразуют внутри себя и выставляют наружу на своей поверхности. Для того, чтобы дело пошло дальше, В-клетка должна пообщаться с Т-клеткой. Т-клетка подходит к В-клетке, распознает ее собственные молекулы и молекулы вирусного материала, который на ней выставлен, и теперь В-клетка получает «добро» на дальнейшую борьбу. (Если взаимодействие между Т- и В-клетками пошло как-то не так, значит, В-клетка до этого что-то сделала неправильно и Т-клетка ее не активирует.) Теперь В-клетки, получившие разрешение на борьбу с вирусом, пытаются сделать так, чтобы связывать его как можно точнее и прочнее. Они начинают делиться и при каждом делении мутируют, так что у каждой новой В-клетки рецептор слегка меняется, и клетки с новыми рецепторами опять проходят отбор при взаимодействии с Т-клетками. Если слегка изменившийся рецептор распознает вирус еще лучше, то В-клетка, у которой он получился, продолжает делиться дальше. И лишь после многих раундов такого естественного отбора В-клетки с наилучшими рецепторами начинают продуцировать антитела (которые по строению идентичны рецепторам). Роберт Эбботт (Robert K. Abbott) и его коллеги предлагают повлиять как раз на процесс отбора. Они исходят из того, что практически у всех людей в иммунной системе присутствует некое количество В-клеток широкого спектра (ранее исследователи установили, что доля таких клеток равна приблизительно одной клетке на миллион). Тогда цель вакцинации – сделать так, чтобы В-клетки широкого спектра отбирались вместо обычных, которые хоть и отшлифованы идеально под определенные вирусные генетические варианты, но очень быстро устаревают. Сама вакцинация представляет собой многоступенчатую процедуру, в ходе которой в организм вводят вирусоподобные компоненты постепенно изменяющегося состава. Каждая ступень должна приближать иммунную систему к производству заветного типа антител. По выражению одного из исследователей, все происходящее выглядит так, как если бы В-клетки, умеющие распознавать квадраты, учили распознавать круги, но учили их этому с помощью пятиугольников. На человеке разработанную стратегию не испытывали, пока что эксперименты ограничиваются мышами, и предварительные результаты можно узнать из статьи в Immunity. Говорить о полноценной вакцине против ВИЧ пока еще очень рано, но, по крайней мере, есть надежда, что ее действительно удастся создать. По материалам reired 24hitech.ru Победить ВИЧ: сложно, но можноИсцеление – не то слово, которое часто используется в связи с термином "ВИЧ-инфекция". 35 лет прошло с момента обнаружения вируса и большую часть времени врачи рассматривали полное выздоровление скорее как фантазию, а не возможную перспективу. Всю потому, что ВИЧ не похож ни на один другой вирус. Он уничтожает те самые иммунные клетки, которые предназначены для того, чтобы с ним бороться. Он разрушает иммунную защиту месяцами, а иногда – годами. На сегодняшний день с заболеванием живут 37 млн человек по всему миру. Однако сегодня ученые больше понимают о том, как вирус "скрывается" в клетках организма и почему наша бдительная иммунная система "не замечает" его. Национальные институты здравоохранения (NIH) США финансируют усилия по лечению ВИЧ, а фонды – например AmfAR – ищут ресурсы, которые позволят полностью искоренить эпидемию. "Абсолютно точно, что ВИЧ можно излечить, – говорит Ровена Джонстон, вице-президент и директор по исследованиям AmfAR. – Вопрос на миллиард долларов: "Как это сделать?". Профессор медицины из Медшколы при Университете Джона Хопкинса Роберт Силичано одним из первых идентифицировал резервуары ВИЧ. "Проблема в том, что такая форма ВИЧ не видна иммунной системе и на нее не влияют лекарственные препараты", – говорит Силичано. По словам доктора, вирус покидает свою укреплённую башню и идёт на штурм лишь тогда, когда человек перестаёт принимать лекарства. В одном из докладов, которые представили на конференции по ретровирусам и оппортунистическим инфекциям 2018 года в Бостоне, исследователи обнаружили убедительные доказательства того, что резервуары могут быть активированы и устранены, по крайней мере – у животных. Дэн Барух и его коллеги из Медицинского центра Beth Israel Deaconess и Гарвардской медицинской школы показали, что препарат, который стимулирует иммунную систему и активирует резервуары, в сочетании с мощным антителом может нейтрализовать ВИЧ у инфицированных обезьян на полгода. "Я думаю, что наши данные повышают вероятность получить препарат для полного вызоровления. Это возможно", – заявил Барух. Такой метод в научной среде называют shock and kill: он основан на "выталкивании" спящего вируса из резеруаров и последующем уничтожении. Это шаг к избавлению людей от пожизненной зависимости от АРВ-препаратов. Этот метод еще не был протестирован на людях и вопрос полного выздоровления еще в процессе изучения. Исследователи напоминают, что на сегодняшний день единственным полностью излечившимся от ВИЧ человеком является "берлинский" пациент, которому пересадили костный мозг от донора с особой мутацией, которая не позволяет вирусу иммунодефицита "прикрепляться" к клеткам. Браун прекратил прием АРВ-препаратов после пересадки. Прошло уже больше 10 лет и его тест на ВИЧ остаётся отрицательным. [Подробнее об излечении Тимоти Рэя Брауна – в материале СПИД.ЦЕНТРа] Случай Брауна доказывает, что полное выздоровление возможно, но врачи дожны добраться до "каждого закутка" организма, где может прятаться вирус, говорит доктор Стивен Дикс, профессор медицины Калифорнийского университета в Сан-Франциско. Сейчас некоторые исследователи даже полагают, что возможно полностью реконструировать иммунную систему человека, чтобы она была способна успешно устранить любой вирус. Этим уже пользуются онкологи в борьбе с опухолями: иммунную систему программируют таким образом, что та сама атаковала злокачественные клетки. "Я настроен оптимистично, поскольку параллели в терапии ВИЧ-инфекции и онкологии настолько тесны, что мы сможем применять товые технологии и в терапии ВИЧ", – говорит Дикс. Никто из специалистов не ожидает, что ВИЧ будет побежден в следующем году или ближайшие пару лет. Но они более чем уверены, что в будущем мы победим эпидемию. Материал основан на данных из статьи Time (There Is No Cure for HIV—But Scientists May Be Getting Closer). Перевод: Дарья Шапошникова. Подписывайтесь на страницу СПИД.ЦЕНТРа в фейсбуке spid.center Андрей Козлов: По оценкам экспертов, достаточно эффективная вакцина против ВИЧ будет создана через 10-13 лет. И у нас, и в мире | Программы | ОТРОльга Орлова: ВИЧ – вирус иммунодефицита человека. Был открыт в 1983 году независимо сразу в двух лабораториях: в Институте Пастера во Франции и в Национальном институте рака США. С тех пор носителями инфекции на нашей планете стали миллионы людей. А история борьбы с этим вирусом полна трагедий и открытий, побед и поражений. Масштаб распространения инфекции требует уже давно создания вакцины. Но как скоро ее можно получить? Об этом по гамбургскому счету мы решили спросить доктора биологических наук, директора биомедицинского центра в Санкт-Петербурге Андрея Козлова. Здравствуйте, Андрей Петрович. Спасибо, что пришли к нам в студию. Андрей Козлов: Здравствуйте. Очень приятно. Андрей Козлов. Родился в Ленинграде в 1959 году. В 1972 году окончил биологический факультет Санкт-Петербургского государственного университета. В 1975 году получил степень кандидата биологических наук. В 1978 году одним из первых в СССР получил грант от Международного агентства по изучению рака на стажировку в Национальном институте рака США в лаборатории первооткрывателя вируса СПИДа доктора Роберта Галло. Прошел путь от студента-стажера в лаборатории до начальника отдела в Федеральном научно-исследовательском центре. В настоящее время совмещает должность директора биомедицинского центра и руководителя лаборатории молекулярной вирусологии государственного научно-исследовательского института особо чистых биопрепаратов. Также возглавляет лабораторию молекулярной вирусологии и онкологии Санкт-Петербургского политехнического университета Петра Великого. Автор более 150 научных работ и 4 монографий. О.О.: Андрей Петрович, в 1987 году в Ленинграде в вашей лаборатории вы впервые зарегистрировали случай ВИЧ-инфицированного в Советском Союзе. Скажите, насколько вы осознавали вообще масштаб проблемы, трагедии? А.К.: В полной мере мы осознавали. И я должен сказать, что здесь, конечно, наука играет роль такого предсказателя, понимаете? Машина времени. Я был постдоком в лаборатории Галло, который один из открывателей вируса. И я был в полном курсе событий, которые разворачивались на наших глазах в Америке, в Индии, потом в Китае. И мы предсказывали, что все так и будет. И надо сказать, что в начале 1990-х нам не верили. Ну, нету эпидемии в России. А в Советском Союзе не могло быть эпидемии, поскольку не было секса, ничего не было, групп риска не было. И поэтому доказательство того, что это пришло, было очень важно. Мы открыли первый случай в рамках так называемого здравоохраненческого скрининга. То есть уже какие-то случаи ВИЧ-инфекции в Москве были, описанные в других местах. Мы первые издали приказ о начале скрининга и первыми начали скрининг здравоохраненческий. И в рамках официального скрининга мы выявили первые случаи ВИЧ-инфекции и первую смерть от СПИДа в СССР. Первые больные вообще девушки были, понимаете? Даже не мужчины, а девушки. И одна из них очень быстро умерла. А другая такая больная очень долго жила. Но, конечно, первая смерть – это был шок. И здравоохранение тогда было не готово к таким случаям совершенно. Все это было важно для развития всей службы СПИДа в целом в стране. О.О.: Но вы же в то время, поскольку вы работали со своими западными коллегами, вы видели, что там начинался этот процесс, когда считалось, что есть такие довольно узкие группы локальные, которые являются распространителями. И то, что эта болезнь сначала называлась болезнь 4G, что это были гаитяне, больные гемофилией, геи и употребляющие героин. Второе название – это gay cancer. К тому времени, когда это было определено в СССР, когда нашли, во-первых, это были в основном работники секс-услуги. Это не была уже палитра 4G. А.К.: У нас тогда не было такого понятия. И, наверное, профессия не очень была распространена. Просто девушки, которые имели много связей. И с иностранными гражданами. О.О.: Но вы уже понимали, что эта болезнь выйдет за узкие группы, которые… А.К.: Мы предсказывали все это. И я на границе 1994 и 1995 годов написал статью, которая говорила о том, что это реальная угроза. Тогда никто в это не верил. Но в это время уже принимали первый закон о СПИДе, и это было важно сказать тогда. У нас в России первый период, ранняя фаза эпидемии, было поровну распределено между гетеросексуальной и гомосексуальной передачей. И не было вообще наркозависимых инфицированных. И мы гадали, почему. О.О.: То есть наркозависимые не входили в группу, которая распространяет ВИЧ-инфекцию? А.К.: Не было совсем. И были вопросы вообще – а работает ли правильно наша скрининговая система? О.О.: Если не определяете… А.К.: Да. И приходилось доказывать, что да, работает. И мы, в частности, внедрили внешний контроль этой службы. И доказали, что служба выявляет все очень хорошо. И действительно, когда ВИЧ пришел в группу наркозависимых, это сразу же было выявлено. И удивительным образом оказалось, что отсутствие передачи у наркозависимых в первый период – это было связано с употреблением грязных домашних приготовлений наркотиков, которые содержали ингибиторы вируса. Это мы доказали в своих работах потом. О.О.: А как получилось, что теперь наркозависимые уже в современной России спустя 20 лет стали одними из основных распространителей. А.К.: Смотрите, это произошло на Украине. О.О.: Это специфика вообще России? А.К.: Нет, на Украине, в Белоруссии и в России это произошло в 1995-1997 годах. В Москве это случилось в 1998. Это было связано с тем, что из Афганистана начался трафик чистого героина. А чистый героин был лишен этих грязных свойств, не ингибировал вирус. И сразу же все наркозависимые перезаражались. И эпидемия вступила в фазу, которая называется фаза концентрированной инфекции. Если раньше было немного случаев… Представляете, за 5 или 10 лет в стране было всего 1000 случаев. А в Питере было 150 случаев. Но это вообще ничего, понимаете? Надо сказать, что вся противоэпидемическая система работала против этого. А тут получился взрыв среди наркозависимых в заражаемости. И оказалось, что мы ничего не можем противопоставить. Просто у нас не было ни опыта работы с этими группами, ни понимания, ни политической воли. И получилось, что вторую фазу борьбы она проиграла просто вчистую. И СПИД уже пришел по-настоящему. Сейчас началась третья фаза. Это фаза генерализации. Это когда уже из этой группы гетеросексуальным путем инфекция переходит в общее население. И сейчас хотя бы нам надо эту фазу попытаться выиграть. О.О.: На какой стадии больной носитель ВИЧ-инфекции является наиболее заразным? А.К.: Есть такая фаза. Она называется острая фаза ВИЧ-инфекции, когда еще ни антигены, ни антитела не выявляются. Только нуклеиновые кислоты. И это наступает через неделю-две после заражения. О.О.: Как правило, в это время человек, конечно, не знает. А.К.: Человек не знает несколько лет об этом. И огромным шагом вперед, который мы в России и в мире осуществили, стало внедрение диагностики. Поскольку известно, что ВИЧ-инфекция долго не проявляется, в латентной форме, и только лабораторным диагнозом можно ее установить. Но устанавливается лабораторным диагнозом эта ВИЧ-инфекция, как правило, на поздних стадиях уже. О.О.: А вот на ранней стадии… А.К.: А ранее она пропускается начисто. О.О.: То есть даже если человек пойдет сдавать анализы… А.К.: Да. Понимаете, получается, что весь пафос профилактики должен быть направлен на раннюю стадию. А мы ее выявить даже не можем. Ее выявляют методом так называемой ПЦР-диагностики. Этот метод у нас уже очень хорошо распространен. О.О.: Да, в связи с онкологией. Надо группу риска тестировать вообще чуть ли не каждую неделю ПЦР-диагностикой. Это дорого и утомительно. Но это надо делатьА.К.: Да. И в России этот метод… В общем, мы Европу опережаем. Но понимаете, что получается? Получается, что надо группу риска тестировать вообще чуть ли не каждую неделю ПЦРом. Это дорого и утомительно. И это надо делать. И надо на профилактику таким образом направлять. Понимаете? Это очень сложная задача. О.О.: Андрей Петрович, конечно, сразу встает вопрос о том, как бы нам, человечеству, получить вакцину от ВИЧ-инфекции. Вы разрабатываете ее много лет. Я только хочу спросить. Когда вы обнаружили первый случай ВИЧ-инфицированного в Советском Союзе, вы вообще понимали, что лично для вас это станет делом ближайших десятилетий, может быть, делом всей вашей жизни? А.К.: Я должен сказать, что у моего поколения научных сотрудников как-то очень было развито вот это чувство ответственности в том плане, что надо защищать свой участок как-то, свой участок компетенции, свой участок ответственности. И так получилось, что поскольку я тогда, допустим, в Питере единственный знал, как надо ставить эти подтверждающие анализы, я организовал в Питере эту лабораторию. Она была одна из первых или первой в Советском Союзе по СПИДу. Это research. А потом мы организовали такую же первую клиническую лабораторию. Смотрите, мы нашли первый случай, мы выделили первый вирус, мы его первыми проклонировали, получили генетический материал для вакцины. И мы просто обязаны были начать делать вакцину. О.О.: Продолжать. А.К.: Понимаете? Хотя я не могу сказать. Я не был вакцинологом, грубо говоря. Но мы провели, я помню, конференцию в 1994 году, где мы поняли, что надо делать вакцину. И с тех пор мы пролоббировали первую программу в 1997 году через наш парламент. Тогда у нас был очень боевитый парламент. Это шло очень в ногу с событиями во всем мире. Американцы начали свою первую программу тоже в 1997 году. И Клинтон тогда заявил, что через 10 лет будет создана вакцина. И это очень мобилизовало вообще научных сотрудников. Хотя через 10 лет вакцина не была такая создана, но был сделан громадный шаг вперед. Надо сказать, что тогда уже Россия заключила со Штатами со всемирным сообществом соглашение о том, что вакцина будет делаться, и Россия будет в этом принимать участие. О.О.: А в тот момент, когда вы поняли, что вы будете делать вакцину от ВИЧ-инфекции, скажите, ведь есть профилактические и терапевтические вакцины, то есть направленные с одной стороны – чтобы не заболеть, а с другой стороны – лечащие. Уже когда заболел человек. Вы в тот момент понимали, что что должно быть первым? А.К.: Тогда в середине 1990-х годов уже появились научные данные об естественной резистентности к ВИЧ. И когда такие данные появляются, это свидетельствует, что вакцина возможна. И, конечно, на первое место выдвигалась, и сейчас она стоит, задача создания профилактической вакцины. О.О.: Чтобы люди не заболевали. А.К.: Да. Когда была разработана высокоэффективная антиретровирусная терапия, выяснилось, что она не излечивает. То есть она берет болезнь под контроль, но терапия фактически пожизненная. И встала задача либо функционального излечения, то есть чтобы человек фактически, хотя у него вирус есть интегрированный, но нету вирусной нагрузки. Это функциональное излечение. Либо даже искоренение вирусных резервуаров. И всем стало ясно, что для этого нужны иммунотерапевтические препараты, или их называют терапевтические вакцины. И сейчас это одно из двух направлений, связанных с вакцинами против ВИЧ. Причем, оказывается, что субстанция, формула может в значительной мере перекрываться в обоих случаях, а различаться будут схемы введения и так далее. Причем, ясно, что терапевтическая вакцина уже должна использоваться на ВИЧ-инфицированных, а профилактическая – на здоровых людях. Соответственно, там другие иммунологические механизмы. С учетом того, что у ВИЧ-инфицированных уже подорван иммунитет в какой-то мере. И схемы испытаний различаются. Я должен сказать, что профилактическая вакцина, конечно, стоит значительно дороже. Просто значительно дороже. С чем это связано? С тем, что группы испытуемых в случае профилактической вакцины должны включать тысячи, иногда десятки тысяч людей. Вот сейчас начинается… О.О.: А это, конечно, очень дорогие исследования. А.К.: Это 100-150 млн долларов клиническое испытание. Поэтому в мире их проведено всего 5 штук. Сейчас начинается очередное в Южной Африке, которое повторяет схему RV 144 - исследование, которое было проведено армией США в Таиланде. Понимаете, что получается? Научное сообщество изучает в противоречиях, медленно движется. А армия взяла и довольно простую вакцину испытала. И получила результат. О.О.: Помимо вашего биомедицинского центра, есть еще разработчики вакцины. Насколько вы в этом смысле синхронны или в контакте? А.К.: Да в полном контакте. Дело в том, что когда мы в 1997 году… О.О.: Вы как-то вместе выплываете на одной лодке? А.К.: Пролоббировали эту программу, я был ее координатором. И мы тогда организовали исследования в Питере, Москве и Новосибирске. И в Питере и Новосибирске эти исследования продолжаются. Руководит ими Александр Ильичев. У них фантастическая вакцина по своей сложности и перспективности. Они прошли первую фазу. Мы им сейчас помогаем организовать вторую фазу клинических испытаний. О.О.: То есть вы прошли вторую фазу, а они подошли ко второй фазе. А.К.: И, более того, мы даже договорились, что мы будем использовать наши две кандидатные вакцины в формате prime boost. Prime – это первая иммунизация нашей вакцины, а последующая иммунизация их вакцины. Оказывается, это работает. О.О.: То есть вы имеете в виду, что на одном организме… То есть сначала, например, вашу, а потом их. А через какой срок нужно произвести? Как это происходит? А.К.: Вы знаете, схемы различны. И как раз самое интересное – это попасть в нужные интервалы, в нужный способ доставки. И таким образом получается, что формула вакцины – это не только формула молекулярная, а это еще и формула такая медицинская, понимаете? И я должен сказать, что вот это успешное испытание RV 144 использовало формат prime boost, О.О.: Это в Таиланде? А.К.: Да, да. И сейчас его воспроизводят на соответствующем вирусе в Южной Африке, причем, используя локальный вирус. Мы делаем нашу вакцину тоже на нашем локальном вирусе, понимаете? И в этом смысле мы это делаем правильно, потому что пока еще не научились ко всем вирусам делать вакцину. О.О.: Есть множество генетических штаммов у вируса. Как с этим быть? А.К.: Это сложная проблема, которая, тем не менее, нарисуется. О.О.: Возможна ли универсальная вакцина? А.К.: Возможна или нет, мы посмотрим. О.О.: Это пока неясно. А.К.: Но усилия к этому прилагаются. Причем, понимаете, когда есть научный метод, он определяет, как это делать. И он определяет. Он выискивает консервативные участки и пытается сделать так, чтобы иммунный ответ вызывался на все субтипы вируса. А их сейчас там больше десяти. Оказывается, что при заражении вирусом имеет эффект так называемого генетического бутылочного горлышка. То есть оказывается, что атакуется человек миллионами частиц, а вызывает заражение только одна. О.О.: Как вы это поняли? А.К.: Сейчас я расскажу, как. И сначала это было установлено в 2009 году для сексуальной передачи. И в 2010 нами для передачи наркозависимых. Никто не верил. Все думали, что инфицирование одной вирусной частицей происходит в результате отбора на слизистых оболочках. То есть все рвутся, но проходит через эту слизистую оболочку только одна частица. А наркозависимые же прямо вводят этот вирус себе. И вдруг оказалось, что и там происходит заражение одной вирусной частицей. Делается это следующим образом. Надо поймать раннюю стадию заражения буквально неделю или две, и мы научились это делать. Титруются эти вирусы до такого состояния, чтобы в пробирке была только одна нуклеиновая кислота. И после этого они секвенируются, читается генетический код. И если эти сиквенсы одинаковые, это говорит о том, что вирус был один. Сейчас эти методы сиквенса же эволюционируют. И сейчас используется уже так называемое секвенирование следующего поколения. И если мы установили этот эффект на десятках сиквенсов, то сейчас мы его подтвердили на тысячах сиквенсов. То есть таким образом мы установили фундаментальное явление о том, что заражение происходит одной вирусной частицей в большинстве случаев. И именно против этих вирусных частиц надо делать вакцину. О.О.: Ваша вакцина ДНК-4 разработана консорциумом, включая ваш биомедицинский центр. Вы с учетом уже новых знаний и исследований провели вторую клиническую фазу. Но что дальше? Ведь нашу программу, как и другие программы, посвященные проблеме ВИЧ-инфекции, смотрят люди и родственники, смотрят больные и смотрят родственники этих больных, и они смотрят на вас с большой надеждой. Вы можете как-то обнадежить? А.К.: Я могу обнадежить вот каким образом. Что, согласно экспертным оценкам, которые я разделяю, достаточно эффективная создана будет создана между 2026 и 2030 годом. И у нас, и в мире. О.О.: Неужели так долго? А.К.: Если не дольше еще будет. Хочется, чтоб так быстро это произошло. Теперь что более конкретно? Мы надеемся, что наши испытания продолжатся и что те люди, которые хотят в них принять участие, смогут в них принять участие. На нас выходит очень много ВИЧ-инфицированных, которых мы записываем в эти списки потенциальных участников. Но потом все равно получается, что их отбирает медицинская комиссия по показателям. Но, тем не менее, нам нужны добровольцы. Ведь на самом деле разработка вакцины – это взаимодействие и сообщества. О.О.: Знаете, я просто хочу… А.К.: И еще одна очень важная вещь, которую здесь нужно помнить и говорить. Дело в том, что разработка вакцины, решение проблемы вакцины – это не разработка одного конкретного кандидата. Это разработка инфраструктуры и системы, которая порождает целую серию кандидатных вакцин. Вот смотрите. Мы сейчас закончили вторую фазу клинических испытаний и начали доклинические испытания одного из следующих компонентов вакцины. Понимаете? И это сейчас происходит. И мы имеем поддержку на это и так далее. И я только что вам рассказывал, что есть очень фундаментальные исследования вирусных частиц, сиквенсов и так далее. Есть исследования доклинические на животных, есть клинические исследования разных фаз. И все это вместе создает такую ситуацию, что общество продуцирует один за другим кандидатные вакцины, одну кандидатную вакцину за другой. И отсюда вытекает вероятность того, что проблема будет решена. Причем, эта вероятность уже повышается и зависит от политической воли и поддержки общества. О.О.: Знаете, есть опыт в Соединенных Штатах, как общество реагировало на эту проблему. Сначала это были сообщества тех, кто являлся носителями ВИЧ-инфекции, их родственники. И известны истории, это описано, как они боролись за то, чтобы правительство выделяло деньги на исследования ВИЧ и на создание лекарств от СПИДа. И там тогда они делились на группы. То есть одни, допустим, занимались радикальными протестами и пытались обратить внимание целиком больших масс. Другие шли, надевали приличные пиджаки, одежду, шли в конгресс и пробивали там, взаимодействовали с политиками. Третьи вступали во взаимодействие с научным сообществом, предлагали себя в качестве испытуемых и убеждали ученых, помогали им. И плюс еще была большая проблема с Food and drug administration, чтобы срок между тем, как лекарство прошло испытание и до того, как оно выходит в производство, чтобы сократить этот срок. Потому что больные умирали, и хотели их таким образом… То есть там есть определенный опыт, как нужно развернуть неповоротливую государственную машину и общественное сознание в сторону этой проблемы. Как у нас эту машину повернуть? Сообщество ВИЧ-инфицированных показывает удивительный пример обратной связи с сообществом, которое лечит, развивает науку и так далееА.К.: Вообще сообщество ВИЧ-инфицированных показывает удивительный пример обратной связи с сообществом, которое лечит, развивает науку и так далее. В кардиологии этого нету. А здесь есть. И вот это сообщество, активисты в значительной мере повлияли на цену лекарства между прочим, в частности, для Африки. Чтобы в Африке эти лекарства были не такие дорогие. И это фантастическое достижение. Я видел эти протестные акции, в том числе как директора вуза обливали из ведра водой, понимаете? И все это сработало в конце концов. О.О.: Это Всемирная организация здравоохранения. А.К.: Да. И это сработало в конце концов. Опять же, есть международная организация AIDS Vaccine Advocacy Coalition. Это Коалиция в защиту вакцины от СПИДа. Они лоббируют эти огромные средства, которые выделяются. Причем, смотрите, если брать Америку, то на ВИЧ, допустим, происходит снижение общего бюджета, а бюджет на вакцину растет. И, понимаете, получается, что у нас тут разрабатывали по указанию премьер-министра новую стратегию борьбы со СПИДом. И слово "вакцина" вообще забыли. То есть один раз упомянули, что она якобы невозможна или сложна. Причем, это какое-то заблуждение на границе с мракобесием, по-моему, что вакцина от СПИДа невозможна. Это мне напоминает другие заблуждения в области СПИДа. Первое было то, что СПИДа нет вообще. Вот Африка вымерла, но СПИДа нету. Потом – ладно, СПИД есть, но вируса нету. То есть это все придумали ученые и бизнесмены, чтобы там это… О.О.: Глобальное потепление, СПИД. Чтобы выкачивать средства из правительства. А.К.: Да. И вируса нету. Раз вируса нету, диагностика не нужна, лекарства тоже не нужны. Потом приходится смириться все-таки, что раз лекарство работает, то все-таки, значит, наверное, вирус тоже есть. Вирус есть, но вакцина теперь невозможна. Получается, что весь мир делает вакцину, и он идет не в ногу. То есть получается, что вакцину делает моя лаборатория и лаборатория Ильичева. В инициативном порядке. А государство вроде бы как-то и ни при чем. Это должно быть исправлено, это будет исправлено, конечно. О.О.: Большое спасибо. У нас в программе был доктор биологических наук, директор биомедицинского центра Андрей Козлов. otr-online.ru Можно ли сделать вакцину против ВИЧ? С помощью ступенчатой вакцинации иммунную систему хотят научить вырабатывать редкий тип антител, эффективно нейтрализующих ВИЧ. По данным Всемирной организации здравоохранения, в 2016 году с ВИЧ во всем мире жили 36,7 миллионов человек, 1,8 миллиона заразилось, а 1 миллион умер от развившегося СПИДа. Лекарства, которое полностью уничтожало бы ВИЧ, пока не существует. Антиретровирусные препараты, которые инфицированные люди вынуждены принимать пожизненно, сдерживают размножение вируса, но целиком его истребить не могут. Дело в том, что когда ВИЧ проникает в клетку, он встраивается в ДНК, где становится недосягаемым для лекарств и невидимым для иммунной системы. Там он может тихо «отсиживаться» и не приступать к размножению, пока не настанет безопасный момент.
Известен лишь один случай полного излечения от ВИЧ. Тимоти Браун, прославившийся как «берлинский пациент», в 2007 году перенес трансплантацию костного мозга (напомним, что именно костный мозг – резервуар иммунных клеток) от донора, который обладал естественной устойчивостью к ВИЧ. (Донор был из 1% тех счастливчиков, у которых на клетках нет рецептора, с помощью которого ВИЧ в них попадает.) С первого дня после трансплантации пациент прекратил принимать антиретровирусные препараты и больше к ним не возвращался, и в дальнейшем вирус у него так и не смогли найти ни в какой форме. К сожалению, случай с Тимоти Брауном остается исключением. У других пациентов полного избавления от вируса не случалось, к тому же замещение зараженной иммунной системы с помощью трансплантации от донора – очень сложная и рискованная процедура. С ВИЧ также можно бороться методами генной терапии. У инфицированного человека забирают Т-клетки из крови и редактируют их геном: с помощью технологии CRISPR/Cas9 (о которой мы неоднократно писали) удаляют ген того самого рецептора, которого нет у людей с естественной устойчивостью к ВИЧ. Как несложно догадаться, на деле в этом направлении все обстоит гораздо сложнее, чем на словах, и пока что о молекулярно-генетическом лекарстве от ВИЧ говорить рано. Но, как известно, предотвратить болезнь лучше, чем ее лечить – иными словами, против ВИЧ хорошо бы иметь вакцину. Однако, как и в случае с лекарством, 30 лет поисков вакцины против него не увенчались успехом. При вакцинировании иммунитет должен запомнить характерные молекулярные признаки вируса. Но вирусы легко мутируют, а ВИЧ мутирует особенно быстро – из-за того, что фермент, который он использует для копирования своей генетической информации, допускает много ошибок. В течение года с момента инфицирования популяция ВИЧ может достичь такого же генетического разнообразия, какого достигает за то же время вирус гриппа в масштабе всего мира. Поэтому новая вакцина от гриппа у нас – каждый год, а вакцины от ВИЧ нету вовсе. По этой же причине организм не в состоянии победить ВИЧ самостоятельно. Иммунная система не поспевает за изменчивостью вируса: пока она изобретает антитела против одних генетических вариантов, уже вовсю плодятся другие, против которых антитела не работают. Но сравнительно недавно надежда на создание вакцины появилась вновь, когда исследователи открыли особый тип антител – нейтрализующие антитела широкого спектра действия. Они сильно мутированы (изменены) по сравнению с обычными антителами и направлены против консервативных участков вируса (то есть таких, которые слабее всего изменяются от поколения к поколению). В исследованиях последних лет было установлено, что они способны нейтрализовать до 98% всех генетических вариантов ВИЧ. Иммунная система в какой-то момент сама начинает стабильно вырабатывать такие антитела, но этот момент наступает через несколько лет после заражения – слишком поздно. Сотрудники Института аллергии и иммунологии в Ла-Холья и Института Скриппса разработали стратегию вакцинации, которая учит иммунную систему вырабатывать антитела широкого спектра быстро. Чтобы понять, что именно тут имеется в виду, нужно представлять, как вообще иммунные клетки начинают синтезировать антитела против патогена. Антитела производят В-лимфоциты. При этом сами они могут взаимодействовать с чужеродными молекулами, в том числе и с вирусными белками. У нас постоянно появляются В-клетки с самыми разными рецепторами для распознавания чужаков, так что для любого вируса обязательно найдутся В-клетки, которые схватят его молекулы. Вирусный материал В-клетки поглощают, преобразуют внутри себя и выставляют наружу на своей поверхности. Для того, чтобы дело пошло дальше, В-клетка должна пообщаться с Т-клеткой. Т-клетка подходит к В-клетке, распознает ее собственные молекулы и молекулы вирусного материала, который на ней выставлен, и теперь В-клетка получает «добро» на дальнейшую борьбу. (Если взаимодействие между Т- и В-клетками пошло как-то не так, значит, В-клетка до этого что-то сделала неправильно и Т-клетка ее не активирует.) Теперь В-клетки, получившие разрешение на борьбу с вирусом, пытаются сделать так, чтобы связывать его как можно точнее и прочнее. Они начинают делиться и при каждом делении мутируют, так что у каждой новой В-клетки рецептор слегка меняется, и клетки с новыми рецепторами опять проходят отбор при взаимодействии с Т-клетками. Если слегка изменившийся рецептор распознает вирус еще лучше, то В-клетка, у которой он получился, продолжает делиться дальше. И лишь после многих раундов такого естественного отбора В-клетки с наилучшими рецепторами начинают продуцировать антитела (которые по строению идентичны рецепторам). Роберт Эбботт (Robert K. Abbott) и его коллеги предлагают повлиять как раз на процесс отбора. Они исходят из того, что практически у всех людей в иммунной системе присутствует некое количество В-клеток широкого спектра (ранее исследователи установили, что доля таких клеток равна приблизительно одной клетке на миллион). Тогда цель вакцинации – сделать так, чтобы В-клетки широкого спектра отбирались вместо обычных, которые хоть и отшлифованы идеально под определенные вирусные генетические варианты, но очень быстро устаревают. Сама вакцинация представляет собой многоступенчатую процедуру, в ходе которой в организм вводят вирусоподобные компоненты постепенно изменяющегося состава. Каждая ступень должна приближать иммунную систему к производству заветного типа антител. По выражению одного из исследователей, все происходящее выглядит так, как если бы В-клетки, умеющие распознавать квадраты, учили распознавать круги, но учили их этому с помощью пятиугольников. На человеке разработанную стратегию не испытывали, пока что эксперименты ограничиваются мышами, и предварительные результаты можно узнать из статьи в Immunity. Говорить о полноценной вакцине против ВИЧ пока еще очень рано, но, по крайней мере, есть надежда, что ее действительно удастся создать. СМОТРЕТЬ КОММЕНТАРИИ ✎ Комментариев нет ЧИТАЙТЕ ТАКЖЕ: ryb.ru |
г.Самара, ул. Димитрова 131 [email protected] |
 |



 Распространенность ВИЧ среди взрослого населения мира по данным на 2015 год.
Распространенность ВИЧ среди взрослого населения мира по данным на 2015 год.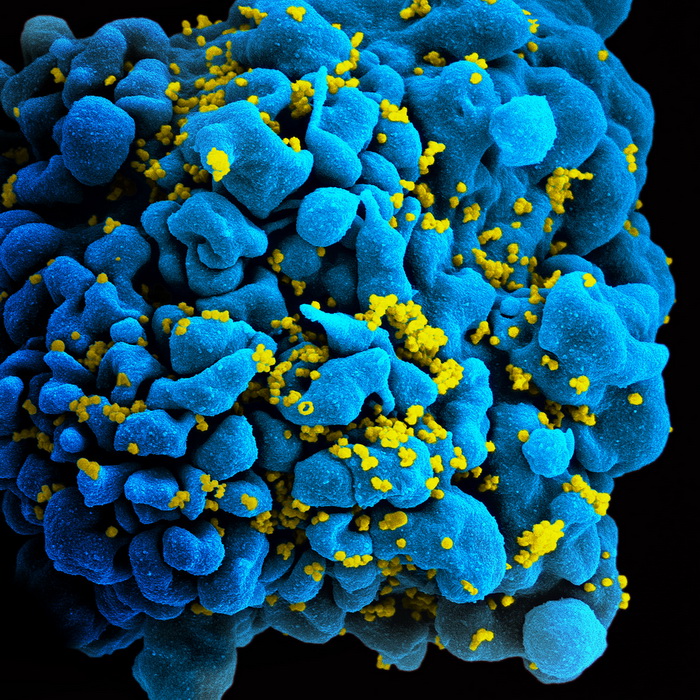 Электронная микрофотография Т-клетки иммунной системы, зараженной ВИЧ. Желтые шишки – места, где вирусные частицы выходят из клетки. (Фото: Flickr.com / NIAID.)
Электронная микрофотография Т-клетки иммунной системы, зараженной ВИЧ. Желтые шишки – места, где вирусные частицы выходят из клетки. (Фото: Flickr.com / NIAID.) Распространенность ВИЧ среди взрослого населения мира по данным на 2015 год. (Иллюстрация: ВОЗ.)
Распространенность ВИЧ среди взрослого населения мира по данным на 2015 год. (Иллюстрация: ВОЗ.) Электронная микрофотография Т-клетки иммунной системы, зараженной ВИЧ. Желтые шишки – места, где вирусные частицы выходят из клетки. (Фото: Flickr.com / NIAID.)
Электронная микрофотография Т-клетки иммунной системы, зараженной ВИЧ. Желтые шишки – места, где вирусные частицы выходят из клетки. (Фото: Flickr.com / NIAID.) Распространенность ВИЧ среди взрослого населения мира по данным на 2015 год. (Иллюстрация: ВОЗ.)‹›
Распространенность ВИЧ среди взрослого населения мира по данным на 2015 год. (Иллюстрация: ВОЗ.)‹› 









