Содержание
Организация вакцинопрофилактики в образовательных учреждениях — Бюджетное учреждение Ханты-Мансийского автономного округа — Югры
Одним из главных разделов деятельности школьных медицинских работников является прививочная работа, которая проводится согласно плану, предоставляемому прививочной картотекой ДП.
В работе медицинские работники руководствуются следующими приказами:
— Федеральный закон от 17 сентября 1998г. № 157-Ф «Об иммунопрофилактике инфекционных болезней»,
– Приказом МЗ РФ от 21 марта 2014 года № 125н «Об утверждении национального календаря профилактических прививок и календаря профилактических прививок по эпидемическим показаниям»;
— СП 3.3.2342-08 от 03.03.08г. «Обеспечение безопасности иммунизации»;
— СП 3.3.2.3332-16 «Условия транспортирования и хранения иммунобиологических лекарственных препаратов».
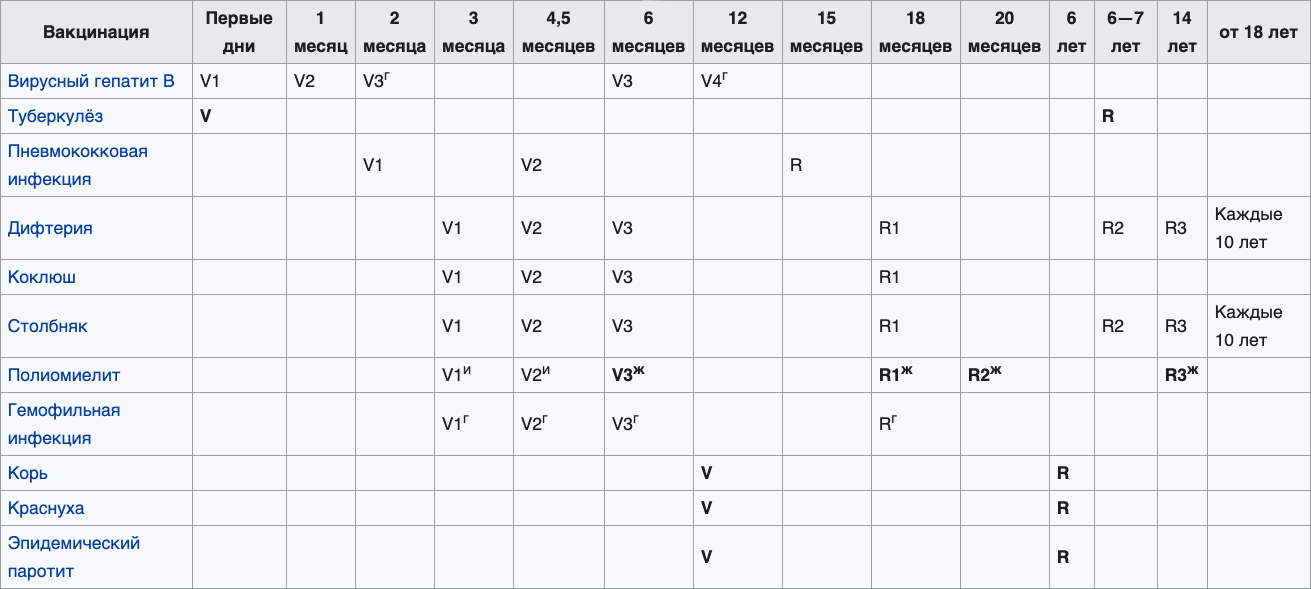
КАЛЕНДАРЬ ПРОФПРИВИВОК (приказ – 125 н)
На каждую прививку родители (законные представители) несовершеннолетних в возрасте до 15 лет дают информированное согласие.
В начале учебного года (сентябрь) в школе проводится массовая иммуннодиагностика туберкулёза детям с 1-го по 8-е классы, подросткам с 9-го по 11 классы иммуннодиагностика туберкулёза проводится весной (март-апрель). По окончании иммуннодиагностики туберкулёза всем детям с 1-го по 11-е классы проводится обязательная вакцинация против гриппа. Перед вакцинацией все дети осматриваются врачом (фельдшером), проводится термометрия. В случае противопоказаний к вакцинации прививки откладываются до выздоровления. Через месяц после противогриппозной прививки продолжается вакцинация детей и подростков по индивидуальному плану вакцинации, согласно национальному календарю профилактических прививок.
|
Программирование, разработка версии для слабовидящих — Интернет-лаборатория «Делиссимо»
Сайт использует файлы cookie.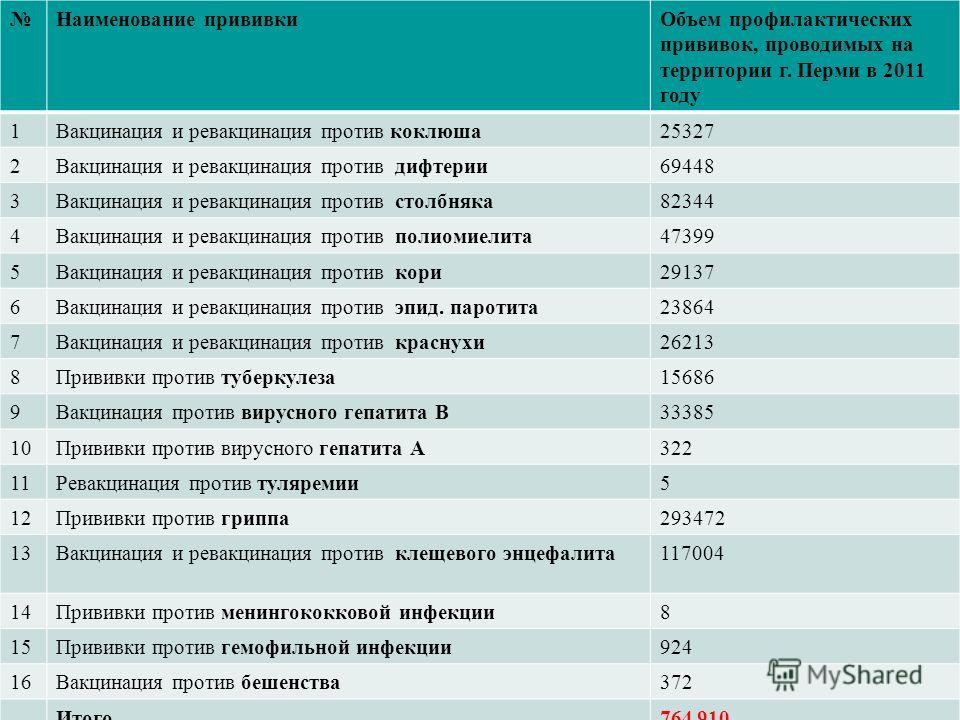 Они позволяют узнавать Вас и получать информацию о Вашем пользовательском опыте. Если Вы не хотите, чтобы ваши данные обрабатывались, вы должны покинуть сайт. Если Вы продолжаете пользоваться сайтом, Вы ДАЕТЕ СОГЛАСИЕ на использование файлов cookie, обработку и хранение Ваших персональных данных.
Они позволяют узнавать Вас и получать информацию о Вашем пользовательском опыте. Если Вы не хотите, чтобы ваши данные обрабатывались, вы должны покинуть сайт. Если Вы продолжаете пользоваться сайтом, Вы ДАЕТЕ СОГЛАСИЕ на использование файлов cookie, обработку и хранение Ваших персональных данных.
Ок, даю согласие
Календарь вакцинации
| Месяцы жизни | 0 | 1 | 2 | 3 | 4.5 | 6 | 9 | 12 | 15 | 18 | 20 | 23 |
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Туберкулез | 3-7 дней | |||||||||||
| Гепатит B | V1 | V2 | V3 | |||||||||
| V1 | V2 | V3 | V4 | |||||||||
| Пневмококковая инфекция | V1 | V2 | 1RV | |||||||||
| Ротавирусная инфекция | V1 | V2 | V3 | |||||||||
| Коклюш | V1* | V2* | V3* | 1RV* | ||||||||
| Дифтерия | ||||||||||||
| Столбняк | ||||||||||||
| Полиомиелит | V1 ИПВ* | V2* | V3 ИПВ /ОПВ* | 1RV ИПВ /ОПВ* | 2RV ОПВ | |||||||
| Гемофильная инфекция | V1* | V2* | V* | 1RV | ||||||||
| Менингококковая инфекция | V1 | V2 | ||||||||||
| Ветряная оспа | V1 | |||||||||||
| Корь | V1ККП | |||||||||||
| Краснуха | ||||||||||||
| Эпидемический паротит | ||||||||||||
| Вирусный гепатит А | ||||||||||||
| Грипп | Ежегодно | |||||||||||
| Клещевой вирусный энцефалит | ||||||||||||
Вакцино-вызванные петлевые антитела V3 у макак-резусов и контроль вируса иммунодефицита человека у обезьян, экспрессирующего вирус иммунодефицита человека первого типа.
 Конверт для изолята первичного пациента
Конверт для изолята первичного пациента
Симмондс П., Вебер Дж. Нейтрализация первичных и адаптированных к Т-клеточной линии изолятов вируса иммунодефицита человека типа 1: роль V3-специфических антител. Джей Ген Вирол. 1998; 79: 77–82. [PubMed] [Академия Google]
2. Бу-Хабиб Д.С., Родерикес Г., Оравец Т., Берман П.В., Луссо П., Норкросс М.А. Загадочная природа эпитопов области оболочки V3 защищает первичный моноцитотропный вирус иммунодефицита человека типа 1 от нейтрализации антителами. Дж Вирол. 1994;68:6006–6013. [Бесплатная статья PMC] [PubMed] [Google Scholar]
3. Бурес, Р., А. Гайтан, Т. Чжу, К. Грациози, К. МакГрат, Дж. Тарталья, П. Кодрелье, Р. Э. Л. Хабиб, М. Клейн, А. Лаззарин, Д. Стейблейн, М. Дирс, Л. Кори, М. Л. Гринберг, Д. Х. Шварц и Д. К. Монтефиори. Иммунизация рекомбинантными векторами оспы канареек, экспрессирующими заякоренный в мембране gp120, с последующей бустерной стимуляцией белком gp160 не приводит к образованию антител, которые нейтрализуют первичные изоляты R5 вируса иммунодефицита человека типа 1.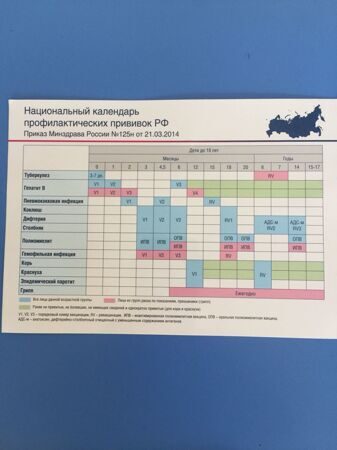 AIDS Res. Гум. Ретровирусы, в печати. [PubMed]
AIDS Res. Гум. Ретровирусы, в печати. [PubMed]
4. Бертон Д. Р. Вакцина против ВИЧ типа 1: взгляд на антитела. Proc Natl Acad Sci USA. 1997; 94:10018–10023. [Бесплатная статья PMC] [PubMed] [Google Scholar]
5. Cheingsong-Popov R, Osmanov S, Pau CP, Schochetman G, Barin F, Holmes H, Francis G, Ruppach H, Dietrich U, Lister S, Weber J ● Серотипирование инфекций ВИЧ-1: определение, связь с генетическими подтипами вируса и оценка результатов анализа. AIDS Res Hum Retroviruses. 1998;14:311–318. [PubMed] [Google Scholar]
6. Чоу Х., Фарзан М., Сан Й., Салливан Н., Роллинз Б., Понат П.Д., Ву Л., Маккей С.Р., ЛаРоса Г., Ньюман В., Джерард Н., Джерард С., Содроски Дж. Рецепторы β-хемокинов CCR3 и CCR5 способствуют инфицированию первичными изолятами ВИЧ-1. Клетка. 1996; 85: 1135–1148. [PubMed] [Google Scholar]
7. Cocchi F, DeVico AL, Garzino-Demo A, Cara A, Gallo RC, Lusso P. Домен V3 гликопротеина gp120 оболочки ВИЧ-1 имеет решающее значение для хемокин-опосредованной блокады инфекционное заболевание.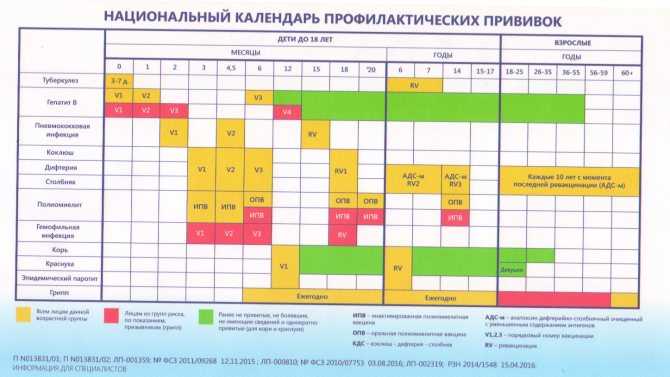 Нат Мед. 1996;2:1244–1247. [PubMed] [Google Scholar]
Нат Мед. 1996;2:1244–1247. [PubMed] [Google Scholar]
8. Кроуфорд Дж. М., Эрл П. Л., Мосс Б., Рейманн К. А., Вайанд М. С., Мэнсон К. Х., Билска М., Чжоу Дж. Т., Пауза К. Д., Паррен П. В. Х. И., Бертон Д. Р., Содроски Д. Г., Летвин Н. Л., Монтефиори Д. С. Характеристика первичных изолятоподобных вариантов обезьяно-человеческого вируса иммунодефицита. Дж Вирол. 1999;73:10199–10207. [Статья бесплатно PMC] [PubMed] [Google Scholar]
9. Daar E S, Li X L, Moudgil T, Ho D D. Для нейтрализации первичных изолятов вируса иммунодефицита человека типа 1 требуются высокие концентрации рекомбинантного растворимого CD4. Proc Natl Acad Sci USA. 1990;87:6574–6578. [Бесплатная статья PMC] [PubMed] [Google Scholar]
10. Эмини Э.А., Шлейф В.А., Нанберг Дж.Х., Конли А.Дж., Эда Ю., Токиёси С., Путни С.Д., Мацусита С., Кобб К.Е., Джетт С.М., Эйхберг Дж.В., Мурти K K. Профилактика ВИЧ-1-инфекции у шимпанзе с помощью домен-специфического моноклонального антитела gp120 V3. Природа. 1992; 355: 728–730. [PubMed] [Google Scholar]
[PubMed] [Google Scholar]
11. Etemad-Moghadam B, Karlsson GB, Halloran M, Sun Y, Schenten D, Fernandes M, Letvin NL, Sodroski J. Характеристика гликопротеиновых эпитопов оболочки вируса иммунодефицита обезьян, распознаваемых путем нейтрализации антитела инфицированных макак. Дж Вирол. 1998;72:8437–8445. [Бесплатная статья PMC] [PubMed] [Google Scholar]
12. Girard M, Kieny M-P, Pinter A, Barre-Sinoussi F, Nara P, Kolbe H, Kusumi K, Chaput A, Reinhart T, Muchmore E, Ronco J , Качорек М., Гомар Э., Глюкман Дж. К., Фульц П. Н. Иммунизация шимпанзе обеспечивает защиту от заражения вирусом иммунодефицита человека. Proc Natl Acad Sci USA. 1991; 88: 542–546. [Бесплатная статья PMC] [PubMed] [Google Scholar]
13. Harada S, Koyanagi Y, Yamamoto N. Инфекция HTL V-III/LAV в клетках, несущих HTLV-I MT-2 и MT-4, и применение в анализ бляшек. Наука. 1985;229:563–566. [PubMed] [Google Scholar]
14. Haynes B F, Torres J V, Langlois A J, Bolognesi DP, Gardner MB, Palker T J, Scearce RM, Jones DM, Moody MA, McDanal C, Matthews T J. Индукция нейтрализующих антител HIVMN у приматов, использующих режим прайм-бустинг гибридных синтетических оболочечных пептидов gp120. Дж Иммунол. 1993; 151:1646–1653. [PubMed] [Google Scholar]
Индукция нейтрализующих антител HIVMN у приматов, использующих режим прайм-бустинг гибридных синтетических оболочечных пептидов gp120. Дж Иммунол. 1993; 151:1646–1653. [PubMed] [Google Scholar]
15. Javaherian K, Langlois A J, McDanal C, Ross K L, Eckler LI, Jellis CL, Profy AT, Rusche J R, Bolognesi DP, Putney S D, Matthews T J. Основной нейтрализующий домен белок оболочки вируса иммунодефицита человека 1 типа. Proc Natl Acad Sci USA. 1989;86:6768–6772. [Бесплатная статья PMC] [PubMed] [Google Scholar]
16. Joag SV, Li Z, Foresman L, Stephens E B, Zhao L J, Adany I, Pinson DM, McClure H M, Narayan O. Химерный вирус иммунодефицита обезьяны/человека, который вызывает прогрессирующую потерю CD4 + Т-клеток и СПИД у свинохвостых макак. Дж Вирол. 1996;70:3189–3197. [Бесплатная статья PMC] [PubMed] [Google Scholar]
17. Летвин Н.Л., Монтефиори Д.К., Ясутоми Ю., Перри Х.К., Дэвис М.Е., Лекутис С., Алрой М., Фрид Д.Л., Лорд С.И., Хандт Л.К., Лю М.А., Шивер JW. Мощный, защитный иммунный ответ против ВИЧ, генерируемый бимодальной ДНК оболочки ВИЧ плюс белковая вакцинация. Proc Natl Acad Sci USA. 1997;94:9378–9383. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Мощный, защитный иммунный ответ против ВИЧ, генерируемый бимодальной ДНК оболочки ВИЧ плюс белковая вакцинация. Proc Natl Acad Sci USA. 1997;94:9378–9383. [Бесплатная статья PMC] [PubMed] [Google Scholar]
18. Ляо Х., Этемад-Могадам Б., Монтефиори Д.К., Сунь Й., Содроски Дж., Скирс Р.М., Домс Р.В., Томасч Дж.Р., Робинсон С., Летвин Н.Л., Хейнс Б. F. Индукция антител у морских свинок и макак-резусов к оболочке вируса иммунодефицита человека типа 1: нейтрализация непатогенных и патогенных первичных изолятов штаммов вируса иммунодефицита обезьяны/человека. Дж Вирол. 2000; 74: 254–263. [Бесплатная статья PMC] [PubMed] [Google Scholar]
19. Mascola JR, Lewis MG, Stiegler G, Harris D, VanCott TC, Hayes D, Louder MK, Brown CR, Sapan CV, Frankel SS, Lu Y, Robb ML, Katinger H, Birx DL. Защита макак против патогенного вируса иммунодефицита обезьян/человека 89.6PD путем пассивного переноса нейтрализующих антител. Дж Вирол. 1999;73:4009–4018. [Бесплатная статья PMC] [PubMed] [Google Scholar]
20. Mascola JR, Stiegler G, VanCott TC, Katinger H, Carpenter CB, Hanson CE, Beary H, Hayes D, Frankel SS, Birx DL, Lewis MG. Защита макак от вагинальной передачи патогенного химерного вируса ВИЧ-1/ВИО путем пассивного введения нейтрализующих антител. Нат Мед. 2000; 6: 207–210. [PubMed] [Академия Google]
Mascola JR, Stiegler G, VanCott TC, Katinger H, Carpenter CB, Hanson CE, Beary H, Hayes D, Frankel SS, Birx DL, Lewis MG. Защита макак от вагинальной передачи патогенного химерного вируса ВИЧ-1/ВИО путем пассивного введения нейтрализующих антител. Нат Мед. 2000; 6: 207–210. [PubMed] [Академия Google]
21. Макдугал Дж. С., Кеннеди М. С., Орлофф С. Л., Николсон Дж. К. А., Спира Т. Дж. Механизм нейтрализации вируса иммунодефицита человека типа 1 (ВИЧ-1): необратимая инактивация инфекционности антителом против ВИЧ-1. Дж Вирол. 1996; 70: 5236–5245. [Бесплатная статья PMC] [PubMed] [Google Scholar]
22. Montefiori D C, Collman R G, Fouts TR, Zhou J Y, Bilska M, Hoxie J A, Moore J P, Bolognesi D P. Доказательства того, что антитело-опосредованная нейтрализация иммунодефицита человека вирус типа 1 не зависит от использования корецепторов. Дж Вирол. 1998;72:1886–1893. [Бесплатная статья PMC] [PubMed] [Google Scholar]
23. Montefiori D C, Pantaleo G, Fink L M, Zhou J T, Zhou J Y, Bilska M, Miralles G D, Fauci A S. Нейтрализующие и усиливающие инфекцию реакции антител на человека вирус иммунодефицита 1 типа у длительно непрогрессирующих. J заразить дис. 1996; 173: 60–67. [PubMed] [Google Scholar]
Нейтрализующие и усиливающие инфекцию реакции антител на человека вирус иммунодефицита 1 типа у длительно непрогрессирующих. J заразить дис. 1996; 173: 60–67. [PubMed] [Google Scholar]
24. Монтефиори Д. К., Рейманн К. А., Вайанд М. С., Мэнсон К., Льюис М. Г., Коллман Р. Г., Содроски Дж. Г., Болоньези Д. П., Летвин Н. Л. Нейтрализующие антитела в сыворотке макак, инфицированных химерным обезьяноподобным вирус иммунодефицита человека, содержащий оболочечные гликопротеины либо адаптированного для лаборатории варианта, либо первичного изолята вируса иммунодефицита человека типа 1. J Virol. 1998;72:3427–3431. [Статья бесплатно PMC] [PubMed] [Google Scholar]
25. Montefiori DC, Robinson WE, Jr, Schuffman SS, Mitchell WM. Оценка противовирусных препаратов и нейтрализующих антител к вирусу иммунодефицита человека с помощью быстрого и чувствительного микротитровального анализа инфекции . Дж. Клин Микробиол. 1988; 26: 231–235. [PMC free article] [PubMed] [Google Scholar]
26. Палкер Т.Дж., Кларк М.Е., Ланглуа А.Дж., Мэтьюз Т.Дж., Вайнхолд К.Дж., Рэндалл Р.Р., Болоньези Д.П., Хейнс Б.Ф. Типоспецифическая нейтрализация вируса иммунодефицита человека с антителами к кодируемым env синтетическим пептидам. Proc Natl Acad Sci USA. 1988;85:1932–1936. [PMC free article] [PubMed] [Google Scholar]
Палкер Т.Дж., Кларк М.Е., Ланглуа А.Дж., Мэтьюз Т.Дж., Вайнхолд К.Дж., Рэндалл Р.Р., Болоньези Д.П., Хейнс Б.Ф. Типоспецифическая нейтрализация вируса иммунодефицита человека с антителами к кодируемым env синтетическим пептидам. Proc Natl Acad Sci USA. 1988;85:1932–1936. [PMC free article] [PubMed] [Google Scholar]
27. Палкер Т.Дж., Мэтьюз Т.Дж., Ланглуа А., Таннер М.Е., Мартин М.Е., Скирс Р.М., Ким Дж.Е., Берзофски Дж.А., Болоньези Д.П., Хейнс Б.Ф. Поливалентный иммунодефицит человека вирусный синтетический иммуноген, состоящий из участков оболочечных Т-хелперных клеток gp120 и эпитопов нейтрализации В-клеток. Дж Иммунол. 1989; 142:3612–3619. [PubMed] [Google Scholar]
28. Reimann K A, Li J T, Veazey R, Halloran M, Park I-W, Karlsson G B, Sodroski J, Letvin N L. Химерный вирус иммунодефицита обезьяны/человека, экспрессирующий вирус иммунодефицита человека у первичного пациента изолировать тип 1 env вызывает СПИДоподобное заболевание после пассажа in vivo у макак-резусов. Дж Вирол. 1996; 70: 6922–6928. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Дж Вирол. 1996; 70: 6922–6928. [Бесплатная статья PMC] [PubMed] [Google Scholar]
29. Reimann K A, Li J T, Voss G, Lekutis C, Tenner-Racz K, Racz P, Lin W, Montefiori D C, Lee-Parritz D E, Lu Y, Коллман Р.Г., Содроски Дж., Летвин Н.Л. Ген env , полученный из первичного изолята вируса иммунодефицита человека типа 1, придает высокую репликативную способность in vivo химерному вирусу иммунодефицита обезьяны/человека у макак-резусов. Дж Вирол. 1996;70:3198–3206. [Бесплатная статья PMC] [PubMed] [Google Scholar]
30. Робинсон Х.Л., Монтефиори Д.К., Джонсон Р.П., Мэнсон К.Х., Калиш М.Л., Лифсон Дж.Д., Ризви Т.А., Лу С., Ху С.Л., Маццара Г.П., Паникали Д.Л., Херндон Дж. Г., Гликман Р., Кандидо М. А., Лиди С. Л., Вайанд М. С., МакКлюр Х. М. Нейтрализация независимого от антител сдерживания вируса иммунодефицита путем праймирования ДНК и бустерной иммунизации рекомбинантным вирусом оспы. Нат Мед. 1999; 5: 526–534. [PubMed] [Google Scholar]
31. Руше Дж. Р., Джавахериан К. , МакДанал С., Петро Дж., Линн Д. Л., Гримейла Р., Ланглуа А. Дж., Галло Р. С., Артур Л. О., Фишингер П. Дж., Болоньези Д. П., Патни С. Д., Мэтьюз Т. Дж. Антитела, которые ингибируют слияние клеток, инфицированных вирусом иммунодефицита человека, связывают 24-аминокислотную последовательность gp120 вирусной оболочки. Proc Natl Acad Sci USA. 1988;85:3198–3202. [Бесплатная статья PMC] [PubMed] [Google Scholar]
, МакДанал С., Петро Дж., Линн Д. Л., Гримейла Р., Ланглуа А. Дж., Галло Р. С., Артур Л. О., Фишингер П. Дж., Болоньези Д. П., Патни С. Д., Мэтьюз Т. Дж. Антитела, которые ингибируют слияние клеток, инфицированных вирусом иммунодефицита человека, связывают 24-аминокислотную последовательность gp120 вирусной оболочки. Proc Natl Acad Sci USA. 1988;85:3198–3202. [Бесплатная статья PMC] [PubMed] [Google Scholar]
32. Safrit J T, Lee A Y, Andrews C A, Koup R A. Область третьей вариабельной петли gp120 ВИЧ-1 распознается HLA-B7-рестриктированными CTL. от двух острых серопозитивных пациентов. Дж Иммунол. 1994; 153:3822–3830. [PubMed] [Google Scholar]
33. Salter RD, Howell DN, Cresswell P. Ген, регулирующий экспрессию антигена HLA класса I в гибридах лимфобластов T-B. Иммуногенетика. 1985; 21: 235–246. [PubMed] [Академия Google]
34. Schwartz G, Wolfs T, Goudsmit J. Характеристика специфичности ответа человеческих антител на домен нейтрализации V3 ВИЧ-1. AIDS Res Hum Retroviruses. 1992; 8: 1897–1908. [PubMed] [Google Scholar]
1992; 8: 1897–1908. [PubMed] [Google Scholar]
35. Сет А., Урманов И., Шмитц Дж. Э., Курода М. Дж., Лифтон М. А., Никерсон С. Э., Вятт Л., Кэрролл М., Мосс Б., Вензон Д., Летвин Н. Л., Хирш В. М. Иммунизация с помощью модифицированный вирус коровьей оспы, экспрессирующий вирус иммунодефицита обезьян (SIV) Gag-Pol, вызывает анамнестический Gag-специфический цитотоксический ответ Т-лимфоцитов и связан со снижением виремии после заражения SIV. Дж Вирол. 2000; 74: 2505–2509.. [Статья бесплатно PMC] [PubMed] [Google Scholar]
36. Spenlehauer C, Saragosti S, Fleury HJA, Kim A, Aubertin AM, Moog C. Исследование петли V3 в качестве эпитопа-мишени для антител, участвующих в нейтрализации первичные изоляты по сравнению с адаптированными к Т-клеточной линии штаммами вируса иммунодефицита человека типа 1. J Virol. 1998;72:9855–9864. [Статья PMC free] [PubMed] [Google Scholar]
37. Стризки Дж. М., Тернер Дж. Д., Коллман Р. Г., Хокси Дж., Гонсалес-Скарано Ф. Моноклональное антитело (12G5), направленное против CXCR-4, ингибирует инфекцию, вызванную двойным изолят вируса иммунодефицита человека типа 1 ВИЧ-1 89,6 , но не Т-тропный изолят ВИЧ-1 HxB . Дж Вирол. 1997; 71: 5678–5683. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Дж Вирол. 1997; 71: 5678–5683. [Бесплатная статья PMC] [PubMed] [Google Scholar]
38. Trkola A, Dragic T, Arthos J, Binley JM, Olson WC, Allaway GP, Cheng-Mayer C, Robinson J, Maddon PJ, Moore JP. CD4 -зависимые, чувствительные к антителам взаимодействия между ВИЧ-1 и его корецептором CCR-5. Природа. 1996; 384: 184–187. [PubMed] [Google Scholar]
39. Уголини С., Мондор И., Паррен П.У.Х.И., Бертон Д.Р., Тилли С.А., Классе П.Дж., Саттентау К.Дж. Ингибирование прикрепления вируса к CD4 + клеток-мишеней является основным механизмом нейтрализации ВИЧ-1, адаптированного к линии Т-клеток. J Эксперт Мед. 1997;186:1287–1298. [PMC free article] [PubMed] [Google Scholar]
40. Valenzuela A, Blanco J, Krust B, Franco R, Hovanessian AG. Нейтрализующие антитела против петли V3 вируса иммунодефицита человека типа 1 gp120 блокируют CD4-зависимую и — независимое связывание вируса с клетками. Дж Вирол. 1997; 71:8289–8298. [Статья бесплатно PMC] [PubMed] [Google Scholar]
41. Vancott TC, Polonis VR, Loomis LD, Michael NL, Nara PL, Birx DL. Дифференциальная роль V3-специфических антител в анализах нейтрализации, включающих первичные и лабораторные исследования. адаптированные изоляты ВИЧ типа 1. AIDS Res Hum Retroviruses. 1995;11:1379–1390. [PubMed] [Google Scholar]
Vancott TC, Polonis VR, Loomis LD, Michael NL, Nara PL, Birx DL. Дифференциальная роль V3-специфических антител в анализах нейтрализации, включающих первичные и лабораторные исследования. адаптированные изоляты ВИЧ типа 1. AIDS Res Hum Retroviruses. 1995;11:1379–1390. [PubMed] [Google Scholar]
42. Vogel T, Kurth R, Norley S. Большинство нейтрализующих абс у пациентов с ВИЧ-1 распознают линейные последовательности петли V3. Исследования с использованием множественных антигенных пептидов MN ВИЧ-1. Дж Иммунол. 1994; 153:1895–1904. [PubMed] [Google Scholar]
43. Wu L, Gerard N P, Wyatt R, Choe H, Parolin C, Ruffing N, Borsetti A, Cardoso A A, Desjardin E, Newman W, Gerard C, Sodroski J. CD4-индуцированный взаимодействие первичных гликопротеинов gp120 ВИЧ-1 с хемокиновым рецептором CCR-5. Природа. 1996;384:179–183. [PubMed] [Google Scholar]
44. Zhou J Y, Montefiori D C. Опосредованная антителами нейтрализация первичных изолятов вируса иммунодефицита человека типа 1 в мононуклеарных клетках периферической крови не зависит от исходного состояния активации клеток. Дж Вирол. 1997; 71: 2512–2517. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Дж Вирол. 1997; 71: 2512–2517. [Бесплатная статья PMC] [PubMed] [Google Scholar]
45. Zwart G, Back NK T, Ramautarsing C, Valk M, van der Hoek L, Goudsmit J. Частая и ранняя способность нейтрализовать MN ВИЧ-1 в сыворотке от голландского ВИЧ -1 сероконвертеры связаны с реактивностью антител к пептидам домена gp120 V3. AIDS Res Hum Retroviruses. 1994;10:245–251. [PubMed] [Google Scholar]
Дифференциальная индукция коронных антител против V3 с режимами связывания колыбели и ковша в ответ на вакцинацию с помощью оболочки ВИЧ-1
1. Ivanoff LA, Dubay JW, Morris JF, Roberts SJ, Gutshall Л., Штернберг Э.Дж. и соавт. Область петли V3 белка оболочки gp120 ВИЧ-1 необходима для инфекционности вируса. Вирусология. 1992; 187: 423–432. [PubMed] [Google Scholar]
2. Набатов А.А., Поллакис Г., Линнеманн Т., Клифиус А., Чалаби М.И., Пакстон В.А. Внутрипациентные изменения в участках gp120 V1V2 и V3 вируса иммунодефицита человека типа 1 по-разному модулируют использование корецепторов, ингибирование вируса хемокинами CC/CXC, растворимым CD4 и моноклональными антителами b12 и 2G12. Журнал вирусологии. 2004; 78: 524–530. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Журнал вирусологии. 2004; 78: 524–530. [Бесплатная статья PMC] [PubMed] [Google Scholar]
3. Xiang Y, Liu W, Chen Y, Zhang C, Su W, Zhang Y, et al. Вариабельная петля 3 в оболочечном гликопротеине имеет решающее значение для использования атипичного корецептора штаммом ВИЧ-1. ПлоС один. 2014;9:e98058. [Статья бесплатно PMC] [PubMed] [Google Scholar]
4. Hung CS, Vander Heyden N, Ratner L. Анализ критического домена в петле V3 gp120 вируса иммунодефицита человека типа 1, участвующего в утилизации CCR5. Журнал вирусологии. 1999;73:8216–8226. [Бесплатная статья PMC] [PubMed] [Google Scholar]
5. Jiang X, Burke V, Totrov M, Williams C, Cardozo T, Gorny MK, et al. Консервативные структурные элементы в короне V3 gp120 ВИЧ-1. Структурная и молекулярная биология природы. 2010;17:955–961. [PubMed] [Google Scholar]
6. Hioe CE, Wrin T, Seaman MS, Yu X, Wood B, Self S, et al. Моноклональные антитела против V3 проявляют широкую нейтрализующую активность в отношении нескольких подтипов ВИЧ-1. ПлоС один. 2010;5:e10254. [Бесплатная статья PMC] [PubMed] [Google Scholar]
ПлоС один. 2010;5:e10254. [Бесплатная статья PMC] [PubMed] [Google Scholar]
7. Gottardo R, Bailer RT, Korber BT, Gnakaran S, Phillips J, Shen X, et al. Плазменный IgG к линейным эпитопам в областях V2 и V3 gp120 ВИЧ-1 коррелирует со сниженным риском инфекции в испытании эффективности вакцины RV144. ПлоС один. 2013;8:e75665. [Бесплатная статья PMC] [PubMed] [Google Scholar]
8. Huang CC, Tang M, Zhang MY, Majeed S, Montabana E, Stanfield RL, et al. Структура ядра gp120 ВИЧ-1, содержащего V3. Наука. 2005; 310:1025–1028. [Бесплатная статья PMC] [PubMed] [Google Scholar]
9. Huang CC, Lam SN, Acharya P, Tang M, Xiang SH, Hussan SS, et al. Структуры N-конца CCR5 и тирозин-сульфатированного антитела с gp120 и CD4 ВИЧ-1. Наука. 2007; 317:1930–1934. [Бесплатная статья PMC] [PubMed] [Google Scholar]
10. Walker LM, Huber M, Doores KJ, Falkowska E, Pejchal R, Julien JP, et al. Широкий охват нейтрализации ВИЧ несколькими сильнодействующими антителами. Природа. 2011; 477:466–470. [Бесплатная статья PMC] [PubMed] [Google Scholar]
[Бесплатная статья PMC] [PubMed] [Google Scholar]
11. Pejchal R, Doores KJ, Walker LM, Khayat R, Huang PS, Wang SK, et al. Мощное и широкое нейтрализующее антитело распознает и проникает через гликановый щит ВИЧ. Наука. 2011; 334:1097–1103. [Бесплатная статья PMC] [PubMed] [Google Scholar]
12. Mouquet H, Scharf L, Euler Z, Liu Y, Eden C, Scheid JF, et al. Распознавание N-гликанов сложного типа мощными широко нейтрализующими антителами к ВИЧ. Труды Национальной академии наук Соединенных Штатов Америки. 2012;109:E3268–E3277. [Бесплатная статья PMC] [PubMed] [Google Scholar]
13. Zolla-Pazner S. Улучшение природы: фокусировка иммунного ответа на петле V3. Антитела человека. 2005; 14:69–72. [PubMed] [Google Scholar]
14. Davis KL, Bibollet-Ruche F, Li H, Decker JM, Kutsch O, Morris L, et al. Оболочечные химеры вируса иммунодефицита человека типа 2 (ВИЧ-2)/ВИЧ-1 выявляют высокие титры широко реагирующих ВИЧ-1 V3-специфических антител в плазме человека. Журнал вирусологии. 2009;83:1240–1259. [Бесплатная статья PMC] [PubMed] [Google Scholar]
2009;83:1240–1259. [Бесплатная статья PMC] [PubMed] [Google Scholar]
15. Davis KL, Gray ES, Moore PL, Decker JM, Salomon A, Montefiori DC, et al. Антитела, специфичные к ВИЧ-1 V3, с высоким титром, с широкой реактивностью, но низкой нейтрализующей активностью при острой инфекции и после вакцинации. Вирусология. 2009 г.;387:414–426. [Бесплатная статья PMC] [PubMed] [Google Scholar]
16. Kumar R, Tuen M, Liu J, Nadas A, Pan R, Kong X, et al. Выделение широко реагирующих антител против модулированных гликаном нейтрализующих эпитопов V3 ВИЧ-1 с помощью иммунных комплексных вакцин. вакцина. 2013;31:5413–5421. [Бесплатная статья PMC] [PubMed] [Google Scholar]
17. Visciano ML, Tuen M, Gorny MK, Hioe CE. In vivo изменение гуморального ответа на гликопротеин gp120 оболочки ВИЧ-1 антителами к CD4-связывающему сайту gp120. Вирусология. 2008;372:409–420. [Бесплатная статья PMC] [PubMed] [Google Scholar]
18. Zolla-Pazner S, Cohen S, Pinter A, Krachmarov C, Wrin T, Wang S, et al.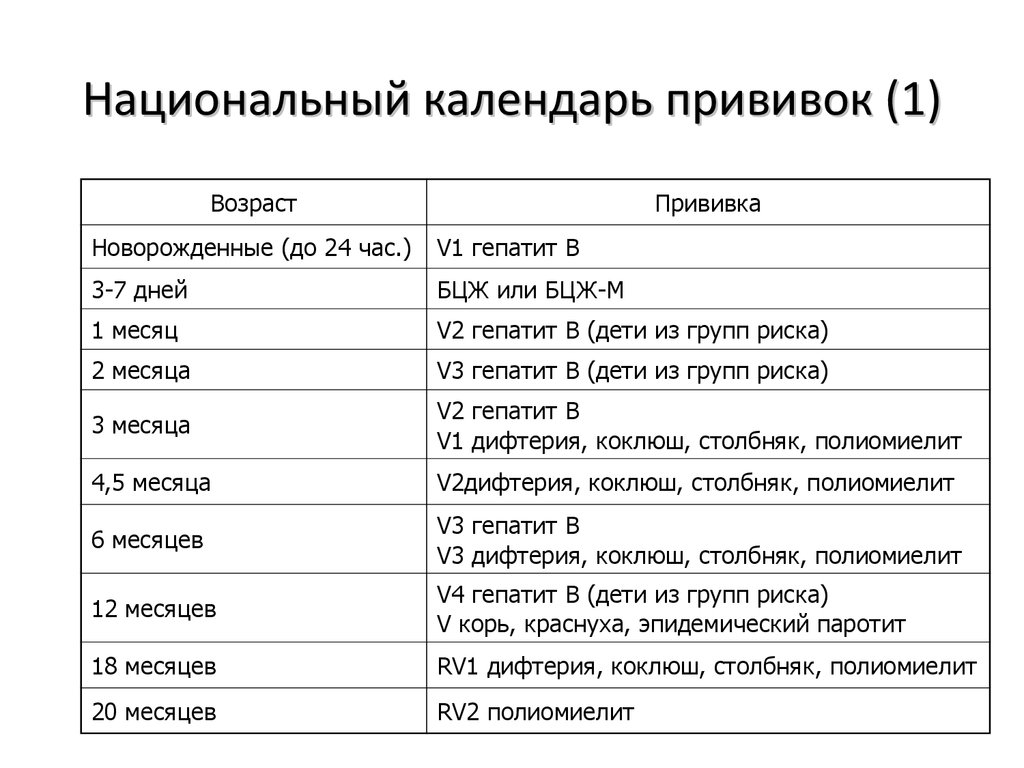 Межклеточные нейтрализующие антитела против ВИЧ-1, индуцированные у кроликов путем фокусировки иммунного ответа на нейтрализующем эпитопе. Вирусология. 2009; 392:82–93. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Межклеточные нейтрализующие антитела против ВИЧ-1, индуцированные у кроликов путем фокусировки иммунного ответа на нейтрализующем эпитопе. Вирусология. 2009; 392:82–93. [Бесплатная статья PMC] [PubMed] [Google Scholar]
19. Hessell AJ, McBurney S, Pandey S, Sutton W, Liu L, Li L, et al. Индукция нейтрализующих антител у макак-резусов с использованием мимотопных пептидов V3. вакцина. 2016;34:2713–2721. [Бесплатная статья PMC] [PubMed] [Google Scholar]
20. Hessell AJ, Malherbe DC, Pissani F, McBurney S, Krebs SJ, Gomes M, et al. Достижение мощного ответа аутологичных нейтрализующих антител против вирусов ВИЧ-1 уровня 2 путем стратегического выбора иммуногенов оболочки. Журнал иммунологии. 2016;196:3064–3078. [Бесплатная статья PMC] [PubMed] [Google Scholar]
21. Шолух А.М., Мухтар М.М., Гумберт М., Эссоно С.С., Уоткинс Д.Д., Вьяс Х.К. и соавт. Выделение моноклональных антител с заданной конформационной специфичностью эпитопа. ПлоС один. 2012;7:e38943. [Бесплатная статья PMC] [PubMed] [Google Scholar]
22. Klein F, Nogueira L, Nishimura Y, Phad G, West AP, Jr, Halper-Stromberg A, et al. Усиленная иммунотерапия ВИЧ-1 с помощью обычно возникающих антител, нацеленных на ускользающие варианты вируса. Журнал экспериментальной медицины. 2014; 211:2361–2372. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Klein F, Nogueira L, Nishimura Y, Phad G, West AP, Jr, Halper-Stromberg A, et al. Усиленная иммунотерапия ВИЧ-1 с помощью обычно возникающих антител, нацеленных на ускользающие варианты вируса. Журнал экспериментальной медицины. 2014; 211:2361–2372. [Бесплатная статья PMC] [PubMed] [Google Scholar]
23. Pan R, Sampson JM, Chen Y, Vaine M, Wang S, Lu S, et al. Кроличьи моноклональные антитела против ВИЧ-1, выработанные в результате иммунизации, могут имитировать способы связывания антигена антител, полученных от ВИЧ-1-инфицированных людей. Журнал вирусологии. 2013;87:10221–10231. [Бесплатная статья PMC] [PubMed] [Google Scholar]
24. Kumar R, Pan R, Upadhyay C, Mayr L, Cohen S, Wang XH, et al. Функциональная и структурная характеристика человеческого V3-специфического моноклонального антитела 2424 с нейтрализующей активностью против ВИЧ-1 JRFL. Журнал вирусологии. 2015;89:9090–9102. [Бесплатная статья PMC] [PubMed] [Google Scholar]
25. Sanders RW, Derking R, Cupo A, Julien JP, Yasmeen A, de Val N, et al. Расщепленный растворимый тример Env ВИЧ-1 нового поколения, BG505 SOSIP.664 gp140, экспрессирует множественные эпитопы для широко нейтрализующих, но не ненейтрализующих антител. Возбудители PLoS. 2013;9:e1003618. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Расщепленный растворимый тример Env ВИЧ-1 нового поколения, BG505 SOSIP.664 gp140, экспрессирует множественные эпитопы для широко нейтрализующих, но не ненейтрализующих антител. Возбудители PLoS. 2013;9:e1003618. [Бесплатная статья PMC] [PubMed] [Google Scholar]
26. Stanfield RL, Gorny MK, Williams C, Zolla-Pazner S, Wilson IA. Структурное обоснование широкой нейтрализации ВИЧ-1 человеческим моноклональным антителом 447-52D. Структура. 2004; 12:193–204. [PubMed] [Google Scholar]
27. Gorny MK, Sampson J, Li H, Jiang X, Totrov M, Wang XH, et al. Моноклональные антитела человека против V3 ВИЧ-1, кодируемые генами лямбда VH5-51/VL, определяют консервативную антигенную структуру. ПлоС один. 2011;6:e27780. [Бесплатная статья PMC] [PubMed] [Google Scholar]
28. Killikelly A, Zhang HT, Spurrier B, Williams C, Gorny MK, Zolla-Pazner S, et al. Термодинамические характеристики антигенсвязывающего сайта mAb 447-52D, нацеленного на третью вариабельную область gp120 ВИЧ-1. Биохимия. 2013;52:6249–6257. [Бесплатная статья PMC] [PubMed] [Google Scholar]
2013;52:6249–6257. [Бесплатная статья PMC] [PubMed] [Google Scholar]
29. Gorny MK, Wang XH, Williams C, Volsky B, Revesz K, Witover B, et al. Предпочтительное использование сегмента гена VH5-51 иммунным ответом человека для кодирования антител против домена V3 ВИЧ-1. Молекулярная иммунология. 2009 г.;46:917–926. [Бесплатная статья PMC] [PubMed] [Google Scholar]
30. Upadhyay C, Mayr LM, Zhang J, Kumar R, Gorny MK, Nadas A, et al. Различные механизмы регулируют экспозицию нейтрализующих эпитопов в петлях V2 и V3 оболочки ВИЧ-1. Журнал вирусологии. 2014;88:12853–12865. [Бесплатная статья PMC] [PubMed] [Google Scholar]
31. Монтефиори, округ Колумбия. Оценка нейтрализующих антител против ВИЧ, SIV и SHIV в анализе репортерного гена люциферазы. В: Колиган Джон Э. и др., Редакторы. Современные протоколы в иммунологии. 2005. Глава 12: Блок 12 1. [PubMed] [Google Scholar]
32. Кумар Р., Туен М., Ли Х., Це Д.Б., Хиое К.Е. Улучшение иммуногенности gp120 оболочки ВИЧ-1 путем удаления гликанов и образования иммунных комплексов. вакцина. 2011;29:9064–9074. [Бесплатная статья PMC] [PubMed] [Google Scholar]
вакцина. 2011;29:9064–9074. [Бесплатная статья PMC] [PubMed] [Google Scholar]
33. Burke V, Williams C, Sukumaran M, Kim SS, Li H, Wang XH, et al. Структурная основа перекрестной реактивности генетически родственных моноклональных антител человека против ВИЧ-1: значение для разработки иммуногенов на основе V3. Структура. 2009; 17: 1538–1546. [Бесплатная статья PMC] [PubMed] [Google Scholar]
34. Gilbert PB, Peterson ML, Follmann D, Hudgens MG, Francis DP, Gurwith M, et al. Корреляция между иммунологическим ответом на вакцину с рекомбинантным гликопротеином 120 и заболеваемостью ВИЧ-1 в 3-й фазе испытания профилактической вакцины против ВИЧ-1. Журнал инфекционных болезней. 2005; 191:666–677. [PubMed] [Google Scholar]
35. Шмелков Э., Надас А., Светнам Дж., Золла-Пазнер С., Кардозо Т. Непрямое обнаружение эпитоп-специфического ответа на иммунизацию gp120 ВИЧ-1 у людей. ПлоС один. 2011;6:e27279. [Бесплатная статья PMC] [PubMed] [Google Scholar]
36. Pitisuttithum P, Gilbert P, Gurwith M, Heyward W, Martin M, van Griensven F, et al. Рандомизированное двойное слепое плацебо-контролируемое исследование эффективности двухвалентной рекомбинантной вакцины против ВИЧ-1 на основе гликопротеина 120 среди потребителей инъекционных наркотиков в Бангкоке, Таиланд. Журнал инфекционных болезней. 2006; 194:1661–1671. [PubMed] [Google Scholar]
Рандомизированное двойное слепое плацебо-контролируемое исследование эффективности двухвалентной рекомбинантной вакцины против ВИЧ-1 на основе гликопротеина 120 среди потребителей инъекционных наркотиков в Бангкоке, Таиланд. Журнал инфекционных болезней. 2006; 194:1661–1671. [PubMed] [Google Scholar]
37. Flynn NM, Forthal DN, Harro CD, Judson FN, Mayer KH, Para MF, et al. Плацебо-контролируемое испытание фазы 3 вакцины на основе рекомбинантного гликопротеина 120 для предотвращения заражения ВИЧ-1. Журнал инфекционных болезней. 2005;191: 654–665. [PubMed] [Google Scholar]
38. Felsovalyi K, Nadas A, Zolla-Pazner S, Cardozo T. Различные образцы последовательности характеризуют область V3 gp120 ВИЧ типа 1 из подтипов A и C. Исследования СПИДа и ретровирусов человека. 2006; 22: 703–708. [PMC free article] [PubMed] [Google Scholar]
39. Stanfield R, Cabezas E, Satterthwait A, Stura E, Profy A, Wilson I. Двойные конформации петли V3 gp120 ВИЧ-1 в комплексах с различными нейтрализующими фабриками . Структура. 1999; 7: 131–142. [PubMed] [Академия Google]
Структура. 1999; 7: 131–142. [PubMed] [Академия Google]
40. Sharon M, Kessler N, Levy R, Zolla-Pazner S, Gorlach M, Anglister J. Альтернативные конформации петель V3 ВИЧ-1 имитируют бета-шпильки в хемокинах, что предполагает механизм избирательности корецепторов. Структура. 2003; 11: 225–236. [PubMed] [Google Scholar]
41. Almond DKT, Kong X, Zolla-Pazner S&, Cardozo T. Динамическая характеристика коронки петли V3. Противовирусная терапия. 2007; 12:13–31. [Google Scholar]
42. Wagh K, Bhattacharya T, Williamson C, Robles A, Bayne M, Garrity J, et al. Оптимальные комбинации широко нейтрализующих антител для профилактики и лечения инфекции ВИЧ-1 Clade C. Возбудители PLoS. 2016;12:e1005520. [Бесплатная статья PMC] [PubMed] [Google Scholar]
43. Kong R, Louder MK, Wagh K, Bailer RT, deCamp A, Greene K, et al. Улучшение эффективности и широты нейтрализации за счет комбинирования широко реагирующих антител к ВИЧ-1, нацеленных на основные эпитопы нейтрализации. Журнал вирусологии. 2015; 89: 2659–2671. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Журнал вирусологии. 2015; 89: 2659–2671. [Бесплатная статья PMC] [PubMed] [Google Scholar]
44. Gautam R, Nishimura Y, Pegu A, Nason MC, Klein F, Gazumyan A, et al. Одна инъекция антител против ВИЧ-1 защищает от повторных заражений SHIV. Природа. 2016; 533:105–109. [Бесплатная статья PMC] [PubMed] [Google Scholar]
45. Saunders KO, Wang L, Joyce MG, Yang ZY, Balazs AB, Cheng C, et al. Широко нейтрализующий перенос гена антитела к вирусу иммунодефицита человека типа 1 защищает нечеловеческих приматов от заражения вирусом иммунодефицита обезьян и человека через слизистые оболочки. Журнал вирусологии. 2015;89:8334–8345. [Бесплатная статья PMC] [PubMed] [Google Scholar]
46. Caskey M, Klein F, Lorenzi JC, Seaman MS, West AP, Jr, Buckley N, et al. Виремия подавляется у людей, инфицированных ВИЧ-1, с помощью широкого нейтрализующего антитела 3BNC117. Природа. 2015; 522: 487–491. [Бесплатная статья PMC] [PubMed] [Google Scholar]
47. Stoddart CA, Galkina SA, Joshi P, Kosikova G, Long BR, Maidji E, et al.


 )
) С 15-ти летнего возраста информированное согласие подростки пишут сами.
С 15-ти летнего возраста информированное согласие подростки пишут сами.