Праздничные дни
Изменения в приеме участков УВАЖАЕМЫЕ РОДИТЕЛИ! Дома, находящиеся по адресу: г.Абакан, ул.Торосова 7; ул.Торосова 7а
с 01.01.2023г. будут обслуживаться у
ДПО №3, кабинет №219, врач-педиатр
Режим работы участка: Понедельник
Вторник
Среда
Четверг
Пятница
Телефон для записи на прием: Call-центр
Изменения в работе Уважаемые родители!
В связи с техническими работами (капитальным
Приемы детского населения 6 и 33
Прием врача педиатра будет осуществляться по
Вызов медицинского работника на дом
Так же заявку на вызов врача можно отправить
Работа в выходные дни Уважаемые родители, в выходные дни наше
В субботу: Дежурный педиатр ведёт приём с 8.00 до 14.00 в отделении по
В
Вызвать медработника на дом можно с 8.00 до 16.00 по
В другое время родители могут обратиться за скорой и неотложной помощью
Стационар продолжает работать в прежнем режиме по адресу ул.
ВНИМАНИЕ❗️
В воскресенье с
Оказание медицинской помощи при укусе клеща
☎️Все
При укусе клеща Уважаемые родители и пациенты! В целях оказания медицинской помощи
— в рабочие дни (понедельник–пятница) на
базе приемного отделения ГБУХ РХ «РДКБ»,
-в выходные и праздничные дни на базе
ул. Чертыгашева, 63, круглосуточно; При наличии показаний, введение
— в рабочие дни в процедурном кабинете 1
-в выходные и праздничные дни введение
Исследование клеща на наличие маркеров
Ремонт поликлинического отделения №1 Уважаемые родители и пациенты! С 24. С уважением администрация ГБУЗ РХ «РДКБ» Вызов на дом Памятка для граждан о действиях в случае
C 02.11.20, проживающие в городе Абакане,
В письме
Заявки принимаются в рабочие дни с
С уважением Администрация ГБУЗ РХ «РДКБ» Объявление Уважаемые родители и пациенты! В период с 27
С уважением, Администрация. Обследование перед поездкой в оздоровительные лагеря Уважаемые родители! Для обследования детей в загородный
для пациентов ДПО 1, 2,4 в с 8.00 до 15.00 , с понедельника по пятницу Выдача справок будет
ДПО 1 и 2 в каб. 210,
Справка действительна
С Уважением Администрация ГБУЗ РХ «РДКБ» Оказание неотложной помощи Уважаемые родители! С уважением, Администрация ГБУЗ РХ «РДКБ». Чек-лист «Коронавирусная инфекция» Уважаемые родители! В целях качественного и быстрого прохождения
С уважением, Администрация. Порядок допуска детей По
1. Допуск детей,
2. Детям, посещающим
— законные
— законному
— в случае
Порядок допуска детей в дежурные группы ДОУ г. Абакана в период
1. Допуск детей,
2. Детям, посещающим
— законные
— законному
— в случае
Рекомендации для населения Праздничные дни Уважаемые родители! Администрация ГБУЗ РХ «Республиканская детская клиническая
13 июня осуществляется прием врача-педиатра по ул.
13 июня работает рентгенологический
12, 13, 14 июня работает процедурный кабинет по
13 июня вызов
12 и 14
Памятка для родителей на период коронавирусной инфекции Внимание Уважаемые родители!
В целях реализации
С уважением, Администрация. Информация о новой короновирусной инфекции Европейская неделя иммунизации 20-26 апреля — Европейская неделя
Что надо знать о коронавирусе Порядок работы кабинетов экстренной профилактики ГБУЗ РХ «РДКБ» (при укусе клеща)
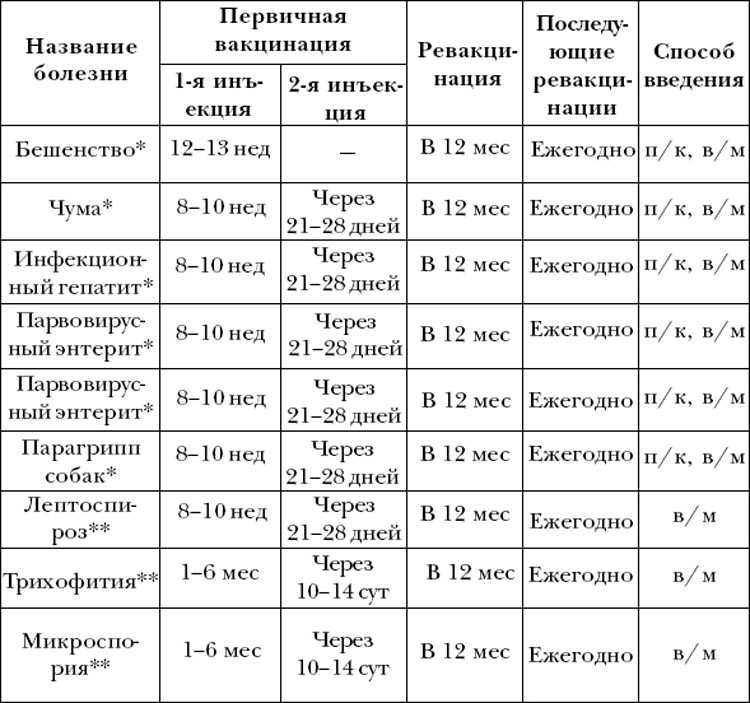
Памятка о гриппе Памятка | |||||||||||
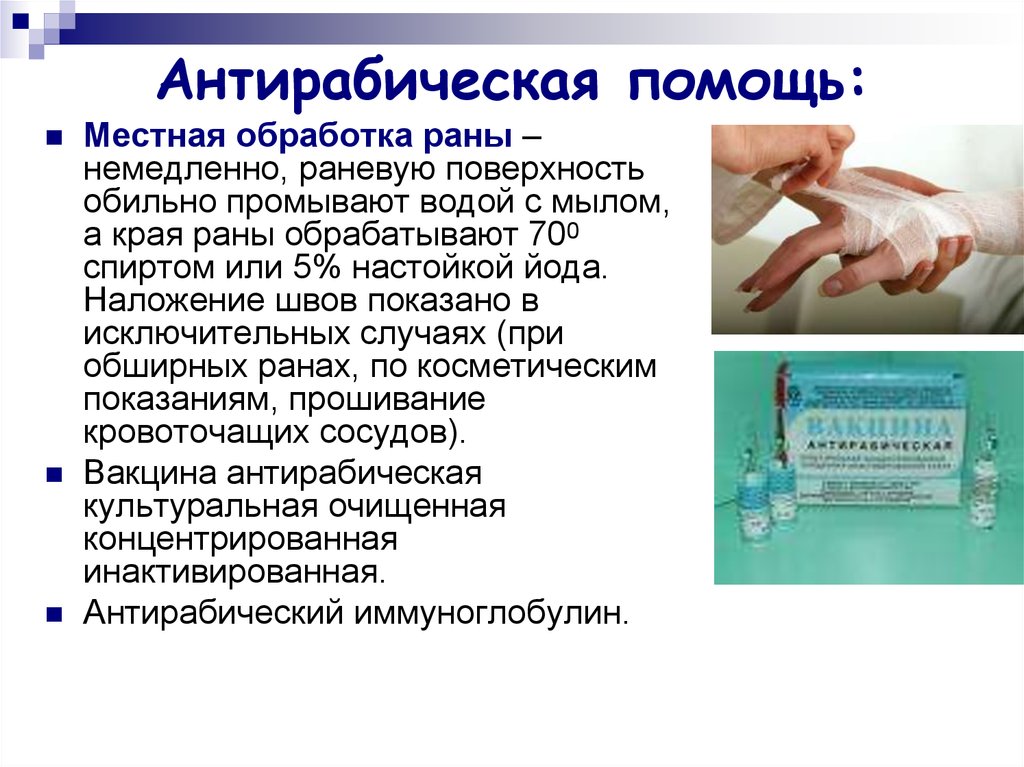
Вакцина против бешенства -Профилактика заболеваний
ВАКЦИНА АНТИРАБИЧЕСКАЯ
(Вакцина антирабическая культуральная концентрированная очищенная инактивированная сухая)
Производитель: Предприятие по производству бактерийных и вирусных препаратов Института полиомиелита и вирусных энцефалитов им.М.П.Чумакова РАМН ФГУП (Россия)
Состав: Одна доза (1,0 мл) вакцины содержит: специфический антиген вируса бешенства штамм «Внуково-32» – не менее 2,5 МЕ (Международных Единиц) – активный компонент, альбумин – 5,0 мг (раствор для инфузий) – стабилизатор, сахарозу – 75,0 мг – стабилизатор, желатин – 10,0 мг – формообразователь. Препарат не содержит консервантов и антибиотиков.
Препарат не содержит консервантов и антибиотиков.
Форма выпуска: Растворенная вакцина представляет собой прозрачную или слабо опалесцирующую жидкость от бесцветного до светло-желтого цвета.
Показания к применению: Лечебно-профилактическая или профилактическая иммунизация человека против бешенства. Лечебно-профилактической иммунизации подлежат все лица, подвергшиеся риску заражения бешенством (в случае контакта и укусов людей больными бешенством животными, животными с подозрением на заболевание бешенством, дикими или неизвестными животными). С профилактической целью иммунизируют лиц, имеющих высокий риск заражения бешенством (сотрудники лабораторий, работающие с уличным вирусом бешенства; ветеринарные работники; егеря, охотники, лесники; лица, выполняющие работы по отлову и содержанию животных и другие профессиональные группы).
Схема вакцинации: Содержимое ампулы с вакциной должно быть растворено в 1,0 мл воды для инъекций. Время растворения не должно превышать 5 мин. Хранение растворенной вакцины более 5 мин не допускается. Вакцинированный должен находиться под медицинским наблюдением не менее 30 мин.
Время растворения не должно превышать 5 мин. Хранение растворенной вакцины более 5 мин не допускается. Вакцинированный должен находиться под медицинским наблюдением не менее 30 мин.
При лечебно-профилактической иммунизации вакцина применяется совместно с антирабическим иммуноглобулином (АИГ). При профилактической иммунизации инъекции проводятся на 0, 7 и 30 день по 1,0 мл (первичная иммунизация). Первая ревакцинация проводится через 1 год. Последующие – каждые 3 года.
Противопоказания для профилактической иммунизации:
– Острые инфекционные и неинфекционные заболевания, хронические заболевания в стадии обострения или декомпенсации – прививки проводят не ранее одного месяца после выздоровления (ремиссии).
– Системные аллергические реакции на предшествующее введение антирабического иммуноглобулина (генерализованная сыпь, отек Квинке и др.).
– Беременность
Противопоказания для лечебно-профилактической иммунизации отсутствуют.
Преимущества:
Данная вакцина является вакциной III поколения. Это – высокоочищенный препарат, являющийся эффективным и безопасным средством, обеспечивающим надежную защиту от заболевания бешенством. Высокое качество концентрированной вакцины позволяет существенно сократить схему полного курса вакцинации – до 6 инъекций и уменьшить разовую прививочную дозу до 1 мл (вместо 21 прививки по 3 мл – при использовании неконцентрированной вакцины).
Опыт применения: Препарат был разработан в 1986 году учеными Института полиомиелита и вирусных энцефалитов и производится из аттенуированного штамма фиксированного вируса бешенства «Внуково-32». За счет высокой степени очистки и освобождения от чужеродных белков вакцина не вызывает побочных реакций. Высокая иммуногенная активность была подтверждена двумя сотрудничающими центрами Вcемирной организации здравоохранения (США и Англии).
КОКАВ
(Вакцина антирабическая культуральная концентрированная очищенная инактивированная).
Производитель: НПО «Микроген» (Россия)
Состав: вакцинный вирус бешенства, штамм «Внуково-32», инактивированный; стабилизаторы: альбумин раствор для инфузий 10%, сахароза, желатин.
Форма выпуска: лиофилизат для приготовления раствора для внутримышечного введения. Растворенная вакцина представляет собой прозрачную или слегка опалесцирующую жидкость от бесцветного до светло-желтого цвета.
Показания к применению: Лечебно-профилактическая и профилактическая иммунизация человека против бешенства.
Схема вакцинации:
Лечебно-профилактическая иммунизация
Показания. Контакт и укусы людей больными бешенством животными, животными с подозрением на заболевание бешенством, дикими или неизвестными животными. Лечебно-профилактической иммунизации подлежат все лица, подвергшиеся риску заражения бешенством. Если имеются показания к комбинированному лечению, то сначала вводится АИГ и, не более чем через 30 мин, после него вводится КОКАВ.
Профилактическая иммунизация
Показания. С профилактической целью иммунизируют лиц, имеющих высокий риск заражения бешенством (сотрудники лабораторий, работающие с уличным вирусом бешенства; ветеринарные работники; егеря, охотники, лесники; лица, выполняющие работы по отлову и содержанию животных и другие профессиональные группы).
Вакцина вводится внутримышечно в дельтовидную мышцу плеча по 1,0 мл в 0, 7 и 30 день. Ревакцинацию проводят однократно, в дозе 1,0 мл через год и далее каждые три года
Противопоказания:
– Острые инфекционные и неинфекционные заболевания, хронические заболевания в стадии обострения или декомпенсации – прививки проводят не ранее одного месяца после выздоровления (ремиссии).
– Системные аллергические реакции на предшествовавшее введение вакцины КОКАВ (генерализованная сыпь, отек Квинке и др.).
– Аллергические реакции на антибиотики.
– Беременность
ВАКЦИНА ОТ БЕШЕНСТВА | Медицинские рекомендации MSF
Скачать
На этой странице
Показания
- Профилактика бешенства после воздействия II и III категорий
Состав, формы, способ введения
- Инактивированная вирусная вакцина, приготовленная из клеточных культур (CCEEV): в эмбриональном яйце или очищенных клетках (эмбриональных клетках кур, Vero-клетках или диплоидных клетках человека)
- Порошок для инъекций во флаконе с монодозой, растворяемом во всем флаконе разбавителя (0,5 мл или 1 мл, поставляется производителем)
- В/м маршрут:
НЕ ВВОДИТЬ В ЯГОДНИЧНУЮ МЫШЦУ.
- Дети младше 2 лет: инъекция в переднебоковую часть бедра
- Детям ≥ 2 лет и взрослым: инъекция в дельтовидную мышцу
- ID маршрута:
- Детям и взрослым: инъекция в дельтовидную мышцу (или переднебоковую часть бедра или надлопаточную область)
Дозировка и схема вакцинации
- Дети и взрослые: одна доза в/м = 0,5 или 1 мл, в зависимости от используемой вакцины; одна доза внутривенно = 0,1 мл, в зависимости от того, какая вакцина использовалась
- Графики вакцинации могут различаться в разных странах, ознакомьтесь с национальными рекомендациями. График зависит от статуса вакцинации пациента на момент заражения и используемого пути введения (следуйте инструкциям производителя).
- Первую дозу вакцины следует вводить как можно скорее после заражения, даже если пациент обращается за медицинской помощью спустя долгое время после контакта (инкубационный период бешенства может длиться несколько месяцев).
 Пациент должен получить все рекомендуемые дозы.
Пациент должен получить все рекомендуемые дозы. - Если введение дозы вакцины задерживается или изменяется способ введения, продолжайте вакцинацию в соответствии с выбранным путем введения и не возобновляйте вакцинацию по графику.
Простейшие схемы вакцинации, одобренные ВОЗ, следующие:
№ вакцинация против бешенства
или неполная вакцинация
или полная вакцинация НТВ
или неизвестно прививочный статус
Полная вакцинация
CCEEV
(а)
Цитата
а.
Существует два возможных графика внутримышечного введения: схема Загреба (2-0-1-0-1) в течение 21 дня или схема Эссена с 4 дозами (1-1-1-1-0) в течение 14–28 дней. .
(б)
Цитата
б.
Другой возможный график интрадермального введения: 4 дозы интрадермального введения (по 1 дозе в каждую руку и по 1 дозе в каждое бедро) в D0.
Д0
2 дозы
(с)
Цитата
в.
А также однократная доза антирабического иммуноглобулина в рану при воздействии III категории на D0.
(по 1 дозе в каждую руку или бедро
)
(с)
Цитата
в.
А также однократная доза антирабического иммуноглобулина в рану при воздействии III категории на D0.
2 дозы
(с)
Цитата
в.
А также однократная доза антирабического иммуноглобулина в рану при воздействии III категории на D0.
(по 1 дозе в каждую руку)
1 доза
Д3
2 дозы
(по 1 дозе в каждую руку)
1 доза
Д7
1 доза
2 дозы
(по 1 дозе в каждую руку)
(г)
Цитата
д.
Последнюю инъекцию можно вводить между 14 и 28 днями.
Д21
1 доза
- Пациент с ослабленным иммунитетом: 1 доза в D0, D7 и между D21 и D28 внутримышечно или внутрикожно (а также однократная доза антирабического иммуноглобулина)
Противопоказания, побочные эффекты, меры предосторожности
- Не применять одновременно с кортикостероидами (снижается эффективность вакцины).
- Может вызывать: доброкачественные местные реакции в месте инъекции (боль, уплотнение), лихорадку, недомогание, головную боль, утомляемость, желудочно-кишечные расстройства; редко: анафилактическая реакция.

- Убедитесь, что вакцина не попала в кровеносный сосуд (риск шока): аспирируйте перед инъекцией, чтобы убедиться, что игла не находится в вене.
- ИД вакцинация: неправильная техника ИД приводит к неэффективности лечения. Если правильный метод идентификации не может быть гарантирован, используйте маршрут обмена мгновенными сообщениями.
- При одновременном введении с антирабическим иммуноглобулином и другими вакцинами используйте разные шприцы и места для инъекций.
- Беременность и кормление грудью : нет противопоказаний
- Вакцину против бешенства применяют также для предэкспозиционной вакцинации лиц с высоким риском заражения (длительное пребывание в эндемичных по бешенству районах, контакт специалистов с животными, восприимчивыми к переносчику вируса).
- Избегайте использования вакцин, приготовленных из нервной ткани животных (НТВ): они менее иммуногенны, чем вакцины CCEEV, и чаще вызывают серьезные побочные эффекты.

Хранение
- Порошок: от 2 °C до 8 °C. Не мерзни.
- Разбавитель: для хранения не требуется холодовая цепь. Однако по крайней мере за 12 часов до разведения вакцины разбавитель необходимо охладить при температуре от 2°C до 8°C, чтобы разбавитель и лиофилизированный порошок имели одинаковую температуру: разница температур во время разведения может снизить эффективность вакцины. Не мерзни.
- Восстановленная вакцина: использовать немедленно.
- (a) Существует два возможных графика внутримышечного введения: схема Загреба (2-0-1-0-1) в течение 21 дня или схема Эссена с 4 дозами (1-1-1-1-0 ) от 14 до 28 дней.
- (b) Другой возможный график интрадермального введения: 4 дозы интрадермального введения (по 1 дозе в каждую руку и по 1 дозе в каждое бедро) в D0.
- (с)
А также однократная доза антирабического иммуноглобулина в рану при воздействии III категории на D0.
- (d) Последняя инъекция может быть введена между 14 и 28 днями.
Позиция ВОЗ в отношении иммунизации против бешенства – обновления 2018 г.
- Список журналов
- Спонсорские документы Elsevier
- PMC6863036
Вакцина. 2019 3 октября; 37 (Приложение 1): A85–A87.
doi: 10.1016/j.vaccine.2018.10.014
, A, ⁎ , B и, от инации Discalf Sage WG на бешенстве
. Бешенство — забытое зоонозное заболевание, от которого ежегодно умирает около 59 000 человек [1]. Преимущественно страдает сельское население в Африке и Азии, и примерно 40% случаев приходится на детей в возрасте до 15 лет. Передается через укусы и царапины от инфицированных животных, собаки несут ответственность за 99% случаев заболевания человека бешенством [2]. Хотя при появлении клинических признаков бешенство может привести к летальному исходу, его можно предотвратить с помощью (i) массовой вакцинации собак для борьбы с болезнью в ее источнике; (ii) осведомленность о бешенстве и необходимость лечения в случае заражения; (iii) своевременная постконтактная профилактика (ПКП) для людей, потенциально подверженных риску заражения бешенством; и (iv) доконтактная профилактика (ДКП) для лиц с высоким риском заражения вирусом бешенства.
Передается через укусы и царапины от инфицированных животных, собаки несут ответственность за 99% случаев заболевания человека бешенством [2]. Хотя при появлении клинических признаков бешенство может привести к летальному исходу, его можно предотвратить с помощью (i) массовой вакцинации собак для борьбы с болезнью в ее источнике; (ii) осведомленность о бешенстве и необходимость лечения в случае заражения; (iii) своевременная постконтактная профилактика (ПКП) для людей, потенциально подверженных риску заражения бешенством; и (iv) доконтактная профилактика (ДКП) для лиц с высоким риском заражения вирусом бешенства.
ПКП вводят после потенциального контакта с вирусом бешенства и включают тщательное промывание раны, серию вакцинаций против бешенства и иногда введение антирабического иммуноглобулина (АИГ) (). RIG могут быть получены из источников лошадиных (eRIG), человеческих (hRIG) или моноклональных антител (mAb) [3]. ДКП состоит из серии прививок от бешенства, которые вводятся до потенциального контакта. ДКП рекомендуется лицам с высоким риском заражения бешенством, например, лицам с профессиональным риском, субпопуляциям в высокоэндемичных условиях, у которых нет доступа к своевременной и адекватной ПКП, а также путешественникам, которые могут подвергаться высокому риску заражения [3]. Хотя ПКП и ДКП можно вводить внутримышечно (в/м) или внутрикожно (в/к), интрадермальная вакцинация является экономичной как по дозе, так и по стоимости [4]. Современные вакцины против бешенства на основе очищенных клеточных культур и яичных эмбрионов обладают высокой иммуногенностью, эффективностью и безопасностью для применения у людей всех возрастов [3].
ДКП рекомендуется лицам с высоким риском заражения бешенством, например, лицам с профессиональным риском, субпопуляциям в высокоэндемичных условиях, у которых нет доступа к своевременной и адекватной ПКП, а также путешественникам, которые могут подвергаться высокому риску заражения [3]. Хотя ПКП и ДКП можно вводить внутримышечно (в/м) или внутрикожно (в/к), интрадермальная вакцинация является экономичной как по дозе, так и по стоимости [4]. Современные вакцины против бешенства на основе очищенных клеточных культур и яичных эмбрионов обладают высокой иммуногенностью, эффективностью и безопасностью для применения у людей всех возрастов [3].
Таблица 1
Категории риска заражения бешенством ВОЗ и показания для ПКП [3].
| ВОЗ Категории бешенства. Экспозиция | PEP Индикации |
|---|---|
Категория I (т.е. отсутствие воздействия): прикосновение или кормление животного. (т.е. воздействие): незначительные царапины или ссадины без кровотечения (т.е. воздействие): незначительные царапины или ссадины без кровотечения | Показана ПКП (только промывание ран и вакцинация) Относиться к категории III, если контакт был с летучей мышью |
| Категория III (т.е. серьезное воздействие): одиночные или множественные чрескожные укусы или царапины, загрязнение слизистой оболочки или поврежденной кожи слюной от облизываний животных, воздействие вследствие прямого контакта с летучие мыши | Показана ПКП (промывание ран, вакцина и АИГ) |
Открыть в отдельном окне
Стратегическая консультативная группа экспертов по иммунизации (SAGE) создала Рабочую группу (РГ) по вакцинам против бешенства и иммуноглобулинам в 2017 г., чтобы провести всесторонний обзор фактических данных и предложить изменения в SAGE по рекомендуемой профилактике бешенства [5], [6]. Это первый набор рекомендаций по иммунизации против бешенства, разработанных в ходе систематического процесса рабочей группы и заменяющий рекомендации 2010 года. Обновление позиции ВОЗ по вакцинам против бешенства от 2018 г. отвечает потребности в более программно осуществимых рекомендациях, направленных на улучшение показателей общественного здравоохранения в отношении бешенства при сохранении самого высокого уровня индивидуальной эффективности [5]. Устраняя несоответствие между предыдущими рекомендациями ВОЗ и текущей практикой использования ПКП и ДКП в эндемичных районах, обновление направлено на рассмотрение самых последних имеющихся данных для улучшения доступа к жизненно важной помощи для уязвимых групп населения. Это включает в себя акцент на улучшении проведения ПКП против бешенства, чтобы лучше удовлетворить потребности недостаточно обслуживаемых групп населения с помощью более коротких, менее дорогостоящих и более осуществимых протоколов ПКП и ДКП, а также для разумного использования АИГ без ущерба для эффективности. Пересмотренная позиция ВОЗ дополняет другие параллельные усилия по предоставлению четких и практических рекомендаций по профилактике бешенства, такие как 3-я консультация экспертов ВОЗ по бешенству [2], текущие обновления диагностического руководства ВОЗ по лабораторным методам при бешенстве и Глобальный стратегический План по прекращению смертности людей от бешенства, передаваемого собаками, к 2030 году [7].
Обновление позиции ВОЗ по вакцинам против бешенства от 2018 г. отвечает потребности в более программно осуществимых рекомендациях, направленных на улучшение показателей общественного здравоохранения в отношении бешенства при сохранении самого высокого уровня индивидуальной эффективности [5]. Устраняя несоответствие между предыдущими рекомендациями ВОЗ и текущей практикой использования ПКП и ДКП в эндемичных районах, обновление направлено на рассмотрение самых последних имеющихся данных для улучшения доступа к жизненно важной помощи для уязвимых групп населения. Это включает в себя акцент на улучшении проведения ПКП против бешенства, чтобы лучше удовлетворить потребности недостаточно обслуживаемых групп населения с помощью более коротких, менее дорогостоящих и более осуществимых протоколов ПКП и ДКП, а также для разумного использования АИГ без ущерба для эффективности. Пересмотренная позиция ВОЗ дополняет другие параллельные усилия по предоставлению четких и практических рекомендаций по профилактике бешенства, такие как 3-я консультация экспертов ВОЗ по бешенству [2], текущие обновления диагностического руководства ВОЗ по лабораторным методам при бешенстве и Глобальный стратегический План по прекращению смертности людей от бешенства, передаваемого собаками, к 2030 году [7].
Основные изменения в позиции ВОЗ по бешенству представлены ниже; документ с изложением позиции по бешенству от 2018 г. содержит подробное описание литературы и рекомендаций [3].
3.1. Резюме обновленных рекомендаций по ПКП и ДКП [3]
Имеющиеся данные показывают, что современные вакцины против бешенства (>2,5 МЕ/внутримышечная доза) при внутрикожном введении для ПКП или ДКП обладают иммуногенностью и эффективностью, эквивалентной или превышающей внутримышечное введение [8]. ]. При внутрикожном введении используется 0,1 мл CCEEV, а при в/м введении используется полный флакон (0,5 мл или 1 мл) для каждой дозы. Вакцины против бешенства и АИГ считаются безопасными для использования у беременных и кормящих женщин, ВИЧ-инфицированных и других лиц с потенциально ослабленным иммунитетом.
Интенсивное промывание раны с мылом, моющим средством и большим количеством воды должно быть выполнено немедленно или как можно скорее при всех укусах, царапинах и обнажениях слизистой оболочки. Ранее рекомендованные ВОЗ схемы вакцинации против бешенства остаются приемлемыми, однако теперь ВОЗ также рекомендует более новые, более короткие схемы вакцинации, которые снижают стоимость, количество вакцины и количество посещений клиники, необходимых как для ПКП, так и для ДКП. Эти новые схемы ПКП для иммунологически наивных лиц (всех возрастных групп) включают (а) внутривенное введение в 2 места в дни 0, 3 и 7 или (б) внутримышечное введение в 1 место в дни 0, 3, 7 и окончательную дозу между 14 днями. –28.
Ранее рекомендованные ВОЗ схемы вакцинации против бешенства остаются приемлемыми, однако теперь ВОЗ также рекомендует более новые, более короткие схемы вакцинации, которые снижают стоимость, количество вакцины и количество посещений клиники, необходимых как для ПКП, так и для ДКП. Эти новые схемы ПКП для иммунологически наивных лиц (всех возрастных групп) включают (а) внутривенное введение в 2 места в дни 0, 3 и 7 или (б) внутримышечное введение в 1 место в дни 0, 3, 7 и окончательную дозу между 14 днями. –28.
RIG показан при воздействии категории III для иммунологически наивных лиц. Независимо от наличия АИГ, все пациенты, подвергшиеся воздействию вакцины категории III, должны быть немедленно вакцинированы против бешенства. АИГ следует вводить только однократно, желательно в начале ПКП и не более чем через 7 дней после введения первой дозы вакцины против бешенства. Кожные пробы перед введением eRIG ненадежны и не должны выполняться. Антирабические mAb, если они доступны, представляют собой потенциальную альтернативу RIG.
Если доступно ограниченное количество АИГ, его назначение должно быть приоритетным для пациентов с высоким риском, воздействие категории III: множественные укусы; люди с глубокими ранами или укусами частей тела с высокой иннервацией, таких как голова, шея и руки; больные с выраженным иммунодефицитом; и случаи, когда укус животного является подтвержденным или вероятным случаем бешенства, или когда укусы, царапины или обнажение слизистой оболочки были вызваны летучей мышью.
АИГ следует инфильтрировать в рану и вокруг нее до максимального расчетного объема 1 . Если раны большие или множественные, максимальный рассчитанный объем АИГ можно развести физиологическим буферным раствором, чтобы обеспечить достаточный объем для полной инфильтрации раны. Напротив, если расчетная доза АИГ больше, чем можно полностью ввести в рану и вокруг нее, ВОЗ больше не рекомендует вводить оставшуюся часть расчетной дозы АИГ в/м в удаленное от раны место. Таким образом, если расчетная доза АИГ 1 , вероятно, слишком велика для местной инфильтрации раны, ее можно разделить на отдельные шприцы меньшего размера, а оставшийся неиспользованный АИГ можно использовать в тот же день для других пациентов, если хранить и обращаться с ним асептически.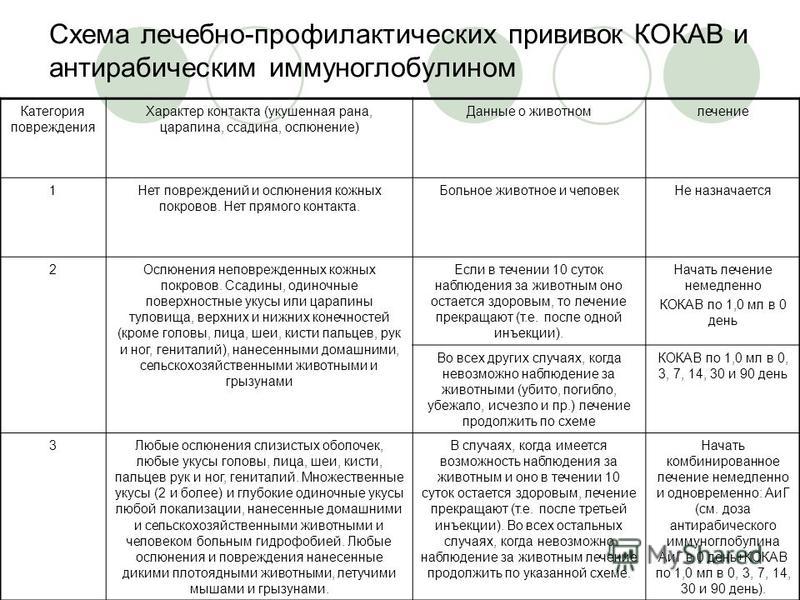 Неиспользованный фракционированный АИГ следует утилизировать в конце дня.
Неиспользованный фракционированный АИГ следует утилизировать в конце дня.
ДКП следует рассматривать только для лиц с высоким риском заражения бешенством (см. документ с изложением позиции) [3]. Лица с документально подтвержденным предыдущим введением вакцины против бешенства или по крайней мере 2 предыдущими введениями вакцины против бешенства в качестве ПКП считаются ранее иммунизированными, и в случае заражения им может быть полезна сокращенная ПКП без АИГ. Схемы ДКП, которые в настоящее время рекомендуются для людей всех возрастных групп: (а) 2-местная инъекция в дни 0 и 7 или (б) 1-место в/м в дни 0 и 7.
3.2. Будущие исследования вакцин против бешенства нуждаются в
Процесс обзора рабочей группы по бешенству выявил пробелы в методологических рекомендациях по оценке не меньшей эффективности новых схем ПКП и ДКП против бешенства, факторов, определяющих клинические исходы у лиц с ослабленным иммунитетом, и передовой практики, основанной на фактических данных, для повторных контактов.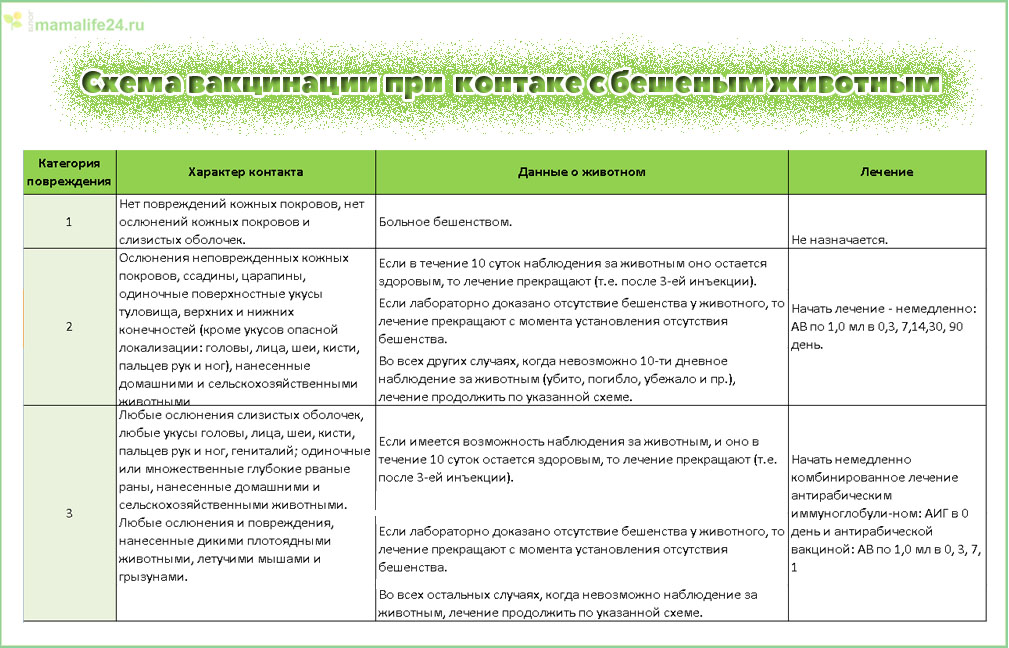 Он подчеркнул необходимость в новых вакцинах с улучшенной термостабильностью, увеличенным сроком хранения и уменьшенным объемом упаковки; и новые инструменты для улучшения доставки на уровне сообщества; и вакцины с улучшенными профилями, которые будут защищать от лиссавирусов, отличных от вируса бешенства. Необходимы дополнительные доказательства возможности еще более коротких схем ПКП и ДКП, таких как ДКП за один визит в условиях, эндемичных по бешенству (включая особые группы населения).
Он подчеркнул необходимость в новых вакцинах с улучшенной термостабильностью, увеличенным сроком хранения и уменьшенным объемом упаковки; и новые инструменты для улучшения доставки на уровне сообщества; и вакцины с улучшенными профилями, которые будут защищать от лиссавирусов, отличных от вируса бешенства. Необходимы дополнительные доказательства возможности еще более коротких схем ПКП и ДКП, таких как ДКП за один визит в условиях, эндемичных по бешенству (включая особые группы населения).
В целом, пересмотренные рекомендации сделают схемы вакцинации против бешенства более эффективными, позволяя использовать более короткие, экономичные и экономичные схемы инъекционной вакцинации, а также уменьшая потребность в АИГ () [9]. Теперь задача состоит в том, чтобы страны и сообщества внедрили эти изменения, чтобы улучшить доступ к жизненно важной ПКП и снизить бремя этого смертельного заболевания.
Таблица 2
Обзор основных изменений в обновлении 2018 г. документа с изложением позиции ВОЗ в отношении вакцин против бешенства.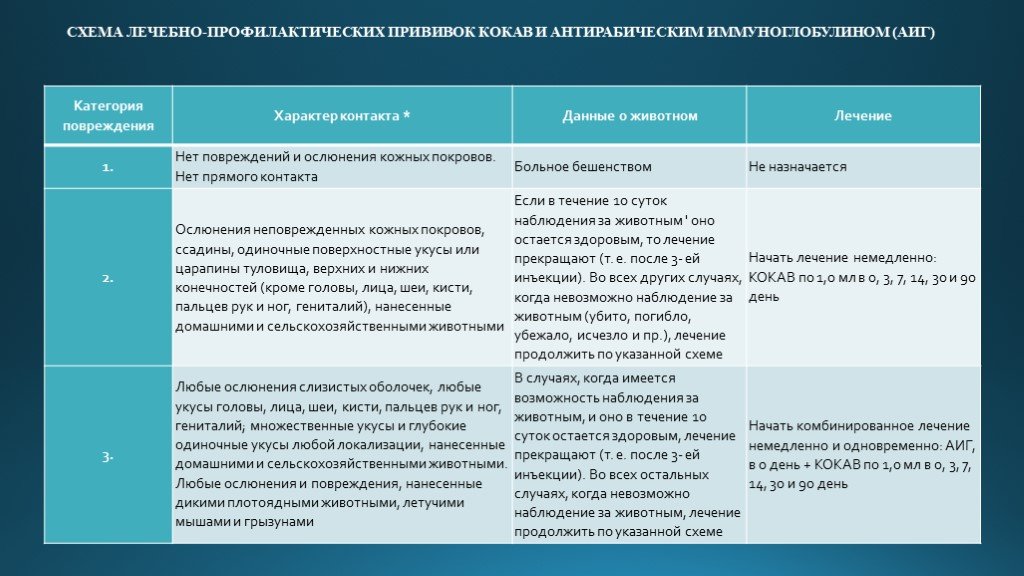
| Тема | 2010 Position Paper | 2018 Position Paper | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Режим PEP | 3–4weeks 4–5 визитов | 3–4weeks 4–5 визитов | 3–4weeks 4–5 Visits | 3–4weeks 4–5 визитов | | 3–4weeks | 4–5 визитов 3–4weeks | 4–5. Продолжительность режима подготовки 3–4weeks | 3 Посещения 1WEEK | 2 Посещения Доза вакцины | ID: 0,8 мл | IM: 5ML ID: 0,8 мл | IM: 5ML ID: 0,8ML | IM: 5ML . |  Режим инфильтрации RIG | Полный расчетный объем в ране и вокруг нее. Остаточный объем внутримышечно, на удаленном участке. | Только внутри и вокруг раны, до максимального расчетного объема. Нет администрирования IM. | Распределение RIG | Все воздействия категории III | Воздействия категории высокого риска III | |
Открыть в отдельном окне облегчение и доступ к ПКП и ДКП от бешенства. Производителям вакцин настоятельно рекомендуется подавать заявку на изменение лицензии в национальные регулирующие органы для включения на этикетке внутрикожного введения и рекомендованных ВОЗ графиков использования в качестве разрешенного использования.
Кроме того, поощряется разработка, лицензирование и использование продуктов mAb в качестве альтернативы eRIG или hRIG, поскольку mAb могут производиться стандартного качества в больших количествах, в производственном процессе не используются животные и они обладают более высокой эффективностью и снижение риска нежелательных явлений. На сегодняшний день в 2017 г. лицензирован один продукт mAb [5]. Было бы полезно разработать продукты, содержащие два или более mAb с неперекрывающимися эпитопами. Кроме того, ВОЗ рекомендует вести реестр для мониторинга эффективности продуктов mAb после лицензирования.
На сегодняшний день в 2017 г. лицензирован один продукт mAb [5]. Было бы полезно разработать продукты, содержащие два или более mAb с неперекрывающимися эпитопами. Кроме того, ВОЗ рекомендует вести реестр для мониторинга эффективности продуктов mAb после лицензирования.
Обновление позиции ВОЗ в отношении иммунизации против бешенства за 2018 г. является важным шагом на пути к улучшению результатов общественного здравоохранения в отношении бешенства, повышению справедливости в отношении здоровья и, в конечном счете, к достижению глобальной цели по нулевой смертности людей от бешенства к 2030 г. во всем мире. Теперь перед странами стоит задача реализовать эти рекомендации для спасения жизней и содействия более широким усилиям по устранению смертности от этого заболевания, которое можно предотвратить с помощью вакцин.
Авторы хотели бы поблагодарить всех членов рабочей группы SAGE по бешенству и отдельных лиц, которые активно участвовали в обсуждении вакцин против бешенства в SAGE.
D Закрытие конфликта интересов
KLOB имеет гранты на исследования, не связанные с бешенством, от GSK и Pfizer. Она работает в составе внешних экспертных консультативных групп, не связанных с бешенством, в компаниях Merck и санофи Пастер.
1 Максимальная доза RIG составляет 40 МЕ/кг массы тела для лошадиных RIG и продуктов F(ab)’2 и 20 МЕ/кг массы тела для человека RIG.
1. Хэмпсон К., Кудевиль Л., Лембо Т., Самбо М., Киффер А., Атлан М. Глобальный альянс партнеров по борьбе с бешенством для профилактики бешенства. Оценка глобального бремени эндемического собачьего бешенства. PLoS Negl Trop Dis. 2015;9(4) [Бесплатная статья PMC] [PubMed] [Google Scholar]
2. ВОЗ. Консультация экспертов ВОЗ по бешенству, третий отчет: Отчет ВОЗ № 1012 из технической серии. Женева; 2018. ISBN 978-92-4-121021-8.
3. ВОЗ. Вакцины против бешенства: позиционный документ ВОЗ – апрель 2018 г. Еженедельный эпидемиологический бюллетень, № 16; 2018, 93.

 01.-
01.-
 Чертыгашева 59, корпус № 3, кабинет № 325, в
Чертыгашева 59, корпус № 3, кабинет № 325, в
 С.
С.

 Чертыгашева, 59, с 08-00 до 16-00, с 16-00 до 08-00 на
Чертыгашева, 59, с 08-00 до 16-00, с 16-00 до 08-00 на 01.2022 прием врачей-
01.2022 прием врачей-
 00.
00. 132, с 8 до 12
132, с 8 до 12




 Абакан, ул. Чертыгашева, 63)
Абакан, ул. Чертыгашева, 63)
 Пациент должен получить все рекомендуемые дозы.
Пациент должен получить все рекомендуемые дозы.