Содержание
Реактивация рубцов после прививки БЦЖ после вакцинации мРНК-Covid-вакциной: два сообщения о случаях заболевания
- Список журналов
- BMC заражает дис
- т.21; 2021
- PMC8685493
BMC Infect Dis. 2021; 21: 1264.
Published online 2021 Dec 20. doi: 10.1186/s12879-021-06949-0
, 1 , 2 , 2 , 3 , 4, 5 , 2, 6 и 1
Авторская информация Примечания Примечания к общению и получению лицензий. работники (HCW) из датских больниц в рандомизированном исследовании, оценивающем, обеспечивает ли Bacille Calmette-Guérin (BCG) защиту от COVID-19. Участники были рандомизированы в соотношении 1:1 к БЦЖ и физиологическому раствору и наблюдались в течение 6 месяцев. С декабря 2020 года медработникам предлагались вакцины против Covid-19. В большинстве случаев после прививки БЦЖ остается характерный рубец. Реактивация рубца БЦЖ была описана у детей во время вирусных инфекций и после вакцинации против гриппа, но в основном она связана с болезнью Кавасаки, заболеванием с патогенезом, вероятно, сходным с детским осложнением Covid-19 MIS-C: мультисистемный воспалительный синдром. Реактивация рубцов после неонатальной вакцинации БЦЖ недавно была описана у четырех женщин после Covid-19.мРНК вакцинация. У двух участников нашего исследования наблюдалась реактивация их новых рубцов БЦЖ после вакцинации мРНК Covid-19 через 6–8 месяцев после БЦЖ.
Участники были рандомизированы в соотношении 1:1 к БЦЖ и физиологическому раствору и наблюдались в течение 6 месяцев. С декабря 2020 года медработникам предлагались вакцины против Covid-19. В большинстве случаев после прививки БЦЖ остается характерный рубец. Реактивация рубца БЦЖ была описана у детей во время вирусных инфекций и после вакцинации против гриппа, но в основном она связана с болезнью Кавасаки, заболеванием с патогенезом, вероятно, сходным с детским осложнением Covid-19 MIS-C: мультисистемный воспалительный синдром. Реактивация рубцов после неонатальной вакцинации БЦЖ недавно была описана у четырех женщин после Covid-19.мРНК вакцинация. У двух участников нашего исследования наблюдалась реактивация их новых рубцов БЦЖ после вакцинации мРНК Covid-19 через 6–8 месяцев после БЦЖ.
Клинические случаи
Две женщины-медики, которые были случайным образом распределены для получения БЦЖ в исследовании БЦЖ-ДАНИЯ-COVID, спонтанно сообщили о зуде и секреции в месте рубца БЦЖ после вакцинации мРНК Covid-19 (Moderna и Pfizer-BioNTech ) через 6–8 месяцев после включения и вакцинации БЦЖ. Один участник, у которого была более выраженная кожная реакция БЦЖ, заметил повторное появление симптомов как после первой, так и после второй дозы вакцины против COVID, в то время как другой участник отметил симптомы только после второй дозы. Оба были вакцинированы БЦЖ в детстве, и в более старых шрамах не было отмечено реактивации. Никакого лечения не требовалось и не проводилось.
Один участник, у которого была более выраженная кожная реакция БЦЖ, заметил повторное появление симптомов как после первой, так и после второй дозы вакцины против COVID, в то время как другой участник отметил симптомы только после второй дозы. Оба были вакцинированы БЦЖ в детстве, и в более старых шрамах не было отмечено реактивации. Никакого лечения не требовалось и не проводилось.
Выводы
Реактивация рубца БЦЖ после введения мРНК-вакцины могла быть вызвана перекрестной реактивностью между БЦЖ и SARS-CoV-2. В обоих случаях симптомы были неприятными, но проходили сами по себе и не оставляли последствий. Таким образом, риск реактивации в месте рубца не является причиной для отказа от вакцинации какой-либо из вакцин.
Ключевые слова: БЦЖ, мРНК вакцинация против Covid-19, перекрестная реакция, клинический случай
Вакцины предназначены для обеспечения защиты от определенного микроорганизма, вызывая защитный иммунитет против определенного заболевания. Ряд обсервационных исследований и рандомизированных контролируемых испытаний показывают, что, кроме того, некоторые вакцины могут вызывать положительные неспецифические эффекты, повышая способность иммунной системы справляться с гетерологичными патогенами. Продолжаются клинические испытания, чтобы проверить, могут ли вакцины с известными полезными неспецифическими эффектами служить временными вакцинами против коронавирусной болезни 2019 г.(COVID-19). Одной из исследуемых вакцин является Bacille Calmette-Guérin (BCG), живой аттенуированный штамм Mycobacterium bovis , используемый против туберкулеза (ТБ).
Ряд обсервационных исследований и рандомизированных контролируемых испытаний показывают, что, кроме того, некоторые вакцины могут вызывать положительные неспецифические эффекты, повышая способность иммунной системы справляться с гетерологичными патогенами. Продолжаются клинические испытания, чтобы проверить, могут ли вакцины с известными полезными неспецифическими эффектами служить временными вакцинами против коронавирусной болезни 2019 г.(COVID-19). Одной из исследуемых вакцин является Bacille Calmette-Guérin (BCG), живой аттенуированный штамм Mycobacterium bovis , используемый против туберкулеза (ТБ).
В большинстве стран, где туберкулез все еще является проблемой общественного здравоохранения, БЦЖ рекомендуется всем новорожденным при рождении или как можно раньше после этого. В странах с низкой заболеваемостью туберкулезом, как, например, в Дании, вакцина БЦЖ вводится только группам высокого риска. До 97% людей, получающих вакцину БЦЖ, испытывают кожную реакцию в месте инъекции через 2–4 недели после вакцинации [1, 2]. Реакция заживает в течение 2–5 месяцев. В большинстве случаев прививка оставляет рубец диаметром около пяти мм. Обсервационные исследования и рандомизированные контролируемые исследования показывают, что вакцинация БЦЖ при рождении связана со снижением неонатальной смертности на 30-50% [3, 4]. БЦЖ индуцирует защиту от инфекций, таких как сепсис и респираторные инфекции [4, 5].
Реакция заживает в течение 2–5 месяцев. В большинстве случаев прививка оставляет рубец диаметром около пяти мм. Обсервационные исследования и рандомизированные контролируемые исследования показывают, что вакцинация БЦЖ при рождении связана со снижением неонатальной смертности на 30-50% [3, 4]. БЦЖ индуцирует защиту от инфекций, таких как сепсис и респираторные инфекции [4, 5].
Основываясь на этих выводах, в настоящее время во всем мире проводится более 20 испытаний, чтобы проверить, может ли вакцинация БЦЖ обеспечить полную или частичную защиту от заражения Covid-19. Одним из них является исследование BCG-DENMARK-COVID ({«type»:»clinical-trial»,»attrs»:{«text»:»NCT04373291″,»term_id»:»NCT04373291″}}NCT04373291), которое от С мая 2020 г. по январь 2021 г. было зачислено 1233 медицинских работника (HCW) в девять датских больниц [6]. Участники были рандомизированы 1:1 для получения стандартной дозы БЦЖ-Дания или физиологического раствора путем внутрикожного введения в правую дельтовидную область, чтобы отличить любую реакцию или образование рубца от предыдущей иммунизации БЦЖ, которую традиционно вводят в левую дельтовидную область. За участниками следили в течение 6 месяцев с еженедельными анкетами о симптомах и прогулах на работе.
За участниками следили в течение 6 месяцев с еженедельными анкетами о симптомах и прогулах на работе.
Специфические вакцины против COVID-19 были разработаны с беспрецедентной скоростью и с 27 декабря 2020 года переданы медработникам, работающим в датских больницах. Таким образом, многие участники получили или получат вакцины против Covid-19 во время последующего наблюдения. Два участвовавших медработника, рандомизированных для получения БЦЖ, сообщили о повторяющихся симптомах на месте рубца БЦЖ после введения мРНК вакцин против Covid-19.
Случай 1
53-летняя участница исследования БЦЖ-ДАНИЯ-COVID была включена в исследование в начале июня 2020 года и рандомизирована для получения БЦЖ, которую вводили внутрикожно в правую дельтовидную область. Затем последовала довольно сильная местная кожная реакция на вакцину с прозрачными желтоватыми серозными выделениями из места инъекции, продолжавшаяся от 4 до 5 месяцев. Кроме того, были отмечены опухшие и болезненные лимфатические узлы в подмышечной впадине на вакцинированной стороне. Симптомы лимфатических узлов привели к тому, что в январе 2021 года ее обследовали на предмет рака груди. Участница была вакцинирована БЦЖ в детстве при поступлении в школу, и во время процедуры включения в исследование на ее правом плече был отмечен шрам от детской вакцинации. По словам ее матери, она также сильно отреагировала на прививку БЦЖ в детстве. Насколько ей (и ее матери) известно, она никогда не болела туберкулезом. Участник здоров и не принимает лекарств.
Симптомы лимфатических узлов привели к тому, что в январе 2021 года ее обследовали на предмет рака груди. Участница была вакцинирована БЦЖ в детстве при поступлении в школу, и во время процедуры включения в исследование на ее правом плече был отмечен шрам от детской вакцинации. По словам ее матери, она также сильно отреагировала на прививку БЦЖ в детстве. Насколько ей (и ее матери) известно, она никогда не болела туберкулезом. Участник здоров и не принимает лекарств.
К концу января 2021 года ей сделали первую прививку Moderna Covid-19 в левую руку. За время наблюдения других вакцин она не получала. Участник отреагировал на вакцину Covid-19 лихорадкой, мышечной болью и сильной местной реакцией (участок покраснел и воспалился), которая прошла в течение нескольких дней. Через один-два дня после вакцинации рубец в месте пробной вакцинации БЦЖ начал чесаться, и у нее возобновились выделения из этого места, а лимфатические узлы стали более болезненными. Зуд и выделения держались неделю.
Через три недели ей сделали вторую прививку Модерна, после чего она снова почувствовала себя плохо. Кроме того, на этот раз место введения БЦЖ начало чесаться на следующий день. Других симптомов не было, выделения из рубца БЦЖ не появлялись. Зуд длился 2 недели. Никакого лечения не требовалось и не проводилось. Опять же, она не заметила симптомов от детского рубца БЦЖ.
Случай 2
49-летняя участница была включена и рандомизирована в группу БЦЖ в июне 2020 г. Вакцину вводили внутрикожно в правую дельтовидную область. Она не знала, что в детстве делала прививку БЦЖ. Однако, когда ее включили в исследование, на правой руке был отмечен шрам от БЦЖ. В октябре 2020 г. ей сделали прививку от гриппа (Ваксигриптетра®). Реакции на пробный рубец БЦЖ не отмечено. Участница ежедневно принимает омепразол для лечения гастроэзофагеальной рефлюксной болезни и левоцетиризин (Xyzal®) для лечения хронической крапивницы.
В конце декабря 2020 года она получила вакцину Pfizer-BioNTech Covid-19 в левую руку без какой-либо последующей реакции ни на одном из участков рубца БЦЖ. После второй дозы вакцины Pfizer-BioNTech в конце января 2021 года, также в левой руке, она отметила зуд, прозрачную желтоватую секрецию и небольшое кровотечение из места рубца БЦЖ на правой руке. У нее не было опухших лимфатических узлов. Симптомы продолжались в течение 2 недель и разрешились без лечения. Реакции на месте шрама от детской БЦЖ не было. Никаких других симптомов после вакцины Pfizer-BioNTech у нее не было.
После второй дозы вакцины Pfizer-BioNTech в конце января 2021 года, также в левой руке, она отметила зуд, прозрачную желтоватую секрецию и небольшое кровотечение из места рубца БЦЖ на правой руке. У нее не было опухших лимфатических узлов. Симптомы продолжались в течение 2 недель и разрешились без лечения. Реакции на месте шрама от детской БЦЖ не было. Никаких других симптомов после вакцины Pfizer-BioNTech у нее не было.
После введения вакцин мРНК Covid-19 у двух медработников, которые недавно были вакцинированы БЦЖ в рамках исследования БЦЖ-ДАНИЯ-COVID, произошла реактивация в месте введения экспериментальных вакцин БЦЖ, введенных 6–8 месяцами ранее. Реактивации шрамов от БЦЖ у детей не было. Участник, наиболее сильно отреагировавший после вакцинации БЦЖ как в детстве, так и при включении в исследование БЦЖ-ДАНИЯ-COVID, уже после первого заражения Covid-19 испытывал симптомы на месте рубца БЦЖ.вакцинации, тогда как участник, у которого были только умеренные симптомы после прививки БЦЖ 6 месяцев назад, отметил реактивацию только после второй инъекции.
Ранее сообщалось о реактивации рубцов БЦЖ после вакцинации против гриппа [7, 8], но у участника, получившего вакцину против гриппа за 2 месяца до вакцинации против Covid-19, таких реакций не наблюдалось.
В двух недавних сообщениях описывались сходные реакции в рубцах после вакцинации БЦЖ у новорожденных у четырех медицинских работников в возрасте от 28 до 45 лет после мРНК Covid-19.вакцины [9, 10]. Реактивация рубцов БЦЖ описана также при вирусных инфекциях у детей, например, при кори и вирусе герпеса человека 6-го типа [11–13]. Однако реактивация рубцов БЦЖ в основном была связана с болезнью Кавасаки (БК), а местные реакции, такие как эритема и уплотнение в месте рубца БЦЖ, даже предлагались в качестве диагностического инструмента при диагностике БК [14]. В исследовании, проведенном в Сингапуре, где всем новорожденным вводят БЦЖ, сообщается, что у 43% пациентов с БЦЖ развилась реактивация в месте рубца БЦЖ, чаще всего у самых маленьких детей [13]. Исследование показало, что более высокая распространенность среди самых маленьких детей была связана с более коротким периодом времени между прививкой БЦЖ и началом БК, а не с возрастом как таковым [13]. Это может объяснить, почему мы наблюдали реактивацию только в самых последних шрамах БЦЖ.
Это может объяснить, почему мы наблюдали реактивацию только в самых последних шрамах БЦЖ.
Интересно, что было выявлено новое педиатрическое заболевание, связанное с Covid-19, называемое мультисистемным воспалительным синдромом у детей (MIS-C), с патогенезом и клиническими проявлениями, сходными с БК [15]. Тот факт, что COVID-19 может вызывать MIS-C, что MIS-C напоминает KD, а KD связан с реактивацией БЦЖ, указывает на некоторую степень общей этиологии. Патофизиология MIS-C до сих пор неизвестна [15]. MIS-C в основном был диагностирован в странах с высоким уровнем дохода, где БЦЖ не используется широко, и, насколько нам известно, у детей, страдающих MIS-C, не было зарегистрировано реактивации рубцов БЦЖ. Однако это, вероятно, связано с редкостью MIS-C и низкой эпидемиологической вероятностью того, что это произойдет у ребенка, вакцинированного БЦЖ. С другой стороны, на основании имеющихся данных можно ожидать реактивации рубца БЦЖ у детей с MIS-C в странах, где БЦЖ используется рутинно.
Было показано, что живые организмы БЦЖ остаются у мышей, вакцинированных БЦЖ, до 5 месяцев [16], и их культивируют у детей, рожденных от ВИЧ-позитивных матерей, через 9 лет после введения БЦЖ при рождении [17]. Однако маловероятно, что изменения, наблюдаемые в двух случаях, связаны с живыми бактериями БЦЖ. Таким образом, более вероятно, что местная реакция была вызвана перекрестной реактивностью между микробными компонентами БЦЖ, сохраняющимися в месте вакцинации, и вакцинами против SARS-CoV-2. Анализ in silico показал, что вакцина БЦЖ может генерировать перекрестно-реактивные Т-клетки против SARS-CoV-2 [18]. В подтверждение этого вывода недавно были идентифицированы восемь пептидов, полученных из БЦЖ, со значительной гомологией последовательностей с пептидами, полученными либо из неструктурного белка 3 (NSP3), либо из неструктурного белка 13 (NSP13) SARS-CoV-2 [19].]. Интересно, что человеческие CD4+ и CD8+ T-клетки, примированные пептидом, полученным из БЦЖ, проявляли повышенную реактивность по отношению к соответствующему пептиду, полученному из SARS-CoV-2, что подтверждает гипотезу о том, что вакцинация БЦЖ индуцирует перекрестно-реактивные Т-клеточные ответы, специфичные для SARS-CoV-2 [19]. ]. Кроме того, высокая гомология белка оболочки SARS-CoV-2 с консенсусным белком LytR C, уникальным для Mycobacteria , указывает на то, что вакцинация БЦЖ индуцирует специфический иммунитет против SARS CoV-2, который нацелен на белок оболочки вируса, необходимый для инфекционности. 20]. Таким образом, реактивация рубца БЦЖ у двух медработников после введения мРНК-вакцины могла быть вызвана иммунологической реакцией из-за перекрестной реактивности между БЦЖ и SARS-CoV-2.
]. Кроме того, высокая гомология белка оболочки SARS-CoV-2 с консенсусным белком LytR C, уникальным для Mycobacteria , указывает на то, что вакцинация БЦЖ индуцирует специфический иммунитет против SARS CoV-2, который нацелен на белок оболочки вируса, необходимый для инфекционности. 20]. Таким образом, реактивация рубца БЦЖ у двух медработников после введения мРНК-вакцины могла быть вызвана иммунологической реакцией из-за перекрестной реактивности между БЦЖ и SARS-CoV-2.
В исследовании BCG-DENMARK-COVID 614 медработников были рандомизированы для получения БЦЖ. Два участника сообщили о реактивации рубца БЦЖ после вакцинации против Covid-19. В обоих случаях симптомы были раздражающими, но самоограничивающимися и не оставляли последствий. Оба участника были рады внести свой вклад в испытание и были бы рады участвовать в подобных испытаниях в будущем. В нашем случае один участник почувствовал, что ее общее состояние здоровья улучшилось по сравнению с состоянием до испытания, тогда как участник из второго случая почувствовал, что ее общее состояние не изменилось.
Ограничение зарегистрированных случаев заключается в том, что не проводилось никаких тестов для выяснения патогенеза, вызывающего симптомы. Тем не менее, два участника испытали симптомы до такой степени, что они спонтанно сообщили о них, поэтому для клиницистов важно знать о возможности наблюдения подобных реакций, а также представляется целесообразным предупредить врачей о том факте, что реактивация рубца БЦЖ может быть индикатор МИС-Ц. Тем не менее, нет причин избегать вакцинации любой из мРНК Covid-19.вакцина.
Неприменимо.
| BCG | Bacillus Calmette-Guérin |
| Covid-19 | Coronavirus disease 2019 |
| HCW | Health care workers |
| KD | Kawasaki disease |
| MIS- C | Мультисистемный воспалительный синдром у детей |
| Туберкулез | Туберкулез |
LM и P-EK придумали идею и составили рукопись.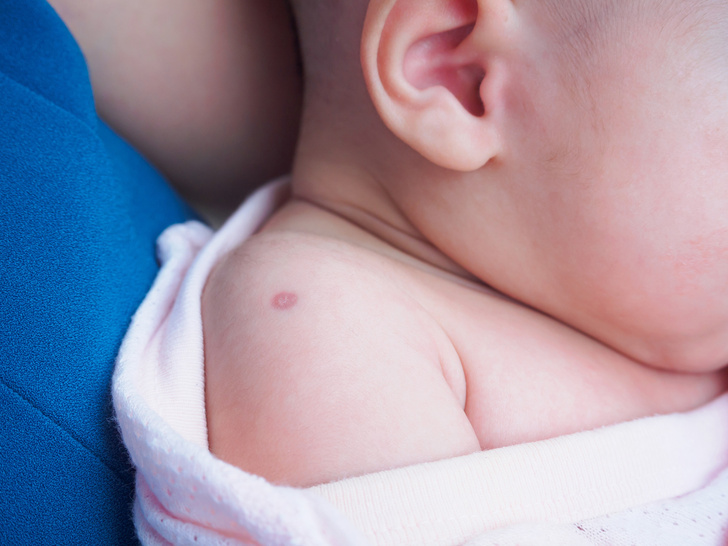 AMRM способствовал сбору историй болезни. LM, PK, AMRM, FSB, AO, MGN и CSB внесли свой вклад в пересмотр рукописи. Все авторы читали и одобрили окончательный вариант рукописи.
AMRM способствовал сбору историй болезни. LM, PK, AMRM, FSB, AO, MGN и CSB внесли свой вклад в пересмотр рукописи. Все авторы читали и одобрили окончательный вариант рукописи.
Для этого отчета не было получено финансирования.
Все данные содержатся в рукописи.
Одобрение этики и согласие на участие
Неприменимо.
Согласие на публикацию
От обоих пациентов было получено письменное информированное согласие на публикацию данного клинического случая.
Конкурирующие интересы
Авторы заявляют об отсутствии конкурирующих интересов.
Примечание издателя
Springer Nature остается нейтральной в отношении юрисдикционных претензий в опубликованных картах и институциональной принадлежности.
Либин Мохамед, электронная почта: moc.liamtoh@nisaqnibiL.
Пол-Эрик Кофоед, электронная почта: kd.dysr@deofok. kire.luop.
kire.luop.
1. Roth A, et al. Шрам от вакцинации БЦЖ связан с лучшей выживаемостью детей в Гвинее-Бисау. Int J Эпидемиол. 2005;34(3):540–547. дои: 10.1093/ije/dyh492. [PubMed] [CrossRef] [Google Scholar]
2. Schaltz-Buchholzer F, et al. Кожные реакции БЦЖ в возрасте 2 месяцев связаны с лучшей выживаемостью в младенчестве: проспективное обсервационное исследование в Гвинее-Бисау. BMJ Глоб Здоровье. 2020;5(9):e002993. doi: 10.1136/bmjgh-2020-002993. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
3. Higgins JP, et al. Ассоциация вакцин, содержащих БЦЖ, АКДС и корь, с детской смертностью: систематический обзор. бмж. 2016;355:i5170. doi: 10.1136/bmj.i5170. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
4. Biering-Sørensen S, et al. Раннее БЦЖ-Дания и неонатальная смертность среди детей с массой тела <2500 г: рандомизированное контролируемое исследование. Клин Инфекция Дис. 2017;65(7):1183–1190. doi: 10.1093/cid/cix525. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
5. Schaltz-Buchholzer F, et al. Ранняя вакцинация БЦЖ, госпитализации и случаи смерти в больницах: анализ вторичного исхода в 3 рандомизированных исследованиях в Гвинее-Бисау. J заразить дис. 2018;219(4):624–632. doi: 10.1093/infdis/jiy544. [PubMed] [CrossRef] [Академия Google]
Schaltz-Buchholzer F, et al. Ранняя вакцинация БЦЖ, госпитализации и случаи смерти в больницах: анализ вторичного исхода в 3 рандомизированных исследованиях в Гвинее-Бисау. J заразить дис. 2018;219(4):624–632. doi: 10.1093/infdis/jiy544. [PubMed] [CrossRef] [Академия Google]
6. Madsen AMR, et al. Использование вакцины БЦЖ для усиления неспецифической защиты медицинских работников во время пандемии COVID-19: структурированное резюме протокола исследования для рандомизированного контролируемого исследования в Дании. Испытания. 2020;21(1):799. doi: 10.1186/s13063-020-04714-3. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
7. Chavarri-Guerra Y, Soto-Perez-de-Celis E. Эритема на шраме от бациллы Calmette-Guerin после вакцинации против гриппа. Rev Soc Bras Med Trop. 2019;53:e20190390. doi: 10.1590/0037-8682-0390-2019. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
8. Кондо М., Гото Х., Ямамото С. Первый случай покраснения и эрозии в месте прививки бациллой Кальметта-Герена после вакцинации против гриппа. J Дерматол. 2016;43(10):1229–1231. doi: 10.1111/1346-8138.13365. [PubMed] [CrossRef] [Google Scholar]
J Дерматол. 2016;43(10):1229–1231. doi: 10.1111/1346-8138.13365. [PubMed] [CrossRef] [Google Scholar]
9. Lim DW, Ng DHL, Low JG. Вспышка шрама Bacillus Calmette-Guerin после вакцины мРНК SARS-CoV-2. CMAJ. 2021;193(30):E1178. дои: 10.1503/cmaj.210696. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
10. Lopatynsky-Reyes EZ, Acosta-Lazo H, Ulloa-Gutierrez R, et al. Местное воспаление кожи после введения БЦЖ в качестве новой реакции после вакцинации мРНК COVID-19 у двух международных медицинских работников. Куреус. 2021 г.: 10.7759/cureus.14453. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
11. Kakisaka Y, et al. Вирус герпеса человека типа 6 может вызывать кожные поражения в месте прививки БЦЖ, сходные с болезнью Кавасаки. Тохоку J Exp Med. 2012;228(4):351–353. doi: 10.1620/tjem.228.351. [PubMed] [CrossRef] [Академия Google]
12. Muthuvelu S, et al. Инфекция кори, вызывающая реактивацию Bacillus Calmette-Guérin: клинический случай. БМС Педиатр. 2019;19(1):251. doi: 10.1186/s12887-019-1635-z. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
БМС Педиатр. 2019;19(1):251. doi: 10.1186/s12887-019-1635-z. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
13. Loh ACE, Kua PHJ, Tan ZL. Эритема и уплотнение бациллы Кальметта-Герена для диагностики болезни Кавасаки. Singapore Med J. 2019;60(2):89–93. doi: 10.11622/smedj.2018084. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
14. Резай М.С., Шахмохаммади С. Эритема в месте прививки БЦЖ у пациентов с болезнью Кавасаки. Матер Социомед. 2014;26(4):256–260. doi: 10.5455/msm.2014.26.256-260. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
15. Цзян Л. и др. COVID-19 и мультисистемный воспалительный синдром у детей и подростков. Ланцет Infect Dis. 2020;20(11):e276–e288. doi: 10.1016/S1473-3099(20)30651-4. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
16. Olsen AW, et al. Влияние оставшихся живых организмов БЦЖ у вакцинированных мышей на поддержание иммунитета к туберкулезу. Сканд Дж. Иммунол. 2004;60(3):273–277. doi: 10.1111/j.0300-9475.2004.01471.x. [PubMed] [CrossRef] [Академия Google]
doi: 10.1111/j.0300-9475.2004.01471.x. [PubMed] [CrossRef] [Академия Google]
17. Путанакит Т. и др. Синдром восстановления иммунитета, вызванный бациллой Кальметта-Герена, после начала антиретровирусной терапии у детей с ВИЧ-инфекцией. Клин Инфекция Дис. 2005;41(7):1049–1052. дои: 10.1086/433177. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
18. Tomita Y, et al. Вакцина БЦЖ может генерировать перекрестно-реактивные Т-клетки против SARS-CoV-2: анализ in silico и гипотеза. вакцина. 2020;38(41):6352–6356. doi: 10.1016/j.vaccine.2020.08.045. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
19. Eggenhuizen PJ, et al. Пептиды, полученные из вакцины БЦЖ, вызывают перекрестную реактивность Т-клеток SARS-CoV-2. medRxiv. 2020. 2020.11.21.20236018. [Бесплатная статья PMC] [PubMed]
20. Nuovo G, et al. Сильная гомология между белком оболочки SARS-CoV-2 и Mycobacterium sp. Антиген позволяет быстро диагностировать микобактериальные инфекции и может обеспечить специфический иммунитет против SARS-CoV-2 через вакцину БЦЖ. Энн Диагн Патол. 2020;48:151600. doi: 10.1016/j.anndiagpath.2020.151600. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Энн Диагн Патол. 2020;48:151600. doi: 10.1016/j.anndiagpath.2020.151600. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Статьи из BMC Infectious Diseases предоставлены здесь с разрешения BioMed Central
рубцов после прививки БЦЖ связаны со снижением младенческой смертности
Источник/раскрытие информации
Источник:
Berendsen MLT, et al. J Pediatr Infect Dis Soc . 2019; doi: 10.1093/jpids.piy142.
Вы успешно добавили оповещения. Вы получите электронное письмо, когда будет опубликован новый контент.
Щелкните здесь, чтобы управлять оповещениями по электронной почте
Нам не удалось обработать ваш запрос. Пожалуйста, повторите попытку позже.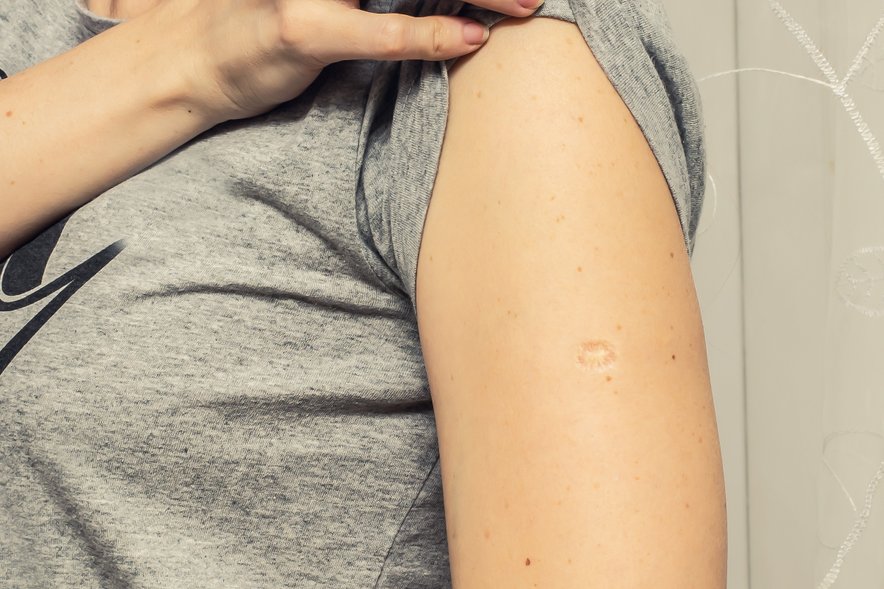 Если у вас по-прежнему возникает эта проблема, свяжитесь с нами по адресу [email protected]. Согласно результатам рандомизированного контролируемого исследования, опубликованного в0063 Журнал детских инфекционных болезней s Общество. Исследователи писали, что влияние противотуберкулезной вакцины на смертность было не таким сильным, когда рубцы были только у ребенка.
Если у вас по-прежнему возникает эта проблема, свяжитесь с нами по адресу [email protected]. Согласно результатам рандомизированного контролируемого исследования, опубликованного в0063 Журнал детских инфекционных болезней s Общество. Исследователи писали, что влияние противотуберкулезной вакцины на смертность было не таким сильным, когда рубцы были только у ребенка.
Предыдущие исследования продемонстрировали преимущества некоторых живых вакцин, в том числе БЦЖ, для выживания детей за счет «усиления защиты от нецелевых инфекций».
«Шрамы БЦЖ являются надежными маркерами правильно проведенной вакцинации БЦЖ и указывают на то, что иммунная система обучена обеспечивать некоторую защиту от нетуберкулезных заболеваний» Питер Ааби, доктор медицинских наук, , профессор Bandim Health Project, рассказал об инфекционных заболеваниях у детей . «Если у матери также имеется рубец БЦЖ, вакцинация ребенка БЦЖ обеспечит дополнительную защиту от нетуберкулезных заболеваний. Подготовка от матери может иметь большое значение для того, как ребенок отреагирует на вакцинацию, и в текущей практике это не принимается во внимание».
Подготовка от матери может иметь большое значение для того, как ребенок отреагирует на вакцинацию, и в текущей практике это не принимается во внимание».
Исследователи включили почти 6500 детей в возрасте 4,5 месяцев в исследование, посвященное ранней вакцинации против кори. Дети находились под наблюдением до 36 месяцев. Ааби и его коллеги сравнили показатели смертности детей в зависимости от того, был ли шрам от БЦЖ у матери, ребенка или у обоих.
Исследователи сосредоточились на 2 213 детях, которые не получали добавки витамина А для новорожденных или раннюю вакцинацию против кори. Они выявили рубцевание БЦЖ у 83% этих детей и 44% матерей. Дети, у матерей которых были рубцы БЦЖ, чаще сами имели рубцы БЦЖ (отношение рисков = 1,01; 95% ДИ, 0,98–1,05).
У матери и ребенка видны рубцы от прививки БЦЖ. Эти рубцы как у матерей, так и у их младенцев связаны со снижением младенческой смертности.
Источник: Rebecca Fabricius, Bandim Health Project
У детей, у которых были рубцы от БЦЖ, уровень смертности в возрасте от 4,5 до 36 месяцев был ниже на 41% (95% ДИ, 5%-64%).
