Содержание
Вакцина АКДС
Фото:
открытый источник
Источник:
Вакцинация необходима – в этом убеждают врачи всего мира. Прививка АКДС детям ежегодно спасает тысячи жизней, предупреждая тяжелое течение болезней. Она создана для профилактики коклюша, дифтерии, столбняка.
Что такое АКДС
Про прививку АКДС (расшифровка названия и побочные эффекты, сроки применения) знает большинство родителей. Вакцина изготовлена в России и предназначена для защиты от трех тяжелых болезней – коклюш, дифтерия, столбняк. Вакцина АКДС состоит из двух анатоксинов (вызывающих столбняк, дифтерию) и мертвых палочек коклюша.
Благодаря такому составу вакцина АКДС инициирует иммунитет к конкретным инфекциям. Хотя многие знают, от чего ставят прививку АКДС, куда делают укол (расшифровка названия – адсорбированная коклюшно-дифтерийно-столбнячная вакцина), страхов, связанных с ней, остается очень много. Родители обеспокоены возможными осложнениями, чаще всего провоцируемыми коклюшным агентом.
Это любопытно: многие родители знают, как называется платная вакцина АКДС – Пентаксим. Такой укол придется оплатить. А вот отечественный препарат доступен бесплатно.
Аналоги прививки
Поскольку многие сомневаются в том, насколько хорошо, как переносится прививка АКДС, изготовленная в России, востребованы зарубежные заменители. Аналогичные АКДС импортные вакцины, разрешенные в нашей стране – Инфанрикс, Пентаксим, ИнфанриксГекса. Две последние создают иммунитет к большему количеству болезней. Аналогичные АКДС импортные вакцины Пентаксим и Инфанрикс лучше переносятся, реже вызывают побочные эффекты.
Важно не только знать, какие вакцины АКДС бывают, но и представлять, как они вводятся. Пентаксим рекомендован к применению курсом из 3 доз. Первый укол делают в 3-месячном возрасте. В отличие от обычной АКДС импортная вакцина Пентаксим (и Инфанрикс) минимально беспокоит малыша и редко сопровождается побочными эффектами. Второй раз препарат вводят через полтора месяца; третий – в полугодовалом возрасте./90/90.jpg) График вакцинации прививки (АКДС и импортных альтернатив) можно изменить: впервые сделать укол в 2-месячном возрасте, сократить паузы до месяца.
График вакцинации прививки (АКДС и импортных альтернатив) можно изменить: впервые сделать укол в 2-месячном возрасте, сократить паузы до месяца.
Это любопытно: отечественная, бельгийская, французская вакцина АКДС – способ защитить ребенка от смертельных болезней. Можно ли отказаться от прививки АКДС? Да, это возможно, но врачи рекомендуют обеспокоенным родителям заменить препарат на импортный, но не отказываться от вакцинации полностью.
Инфанрикс – аналог прививки АКДС от бельгийских ученых. Курс начинают в 3-месячном возрасте. Известно, сколько раз делают прививку (как АКДС) – трижды. В 18-месячном возрасте ребенка вакцинируют повторно.
ИнфанриксГекса выигрывает широтой создаваемого иммунитета. Известно, для чего нужна прививка АКДС – чтобы сформировать защиту от коклюша, дифтерии и столбняка. ИнфанриксГекса создает защиту не только от этих болезней, но и от полиомиелита, гепатита В, гемофильной палочки. Вводится курсом из 3 уколов. Когда делают прививку (аналог АКДС), объяснит врач, осмотрев ребенка.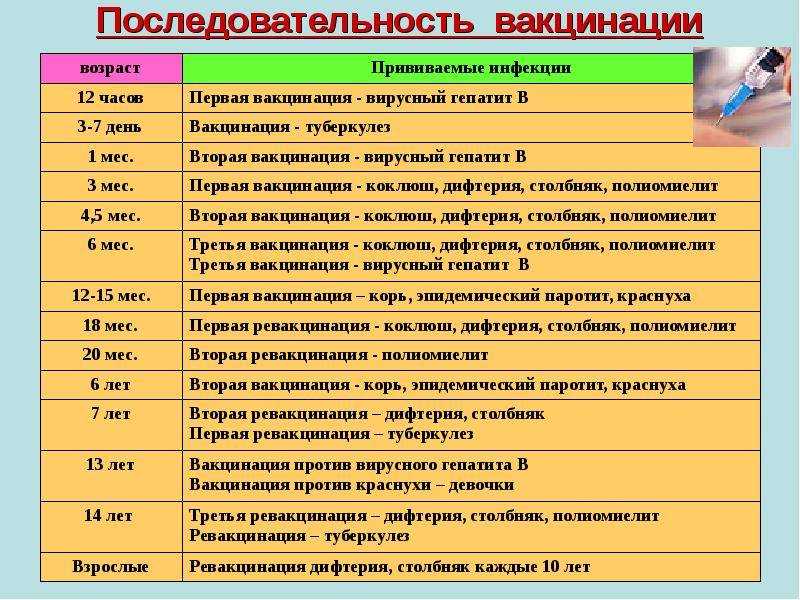 Обычно начинают в возрасте 3 месяцев, но можно сместить начало на 2-месячный возраст.
Обычно начинают в возрасте 3 месяцев, но можно сместить начало на 2-месячный возраст.
Хороший аналог АКДС – Адасель. Родители, наслышанные, чем опасна прививка АКДС, нередко выбирают альтернативой Адасель, разрешенный в возрасте старше 4 лет. Врачи, объясняя, в каком возрасте делают прививку АКДС, отмечают, что она предназначена для маленьких детей; если лекарство не применяли, защиту от коклюша дает именно Адасель. В отличие от прививки АКДС ревакцинация Адасель необходима каждые 10 лет. Вакцина Адасель вместо всех АКДС – это разумный вариант, проигрывающий только ценой.
Календарь прививок
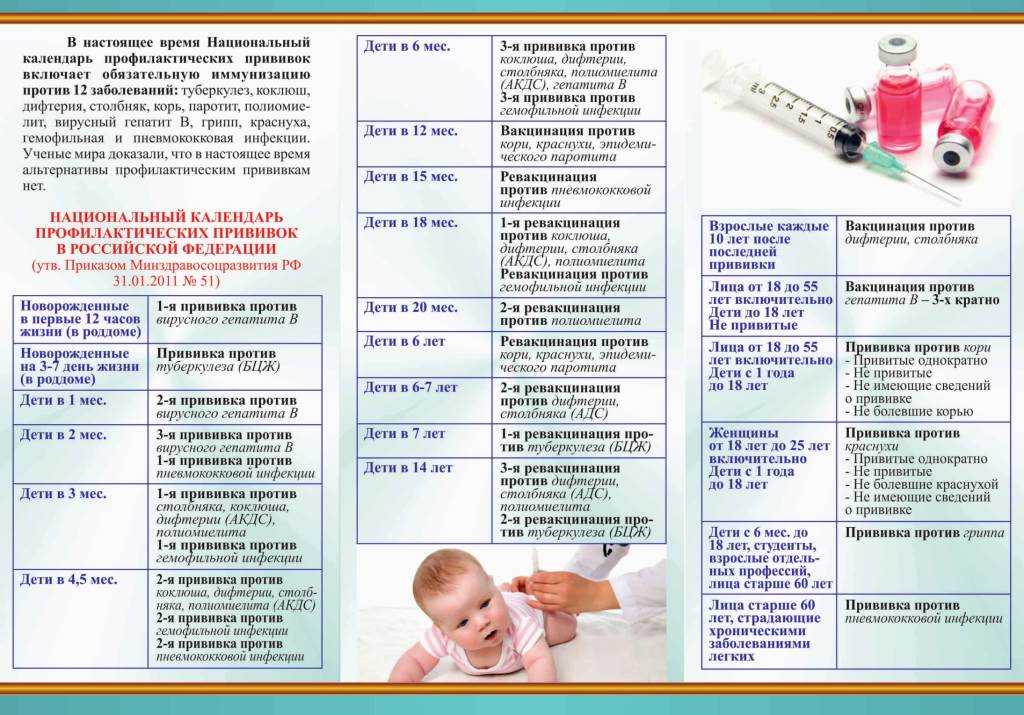
Известно, сколько прививок АКДС нужно: 3. Принятый в России календарь рекомендует впервые вводить препарат в 3 месяца, затем в 4,5 и в 6 месяцев. Зная, от чего делается прививка АКДС (и последствия ее применения), родители обычно соглашаются на введение препарата ребенку в 3-месячном возрасте. Иногда врач советует сместить срок на месяц. Технику введения вакцины АКДС родителям знать не нужно – своими руками делать укол запрещено.
Известно, в каком возрасте делается прививка АКДС для ревакцинации: в 18 месяцев.
АКДС взрослым и детям
Нередко прививка АКДС взрослым из-за побочных эффектов кажется страшной и опасной. Действительно, иногда поднимается температура после прививки АКДС, возможно покраснение кожи и другие реакции; однако позитивные последствия вакцинации превышают эти недостатки.
Взрослым вакцина АКДС не ставится.
Осложнения после прививки
При правильной подготовке к прививке АКДС вероятность осложнений минимальна. Обычно укол вызывает:
- локальную боль;
- жжение, зуд участка кожи;
- небольшой отек;
- кратковременный жар;
- потерю сна и аппетита;
- капризность.
Если учтены противопоказания к АКДС вакцине у детей, настоящих осложнений не возникает. Самые опасные побочные реакции – судороги, аллергия, шок. Чтобы предупредить опасную ситуацию, вакцинированного ребенка 30 минут наблюдают врачи.
Это любопытно: важно знать, сколько действует прививка АКДС: иммунитет от коклюша сохраняется только 4 года и его нужно обновлять.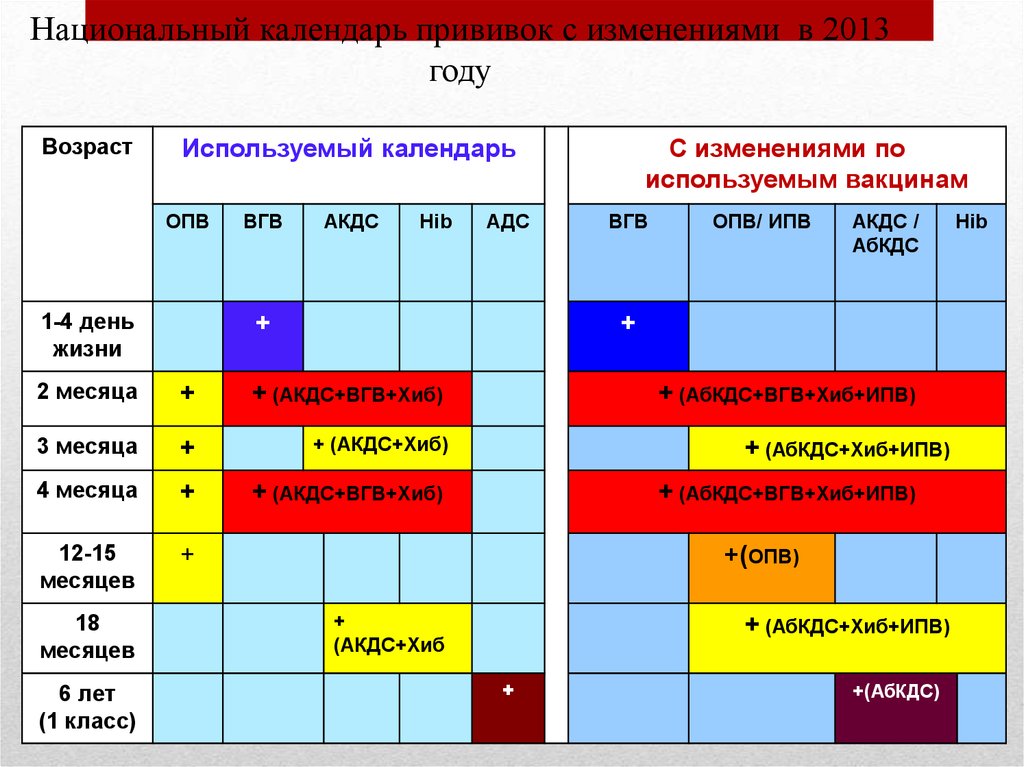
Подготовка к прививке и медотвод
Анализы перед прививкой АКДС:
- общий урины;
- общий крови.
Ребенка осматривает невропатолог.
Врачи рекомендуют заранее купить лекарства с парацетамолом, анальгин.
Причины для медотвода:
- иммунодефицит;
- иммуносупрессия;
- онкология;
- сильная реакция на вакцины;
- прогрессирующие патологии нервной системы;
- перенесенные ранее афебрильные судороги.
Ревакцинация
Ревакцинация АКДС проводится 1 раз в возрасте 18 месяцев. Впоследствии рекомендована ревакцинация другими препаратами от коклюша. Прививки ставят в 7 и 14 лет; взрослым – каждые 10 лет.
Автор: Татьяна Борисова
расшифровка, от чего делают, инструкция по применению вакцины
Для защиты от тяжелых инфекционных и вирусных патологий используют вакцинирование. Пока что это единственный надежный метод профилактики. Прививать начинают в первые месяцы жизни малыша. Так, всем родителям педиатры предлагают иммунизировать ребенка АКДС.
Так, всем родителям педиатры предлагают иммунизировать ребенка АКДС.
Отзывы о данном препарате противоречивые. Чтобы решить, стоит ли соглашаться на такую профилактику, надо рассмотреть, что собой представляет вакцина АКДС: общую информацию, мнения врачей, аналоги.
Оглавление
- 1 Что такое прививка АКДС: расшифровка
- 2 Страна-производитель
- 3 Что входит в состав и от каких болезней она защищает?
- 4 Живая вакцина или инактивированная?
- 5 Когда делают детям и взрослым прививку от дифтерии, столбняка и коклюша: сроки вакцинации
- 6 Обязательно ли прививаться?
- 7 Официальная инструкция по применению адсорбированной коклюшно-дифтерийно-столбнячной вакцины
- 7.1 Куда правильно ставить укол?
- 7.2 Алгоритм и техника вакцинации
- 8 Противопоказания к проведению вакцинации и ревакцинации
- 9 Чем опасна прививка: побочные эффекты и последствия
- 10 Как легче перенести иммунизацию?
- 11 Через сколько дней можно делать другую прививку?
- 12 Названия аналогов российского и импортного производства
- 13 АКДС, Пентаксим, Инфанрикс или Тетракок: что лучше выбрать?
- 14 Видео по теме
Что такое прививка АКДС: расшифровка
Расшифровывается АКДС следующим образом: адсорбированная коклюшно-дифтерийно-столбнячная прививка.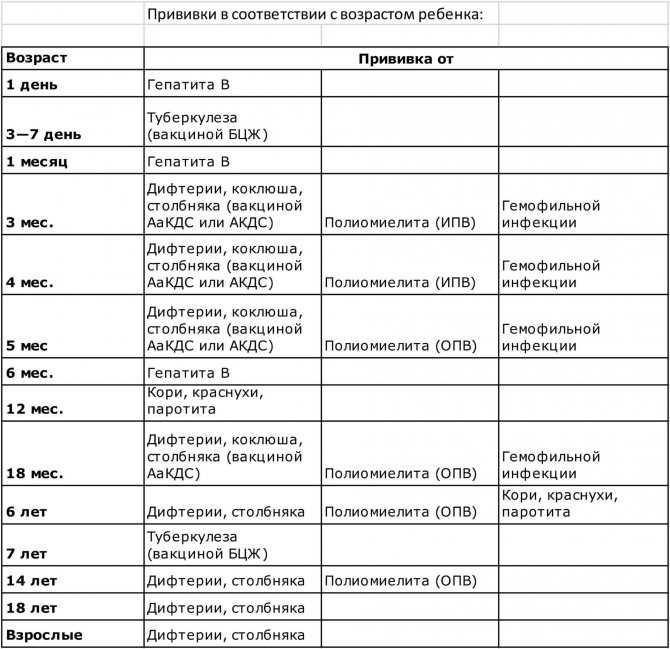 Препарат есть в международной номенклатуре. Там он обозначается DTP.
Препарат есть в международной номенклатуре. Там он обозначается DTP.
Вакцина является комбинированной: она защищает сразу от трех опасных инфекционных заболеваний, которые могут приводить к инвалидизации и смерти. В местных поликлиниках АКДС прививают бесплатно.
Вакцина АКДС
Страна-производитель
Страной-производителем АКДС выступает Россия. Вакцина была разработана еще в советские времена. Несмотря на появление новых, более совершенных прививок, АКДС активно используется для иммунизации детей и сегодня.
Выпуском такого препарата занимается две отечественные фармацевтические организации:
- ФГУП НПО «Микроген»;
- ОАО «Биомед им. Мечникова».
Также есть прививки АДС и АДС-М. Они предназначены для тех лиц, которые переболели коклюшем или плохо переносят высокую дозу вакцины АКДС.
Что входит в состав и от каких болезней она защищает?
Показанием к использованию АКДС является профилактика коклюша, дифтерии и столбняка. В АКДС содержатся анатоксины – инактивированные токсины патогенов, ослабленных формалином.
В АКДС содержатся анатоксины – инактивированные токсины патогенов, ослабленных формалином.
В 0,5 мл раствора присутствуют такие компоненты:
- целые инактивированные клетки коклюшной палочки концентрацией 10 млрд единиц;
- дифтерийный токсоид в дозировке 15 флокулирующих единиц;
- анатоксин палочки столбняка – 5 антитоксиносвязующих единиц;
- консервант мертиолят – от 45 до 50 мкг;
- гидроксид алюминия – 0,5-0,55 мг;
- формалин в количестве 40-62 мкг.
У некоторых детей имеется непереносимость яичного белка. В этом случае АКДС колоть не противопоказано, поскольку при производстве средства, такой элемент не применяется.
Живая вакцина или инактивированная?
Все прививочные средства делятся на живые и мертвые вакцины. Первые содержат ослабленные вирусы и бактерии. Они выпускаются в виде оральных капель.
Примером такой прививки можно назвать отечественную вакцину от полиомиелита. В препаратах второй группы болезнетворные микроорганизмы обезвреженные, убитые. Такие средства могут содержать анатоксины или мертвые клетки патогенов.
Такие средства могут содержать анатоксины или мертвые клетки патогенов.
Выпускаются инактивированные прививки в виде раствора для инъекционного введения. АКДС относится к неживым вакцинам, поскольку имеет в составе анатоксины дифтерийной, столбнячной палочек и убитый возбудитель коклюша.
Когда делают детям и взрослым прививку от дифтерии, столбняка и коклюша: сроки вакцинации
АКДС делают детям до 4-летнего возраста и ранее непривитым от коклюша взрослым. Иммунопрофилактику проводят по утвержденному графику. При наличии временных противопоказаний, вакцинацию могут перенести на определенный срок, но при возобновлении курса используют аналогичные дозы и придерживаются тех же интервалов между уколами.
Стандартная схема прививания ребенка АКДС:
- первую инъекцию делают в трехмесячном возрасте;
- второй раз препарат вводят в 4,5 месяца;
- третью вакцинацию выполняют в полгода.
Трехкратный курс позволяет выработать стойкий иммунитет. Допускается сокращение интервала между уколами до 30 дней.
Допускается сокращение интервала между уколами до 30 дней.
Детей старше 4 лет прививают препаратом без коклюшного компонента (АДС, АДС-М). В 1,5 года, в 7 и 14 лет проводят ревакцинации с целью поддержки крепости защитных сил. Взрослым АКДС колют лишь в том случае, если в детском возрасте они не были привиты таким средством.
Стандартный курс включает три инъекции, сделанные с 45-дневным перерывом. Вакцинированных в младенчестве мужчин и женщин прививают каждые 10 лет препаратом АДС или АДС-М.
Обязательно ли прививаться?
Вакцина АКДС включена в российский Национальный прививочный календарь. Поэтому колют препарат в обязательном порядке всем новорожденным, у которых отсутствуют противопоказания.
Без согласия родителей средство вводить запрещается. Мать или отец вправе написать отказ от АКДС, основываясь на положениях соответствующих законов.
Но популярный педиатр Комаровский, мнение которого многие родители считают авторитетным, не советует игнорировать вакцинацию без веских на то причин.
Врач предупреждает, что столбняк, коклюш и дифтерия, являются очень заразными заболеваниями и последствия этих патологий гораздо тяжелее переносятся, чем побочные эффекты от прививки.
Официальная инструкция по применению адсорбированной коклюшно-дифтерийно-столбнячной вакцины
Чтобы вакцинация АКДС привела к формированию крепкого специфического иммунитета, надо использовать препарат правильно. Для этого необходимо изучить аннотацию, которую производитель поставляет в комплекте с ампулой. Медперсонал должен знать технику постановки укола, оптимальное место для инъекции, последовательность действий.
Куда правильно ставить укол?
Вводят АКДС в мышцу. Этот метод оптимальный, способствует оперативному высвобождению инфекционных агентов. Если колоть препарат подкожно, то компоненты прививки будут высвобождаться слишком долго и не приведут к формированию стойкого иммунитета.
Маленьким детям вводят АКДС в область наружной бедренной поверхности. Детям старше двух лет и взрослым, прививку колют в дельтовидную мышцу.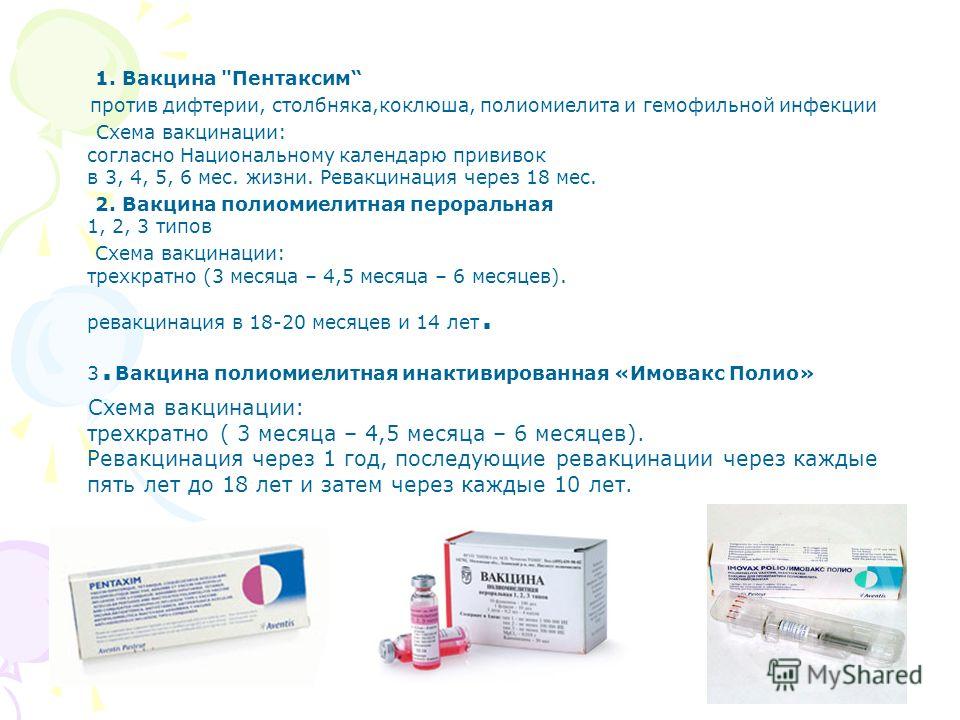
В ягодицу препарат вводить категорически запрещено, тому есть ряд причин:
- есть риск повреждения седалищного нерва;
- в этой области сосредоточено большое количество жировой ткани, поэтому добраться до мышцы будет сложнее;
- есть большая вероятность прокола кровеносного сосуда.
Бедро и плечо лишены толстой жировой прослойки, поэтому в этих местах легче попасть иглой в мышцу.
Алгоритм и техника вакцинации
При проведении иммунизации отечественным средством АКДС надо соблюдать правильную технику вакцинации и следовать утвержденному алгоритму действий.
Это поможет сформировать качественный иммунитет и предупредить развитие побочных реакций и осложнений. Прежде чем набирать в шприц препарат, надо убедиться в его пригодности для использования.
Следует обратить внимание на такие моменты;
- целостность ампулы;
- дату выпуска средства;
- условия хранения;
- физические свойства жидкости.

Раствор должен быть однородным, без каких-либо посторонних включений (хлопьев, нитей), прозрачным.
Колоть разрешается только вакцину с действующим сроком годности.
Алгоритм и техника введения АКДС:
- нагреть ампулу до комнатной температуры, встряхнуть ее для получения однородной смеси;
- обработать емкость спиртом;
- вскрыть ампулу и набрать в стерильный шприц все содержимое;
- протереть антисептическим средством кожу в зоне инъекции;
- сделать прокол, убедиться, что игла попала в мышцу и ввести препарат, нажав на поршень шприца;
- снова обработать спиртом эпидермис в месте введения средства.
Эффективность АКДС составляет 80-85%. Привитый может заразиться коклюшем, столбняком и дифтерией. Но в этом случае человек перенесет болезнь в облегченной форме.
Противопоказания к проведению вакцинации и ревакцинации
Любое лекарство имеет свои противопоказания. Препарат запрещается вводить при определенных состояниях, ввиду высокого риска развития побочных эффектов. Все ограничения делятся на временные и постоянные.
Все ограничения делятся на временные и постоянные.
К первой группе противопоказаний к введению АКДС взрослым и детям относятся такие:
- состояние аллергии на продукты питания, средства гигиены и другие вещества;
- терапия медикаментами, которые угнетают работу иммунной системы;
- кашель, насморк и другие признаки простуды;
- острое течение инфекционных патологий;
- повышенная температура;
- прорезывание зубов у детей;
- обострение заболеваний органов и систем хронического типа;
- употребление алкогольных напитков накануне или в день планируемой манипуляции;
- гепатит;
- общее недомогание;
- интоксикация любого характера;
- беременность;
- недавно перенесенная операция;
- туберкулез.
В перечень постоянных противопоказаний включены следующие состояния:
- иммунодефицит;
- развитие выраженных патологических реакций от предыдущей дозы вакцины;
- аллергия на составляющие АКДС;
- неизлечимые патологии нервной системы.

Чем опасна прививка: побочные эффекты и последствия
В АКДС содержатся цельноклеточный коклюшный элемент, гидроксид алюминия и мертиолят. Эти вещества часто провоцируют развитие негативной симптоматики.
Нормальной реакцией считается незначительная гипертермия, слабость и ухудшение аппетита. Также допустимы местные проявления в виде покраснения, пастозности и болезненности области прокола.
Вероятные побочные эффекты от АКДС:
- лихорадка;
- судорожные припадки;
- образование в месте инъекции уплотнения и красноты диаметром более 8 см;
- аллергия в виде синдромов Лайелла и Стивенса-Джонсона, крапивницы, анафилаксии, отека Квинке;
- паралич конечностей;
- снижение или повышение давления;
- менингит;
- энцефалит.
Если после прививки появились лихорадка, которая не устраняется жаропонижающими препаратами, одышка, судорожные припадки, человек теряет сознание, то нужно вызывать скорую помощь.
Передозировка АКДС теоретически возможна. Но препарат фасуется в ампулы в количестве 0,5 мл. Это стандартная доза для детей и взрослых. Если колоть препарат правильно, соблюдать установленные промежутки между инъекциями, то никаких плохих последствий быть не должно.
Как легче перенести иммунизацию?
Чтобы иммунизация прошла максимально легко, нужно придерживаться рекомендаций врачей. Идти на прививку стоит на голодный желудок, полностью здоровым.
Накануне вакцинации доктор может порекомендовать начать прием жаропонижающих и антигистаминных препаратов. Детям временно отменяется терапия витамином Д.
После прививки специалисты советуют:
- не гулять в общественных местах;
- употреблять здоровую пищу;
- исключить из меню высокоаллергенные блюда;
- не мочить место прокола и не купаться пару дней;
- ограничить физическую активность;
- отказаться от приема спиртных напитков.
Через сколько дней можно делать другую прививку?
АКДС разрешается колоть в один день с полиомиелитной вакциной и другими прививками, входящими в Национальный календарь иммунопрофилактики. Исключение составляет БЦЖ. Противотуберкулезную вакцину вводят спустя месяц после инъекции АКДС.
Исключение составляет БЦЖ. Противотуберкулезную вакцину вводят спустя месяц после инъекции АКДС.
Названия аналогов российского и импортного производства
У некоторых лиц АКДС провоцирует развитие осложнений, вызывает аллергию. В этом случае доктора рекомендуют замену этой вакцины на отечественный или импортный аналог.
Вместо АКДС можно использовать такие препараты:
- Пентаксим (Франция). Защищает от гемофильной инфекции, палочек дифтерии, коклюша, столбняка, вируса полиомиелита;
- Бубо-М (Россия). Способствует выработке антител к гепатиту В, столбняку и дифтерии;
- Тетракок (Франция). Применяется для профилактики заражения дифтерией, полиомиелитом, коклюшем и столбняком;
- Инфанрикс (Бельгия). Защищает от дифтерийных, коклюшных и столбнячных палочек;
- АДС (Россия). Это тот же АКДС, но без коклюшного компонента;
- АДС-М (Россия).
 Содержит те же элементы, что и АДС, но в меньшей дозе.
Содержит те же элементы, что и АДС, но в меньшей дозе.
АКДС, Пентаксим, Инфанрикс или Тетракок: что лучше выбрать?
Иногда вакцинируемые лица не могут применять АКДС из-за индивидуальных особенностей организма, в этом случае им приходится прививаться импортными вакцинами. Считается, что такие препараты проходят лучшую очистку, не содержат мертиолят и прочие соединения, которые могут нанести вред организму.
Вакцинация импортными средствами будет платной. В стоимость входит цена препарата и услуга медперсонала. АКДС колют в рамках плановой иммунизации на бесплатной основе.
Подбирать вакцину должен исключительно лечащий специалист, на основании жалоб и предпочтений вакцинируемого. В качестве альтернативы АКДС, доктор может предложить: Инфанрикс, Тетракок или Пентаксим.
При желании уберечь ребенка от полиомиелита и гемофильных заболеваний, стоит выбирать Пентаксим. Если ХИБ-компонент плохо переносится, то лучше иммунизироваться Тетракоком.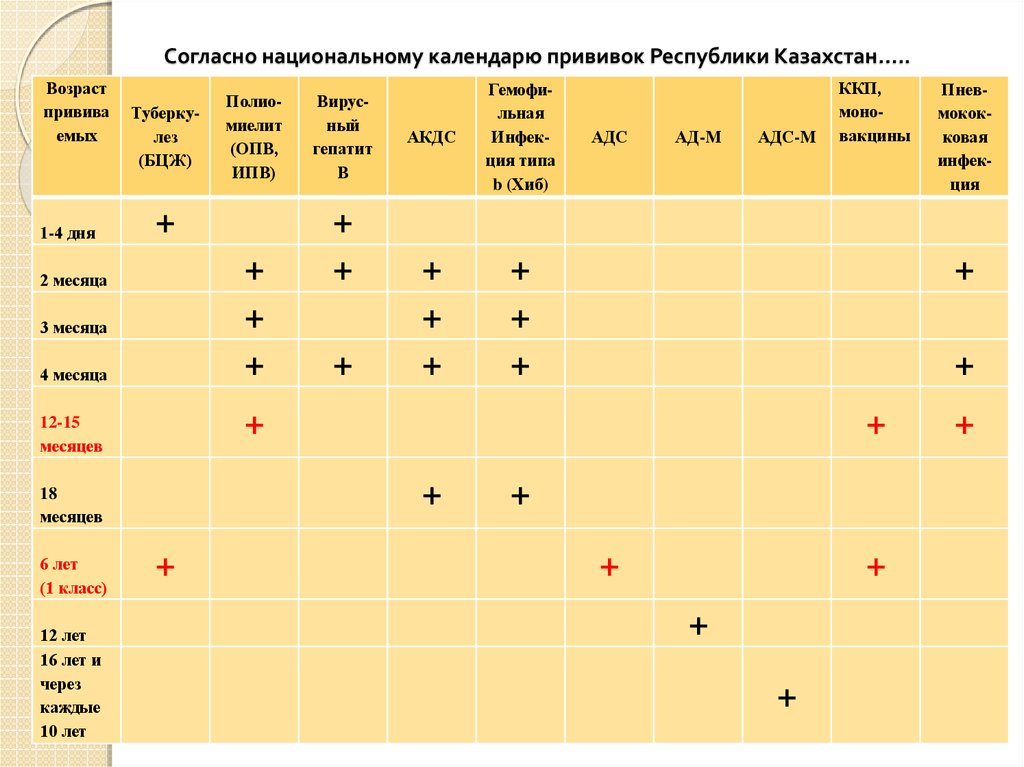
Видео по теме
Обязательно делать прививку АКДС, сколько раз, в каком возрасте и с каким интервалом? Какие возможны реакции и осложнения, связанные с вакциной АКДС? Отвечает доктор Комаровский:
Таким образом, АКДС защищает от заражения палочками столбняка, дифтерии, микробами коклюша. Препарат содержит анатоксины патогенов, мертиолят, формальдегид и гидроксид алюминия. Последние три вещества опасны и редко применяются в современных импортных вакцинах. Поэтому некоторые решают проходить иммунизацию зарубежными аналогами.
Системная серология для расшифровки инфекции и иммунного ответа антител на ВИЧ-1
Статьи, представляющие особый интерес, опубликованные в течение годового периода обзора, отмечены как:
1. Арнольд К.Б., Чанг А.В. Перспективы системных серологических исследований.
Иммунология
2018;153(3):279–89. [Бесплатная статья PMC] [PubMed] [Google Scholar]
2. Чанг А.В., Альтер Г. Системная серология: профилирование гуморального иммунитета против ВИЧ, индуцированного вакциной.
Ретровирусология
2017;14(1):57. [Бесплатная статья PMC] [PubMed] [Google Scholar]
3. Акерман М.Е., Барух Д.Х., Альтер Г. Системная серология для оценки испытаний вакцины против ВИЧ.
Иммунол Rev
2017;275(1):262–70. [бесплатная статья PMC] [PubMed] [Google Scholar]
4. Плоткин С.А. Корреляты защиты, индуцированной вакцинацией.
Клин Вакцина Иммунол
2010;17(7):1055–65. [Бесплатная статья PMC] [PubMed] [Google Scholar]
5. Mascola JR. Исследования пассивного переноса для выяснения роли опосредованной антителами защиты от ВИЧ-1.
вакцина
2002; 20 (15): 1922–195. [PubMed] [Академия Google]
6. Кроули А.Р., Акерман М.Е. Имейте в виду пробел: как межвидовая изменчивость IgG и его рецепторов может усложнить сравнение эффекторной функции человека и нечеловеческих приматов.
Границы в иммунологии
2019; в печати. [Статья бесплатно PMC] [PubMed]
* В этом обзоре перечислены многие исследования, показывающие взаимосвязь между эффекторной функцией антител и противовирусными эффектами на моделях животных и людей, а также описаны различия в биологии антител и рецепторов антител между макаками-резусами и людьми.
7. Corey L, Gilbert PB, Tomaras GD, et al.
Иммунные корреляты защиты от вакцин против заражения ВИЧ-1.
Sci Transl Med
2015;7(310):310rv7. [Бесплатная статья PMC] [PubMed] [Google Scholar]
8. Томарас Г.Д., Плоткин С.А. Сложные иммунные корреляты защиты в испытаниях эффективности вакцины против ВИЧ-1.
Иммунол Rev
2017;275(1):245–61. [Бесплатная статья PMC] [PubMed] [Google Scholar]
9. Bournazos S, Klein F, Pietzsch J, et al.
Широко нейтрализующие антитела против ВИЧ-1 требуют эффекторных функций Fc для активности in vivo.
Клетка
2014;158(6):1243–53. [Бесплатная статья PMC] [PubMed] [Google Scholar]
10. Halper-Stromberg A, Lu CL, Klein F, et al.
Широко нейтрализующие антитела и вирусные индукторы уменьшают отскок от латентных резервуаров ВИЧ-1 у гуманизированных мышей.
Клетка
2014;158(5):989–99. [Бесплатная статья PMC] [PubMed] [Google Scholar]
11. Hessell AJ, Hangartner L, Hunter M, et al.
Рецептор Fc, но не связывание комплемента, важен для защиты антител от ВИЧ.
Природа
2007;449(7158):101–4. [PubMed] [Google Scholar]
12. Horwitz JA, Bar-On Y, Lu CL, et al.
Ненейтрализующие антитела изменяют течение ВИЧ-1
Заражение в естественных условиях. Клетка
2017; 170(4):637–48.
е10. [Бесплатная статья PMC] [PubMed] [Google Scholar]
*Это исследование продемонстрировало способность ненейтрализующего антитела оказывать эволюционное давление на вирус ВИЧ-1 in vivo.
13. Парсонс М.С., Ли В.С., Кристенсен А.Б. и др.
Fc-зависимые функции дублируют эффективность анти-ВИЧ-антитела PGT121 у макак.
Джей Клин Инвест
2019;129(1):182–91. [Статья бесплатно PMC] [PubMed] [Google Scholar]
*Это исследование показало, что эффекторная функция может не способствовать защите, обеспечиваемой очень широкими и сильнодействующими нейтрализующими антителами. Это также важное наблюдение в свете данных о мышиных моделях ВИЧ-инфекции, которые предполагают роль Fc-механизмов в противовирусной активности PGT121.
Это также важное наблюдение в свете данных о мышиных моделях ВИЧ-инфекции, которые предполагают роль Fc-механизмов в противовирусной активности PGT121.
14. Moldt B, Shibata-Koyama M, Rakasz EG, et al.
Нефукозилированный вариант моноклонального антитела против ВИЧ-1 b12 обладает усиленной противовирусной активностью, опосредованной FcgammaRIIIa, in vitro, но не улучшает защиту от заражения SHIV слизистой у макак.
Джей Вирол
2012;86(11):6189–96. [Бесплатная статья PMC] [PubMed] [Google Scholar]
15. Nimmerjahn F, Gordan S, Lux A. FcgammaR-зависимые механизмы цитотоксической, агонистической и нейтрализующей активности антител.
Тренды Иммунол
2015;36(6):325–36. [PubMed] [Академия Google]
16. Ниммерьян Ф., Раветч СП. Рецепторы Fcgamma как регуляторы иммунных реакций.
Нат Рев Иммунол
2008;8(1):34–47. [PubMed] [Google Scholar]
17. Bouharoun-Tayoun H, Oeuvray C, Lunel F, et al.
Механизмы, лежащие в основе опосредованного моноцитами антителозависимого уничтожения бесполых кровяных стадий Plasmodium falciparum.
J Эксперт Мед
1995;182(2):409–18. [Бесплатная статья PMC] [PubMed] [Google Scholar]
18. DiLillo DJ, Tan GS, Palese P, et al.
Широко нейтрализующие антитела, специфичные к стеблю гемагглютинина, требуют взаимодействия FcgammaR для защиты от вируса гриппа in vivo.
Нат Мед
2014;20(2):143–51. [Бесплатная статья PMC] [PubMed] [Google Scholar]
19. Gunn BM, Yu WH, Karim MM, et al.
Роль функции Fc в терапевтической защите от вируса Эбола, опосредованной моноклональными антителами.
Клеточный микроб-хозяин
2018;24(2):221–33
е5. [Статья бесплатно PMC] [PubMed] [Google Scholar]
*В этом исследовании используется машинное обучение для моделирования важности эффекторной функции антител в условиях инфекции Эбола.
20. Jegerlehner A, Schmitz N, Storni T, et al.
Вакцина против гриппа А на основе внеклеточного домена M2: слабая защита, опосредованная антителозависимой активностью NK-клеток.
Дж Иммунол
2004;172(9): 5598–605. [PubMed] [Google Scholar]
21. Коль С., Лоо Л.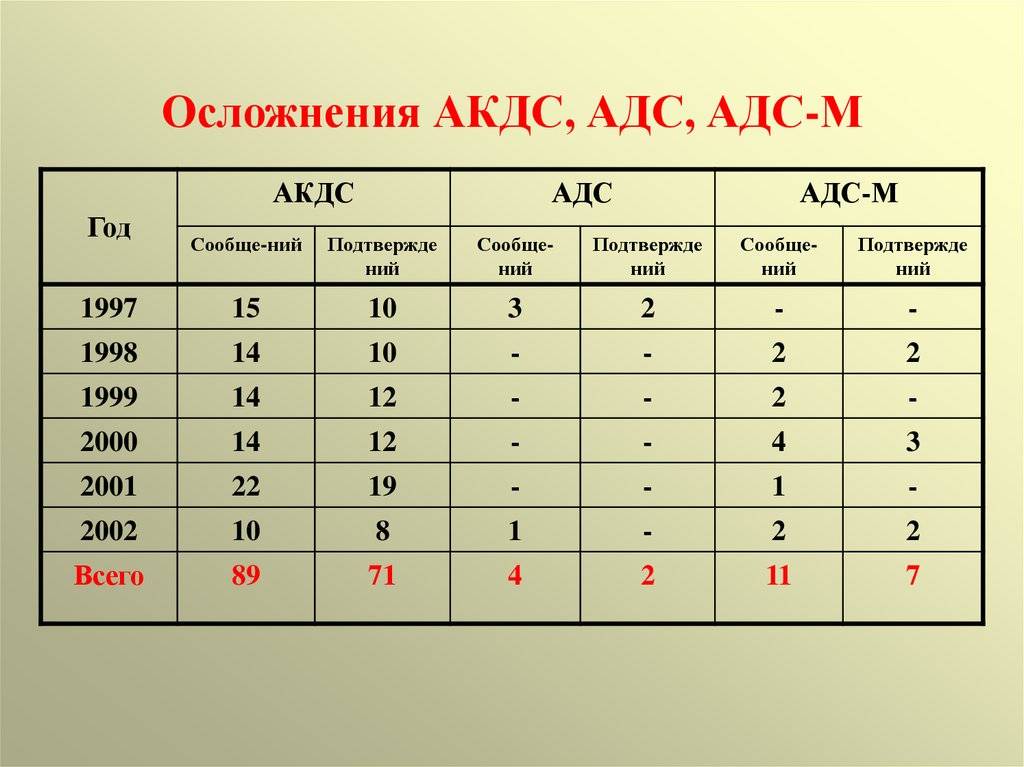 С. Защита новорожденных мышей от инфекции, вызванной вирусом простого герпеса: возможная антителозависимая клеточная цитотоксичность in vivo.
С. Защита новорожденных мышей от инфекции, вызванной вирусом простого герпеса: возможная антителозависимая клеточная цитотоксичность in vivo.
Дж Иммунол
1982;129(1):370–6. [PubMed] [Google Scholar]
22. Ши Дж., Макинтош Р.С., Плесс Р.Дж. Терапевтические средства на основе антител и Fc-рецепторов для лечения малярии.
Clin Sci (Лондон)
2006;110(1):11–9. [PubMed] [Google Scholar]
23. Warfield KL, Swenson DL, Olinger GG, et al.
Вакцина на основе частиц, подобных вирусу Эбола, защищает нечеловеческих приматов от летального заражения вирусом Эбола.
J заразить Dis
2007;196
Приложение 2:S430–7. [PubMed] [Google Scholar]
24. Chung AW, Ghebremichael M, Robinson H, et al.
Полифункциональные профили Fc-эффектора, опосредованные отбором подкласса IgG, отличают вакцины RV144 и VAX003.
Sci Transl Med
2014;6(228):228ra38. [PubMed] [Google Scholar]
25. Tomaras GD, Ferrari G, Shen X, et al.
Вакцино-индуцированный плазменный IgA, специфичный к области C1 оболочки ВИЧ-1, блокирует связывание и эффекторную функцию IgG.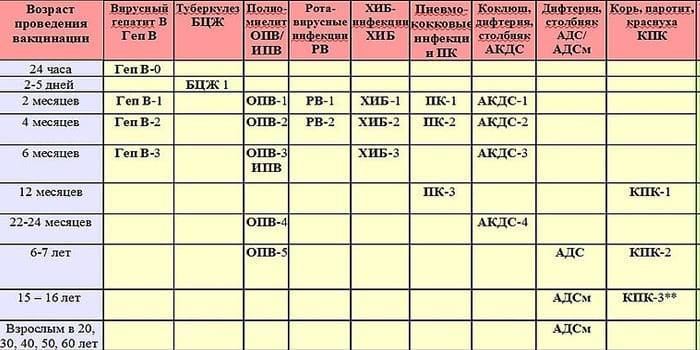
Труды Национальной академии наук Соединенных Штатов Америки
2013;110(22):9019–24. [Бесплатная статья PMC] [PubMed] [Google Scholar]
26. Doria-Rose NA, Altae-Tran HR, Roark RS, et al.
Картирование ответов поликлональных антител к ВИЧ-1 с помощью дактилоскопирования нейтрализации нового поколения.
PLoS Патог
2017;13(1):e1006148. [Статья бесплатно PMC] [PubMed] [Google Scholar]
*В этом исследовании сообщается о широко используемом подходе на основе машинного обучения для определения эпитопной специфичности нейтрализующих антител, присутствующих в поликлональных образцах сыворотки.
27. Георгиев И.С., Дориа-Роуз Н.А., Чжоу Т. и соавт.
Определение распознавания антител в поликлональных сыворотках по образцам нейтрализации изолята ВИЧ-1.
Наука
2013;340(6133):751–6. [PubMed] [Академия Google]
28. Реркс-Нгарм С., Питисуттитум П., Нитайапхан С. и соавт.
Вакцинация ALVAC и AIDSVAX для предотвращения заражения ВИЧ-1 в Таиланде.
N Engl J Med
2009;361(23):2209–20. [PubMed] [Google Scholar]
29. Edlefsen PT, Rolland M, Hertz T, et al.
Edlefsen PT, Rolland M, Hertz T, et al.
Комплексный ситовой анализ прорывных последовательностей ВИЧ-1 в испытании эффективности вакцины RV144.
вычислительная биология PLoS
2015;11(2):e1003973. [Бесплатная статья PMC] [PubMed] [Google Scholar]
30. Fong Y, Shen X, Ashley VC, et al.
Модификация связи между Т-клеточным иммунным ответом и риском инфицирования вирусом иммунодефицита человека типа 1 с помощью вакцин-индуцированного ответа антител в исследовании HVTN 505.
J заразить Dis
2018;217(8):1280–8. [Бесплатная статья PMC] [PubMed] [Google Scholar]
*Данное исследование представляет собой пример анализа случай-контроль в отношении вакцины, которая не соответствовала общим критериям конечной точки эффективности.
31. Janes HE, Cohen KW, Frahm N, et al.
Более высокие Т-клеточные ответы, индуцированные ДНК/rAd5 профилактической вакциной против ВИЧ-1, связаны с более низким риском инфицирования ВИЧ-1 в испытании эффективности.
J заразить Dis
2017;215(9):1376–85. [Бесплатная статья PMC] [PubMed] [Google Scholar]
32. Li SS, Gilbert PB, Tomaras GD, et al.
Li SS, Gilbert PB, Tomaras GD, et al.
Полиморфизмы FCGR2C ассоциируются с защитой вакцины против ВИЧ-1 в испытании RV144.
Джей Клин Инвест
2014;124(9): 3879–90. [Бесплатная статья PMC] [PubMed] [Google Scholar]
33. Prentice HA, Tomaras GD, Geraghty DE, et al.
Гены HLA класса II модулируют индуцированный вакциной ответ антител, чтобы повлиять на приобретение ВИЧ-1.
Sci Transl Med
2015;7(296):296ra112. [Бесплатная статья PMC] [PubMed] [Google Scholar]
34. Rolland M, Edlefsen PT, Larsen BB, et al.
Повышена эффективность вакцины против ВИЧ-1 против вирусов с генетическими сигнатурами в Env V2.
Природа
2012;490(7420):417–20. [Бесплатная статья PMC] [PubMed] [Google Scholar]
35. Perez LG, Martinez DR, deCamp AC, et al.
V1V2-специфический активирующий комплемент сывороточный IgG как коррелят снижения риска инфицирования ВИЧ-1 при RV144.
PLoS один
2017;12(7):e0180720. [Бесплатная статья PMC] [PubMed] [Google Scholar]
36. Yates NL, Liao HX, Fong Y, et al.
Индуцированный вакциной Env V1-V2 IgG3 коррелирует с более низким риском инфицирования ВИЧ-1 и снижается вскоре после вакцинации.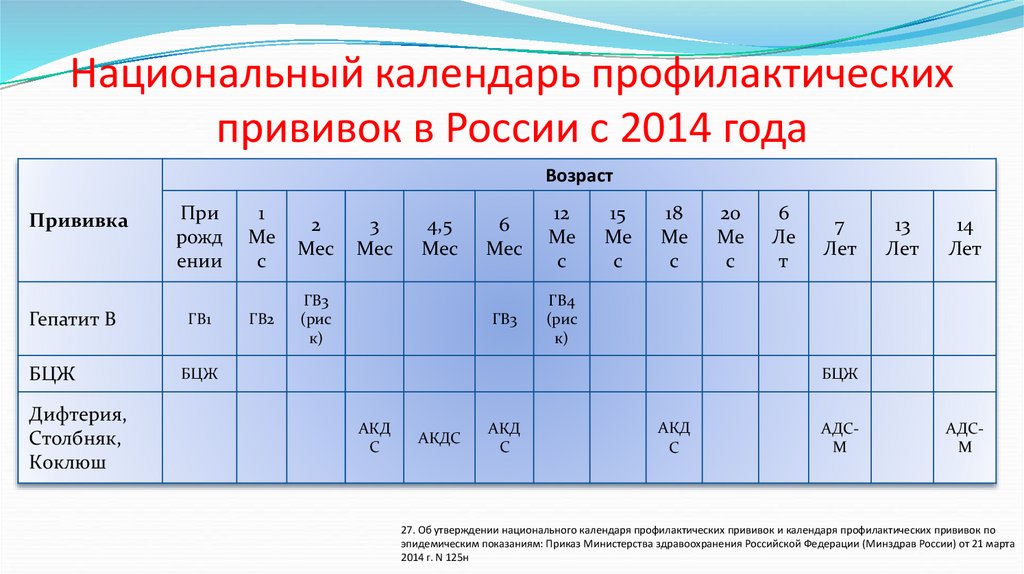
Sci Transl Med
2014;6(228):228ra39. [Бесплатная статья PMC] [PubMed] [Google Scholar]
37. Zolla-Pazner S, deCamp A, Gilbert PB, et al.
Вакцино-индуцированные IgG-антитела к областям V1V2 нескольких подтипов ВИЧ-1 коррелируют со снижением риска заражения ВИЧ-1.
PLoS один
2014;9(2):e87572. [Бесплатная статья PMC] [PubMed] [Google Scholar]
38. Haynes BF, Gilbert PB, McElrath MJ, et al.
Иммунокорреляционный анализ испытаний эффективности вакцины против ВИЧ-1.
N Engl J Med
2012;366(14):1275–86. [Бесплатная статья PMC] [PubMed] [Google Scholar]
39. Ackerman ME, Das J, Pittala S, et al.
Путь иммунизации определяет множество механизмов вакциноопосредованной защиты от ВИО.
Нат Мед
2018. [Статья бесплатно PMC] [PubMed]
**Это исследование показывает обобщение коррелятов защиты, выявленных для вакцины с аденовирусным вектором, оцененной в NHP, и схемы, подобной RV144, протестированной в NHP. Подмножество коррелятов было дополнительно подтверждено у людей.
40. Брэдли Т., Поллара Дж., Сантра С. и др.
Брэдли Т., Поллара Дж., Сантра С. и др.
Пентавалентная вакцина против ВИЧ-1 защищает от заражения вирусом иммунодефицита обезьян и человека.
Нац Коммуна
2017;8:15711. [Статья бесплатно PMC] [PubMed] [Google Scholar]
**Это исследование выявляет корреляты защиты и различает группы иммунизации, а также служит в качестве независимой когорты для проверки модели защиты, полученной из схемы вакцинации против аденовируса и белка.
41. Neidich SD, Fong Y, Li SS, et al.
Функции Fc-эффектора антитела снижают риск заражения ВИЧ-1 у вакцинированных людей. в ревизии
**Данное исследование подтверждает корреляты защиты, наблюдаемые в двух более ранних исследованиях NHP в клинике.
42. Ричардсон С.И., Чанг А.В., Натараджан Х. и др.
Эффекторная функция ВИЧ-специфического Fc на ранних стадиях инфекции предсказывает развитие широко нейтрализующих антител.
PLoS Патог
2018;14(4):e1006987. [Бесплатная статья PMC] [PubMed] [Google Scholar]
*Это исследование определяет различия в раннем иммунном ответе, которые отличают субъектов, у которых будут вырабатываться широко нейтрализующие антитела, от тех, у кого этого не происходит.
43. Lai JI, Licht AF, Dugast AS, et al.
Различные подклассы антител и профили специфичности, но не защитные аллели HLA-B, связаны с вариабельной эффекторной функцией антител среди контролеров ВИЧ-1.
Журнал вирусологии
2014;88(5):2799–809. [Бесплатная статья PMC] [PubMed] [Google Scholar]
44. Vaccari M, Gordon SN, Fourati S, et al.
Адъювантно-зависимые врожденные и адаптивные иммунные сигнатуры риска заражения SIVmac251.
Нат Мед
2016;22(7):762–70. [Бесплатная статья PMC] [PubMed] [Google Scholar]
45. Huang Y, Ferrari G, Alter G и др.
Разнообразие эффекторной активности противовирусных IgG, наблюдаемое у ВИЧ-инфицированных и вакцинированных субъектов.
Дж Иммунол
2016;197(12):4603–12. [Бесплатная статья PMC] [PubMed] [Google Scholar]
46. Акерман М.Е., Михайлова А., Браун Е.П., и соавт.
Реакция полифункциональных ВИЧ-специфических антител связана со спонтанным контролем над ВИЧ.
PLoS Патог
2016;12(1):e1005315. [Бесплатная статья PMC] [PubMed] [Google Scholar]
47. Fourati S, Ribeiro SP, Blasco Tavares Pereira Lopes F, et al.
Fourati S, Ribeiro SP, Blasco Tavares Pereira Lopes F, et al.
Интегрированный системный подход определяет противовирусные пути, обеспечивающие защиту с помощью вакцины против ВИЧ RV144.
Нац Коммуна
2019;10(1):863. [Бесплатная статья PMC] [PubMed] [Google Scholar]
*Это исследование связывает профили транскрипции с гуморальными реакциями и результатами эффективности вакцин.
48. Francica JR, Zak DE, Linde C, et al.
Врожденные транскрипционные эффекты адъювантов на величину, качество и устойчивость реакций оболочки ВИЧ в NHP.
Кровь Adv
2017;1(25):2329–42. [Бесплатная статья PMC] [PubMed] [Google Scholar]
49. Choi I, Chung AW, Suscovich TJ, et al.
Методы машинного обучения позволяют проводить прогнозное моделирование характеристик антител: функциональных взаимосвязей у вакцин против RV144.
вычислительная биология PLoS
2015;11(4):e1004185. [Бесплатная статья PMC] [PubMed] [Google Scholar]
50. Alter G, Dowell KG, Brown EP, et al.
Определение гуморального иммунного ответа с высоким разрешением коррелирует с эффективным иммунитетом против ВИЧ.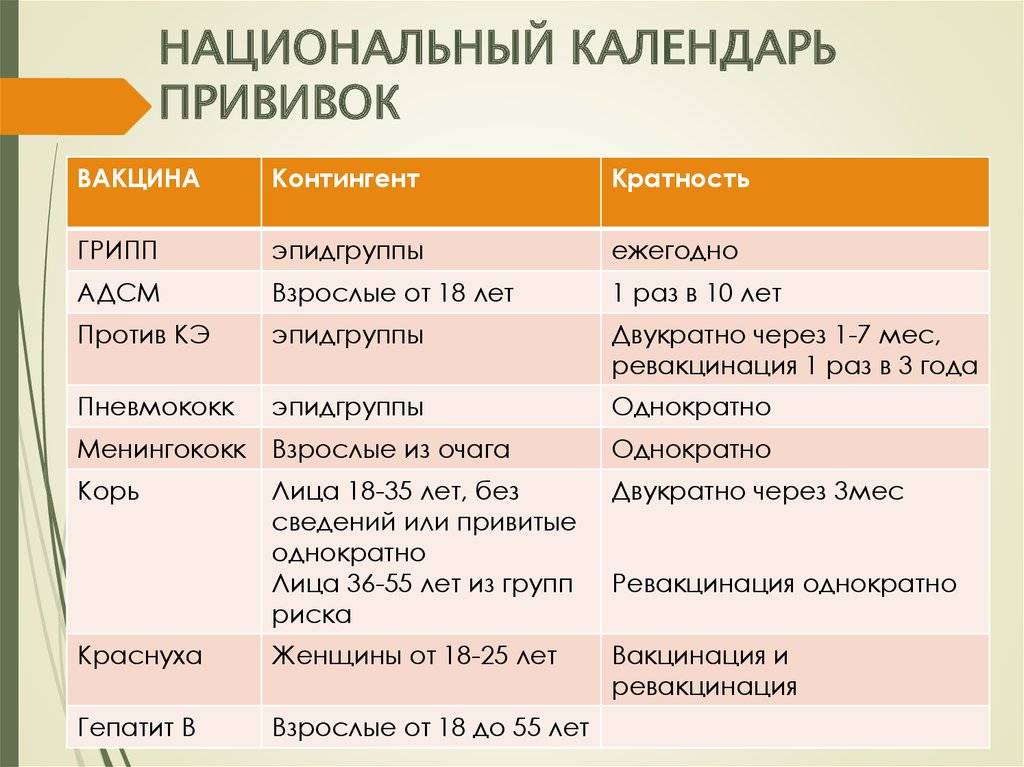
Мол Сист Биол
2018;14(3):e7881. [Бесплатная статья PMC] [PubMed] [Google Scholar]
**В этом исследовании используется профилирование гуморального ответа для дифференциации ВИЧ-инфицированных субъектов, которые прогрессируют, от тех, кто контролирует вирус, и определяют характеристики функционально сильных антител. Выявленные особенности соответствуют биологической интуиции, а некоторые из них были подтверждены экспериментально.
51. Гийон И, Андр, #233, и др.
Введение в выбор переменных и признаков.
J Mach Узнать Res
2003;3:1157–82. [Google Scholar]
52. Briney B, Inderbitzin A, Joyce C, et al.
Общность, несмотря на исключительное разнообразие исходного репертуара человеческих антител.
Природа
2019;566(7744):393–7. [Бесплатная статья PMC] [PubMed] [Google Scholar]
** В этом документе определяется степень сходства и различий между последовательностями иммуноглобулина у разных субъектов. Он представляет собой технический подвиг и проливает свет на потенциальную ценность и обобщаемость наблюдений, связанных с данными секвенирования антител.
53. Kwong PD, Chuang GY, DeKosky BJ, et al.
Антителомика: биоинформатические технологии для понимания В-клеточного иммунитета к ВИЧ-1.
Иммунол Rev
2017;275(1):108–28. [Статья бесплатно PMC] [PubMed] [Google Scholar]
*Эта статья представляет собой поучительный обзор подходов к секвенированию антител и их ценности для иммунобиологии, разработки и оценки вакцин.
54. Lee J, Paparoditis P, Horton AP, et al.
Стойкие клонотипы антител доминируют в реакции сыворотки на грипп в течение нескольких лет и при повторных вакцинациях.
Клеточный микроб-хозяин
2019;25(3):367–76 e5. [Статья бесплатно PMC] [PubMed] [Google Scholar]
*Это исследование сопоставляет последовательности антител, специфичных для гриппа, с соответствующими белковыми продуктами в сыворотке и отслеживает клональные семейства с течением времени у субъекта. Подобные исследования привели к важному пониманию разнообразия сывороточных антител-оме, а также пролили свет на потенциальные различия в репертуарах последовательностей антител между различными типами В-клеток.
55. Eyer K, Doineau RCL, Castrillon CE, et al.
Одноклеточное глубокое фенотипирование IgG-секретирующих клеток для иммунного мониторинга с высоким разрешением.
Нат Биотехнолог
2017;35(10):977–82. [PubMed] [Google Scholar]
** В этой статье описывается микрожидкостный подход к инкапсуляции и оценке антител, секретируемых отдельными В-клетками. В этом исследовании сообщается о скорости секреции и сродстве, но подход может быть адаптирован к другим интересующим оценкам.
56. Sanchez-Lockhart M, Reyes DS, Gonzalez JC, et al.
Качественное профилирование гуморального иммунного ответа, вызванного rVSV-DeltaG-EBOV-GP, с использованием системного серологического анализа, программируемых массивов доменов.
Представитель ячейки
2018;24(4):1050–9е5. [PubMed] [Google Scholar]
57. Xu GJ, Kula T, Xu Q, et al.
Вирусная иммунология. Комплексное серологическое профилирование человеческих популяций с использованием синтетического вирома человека.
Наука
2015;348(6239):ааа0698. [Бесплатная статья PMC] [PubMed] [Google Scholar]
[Бесплатная статья PMC] [PubMed] [Google Scholar]
58. Bianchi M, Turner HL, Nogal B, et al.
Картирование эпитопов на основе электронной микроскопии определяет специфичность поликлональных антител, вырабатываемых во время иммунизации тримером оболочки ВИЧ-1 BG505.
Иммунитет
2018;49(2):288–300
е8. [Бесплатная статья PMC] [PubMed] [Google Scholar]
*В этом документе описывается, как образцы поликлональной сыворотки могут быть оценены на их эпитопную специфичность с помощью электронной микроскопии. Определение эпитопов, распознаваемых смесями антител, в прошлом было сложной задачей, и этот прогресс может оказаться полезным.
59. Lopez R, Regier J, Cole MB, et al.
Глубокое генеративное моделирование для транскриптомики одиночных клеток.
Нат Методы
2018;15(12):1053–1058. [Бесплатная статья PMC] [PubMed] [Google Scholar]
** В этой статье описывается значительный прогресс в анализе данных секвенирования РНК одиночных клеток, обеспечиваемый байесовским глубоким обучением.
60. Way GP, Greene CS. Байесовское глубокое обучение для анализа отдельных клеток.
Нат Методы
2018;15(12):1009–10. [PubMed] [Google Scholar]
61. Мессина Н.Л., Циммерманн П., Кертис Н. Влияние вакцин на гетерологичный адаптивный иммунитет.
Клин микробиол инфекция
2019. [PubMed]
*Это один из серии обзоров, посвященных гетерологичному или обученному иммунитету.
62. Sanchez-Ramon S, Conejero L, Netea MG, et al.
Вакцины на основе обученного иммунитета: новая парадигма разработки противоинфекционных составов широкого спектра действия.
Фронт Иммунол
2018;9:2936. [Бесплатная статья PMC] [PubMed] [Google Scholar]
*Это один из набора обзоров, посвященных гетерологичному или тренированному иммунитету.
63. Утхаякумар Д., Пэрис С., Чапат Л. и др.
Неспецифические эффекты вакцин, проиллюстрированные на примере БЦЖ: от наблюдений к демонстрациям.
Фронт Иммунол
2018;9:2869. [Бесплатная статья PMC] [PubMed] [Google Scholar]
*Это один из набора обзоров, посвященных гетерологичному или тренированному иммунитету.
64. Чанг А.В., Кумар М.П., Арнольд К.Б. и др.
Анализ гуморального иммунитета против ВИЧ, индуцированного поликлональной вакциной, с использованием системной серологии.
Клетка
2015;163(4):988–98. [Бесплатная статья PMC] [PubMed] [Google Scholar]
65. Fouts TR, Bagley K, Prado IJ, et al.
Баланс клеточного и гуморального иммунитета определяет уровень защиты вакцинами против ВИЧ в моделях ВИЧ-инфекции у макак-резусов.
Труды Национальной академии наук Соединенных Штатов Америки
2015. [Бесплатная статья PMC] [PubMed]
66. Jones AT, Shen X, Walter KL, et al.
Вакцинация против ВИЧ-1 с помощью безыгольной пероральной инъекции вызывает сильный иммунитет слизистых оболочек и защищает от заражения SHIV.
Нац Коммуна
2019;10(1):798. [Бесплатная статья PMC] [PubMed] [Google Scholar]
*В этом исследовании исследуется путь и способ иммунизации при NHP. Подходы ML идентифицируют ответы Т-клеток и зависимое от антител ингибирование клеточного вируса как корреляты защиты.
67. Malherbe DC, Mendy J, Vang L, et al.
Malherbe DC, Mendy J, Vang L, et al.
Комбинированные аденовирусные и белковые вакцины предотвращают инфекцию или снижают вирусную нагрузку после заражения слизистых оболочек гетерологичным вирусом иммунодефицита обезьяны-человека Clade C.
Джей Вирол
2018;92(2). [Бесплатная статья PMC] [PubMed] [Google Scholar]
68. Sui Y, Lewis GK, Wang Y, et al.
Эффективность мукозальной вакцины против интраректального SHIV не зависит от ответа антител против Env.
Джей Клин Инвест
2019;129(3):1314–28. [Статья бесплатно PMC] [PubMed] [Google Scholar]
**Это исследование связывает понятие тренированного иммунитета с условиями ВИЧ-инфекции, демонстрируя, что связанные с вакциной изменения в микробиоме кишечника могут быть связаны с результатами защиты, в отличие от прямого результате адаптивного иммунитета.
69. Barouch DH, Alter G, Broge T, et al.
Защитная эффективность аденовирусных/белковых вакцин против заражения SIV у макак-резусов.
Наука
2015;349(6245): 320–4. [Бесплатная статья PMC] [PubMed] [Google Scholar]
70. Парки C
Парки C
G-106 Вакцинация слизистой оболочки способной к репликации VSV-HIV-химерой, доставляющей тримеры Env, защищает макак-резусов от ректальной инфекции SHIV.
Журнал JAIDS о синдромах приобретенного иммунодефицита
2017;74:58. [Google Scholar]
71. Singh S, Ramirez-Salazar EG, Doueiri R, et al.
Контроль инфицирования гетерологичным вирусом иммунодефицита обезьян SIVsmE660 с помощью схем коиммунизации ДНК и белков в сочетании с различными адъювантами на основе толл-подобных рецепторов-4 у макак.
Джей Вирол
2018;92(15). [Статья бесплатно PMC] [PubMed] [Google Scholar]
*Это исследование обнаруживает связь между реакцией антител слизистой оболочки и защитой от инфекции, что служит хорошим напоминанием о важности иммунитета на передовой и важности определения профиля Ig слизистой оболочки. как дополнение к оценке сывороточного Ig.
72. Садананд С., Дас Дж., Чанг А.В. и др.
Временная изменчивость ВИЧ-специфических антител подкласса IgG во время острой инфекции отличает спонтанных контролеров от хронических прогрессоров.
СПИД
2018;32(4):443–50. [Бесплатная статья PMC] [PubMed] [Google Scholar]
*Это исследование выявляет различия во времени индукции ответов IgG2 и IgG3, нацеленных на оболочку, как дискриминаторов между прогрессорами и контроллерами.
73. Лофано Г., Горман М.Дж., Юсиф А.С. и соавт.
Гликозилирование Fc антиген-специфического антитела усиливает гуморальный иммунитет за счет рекрутирования комплемента.
Научный Иммунол
2018;3(26). [Бесплатная статья PMC] [PubMed] [Google Scholar]
** В этом исследовании используются наблюдения ML, примененные к когорте субъектов, у которых вырабатываются и не вырабатываются нейтрализующие антитела широкого спектра, и продолжается экспериментальная связь фенотипических различий с механизмом, посредством которого гуморальные можно повысить иммунитет. Это захватывающий пример открытия новой биологии на основе паттернов, выявленных с помощью машинного обучения.
74. Cheng HD, Grimm SK, Gilman MS, et al.
Тонкая сигнатура эпитопа широты нейтрализации антител в сайте связывания CD4 оболочки ВИЧ-1.
JCI Insight
2018;3(5). [Статья бесплатно PMC] [PubMed] [Google Scholar]
*Это исследование определяет сигнатуры уровня аминокислот эпитопов CD4bs-специфических нейтрализующих антител в панели моноклональных антител, а также в наборе поликлональных образцов сыворотки.
75. Миллер-Новак Л.К., Дас Дж., Мюзик Т.А., и соавт.
Анализ комплемент-опосредованного лизиса вируса иммунодефицита обезьян (SIV) и SIV-инфицированных клеток выявляет половые различия в индуцированных вакцинами иммунных реакциях у макак-резусов.
Джей Вирол
2018;92(19). [Статья бесплатно PMC] [PubMed] [Google Scholar]
*Это продолжение исследования иммунизации NHP фокусируется на различиях в иммунном ответе, связанном с полом, и при этом указывает на эту переменную как на потенциально важный модификатор ответа на вакцину и/или эффективность.
76. Barouch DH, Tomaka FL, Wegmann F, et al.
Оценка мозаичной вакцины против ВИЧ-1 в многоцентровом рандомизированном двойном слепом плацебо-контролируемом клиническом исследовании фазы ½a (APPROACH) и на макаках-резусах (NHP 13–19). ).
).
Ланцет
2018;392(10143):232–43. [Бесплатная статья PMC] [PubMed] [Google Scholar]
*В этом исследовании сообщается об иммуногенности новой вакцины против ВИЧ у людей, а также о ее соответствующем профиле и результатах защиты в модели NHP.
77. Дугаст А.С., Стамататос Л., Тонелли А. и соавт.
Независимая эволюция Fc- и Fab-опосредованной активности ВИЧ-1-специфических противовирусных антител после острой инфекции.
Евр Дж Иммунол
2014;44(10):2925–37. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Системная серология для расшифровки инфекции и индуцированного вакциной гуморального ответа на ВИЧ-1
Обзор
. 2019 июль; 14 (4): 253-264.
doi: 10.1097/COH.0000000000000558.
Шривамши Питтала
1
, Кайл С Моррисон
2
, Маргарет Э. Акерман
Акерман
2
3
Принадлежности
- 1 Кафедра компьютерных наук.
- 2 Программа молекулярной и клеточной биологии.
- 3 Инженерная школа Тайера, Дартмутский колледж, Ганновер, Нью-Гемпшир, США.
PMID:
31033729
PMCID:
PMC6581188
DOI:
10.1097/COH.0000000000000558
Бесплатная статья ЧВК
Обзор
Шривамши Питтала и др.
Curr Opin ВИЧ СПИД.
2019июль
Бесплатная статья ЧВК
. 2019 июль; 14 (4): 253-264.
doi: 10.1097/COH.0000000000000558.
Авторы
Шривамши Питтала
1
, Кайл С Моррисон
2
, Маргарет Э. Акерман
2
3
Принадлежности
- 1 Кафедра компьютерных наук.
- 2 Программа молекулярной и клеточной биологии.
- 3 Инженерная школа Тайера, Дартмутский колледж, Ганновер, Нью-Гемпшир, США.

PMID:
31033729
PMCID:
PMC6581188
DOI:
10.1097/COH.0000000000000558
Абстрактный
Цель обзора:
Экспериментальные и аналитические достижения позволили проводить систематические исследования гуморальных иммунных реакций с высоким разрешением и начинают определять механизмы иммунитета к ВИЧ.
Недавние выводы:
Высокопроизводительные, богатые информацией экспериментальные и аналитические методы, будь то геномные, протеомные или транскриптомные, прочно закрепили свою ценность в самых разных областях. Рассмотрение этих инструментов как траулеров в «рыболовных экспедициях» исчезло, поскольку «открытие на основе данных» стало цениться как незаменимое средство для развития фундаментального понимания биологических систем. В совокупности исследования ВИЧ-1-инфекции и вакцинации, включая функциональные, биофизические и биохимические подходы к гуморальному профилированию, позволили получить представление о фенотипических характеристиках отдельных антител и пулов антител. Связывание этих показателей с клиническим статусом, результатами защиты/эффективности и данными клеточного профилирования с использованием машинного обучения дало возможность выявить непредвиденные механизмы действия и получить представление об основных иммунологических процессах, которые в противном случае было бы трудно расшифровать.
Рассмотрение этих инструментов как траулеров в «рыболовных экспедициях» исчезло, поскольку «открытие на основе данных» стало цениться как незаменимое средство для развития фундаментального понимания биологических систем. В совокупности исследования ВИЧ-1-инфекции и вакцинации, включая функциональные, биофизические и биохимические подходы к гуморальному профилированию, позволили получить представление о фенотипических характеристиках отдельных антител и пулов антител. Связывание этих показателей с клиническим статусом, результатами защиты/эффективности и данными клеточного профилирования с использованием машинного обучения дало возможность выявить непредвиденные механизмы действия и получить представление об основных иммунологических процессах, которые в противном случае было бы трудно расшифровать.
Резюме:
Недавние данные показывают, что систематический сбор данных и применение подходов машинного обучения могут идентифицировать гуморальные иммунные корреляты, которые можно обобщить для различных иммуногенов ВИЧ-1 и схем вакцинации и которые можно перевести между модельными организмами и клиникой. Эти результаты дают убедительное обоснование полезности и дальнейшего расширения этих подходов как для поддержки разработки вакцин, так и в более широком смысле для определения механизмов иммунитета.
Эти результаты дают убедительное обоснование полезности и дальнейшего расширения этих подходов как для поддержки разработки вакцин, так и в более широком смысле для определения механизмов иммунитета.
Заявление о конфликте интересов
Цифры
Рисунок 1. Особенности ответа антител.
Рисунок 1. Особенности ответа антител.
Вариабельный домен Ig (Fv), ответственный за патоген…
Рисунок 1. Особенности ответа антител.
Вариабельный домен Ig (Fv), ответственный за распознавание патогена, различается по своей антигенной и эпитопной специфичности, авидности, аффинности и широте распознавания, а также по тому, приводит ли это распознавание к нейтрализации инфекционности.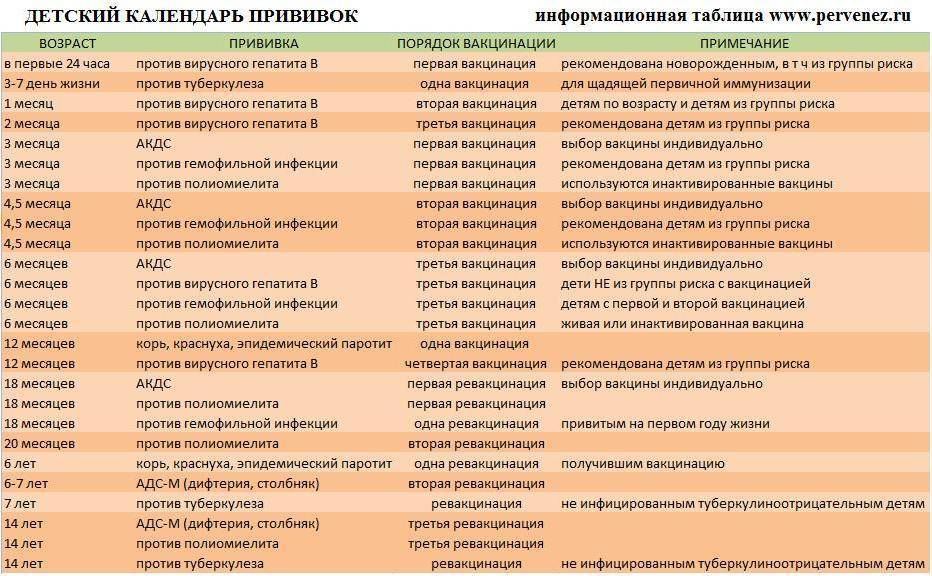 Константный или кристаллизуемый домен (Fc), ответственный за распознавание врожденным иммунитетом, различается по изотипу, подклассу и профилю гликозилирования, которые влияют на сродство антитела к Fc-рецепторам и классу(ам) Fc-рецепторов, способных взаимодействовать. Изображение из документа: 10.2210/rcsb_pdb/mom_2001_9.
Константный или кристаллизуемый домен (Fc), ответственный за распознавание врожденным иммунитетом, различается по изотипу, подклассу и профилю гликозилирования, которые влияют на сродство антитела к Fc-рецепторам и классу(ам) Fc-рецепторов, способных взаимодействовать. Изображение из документа: 10.2210/rcsb_pdb/mom_2001_9.
Рисунок 2. Примеры гуморального иммунного ответа…
Рисунок 2. Примеры анализа гуморального иммунного ответа, поддерживаемого машинным обучением.
Неконтролируемые методы (вверху)…
Рисунок 2. Примеры анализа гуморального иммунного ответа, поддерживаемого машинным обучением.
Неконтролируемые методы (вверху), включая анализ основных компонентов (слева), иерархическую кластеризацию (в центре) и корреляционные сети (справа), отображают основные аспекты вариаций, величин и лежащих в основе взаимосвязей между гуморальными характеристиками реакции и субъектами. Методы с учителем (внизу) моделируют, как данные можно использовать для прогнозирования интересующих параметров, таких как группа (слева), активность антител (в центре) или результат заражения (справа).
Методы с учителем (внизу) моделируют, как данные можно использовать для прогнозирования интересующих параметров, таких как группа (слева), активность антител (в центре) или результат заражения (справа).
Рисунок 3. Оценка точности и надежности модели.
Рисунок 3. Оценка точности и надежности модели.
Левый . При повторной перекрестной проверке данные разбиваются…
Рисунок 3. Оценка точности и надежности модели.
Левый . При повторной перекрестной проверке данные разбиваются на разные обучающие и тестовые наборы. Модели, извлеченные из обучающих данных, применяются к пропущенным тестовым данным. Показанный пример изучает правила активности ADCP из крайних значений и применяет эти правила к образцам с промежуточной активностью.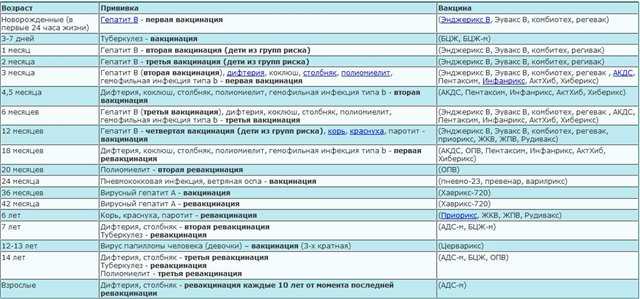 Центр . Точность производительности можно определить, характеризуя степень согласия между моделью и наблюдением для моделей классификации и регрессии. Справа . Перестановочное тестирование, при котором производительность рандомизированных данных сравнивается с фактическими данными, предлагает средства для оценки надежности модели. В этом случае фактические данные могут быть использованы для моделирования активности антител с такой же точностью, как экспериментальные данные могут быть воспроизведены экспериментально, и значительно лучше, чем когда модели изучаются на основе переставленных данных или контрольных данных, таких как данные, относящиеся к другому патогену. .
Центр . Точность производительности можно определить, характеризуя степень согласия между моделью и наблюдением для моделей классификации и регрессии. Справа . Перестановочное тестирование, при котором производительность рандомизированных данных сравнивается с фактическими данными, предлагает средства для оценки надежности модели. В этом случае фактические данные могут быть использованы для моделирования активности антител с такой же точностью, как экспериментальные данные могут быть воспроизведены экспериментально, и значительно лучше, чем когда модели изучаются на основе переставленных данных или контрольных данных, таких как данные, относящиеся к другому патогену. .
Рисунок 4. Оценка качества и достоверности модели.
Рисунок 4. Оценка качества и достоверности модели.
Левый . Качество прогноза, определяемое корреляцией…
Рисунок 4. Оценка качества и достоверности модели.
Левый . Качество прогноза, определяемое коэффициентом корреляции между моделями, прошедшими перекрестную проверку, полученными на основе фактических (зеленый) и пермутированных (черный) данных для набора из десяти эффекторных функций антител (A-J). Хотя производительность значительно различается (0,2 < r < 0,9) для моделей, извлеченных из реальных данных, переставленные данные постоянно дают практически случайную производительность (r ~ 0,1). Взаимосвязь между качеством прогнозирования и отношением сигнала к шуму, которая предполагает, что модели могут быть ограничены рабочими характеристиками анализов на основе клеток, такими как отношение сигнала к шуму (здесь) и воспроизводимость анализа (50). Справа . Биологическая валидность моделей может быть подтверждена предшествующими знаниями, такими как достоверность предсказаний активации NK типов антител, о которых известно, что они обладают такой активностью (IgG1 и IgG3) (49). ) и подтверждено экспериментально, например, путем наблюдения за снижением активности при истощении IgG3 (24).
) и подтверждено экспериментально, например, путем наблюдения за снижением активности при истощении IgG3 (24).
См. это изображение и информацию об авторских правах в PMC
Похожие статьи
Системная серология для оценки испытаний вакцины против ВИЧ.
Аккерман М.Э., Баруш Д.Х., Альтер Г.
Акерман М.Е. и соавт.
Immunol Rev. 2017 Jan; 275(1):262-270. doi: 10.1111/imr.12503.
Иммунол Ред. 2017.PMID: 28133810
Бесплатная статья ЧВК.Обзор.
Сравнение иммунного ответа взрослых и младенцев на ВИЧ-инфекцию и вакцинацию.
Мартинес Д.Р., Пермар С.Р., Фуда Г.Г.
Мартинес Д.Р. и соавт.
Клин Вакцина Иммунол. 2015 9 декабря; 23(2):84-94. doi: 10.1128/CVI.00565-15. Печать 2016 Февраль.
Клин Вакцина Иммунол. 2015.PMID: 26656117
Бесплатная статья ЧВК.Обзор.
Реакция антител у ВИЧ-1-инфицированных доноров.
Ричардсон С.И., Мур PL.
Ричардсон С.И. и соавт.
Curr Opin ВИЧ СПИД. 2019 июль; 14 (4): 233-239. doi: 10.1097/COH.0000000000000559.
Curr Opin ВИЧ СПИД. 2019.PMID: 31033730
Бесплатная статья ЧВК.Обзор.
Модуляция функциональных профилей Т-клеток CD4, индуцированных вакциной, путем изменения компонентов схем вакцинации против ВИЧ у людей.
Писсани Ф., Шульте Б., Эллер М.А., Шульц Б.Т., Ратто-Ким С., Марович М., Тонгчароен П., Шриплиенчан С., Реркс-Нгарм С., Питисуттитум П., Эссер С., Альтер Г., Робб М.Л., Ким Д.Х., Майкл Н.Л. , Стрик Х.
Писсани Ф. и др.
Дж Вирол. 2018 12 ноября; 92 (23): e01143-18. doi: 10.1128/ОВИ.01143-18. Печать 2018 1 декабря.
2018 12 ноября; 92 (23): e01143-18. doi: 10.1128/ОВИ.01143-18. Печать 2018 1 декабря.
Дж Вирол. 2018.PMID: 30209165
Бесплатная статья ЧВК.Широко нейтрализующие антитела: что необходимо, чтобы перейти от редкого случая инфекции ВИЧ-1 к эффективности вакцины?
Суббараман Х., Шанц М., Тркола А.
Суббараман Х. и др.
Ретровирусология. 2018 июл 28;15(1):52. doi: 10.1186/s12977-018-0433-2.
Ретровирусология. 2018.PMID: 30055627
Бесплатная статья ЧВК.Обзор.
Посмотреть все похожие статьи
Цитируется
Тензорно-структурированная декомпозиция улучшает системный серологический анализ.
Тан З.С., Мерфи М.С., Алпай Х.С., Тейлор С.Д., Мейер А.С.
Тан З. С. и соавт.
С. и соавт.
Мол Сист Биол. 2021 сен;17(9):e10243. doi: 10.15252/msb.202110243.
Мол Сист Биол. 2021.PMID: 34487431
Бесплатная статья ЧВК.Иммунопрофилирование коррелятов защиты от инфекции SHIV у макак-резусов, вакцинированных адъювантным белком оспы ВИЧ-1.
Лу П., Герин Д.Дж., Лин С., Чаудхури С., Акерман М.Е., Болтон Д.Л., Валлквист А.
Лу П. и др.
Фронт Иммунол. 2021 11 мая; 12:625030. дои: 10.3389/fimmu.2021.625030. Электронная коллекция 2021.
Фронт Иммунол. 2021.PMID: 34046030
Бесплатная статья ЧВК.Отличительные особенности и функции системного и слизисто-гуморального иммунитета у выздоравливающих лиц с SARS-CoV-2.
Батлер С.Э., Кроули А.Р., Натараджан Х., Сюй С., Вайнер Дж.А., Бобак К.




 Содержит те же элементы, что и АДС, но в меньшей дозе.
Содержит те же элементы, что и АДС, но в меньшей дозе.
 2018 12 ноября; 92 (23): e01143-18. doi: 10.1128/ОВИ.01143-18. Печать 2018 1 декабря.
2018 12 ноября; 92 (23): e01143-18. doi: 10.1128/ОВИ.01143-18. Печать 2018 1 декабря. С. и соавт.
С. и соавт.