Содержание
Своевременная вакцинация — надёжная защита от инфекционных болезней.
Инфекционные болезни во все времена были главными врагами человека. История знает множество примеров опустошительных последствий оспы, чумы, холеры, тифа, дизентерии, кори, гриппа.
Вакцинация – это самое эффективное и экономически выгодное средство защиты против инфекционных болезней, известных современной медицине. Тяжёлые страдания, которые причиняли инфекции в прошлом, должны служить постоянным напоминанием о необходимости своевременного проведения профилактических прививок.
Вакцины позволили человечеству достичь невероятных результатов в борьбе с инфекциями. В мире полностью ликвидирована натуральная оспа — заболевание, ежегодно уносившее жизни миллионов человек. Практически исчез полиомиелит, продолжается глобальная ликвидация кори. В сотни и даже тысячи раз снижена заболеваемость дифтерией, краснухой, коклюшем, эпидемическим паротитом, вирусным гепатитом B и многими другими
опасными инфекционными заболеваниями.
Как свидетельствует мировой опыт, прекращение массовой иммунизации даже при ничтожно малой заболеваемости ведёт к возвращению инфекционных заболеваний и развитию эпидемий.
Классические вакцинные препараты можно разделить на три группы:
- Живые вакцины
Действующим началом в них служат ослабленные микроорганизмы, потерявшие способность вызывать заболевание, но стимулирующие иммунный ответ. К этой группе относятся вакцины против кори, краснухи, полиомиелита, эпидемического паротита и гриппа.
- Инактивированные вакцины
Они содержат убитые патогенные микроорганизмы или их фрагменты. Примером служат вакцины против гриппа, клещевого энцефалита, бешенства, брюшного тифа.
- Анатоксины— бактериальные токсины в измененной безвредной форме.
К ним относятся известные и широко применяемые вакцины против дифтерии, столбняка, коклюша.
В рамках Национального календаря профилактических прививок обязательными являются следующие прививки.
Всем не имеющим прививок против дифтерии и столбняка, проводится вакцинация (состоит из 2-х прививок) и ревакцинация. В последующем ревакцинации проводятся каждые 10 лет от последней прививки.
Вакцинация против вирусного гепатита В проводится лицам в возрасте до 55 лет, не привитым ранее. Вакцинальный комплекс состоит их 3-х прививок.
Всем лицам до 35 лет не привитым ранее против кори, не болевшим корью, не имеющим сведений о прививках против кори проводятся две прививки с интервалом не менее 3-х месяцев. Лицам, привитым однократно, проводится ревакцинация против кори.
Вакцинации против краснухи подлежат девушки и женщины от 18 до 25 лет, не болевшие краснухой, не привитые ранее, не имеющие сведений о прививках против краснухи, привитые однократно.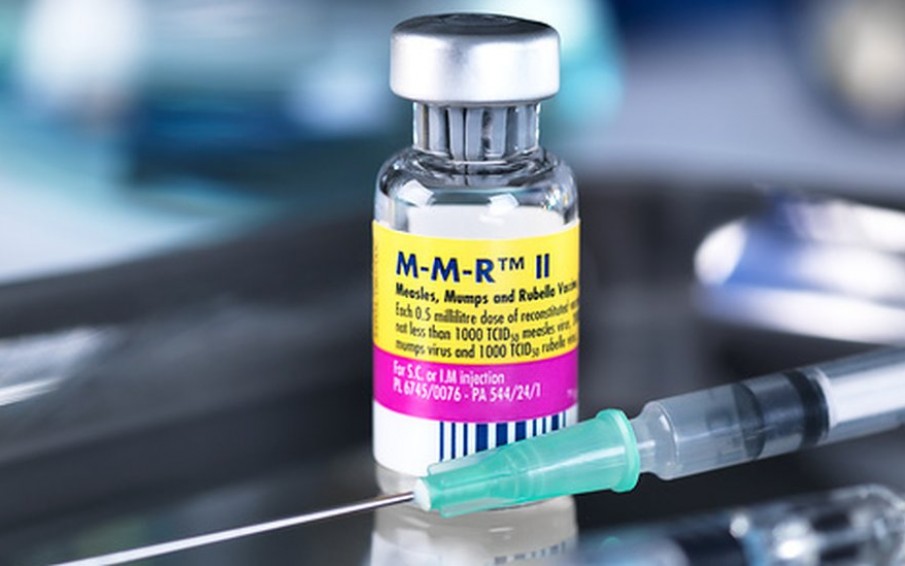
Вакцинация против гриппа проводится ежегодно лицам из групп риска – медицинским работникам, работникам образования, транспорта, сферы обслуживания, студентам высших и средних учебных заведений, лицам старше 60 лет, лицам, подлежащим призыву на военную службу; лицам с хроническими заболеваниями, в том числе с заболеваниями легких, сердечно-сосудистыми заболеваниями, метаболическими нарушениями и ожирением.
Бывают ли осложнения после прививок?
Современные вакцины не вызывают серьезных побочных реакций. Возможна болезненность в месте введения, легкое повышение температуры, очень редко — аллергические реакции. Эти явления быстро проходят сами. Общая частота каких-либо побочных явлений составляет 2-5%.
Перечень медицинских противопоказаний к проведению профилактических прививок:
- Все вакцины — сильная реакция или поствакцинальное осложнение на предыдущее введение
- Всеживыевакцины,в т.
 ч. оральная живая полиомиелитная вакцина (ОПВ) — иммунодефицитное состояние (первичное), иммуносупрессия, злокачественные новообразования. Беременность.
ч. оральная живая полиомиелитная вакцина (ОПВ) — иммунодефицитное состояние (первичное), иммуносупрессия, злокачественные новообразования. Беременность. - БЦЖ — вес ребёнка при рождении менее 2000 г., келоидный рубец, в том числе после предыдущей дозы
- АКДС — прогрессирующие заболевания нервной системы, афебрильные судороги в анамнезе
- Живая кореваявакцина(ЖКВ), живая паротитнаявакцина|(ЖПВ),краснушная,атакже комбинированныеди- и тривакцины(корь-паротит, |корь-краснуха-паротит)
- Вакцина против вирусного гепатита В — аллергическая реакция на пекарские дрожжи
- Вакцины АДС, АДС-М, АД-М — постоянных противопоказаний не имеют
*Острые инфекционные и неинфекционные заболевания, обострение хроническихзаболеванийявляютсявременнымипротивопоказаниями для проведения прививок. Плановые прививки проводятся через 2-4недели после выздоровления или в периодреконвалесценцииилиремиссии.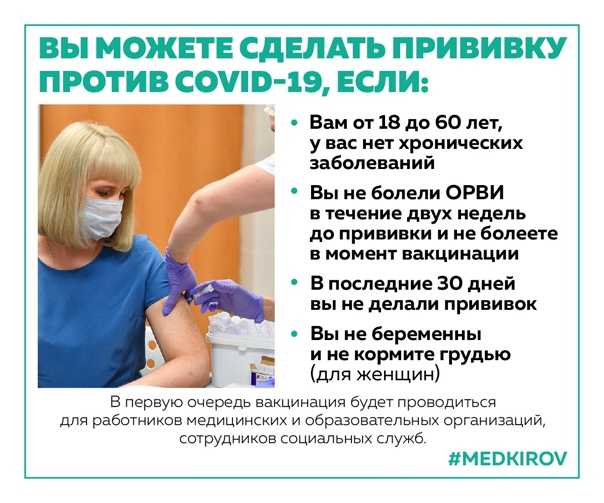 При нетяжелых ОРВИ, острых кишечных заболеваниях прививки проводятся сразу после нормализации температуры.
При нетяжелых ОРВИ, острых кишечных заболеваниях прививки проводятся сразу после нормализации температуры.
Противопоказано введение живых вакцин беременным, что связано не столько с опасностью их тератогенного влияния (подобных случаев в мировой литературе не описано), сколько с возможностью связать с вакцинацией рождение неполноценного ребенка, например, с врожденным дефектом или наследственным заболеванием.
После введения краснушной вакцины женщинам детородного возраста назначаются противозачаточные средства в течение 2 месяцев. В случае введения этой вакцины при недиагностированной беременности, ее прерывание не проводится.
Зарубежные препараты коревой и паротитной вакцин готовятся на куриных эмбрионах и поэтому их не вводят лицам с анафилактическими реакциями на куриный белок (немедленная шоковая реакция или отек тканей лица и гортани). Отечественные коревая и паротитная вакцины готовятся на яйцах японских перепелов, хотя это противопоказание к ним напрямую не относится, следует иметь в виду возможность перекрестных аллергических реакций.
Профилактические прививки проводятся гражданам в медицинских организациях бесплатно. Перед проведением профилактической прививки лицу, подлежащему вакцинации, разъясняется необходимость иммунопрофилактики инфекционных болезней, возможные поствакцинальные реакции и осложнения, а также последствия отказа от проведения профилактической прививки. Перед проведением прививки проводится осмотр пациента врачом или фельдшером. О проведении иммунизации в детских дошкольных учреждениях и школах родители детей должны быть оповещены заранее.
Календарь прививок по эпидемическим показаниям
Кроме Национального календаря, существует еще Календарь прививок по эпидемическим показаниям — в случае осложнения санитарно-эпидемиологической обстановки или при угрозе возникновения эпидемии (стихийные бедствия, крупные аварии на водопроводной и канализационной сети).
Входящими в группу риска считаются призывники. Согласно календарю, их необходимо вакцинировать против менингококковой инфекции, пневмококковой инфекции, ветряной оспы и гриппа.
Прививки от «клеща»
К эпидемическим показаниям относятся и поездки в регионы с неблагополучной эпидемической обстановкой по клещевому энцефалиту. У коренного населения, которое длительное время проживает в очагах клещевого энцефалита, в крови обнаруживаются антитела к нему — то есть иммунитет от этой болезни. А вот предохранить от клещевого энцефалита приезжих может только вакцинация.
Прививка от клещевого энцефалита проводится с помощью инактивированных вакцин, которые вводятся как минимум двумя дозами с интервалом не меньше месяца. Третья прививка делается для ревакцинации. Даже «экстренная» схема вакцинации требует не меньше полутора месяцев. Эта вакцина не защищает от болезни Лайма (клещевого боррелиоза), клещевого сыпного тифа и других инфекций, которые переносят клещи.
Случай лейкоцитокластического васкулита после вакцинации против SARS-COV-2
- Список журналов
- Коллекция Elsevier для чрезвычайных ситуаций в области общественного здравоохранения
- PMC8536729
J Emerg Med. 2022 авг.; 63(2): e62–e65.
2022 авг.; 63(2): e62–e65.
Опубликовано в сети 23 октября 2021 г. doi: 10.1016/j.jemermed.2021.10.005
* †, 1 и * †
Авторская информация Статья Примечания к авторским правам и лицензионной информации
Справочный фон
. Хотя вакКранизация против корезавирусной информации
. 2) в целом доказано, что он безопасен, но возникают редкие, но потенциально серьезные побочные реакции. Лейкоцитокластический васкулит (LCV) представляет собой васкулит мелких сосудов, который был связан с другими иммунизациями, но, насколько нам известно, ранее не сообщалось о связи с вакцинами, направленными против SARS-CoV-2.
Отчет о болезни
Мы сообщаем о случае 22-летнего мужчины с неизвестной историей болезни, который поступил в отделение неотложной помощи с 2-дневным мигрирующим артритом лодыжек и пальпируемой пурпурой на двусторонних нижних конечностях, возникающей 10 дней после получения вакцины Johnson & Johnson SARS-CoV-2. Клиническая картина пациента свидетельствовала о лейкоцитокластическом васкулите, и этот диагноз был подтвержден при биопсии кожи.
Клиническая картина пациента свидетельствовала о лейкоцитокластическом васкулите, и этот диагноз был подтвержден при биопсии кожи.
Почему об этом должен знать врач скорой помощи? Распознавание васкулитов важно для своевременного лечения и профилактики осложнений. У пациента с пальпируемой пурпурой после иммунизации против SARS-CoV-2 врач неотложной помощи должен немедленно рассмотреть вопрос о LCV, хотя лечение чаще всего полностью амбулаторное, а клиническое течение обычно легкое и саморазрешающееся.
Ключевые слова: лейкоцитокластический васкулит, SARS-CoV-2, COVID, вакцина, пурпура Шенлейна-Геноха
Лейкоцитокластический васкулит (LCV) — васкулит мелких сосудов, который чаще всего характеризуется пальпируемой пурпурой на нижних конечностях. При возникновении у детей в сочетании с болью в животе, артритом или поражением почек заболевание известно как иммуноглобулиновый A (IgA) васкулит или пурпура Шенлейна-Геноха. Во всех формах патофизиология LCV включает отложение иммунных комплексов в мелких сосудах, а также активацию системы комплемента.
Этиология LCV остается несколько неясной, но считается, что, как и в случае других васкулитов, определенную роль играют различные генетические, экологические и иммунные факторы. Был идентифицирован ряд специфических провоцирующих факторов, в том числе лекарственные препараты (особенно антибиотики, нестероидные противовоспалительные препараты [НПВП] и диуретики), микробные патогены (вирус гепатита В, вирус гепатита С, вирус иммунодефицита человека [ВИЧ], вирус Эпштейна-Барр вирус [EBV] и стрептококков ), злокачественные новообразования, воспалительные заболевания кишечника и заболевания соединительной ткани (системная красная волчанка, синдром Шегрена, ревматоидный артрит). Сообщения о случаях заболевания продемонстрировали связь между прививками, такими как грипп, и развитием LCV, а одно исследование методом случай-контроль выявило корреляцию между вакцинацией против кори, эпидемического паротита и краснухи и повышенным риском пурпуры Шенлейна-Геноха у детей (1, 2, 3, 4). В 50% случаев не удается обнаружить идентифицируемую причину, и васкулит считается идиопатическим.
В 50% случаев не удается обнаружить идентифицируемую причину, и васкулит считается идиопатическим.
Многое остается неизвестным о влиянии инфекции SARS-CoV-2 на иммунную функцию. Тяжелые случаи коронавирусной болезни 2019 (COVID-19) были связаны с нарушением регуляции как врожденной, так и приобретенной иммунной системы, и, действительно, были сообщения о случаях подтипов васкулита IgA после заражения COVID-19. Однако на сегодняшний день нам неизвестно ни об одном ранее зарегистрированном случае LCV после вакцинации против вируса SARS-CoV-2.
22-летний ранее здоровый мужчина поступил в отделение неотложной помощи с жалобами на отек лодыжек и сыпь на нижних конечностях. Он впервые заметил отек и боль в левой лодыжке за 2 дня до этого. Позже в тот же день он начал замечать пурпурную сыпь на ступнях, распространяющуюся вверх к голеням. За день до презентации отек левой лодыжки прошел, но правая лодыжка стала опухшей и болезненной. Сыпь продолжала распространяться, хотя и оставалась ограниченной его голенью.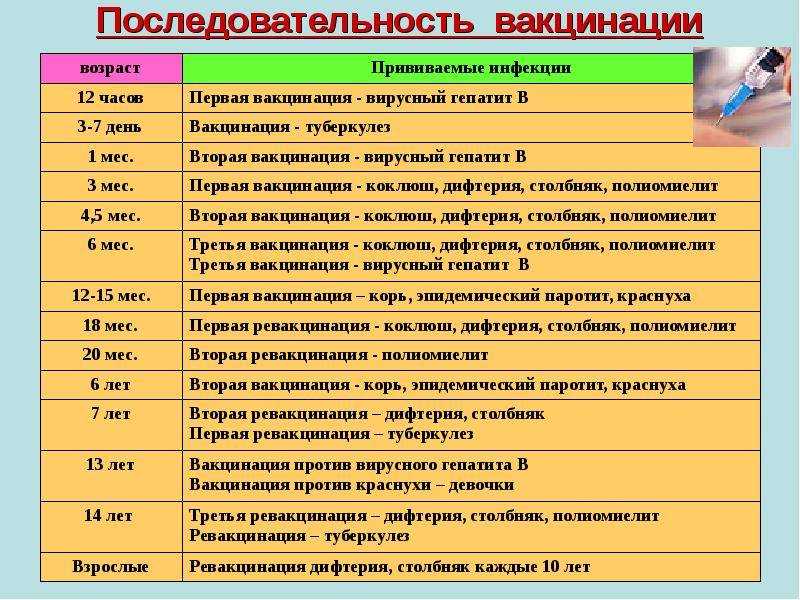 Он не сообщил об отсутствии других высыпаний или кровоподтеков, кровотечений из слизистых оболочек, лихорадки, миалгии, утомляемости, болей в животе или гематурии.
Он не сообщил об отсутствии других высыпаний или кровоподтеков, кровотечений из слизистых оболочек, лихорадки, миалгии, утомляемости, болей в животе или гематурии.
Пациент получил вакцину против SARS-CoV-2 компании Johnson & Johnson 10 дней назад, после чего в течение 1 дня у него наблюдалась субфебрильная температура без сопутствующих симптомов. Кроме того, у пациента не было недавнего анамнеза болезни, кроме какой-либо изолированной ринореи месяц назад, которая не сопровождалась лихорадкой, кашлем или болью в горле. Презентация была в мае, вне типичного вирусного сезона в этом ED. Кроме того, презентация была во время пандемии COVID-19, когда маски оставались обязательными, а показатели заболеваемости гриппом и другими респираторными вирусами были ниже исходного уровня (5). У пациента не было в анамнезе аллергии или аутоиммунных заболеваний, и он не принимал лекарства, отпускаемые по рецепту или без рецепта. У него не было недавних поездок и контакта с животными.
При осмотре у больного нет дистресса, нет лихорадки 36,8°С, гемодинамически стабильное артериальное давление 129/83 мм рт. ст. Первоначально у него была тахикардия с частотой 109 ударов в минуту, но частота сердечных сокращений снизилась до 79 ударов в минуту после введения НПВП для купирования боли. У него была отмечена разбросанная фиолетовая пальпируемая пурпура на тыльной поверхности обеих стоп и передних поверхностях обеих нижних конечностей дистальнее коленей. Самое большое поражение было 3 см в диаметре, все они не бледнели, и ни одно из них не было болезненным. Его правая лодыжка была опухшей, болезненной и покрасневшей, с болью при активных и пассивных движениях.
ст. Первоначально у него была тахикардия с частотой 109 ударов в минуту, но частота сердечных сокращений снизилась до 79 ударов в минуту после введения НПВП для купирования боли. У него была отмечена разбросанная фиолетовая пальпируемая пурпура на тыльной поверхности обеих стоп и передних поверхностях обеих нижних конечностей дистальнее коленей. Самое большое поражение было 3 см в диаметре, все они не бледнели, и ни одно из них не было болезненным. Его правая лодыжка была опухшей, болезненной и покрасневшей, с болью при активных и пассивных движениях.
представляет собой репрезентативную фотографию нижних конечностей пациента.
Открыть в отдельном окне
Нижние конечности пациента
Лабораторные данные: 1+ гематурия в моче, 1 эритроцит/поле сильного увеличения, 1 лейкоцит/поле сильного увеличения, бактерии отсутствуют в осадке мочи. Химический состав сыворотки отличался нормальной функцией почек, с азотом мочевины крови 9 мг/дл и креатинином 0,88 мг/дл. Общий анализ крови показал умеренный лейкоцитоз при 10,3×10 3 /мл и нормальные тромбоциты при 307×10 3 /мл. Коагуляционные исследования были в пределах нормы, протромбиновое время 14,1 с, частичное тромбопластиновое время 35,5 с. Дерматолог проконсультировался и рекомендовал ряд вторичных лабораторных исследований, а также биопсию для подтверждения диагноза и изучения возможных триггеров. Они рекомендовали кратковременную госпитализацию, чтобы обеспечить контроль боли и отсутствие острого ухудшения, но не считали необходимым получение вторичных лабораторных данных до выписки, поскольку LCV чаще всего можно лечить амбулаторно даже при первом обращении. Примечательные лабораторные данные, полученные после выписки, включали снижение C3 до 61 мг/дл, отрицательный тест на антинейтрофильные цитоплазматические антитела (ANCA), пограничный повышенный ревматоидный фактор 16 МЕ/мл и повышенный титр антител к стрептолизину-О (ASO). из 944. Цитомегаловирус (CMV) IgG был положительным, CMV IgM был отрицательным, а антитела к EBV и ВИЧ были отрицательными. Тест полимеразной цепной реакции SARS-CoV-2 был отрицательным.
Коагуляционные исследования были в пределах нормы, протромбиновое время 14,1 с, частичное тромбопластиновое время 35,5 с. Дерматолог проконсультировался и рекомендовал ряд вторичных лабораторных исследований, а также биопсию для подтверждения диагноза и изучения возможных триггеров. Они рекомендовали кратковременную госпитализацию, чтобы обеспечить контроль боли и отсутствие острого ухудшения, но не считали необходимым получение вторичных лабораторных данных до выписки, поскольку LCV чаще всего можно лечить амбулаторно даже при первом обращении. Примечательные лабораторные данные, полученные после выписки, включали снижение C3 до 61 мг/дл, отрицательный тест на антинейтрофильные цитоплазматические антитела (ANCA), пограничный повышенный ревматоидный фактор 16 МЕ/мл и повышенный титр антител к стрептолизину-О (ASO). из 944. Цитомегаловирус (CMV) IgG был положительным, CMV IgM был отрицательным, а антитела к EBV и ВИЧ были отрицательными. Тест полимеразной цепной реакции SARS-CoV-2 был отрицательным.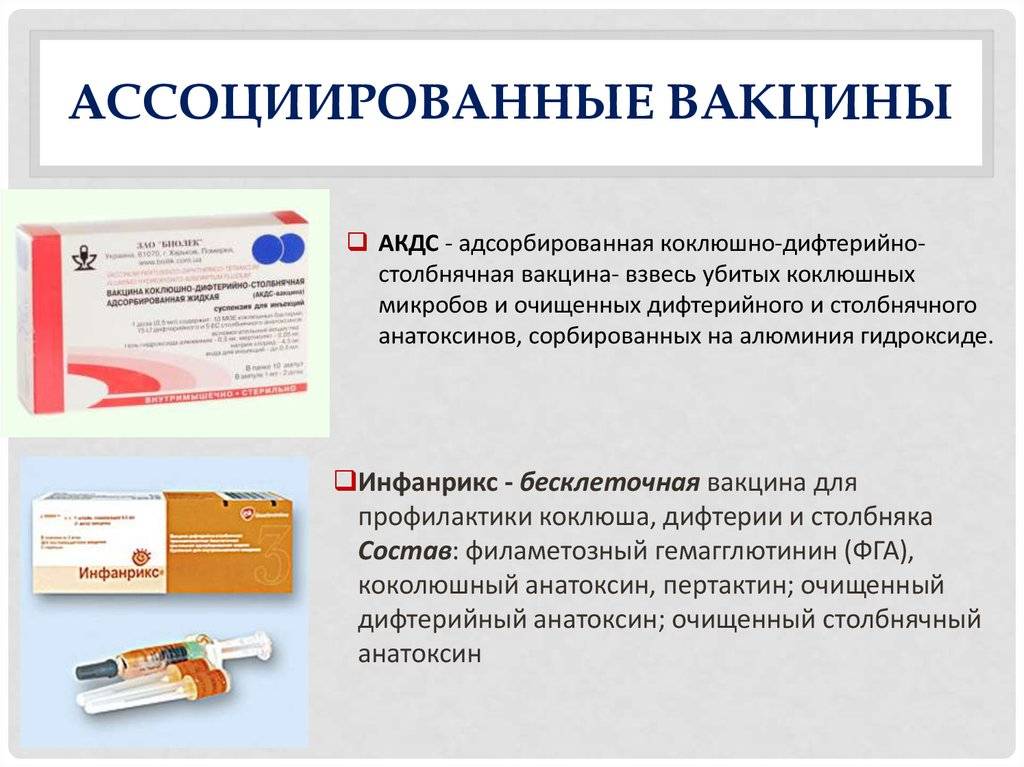
Биопсия очагов показала периваскулярный и интерстициальный нейтрофильный инфильтрат с эозинофилами. Была проведена иммунофлуоресценция, которая продемонстрировала периваскулярное отложение IgA и C3, а также IgG. Окончательный отчет о патологии, который был получен через 1 неделю после выписки, частично гласил: «в контексте результатов иммунофлуоресценции внешний вид наиболее наводит на мысль о лейкоцитокластическом васкулите. Клиническая корреляция необходима для определения этиологии». Пациент наблюдался в дерматологической клинике по поводу подтвержденного биопсией LCV; Согласно обзору диаграммы, сыпь и отек уменьшались.
У пациента, поступающего в отделение неотложной помощи с пурпурой, дифференциальный диагноз включает состояния, начиная от опасных для жизни (например, менингококкемия, диссеминированное внутрисосудистое свертывание крови, тромботическая тромбоцитопеническая пурпура) до относительно доброкачественных (например, иммунная тромбоцитопения) (6). Непальпируемая пурпура чаще всего связана с патологиями тромбоцитопении.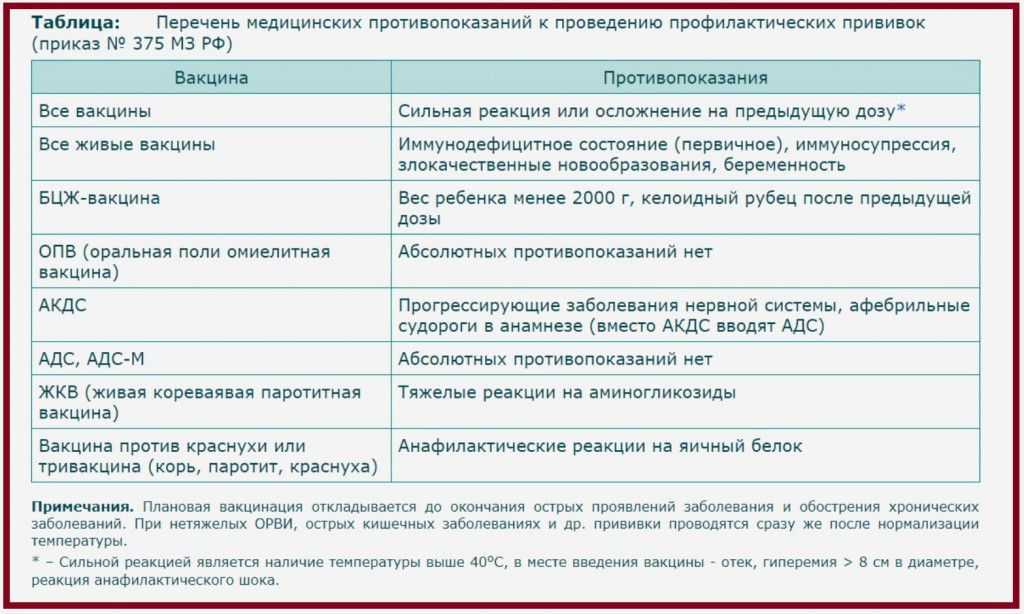 У пациента с нормальными показателями тромбоцитов и показателей коагуляции и наличием других признаков и симптомов, таких как мигрирующий артрит и микроскопическая гематурия, высока вероятность васкулита. Различные васкулиты мелких сосудов с дерматологическими проявлениями, включая пальпируемую пурпуру и сопутствующие симптомы, могут помочь в дифференциальной диагностике. IgA-васкулит, форма LCV, может проявляться артритом и почечной недостаточностью. Эозинофильный гранулематоз с полиангиитом и гранулематоз с полиангиитом часто сочетаются с синуситом и некоторыми формами поражения легких и связаны с ANCA-позитивностью. Узелковый полиартериит, который обычно классифицируется как заболевание средних сосудов, но может вызывать пурпуру, часто проявляется желудочно-кишечными симптомами, поражением почек и невропатией.
У пациента с нормальными показателями тромбоцитов и показателей коагуляции и наличием других признаков и симптомов, таких как мигрирующий артрит и микроскопическая гематурия, высока вероятность васкулита. Различные васкулиты мелких сосудов с дерматологическими проявлениями, включая пальпируемую пурпуру и сопутствующие симптомы, могут помочь в дифференциальной диагностике. IgA-васкулит, форма LCV, может проявляться артритом и почечной недостаточностью. Эозинофильный гранулематоз с полиангиитом и гранулематоз с полиангиитом часто сочетаются с синуситом и некоторыми формами поражения легких и связаны с ANCA-позитивностью. Узелковый полиартериит, который обычно классифицируется как заболевание средних сосудов, но может вызывать пурпуру, часто проявляется желудочно-кишечными симптомами, поражением почек и невропатией.
Классическим проявлением LCV является пальпируемая пурпура, появляющаяся на голенях, как у этого пациента. Поражения обычно безболезненны, но иногда сопровождаются зудом или легкой болезненностью. У пациентов с IgA-подтипом LCV классически проявляются мигрирующие артралгии или артриты или поражение почек с гематурией, что также наблюдалось у этого пациента. Идентифицируемые триггеры для LCV, которые могут включать лекарства, вирусные или другие инфекции и, возможно, вакцинацию, как правило, возникают за 7–10 дней до развития кожных проявлений, что согласуется с временным течением, наблюдаемым в этом случае, если SARS -Вакцина CoV-2 была, по сути, провоцирующей причиной. У этого пациента действительно был положительный титр ASO, предполагающий стрептококковую инфекцию в качестве еще одного возможного триггера, но у него не было недавней истории инфекции верхних дыхательных путей, ангины или инфекции кожи.
У пациентов с IgA-подтипом LCV классически проявляются мигрирующие артралгии или артриты или поражение почек с гематурией, что также наблюдалось у этого пациента. Идентифицируемые триггеры для LCV, которые могут включать лекарства, вирусные или другие инфекции и, возможно, вакцинацию, как правило, возникают за 7–10 дней до развития кожных проявлений, что согласуется с временным течением, наблюдаемым в этом случае, если SARS -Вакцина CoV-2 была, по сути, провоцирующей причиной. У этого пациента действительно был положительный титр ASO, предполагающий стрептококковую инфекцию в качестве еще одного возможного триггера, но у него не было недавней истории инфекции верхних дыхательных путей, ангины или инфекции кожи.
Вакцины, разработанные для SARS-CoV-2, вызывают реакции врожденной иммунной системы, а также адаптивной иммунной системы (Т-лимфоциты и В-лимфоциты), что приводит к выработке как цитокинов, так и антител (7). Вакцина Johnson & Johnson доставляет генетический шиповидный белок SARS-CoV-2 на аденовирусный вектор Ad26, который обладает высокой иммуногенностью (8). Аденовирус запускает высвобождение цитокинов, в том числе интерлейкина (ИЛ)-6, ИЛ-12 и фактора некроза опухоли-альфа, а также выработку антител и активацию Т-клеток (9).). Чрезмерно активный иммунологический ответ может привести к образованию аберрантных комплексов антител и инфильтрации нейтрофилов в стенках мелких сосудов и вокруг них.
Аденовирус запускает высвобождение цитокинов, в том числе интерлейкина (ИЛ)-6, ИЛ-12 и фактора некроза опухоли-альфа, а также выработку антител и активацию Т-клеток (9).). Чрезмерно активный иммунологический ответ может привести к образованию аберрантных комплексов антител и инфильтрации нейтрофилов в стенках мелких сосудов и вокруг них.
Клиническое течение LCV обычно легкое и саморазрешающееся, а при отсутствии системных осложнений (например, нефрита) обычно требуется только поддерживающая терапия. Часто рекомендуются покой, приподнятое положение ног и компрессионные чулки, учитывая тенденцию к развитию поражений в зависимых областях. НПВП можно использовать для обезболивания, а антигистаминные препараты — для лечения зуда (10,11). Глюкокортикоиды могут быть использованы при длительном течении заболевания, хотя данные в поддержку использования кортикостероидов получены только из клинических случаев. У взрослых с IgA-нефритом глюкокортикоиды рекомендуются при повышенном уровне креатинина в сыворотке, протеинурии более 1 г в день или подтвержденном биопсией поражении почек (12). Пациенты с артритом обычно хорошо реагируют на терапию НПВП, но терапия глюкокортикоидами может быть эффективной при стойкой боли.
Пациенты с артритом обычно хорошо реагируют на терапию НПВП, но терапия глюкокортикоидами может быть эффективной при стойкой боли.
Поскольку большая часть населения проходит вакцинацию против SARS-CoV-2, врачи скорой помощи могут наблюдать редкие побочные реакции, потенциально связанные с нарушением регуляции иммунитета, такие как LCV. Хотя само по себе состояние редко угрожает жизни, пациентам с подозрением на LCV может помочь быстрое распознавание, идентификация недавнего или текущего триггера, а также оценка и лечение связанных симптомов.
1. Чен С.Х., Коэн П.Р. Кожный лейкоцитокластический васкулит после вакцинации против гриппа у пожилых людей: сообщение о буллезной пурпуре у восьмидесятилетнего человека после введения вакцины против гриппа. Куреус. 2018;10:e2323. [Бесплатная статья PMC] [PubMed] [Google Scholar]
2. Малек А., Гомес-Вильегас С.И., де ла Хос А., Новбахт С., вакцинация Ариас СА.А. 19-летний мужчина с IgA-васкулитом после. Braz J Infect Dis. 2018;22:442–444. [Бесплатная статья PMC] [PubMed] [Google Scholar]
[Бесплатная статья PMC] [PubMed] [Google Scholar]
3. Monjazeb S, Philips RC, Wilkerson M. Случай лейкоцитокластического васкулита после вакцинации против гриппа. JAAD Case Rep. 2016; 2:340–342. [Бесплатная статья PMC] [PubMed] [Google Scholar]
4. Da Dalt L, Zerbinati C, Strafella MS, et al. Пурпура Шенлейна-Геноха и использование лекарств и вакцин в детстве: исследование случай-контроль. Ital J Pediatr. 2016;42:60. [Бесплатная статья PMC] [PubMed] [Google Scholar]
5. Olsen SJ, Winn AK, Budd AP, et al. Изменения активности гриппа и других респираторных вирусов во время пандемии COVID-19 — США, 2020–2021 гг. MMWR Morb Mortal Wkly Rep. 2021; 70: 1013–1019. [Бесплатная статья PMC] [PubMed] [Google Scholar]
6. Томас А.Е., Бэрд С.Ф., Андерсон Дж. Пурпурная и петехиальная сыпь у взрослых и детей: начальная оценка. BMJ (Clin Res Ed) 2016;352:i1285. [PubMed] [Google Scholar]
7. Беттини Э., Лоччи М. Вакцины мРНК SARS-CoV-2: иммунологический механизм и не только.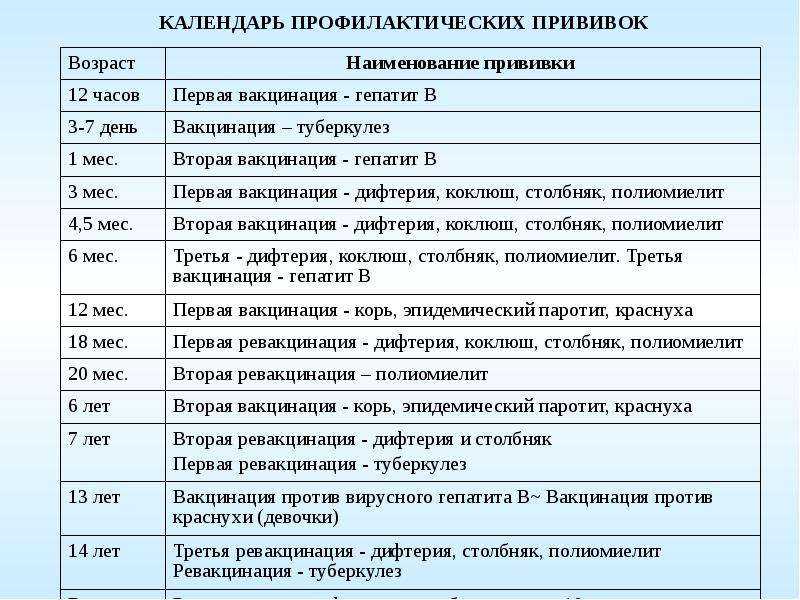 Вакцина. 2021;9:147. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Вакцина. 2021;9:147. [Бесплатная статья PMC] [PubMed] [Google Scholar]
8. Sadoff J, Le Gars M, Shukarev G, et al. Промежуточные результаты фазы 1-2а испытания вакцины Ad26.COV2.S Covid-19. N Engl J Med. 2021; 384: 1824–1835. [Бесплатная статья PMC] [PubMed] [Google Scholar]
9. Тацис Н., Эртл Х.К. Аденовирусы как переносчики вакцин. Мол Тер. 2004; 10: 616–629. [Бесплатная статья PMC] [PubMed] [Google Scholar]
10. Фетт Н. Ведение взрослых с идиопатическим кожным васкулитом мелких сосудов. UpToDate 2020. Доступно по адресу: https://www.uptodate.com/contents/management-of-adults-with-idiopathic-cutaneous-small-vessel-vasculitis. По состоянию на 7 ноября 2021 г.
11. Ниаудет П., Аппель Г.Б., Хундер Г.Г. IgA-васкулит (пурпура Шенлейна-Геноха): почечные проявления. UpToDate 2020. Доступно по адресу: https://www.uptodate.com/contents/iga-vasculitis-henoch-schonlein-purpura-kidney-manifestations. По состоянию на 7 ноября 2021 г.
12. Рассел Дж. П., Гибсон Л. Е. Первичный кожный васкулит мелких сосудов: подход к диагностике и лечению. Int J Дерматол. 2006; 45:3–13. [PubMed] [Академия Google]
Е. Первичный кожный васкулит мелких сосудов: подход к диагностике и лечению. Int J Дерматол. 2006; 45:3–13. [PubMed] [Академия Google]
Лейкоцитокластический васкулит (кожный васкулит мелких сосудов) после COVID-19вакцинация
- Список журналов
- Коллекция Elsevier для чрезвычайных ситуаций в области общественного здравоохранения
- PMC8712260
J Аутоиммун. 2022 февраль; 127: 102783.
Опубликовано в сети 28 декабря 2021 г. doi: 10.1016/j.jaut.2021.102783
, a, b, ∗ , b, c , a, b , a, b , c , a, d and a , d
Информация об авторе Примечания к статье Информация об авторских правах и лицензиях Отказ от ответственности
Прививки могут вызывать побочные эффекты со стороны кожи из-за неспецифического воспаления или иммуноопосредованных реакций.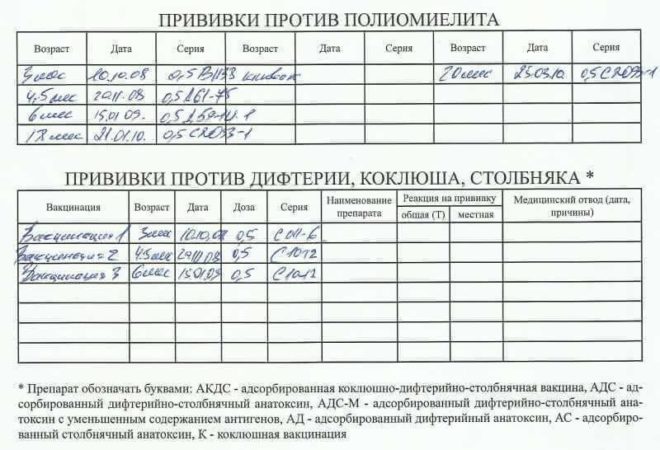 Наблюдаются несколько типов васкулита. Мы сообщаем о 71-летней женщине, у которой развился кожный васкулит мелких сосудов после второй дозы Vaxzevria COVID-19.вакцинация, показывающая лейкоцитокластический васкулит при гистопатологическом исследовании биопсии кожи.
Наблюдаются несколько типов васкулита. Мы сообщаем о 71-летней женщине, у которой развился кожный васкулит мелких сосудов после второй дозы Vaxzevria COVID-19.вакцинация, показывающая лейкоцитокластический васкулит при гистопатологическом исследовании биопсии кожи.
Кожный васкулит мелких сосудов — редкое состояние, которое может быть идиопатическим или вторичным по отношению к основным инфекциям, заболеваниям соединительной ткани, злокачественным новообразованиям и лекарственным препаратам. Патогенез включает отложение иммунных комплексов в мелких кровеносных сосудах, что приводит к активации системы комплемента и рекрутированию лейкоцитов.
Сообщалось об обострении васкулита мелких сосудов после введения различных вакцин, особенно вакцины против гриппа. Ожидается, что вакцина против SARS-CoV-2 приведет к активации В- и Т-клеток и образованию антител. Мы предполагаем, что лейкоцитокластический васкулит, вызванный отложением иммунных комплексов в мелких сосудах кожи, может быть редким побочным эффектом Vaxzevria COVID-19.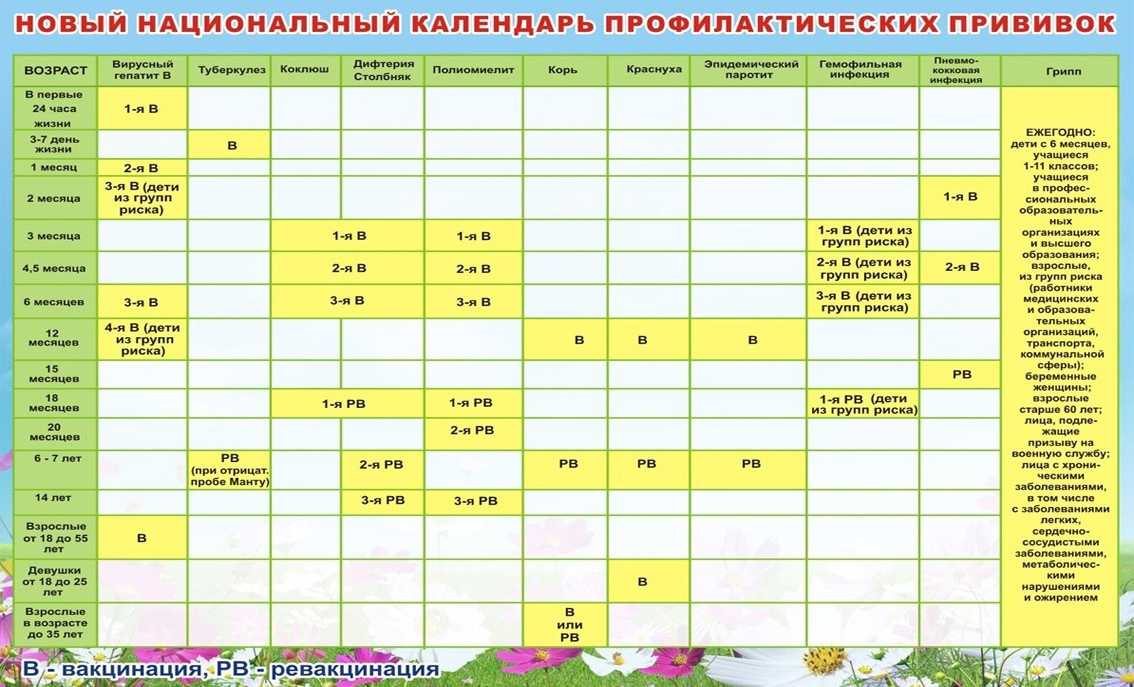 вакцинация.
вакцинация.
Ключевые слова: Побочные реакции на вакцины, кожный васкулит мелких сосудов, лейкоцитокластический васкулит, вакцина COVID-19, вакцина SARS-CoV-2, вакцина Vaxzevria
Прививки, как правило, безопасны и имеют решающее значение для профилактики инфекционных заболеваний. Побочные эффекты прививок обычно легкие, хорошо переносятся и могут включать кожные реакции [1]. Они подразделяются на местные реакции, в основном из-за неспецифического воспаления и раздражения в месте инъекции, и генерализованные реакции, которые обычно являются иммуноопосредованными и могут быть связаны с системными симптомами [1]. Кожные побочные эффекты, связанные с недавно одобренным COVID-19часто сообщалось о прививках, в основном включая отсроченные обширные местные реакции (уплотненные, эритематозные бляшки, появляющиеся более чем через 4 дня после вакцинации), местные реакции в месте инъекции, крапивницу, кореподобные реакции, эритромелалгию (эритематозные, отечные руки и ноги с ощущением жжения), герпес опоясывающий лишай и обморожения [2]. Мы сообщаем о пациенте, у которого развился кожный васкулит мелких сосудов после вакцинации против COVID-19.
Мы сообщаем о пациенте, у которого развился кожный васкулит мелких сосудов после вакцинации против COVID-19.
71-летняя женщина с фиброзно-кистозной мастопатией и артериальной гипертензией в анамнезе, получавшая лечение атенололом, поступила в отделение неотложной помощи по поводу кожных поражений, связанных с ощущением жжения, которые появились днем ранее на обеих ногах. Она получила вторую дозу Vaxzevria COVID-19.вакцины (AstraZeneca) пятью днями ранее и не сообщали о какой-либо известной аллергии или введении новых лекарств в предыдущие недели. При физикальном осмотре на обеих голенях были обнаружены пурпурные пятна и папулы.
А). Общий анализ крови показал 11 880 лейкоцитов/мм 3 (норма 4000–10 000/мм 3 ) с преобладанием нейтрофилов. Уровень D-димера в плазме составлял 806 нг/мл (нормальный диапазон, 200–350 мг/дл), а С-реактивный белок в сыворотке – 5,07 мг/дл (нормальный диапазон, <0,50 мг/дл). Антинуклеарные антитела, экстрагируемый ядерный антиген и антинейтрофильные цитоплазматические антитела были отрицательными.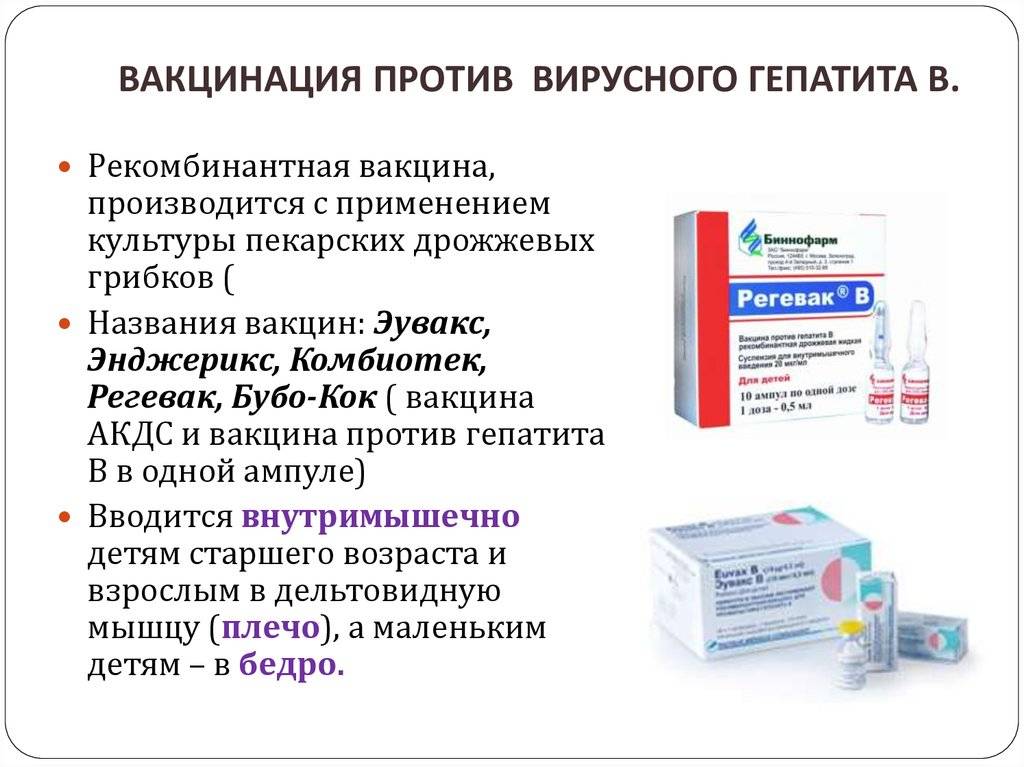 Уровни комплемента С3 и С4 были соответственно 83 мг/дл (нормальный диапазон, 90–180 мг/дл) и <8 мг/дл (нормальный диапазон, 10–40 мг/дл). Уровень ревматоидного фактора (РФ) составлял 17 МЕ/мл (нормальный диапазон, < 15 МЕ/мл). При ультразвуковой допплерографии нижних конечностей признаков тромбоза поверхностных и глубоких вен не выявлено. При гистопатологическом исследовании биоптата пальпируемого пурпурного образования выявлен периваскулярный инфильтрат, преимущественно состоящий из лимфоцитов и нейтрофилов, экстравазация эритроцитов в дерму, с фибриноидным некрозом мелких сосудов и лейкоцитоклазией (,
). Прямая иммунофлюоресценция при биопсии кожи непальпируемого очага показала линейное и зернистое отложение IgM в мелких сосудах. Был поставлен диагноз: кожный васкулит мелких сосудов (лейкоцитокластический васкулит). Пациенту был начат пероральный прием преднизолона в дозе 20 мг в день с постепенным снижением дозы в течение 14 дней с полным клиническим исчезновением кожных поражений.
Уровни комплемента С3 и С4 были соответственно 83 мг/дл (нормальный диапазон, 90–180 мг/дл) и <8 мг/дл (нормальный диапазон, 10–40 мг/дл). Уровень ревматоидного фактора (РФ) составлял 17 МЕ/мл (нормальный диапазон, < 15 МЕ/мл). При ультразвуковой допплерографии нижних конечностей признаков тромбоза поверхностных и глубоких вен не выявлено. При гистопатологическом исследовании биоптата пальпируемого пурпурного образования выявлен периваскулярный инфильтрат, преимущественно состоящий из лимфоцитов и нейтрофилов, экстравазация эритроцитов в дерму, с фибриноидным некрозом мелких сосудов и лейкоцитоклазией (,
). Прямая иммунофлюоресценция при биопсии кожи непальпируемого очага показала линейное и зернистое отложение IgM в мелких сосудах. Был поставлен диагноз: кожный васкулит мелких сосудов (лейкоцитокластический васкулит). Пациенту был начат пероральный прием преднизолона в дозе 20 мг в день с постепенным снижением дозы в течение 14 дней с полным клиническим исчезновением кожных поражений.
Открыть в отдельном окне
А. Дерматологическое обследование. Симметрично распределенные пурпурные пятна и папулы, расположенные на голенях. B, C. Гистопатологическое исследование (окраска H&E). Срезы показывают периваскулярный воспалительный инфильтрат, состоящий преимущественно из нейтрофилов (черная стрелка), фибриноидный некроз (белая стрелка) и экстравазацию эритроцитов (красная стрелка). Увеличение × 10 (B), увеличение × 40 (C). (Для интерпретации ссылок на цвет в легенде к этому рисунку читатель может обратиться к веб-версии этой статьи.)
Открыть в отдельном окне
Гистопатологическое исследование (окраска H&E x 20). На срезе видна тяжелая нейтрофильная инфильтрация, небольшое количество лимфоцитов и редкие эозинофилы вокруг поверхностных сосудов (черная стрелка). Также имеется экстравазация эритроцитов в дерму (красная стрелка), фибриноидный некроз мелких сосудов и лейкоцитоклазия (белая стрелка). (Для интерпретации ссылок на цвет в легенде к этому рисунку читатель может обратиться к веб-версии этой статьи. )
)
Термин лейкоцитокластический васкулит (ЛЦВ) относится к патологическому признаку васкулита мелких сосудов, а именно к фрагментации ядер нейтрофилов (лейкоцитоклазия, также называемая «ядерной пылью»), которые составляют воспалительный инфильтрат в стенке артериол, капилляров и посткапиллярные венулы; сопутствующие гистопатологические признаки включают внесосудистые эритроциты и фибриноидный некроз стенок сосудов [3,4].
Гистологические признаки LCV могут быть обнаружены при: ANCA-ассоциированном васкулите, иммунокомплексном васкулите, таком как криоглобулинемический васкулит, IgA-васкулите (пурпура Геноха–Шенлейна), гипокомплементемическом уртикарном васкулите (анти-C1q-васкулит) и IgM/IgG иммунном комплексе васкулит (ранее известный как гиперчувствительный васкулит), васкулит, связанный с системными заболеваниями (например, ревматоидным артритом, системной красной волчанкой и саркоидозом) и васкулит, вторичный по отношению к инфекциям, лекарствам, сепсису или раку [3,4].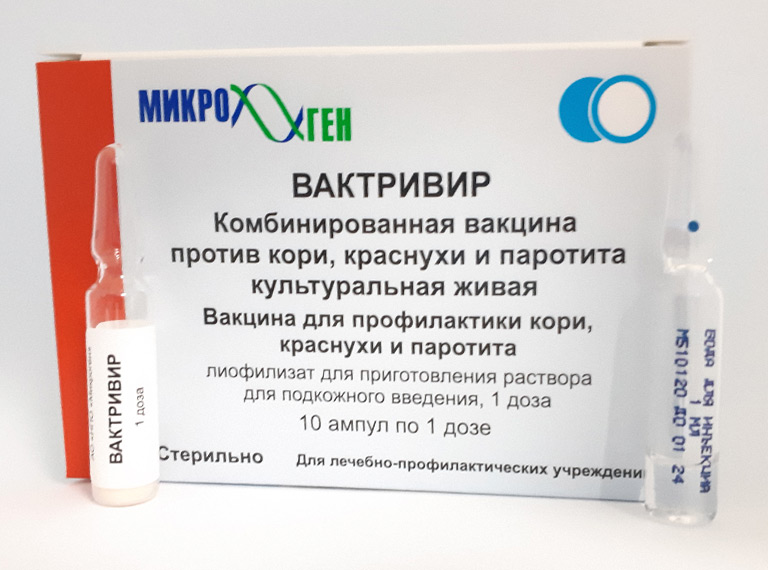
Сообщалось о преципитации или обострении васкулита, вторичного по отношению к различным вакцинам, таким как вирус гриппа, вирус гепатита А/В, бацилла Кальметта-Герена, вирус папилломы человека и ротавирус [[5], [6], [7]]. Однако, насколько нам известно, LCV, связанный с вакциной против COVID-19, очень редко сообщается, несмотря на большое количество людей, которые уже прошли эту вакцинацию (
).
Таблица 1
Краткое изложение опубликованных случаев LCV, связанных с COVID-19вакцина.
| Case | Age, Sex | Comorbidities | Vaccine | Time to onset | Systemic involvement | DIF | Treatment |
|---|---|---|---|---|---|---|---|
Sandhu et Al [13]. | 55, F | NO | VAXZEVRIA (Astrazeneca): 1st DOSE | 5 дней | NO | SELECT | .0213 |
| 48, M | Hypertension | Vaxzevria (AstraZeneca): 2nd dose | 2 days | No | Negative | Oral prednisolone @0.5 mg/kg/day, tapered over 2 weeks | |
| Коэн и др. [6]. | 46, F | Псориаз, псориатический артрит, синдром раздраженного кишечника | Comirnaty (Pfizer-BioNTech): 1-я и 2-я доза | 2 дня | Нет | Нет в наличии | Топические стероиды и постепенное снижение дозы преднизолона |
Larson et Al [14]. | 83, F | NO | Comirnaty (Pfizer -Biontech): 2 -я доза | 5 Days | Повышенные уровни CRP, ESR и RF — стероиды | ||
| Бостан и др. [7]. | 33, М | № | Инактивированный COVID-19вакцина: 1-я доза | 3 дня | № | IgA | Местно мометазона фуроат два раза в день |
| Kar et al [11]. | 46, F | NO | Коваксин (Bharat Biotech): 1 -я доза | 5 дней | no | lettation, Restamins, и Antihistimines, 9021, | , 9021, | .23, F | № | CoronaVac (Sinovac): 1-я доза | 36 ч | № | C3 и фибриноген | 2 дозы внутримышечно и 4 дозы внутривенно дексаметазона (4 мг каждые 8 ч) с последующим пероральным приемом преднизолона (10 мг 2 раза в день) 2 6 F | № | CoronaVac (Sinovac): 1-я доза | 4 часа | № | IgA, IgM и C3 | 2 дозы внутримышечно и 4 дозы внутривенно дексаметазона (4 мг колихина) перорально каждые 8 ч мг два раза в день) и напроксен (250 мг два раза в день) в течение 4 недель |
Открыть в отдельном окне
М: Мужской; Ф: Женский; DIF: прямая иммунофлуоресценция; СРБ: С-реактивный белок; СОЭ: скорость оседания эритроцитов; РФ: ревматоидный фактор.
Типичная клиническая картина кожного LCV состоит из симметрично расположенных, не бланшируемых пурпурных папул, в основном расположенных на голенях или в зависимых областях. Другие клинические проявления LCV могут включать язвы, пустулы и везикулы [4,8]. Кожный LCV может сопровождаться системными симптомами, такими как лихорадка, недомогание или артралгии, и менее чем у половины пациентов васкулитом, поражающим другие органы, в основном почки или желудочно-кишечный тракт [8]. В дерматологическом дополнении к номенклатуре васкулитов, принятой на конференции Chapel Hill Consensus Conference, признается, что LCV может представлять собой кожное проявление системного васкулита, кожно-ограниченное или кожно-доминантное выражение или вариант системного васкулита, или моноорганный васкулит, который отличается от признанного системного васкулита. васкулиты [3].
У нашего пациента полное физическое обследование и биохимия сыворотки не выявили признаков внекожного поражения, что подтверждает общую безопасность вакцинации против COVID-19, несмотря на явно тревожную клиническую картину.
Точный патогенез связанного с вакцинацией лейкоцитокластического васкулита еще предстоит определить, но вакцина против SARS-CoV-2 может приводить к активации аутореактивных B/T-клеток, образованию антител и отложению иммунных комплексов в мелких сосудах, что приводит к активации системы комплемента и рекрутирования лейкоцитов [4,6,7,9,10]. Ответственная частица в качестве антигена для таких реакций неизвестна, однако можно предположить, что воспалительная реакция на компонент вакцины, кодирующий гликопротеин шипа SARS-CoV-2, нацелена на эндотелий и приводит к васкулиту мелких сосудов [[11], [12], [ 13]].
Наш отчет добавляет к кожным побочным эффектам вакцинации против COVID-19, подчеркивая, что лейкоцитокластический васкулит может быть редкой побочной реакцией на вакцинацию против SARS-CoV-2, ограниченной кожными проявлениями.
Fiorillo G: концептуализация, обзор литературы, написание, рецензирование и редактирование окончательного варианта рукописи. Pancetti S: гистопатологический анализ, получение результатов патологии, сбор данных. Cortese A: исследования, обзор литературы, написание и редактирование. Toso F: исследования, формальный анализ, сбор и анализ данных. Манара С.: гистопатологический анализ, наблюдение, рецензирование окончательной рукописи. Костанцо А: наблюдение, участие в патогенезе, рецензирование окончательной версии рукописи. Боррони Р.: концептуализация, методология, надзор, рецензирование и редактирование окончательного варианта рукописи. Все авторы одобрили окончательный вариант рукописи.
Cortese A: исследования, обзор литературы, написание и редактирование. Toso F: исследования, формальный анализ, сбор и анализ данных. Манара С.: гистопатологический анализ, наблюдение, рецензирование окончательной рукописи. Костанцо А: наблюдение, участие в патогенезе, рецензирование окончательной версии рукописи. Боррони Р.: концептуализация, методология, надзор, рецензирование и редактирование окончательного варианта рукописи. Все авторы одобрили окончательный вариант рукописи.
Это исследование не получило какого-либо специального гранта от финансирующих агентств в государственном, коммерческом или некоммерческом секторах.
1. Розенблатт А.Е., Штейн С.Л. Кожные реакции на прививки. клин. Дерматол. 2015 г., май-июнь; 33(3):327–332. doi: 10.1016/j.clidermatol.2014.12.009. Epub 2014, 8 декабря. PMID: 25889134. [PubMed] [CrossRef] [Google Scholar]
2. МакМахон Д.Э., Коварик С.Л., Дамский В., Розенбах М., Липофф Дж.Б., Тяги А., Чемберлин Г., Фати Р. ., Назарян Р.М. , Десаи С.Р., Лим Х.В., Тьер Б.Х., Хруза Г.Дж., Френч Л.Е., Блюменталь К., Фокс Л.П., Фримен Э.Е. Клиническая и патологическая корреляция кожного COVID-19вакцинные реакции, включая V-REPP: исследование на основе регистра. Варенье. акад. Дерматол. 2021, 10 сентября; –9622(21):S0190. doi: 10.1016/j.jaad.2021.09.002. 02442-7 Epub перед печатью. PMID: 34517079; PMCID: PMC8431833. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
, Десаи С.Р., Лим Х.В., Тьер Б.Х., Хруза Г.Дж., Френч Л.Е., Блюменталь К., Фокс Л.П., Фримен Э.Е. Клиническая и патологическая корреляция кожного COVID-19вакцинные реакции, включая V-REPP: исследование на основе регистра. Варенье. акад. Дерматол. 2021, 10 сентября; –9622(21):S0190. doi: 10.1016/j.jaad.2021.09.002. 02442-7 Epub перед печатью. PMID: 34517079; PMCID: PMC8431833. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
3. Fraticelli P., Benfaremo D., Gabrielli A. Диагностика и лечение лейкоцитокластического васкулита. Стажер Эмердж. Мед. 2021 июнь; 16 (4): 831–841. doi: 10.1007/s11739-021-02688-x. Epub 2021, 13 марта. PMID: 33713282; PMCID: PMC8195763. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
4. Ираджи Ф., Галехдари Х., Сиадат А.Х., Бокаи Джази С. Кожный лейкоцитокластический васкулит, вторичный по отношению к инфекции COVID-19: клинический случай. клин. Отчет по делу, 18 декабря 2020 г .; 9 (2): 830–834. doi: 10.1002/ccr3.3596. PMID: 33598253; PMCID: PMC7869328. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
[Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
5. Бонетто С., Тротта Ф., Феличетти П., Аларкон Г.С., Сантуччио С., Бахтиар Н.С., Браухли Пернус Ю., Чендлер Р., Джироломони Г., Хадден Р.Д., Кукуку М., Озен С., Пахуд Б., Топ К., Варриччио Ф., Уайз Р.П., Занони Г., Живкович С., Бонхёффер Дж., Брайтонская рабочая группа по васкулиту Васкулит как нежелательные явления после иммунизации — систематический обзор литературы. вакцина. 2016 12 декабря; 34 (51): 6641–6651. doi: 10.1016/j.vaccine.2015.090,026. Epub 2015 Sep 21. PMID: 26398442. [PubMed] [CrossRef] [Google Scholar]
6. Cohen S.R., Prussick L., Kahn J.S., Gao DX., Radfar A., Rosmarin D. 19 вакцина. Междунар. Дж. Дерматол. 2021 авг; 60 (8): 1032–1033. doi: 10.1111/ijd.15623. Epub 2021, 30 апреля. PMID: 33928638; PMCID: PMC8239799. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
7. Бостан Э., Гульсерен Д., Гокоз О. Новый лейкоцитокластический васкулит после COVID-19вакцина. Междунар. Дж. Дерматол. 9 июля 2021 г. doi: 10.1111/ijd.15777. Epub перед печатью. PMID: 34241833. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Дерматол. 9 июля 2021 г. doi: 10.1111/ijd.15777. Epub перед печатью. PMID: 34241833. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
8. Кампродон Гомес М., Гонсалес-Крус К., Феррер Б., Барбера М.Дж. Лейкоцитокластический васкулит у пациента с COVID-19 с положительная ПЦР SARS-CoV-2 при биопсии кожи. BMJ Case Rep. 29 октября 2020 г.; 13 (10) doi: 10.1136/bcr-2020-238039. PMID: 33122236; PMCID: PMC7597471. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
9. Доктор В., Хади А., Хади А., Фелпс Р., Гудхарт Х. Erythema elevatum diutinum: отчет о клиническом случае и обзор литературы. Междунар. Дж. Дерматол. 2019 апр; 58 (4): 408–415. doi: 10.1111/ijd.14169. Epub 2018 Aug 3. PMID: 30074624. [PubMed] [CrossRef] [Google Scholar]
10. Baigrie D., Bansal P., Goyal A., Crane J.S. StatPearls [Интернет]. Остров сокровищ (Флорида) StatPearls Publishing; 2021 11 августа. Лейкоцитокластический васкулит. 2021 янв.–. PMID: 29489227. [Google Scholar]
11. Кар Б.Р., Сингх Б.С., Мохапатра Л., Агравал И. Кожный васкулит мелких сосудов после COVID-19вакцина. Дж. Космет. Дерматол. 2021 ноябрь; 20 (11): 3382–3383. doi: 10.1111/jocd.14452. Epub 2021 Sep 16. PMID: 34529877. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Кар Б.Р., Сингх Б.С., Мохапатра Л., Агравал И. Кожный васкулит мелких сосудов после COVID-19вакцина. Дж. Космет. Дерматол. 2021 ноябрь; 20 (11): 3382–3383. doi: 10.1111/jocd.14452. Epub 2021 Sep 16. PMID: 34529877. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
12. Bencharattanaphakhi R., Rerknimitr P. Sinovac Кожный лейкоцитокластический васкулит, вызванный вакциной COVID-19. Представитель JAAD, декабрь 2021 г.; 18:1–3. doi: 10.1016/j.jdcr.2021.10.002. Epub 2021, 9 октября. PMID: 34660867; PMCID: PMC8501511. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
13. Sandhu S., Bhatnagar A., Kumar H., Dixit P.K., Paliwal G., Suhag D.K., Patil C., Mitra D. Лейкоцитокластический васкулит как кожное проявление ChAdOx1 nCoV-19вакцина против коронавируса (рекомбинантная) Дерматол. тер. 2021 ноябрь;34(6) doi: 10.1111/dth.15141. Epub 2021, 5 октября. PMID: 34546608; PMCID: PMC8646583. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
14.

 ч. оральная живая полиомиелитная вакцина (ОПВ) — иммунодефицитное состояние (первичное), иммуносупрессия, злокачественные новообразования. Беременность.
ч. оральная живая полиомиелитная вакцина (ОПВ) — иммунодефицитное состояние (первичное), иммуносупрессия, злокачественные новообразования. Беременность. ].
].