|
|
||||||||||
|
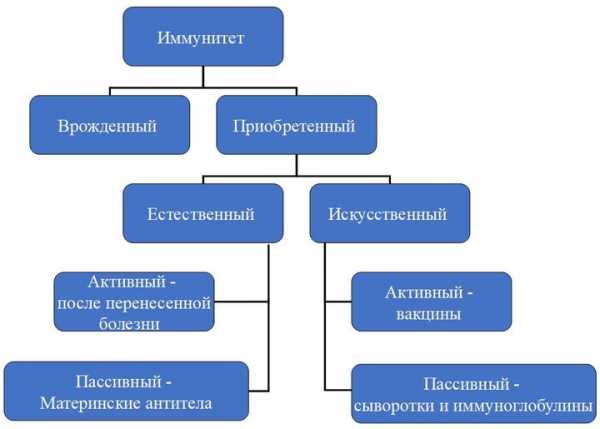
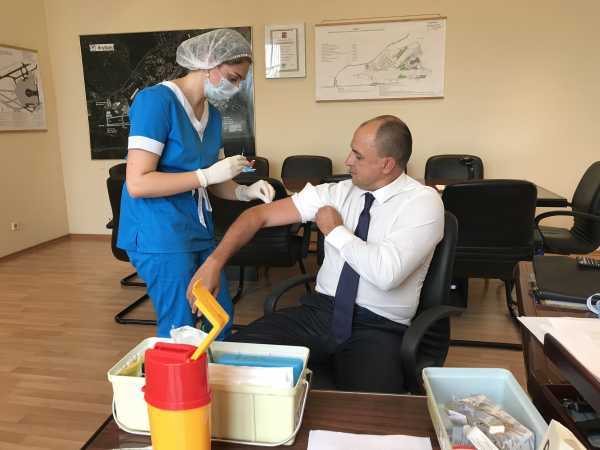
«Далеко ли до вакцины от ВИЧ?» Объясняем на пальцах. Прививки при вич инфекции«Далеко ли до вакцины от ВИЧ?» Объясняем на пальцахКакие бывают вакцины? Перед тем как говорить о вакцине против ВИЧ, стоит начать с более общего вопроса: что мы понимаем под прививками и вакцинами с научной точки зрения? По механизму возникновения иммунитет делится на два вида: врожденный и приобретенный. Первый есть у каждого человека с рождения, он выработан эволюционно. Благодаря нему человек не болеет многими болезнями, которыми, например, страдают животные. Второй возникает в течение жизни и у каждого может отличаться в зависимости от того, с какими возбудителями человеку довелось встретиться. по теме ЛечениеКак устроен иммунитет: Объясняем по пунктамПриобретенный иммунитет может быть активным (он возникает вследствие реакции организма на перенесенную болезнь, присутствие возбудителя в организме), а может быть пассивным, когда антитела, например, передаются от матери ребенку во время беременности. Пока мы не знаем точно, как возникает приобретенный активный иммунитет к ВИЧ-инфекции и сколько он держится, но знаем, что антитела к ней вырабатываются (даже несмотря на то, что организм самостоятельно не в силах справиться с ВИЧ). Именно по этим антителам, как правило, и ставится диагноз, если мы пользуемся экспресс-тестами. В случае с ВИЧ существует и пассивный иммунитет. Но при передаче вируса от матери ребенку, к сожалению, он не обладает достаточным защитным эффектом. Еще одно направление — это искусственный иммунитет. Он тоже бывает активным и пассивным. Пассивный — это иммуноглобулины, выработанные либо у лабораторных животных, либо у других иммунизированных лиц, и сыворотки. Активный же достигается собственно путем вакцинации. Вакцина — это биологический препарат, как правило, либо «убитый», либо живой, но ослабленный возбудитель болезни. Основная цель его введения в организм — и есть создание искусственного активного иммунитета. Вакцины бывают профилактические (защитные) и лечебные. Они различаются по типу воздействия на организм и по своим результатам. Пассивный иммунитет возникает быстрее, сразу после того, как в организм ввели чужие антитела. Однако он бывает совсем недолговременным. Активный иммунитет держится долго, чаще — пожизненно, но и возникает не сразу.
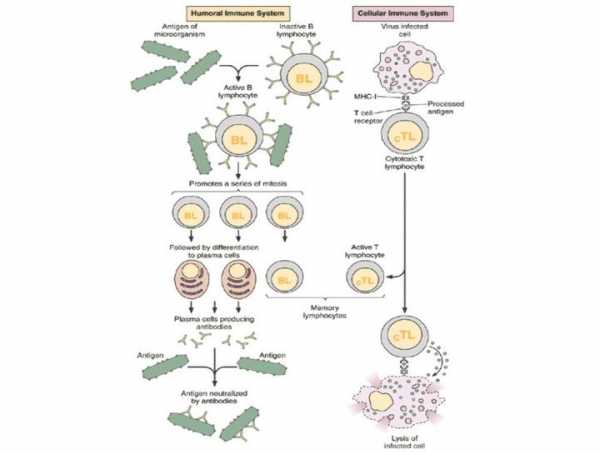
Иммунный ответ: как это все работает? Чтобы понять, как работает наш естественный иммунитет и почему организм сам не может справиться с ВИЧ-инфекцией, необходимо разобраться с тем, что такое иммунный ответ. Ученые обычно говорят о гуморальном и клеточном иммунитете. Принцип работы гуморального заключается в следующем: в нашем организме есть специальные клетки — лимфоциты. Они постоянно циркулируют в крови и проверяют все, что попадается им на пути, по принципу свой/чужой. по теме ЛечениеГид по вакцинам. Когда и какую прививку сделать? А главное: надо ли вообще прививаться? (Спойлер: конечно, надо)Как правило, организм знает заранее, как свои клетки отличить от чужеродных. Делает он это, ориентируясь по так называемым «антигенам» — белкам с поверхности вируса. Когда лимфоциты, а вернее их подтип, известный как В-клетки, встречают вирус, соединившись с ним, они передают информацию, что в крови обнаружен какой-то чужеродный остальным клеткам агент, и превращаются либо в «плазматические клетки», вырабатывающие антитела, которые потом соединятся с возбудителем-вирусом и убьют его, либо в «клетки памяти». Они остаются в организме, даже когда мы выздоравливаем, и играют роль своеобразной «библиотеки». Если организм успешно справился с болезнью, благодаря этим клеткам он запоминает «врага», и при новой встрече с ним реагирует гораздо быстрее. Обычно на весь процесс — от встречи до выработки антител — уходит от нескольких недель до месяцев. Например, антитела к ВИЧ-инфекции появляются где-то через месяц после заражения, соответственно, все это время вирус может циркулировать в организме. Почему они неэффективны? Во-первых, потому что появляются слишком поздно. Во-вторых, потому что вирус, с которым мы имеем дело, очень изменчив. Если даже В-клетки обнаружили его антиген, выработали к нему антитела, способные нейтрализовать заразу, то за время, которое ушло на все это, сам вирус успевает мутировать и оказаться неуязвимым для выработанного организмом оружия. Когда мы говорим о клеточном иммунитете, речь идет об уничтожении тех вирусов, которые преодолели гуморальный барьер и успели забраться в саму клетку. В нем участвуют уже другие клетки: Т-лимфоциты, к ним относятся в том числе известные CD4 и CD8. Они действуют не против возбудителей, циркулирующих в крови, а распознают «измененную», то есть зараженную вирусом клетку, и разрушают ее. Клетки CD4 частично регулируют весь процесс и выполняют функцию клеток памяти. Их принято называть хелперами. CD8 — собственно занимаются уничтожением, за это их зовут киллерами. ВИЧ — единственный вирус, который поражает не просто клетки организма, а собственно клетки иммунной системы. Той самой, которая с вирусом должна, по идее, бороться.
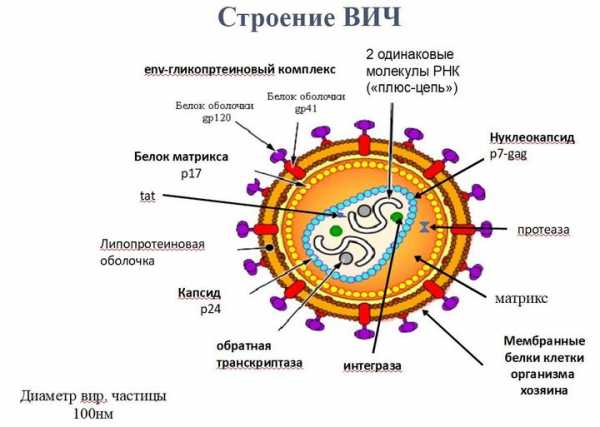
Несмотря на то, что ВИЧ поражает не киллеры, а клетки CD4, то есть хелперы, в случае с ВИЧ-инфекцией возникает порочный круг. При попытке избавиться от «врага» самостоятельно организм активирует систему уничтожения вирусов, в том числе и CD4-клетки, а вместе с тем, стало быть, активирует и дупликацию вируса. Именно поэтому против ВИЧ-инфекции иммунитет не может сработать так, как это было бы с любым другим вирусом. Какие возникают трудности при создании вакцины против ВИЧ? На данный момент в рамках более ста испытаний уже протестировано более сорока видов вакцин с участием тысяч добровольцев, и есть целая система, в которой регистрируются все исследования по вакцинации от ВИЧ. Последнее время в разного рода СМИ регулярно появляется информация, что той или иной компанией разрабатывается новая вакцина против ВИЧ. Однако обнадеживающих результатов не так уж и много. Почему? по теме ПрофилактикаКалендарь прививок для ВИЧ+: Когда и как нужно прививатьсяЛучшая из существующих вакцин, которая дошла до третьей фазы исследований, показала свою защитную эффективность только в 60 % случаев в течение одного года, а в течение уже трех лет — только в 30 %. Это очень мало для вакцины. Она должна давать до 90 % эффективности. И связано это с тем, что существует ряд препятствий для создания вакцины от ВИЧ-инфекции. Во-первых, такая вакцина не может состоять из ослабленного или живого вируса, как многие другие. Если ввести даже одну-две частицы ВИЧ в организм, это вызовет не иммунный ответ, а инфицирование организма. Во-вторых, и мы об этом уже сказали, вирус находится внутри CD4-лимфоцитов. Мы пока не научились извлекать вирус из клетки, не повреждая ее саму. И на данный момент до конца не понимаем, какие именно механизмы могли бы обеспечить полную защиту от ВИЧ-инфекции. В-третьих, многие вакцины пока разрабатываются, испытываются на подопытных животных: мышах, свиньях. В случае с ВИЧ кроме обезьян, на которых можно было бы воспроизвести инфекцию, у нас нет подходящих подопытных животных, результаты работы с которыми можно было бы легко перенести на человека. Исследования на людях дороги и имеют ряд этических ограничений. Можно было бы привить группу здоровых добровольцев, но инфицировать их, чтобы проверить, как работает вакцина, врачи не могут. Ни один подопытный на такое не согласится. А вдруг вакцина не сработает?
Более того, врачи не имеют права провоцировать рискованное поведение своих пациентов: дать вакцину и рекомендовать прекратить пользоваться презервативами, или попросить использовать по возможности нестерильные инструменты. «Вы попробуйте, а мы посмотрим!» Разработки вакцины. Дорожная карта Тем не менее ученым уже удалось выработать основные направления в иммунотерапии ВИЧ-инфекции. С одной стороны — это попытка активации специфического иммунитета, который не срабатывает при естественном течении ВИЧ-инфекции. С другой стороны — профилактическая пассивная иммунизация. Что значит пассивная? Мы подозреваем, что существуют люди, которые не инфицируются ВИЧ даже при достаточно частом контакте с вирусом. Видимо, у них возникает хороший иммунный ответ, и иммунная система справляется с вирусом самостоятельно. А значит, мы можем попытаться либо взять у уже иммунизированных лиц готовые антитела, либо создать их генно-инженерным путем, чтобы потом ввести в организм. по теме ЭпидемияУчёные выяснили, как вирусы обманывают иммунитетКлинические исследования в области ВИЧ-инфекции по пассивной иммунизации начались еще в начале 80-х годов, то есть одновременно с обнаружением самого вируса. И самые большие ставки в случае с пассивным иммунитетом сейчас делаются на так называемые «нейтрализующие антитела широкого спектра действия». Это антитела, которые были впервые обнаружены и описаны в 2001 году. Они встречаются как раз у того типа пациентов, который мы только что назвали. В эксперименте на животных было показано: если у организма есть эти антитела, даже в случае нарочного введения вируса заражения не происходит. Интересно, что эти антитела не убивают вирус, но они могут с ним соединяться, блокируя его рецепторы, как бы окружая и покрывая вирус, не давая ему обычным способом проникнуть в клетку. Через какое-то время вирус, не найдя клетки, где он может размножиться, погибает. Предполагается, что, если именно эти антитела удастся искусственно синтезировать либо «вырастить» в организме уже иммунизированных животных, а потом перевезти их или каким-то образом ввести здоровым людям, это может предотвратить развитие ВИЧ-инфекции. Механизм действия антител широкого спектраЧто касается «активного» иммунитета, в 2017 году было начато исследование, оно проводится в странах Африки, где самая высокая распространенность ВИЧ, и в его рамках в ближайшие годы предполагается привить около 2 600 сексуально активных женщин в возрасте от 16 до 35 лет. Суть этой экспериментальной вакцины заключается в том, что состоит она из двух разных антигенов, синтезированных искусственно, но идентичных белкам настоящего вируса. Искусственная комбинация белков не может сама по себе вызвать развитие инфекции, но, по идее, должна вызвать развитие антител — такое, каким бы оно было в норме при попадании вируса в организм. В течение первых 12 месяцев исследования каждая из женщин, участвующих в нем, получит шесть инъекций: три инъекции — в течение первого месяца и по одной — каждый последующий. Первые результаты ожидаются где-то к 2021 году. Однако здесь есть нюансы: белки, с которыми работают ученые в рамках указанного исследования, аналогичны для субтипа ВИЧ, распространенного в Африке, но редко встречающегося у нас, в России. Когда человечество приступит к разработке подобной вакцины против «российского ВИЧ», пока сказать сложно. Однако очевидно, что не в ближайшие месяцы. Итоги: ДКП, ПКП, АРВТ Возвращаясь к поставленному вопросу: далеко ли нам до вакцины против ВИЧ? То есть «прививки»? Далеко. В настоящее время есть некоторые инфекции, которые человечество эффективно научилась контролировать с помощью вакцинации, а некоторые и вовсе победить, как оспу. Но рассчитывать на скорый результат в случае с ВИЧ пока не приходится. Возможно, комбинация всех перечисленных подходов, пассивного и активного иммунитета, одновременно сможет стать эффективной, чтобы оказывать профилактическое воздействие. Однако пока в контексте ВИЧ-инфекции действовать нам придется на популяционном уровне — традиционными способами профилактики распространения заболевания. В первую очередь это: практики более безопасного сексуального поведения, использование стерильных инструментов во всех медицинских сферах, доконтактная профилактика, постконтактная профилактика и эффективная антиретровирусная терапия. spid.center
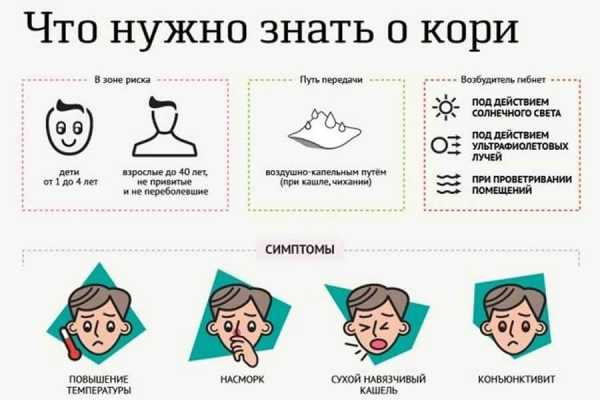
medi.ru Вопросы и ответы по вакцинации ВИЧ-инфицированныхВОПРОСЫ И ОТВЕТЫ: ВАКЦИНАЦИЯ ВИЧ-ИНФИЦИРОВАННЫХ ЛИЦ В.К. ТаточенкоНаучный центр здоровья детей РАМН, Москва Какие из управляемых инфекций протекают особенно тяжело у инфицированных ВИЧ лиц?Тяжело протекает корь с вовлечением легких у 75%, достигающая 50% летальности. Повышенная воспримчивость ВИЧ-инфицированных к кори, возможно, связана с более низким уровнем у них трансплацентарных антител. Инфицированные ВИЧ дети склонны к диссеминированным формам туберкулеза, улучшение на фоне лечения наступает медленно и далеко не у всех больных.Заболеваемость пневмококковой инфекцией у инфицированных ВИЧ детей в 100-150 раз выше, чем у неинфицированных с тяжелым течением заболевания. Высока и заболеваемость инфекцией, вызванной H. influenzae, однако, в отличие от здоровых детей, среди возбудителей, вызывающих инфекцию, преобладают другие, нежели b, серотипы.Гепатит В у этих детей протекает в отсутствие признаков тяжести. Также ВИЧ-инфекция лишь незначительно повышает риск тяжелого течения гриппа. Большинство детей с относительно сохранным иммунным статусом болеют ветряной оспой средней тяжести, но при числе CD4+ Каковы правила проведения прививок инактивированными вакцинами ВИЧ-инфицированных лиц?В связи с сохранением способности ВИЧ-инфицированных отвечать на вакцинные антигены, прививки АКДС и вакциной гепатита В должны проводится как инфицированным ВИЧ детям, так и детям с неподтвержденным инфицированием (от ВИЧ-инфицированных матерей) в обычные календарные сроки, вне зависимости от тяжести клинических проявлений и иммунологической классификации. Безопасность вакцинации коклюшной вакциной детей инфицированных ВИЧ матерей подтверждена в проспективном совместном исследовании в Европе (239 человеко-лет наблюдения). Насколько полноценно отвечают ВИЧ-инфицированные лица на введение инактивированных вакцин?Иммунный ответ на некоторые вакцины у таких детей может быть снижен, так что, например, после введения столбнячного анатоксина титры антител были ниже и быстрее снижались до уровня ниже защитного. На гепатитную В вакцину в дозе 20 мкг (по схеме 0-1-6) защитные уровни определяются лишь у 80% инфицированных ВИЧ детей. Это указывает на целесообразность серологического контроля и введения дополнительных доз в случае слабого ответа на вакцины.Дети, неинфицированные ВИЧ в родах, (у которых антитела к ВИЧ исчезают), дают хороший ответ на вакцины, что указывает на целесообразность вакцинации против гепатита В новорожденных от ВИЧ-инфицированных матерей. Как защитить ВИЧ-инфицированных детей от полиомиелита?Ввиду нежелательности использования у ВИЧ-инфицированных детей оральной полиомиелитной вакцины, их следует прививать инактивированной полиовакциной (ИПВ) в обычные календарные сроки. Это же относится ко всем детям ВИЧ-инфицированных матерей (до установления их статуса в отношении ВИЧ-инфекции). Частота сероконверсии и уровни антител у ВИЧ-инфицированных детей мало отличаются от таковых у ВИЧ-негативных. Как вакцинировать ВИЧ-инфицированных детей живыми вирусными парентеральными вакцинами?ВОЗ рекомендует вакцинацию ВИЧ-инфицированных против кори, а также против краснухи и эпидемического паротита, вопреки описанию тяжелого поражения легких, связанного с противокоревой прививкой. Безопасность иммунизации этими вакцинами была подтверждена отсутствием побочных реакций после вакцинации против кори. Исключение составляют дети с тяжелой иммуносупрессией (категория 3 по классификации).Частота специфических реакций на коревую вакцину у детей матерей с ВИЧ-инфекцией и ВИЧ-отрицательных матерей не различается. Однако частота сероконверсии и титры антител у первых были ниже, в основном, за счет детей с более низким уровнем CD4+. Показатели сероконверсии к краснухе отличаются мало. Сниженный иммунный ответ явился основанием для рекомендаций ряда авторов введения второй дозы в возможно более близкий период (через 4 недели), хотя, по мнению других, повторная доза ненамного улучшает результаты вакцинации. Опасно ли введение БЦЖ инфицированным ВИЧ больным?БЦЖ у инфицированных ВИЧ детей раннего возраста может вызвать генерализованное поражение, однако это наблюдается редко. Чаще возникает регионарный лимфаденит. Это явилось основанием для отводов от введения этой вакцины всем детям ВИЧ-инфицированных матерей вне зависимости от их статуса, в соответствии с нормативными документами МЗ РФ.Однако, в когортных исследованиях было показано, что вакцинация новорожденных от ВИЧ-инфицированных матерей сопровождается лишь небольшим учащением слабых и умеренно выраженных реакций и отсутствием серьезных осложнений. С учетом тяжести туберкулеза у ВИЧ-инфицированных детей в развивающихся странах, ВОЗ рекомендована вакцинация при рождении всех детей, вне зависимости от ВИЧ-статуса матери. Может ли вакцинация ВИЧ-инфицированных лиц отрицательно повлиять на иммунный статус вакцинируемого и течение ВИЧ-инфекции?Такие опасения высказывались, но оказались напрасными: ни количество CD4+ клеток, ни содержание ВИЧ в крови больных до и после введения вакцин (гриппозной, АКДС) значимо не отличались, что лишний раз указывает на безвредность вакцинации. Следует ли считать вакцинированных ВИЧ-инфицированных детей защищенными от соответствующей инфекции?Ввиду того, что эти дети могут не давать адекватного иммунного ответа на вакцину, в случае контакта c инфекцией им целесообразно проводить пассивную иммунопрофилактику соответствующими специфическими иммуноглобулинами или сыворотками (противостолбнячными, противокоревыми). В основном, это относится к детям с клиническими проявлениями ВИЧ-инфекции.В семьях, где есть инфицированные ВИЧ лица и серонегативные дети, вакцинация должна проводиться со всей тщательностью всеми вакцинами (включая гриппозную), заменяя лишь ОПВ на ИПВ. Какие прививки вне календаря прививок желательно провести ВИЧ-инфицированным лицам?Ввиду особой тяжести течения настоятельно рекомендуется проведение активной профилактики пневмококковой инфекции, а также гриппа соответствующими убитыми вакцинами (в частности, ПНЕВМО 23 - после 2 лет). В ответ на гриппозную вакцину эти дети вырабатывают антитела столь же часто, как и их неинфицированные сверстники, хотя уровни антител у них, особенно при наличии даже минимальных клинических проявлений ВИЧ-инфекции, несколько ниже. Ответ на пневмококковую вакцину, однако, у ВИЧ-инфицированных хуже, чем у свободных от ВИЧ-инфекции лиц. medi.ru Вакцинопрофилактика у детей с вич-инфекцией.Вакцинопрофилактика детей проводится по месту жительства под контролем врачей Республиканского и областного центра профилактики СПИД. В поствакцинальном периоде проводится патронаж ребенка на 3-4-е и 10-11-е сутки. При возможности, осуществляется госпитализация ребенка в поствакцинальном периоде. Перед вакцинацией за 1-2 недели целесообразно назначить поливитамины, содержащие витамин А. Основные принципы иммунизации ВИЧ-инфицированных детей: - рекомендуется максимально возможное сохранение принятого в нашей стране прививочного календаря; - исключение из прививочного календаря вакцины БЦЖ; - дети с ВИЧ-инфекцией на стадии 2(АИ) – 3 (ПГЛ) при отсутствии других противопоказаний, не связанных с ВИЧ-инфекцией, прививаются в соответствии с обычным прививочным календарем; - дети с ВИЧ-инфекцией на стадии 1 (острая инфекция) прививаются не ранее, чем через месяц после исчезновения клинических симптомов острой инфекции; - дети, наблюдаемые в период сероконверсии, при отсутствии клинических симптомов острой стадии ВИЧ-инфекции прививаются после стабилизации показателей иммунного блота; - дети с ВИЧ-инфекцией на стадии вторичных заболеваний (4ст) прививаются в период ремиссии вторичного заболевания длительностью более 1 месяца; - детям на стадии СПИД проводится пассивная иммунизация по эпидемиологическим или клиническим показаниям; - дети с тромбоцитопенией (тромбоцитов менее 150х10/л), вне зависимости от стадии ВИЧ-инфекции, прививаются ранее, чем через 1 месяц после стойкой нормализации количества тромбоцитов, после вакцинации через 3-4 недели целесообразно введение поливалентного иммуноглобулина, по эпидемиологическим показаниям при сохранении тромбоцитопении проводится пассивная иммунизация. Следует подчеркнуть, что дети с ВИЧ-инфекцией при прогрессировании заболевания теряют антитела, ассоциированные с вакциной. Поэтому в случае контакта с инфекционными больными, независимо от прививочного анамнеза с профилактической целью показано введение специфического иммуноглобулина или соответствующих антибактериальных препаратов. При отсутствии специфических иммунопрепаратов возможно введение поливалентного человеческого иммуноглобулина внутривенно (в возрасте до 5 лет два дня подряд, детям старшего возраста по 50 мл два дня подряд). 10. Задания для самостоятельной работы студента.1. Изучение приложений к приказу МЗ РБ № 317 от 10.07.1995 года и информационного письма «ВИЧ-инфекция (клиника, диагностика и современные принципы лечения»). - Минск, 1998.-14с. 2. Изучение методических рекомендаций «Этиотропная терапия ВИЧ-инфекции и сопутствующих заболеваний». Минск, 1999,-26с. 3. Изучение методических рекомендаций «Применение цитокинов в терапии ВИЧ-инфекции». Санкт-Петербург, 2000.-26с. 4. Курация больных или работа с архивными историями болезни. 5. Отработка методов физикального обследования больных ВИЧ/СПИД в том числе на пациентах без ВИЧ/СПИД. 11. Самоконтроль усвоения темы:1. ВИЧ относится к ретровирусам потому что имеет: 1. РНК двунитчатую. 2. Фермент гиалуронидазу. 3. Фермент ревертазу (обратную транскриптазу). 4. Рецепторы на оболочке для СД-4 клеток. 2. Провирус ВИЧ это: 1. Ревертаза. 2 Поверхностный белок др. 120. 3. Серцевинный белок р 2. 4. ДНК вируса, интегрированная в геном клетки. 3. Пути передачи ВИЧ от матери детям: 1. Трансплацентарный. 2. В процессе родов. 3. При бытовых контактах. 4. При поцелуях. 5. При кормлении грудью. 4. Причина развития СПИД при ВИЧ-инфекции: 1. Агранулоцитарные реакции. 2. Снижение количества Т-хельперных лимфоцитов. 3. Снижение количества Т-супрессорных лимфоцитов. 4. Снижение количества лимфоцитов-киллеров. 5. Снижение количества В-лимфоцитов. 5. Начальная (острая) ВИЧ-инфекция заканчивается: 1. Летально. 2 Выздоровлением клиническим. 3. Полным выздоровлением с эрадикацией вируса. 4. Развитием саркомы Капоши. 6. Проявление врожденной ВИЧ-инфекции; 1. Дисморфия костей черепа. 2. Гепатомегалия. 3. Макросомия. 4. Врожденные пороки сердца. 7. Тип развития СПИДа, не характерного для детей; 1. Пневмонический. 2. Опухолевый. 3. Церебральный. 4. Диарейный. 8. Материнские анти-ВИЧ антитела у ребенка могут определяться в течение6 1. Первого месяца жизни. 2. Первых 3-х месяцев. 3. 6 месяцев. 4. 1 года. 5.полутора лет. 9. К СПИД-маркерным заболеваниям у детей относятся; 1. Врожденная дисморфия костей черепа. 2. Лимфоидная интерстициальная пневмония. 3. Токсоплазмоз ЦНС и внутренних органов. 4. Кандидамикоз. 5. Герпетическая инфекция. 10. Этиотропная терапия ВИЧ-инфекции проводится: 1. Непрерывно с момента диагностики. 2. Только при САС. 3. Последовательно применяя препараты с начала одной, а затем по необходимости и других групп. 4. Одновременно используя препараты разных групп. studfiles.net Делают ли прививки ВИЧ-инфицированным людямУ пациентов, страдающим ВИЧ-инфекцией иммунная система ослаблена этим вирусом. Любые прививки на какое-то время также ослабляют защитные силы организма. Закономерно встаёт вопрос — можно ли делать обычные прививки при ВИЧ-инфекции? Не все прививки опасны для инфицированных больных. Вакцины делятся на живые и инактивированные (убитые или ослабленные). После введения живого препарата человек переносит лёгкую форму заболевания, после чего вырабатывается иммунитет. Вот такая прививка представляет опасность для больных ВИЧ. Но есть инактивированные вакцины, после которых человек не заболевает. Для инфицированных ВИЧ людей гораздо большую опасность представляет заражение инфекцией. Ослабленный иммунитет не даст возможность с ней справиться. Поэтому инфицированным людям жизненно необходимы прививки от следующих заболеваний. 1. От гриппа прививают людей до начала разгара сезонной эпидемии. 2.Прививка от кори, краснухи и паротита делают здоровым людям один раз в жизни. Но у инфицированных людей эту живую вакцину делают не всегда — сначала проверяют уровень иммунного статуса. Допустимый уровень должен быть не меньше 200 клеток на 1 мл. 3.Прививка от гепатита — ВИЧ-инфицированным людям она необходима. Вакцинация от вируса A защищает человека на 20, от гепатита B — на 10 лет. 4.Прививка от пневмонии необходима больным ВИЧ, потому что они подвержены заражению в 100 раз чаще, чем здоровые. Ведь в случае заболевания болезнь заканчивается летальным исходом. Прививка защищает людей на 5 лет. 5.От дифтерии и столбняка после прививки в детском возрасте ревакцинацию делают раз в 10 лет. Но инфицированным ВИЧ пациентам её делают под контролем уровня иммунитета. Больным ВИЧ-инфекцией прививки делают в центре борьбы со СПИДом под наблюдением врачей. За 2 недели до вакцинации им проводят курс витаминотерапии для поддержки иммунитета. Некоторые прививки для этих больных являются обязательными. Источник: http://privivku.ru/novosti-vakcinacii/vakcina-ot-vich.html#delayut-li-privivki-vich-infitsirovannym-lyudyam sofdac24.ru Вакцинация и ВИЧ-инфекция - Медицинский портал EUROLABПо мере прогрессирования ВИЧ-инфекции присоединяются бактериальные, вирусные, грибковые и онкологические заболевания (саркома Капоши, первичная лимфома и пр.). ВИЧ-инфицированные лица относятся к группе людей высокого и постоянного риска заражения, в связи с этим крайне важной является правильная и своевременная специфическая профилактика возможных сопутствующих инфекций. При иммунизации ВИЧ-инфицированных лиц любыми вакцинами соблюдаются все противопоказания, существующие для здоровых людей Кроме того, имеется ряд дополнительных требований:
Помимо АКДС, ИПВ и гепатитной В вакцин ВИЧ-инфицированным детям рекомендуется вакцинация гемофилюсной b вакциной с возраста 3 месяца), гриппозной субъединичной или сплит-вакциной (с возраста 6 месяцев) и пневмококковой вакциной (после 2 лет). Ввиду возможного снижения иммунного ответа у этой категории вакцинируемых рекомендуется контролировать результаты иммунизации путем определения титров соответствующих антител. Не может служить поводом для отказа от вакцинации выявление у ребенка без соответствующей клинической картины отклонений показателей иммунного статуса, не достигающих уровней, характерных для конкретного иммунодефицита. Нерезкое снижение уровней иммуноглобулинов, изменения в соотношении субпопуляций лимфоцитов, численности Т-клеток и т.д. закономерно возникают при различных заболеваниях и состояниях. Дети и взрослые, не имеющие клинических проявлений иммунодефицитных состояний, должны прививаться на общих основаниях. www.eurolab.ua ВИЧ инфекция - исследования, лечение, вакцинация, показания и профилактика ВИЧ инфекции Исследования, лечение, вакцинация, показания и профилактика ВИЧ инфекции. ВИЧ инфекцияРеклама
Инфекция, обусловленная вирусом иммунодефицита человека, вызывается ретровирусом ВИЧ-1. Заболевание ведет к прогрессирующему истощению иммунной системы и развитию оппортунистических инфекций и новообразований; в терминальной стадии развивается синдром приобретенного иммунодефицита. Диагноз ставят на основании обнаружения противовирусных антител у детей старше 18 месяцев, а также ПЦР-диа-гностики у детей младше 18 месяцев. Лечение проводят комбинацией анти-ретровирусных препаратов.
В целом патофизиология ВИЧ-инфекции у детей сходна с таковой у взрослых; однако механизм инфицирования, клинические проявления и лечение зачастую различаются. У ВИЧ-инфицированных детей также отмечаются специфические проблемы, связанные с социальной интеграцией.
ВИЧ инфекция — эпидемиология
В США ВИЧ у детей стал появляться примерно в то же время, что и у взрослых, однако в течение нескольких лет клинически не диагностировался. До настоящего времени отмечено более 9300 случаев ВИЧ-инфекции у детей и подростков, что представляет лишь 1 % от общего числа случаев.
Более 90 % детей в США заразились от матерей либо внутриутробно, либо инт-ранатально. Большая часть оставшихся получали трансфузии зараженной крови или ее препаратов. Несколько случаев заражения произошли в результате сексуального насилия. Меньше чем в 5 % случаев не обнаруживают никакого очевидного источника инфицирования. Вертикальный путь передачи отмечается практически во всех случаях регистрируемых заболеваний у детей в США до подросткового возраста.
Во всем мире около 2,5 млн детей живут с ВИЧ-инфекцией, а около 700 тыс. детей инфицируются ежегодно. В Африке в районе Сахары, где эпидемия длится дольше всего, некоторые пренатальные центры сообщают, что от 25 до 40 % всех женщин детородного возраста серопозитивны. ВИЧ-инфекция быстро распространяется в Индии, Китае, Юго-Восточной Азии и некоторых областях Восточной Европы и России. Ежегодно в мире от ВИЧ-инфекции умирает примерно 500 тыс. детей.
Инфицирование ВИЧ инфекцией
Риск инфицирования для младенца, рожденного ВИЧ-положительной матерью, которая не получала антиретровирусную терапию в течение беременности, составляет от 13 до 39 %. Самый высокий риск отмечается у младенцев, рожденных матерями, у которых сероконверсия произошла во время беременности, а также при манифестных формах СПИДа у матери, низком уровне CD4+ Т-лимфоцитов в периферической крови, позднем разрыве плодных оболочек.
Нет причин ограничивать усыновление и прием на воспитание ВИЧ-инфицированных детей. Условия, которые могут представлять повышенный риск для окружающих, могут потребовать специальных мер предосторожности.
Число сотрудников школы, осведомленных о состоянии ребенка, должно быть сведено к минимуму, необходимому для обеспечения должного ухода. У семьи есть право информировать школу, однако лица, вовлеченные в уход и обучение ребенка, должны уважать право ребенка на сохранение тайны. Распространять информацию можно только с согласия родителей или законных опекунов, а также согласия самого ребенка с учетом его возраста.
При высокой вирусной нагрузке, выявляют определением высокой концентрации вирусного белка р24 в крови, количественным выделением вируса или определением концентрации РНК. При родах per vias naturales у близнеца, который рождается первым, риск инфицирования выше, чем у рождающегося вторым, хотя это отношение, по-видимому, может не быть таковым в развивающихся странах.
Кесарево сечение может уменьшить риск передачи ВИЧ-инфекции от матери ребенку. Однако ясно, что риск передачи ВИЧ-инфекции от матери к ребенку может быть значительно снижен при использовании антиретровирусной терапии [включая зидовудин ] у матери и новорожденного. Монотерапия ZDV сокращает риск передачи ВИЧ-инфекции от матери к ребенку приблизительно до 8 %; при применении современных высокоактивных схем антиретровирусной терапии риск передачи ВИЧ-инфекции от матери к ребенку в США составляет менее 2 %.
ВИЧ был обнаружен как в клеточной, так и внеклеточной фракциях грудного молока человека. Передача ВИЧ-инфекции при кормлении грудью отмечается с частотой примерно 6 случаев на 100 детей на грудном вскармливании в год. Общий риск передачи ВИЧ-инфекции через грудное вскармливание оценивается в 12—14 %, отражая различную длительность вскармливания. Риск передачи ВИЧ-инфекции через грудное вскармливание оказывается выше у матерей с более высокой вирусной нагрузкой.
Заражение ВИЧ в подростковом периоде значительно влияет на рост случаев заболевания у людей молодого возраста. Пути передачи у подростков подобны таковым у взрослых, главным образом при незащищенных сексуальных контактах и реже при внутривенной наркомании.
Классификация. ВИЧ-инфекция вызывает широкий спектр заболеваний, из которых СПИД является самым серьезным. Эпидемиологические схемы классификации, принятые CDC, учитывают прогрессирование клинических и иммунологических нарушений. У детей младше 13 лет клинические категории N, А, В и С обозначают асимптоматические и легкие, умеренные и тяжелые манифестные, соответственно.
Категория N: бессимптомная ВИЧ инфекция
Дети, у которых отсутствуют симптомы и признаки, считающиеся следствием ВИЧ-инфекции, или отмечается одно из состояний, перечисленных в категории А Категория А: легкая манифестная Дети с наличием 2 и более условий, перечисленных ниже, при отсутствии условий, перечисленных в категориях В и С Дерматит Гепатомегалия, Лимфаденопатия Паротит. Рецидивирующая или персистирующая инфекция верхних дыхательных путей, синусит или средний отит Спленомегалия.
Категория В: умеренная манифестная ВИЧ инфекция
Дети, которые имеют клинические признаки, характерные для ВИЧ-инфекции, кроме перечисленных в категории А, но не перечисленные в категории С. Примеры включают, но не ограничиваются следующими: Анемия, нейтропения, или тромбоцитопения, сохраняющиеся более 30 дней Бактериальный менингит, пневмония или сепсис Кандидоз ротоглотки, сохраняющийся у детей старше 6 месяцев Кардиомиопатия Цитомегаловирусная инфекция с началом в возрасте до 1 месяца Диарея, рецидивирующая или хроническая Гепатит Герпетический стоматит, рецидивирующий Герпетические бронхит, пневмонит или эзофагит, с началом в возрасте до 1 месяца Герпес зостер по крайней мере 2 отдельных эпизодов или охватывающий более 1 дерматоме Лейомиосаркома Лимфатический интерстициальный пневмонит или легочный комплекс лимфоидной гиперплазии Нефропатия Нокардиоз Длительная лихорадка Токсоплазмоз с началом в возрасте до 1 месяца Ветряная оспа, генерализованные формы.
Категория С: тяжелая манифестная ВИЧ инфекция
Серьезные бактериальные инфекции, многократные или рецидивирующие, следующих типов: септицемия, пневмония, менингит, инфекция кости или сустава, или абсцесс внутреннего органа или полости Кандидоз пищевода или дыхательных путей Кокцидиомикоз, диссеминированный Криптококкоз, внелегочный Криптоспоридиоз или изоспориаз с диареей, персистирующей более 1 месяца Цитомегаловирусная инфекция, с началом в возрасте старше 1 месяца
Энцефалопатия :
1) отсутствие в соответствующем возрасте или потеря приобретенных навыков и умений или снижение интеллектуальных способностей, подтвержденное по стандартным шкалам развития или нейропсихологическими тестами; 2) нарушение роста мозга или приобретенная микроцефалия, демонстрируемые измерением окружности головы, или атрофия головного мозга, демонстрируемая на КТ или МРТ ; 3) приобретенный симметричный моторный дефицит, проявляющийся двумя или более синдромами из нижеперечисленного: парез, патологические рефлексы, атаксия, нарушение походки Герпетическая инфекция, проявляющаяся образованием язв на коже и слизистых оболочках, сохраняющихся более 1 месяца; или бронхитом, пневмонитом или эзофагитом при любой длительности, поражающая детей в возрасте старше 1 месяца Гистоплазмоз, диссеминированный Саркома Капоши Лимфома, первичная, головного мозга.
Мелкоклеточная лимфома
Мелкоклеточная лимфома, или иммунобластная, или крупноклеточная В-клеточная лимфома, или лимфома с неизвестным иммунофенотипом Mycobacterium tuberculosis, с диссеминацией или внелегочной локализации Mycobacterium, другие виды или неидентифицированные виды, с диссеминацией.
Пневмония, вызванная Pneumocystis jiroveci Прогрессирующая мультифокальная лейкоэнцефалопатия Сальмонеллезная септицемия, рецидивирующая Токсоплазмоз головного мозга с началом в возрасте старше 1 месяца Истощение при отсутствии сопутствующей болезни, кроме ВИЧ-инфекции, которая могла объяснить следующие полученные данные:
1) постоянная потеря массы тела более 10 % от исходной, или 2) нисходящее пересечение по крайней мере 2 из следующих перцентильных линий на стандартной кривой массы тела у ребенка старше 1 года, или 3) менее 5-й перцентили на стандартных массо-ростовых кривых при 2 последовательных измерениях с промежутком в 30 дней плюс хроническая диарея или подтвержденное документально повышение температуры тела ВПГ — вирус простого герпеса. 1 Категории формируют однонаправленную иерархию так, что болезнь пациента проходит от категории N к А, затем к В, потом к С. Например, если ребенок имеет гепатомегалию и лимфаденопатию и у него развивается постоянная анемия, то ребенок переходит в категорию В. Если анемия в конечном счете исчезает, то ребенок останется классифицированным в категории В. Если развивается пневмоцистная пневмония, ребенка реклассифициру-ют в категорию С. Точно также иммунологические категории формируют однонаправленную иерархию; если у ребенка с количеством CD4+ лимфоцитов, соответствующим категории 2, отмечается такое повышение CD4+ лимфоцитов на фоне терапии, что количество клеток достаточно, чтобы входить в категорию 1, ребенок, тем не менее, остается классифицированным в иммунологической категории 2.
Адаптировано из: Centers for Disease Control and Prevention. 1994 Revised classification system for HIV infection in children less than 13 years of age; official authorized addenda: HIV infection codes and official guidelines for coding and reporting ICD-9-CM. MMWR 1994; 43, pp. 1—19.
Легкий, умеренный и тяжелый иммунодефицит обозначается как категории 1, 2 или 3 соответственно; они определяются уровнем CD4+ Т-лимфоцитов с учетом возраста ребенка. Таким образом, ребенок, по классификации имеющий стадию ВЗ, будет иметь умеренно выраженные клинические проявления и тяжелое нарушение иммунитета.
При интранатальном инфицировании клинические проявления, как правило, от-сутствут в течение первых нескольких месяцев жизни. Хотя средний возраст появления симптомов составляет примерно 3 года, у некоторых детей клинические проявления отсутствуют до 5 лет и более, и при адекватной антиретровирусной терапии пациенты могут дожить до взрослого возраста. До применения АРВ терапии около 10—15 % детей имели быстропрогрессирующее течение болезни, с развитием симптомов на первом году жизни и смертельным исходом в возрасте 18—36 месяцев; как предполагается, эти дети заразились ВИЧ-инфекцией на более ранних сроках внутриутробного развития. У большинства детей, однако, скорее всего передача инфекции происходит во время родов или в раннем послеродовом периоде, и у них отмечается более медленное прогрессирование заболевания.
Наиболее распространенные проявления ВИЧ-инфекции у детей включают генерализованную лимфаденопатию, гепа-томегалию, спленомегалию, гипотрофию, кандидоз полости рта, поражение ЦНС, лимфатический интерстициальный пневмонит, рецидивирующую бактериемию, оппортунистические инфекции, рецидивирующую диарею, паротит, кардиомиопатию, гепатит, не-фропатию и злокачественные новообразования.
Осложнения. Пневмония, вызванная Pneumocystis jiroveci, является наиболее распространенной тяжелой оппортунистической инфекцией у ВИЧ-инфицированных детей и имеет высокую летальность. Пневмоцистная пневмония может развиваться уже в возрасте 4—6 недель, однако в большинстве случаев наблюдается у младенцев в возрасте между 3 и 6 месяцами, которые заражаются во время родов или незадолго до или после них. У младенцев и детей с пневмоцистной пневмонией характерно развитие подострого диффузного пнев-монита с одышкой в покое, тахипноэ, снижением сатурации 02, непродуктивным кашлем и повышением температуры тела.
Другие распространенные оппортунистические инфекции включают кандидозный эзофагит, генерализованную цитоме-галовирусную инфекцию и хроническую или генерализованную герпетическую или вызванную вирусом ветряной оспы инфекцию и реже осложненные инфекции, вызванные Mycobacterium tuberculosis и Mycobacterium avium, хронический энтерит, вызванный криптоспоридиями или другими микроорганизмами, и диссеминиро-ванные или с поражением ЦНС-инфекции, вызванные криптококками.
Злокачественные новообразования у детей с иммуносупрессией при ВИЧ-инфекции встречаются относительно редко, однако лейомиосаркомы и некоторые лимфомы, включая лимфомы ЦНС и неходжкинские В-клеточные лимфомы, отмечаются значительно более часто, чем у детей без иммуносупрессии. Саркома Капоши встречается очень редко у ВИЧ-инфицированных детей.
Диагноз. ВИЧ-специфические тесты
У детей старше 18 месяцев диагноз ставят на основании серологического исследования с определением антител в сыворотке крови [иммуноферментный анализ и подтверждающая реакция иммунобло-тинга], как и у взрослых. Только крайне редко у ВИЧ-инфицированного ребенка старшего возраста может отмечаться недостаток анти-ВИЧ антител в связи с выраженной гипогаммаглобулинемией.
У детей младше 18 месяцев сохраняются материнские антитела, что приводит к ложноположительным результатам ИФА, поэтому диагноз ставят на основании определения ДНК ВИЧ инфекции методом ПЦР, при этом можно диагностировать приблизительно 30 % от всех случаев при рождении и почти 100 % в возрасте 4—6 месяцев. Вирусологическое исследование имеет приемлемые чувствительность и специфичность, но технически является более требовательным и опасным, поэтому в большинстве лабораторий оно было заменено выявлением ДНК методом ПЦР. Определение РНК ВИЧ методом ПЦР у детей, не получавших АРВ-терапию, также чувствительно, как и определение ДНК методом ПЦР. В то же время в связи с возможной нечувствительностью метода у детей, получающих АРВ-терапию, и возможной неспецифичностью низких концентраций РНК, определение РНК ВИЧ методом ПЦР не рекомендуется для диагностики у детей первого года жизни. Модифицированный тест выявления вирусного антигена р24 менее чувствителен, чем определение ДНК ВИЧ методом ПЦР и вирусологическим методом, и должен использоваться, только если последние недоступны.
Начальный тест определения ДНК ВИЧ методом ПЦР должен быть выполнен специфические экспресс-тесты дадут главным образом ложноположительные результаты. В то же время, если ожидаемая вероятность ВИЧ высокая, прогностическая ценность положительных результатов возрастает.
Перед обследованием ребенка на ВИЧ мать или лицо, ухаживающее за ним, и ребенок, если он достаточно взрослый, должны быть поставлены в известность о возможных психосоциальных рисках и преимуществах обследования. Письменное или устное согласие должно быть получено и зарегистрировано в карте пациента, в соответствии с законами штата и местными и больничными законами и инструкциями. Требования к проведению консультации и получению согласия не должны удержать от проведения обследования, если есть медицинские показания для его проведения; отказ пациента или опекуна дать согласие не освобождает врачей от их профессиональной и юридической ответственности, и иногда разрешение на проведение обследования должно быть получено другими средствами. Результаты обследования должны быть обсуждены лично с семьей, лицом, осуществляющим первичный уход за ребенком, и с самим ребенком, если он достаточно взрослый; если ребенок ВИЧ-положителен, нужно обеспечить соответствующую консультативную помощь и последующее наблюдение. Во всех случаях важно сохранять конфиденциальность.
О детях и подростках, отвечающих критериям СПИДа, нужно сообщить соответствующему отделу здравоохранения. Во многих штатах также необходимо сообщать обо всех случаях ВИЧ-инфицирования.
Другие методы исследования ВИЧ инфецирования
Инфицированным детям требуется определение количества лимфоцитов Т-хелпе-ров CD4+ и Т-супрессоров CD8+ и измерение концентрации вирусной РНК в плазме, чтобы определить стадию болезни и прогноз. Первые в пределах первых двух недель жизни, приблизительно в возрасте 1 месяц, и между 4-м и 6-м месяцами жизни. Положительный тест должен быть подтвержден немедленно с использованием того же или другого метода. Если все последовательные тесты определения ДНК ВИЧ методом ПЦР являются отрицательными, ребенок считается неинфицированным с более чем 95 % достоверностью. Последующие исследования для определения антител проводят, чтобы исключить ВИЧ-инфекцию и подтвердить серореверсию. Если у ребенка в возрасте до 18 месяцев с положительным результатом ИФА, но отрицательными результатами вирусологического исследования развивается СПИД-индикаторная болезнь, то у него диагностируют ВИЧ-инфекцию.
Недавно стали доступными экспресс-тесты для определения анти-ВИЧ антител, являющиеся производными метода ИФА, которые обеспечивают получение результатов в течение минут или часов. Они могут выполняться по экстренным показаниям в пробах слюны, цельной крови или сыворотки. В США эти тесты являются достоверно самыми полезными для скринингового обследования женщин с неизвестным ВИЧ-серостатусом во время родов, таким образом позволяя своевременно проконсультировать женщину, начать АРВ-терапию для предотвращения передачи ВИЧ-инфекции от матери ребенку и провести обследование новорожденного во время первого послеродового визита. Подобные преимущества отмечаются в других эпизодических ситуациях и в развивающихся странах. Экспресс-тесты требуют проведения подтверждающих реакций, например методом вестерн-блота. Если ожидаемая распространенность ВИЧ низкая, даже воначально количество CD4+ Т-лимфоци-тов может быть нормальным, но в конечном счете снизиться. Количество CD8+ Т-лимфоцитов обычно увеличивается в начале и не снижается до поздних стадий заболевания. Эти изменения в популяции Т-лимфоцитов приводят к снижению отношения CD4+: CD8+ клеток, характерному для ВИЧ-инфекции. Концентрация вирусной РНК в плазме у не получавших лечение детей младше 12 месяцев обычно очень высокая. К 24 месяцам концентрация вируса у не получавших лечение детей снижается. Хотя широкие границы колебаний концентрации РНК ВИЧ у детей делают прогностическую ценность ее определения в отношении заболеваемости и летальности более низкой, чем у взрослых, определение концентрации вирусной РНК в плазме в сочетании с определением количества CD4+ Т-лимфоцитов, тем не менее предоставляет более точную информацию о прогнозе, чем определение каждого из маркеров в отдельности. Менее дорогие альтернативные маркеры, такие как общее количество лимфоцитов и уровень альбуминов сыворотки крови, могут также позволять прогнозировать летальность от СПИДа у детей, что может применяться в развивающихся странах.
Хотя концентрация иммуноглобулинов в сыворотке крови не измеряется рутинно, она часто является заметно повышенной, особенно IgG и IgA, однако иногда у детей развивается пангипогаммаглобу-линемия. У пациентов может отмечаться анергия при проведении кожных проб.
При адекватном применении HAART-схем
При адекватном применении HAART-схем большинство перинатально инфицированных детей живут более 5 лет. Около 10—15 % детей в промышленных странах, не получавших лечение, умирают до 4 лет, большая часть их не доживает даже до 18 месяцев. В развивающихся странах смертность от СПИДа среди детей намного выше в первые несколько лет жизни.
Оппортунистические инфекции, особенно пневмоцистная пневмония, прогрессирующие неврологические нарушения, тяжелая дистрофия ассоцируются с неблагоприятным прогнозом; при пнев-моцистной пневмонии летальность составляет от 5 до 40 % у детей, получавших лечение, и практически 100 % у не получавших лечение детей. Также прогноз неблагоприятный у детей, у которых вирус обнаружили рано или при развитии клинических симптомов на первом году жизни. В то же время с появлением HAART и антимикробной профилактики заболеваний, вызванных Р. jiroveci, частота оппортунистических инфекций и злокачественных новобразований резко снизилась у детей, хорошо соблюдающих схемы лечения. При инфицировании ВИЧ в подростковом периоде у пациентов отмечается более медленное прогрессирование болезни, чем у взрослых.
Лечение ВИЧ инфекции у детей
Известно около двух дюжин АРВ препаратов, включая доступные в США комплексные препараты, содержащие несколько АРВ-средств, каждое из которых может вызывать побочные эффекты и взаимодействовать с другими АРВ-препаратами или распространенными антибиотиками, противосудорожными и седативными средствами. Разрабатываются новые АРВ-препараты, иммуно-модуляторы и вакцины.
Стандартное лечение проводят с применением HAART-схем, которые включают комбинации препаратов для максимизации вирусной супрессии и минимиза-цииселекциилекарственно-резистентных штаммов. Наиболее часто HAART состоит из «каркаса» из 2 нуклеозидных ингибиторов обратной транскриптазы, которые комбинируют с ингибитором протеазы или ненуклеозидным ингибитором обратной транскриптазы. Другие комбинации: Частые: около 98 % — локальные реакции в месте введения Редкие: реакции гиперчувствительности (3десь перечислены наиболее часто предлагаемые дозы и заметные побочные эффекты; возможны другие дозы, лекарственные взаимодействия и побочные эффекты. Дополнительная информация см.: Рабочая группа по антиретровирусной терапии и медикаментозному лечению ВИЧ-инфицированных детей, созданная при Национальном педиатрическом и семейном ВИЧ Ресурс-центре, Управлении ресурсами и службами здоровья и Национальном институте здоровья. Руководство по применению антиретровирусных агентов при ВИЧ-инфекции у детей. Доступны по адресу http://www.aidsinfo.nih.gov/.)
TDF функционально отнесен к группе NRTIs, однако по химической структуре является нуклео-тидным ингибитором обратной транскриптазы.
ZDV, ламивудин и абакавир; схемы с двумя ингибиторами протеазы; схемы с применением тенофовира) также используются, однако имеется мало данных, подтверждающих их эффективность как схем первой линии. Результаты монотерапии или терапии двумя нуклеозидными ингибиторами обратной транскриптазы неубедительны. Поскольку мнения экспертов о стратегиях лечения ВИЧ быстро меняются, настоятельно рекомендуется проконсультироваться со специалистом. Постоянно обновляющиеся практические руководства доступны на некоторых вебсайтах, наиболее полезные из них http://www.aidsinfo.nih.gov, http://www.hivguide-lines.org, www.unaids.org.
Терапия будет эффективна только в случае, если семья и ребенок способны соблюдать возможно сложные медикаментозные схемы. Несоблюдение схем лечения не только ведет к неудаче в контроле ВИЧ, но также к селекции лекарственно-резистентных штаммов ВИЧ, что суживает возможности медикаментозной терапии в будущем. Препятствия для соблюдения схем лечения следует выяснить до начала терапии. Они могут включать доступность и вкус таблеток и суспензий; лекарственные взаимодействия с текущей терапией; фармакокинетические факторы, такие как необходимость приема препаратов с пищей или натощак; факт зависимости ребенка в приеме лекарств от других лиц ; у подростков — отрицание болезни или страх, недоверие к медицинскому учреждению и недостаточная поддержка со стороны членов семьи.
Показания при ВИЧ инфекции
Начало АРВ-терапии зависит от вирусологических, иммунологических и клинических критериев; мнения специалистов в их отношении различаются. Целью является подавить репликацию ВИЧ и поддержать или достигнуть нормального количества и процентного содержания CD4+ лимфоцитов.
АРВ-терапия показана всем детям старше 12 месяцев с тяжелыми клиническими или иммунологическими проявлениями вне зависимости от вирусной нагрузки. О назначении терапии следует думать у детей старше 12 месяцев с легкими или умеренными проявлениями, а также при РНК ВИЧ вирусной нагрузке более 100 000 копий/мл. Некоторые эксперты используют более низкий предел этих показателей. Дети без клинических проявлений или иммуносупрессии могут находиться под наблюдением без АРВ-терапии, если РНК ВИЧ вирусная нагрузка у них менее 50 000—100 000 копий/мл.
Терапию следует начать у всех детей младше 12 месяцев при наличии у них клинических проявлений или иммуносупрессии вне зависимости от вирусной нагрузки. Многие специалисты лечат детей младше 12 месяцев при отсутствии проявлений, так как отмечается тенденция к быстрому прогрессированию ВИЧ-инфекции на первом году жизни.
Мониторинг. Клинический и лабораторный мониторинг крайне важен для выявления лекарственной токсичности и неэффективности терапии. Физикаль-ное обследование и мониторинг количества клеток крови, ВИЧ РНК вирусной нагрузки и субпопуляций лимфоцитов следует проводить через каждые 3—4 месяца; биохимический анализ крови, включая печеночные ферменты, липид-ный профиль и уровень амилазы и липазы следует контролировать как минимум 1 или 2 раза в год.
Вакцинация детей при ВИЧ-инфекции, проявляющейся клинически
В целом живые вирусные и бактериальные не должны применяться у детей со СПИДом или другими проявлениями ВИЧ, характеризующимися иммуносупрессией. Исключение составляет вакцина против кори-краснухи-эпи-демического паротита у пациентов, не находящихся в сильной иммуносупрессии ; эту прививку по возможности следует сделать в возрасте 12 месяцев для увеличения вероятности иммунного ответа, т.е. до того, как разовьется снижение иммунитета. Вторую дозу можно ввести уже через 4 недели, чтобы попытаться индуцировать сероконверсию как можно раньше. Если повышен риск контакта с корью, например во время вспышки, вакцинацию следует провести в более раннем возрасте, например в 6—9 месяцев.
Другие детские вакцины, например дифтерийный и столбнячный анатоксины, комбинированные с неклеточной коклюшной вакциной, против гепатита В, конъ-югированные вакцины Haemophylus influenzae тип b и Streptococcus pneumoniae и инактивированная полиомие-литная вакцина вводятся в обычные сроки согласно календарю прививок. Также рекомендуют проводить вакцинацию пневмококковой полисаха-ридной вакциной в 2 года и инактивиро-ванной вакциной против гриппа ежегодно начиная с 6 месяцев.
Так как у детей с клинически проявляющейся ВИЧ-инфекцией обычно отмечается низкий иммунный ответ на вакцинацию, если они контактируют с заболеванием, против которого проводится вакцинация, они должны считаться восприимчивыми к нему, несмотря на вакцинацию. Поэтому при наличии показаний им следует проводить пассивную иммунизацию иммуноглобулином. Иммуноглобулин также необходимо ввести любому неиммунизированному члену семьи, контактному по кори.
Вакцинация у детей с асимптомати-ческой ВИЧ-инфекцией
Таких детей следует вакцинировать АКДС, ИПВ, конъ-югированными вакцинами Н. influenzae тип b и S. pneumoniae, ВГВ и против кори-краснухи-эпидемического паротита согласно общему календарю прививок. Хотя оральная полиомиелитная вакцина не вызывала неблагоприятных эффектов у подобных больных, живые полиовирусы могут выделяться в окружающую среду и передаваться иммуносупрессирован-ным контактным лицам, создавая повышенный риск развития полиомиелита, вызванного вакцинным штаммом.
Вакцинация против ветряной оспы безопасна и рекомендована для пациентов с ранними стадиями ВИЧ-инфекции. Так как ВИЧ-инфицированные дети 2 лет и старше подвержены повышенному риску инвазивной пневмококковой инфекции, они должны быть привиты полисахаридной пневмококковой вакциной в возрасте 2 лет. Рекомендуется также провести ревакцинацию по достижении возраста 3—5 лет. Ежегодно ВИЧ-инфицированных детей старше 6 месяцев следует вакцинировать инакти-вированной вакциной против гриппа.
В США и регионах с низкой заболеваемостью ТБ вакцинация БЦЖ не рекомендуется. Тем не менее в развивающихся странах, где заболеваемость ТБ высокая, ВОЗ рекомендует вакцинировать БЦЖ всех новорожденных без клинических проявлений вне зависимости от ВИЧ-инфицирования матери. Сообщалось о нескольких случаях диссеминированной БЦЖ инфекции у пациентов с тяжелым иммунодефицитом при СПИДе.
Желательно проводить пассивную иммунизацию при контакте с корью, столбняком и ветряной оспой.
Вакцинация серонегативных детей, проживающих вместе с пациентами с клинически проявляющейся ВИЧ-инфекцией
Таких детей, как и серопози-тивных, следует вакцинировать ИПВ, а не ОПВ. Вакцинация против кори-краснухи-эпидемического паротита может проводиться, так как эти вакцинные вирусы не передаются и не вызывают заболевание. Для снижения риска развития гриппа у пациентов с клинически проявляющейся ВИЧ-инфекцией ежегодная вакцинация против гриппа показана всем членам семьи, контактирующим с пациентом.
Вакцинация против ветряной оспы се-ронегативных сибсов и восприимчивых взрослых лиц, ухаживающих за ВИЧ-инфицированным ребенком, всячески поддерживается для предотвращения заражения диким вирусом ветряной оспы, который может вызвать тяжелое заболевание у пациентов с иммунодефицитом; в то же время передача вакцинного вируса ветряной оспы от человека к человеку отмечается редко.
Профилактика ВИЧ инфекции
Адекватная АРВ-терапия направлена на попытки оптимизации здоровья матери, прерывание передачи ВИЧ-инфекции от матери к ребенку и минимизацию токсического воздействия лекарств на плод. В США и других странах, где АРВ-препараты доступны и существует инфраструктура для проведения диагностики ВИЧ, лечение АРВ-препаратами является стандартом у всех ВИЧ-инфицированных беременныхженщин. У ВИЧ-инфицированных женщин, ранее не получавших лечение АРВ-препаратами, не отвечающих критериям для назначения HAART, назначают ZDV внутрь по 300 мг 2 раза в день, начиная с 14—34-й недели гестации, и продолжают в течение всей беременности, а также вводят ZDV внутривенно во время родов в дозе 2 мг/кг в первый час, а затем по 1 мг/ до рождения ребенка. ZDV по 2 мг/кг внутрь 4 раза в день назначается новорожденному в первые 6 недель жизни. Женщинам, которым по клиническим или иммунологическим показателям еще не показано начинать HAART, тем не менее рекомендуют это сделать, если вирусная нагрузка более 1000 копий/мл. Сразу после родов решают, следует ли продолжать терапию матери. Женщины, чей клинический или иммунологический статус удовлетворяет критериям для начала лечения, должны получать комбинированные режимы с использованием нескольких препаратов, предпочтительно включающих ZDV.
Беременность не является противопоказанием для HAART, схем, хотя беременная женщина и ее врач должны обсудить возможные положительные стороны и риск при проведении подобной терапии, а также отсутствие окончательных данных о ее безопасности. Терапия ZDV снижает вероятность инфицирования ребенка от матери с 25 до 8 %; многие комбинации АРВ также эффективны. В США при современных схемах HAART частота передачи ВИЧ от матери к ребенку составляет менее 2 %. Таким образом, хотя конечное решение о приеме АРВ-терапии остается за беременной женщиной, следует акцентировать, что доказанные положительные эффекты терапии перевешивают теоретический риск токсичности для плода.
Большинство экспертов считают, что ВИЧ-инфицированная женщина, уже принимающая АРВ-терапию к моменту наступления беременности, должна продолжать эту терапию, даже во время 1 -го триместра; альтернативное мнение заключается в том, что терапию следует отменить до начала 2-го триместра, затем ее следует возобновить.
Для снижения заражения ребенка от ВИЧ-инфицированной матери, у которой началась родовая деятельность и которая ранее не получала терапию, врачи использовали сочетание комбинированной АРВ-терапии и кесарева сечения. Экспресс-диагностика у беременной женщины с начавшейся родовой деятельностью и отсутствием сведений о ВИЧ-серостатусе может позволить срочно принять соответствующие меры. В таких ситуациях следует экстренно проконсультироваться со специалистом по ВИЧ-инфекции у детей и матерей.
ВИЧ-инфицированной женщине не рекомендуется вскармливание грудью или донорство грудного молока в странах, где безопасны и доступны альтернативные продукты вскармливания. В то же время в странах, где инфекционные заболевания и пониженное питание являются важными причинами ранней детской смертности, а безопасные и доступные искусственные смеси отсутствуют, защита от риска смертельного исхода при инфекции онных заболеваниях органов дыхания и ЖКТ, которую оказывает грудное вскармливание, может уравновесить риск ВИЧ-инфицирования. В этих развивающихся странах ВОЗ рекомендует матерям продолжать кормление грудью.
Профилактика инфицирования в подростковом возрасте
Так как подростки особенно подвержены риску ВИЧ-инфицирования, они должны иметь информацию, возможность пройти обследование и узнать свой серостатус. Подросткам следует рассказать, как передается ВИЧ-инфекция, что это такое, как от нее защититься, включая воздержание от образа жизни, представляющего высокий риск инфицирования, и пропаганду безопасного секса для сексуально активных подростков.
Усилия следует сконцентрировать на подростках, подверженных высокому риску ВИЧ-инфицирования. Согласие пациента обязательно для проведения обследования и раскрытия информации о его серостатусе. Решение о том, сообщать ли о ВИЧ- статусе сексуальному партнеру ВИЧ-инфицированного пациента без его согласия, должно базироваться на вероятности риска для партнера, наличии у него причин предполагать риск и принимать меры предосторожности, наличии законодательно установленных требований о сохранении или раскрытии подобной информации и возможном воздействии на дальнейшие взаимоотношения этой информации.
Профилактика оппортунистических инфекций
Профилактика пневмоцист-ной пневмонии показана ВИЧ-инфицированным детям с выраженным иммунодефицитом. В целом химиопрофилактика продолжается в течение всей жизни, хотя в конце подросткового периода и детям на HAART-схемах лечения с улучшением иммунного статуса можно отменить профилактику, пока иммунологическая категория остается 1 или 2. В настоящее время пожизненная химиопрофилактика вне зависимости от количества CD4+ рекомендована тем, кто перенес эпизод пневмоцистной пневмонии. Профилактика пневмоцистной пневмонии также показана всем новорожденным от ВИЧ-инфицированных матерей начиная с 4—6-й недель жизни. Профилактику можно прекратить при достоверном исключении ВИЧ при последовательных обследованиях методом ПЦР или вирусологическим методом. Препаратом выбора является триметоприм-сульфа-метоксазол по 75 мгТМП/375 мг СМК/м2 внутрь 2 раза в день 3 дня подряд в неделю ; альтернативные схемы используют ту же общую дозу один раз в день 3 дня в неделю или 2 раза в день каждый день недели, или через день. Пациентам 5 лет и старше, которые не переносят ТМП-СМК, можно назначить пентамидин в аэрозоле один раз в месяц. Внутривенные формы пентами-дина также применялись, однако оказались менее эффективными и потенциально более токсичными. Другой альтернативой, особенно у детей младше 5 лет, является дапзон внутрь один раз в день. Другие препараты, которые могут быть эффективны, включают пириметамин с дапзо-ном, пириметамин-сульфадоксин и пер-оральный атоваквон. В то же время опыт применения этих препаратов очень ограничен, и о них следует думать только втом случае, если рекомендованные схемы ребенок не переносит или они не могут быть использованы.
Для профилактики инфекций, вызванных Mycobacterium avium, у детей 6 лет и старше с числом CD4+ лимфоцитов менее 50/мкл препаратами выбора являются азитромицин один раз в неделю или кларитромицин ежедневно, а также ежедневно рифабутин в качестве альтернативы. По профилактике других оппортунистических инфекций, таких как цитомегаловирусная инфекция, грибковые заболевания, токсоплазменный энцефалит, данные ограниченны. otvetkak.ru |
г.Самара, ул. Димитрова 131 [email protected] |
 |