Содержание
История вакцинопрофилактики. Для любознательных. Инфекционные заболевания. Специалисты о прививках
Главное о вакцинации
Учение об инфекционных болезнях уходит вглубь веков
Гиппократ
460-370 д. н. э
Древнегреческий целитель, врач и философ. Выделил медицину в отдельную науку, отделив её от религии.
Основоположником науки эпидемиологии считается Гиппократ. Учил, что заболевание является не наказанием богов, а последствием природных факторов, нарушения питания, привычек и характера жизни человека. До наших дней дошли сочинения Гиппократа «Семь книг об эпидемиях», «О воздухе, водах и местностях» и др.
Гиппократ
460-370 д. н. э
Древнегреческий целитель, врач и философ. Выделил медицину в отдельную науку, отделив её от религии.
1546
Джироламо Фракасторо
1478-1553
Врач, писатель и учёный-исследователь. В 1546 году ввёл в медицину термин «инфекция».
Итальянский врач и астроном Д. Фракасторо разработал учение о контагии — живом, размножающемся начале, способном вызвать болезнь, описал симптомы многих инфекционных заболеваний (оспа, корь, чума, чахотка, бешенство, проказа, сыпной тиф и др. ), был убеждён в специфичности контагий, в том, что они выделяются больным организмом. Он опубликовал книгу «De Contagione et Contagiosis Morbis», в которой сформулировал положение о заразности больного для других — это была важнейшая веха в понимании сути эпидемий.
), был убеждён в специфичности контагий, в том, что они выделяются больным организмом. Он опубликовал книгу «De Contagione et Contagiosis Morbis», в которой сформулировал положение о заразности больного для других — это была важнейшая веха в понимании сути эпидемий.
Джироламо Фракасторо
1478-1553
Врач, писатель и учёный-исследователь. В 1546 году ввёл в медицину термин «инфекция».
XVIII век
Антоний ван Левенгук
1632-1723
Натуралист, конструктор микроскопов, основоположник научной микроскопии.
Даниил Самойлович
1724-1805
Медик, основатель эпидемиологии в Российской империи и первого на Украине научного медицинского товарищества. Член Парижской, Марсельской, Тулузской, Дижонской, Мангеймской, Туринской, Падуанской и других (в целом 13-ти) хирургических академий, а также Российской медицинской коллегии.
Последовательным сторонником этой гипотезы был основоположник отечественной эпидемиологии Д.С. Самойлович. Наблюдая за чумой, он пришел к выводу, что после перенесения чумы к ней остается иммунитет. Одна из главных научных заслуг Д.С. Самойловича — идея о возможности создания искусственного иммунитета против чумы с помощью прививок.
Наблюдая за чумой, он пришел к выводу, что после перенесения чумы к ней остается иммунитет. Одна из главных научных заслуг Д.С. Самойловича — идея о возможности создания искусственного иммунитета против чумы с помощью прививок.
Первым увидел и описал микроорганизмы голландский натуралист Антоний ван Левенгук, который сконструировал микроскоп, дававший увеличение до 300 раз. Он установил шаровидные, палочковидные и извитые формы микробов.
Антоний ван Левенгук
1632-1723
Натуралист, конструктор микроскопов, основоположник научной микроскопии.
Даниил Самойлович
1724-1805
Медик, основатель эпидемиологии в Российской империи и первого на Украине научного медицинского товарищества. Член Парижской, Марсельской, Тулузской, Дижонской, Мангеймской, Туринской, Падуанской и других (в целом 13-ти) хирургических академий, а также Российской медицинской коллегии.
1796
Эдвард Дженнер
1749-1823
Врач, разработал способ вакцинации против натуральной оспы.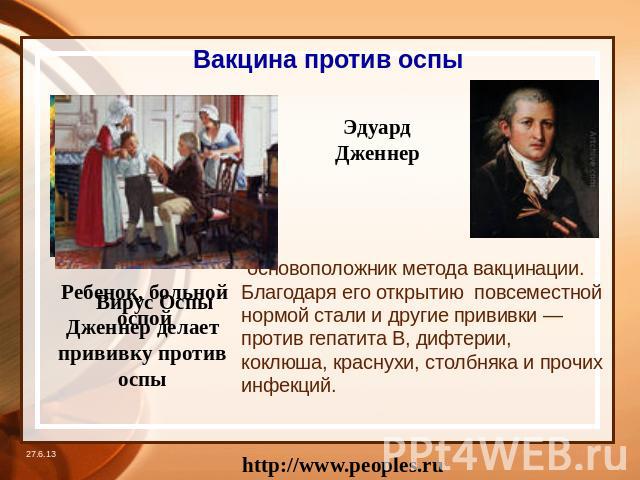 Член Лондонского королевского общества, иностранный член Парижской академии наук.
Член Лондонского королевского общества, иностранный член Парижской академии наук.
Перелом в истории вакцинации связан с именем английского врача Э. Дженнера. Он обратил внимание, что фермеры, работающие с коровами, инфицированными коровьей оспой, не болеют натуральной оспой и предположил, что перенесенная коровья оспа является защитой от человеческой. 14 мая 1796 года врач решился на революционный по тем временам эксперимент — привил коровью оспу мальчику и доказал, что тот стал невосприимчивым к натуральной оспе — все последующие попытки заразить мальчика человеческой оспой были безуспешными. В 1798 году Дженнер издал брошюру с подробным описанием своего исследования, и этот труд стал первым опубликованным отчетом о вакцинации, сделавшим эту практику известной во всём мире.
Эдвард Дженнер
1749-1823
Врач, разработал способ вакцинации против натуральной оспы. Член Лондонского королевского общества, иностранный член Парижской академии наук.
1880-1885
Луи Пастер
1822-1895
Химик и микробиолог. Основоположник микробиологии, создатель научных основ вакцинации. Член Французской академии.
Основоположник микробиологии, создатель научных основ вакцинации. Член Французской академии.
Французский ученый Луи Пастер первым доказал, что болезни, которые мы сегодня называем инфекционными, могут возникать только в результате проникновения в организм микробов из внешней среды. В 1880 году он нашел способ предохранения от заразных заболеваний введением ослабленных возбудителей, который оказался применим ко многим инфекционным болезням. В октябре 1885 года сделаны первые успешные прививки от бешенства людям (в течение года было вакцинировано около 2500 человек из 18 стран).
Луи Пастер
1822-1895
Химик и микробиолог. Основоположник микробиологии, создатель научных основ вакцинации. Член Французской академии.
1882
Роберт Кох
1843-1910
Врач, микробиолог и гигиенист. Лауреат Нобелевской премии по физиологии и медицине. Член Прусской академии наук, иностранный член Лондонского королевского общества, Парижской академии наук, иностранный член-корреспондент Петербургской академии наук.
24 марта 1882 года Роберт Кох объявил о том, что сумел выделить бактерию, вызывающую туберкулёз. Одним из следствий этого открытия было подтверждение факта, что туберкулёз — одно единое заболевание (ранее рассматривали множество форм туберкулёза — туберкулёз лёгких, туберкулёз кожи, костей, кишечника, мочеполовой системы и туберкулёзный менингит — все они считались самостоятельными заболеваниями с собственными названиями). В качестве метода распространения и передачи Кох предположил воздушно-капельный путь — в мокроте больного при кашле он также обнаружил патоген — что показало опасность пациентов с открытой формой туберкулёза.
Кроме этого, Кох открыл бациллу сибирской язвы, холерный вибрион.
В 1905 году за «исследования и открытия, касающиеся лечения туберкулеза» ученый был удостоен Нобелевской премии по физиологии и медицине.
Роберт Кох
1843-1910
Врач, микробиолог и гигиенист. Лауреат Нобелевской премии по физиологии и медицине. Член Прусской академии наук, иностранный член Лондонского королевского общества, Парижской академии наук, иностранный член-корреспондент Петербургской академии наук.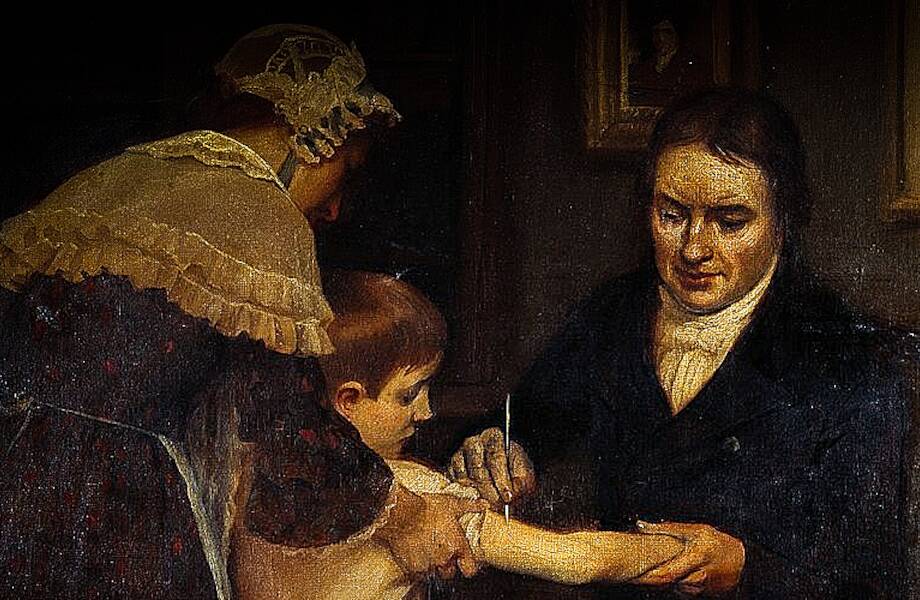
1884
Фридрих Лёффлер
1852-1915
Бактериолог и гигиенист. Один из основоположников медицинской микробиологии.
Пьер Эмиль Ру
1853-1933
Бактериолог. Член Парижской академии наук, иностранный член Лондонского королевского общества, иностранный почётный член Российской академии наук.
Немецкий бактериолог Фридрих Лёффлер сумел выделить в чистом виде бактерию дифтерии — палочки Corynebacterium diphtheriae — и смог культивировать ее для дальнейших исследований. А ученик Пастера Пьер Эмиль Ру показал, как действуют палочки дифтерии и доказал, что все общие явления дифтерии — упадок сердечной деятельности, параличи и прочие смертельные последствия — вызваны не самой бактерией, а вырабатываемым ею ядовитым веществом (токсином), и что вещество это, введённое в организм, вызывает эти явления само по себе, при полном отсутствии в организме дифтерийных микробов.
Фридрих Лёффлер
1852-1915
Бактериолог и гигиенист. Один из основоположников медицинской микробиологии.
Пьер Эмиль Ру
1853-1933
Бактериолог. Член Парижской академии наук, иностранный член Лондонского королевского общества, иностранный почётный член Российской академии наук.
1883-1887
Нестор Монастырский
1847-1888
Врач, первый заведующий хирургической клиники Императорского клинического института.
Артур Николайер
1862-1942
Терапевт. Старший врач университетской больницы Геттингена. Экстраординарный профессор внутренней медицины в Шарите. Отстранен от должности в 1933 году, после принятия нацистами антиеврейских законов. Покончил с собой перед отправкой в гетто.
Сибасабуро Китасато
1853-1931
Врач и бактериолог. Член Японской академии наук, иностранный член Лондонского королевского общества, первый президент медицинской ассоциации Японии.
Научное изучение столбняка началось во второй половине XIX века.
Возбудитель столбняка был открыт почти одновременно русским хирургом Н. Д. Монастырским (в 1883 году) и немецким ученым А. Николайером (в 1884 году).
Николайером (в 1884 году).
Чистую культуру микроорганизма выделил в 1887 г. японский микробиолог С. Китазато, он же в 1890 г. получил столбнячный токсин и (совместно с немецким бактериологом Э. Берингом) создал первую противостолбнячную сыворотку.
В 1923 году французский иммунолог Гастон Рамон получил столбнячный анатоксин, который стал применяться для профилактики заболевания.
Нестор Монастырский
1847-1888
Врач, первый заведующий хирургической клиники Императорского клинического института.
Артур Николайер
1862-1942
Терапевт. Старший врач университетской больницы Геттингена. Экстраординарный профессор внутренней медицины в Шарите. Отстранен от должности в 1933 году, после принятия нацистами антиеврейских законов. Покончил с собой перед отправкой в гетто.
Сибасабуро Китасато
1853-1931
Врач и бактериолог. Член Японской академии наук, иностранный член Лондонского королевского общества, первый президент медицинской ассоциации Японии.
1891 -1894
Эмиль фон Беринг
1854-1917
Врач, бактериолог, иммунолог, серолог. Лауреат Нобелевской премии по физиологии и медицине. Кавалер ордена Почётного легиона.
Гастон Рамон
1854-1917
Ветеринар и биолог. Член Французской академии наук.
26 декабря 1891 года Эмиль фон Беринг спас жизнь больному ребенку, сделав ему первую прививку от дифтерии. До начала XX века дифтерия ежегодно уносила тысячи детских жизней, а медицина была бессильна облегчить их страдания и спасти от тяжелой агонии.
В 1894 году усовершенствованная сыворотка против дифтерии была успешно опробована на 220 больных детях. За спасение детей Берингу в 1901 году была присуждена первая Нобелевская премия по физиологии и медицине.
Профилактическая сыворотка, которая употребляется теперь против дифтерии, была найдена доктором Гастоном Рамоном, работником Пастеровского института в Париже, много лет спустя после открытий Лефлера, Ру и Беринга.
Эмиль фон Беринг
1854-1917
Врач, бактериолог, иммунолог, серолог. Лауреат Нобелевской премии по физиологии и медицине. Кавалер ордена Почётного легиона.
Лауреат Нобелевской премии по физиологии и медицине. Кавалер ордена Почётного легиона.
Гастон Рамон
1854-1917
Ветеринар и биолог. Член Французской академии наук.
конец XIX века
Пауль Эрлих
1854-1915
Врач, иммунолог, бактериолог, химик, основоположник химиотерапии. Лауреат Нобелевской премии.
В конце XIX в. немецкий ученый Пауль Эрлих положил начало учению об антителах как факторах гуморального иммунитета (с помощью белков-антигенов). Также было установлено, что иммунитет определяется как клеточными, так и гуморальными факторами. П. Эрлих в 1908 г. был удостоен Нобелевской премии по физиологии за создание клеточной теории иммунитета, которую он разделил с Ильей Мечниковым.
Пауль Эрлих
1854-1915
Врач, иммунолог, бактериолог, химик, основоположник химиотерапии. Лауреат Нобелевской премии.
1892
Дмитрий Ивановский
1864-1920
Физиолог растений и микробиолог, основоположник вирусологии.
1892 год считается годом открытия новых организмов — вирусов. Впервые существование вируса (как нового типа возбудителя болезней) доказал русский учёный Дмитрий Иосифович Ивановский. Исследования Ивановского подхватили ученые во всем мире.
Впервые существование вируса (как нового типа возбудителя болезней) доказал русский учёный Дмитрий Иосифович Ивановский. Исследования Ивановского подхватили ученые во всем мире.
Дмитрий Ивановский
1864-1920
Физиолог растений и микробиолог, основоположник вирусологии.
1921
Альбер Кальметт
1863-1933
Врач, бактериолог и иммунолог. Член Парижской медицинской академии, Парижской академии наук, иностранный член Лондонского королевского общества.
Камиль Герен
1872-1961
Учёный, ветеринарный врач, бактериолог и иммунолог. Президент ветеринарной академии Франции, президент медицинской Академии Франции
1921 год ознаменовался изобретением живой бактериальной вакцины против туберкулеза (БЦЖ) французскими учеными-микробиологами Альбером Кальметтом и ветеринаром Камилем Гереном (BCG — Bacillebilie’ Calmette-Gue’rin).
Первоначально, их работа охватывала получение культур туберкулёзной палочки и исследования различных питательных сред. При этом они выяснили, что на питательной среде на основе глицерина, желчи и картофеля вырастают туберкулёзные палочки наименьшей вирулентности. С этого момента они изменили ход исследования, чтобы выяснить, нельзя ли посредством повторяющегося культивирования вырастить ослабленный штамм для производства вакцины.
При этом они выяснили, что на питательной среде на основе глицерина, желчи и картофеля вырастают туберкулёзные палочки наименьшей вирулентности. С этого момента они изменили ход исследования, чтобы выяснить, нельзя ли посредством повторяющегося культивирования вырастить ослабленный штамм для производства вакцины.
Исследования продлились до 1919 года, когда вакцина с невирулентными бактериями не вызвала туберкулёз у подопытных животных.
Вакцина БЦЖ выдержала испытание временем, ее эффективность проверена и доказана практикой. В наши дни вакцина БЦЖ является основным препаратом для специфической профилактики туберкулеза, признанным и используемым во всем мире.
Альбер Кальметт
1863-1933
Врач, бактериолог и иммунолог. Член Парижской медицинской академии, Парижской академии наук, иностранный член Лондонского королевского общества.
Камиль Герен
1872-1961
Учёный, ветеринарный врач, бактериолог и иммунолог. Президент ветеринарной академии Франции, президент медицинской Академии Франции
1955
Джонас Солк
1914-1995
Вирусолог. Основатель института биологических исследований Солка.
Основатель института биологических исследований Солка.
Альберт Сейбин
1906-1993
Вирусолог. Член Национальной академии наук США.
12 апреля 1955 г. в США успешно завершилось крупномасштабное исследование, подтвердившее эффективность вакцины Джонаса Солка — первой вакцины против полиомиелита. Результаты пятилетнего, с 1956 по 1961 год, массового применения вакцины превзошли все ожидания: среди детей в возрастных группах, особенно подверженных инфекции, заболеваемость снизилась на 96%. Позже вакцина Солка была заменена на более совершенную, разработанную Альбертом Сэйбином.
Солк и Сэйбин не стали патентовать свои вакцины. Когда Солка спросили, кому принадлежит патент на средство, он ответил: «Патента нет. Разве вы могли бы запатентовать солнце?»
Джонас Солк
1914-1995
Вирусолог. Основатель института биологических исследований Солка.
Альберт Сейбин
1906-1993
Вирусолог. Член Национальной академии наук США.
Из истории отечественной науки
Илья Мечников
1845-1916
Биолог (микробиолог, цитолог, эмбриолог, иммунолог, физиолог и патолог). Один из основоположников эволюционной эмбриологии, первооткрыватель фагоцитоза и внутриклеточного пищеварения, создатель сравнительной патологии воспаления, фагоцитарной теории иммунитета, теории фагоцителлы. Лауреат Нобелевской премии по физиологии и медицине.
Один из основоположников эволюционной эмбриологии, первооткрыватель фагоцитоза и внутриклеточного пищеварения, создатель сравнительной патологии воспаления, фагоцитарной теории иммунитета, теории фагоцителлы. Лауреат Нобелевской премии по физиологии и медицине.
Николай Гамалея
1859-1949
Врач, микробиолог и эпидемиолог. Основатель первой в России бактериологической станции. Внедрил термин «дезинсекция», который положил в основу метода борьбы с сыпным тифом, предположив, что методом передачи тифа служат платяные вши. Почётный член АН СССР, академик АМН СССР. Лауреат Сталинской премии.
Павел Здродовский
1890-1976
Микробиолог и иммунолог. Организовал Институт микробиологии и гигиены. Руководил разработками методов вакцинации против столбняка, дифтерии и других инфекций. Академик АМН СССР. Герой Социалистического Труда. Лауреат Ленинской премии.
Виктор Жданов
1914-1987
Вирусолог, эпидемиолог и организатор здравоохранения. Возглавлял санитарно-эпидемиологическую службу СССР. Директор Института вирусологии им. Д. И. Ивановского. Один из авторов Программы глобальной ликвидации оспы. Академик АМН СССР.
Директор Института вирусологии им. Д. И. Ивановского. Один из авторов Программы глобальной ликвидации оспы. Академик АМН СССР.
Анатолий Смородинцев
1901-1986
Бактериолог, вирусолог, иммунолог. Основатель и первый директор НИИ гриппа. Разработал и внедрил живую вакцину против полиомиелита. Создал вакцины против гриппа, клещевого энцефалита, кори, эпидемического паротита. Академик АМН СССР. Лауреат Сталинской премии. Лауреат Ленинской премии.
Лев Зильбер
1884-1966
Иммунолог и вирусолог, создатель советской школы медицинской вирусологии. Выделил вирус клещевого энцефалита. Трижды арестовывался, в заключении получил дрожжевой препарат против пеллагры. Академик АМН СССР. Лауреат Сталинской премии. Лауреат Государственной премия СССР (посмертно).
Михаил Чумаков
1909-1993
Вирусолог. Организовал массовое производство, провёл клинические испытания и внедрил вакцину против полиомиелита. Основатель и первый директор Института полиомиелита и вирусных энцефалитов РАМН. Академик АМН СССР. Герой Социалистического Труда. Лауреат Сталинской премии. Лауреат Ленинской премии.
Академик АМН СССР. Герой Социалистического Труда. Лауреат Сталинской премии. Лауреат Ленинской премии.
Зинаида Ермольева
1898-1974
Микробиолог и эпидемиолог. Разработала высокоэффективные бактериофаги для диагностики и лечения холеры, брюшного тифа, дифтерии. Создательница отечественных антибиотиков. Директор Института биологической профилактики инфекций. Академик АМН СССР. Лауреат Сталинской премии.
1981-1982
В 1981-82 гг. стала доступной первая вакцина против гепатита В. Сначала в Китае, а затем в США. Пик её применения пришёлся на 1982-88 гг. С 1987 г. на смену плазменной вакцине пришло следующее поколение вакцины против вируса гепатита В, в которой использована технология генной модификации рекомбинантной ДНК в клетках дрожжевого микроорганизма. Её иногда называют генно-инженерной вакциной.
1983
Харальд цур Хаузен
род 1936
Медик и учёный, лауреат Нобелевской премии по физиологии или медицине.
В 1983 году Харальд цур Хаузен обнаружил ДНК папилломавируса в биопсии рака шейки матки, и это событие можно считать открытием онкогенного вируса ВПЧ-16. Исследования Харальда цур Хаузена в области ВПЧ-инфекции легли в основу понимания механизмов канцерогенеза, индуцированного вирусом папилломы. Впоследствии были разработаны вакцины, которые позволяют предотвратить инфекцию вирусами ВПЧ-16 и ВПЧ-18.
Исследования Харальда цур Хаузена в области ВПЧ-инфекции легли в основу понимания механизмов канцерогенеза, индуцированного вирусом папилломы. Впоследствии были разработаны вакцины, которые позволяют предотвратить инфекцию вирусами ВПЧ-16 и ВПЧ-18.
Харальд цур Хаузен
род 1936
Медик и учёный, лауреат Нобелевской премии по физиологии или медицине.
Развитие вакцинопрофилактики | ГОБУЗ «Кольская ЦРБ»
24 марта 1882 года, когда Роберт Кох объявил о том, что сумел выделить бактерию, вызывающую туберкулёз, ученый достиг величайшего за всю свою жизнь триумфа.
Почему все же именно открытие возбудителя туберкулеза называют научным подвигом?
Дело в том, что возбудители болезни туберкулеза – чрезвычайно трудный объект для исследования. В первых препаратах для микроскопии, сделанных Кохом из легочной ткани молодого рабочего, умершего от скоротечной чахотки, ни одного микроба обнаружить не удалось. Не теряя надежды, ученый провел окраску препаратов по собственной методике и впервые под микроскопом увидел неуловимого возбудителя туберкулеза.
На следующем этапе необходимо было получить пресловутые микробактерии в чистой культуре. Еще несколько лет назад Кох нашел способ культивирования микробов не только на подопытных животных, но и в искусственной среде, например, на разрезе сваренного картофеля или в мясном бульоне. Он попытался таким же способом культивировать и бактерии туберкулеза, но они не развивались. Однако когда Кох впрыснул содержимое раздавленного узелка под кожу морской свинки, та погибла в течение нескольких недель, а в ее органах ученый нашел огромное количество палочек. Кох пришел к выводу, что бактерии туберкулеза могут развиваться только в живом организме.
Желая создать питательную среду, подобную живым тканям, Кох решил применить сыворотку животной крови, которую ему удалось раздобыть на бойне. И действительно, в этой среде бактерии быстро размножались. Полученными таким образом чистыми культурами бактерий Кох заразил несколько сотен подопытных животных разных видов, и все они заболели туберкулезом. Ученому было ясно, что возбудитель заболевания найден. В это время мир был возбужден открытым Пастером методом предупреждения заразных болезней с помощью прививок ослабленных культур бактерий, вызывающих данную болезнь. Поэтому Кох считал, что ему удастся тем же способом спасти человечество от туберкулеза.
Ученому было ясно, что возбудитель заболевания найден. В это время мир был возбужден открытым Пастером методом предупреждения заразных болезней с помощью прививок ослабленных культур бактерий, вызывающих данную болезнь. Поэтому Кох считал, что ему удастся тем же способом спасти человечество от туберкулеза.
Он приготовил вакцину из ослабленных бактерий туберкулеза, но предупредить заболевание с помощью этой вакцины ему не удалось. Вакцина эта под названием «туберкулина» до сих пор применяется как вспомогательное средство при диагностике туберкулеза. Кроме этого, Кох открыл бациллу сибирской язвы, холерный вибрион. В 1905 году за «исследования и открытия, касающиеся лечения туберкулеза» ученый был удостоен Нобелевской премии по физиологии и медицине.
26 декабря 1891 года Эмиль фон Беринг спас жизнь больному ребенку, сделав ему первую прививку от дифтерии.
До начала XX века дифтерия ежегодно уносила тысячи детских жизней, а медицина была бессильна облегчить их страдания и спасти от тяжелой агонии.
Немецкий бактериолог Фридрих Лёффлер в 1884 году сумел открыть бактерии, вызывающие дифтерию — палочки Corynebacterium diphtheriae. А ученик Пастера Пьер Эмиль Ру показал, как действуют палочки дифтерии и доказал, что все общие явления дифтерии — упадок сердечной деятельности, параличи и прочие смертельные последствия – вызваны не самой бактерией, а вырабатываемым ею ядовитым веществом (токсином), и что вещество это, введенное в организм, вызывает эти явления само по себе, при полном отсутствии в организме дифтерийных микробов.
Но Ру не умел обезвредить яд и не мог найти способ спасения больных детей. В этом ему помог ассистент Коха Беринг. В поисках средства, которое убивало бы бактерии дифтерии, Беринг делал прививки зараженным животным из разных веществ, но животные погибали. Однажды для прививки он использовал трихлорид йода. Правда, и на этот раз морские свинки тяжело заболели, но ни одна из них не погибла.
Воодушевленный первой удачей, Беринг, дождавшись выздоровления подопытных свинок, сделал им прививку, содержавшую дифтерийный токсин. Животные превосходно выдержали прививку, несмотря на то, что получили огромную дозу токсина. Затем ученый выяснил, что если сыворотку крови перенесших дифтерию и выздоровевших морских свинок ввести заболевшим животным, те выздоравливают. Значит, в крови переболевших появляется какой-то антитоксин, который нейтрализует токсин дифтерийной палочки.
Животные превосходно выдержали прививку, несмотря на то, что получили огромную дозу токсина. Затем ученый выяснил, что если сыворотку крови перенесших дифтерию и выздоровевших морских свинок ввести заболевшим животным, те выздоравливают. Значит, в крови переболевших появляется какой-то антитоксин, который нейтрализует токсин дифтерийной палочки.
В конце 1891 года в клинике детских болезней в Берлине, переполненной детьми, умирающими от дифтерии, была сделана прививка с антитоксином – и ребенок выздоровел. Эффект опыта был впечатляющим, многие дети были спасены, но все же успех был лишь частичным, и сыворотка Беринга не стала надежным средством, спасавшим всех детей. И тут Берингу помог его коллега и друг Пауль Эрлих – будущий изобретатель «препарата 606» (сальварсана) и победитель сифилиса. А тогда он сумел наладить масштабное производство сыворотки, рассчитать правильные дозировки антитоксина и повысить эффективность вакцины.
В 1894 году усовершенствованная сыворотка была успешно опробована на 220 больных детях. За спасение детей Берингу в 1901 году была присуждена первая Нобелевская премия по физиологии и медицине «за работу по сывороточной терапии, главным образом, за её применение при лечении дифтерии, что открыло новые пути в медицинской науке и дало в руки врачам победоносное оружие против болезни и смерти».
За спасение детей Берингу в 1901 году была присуждена первая Нобелевская премия по физиологии и медицине «за работу по сывороточной терапии, главным образом, за её применение при лечении дифтерии, что открыло новые пути в медицинской науке и дало в руки врачам победоносное оружие против болезни и смерти».
Уже позже, в 1913 году, Беринг предложил введение смеси токсина и антитоксина для выработки у детей активного иммунитета. И это оказалось наиболее действенным средством защиты (пассивный иммунитет, возникающий после введения одного только антитоксина, недолговечен). Профилактическая сыворотка, которая употребляется теперь против дифтерии, была найдена доктором Гастоном Рамоном, работником Пастеровского института в Париже, много лет спустя после открытия Лефлера, Ру и Беринга.
В конце XIX в. немецкий ученый Пауль Эрлих (1854-1915) положил начало учению об антителах как факторах гуморального иммунитета. Бурная полемика и многочисленные исследования, предпринятые после этого открытия, привели к весьма плодотворным результатам: было установлено, что иммунитет определяется как клеточными, так и гуморальными факторами.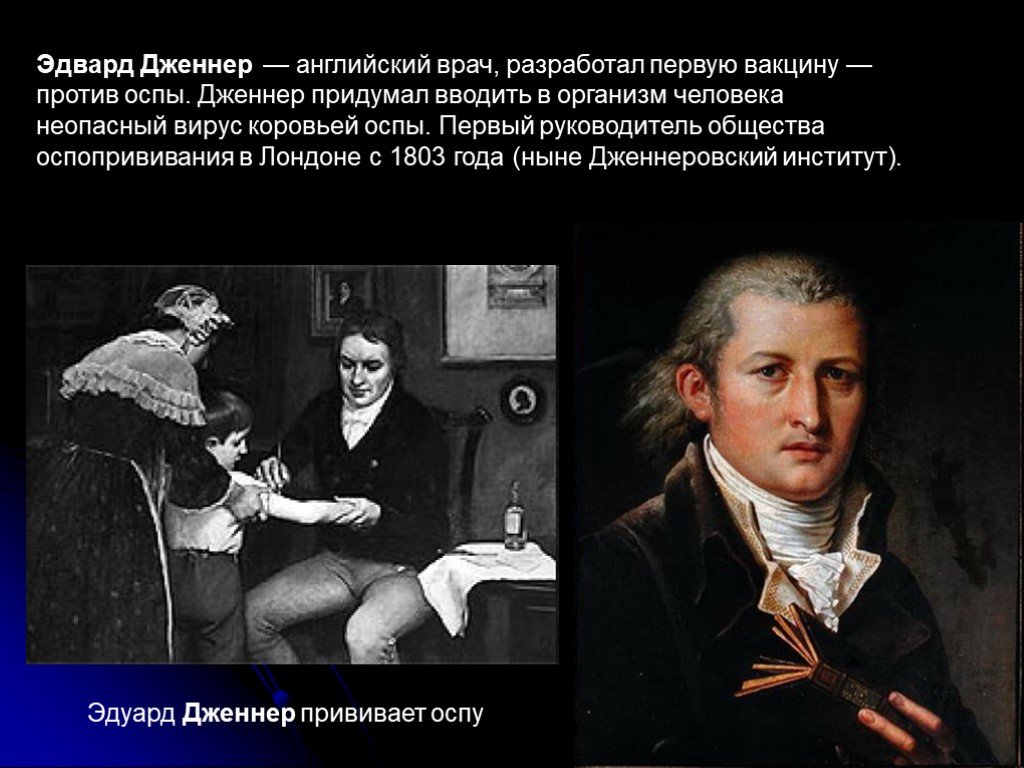 Таким образом, было создано учение об иммунитете. П. Эрлих в 1908 г. был удостоен Нобелевской премии по физиологии за создание клеточной теории иммунитета, которую он разделил с Ильей Ильичом Мечниковым.
Таким образом, было создано учение об иммунитете. П. Эрлих в 1908 г. был удостоен Нобелевской премии по физиологии за создание клеточной теории иммунитета, которую он разделил с Ильей Ильичом Мечниковым.
1892 год считается годом открытия новых организмов — вирусов.
Впервые существование вируса (как нового типа возбудителя болезней) доказал русский учёный Дмитрий Иосифович Ивановский. Дмитрий Иосифович обнаружил вирусы в результате изучения заболевания табачных растений.
Пытаясь найти возбудителя опасной болезни – табачной мозаики (проявляется на многих, особенно тепличных растениях в виде скручивающихся трубочкой, желтеющих и опадающих листьев, в некрозе плодов, нарастающих боковых почек), Ивановский несколько лет занимался исследованиями в Никитском ботаническом саду под Ялтой и в ботанической лаборатории АН.
Зная из работ голландского ботаника А.Д. Майера о том, что мозаичную болезнь табака можно вызвать переносом сока больных растений здоровым, ученый растирал листья больных растений, процеживал сок через полотняный фильтр и впрыскивал его в жилки здоровых листьев табака. Как правило, инфицированные растения перенимали болезнь.
Как правило, инфицированные растения перенимали болезнь.
Ботаник тщательно изучал под микроскопом больные листья, но не обнаружил ни бактерий, ни еще каких-либо микроорганизмов, что неудивительно, так как вирусы размером от 20 до 300 нм (1 нм = 109 м) на два порядка меньше бактерий, и их в оптический микроскоп увидеть нельзя. Считая, что в инфицировании виноваты все-таки бактерии, ботаник стал пропускать сок через специальный фарфоровый фильтр Э. Шамберлана, но, вопреки ожиданиям, инфекционные свойства отфильтрованного сока сохранялись, то есть, фильтр не улавливал бактерии.
Попытка вырастить возбудителя мозаики на обычных питательных средах, как это делается с теми же бактериями, не увенчалась успехом. Обнаружив в клетках инфицированных растений кристаллические включения (кристаллы «И»), ученый пришел к выводу, что возбудителем мозаичной болезни является твердое инфекционное начало – либо фильтрующиеся бактерии, не способные расти на искусственных субстратах, либо неведомые и невидимые микроорганизмы, выделяющие токсины.
О своих наблюдениях Ивановский доложил в 1892 г. на заседании Императорской АН. Исследования Ивановского подхватили ученые во всем мире. Использовав метод фильтрации русского ученого, немецкие врачи Ф. Лефлер и П. Фрош в 1897 г. обнаружили возбудителя ящура крупного рогатого скота. Затем последовал бум открытий вирусов – желтой лихорадки, чумы, бешенства, натуральной оспы, полиомиелита и т. д. В 1917 году были открыты бактериофаги – вирусы, разрушающие бактерии. Естественно, каждое открытие не было задачей «чистой» науки, за ним тут же следовало приготовление противоядия – вакцины, лечение и профилактика заболевания.
1921 год ознаменовался изобретением живой бактериальной вакцины против туберкулеза (БЦЖ).
Туберкулез перестал считаться смертельно опасным заболеванием, когда микробиолог Альбер Кальметт и ветеринар Камиль Герен разработали во Франции в 1908-1921 годах первую вакцину для человека на основе штамма ослабленной живой коровьей туберкулезной бациллы.
В 1908 году они работали в Институте Пастера в Лилле. Их деятельность охватывала получение культур туберкулёзной палочки и исследования различных питательных сред. При этом ученые выяснили, что на питательной среде на основе глицерина, жёлчи и картофеля вырастают туберкулёзные палочки наименьшей вирулентности (от лат. virulentus— ядовитый, сумма свойств микроба, определяющая его болезнетворное действие).
С этого момента они изменили ход исследования, чтобы выяснить, нельзя ли посредством повторяющегося культивирования вырастить ослабленный штамм для производства вакцины. Исследования продлились до 1919 года, когда вакцина с невирулентными (ослабленными) бактериями не вызвала туберкулёз у подопытных животных. В 1921 году ученые создали вакцину БЦЖ (BCG – Bacille bilie’ Calmette-Gue’rin) для применения на людях.
Общественное признание вакцины проходило с трудом, в частности, из-за случавшихся трагедий. В Любеке 240 новорождённых были привиты в 10-дневном возрасте. Все они заболели туберкулёзом, 77 из них умерли.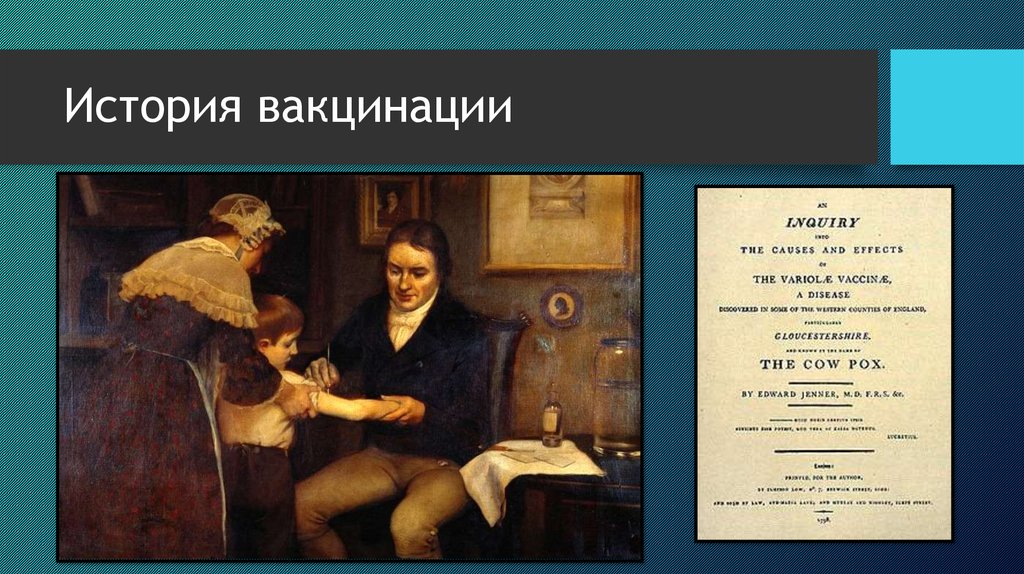 Расследование показало, что вакцина была заражена вирулентным (неослабленным) штаммом, который хранился в том же инкубаторе. Вина была возложена на директора больницы, которого приговорили к 2 годам лишения свободы за халатность, повлёкшую смерть.
Расследование показало, что вакцина была заражена вирулентным (неослабленным) штаммом, который хранился в том же инкубаторе. Вина была возложена на директора больницы, которого приговорили к 2 годам лишения свободы за халатность, повлёкшую смерть.
Многие страны, получившие от Кальметта и Герена штамм БЦЖ (1924-1925 гг.), подтвердили его эффективность и вскоре перешли к ограниченной, а затем и к массовой вакцинации против туберкулеза. В СССР штамм БЦЖ был привезен Л.А. Тарасевичем в 1925 году и обозначен BCG-I.
Вакцина БЦЖ выдержала испытание временем, ее эффективность проверена и доказана практикой. В наши дни вакцина БЦЖ является основным препаратом для специфической профилактики туберкулеза, признанным и используемым во всем мире. Попытки приготовления противотуберкулезной вакцины из других ослабленных штаммов или отдельных фракций микробных клеток пока не дали значимых практических результатов.
В 1923 году французский иммунолог Г. Рамон получил столбнячный анатоксин, который стал применяться для профилактики заболевания. Научное изучение столбняка началось во второй половине XIX века. Возбудитель столбняка был открыт почти одновременно русским хирургом Н. Д. Монастырским (в 1883 году) и немецким ученым А. Николайером (в 1884 году). Чистую культуру микроорганизма выделил в 1887 г. японский микробиолог С. Китазато, он же в 1890 г. получил столбнячный токсин и (совместно с немецким бактериологом Э. Берингом) создал противостолбнячную сыворотку.
Рамон получил столбнячный анатоксин, который стал применяться для профилактики заболевания. Научное изучение столбняка началось во второй половине XIX века. Возбудитель столбняка был открыт почти одновременно русским хирургом Н. Д. Монастырским (в 1883 году) и немецким ученым А. Николайером (в 1884 году). Чистую культуру микроорганизма выделил в 1887 г. японский микробиолог С. Китазато, он же в 1890 г. получил столбнячный токсин и (совместно с немецким бактериологом Э. Берингом) создал противостолбнячную сыворотку.
12 апреля 1955 г. в США успешно завершилось крупномасштабное исследование, подтвердившее эффективность вакцины Джонаса Солка – первой вакцины против полиомиелита. Эксперименты по созданию противополиомиелитной вакцины Солк начал в 1947 году. Вакцина из предварительно умерщвленных формалином полиовирусов была испытана Американским национальным фондом по борьбе с полиомиелитом. Впервые вакцина, созданная из предварительно умерщвленных формалином полиовирусов, прошла испытание в 1953-54 гг. (тогда ее тестировали добровольцы), а с 1955 года она получила уже широкое применение.
Впервые вакцина, созданная из предварительно умерщвленных формалином полиовирусов, прошла испытание в 1953-54 гг. (тогда ее тестировали добровольцы), а с 1955 года она получила уже широкое применение.
В исследовании приняло участие около 1 млн детей в возрасте 6-9 лет, из которых 440 тыс. получили вакцину Солка. По свидетельству очевидцев, родители с воодушевлением делали пожертвования на исследование и охотно записывали своих детей в ряды его участников. Сейчас это трудно представить, но в то время полиомиелит был самой грозной детской инфекцией, и родители со страхом ожидали прихода лета, когда регистрировался сезонный пик инфекции.
Результаты пятилетнего, с 1956 по 1961 год, массового применения вакцины превзошли все ожидания: среди детей в возрастных группах, особенно подверженных инфекции, заболеваемость снизилась на 96%.
В 1954 г. в США было зарегистрировано более 38 тыс. случаев полиомиелита, а спустя 10-летие применения вакцины Солка, в 1965 г., количество случаев полиомиелита в этой стране составило всего 61.
В 1991 году Всемирная организация здравоохранения объявила, что в Западном полушарии полиомиелит побежден. В странах Азии и Африки, благодаря массовым вакцинациям, заболеваемость также резко снизилась. Позже вакцина Солка была заменена на более совершенную, разработанную Альбертом Сэйбином. Однако вклад Джонаса Солка в борьбу с полиомиелитом это ничуть не приуменьшило: в этой области он по сей день считается первопроходцем.
В 1981-82 гг. стала доступной первая вакцина против гепатита В. Тогда в Китае приступили к использованию вакцины, приготовленной из плазмы крови, полученной от доноров из числа больных, которые имели продолжительную инфекцию вирусного гепатита В. В том же году она стала доступна и в США. Пик её применения пришёлся на 1982-88 гг. Вакцинацию проводили в виде курса из трёх прививок с временным интервалом. При постмаркетинговом наблюдении после введения такой вакцины отметили возникновение нескольких случаев побочных заболеваний центральной и периферической нервной системы. В исследовании привитых вакциной лиц, проведённом через 15 лет, подтверждена высокая иммуногенность вакцины, приготовленной из плазмы крови.
В исследовании привитых вакциной лиц, проведённом через 15 лет, подтверждена высокая иммуногенность вакцины, приготовленной из плазмы крови.
С 1987 г. на смену плазменной вакцине пришло следующее поколение вакцины против вируса гепатита В, в которой использована технология генной модификации рекомбинантной ДНК в клетках дрожжевого микроорганизма. Её иногда называют генно-инженерной вакциной. Синтезированный таким способом HBsAg выделяли из разрушаемых дрожжевых клеток. Ни один способ очистки не позволял избавляться от следов дрожжевых белков. Новая технология отличалась высокой производительностью, позволила удешевить производство и уменьшить риск, происходящий из плазменной вакцины.
В 1983 году Харальд цур Хаузен ему обнаружил ДНК папилломавируса в биопсии рака шейки матки, и это событие можно считать открытием онкогенного вируса ВПЧ-16.
Еще в 1976 году была выдвинута гипотеза о взаимосвязи вирусов папилломы человека (ВПЧ) с раком шейки матки. Некоторые разновидности ВПЧ безвредны, некоторые вызывают образование бородавок на коже, некоторые поражают половые органы (передаваясь половым путем). В середине семидесятых Харальд цур Хаузен обнаружил, что женщины, страдающие раком шейки матки, неизменно заражены ВПЧ.
В середине семидесятых Харальд цур Хаузен обнаружил, что женщины, страдающие раком шейки матки, неизменно заражены ВПЧ.
В то время многие специалисты полагали, что рак шейки матки вызывается вирусом простого герпеса, но цур Хаузен нашел в раковых клетках не вирусы герпеса, а вирусы папилломы и предположил, что развитие рака происходит в результате заражения именно вирусом папилломы. Впоследствии ему и его коллегам удалось подтвердить эту гипотезу и установить, что большинство случаев рака шейки матки вызваны одним из двух типов этих вирусов: ВПЧ-16 и ВПЧ-18. Эти типы вируса обнаруживаются примерно в 70% случаях рака шейки матки. Зараженные такими вирусами клетки с довольно большой вероятностью рано или поздно становятся раковыми, и из них развивается злокачественная опухоль.
Исследования Харальда цур Хаузена в области ВПЧ-инфекции легли в основу понимания механизмов канцерогенеза, индуцированного вирусом папилломы. Впоследствии были разработаны вакцины, которые позволяют предотвратить инфекцию вирусами ВПЧ-16 и ВПЧ-18. Это лечение позволяет сократить объем хирургического вмешательства и в целом снизить угрозу, представляемую раком шейки матки.
Это лечение позволяет сократить объем хирургического вмешательства и в целом снизить угрозу, представляемую раком шейки матки.
В 2008 году Нобелевский комитет присудил Нобелевскую премию в области физиологии и медицины Харальду цур Хаузену за открытие того, что вирус папилломы может вызывать рак шейки матки.
Восьмое чудо света: изобретение вакцин
Это первая статья из серии блогов магистрантов Доминиканского университета, посвященных пандемии COVID-19. В этом посте студенты Мелия Гранат-Панело, Натали Хилл, Каван Паттерсон и Энн Маркер описывают важную информацию о вакцинах и их жизненно важную роль в здоровом обществе.
Под редакцией доктора Панкаджа Капахи, профессора Бака
History of Vaccines
CDC заявляет, что вакцины являются одним из наиболее важных мероприятий в области общественного здравоохранения в истории. История вакцин — это длинная книга с множеством глав; давайте посмотрим на некоторые из основных моментов. Концепция вакцин была открыта Эдвардом Дженнером во время вспышки оспы в конце 1700-х годов. Он заметил, что доярки, переболевшие коровьей оспой (форма вируса оспы крупного рогатого скота), были невосприимчивы к инфекции оспы. Он сделал еще один шаг вперед, поместив образец пустулы с руки доярки, зараженной коровьей оспой, под кожу маленького мальчика с помощью процедуры, называемой прививкой. Мальчику сделали прививку один раз в мае и еще раз в июле, после чего он стал невосприимчив к оспе.
Концепция вакцин была открыта Эдвардом Дженнером во время вспышки оспы в конце 1700-х годов. Он заметил, что доярки, переболевшие коровьей оспой (форма вируса оспы крупного рогатого скота), были невосприимчивы к инфекции оспы. Он сделал еще один шаг вперед, поместив образец пустулы с руки доярки, зараженной коровьей оспой, под кожу маленького мальчика с помощью процедуры, называемой прививкой. Мальчику сделали прививку один раз в мае и еще раз в июле, после чего он стал невосприимчив к оспе.
Слово «вакцина» очень часто используется, но его происхождение на самом деле основано на латинском слове «корова» (vacca) и «коровья оспа» (vaccinia); поэтому Дженнер решил назвать эту новую процедуру «прививки» вакцинацией.
Хотя это открытие имело большое значение для искоренения оспы, не все считали этот метод революционным успехом. Фактически, его выводы постоянно отвергались на протяжении всей его жизни. Одним известным врачом на противоположной стороне был доктор П. Чаппон. В своей публикации 1803 года он предупредил об опасности вакцины против оспы. Хотя он выступал против метода, который в конечном итоге спасет миллионы жизней, доктор Чаппон поднимает интересный вопрос. Нижняя часть этой публикации переводится как
Хотя он выступал против метода, который в конечном итоге спасет миллионы жизней, доктор Чаппон поднимает интересный вопрос. Нижняя часть этой публикации переводится как
«Всякое внимание, весь энтузиазм по поводу системы могут исчезнуть, если ее принятие поставит под угрозу жизнь отдельного человека».
Этот образ мышления важно помнить, и именно поэтому у нас есть так много этапов для наших клинических испытаний, которые производят новые лекарства и вакцины.
Кроме того, возникла интересная социокультурная граница вокруг использования бычьего материала в качестве средства вакцинации. На протяжении 1920 века британская колониальная администрация приложила большие усилия для разработки вакцины, но ей пришлось столкнуться с нежеланием индусов, считающих коров священными. Несмотря на то, что Индия была одним из наиболее пострадавших от оспы мест на земном шаре, индийцы считали использование священных животных для этой цели отвратительным, учитывая их религиозные убеждения. Благодаря настойчивой работе представителей общественного здравоохранения и дальнейшей разработке вакцины в конечном итоге подавляющее большинство населения Индии было вакцинировано, и в настоящее время оспа ликвидирована во всем мире.
Благодаря настойчивой работе представителей общественного здравоохранения и дальнейшей разработке вакцины в конечном итоге подавляющее большинство населения Индии было вакцинировано, и в настоящее время оспа ликвидирована во всем мире.
Однако мы должны помнить, что наука не является линейным процессом. Многие, многие неудачи в конечном итоге приводят к чудесному успеху. Каждое открытие добавляет новое измерение в бесконечную паутину, из которой состоит поле. Вакцина против оспы, несмотря на многочисленные вызовы и негативную реакцию, послужила источником вдохновения для новой эры в медицине: пастеровская программа была сформулирована как «une maladie, un vaccin» («от каждой болезни — вакцина»).
Как видно из приведенной выше временной шкалы, существует огромный разрыв между созданием первой вакцины и созданием следующей, а затем происходит внезапный бум открытия многих новых вакцин. Этот тип запаздывания — явление, которое мы можем наблюдать в модели развития новых технологий. Инновации и изобретения — это не линейное развитие, а скорее экспоненциальный бум, когда каждое открытие приводит к появлению новых. В настоящее время вакцины вводятся в хорошо отлаженной системе, начиная с рождения. В настоящее время считается, что многие из этих болезней, такие как вирусы полиомиелита 2 и 3 типа, ликвидированы, хотя в некоторых районах уровень вакцинации снижается, что позволяет этим заболеваниям вновь появляться среди населения.
Инновации и изобретения — это не линейное развитие, а скорее экспоненциальный бум, когда каждое открытие приводит к появлению новых. В настоящее время вакцины вводятся в хорошо отлаженной системе, начиная с рождения. В настоящее время считается, что многие из этих болезней, такие как вирусы полиомиелита 2 и 3 типа, ликвидированы, хотя в некоторых районах уровень вакцинации снижается, что позволяет этим заболеваниям вновь появляться среди населения.
Типы вакцин
Чтобы сделать иммунный ответ более понятным, давайте разберем, что происходит внутри организма, когда вы получаете вакцину. Может помочь, если мы будем относиться к процессу вакцинации как к пожарной тревоге. Противопожарные учения — это тренировочный раунд, когда возникает реальная чрезвычайная ситуация. Вы изучаете маршруты выхода и как добраться до безопасного места, чтобы выполнять эти процедуры быстро и не задумываясь. Вакцина дает нашей иммунной системе возможность подготовиться к чрезвычайной ситуации, подобной этой.
Вакцины могут защитить нас как от вирусных, так и от бактериальных инфекций, но между этими инфекционными агентами есть некоторые ключевые различия. Во-первых, вирус — это неживой агент, который может воспроизводиться только тогда, когда находится в наших клетках. С другой стороны, бактерии могут жить вне нашего тела и свободно размножаться, и их часто лечат антибиотиками.
Каждый из перечисленных ниже типов вакцин работает немного по-разному, но все они содержат некоторую часть вируса или бактерий, так что наша иммунная система может выстроить защиту от них в случае, если вы когда-либо вступите в контакт с настоящей вакциной. Возьмем конкретный пример типа вакцины: аттенуированный вирус. ослабленный вирус вакцина содержит ослабленную вирусную частицу, что делает ее неинфекционной при введении. Поскольку инфекционные агенты были «отключены» в лаборатории, наша иммунная система может распознавать, репетировать и запоминать этот тип патогена, создавать антитела против него и использовать эти антитела, чтобы направить наши иммунные клетки на борьбу с реальным вирусом.
- Вакцины аттенуированные вирусные применяются при ветряной оспе, оспе, кори, паротите, краснухе.
- Инактивированные вакцины используются для вакцины против полиовируса (ИПВ), вакцины против коклюша, вакцины против бешенства и вакцины против вируса гепатита А.
- Субъединичные вакцины предназначены для ВПЧ, гепатита В и менингита.
- Вакцина Nucleic acid представляет собой вакцину против SARS-Cov 2; в частности, он использует мРНК из определенной части вируса, чтобы помочь нашему организму распознать и убить вирус, если он попадет в нашу систему.
Чтобы узнать больше об этом процессе, прочитайте статью «Попытка положить конец пандемии: объяснение вакцин», которая скоро появится в блоге из нашей серии.
Вы слышали о коллективном иммунитете?
Рис. 2: Основные репродукционные показатели (R0) различных заболеваний. R0 указывает на трансмиссивность болезни, усредняя количество людей, инфицированных одним заразным человеком. Из этих болезней корь и оспа были объявлены ликвидированными ВОЗ.
Из этих болезней корь и оспа были объявлены ликвидированными ВОЗ.
Вы можете подумать: «Никто из тех, кого я знаю, никогда не болел корью, но я читал, что добавки в вакцинах опасны! Так почему я должен хотеть поместить это в свое тело или, что еще хуже, в тело моего ребенка из-за болезни, которая не заразила никого за 50 лет?» Ответ таков: причина, по которой вы не слышали о многих, если таковые имеются, случаях заболеваний, от которых регулярно вакцинируются, заключается в том, что они были практически искоренены благодаря тому, что большинство нашего населения было вакцинировано.
Каждый вирус имеет номер, который присваивается в зависимости от того, насколько он заразен, как показано на рис. 2. Этот номер называется R 0 (произносится как «R ноль»). R 0 помогает ученым выяснить, какой процент нашего населения должен быть невосприимчивым к вирусу — либо в результате перенесенной инфекции, либо в результате вакцинации — чтобы предотвратить заражение вирусом других, более уязвимых людей в нашем населении. и переживает гораздо более тяжелый случай заболевания.
и переживает гораздо более тяжелый случай заболевания.
Например, R 0 кори был определен учеными в диапазоне от 12 до 18, а это означало, что для того, чтобы население в целом было практически невосприимчивым к вирусу, 83-94% населения должен стать невосприимчивым, пережив случай кори или получив вакцину против кори. Этот процент называется «порог коллективного иммунитета» и использует R 0 болезни в расчете, отражающем, что чем выше базовый коэффициент воспроизводства болезни, тем большая часть популяции должна быть невосприимчива к болезни, чтобы достичь коллективного иммунитета.
Рисунок 3: Схема коллективного иммунитета. Человек в фиолетовом — инфекционный больной, люди в синем — люди, не имеющие иммунитета к болезни, а люди в зеленом — невосприимчивые. По мере того, как все больше людей становятся невосприимчивыми, меньше людей заражается первоначальным пурпурным пациентом. Так работает коллективный иммунитет.
К счастью, в случае с корью это произошло! К 2000 году достаточное количество населения стало невосприимчивым к кори в результате вакцинации, а не в результате заражения корью, поэтому Всемирная организация здравоохранения классифицировала его как элиминированный вирус. Эта способность населения быть коллективно защищенным от вируса за счет вакцинации большинства его составляющих называется коллективный иммунитет . Несмотря на достижение статуса элиминации, были случаи повторной вспышки кори из-за отказа отдельных лиц от вакцинации.
Эта способность населения быть коллективно защищенным от вируса за счет вакцинации большинства его составляющих называется коллективный иммунитет . Несмотря на достижение статуса элиминации, были случаи повторной вспышки кори из-за отказа отдельных лиц от вакцинации.
Хотя небольшая часть коллективного иммунитета исходит от тех людей, которые заразились этой болезнью и выжили, важно отметить, что ни одна болезнь никогда не была искоренена путем предоставления возможности заразиться ею каждому человеку. Возможно, вы слышали термин «коллективный иммунитет», используемый средствами массовой информации, общественными деятелями или политиками для описания пути к тому, чтобы стать невосприимчивым как население, позволив вирусу свирепствовать и заразить как можно больше людей. Как видно из Швеции во время нынешней пандемии, такой подход имеет серьезные последствия. Швеция — хотя официальная позиция страны заключается в том, что они не пытались целенаправленно достичь коллективного иммунитета посредством полной вирусной инфекции — не приняла меры по блокировке или социальному дистанцированию. Согласно данным, опубликованным на информационной панели ВОЗ по коронавирусу, по состоянию на февраль 2021 года в Швеции пострадало 12 649 человек.смертей от COVID-19, тогда как в соседней Норвегии, которая ввела ограничения, пострадало 607 человек, что на душу населения более чем в десять раз превышает количество смертей в Швеции. Это просто показывает эффективность и важность плановой вакцинации, особенно в условиях кризиса общественного здравоохранения.
Согласно данным, опубликованным на информационной панели ВОЗ по коронавирусу, по состоянию на февраль 2021 года в Швеции пострадало 12 649 человек.смертей от COVID-19, тогда как в соседней Норвегии, которая ввела ограничения, пострадало 607 человек, что на душу населения более чем в десять раз превышает количество смертей в Швеции. Это просто показывает эффективность и важность плановой вакцинации, особенно в условиях кризиса общественного здравоохранения.
Завтра мы расскажем о некоторых подробностях, касающихся конкретно вакцины против COVID-19, и объясним, почему это безопасный выход из этой пандемии.
Пионеры вакцинации — Merck.com
Инновации
Ученые, добившиеся гигантских успехов в борьбе с вирусными заболеваниями и истории вакцин
8 апреля 2022 г.
Поделиться этой статьей -старый Джеймс Фиппс с коровьей оспой, чтобы защитить себя от оспы. Дженнер использовал термин «вакцинация», где «вакка» на латыни означает «корова». На самом деле веками признано, что некоторые болезни никогда не заражают человека после выздоровления. Оспа была первой болезнью, которую люди пытались предотвратить, преднамеренно прививая себя зараженным веществом. 900:05 Доктор Эдвард Дженнер делает прививку 9-летнему Джеймсу Фиппсу от коровьей оспы.
На самом деле веками признано, что некоторые болезни никогда не заражают человека после выздоровления. Оспа была первой болезнью, которую люди пытались предотвратить, преднамеренно прививая себя зараженным веществом. 900:05 Доктор Эдвард Дженнер делает прививку 9-летнему Джеймсу Фиппсу от коровьей оспы.
Спустя восемь десятилетий после того, как Дженнер опубликовал свои открытия, Луи Пастер разработал первую живую аттенуированную бактериальную вакцину. Аттенуация — это процесс, который ослабляет бактерии или вирусы в вакцине, что снижает вероятность возникновения заболевания, но при этом вызывает иммунный ответ, аналогичный естественной инфекции. Потребуется еще много десятилетий, чтобы достижения в фундаментальных и клинических исследованиях позволили ученым понять вирусы достаточно хорошо, чтобы приступить к разработке вакцин, помогающих защитить от определенных вирусных заболеваний.
Доктор Морис Хиллеман
Среди ученых, добившихся гигантских успехов в борьбе с вирусными заболеваниями, были Джонас Солк и Альберт Сабин. Доктор Морис Хиллеман, который возглавлял отдел вирусной и клеточной биологии Merck с 1957 по 1984 год, также принадлежал к этой выдающейся группе пионеров вакцин. Доктор Хиллеман, которому приписывают помощь в разработке более 40 экспериментальных и лицензированных вакцин для людей и животных, и по сей день продолжает вдохновлять ученых в медицинских исследовательских лабораториях.
Доктор Морис Хиллеман, который возглавлял отдел вирусной и клеточной биологии Merck с 1957 по 1984 год, также принадлежал к этой выдающейся группе пионеров вакцин. Доктор Хиллеман, которому приписывают помощь в разработке более 40 экспериментальных и лицензированных вакцин для людей и животных, и по сей день продолжает вдохновлять ученых в медицинских исследовательских лабораториях.
Доктор Хиллеман родился и вырос на ферме в Монтане. Это была тяжелая жизнь, но фермерское прошлое послужило отличной основой для его дальнейшей работы. «Когда ты вырос на ферме, у тебя много общих знаний, — сказал он. После окончания Чикагского университета со степенью доктора микробиологии и химии Хиллеман предпочел работать в фармацевтической компании, а не в академических кругах.
Несмотря на многочисленные достижения, включая помощь в разработке более 40 вакцин для людей и животных, имя д-ра Мориса Хиллемана практически неизвестно широкой публике и прессе. Тем не менее, его влияние на общественное здоровье неоспоримо.
