Содержание
Об этом говорят
|
АКДС: правда и вымысел
Некоторое время назад появилась информация об осложнениях, связанных с прививками АКДС. Можно понять беспокойство родителей, что может быть важнее состояние здоровья собственного ребенка? Но насколько обоснованными являются эти тревоги? За разъяснениями мы обратились к Ольге Евгеньевне Шитовой, заместителю главного врача по педиатрии ФГБУЗ КБ №172 ФМБА России. Надеемся, что пояснения опытного специалиста помогут читателям разобраться в ситуации.
|
— Прививку АКДС прививают против трех инфекций – коклюша, дифтерии и столбняка, — рассказывает Ольга Евгеньевна Шитова, заместитель главного врача по педиатрии Клинической больницы №172 ФМБА России. — Почему это важно и необходимо делать? Чтобы сохранить здоровье, а во многих случаях и жизнь человека. Велика вероятность, что заболевание столбняком или дифтерией может привести к летальному исходу или к серьезным проблемам со здоровьем. До 40% детей первого года жизни больных коклюшем также умирают. То есть все три инфекции очень серьезные, и даже в случае своевременной госпитализации в стационар, таких больных не всегда удается спасти.
Велика вероятность, что заболевание столбняком или дифтерией может привести к летальному исходу или к серьезным проблемам со здоровьем. До 40% детей первого года жизни больных коклюшем также умирают. То есть все три инфекции очень серьезные, и даже в случае своевременной госпитализации в стационар, таких больных не всегда удается спасти.
Многолетняя мировая и отечественная медицинская практики показывают, что единственным эффективным способом защиты от этих инфекций является вакцинация. Тем не менее, всегда были и есть люди, которые по разным соображениям пренебрегают мнением специалистов. Заражение столбняком происходит при попадании инфекции через поврежденные кожные покровы. Согласитесь, как бы вы не оберегали свое чадо от воздействия внешних факторов окружающей среды, полностью защитить ребенка от их воздействия невозможно. Ваши мальчик или девочка не ходят в скафандре, всегда есть риск получить мелкие ссадины, порезы, уколоться и т.д., то есть существует вероятность заражения инфекцией. Кроме того, если ребенок не привит, то при получении травмы ему в рамках экстренной профилактики заболевания столбняком вводятся другие иммунобиологические препараты, которые в силу своего состава, могут вызвать сильные аллергические реакции. Вакцинация же создает индивидуальную невосприимчивость и индивидуальную память.
Кроме того, если ребенок не привит, то при получении травмы ему в рамках экстренной профилактики заболевания столбняком вводятся другие иммунобиологические препараты, которые в силу своего состава, могут вызвать сильные аллергические реакции. Вакцинация же создает индивидуальную невосприимчивость и индивидуальную память.
Цель Всемирной организации здравоохранения (ВОЗ) снизить заболеваемость дифтерией до 0,1 случая заболевания на 100 000 населения в России достигнута. Однако последняя массовая вакцинация взрослого населения против дифтерии проводилась более десяти лет назад. Общая прослойка иммунизированных граждан (так называемый коллективный иммунитет) снижается, что создает дополнительные риски для окружающих. В этих условиях лучше всего защитить себя и своего ребенка прививкой от дифтерии.
Если 7-10 лет назад коклюшем болели единицы, то в последнее время отмечается рост заболевания среди подростков и взрослых. Заболевание у данной категории протекает не всегда типично, что затрудняет диагностику. Это в свою очередь способствует заражению не привитых и детей первого года жизни. Заболевание протекает с приступами мучительного кашля, остановкой дыхания, пневмонией, кровоизлияниями в головной мозг. Длительность сохранения кашля составляет от четырех до шести месяцев. Наш город не исключение. Более того, сейчас рассматривается вопрос о необходимости проведения ревакцинации (повторного введения вакцины) детям в шестилетнем возрасте, для сохранения иммунитета в подростковом возрасте и у взрослых.
Это в свою очередь способствует заражению не привитых и детей первого года жизни. Заболевание протекает с приступами мучительного кашля, остановкой дыхания, пневмонией, кровоизлияниями в головной мозг. Длительность сохранения кашля составляет от четырех до шести месяцев. Наш город не исключение. Более того, сейчас рассматривается вопрос о необходимости проведения ревакцинации (повторного введения вакцины) детям в шестилетнем возрасте, для сохранения иммунитета в подростковом возрасте и у взрослых.
Не думаю, что кому-то нужны такие испытания.
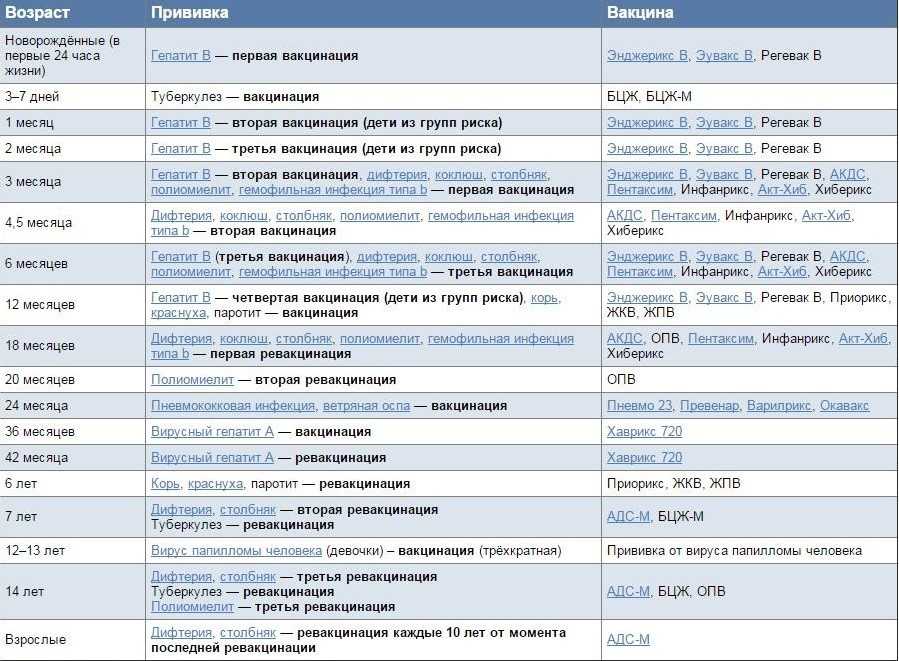
Вакцину АКДС вводят трехкратно с трехмесячного возраста с интервалом в месяц. Это называется вакцинацией. Через полтора года после третьей прививки проводится ревакцинация (повторное введение вакцины). Как правило, в это время ребенку полтора года. В возрасте 6-7 лет, обычно перед поступлением в школу делается еще одна ревакцинация. Правда, на этот раз используется вакцина АДС, то есть проводиться ревакцинация направленная только против дифтерии и столбняка.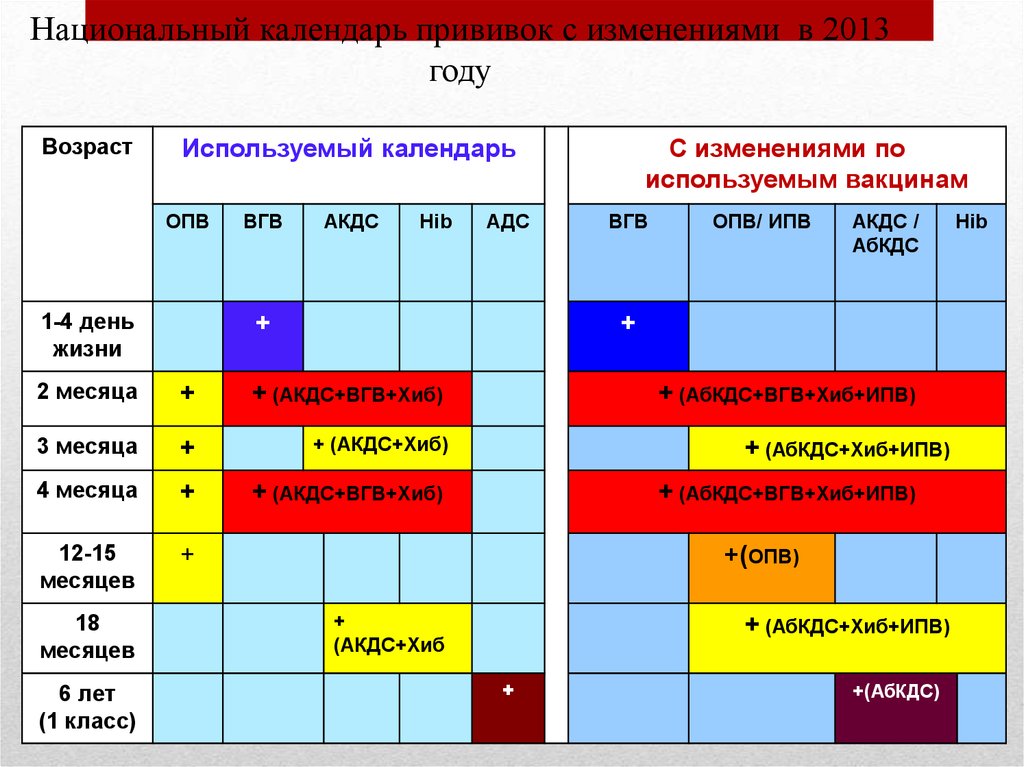 И последняя в детском возрасте ревакцинация делается в 14 лет. Далее, теперь уже взрослому человеку, ревакцинация против дифтерии и столбняка проводится каждые десять лет.
И последняя в детском возрасте ревакцинация делается в 14 лет. Далее, теперь уже взрослому человеку, ревакцинация против дифтерии и столбняка проводится каждые десять лет.
Специалисты никогда не скрывали, что прививка АКДС иногда дает реакции, которые могут беспокоить родителей. И вот почему. С вакциной в организм человека попадают два анатоксина – дифтерийный и столбнячный. Они не могут привести к заболеванию, но зато формируют иммунитет против дифтерии и столбняка. Также в состав отечественной вакцины входят мертвые клетки коклюшной палочки. Они-то и вызывают основные реакции на прививку, которые так часто беспокоят родителей.
Инструкция вакцины АКДС допускает развитие нормальных реакций организма на введение вакцины в виде местных и общих реакций. Реакции на АКДС могут проявиться первые трое суток после вакцинации. Частота местной реакции, особенно на повторные введения составляет от 40-50%. К нормальным (допустимым) общим реакциям относят повышение температуры, недомогание, потеря аппетита, сонливость. Сильной реакцией считают температуру 40 градусов, развитие судорог на фоне температуры. У предрасположенных к аллергии детей возможно усиление кожных проявлений аллергии. Как правило, АКДС детям, у которых имеются особенности в развитии или отклонения в состоянии здоровья, проводят с подготовкой, например, назначают прием антигистаминных препаратов до и после вакцинации, рекомендуя прием одного из двух разрешенных в педиатрии жаропонижающих средств – парацетамол или нурофен в профилактических целях, не дожидаясь повышения температуры.
Сильной реакцией считают температуру 40 градусов, развитие судорог на фоне температуры. У предрасположенных к аллергии детей возможно усиление кожных проявлений аллергии. Как правило, АКДС детям, у которых имеются особенности в развитии или отклонения в состоянии здоровья, проводят с подготовкой, например, назначают прием антигистаминных препаратов до и после вакцинации, рекомендуя прием одного из двух разрешенных в педиатрии жаропонижающих средств – парацетамол или нурофен в профилактических целях, не дожидаясь повышения температуры.
Как отмечалось ранее, помимо общих реакций, есть местные. Собственно именно они стали причиной беспокойства в родительской среде. Местная реакция может проявляться в виде небольшой болезненности в месте укола. Возможно развитие покраснения, уплотнения и припухлости (инфильтрата). До восьми сантиметров в диаметре инфильтрат считается нормальной реакцией организма на прививку.
Объясню, почему возникают местные реакции. Компоненты вакцины в АКДС «насажены» на адьювант – вещество, которое обеспечивает более медленное равномерное всасывание всех составных частей, снижает развитие общих реакций, но при этом вызывает образование местной воспалительной реакции.
Местная реакция самостоятельно проходит в течение двух недель и чаще всего не требует лечения, возможно применение терапии для ускорения рассасывания.
Обычно первая и вторая прививка протекают без реакции. Но поскольку после этого организм уже знает, что ему будут вводить, то, как правило, третья и четвертая реакция дают большую реакцию. К этому и родителям и медработникам следует быть готовыми
Но если родителей беспокоит состояние ребенка после прививки, то необходимо обратиться к педиатру, для наблюдения и оказания медицинской помощи. Самолечением, особенно прикладыванием капустных листков, всяких лепешек, рисованием йодных сеток, заниматься не надо, это, как правило, приводит только к нежелательным последствиям. Надо иметь в виду, что инфильтрат – воспалительная реакция после введения чужеродного вещества. На него организм должен ответить. С этой целью он начинает вырабатывать клетки иммунной системы – лимфоциты, которые устремляются в этот очаг, словно бабочки на огонек в ночи. Там они знакомятся с компонентами вакцины, размножатся и создадут особый клон клеток – Т – лимфоциты памяти. В связи с этим мы видим внешние проявления – покраснение, отек. Все это нормальный ответ организма. Как только лимфоциты «поймут» против кого им надо бороться, с током крови все это рассосется само, без применения каких-либо веществ. Еще раз подчеркиваю: местные реакции были, есть и должны быть. Но если сердобольный родитель начинает сверху греть инфильтрат, прикладывая компрессы, капустные листы, то он усиливает приток крови, то есть еще больше усиливает воспалительную реакцию, что может стать причиной занесения инфекции через место инъекции.
Там они знакомятся с компонентами вакцины, размножатся и создадут особый клон клеток – Т – лимфоциты памяти. В связи с этим мы видим внешние проявления – покраснение, отек. Все это нормальный ответ организма. Как только лимфоциты «поймут» против кого им надо бороться, с током крови все это рассосется само, без применения каких-либо веществ. Еще раз подчеркиваю: местные реакции были, есть и должны быть. Но если сердобольный родитель начинает сверху греть инфильтрат, прикладывая компрессы, капустные листы, то он усиливает приток крови, то есть еще больше усиливает воспалительную реакцию, что может стать причиной занесения инфекции через место инъекции.
Почему нельзя рисовать йодную сетку? Детская кожа нежная, восприимчивая к внешним воздействиям, не имеет таких защитных свойств как у взрослого, поэтому при использовании настойки йода возможно развитие химического ожога. К тому же йод, приобретенный в аптеке, порой долгое время стоит без применения и за это время спиртовая составляющая частично испаряется и концентрация йода увеличивается. Таким образом, возникает ситуация «хотели как лучше, а получилось как всегда».
Таким образом, возникает ситуация «хотели как лучше, а получилось как всегда».
Периодически в обществе возникают разговоры о том, что медицинские работники не разъясняют родителям, что ожидать от прививок и что им делать в случае появления реакций. На самом деле перед прививкой информация матери и отцу предоставляется участковой медицинской сестрой в момент приглашения родителей с ребенком в поликлинику для проведения вакцинации, врачом-педиатром при проведении осмотра ребенка перед прививкой. Кроме того, родитель перед прививкой дает письменное, подчеркиваю письменное, согласие, что ему понятно с какой целью она проводится, какие реакции и осложнения возможны. Далее, когда родитель приходит в прививочный кабинет, процедурная медсестра еще раз дает пояснения относительно вакцины, возможных реакций и что делать в случае их появления. В частности, она предупреждает, что если ребенка что-то будет беспокоить, следует обратиться к врачу или к ней. Также медсестра просит родителя посидеть с ребенком после вакцинации возле прививочного кабинета в течение 30 минут. После это времени, если все нормально, они могут идти домой.
После это времени, если все нормально, они могут идти домой.
Помимо этого, хочу заметить, что в детских поликлиниках в прививочных кабинетах работают медицинские сестры с большим стажем и опытом. На такой ответственный участок другие не допускаются.
Некоторые эмоциональные родители, приходя с ребенком на вакцинацию, сильно волнуются и не всегда могут воспринимать предоставляемую информацию или оказать медицинскому работнику необходимую помощь при проведении вакцинации. Между тем, малышу нужно хорошо зафиксировать ногу (вакцина вводится в бедро), чтобы ребенок не дернулся. Не все мамы способны сделать это. Поэтому, пожалуйста, пусть на прививку с мамой и ребенком приходит папа или близкий родственник, который сможет это сделать.
В заключении хотелось бы сказать следующее. Вакцинация – защита от опасных инфекций. Ребенок – не машина, он индивидуален, у него имеются особенности развития присущие только ему, что способствует проявлению местных и общих реакций. Вакцина же рассчитана на среднестатистического ребенка. Поэтому, если он наблюдается у педиатра, то врач учитывает особенности малыша при подготовке к прививке. Кроме того, у родителя, если у него есть вопросы, всегда есть возможность задать их как врачу, так и патронажной сестре. В случаях, когда вы считаете, что не получили необходимых пояснений, просим обращаться к заведующим детскими поликлиниками по месту жительства, руководители подразделений не откажут вам в помощи.
Поэтому, если он наблюдается у педиатра, то врач учитывает особенности малыша при подготовке к прививке. Кроме того, у родителя, если у него есть вопросы, всегда есть возможность задать их как врачу, так и патронажной сестре. В случаях, когда вы считаете, что не получили необходимых пояснений, просим обращаться к заведующим детскими поликлиниками по месту жительства, руководители подразделений не откажут вам в помощи.
Будьте здоровы!
Лицензированные коклюшные вакцины в США
1.
Заметки с поля
Коклюш — Калифорния, январь–июнь 2010 г. MMWR Morb Mortal Wkly Rep.
2010 г.; 59:817. [Google Scholar]
2.
Октавия С., Синченко В., Гилберт Г.Л., Лоуренс А., Кейл А.Д., Хогг Г., Лан Р. Новые клоны Bordetella pertussis, несущие аллели prn2 и ptxP3, причастные к эпидемии коклюша в Австралии в 2008-2010 гг. J заразить Dis
2012 г.; 205:1220-4; PMID: 22416243; http://dx.doi.org/10.1093/infdis/jis178 [PubMed] [Google Scholar]
3.
Гринберг Д.П., Домланд М., Беттингер Дж. А., Шайфеле Д.В., Гальперин С.А., Уотерс В., Кандола К.; ВОЗДЕЙСТВИЕ Следователи. Эпидемиология коклюша и Haemophilus influenzae типа b в Канаде с использованием исключительно педиатрической комбинированной вакцины против дифтерии-столбняка-бесклеточного коклюша-инактивированного полиовируса-Haemophilus influenzae типа b и противостолбнячной-дифтерийно-бесклеточной коклюшной вакцины подростков-взрослых: последствия для профилактики заболевания В Соединенных Штатах. Педиатр Infect Dis J
А., Шайфеле Д.В., Гальперин С.А., Уотерс В., Кандола К.; ВОЗДЕЙСТВИЕ Следователи. Эпидемиология коклюша и Haemophilus influenzae типа b в Канаде с использованием исключительно педиатрической комбинированной вакцины против дифтерии-столбняка-бесклеточного коклюша-инактивированного полиовируса-Haemophilus influenzae типа b и противостолбнячной-дифтерийно-бесклеточной коклюшной вакцины подростков-взрослых: последствия для профилактики заболевания В Соединенных Штатах. Педиатр Infect Dis J
2009 г.; 28:521-8; PMID: 19436236; http://dx.doi.org/10.1097/INF.0b013e318199d2fc [PubMed] [Google Scholar]
4.
Амирталингам Г. Стратегии борьбы с коклюшем у младенцев. Арка Дис Чайлд
2013; 98:552-5; PMID: 23698594; http://dx.doi.org/10.1136/archdischild-2012-302968 [PubMed] [Google Scholar]
5.
Баррет А.С., Райан А., Бреслин А., Каллен Л., Мюррей А., Гроган Дж., Бурк С., Коттер С. Вспышка коклюша на северо-западе Ирландии, январь-июнь 2010 г. Euro Surveill
2010 г.; 15:15; PMID:20822735 [PubMed] [Google Scholar]
6.
Lavine JS, Bjørnstad ON, de Blasio BF, Storsaeter J. Краткосрочный иммунитет против коклюша, возрастные пути передачи и полезность бустерной вакцины для подростков. вакцина
2012 г.; 30:544-51; PMID: 22119924; http://dx.doi.org/10.1016/j.vaccine.2011.11.065 [бесплатная статья PMC] [PubMed] [Google Scholar]
7.
Черри Д.Д., Бруннел П., Голден Дж.
Доклад Целевой группы по коклюшу и иммунизации против коклюша. Педиатрия
1988 год; 81 (дополнение): 933-84. [Google Scholar]
8.
Onorato IM, Wassilak SG, Meade B. Эффективность цельноклеточной коклюшной вакцины у детей дошкольного возраста в США. ДЖАМА
1992; 267:2745-9; PMID: 1578592; http://dx.doi.org/10.1001/jama.1992.03480200053023 [PubMed] [Google Scholar]
9.
Центры по контролю и профилактике заболеваний (CDC). Январь 1992 — июнь 1995. MMWR Morb Mortal Wkly Rep.
1995 год; 44:525-9; PMID:7603428 [PubMed] [Google Scholar]
10.
Schmitt HJ, von König CH, Neiss A, Bogaerts H, Bock HL, Schulte-Wissermann H, Gahr M, Schult R, Folkens JU, Rauh W, et al. .
.
Эффективность бесклеточной коклюшной вакцины в раннем детстве после бытового воздействия. ДЖАМА
1996; 275:37-41; PMID:8531284; http://dx.doi.org/10.1001/jama.1996.03530250041024 [PubMed] [Google Scholar]
11.
Liese JG, Meschievitz CK, Harzer E, Froeschle J, Hosbach P, Hoppe JE, Porter F, Stojanov S, Niinivaara K, Walker AM и др..
Эффективность двухкомпонентной бесклеточной коклюшной вакцины у детей раннего возраста. Педиатр Infect Dis J
1997 год; 16:1038-44; PMID: 9384336; http://dx.doi.org/10.1097/00006454-199711000-00007 [PubMed] [Google Scholar]
12.
Симондон Ф., Презиози М.П., Ям А., Кейн К.Т., Чабиранд Л., Итман И., Санден Г., Мбоуп С., Хоффенбах А., Кнудсен К. и др..
Рандомизированное двойное слепое исследование по сравнению двухкомпонентной бесклеточной и цельноклеточной коклюшной вакцины в Сенегале. вакцина
1997; 15:1606-12; PMID: 9364690; http://dx.doi.org/10.1016/S0264-410X(97)00100-X [PubMed] [Google Scholar]
13.
Stehr K, Cherry JD, Heininger U, Schmitt-Grohé S, uberall M, Laussucq S, Eckhardt T, Meyer M, Engelhardt R, Christenson P. Сравнительное исследование эффективности в Германии у младенцев, получавших бесклеточный коклюшный компонент Lederle/Takeda Вакцина АКДС (АКДС), цельноклеточная компонентная вакцина АКДС Ледерле или вакцина АКДС. Педиатрия
Сравнительное исследование эффективности в Германии у младенцев, получавших бесклеточный коклюшный компонент Lederle/Takeda Вакцина АКДС (АКДС), цельноклеточная компонентная вакцина АКДС Ледерле или вакцина АКДС. Педиатрия
1998 год; 101:1-11; PMID: 9417143; http://dx.doi.org/10.1542/peds.101.1.1 [PubMed] [Google Scholar]
14.
Гальперин С.А., Бортолусси Р., Маклин Д., Чизхолм Н. Персистенция коклюша в иммунизированной популяции: результаты расширенной программы эпиднадзора за коклюшем в Новой Шотландии. Дж Педиатр
1989 год; 115:686-93; PMID: 2809899; http://dx.doi.org/10.1016/S0022-3476(89)80643-2 [PubMed] [Google Scholar]
15. De Serres G, Boulianne N, Duval B, Déry P, Rodriguez AM, Massé R , Гальперин С. Эффективность цельноклеточной коклюшной вакцины в детских садах и школах. Педиатр Infect Dis J
1996; 15:519-24; PMID:8783349; http://dx.doi.org/10.1097/00006454-199606000-00009 [PubMed] [Google Scholar]
16.
Бенци-Энчилл А.Д., Гальперин С.А., Скотт Дж., МакИсаак К. , Дюкло П. Оценки эффективности цельноклеточной коклюшной вакцины при вспышке среди иммунизированной популяции. вакцина
, Дюкло П. Оценки эффективности цельноклеточной коклюшной вакцины при вспышке среди иммунизированной популяции. вакцина
1997 год; 15:301-6; PMID:9139490; http://dx.doi.org/10.1016/S0264-410X(96)00176-4 [PubMed] [Google Scholar]
17.
Ntezayabo B, De Serres G, Duval B. Возрождение коклюша в Канаде в значительной степени вызвано когортным эффектом. Педиатр Infect Dis J
2003 г.; 22:22-7; PMID: 12544404; http://dx.doi.org/10.1097/00006454-200301000-00009 [PubMed] [Google Scholar]
18.
Кристи К.Д., Маркс М.Л., Маршан К.Д., Райзинг С.Ф. Эпидемия коклюша 1993 года в Цинциннати. Рецидив заболевания в высоко иммунизированной популяции детей. N Engl J Med
1994 год; 331:16-21; PMID:8202096; http://dx.doi.org/10.1056/NEJM199407073310104 [PubMed] [Google Scholar]
19.
Джулиано М., Мастрантонио П., Джамманко А., Пискителли А., Салмасо С., Вассилак С.Г. Антительные ответы и персистенция в течение двух лет после иммунизации двумя бесклеточными вакцинами и одной цельноклеточной вакциной против коклюша. Дж Педиатр
Дж Педиатр
1998; 132:983-8; PMID: 9627590; http://dx.doi.org/10.1016/S0022-3476(98)70395-6 [PubMed] [Google Scholar]
20.
Тролльфорс Б., Рабо Э. Коклюш у взрослых. Br Med J (Clin Res Ed)
1981 год; 283:696-7; PMID: 6793129; http://dx.doi.org/10.1136/bmj.283.6293.696 [бесплатная статья PMC] [PubMed] [Google Scholar]
21.
Плоткин С.А., Оренштейн В., Оффит П.А., ред. Вакцины: Elsevier Saunders, 2013. [Google Scholar]
22.
Коди С.Л., Барафф Л.Дж., Черри Д.Д., Марси С.М., Манкларк Ч.Р. Характер и частота побочных реакций, связанных с иммунизацией АКДС и АКДС у младенцев и детей. Педиатрия
1981; 68:650-60; PMID:7031583 [PubMed] [Google Scholar]
23.
Jefferson T, Rudin M, DiPietrantonj C. Систематический обзор эффектов коклюшных вакцин у детей. вакцина
2003 г.; 21:2003-14; PMID: 12706690; http://dx.doi.org/10.1016/S0264-410X(02)00770-3 [PubMed] [Google Scholar]
24.
Gangarosa EJ, Galazka AM, Wolfe CR, Phillips LM, Gangarosa RE, Miller E, Chen RT. Влияние антивакцинных движений на борьбу с коклюшем: нерассказанная история. Ланцет
Ланцет
1998 год; 351:356-61; PMID: 9652634; http://dx.doi.org/10.1016/S0140-6736(97)04334-1 [PubMed] [Google Scholar]
25.
Уорд К.Н., Брайант Н.Дж., Эндрюс Н.Дж., Боули Дж.С., Орлинг А., Верити К.М., Росс Э.М., Миллер Э. Риск серьезных неврологических заболеваний после иммунизации детей младшего возраста в Великобритании и Ирландии. Педиатрия
2007 г.; 120:314-21; PMID: 17671057; http://dx.doi.org/10.1542/peds.2006-3743 [PubMed] [Google Scholar]
26.
Беркович С.Ф., Харкин Л., МакМахон Дж.М., Пелеканос Дж.Т., Зубери С.М., Виррелл Э.К., Гилл Д.С., Иона Х, Малли Д.С., Шеффер И.Е. Мутации de novo гена натриевого канала SCN1A при предполагаемой вакцинной энцефалопатии: ретроспективное исследование. Ланцет Нейрол
2006 г.; 5:488-92; PMID: 16713920; http://dx.doi.org/10.1016/S1474-4422(06)70446-X [PubMed] [Google Scholar]
27.
Рейес И.С., Се Д.Т., Ло Л.С., Уилфонг А.А. Предполагаемые случаи вакцинной энцефалопатии, повторно диагностированной годы спустя как синдром Драве. Педиатрия
Педиатрия
2011 г.; 128:e699-702; PMID: 21844054 [PubMed] [Google Scholar]
28.
Сато Ю., Кимура М., Фукуми Х. Разработка вакцины против коклюша в Японии. Ланцет
1984 год; 1:122-6; PMID: 6140441; http://dx.doi.org/10.1016/S0140-6736(84)
-8 [PubMed] [Google Scholar]
29.
Романус В., Йонселл Р., Бергквист С.О. Коклюш в Швеции после прекращения общей иммунизации в 1979 г. Pediatr Infect Dis J
1987 год; 6:364-71; PMID: 3588110; http://dx.doi.org/10.1097/00006454-198704000-00005 [PubMed] [Google Scholar]
30.
Эдвардс К.М., Мид Б.Д., Декер М.Д., Рид Г.Ф., Реннелс М.Б., Стейнхофф М.С., Андерсон Э.Л., Инглунд Дж.А., Пичичеро М.Э., Делориа М.А. Сравнение 13 бесклеточных коклюшных вакцин: обзор и серологический ответ. Педиатрия
1995 год; 96:548-57; PMID:7659475 [PubMed] [Google Scholar]
31.
Нобл Г.Р., Бернье Р.Х., Эсбер Э.К., Харград М.С., Хинман А.Р., Кляйн Д., Саах А.Дж. Бесклеточные и цельноклеточные вакцины против коклюша в Японии. Отчет о визите ученых США. ДЖАМА
ДЖАМА
1987 год; 257:1351-6; PMID: 3820444; http://dx.doi.org/10.1001/jama.1987.033
089032 [PubMed] [Google Scholar]
32.
Специальная группа по изучению коклюшных вакцин. Плацебо-контролируемое исследование двух бесклеточных коклюшных вакцин в Швеции – защитная эффективность и побочные эффекты. Ланцет
1988; 1:955-60; PMID: 2896826 [PubMed] [Google Scholar]
33.
Кранц И., Секура Р., Тролльфорс Б., Тарангер Дж., Закриссон Г., Лагергорд Т., Шнеерсон Р., Роббинс Дж. Иммуногенность и безопасность коклюшной вакцины, состоящей из коклюшного токсина, инактивированного перекисью водорода, у детей в возрасте от 18 до 23 месяцев. . Дж Педиатр
1990 г.; 116:539-43; PMID: 2319400; http://dx.doi.org/10.1016/S0022-3476(05)81599-9 [PubMed] [Google Scholar]
34.
Исаксон Дж., Тролльфорс Б., Тарангер Дж., МакДауэлл И., Йоханссон Дж., Лагергорд Т., Роббинс Дж.Б. Безопасность, иммуногенность и открытое ретроспективное исследование эффективности монокомпонентной вакцины против коклюша у детей раннего возраста. Педиатр Infect Dis J
Педиатр Infect Dis J
1994; 13:22-7; PMID:8170728; http://dx.doi.org/10.1097/00006454-199401000-00006 [PubMed] [Google Scholar]
35.
Тролльфорс Б., Тарангер Дж., Лагергард Т., Линд Л., Сунд В., Закриссон Г., Лоу К.У., Блэквелдер В., Роббинс Д.Б. Плацебо-контролируемое исследование вакцины против коклюша. N Engl J Med
1995 год; 333:1045-50; PMID: 7675047; http://dx.doi.org/10.1056/NEJM199510193331604 [PubMed] [Google Scholar]
36.
Storsaeter J, Hallander H, Farrington CP, Olin P, Möllby R, Miller E. Вторичный анализ эффективности двух бесклеточных коклюшных вакцин, оцененных в шведском испытании фазы III. вакцина
1990; 8:457-61; PMID: 2251872; http://dx.doi.org/10.1016/0264-410X(90)
-I [PubMed] [Google Scholar]
37.
Греко Д., Салмасо С., Мастрантонио П., Джулиано М., Тоцци А.Е., Анемона А., Чиофи дельи Атти М.Л., Джамманко А., Паней П., Блэквелдер В.К. и др.; Рабочая группа Progetto Pertosse. Контролируемое испытание двух бесклеточных вакцин и одной цельноклеточной вакцины против коклюша.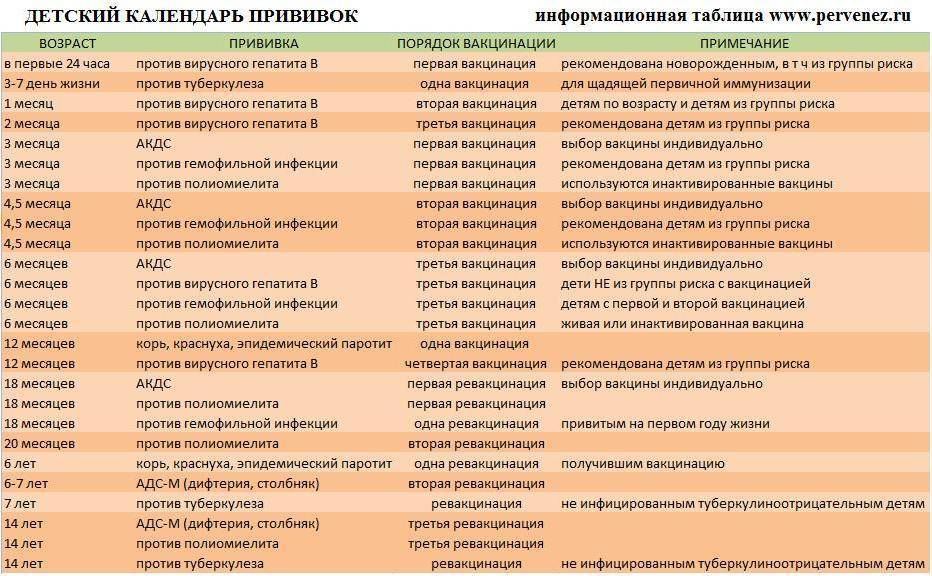 N Engl J Med
N Engl J Med
1996 год; 334:341-8; PMID: 8538704; http://dx.doi.org/10.1056/NEJM199602083340601 [PubMed] [Google Scholar]
38.
Gustafsson L, Hallander HO, Olin P, Reizenstein E, Storsaeter J. Контролируемое испытание двухкомпонентной бесклеточной, пятикомпонентной бесклеточной и цельноклеточной коклюшной вакцины. N Engl J Med
1996 год; 334:349-55; PMID: 8538705; http://dx.doi.org/10.1056/NEJM199602083340602 [PubMed] [Google Scholar]
39.
Эдвардс К.М., Декер М.Д. Бесклеточные коклюшные вакцины для детей раннего возраста. N Engl J Med
1996 год; 334:391-2; PMID: 8538712; http://dx.doi.org/10.1056/NEJM1-99602083340609 [PubMed] [Google Scholar]
40.
Hallander HO, Gustafsson L. Эффективность и действенность бесклеточных коклюшных вакцин: 20-летний опыт Швеции. Вакцины Expert Rev
2009 г.; 8:1303-7; PMID: 19803750; http://dx.doi.org/10.1586/erv.09.88 [PubMed] [Google Scholar]
41.
Черри Джей Ди. Почему вакцины против коклюша неэффективны?
Педиатрия
2012 г.; 129:968-70; PMID: 22529282; http://dx. doi.org/10.1542/peds.2011-2594 [PubMed] [Google Scholar]
doi.org/10.1542/peds.2011-2594 [PubMed] [Google Scholar]
42.
Плоткин С.А. Проблема коклюша. Клин заразить Dis
2014; 58:830-3; PMID: 24363332; http://dx.doi.org/10.1093/cid/cit934 [PubMed] [Google Scholar]
43.
Вакцинация против коклюша: использование бесклеточных коклюшных вакцин среди младенцев и детей младшего возраста. Рекомендации Консультативного комитета по практике иммунизации (ACIP). Представитель MMWR по рекомендациям
1997 год; 46(RR-7):1-25; PMID:9091780 [PubMed] [Google Scholar]
44.
Вакцинация против коклюша: бесклеточная коклюшная вакцина для четвертой и пятой доз серии АКДС обновлена до дополнительного заявления ACIP. Рекомендации Консультативного комитета по практике иммунизации (ACIP). Представитель MMWR по рекомендациям
1992; 41(RR-15):1-5; PMID:1406564 [PubMed] [Google Scholar]
45.
Бродер К.Р., Кортезе М.М., Искандер Дж.К., Крецингер К., Слэйд Б.А., Браун К.Х., Мияльский С.М., Тивари Т., Уэстон Э.Дж., Кон А.С. и др.; Консультативный комитет по практике иммунизации (ACIP). Профилактика столбняка, дифтерии и коклюша среди подростков: рекомендации по использованию столбнячного анатоксина, редуцированного дифтерийного анатоксина и бесклеточной коклюшной вакцины Консультативного комитета по практике иммунизации (ACIP). Представитель MMWR по рекомендациям
Профилактика столбняка, дифтерии и коклюша среди подростков: рекомендации по использованию столбнячного анатоксина, редуцированного дифтерийного анатоксина и бесклеточной коклюшной вакцины Консультативного комитета по практике иммунизации (ACIP). Представитель MMWR по рекомендациям
2006 г.; 55(RR-3):1-34; PMID:16557217 [PubMed] [Google Scholar]
46.
Уэстон В.М., Кляйн Н.П. Кинрикс: новая комбинированная вакцина DTaP-IPV для детей в возрасте 4–6 лет. Вакцины Expert Rev
2008 г.; 7:1309-20; PMID: 18980534; http://dx.doi.org/10.1586/14760584.7.9.1309 [PubMed] [Google Scholar]
47.
Центры по контролю и профилактике заболеваний (CDC). Лицензия FDA на дифтерийно-столбнячный анатоксин и адсорбированную бесклеточную коклюшную вакцину, комбинированную вакцину против гепатита В (рекомбинантную) и полиовирусную вакцину (PEDIARIX) для использования у младенцев. MMWR Morb Mortal Wkly Rep
2003 г.; 52:203-4; PMID:12653460 [PubMed] [Google Scholar]
48.
Герра Ф.А., Блаттер М.М., Гринберг Д. П., Пичичеро М., Норьега Ф.Р.; Исследовательская группа Pentacel. Безопасность и иммуногенность пентавалентной вакцины по сравнению с раздельным введением лицензированных эквивалентных вакцин у младенцев и детей ясельного возраста в США и сохранение антител до дошкольной бустерной дозы: рандомизированное клиническое исследование. Педиатрия
П., Пичичеро М., Норьега Ф.Р.; Исследовательская группа Pentacel. Безопасность и иммуногенность пентавалентной вакцины по сравнению с раздельным введением лицензированных эквивалентных вакцин у младенцев и детей ясельного возраста в США и сохранение антител до дошкольной бустерной дозы: рандомизированное клиническое исследование. Педиатрия
2009 г.; 123:301-12; PMID: 19117896; http://dx.doi.org/10.1542/peds.2007-3317 [PubMed] [Google Scholar]
49.
Yeh SH, Ward JI, Partridge S, Marcy SM, Lee H, Jing J, Curry ES, Howe BJ. Безопасность и иммуногенность пятивалентной комбинированной вакцины против дифтерии, столбняка, коклюша, гепатита В и полиомиелита у детей раннего возраста. Педиатр Infect Dis J
2001 г.; 20:973-80; PMID: 11642632; http://dx.doi.org/10.1097/00006454-200110000-00011 [PubMed] [Google Scholar]
50.
Dennehy PH, Bertrand HR, Silas PE, Damaso S, Friedland LR, Abu-Elyazed R. Совместное введение пероральной человеческой ротавирусной вакцины RIX4414 не влияет на иммунный ответ на антигены, содержащиеся в обычных детских вакцинах в Соединенных Штатах. Педиатрия
Педиатрия
2008 г.; 122:e1062-6; PMID: 18977955; http://dx.doi.org/10.1542/peds.2008-1059 [PubMed] [Google Scholar]
51.
DAPTACEL (Адсорбированная вакцина против дифтерии и столбняка и бесклеточная коклюшная вакцина) Вкладыш в упаковку. Санофи Пастер, 2002. [Google Scholar]
52.
Klein NP, Reisinger KS, Johnston W, Odrljin T, Gill CJ, Bedell L, Dull P. Безопасность и иммуногенность новой четырехвалентной менингококковой CRM-конъюгированной вакцины, вводимой одновременно с плановыми прививками у младенцев. Педиатр Infect Dis J
2012 г.; 31:64-71; PMID: 22094635; http://dx.doi.org/10.1097/INF.0b0-13e31823dce5c [PubMed] [Google Scholar]
53.
Кляйн Н.П., Уэстон В.М., Куриякосе С., Колхе Д., Хоу Б., Фридланд Л.Р., Ван Дер Меерен О. Открытое, рандомизированное, многоцентровое исследование иммуногенности и безопасности DTaP-IPV (Kinrix™) при совместном введении с вакциной MMR с вакциной против ветряной оспы или без нее у здоровых детей дошкольного возраста. вакцина
2012 г. ; 30:668-74; PMID: 22064267; http://dx.doi.org/10.1016/j.vaccine.2011.10.065 [PubMed] [Google Scholar]
; 30:668-74; PMID: 22064267; http://dx.doi.org/10.1016/j.vaccine.2011.10.065 [PubMed] [Google Scholar]
54.
Брайант К.А., Гуртман А., Гирдженти Д., Райзингер К., Джонсон А., Прайд М.В., Паттерсон С., Девлин С., Грубер В.К., Эмини Э.А. и др..
Реакция антител на обычные педиатрические вакцины, вводимые 13-валентной пневмококковой конъюгированной вакциной. Педиатр Infect Dis J
2013; 32:383-8; PMID: 23104129; http://dx.doi.org/10.1097/INF.0b013e318279e9a9 [PubMed] [Google Scholar]
55.
Салмасо С., Мастрантонио П., Вассилак С.Г., Джулиано М., Анемона А., Джамманко А., Тоцци А.Е., Чиофи дельи Атти М.Л., Греко Д.; Рабочая группа II этапа. Стойкость защиты до 33-месячного возраста обеспечивается иммунизацией в младенчестве двумя трехкомпонентными бесклеточными коклюшными вакцинами. вакцина
1998; 16:1270-5; PMID: 9682390; http://dx.doi.org/10.1016/S0264-410X(98)00040-1 [PubMed] [Google Scholar]
56.
Салмасо С., Мастрантонио П., Тоцци А.Е., Стефанелли П., Анемона А., Чиофи М. Л., Джамманко А.; Рабочая группа III этапа. Устойчивая эффективность в течение первых 6 лет жизни трехкомпонентных бесклеточных коклюшных вакцин, вводимых в младенчестве: опыт Италии. Педиатрия
Л., Джамманко А.; Рабочая группа III этапа. Устойчивая эффективность в течение первых 6 лет жизни трехкомпонентных бесклеточных коклюшных вакцин, вводимых в младенчестве: опыт Италии. Педиатрия
2001 г.; 108:Е81; PMID: 11694665; http://dx.doi.org/10.1542/peds.108.5.e81 [PubMed] [Google Scholar]
57.
Куинн Х.Э., Снеллинг Т.Л., Макартни К.К., Макинтайр П.Б. Продолжительность защиты после первой дозы бесклеточной коклюшной вакцины у детей раннего возраста. Педиатрия
2014; 133:e513-9; PMID: 24515514; http://dx.doi.org/10.1542/peds.2013-3181 [PubMed] [Google Scholar]
58.
Olin P, Gustafsson L, Barreto L, Hessel L, Mast TC, Rie AV, Bogaerts H, Storsaeter J. Снижение заболеваемости коклюшем в Швеции после введения бесклеточной коклюшной вакцины. вакцина
2003 г.; 21:2015-21; PMID: 12706691; http://dx.doi.org/10.1016/S0264-410X(02)00777-6 [PubMed] [Google Scholar]
59.
Густафссон Л., Хессель Л., Сторсетер Дж., Олин П. Длительное наблюдение за шведскими детьми, вакцинированными бесклеточными коклюшными вакцинами в возрасте 3, 5 и 12 месяцев, указывает на необходимость ревакцинации в возрасте от 5 до 7 лет. . Педиатрия
. Педиатрия
2006 г.; 118:978-84; PMID: 16950988; http://dx.doi.org/10.1542/peds.2005-2746 [PubMed] [Google Scholar]
60.
Викерс Д., Росс А.Г., Майнар-Хайме Р.К., Нойдорф С., Шах С. Программы вакцинации против коклюша цельноклеточными и бесклеточными и заболеваемость коклюшем среди младенцев и детей младшего возраста. CMAJ
2006 г.; 175:1213-7; PMID: 17098950; http://dx.doi.org/10.1503/cmaj.051637 [бесплатная статья PMC] [PubMed] [Google Scholar]
61.
Беттингер Дж.А., Гальперин С.А., Де Серрес Г., Шайфеле Д.В., Тэм Т. Влияние перехода от цельноклеточной коклюшной вакцины к бесклеточной на эпидемиологию госпитализированных детей с коклюшем в Канаде. Педиатр Infect Dis J
2007 г.; 26:31-5; PMID:17195702; http://dx.doi.org/10.1097/01.inf.0000247055.81541.04 [PubMed] [Google Scholar]
62.
Лавин Дж., Броутин Х., Харвилл Э.Т., Бьорнстад О.Н. Несовершенный вакцино-индуцированный иммунитет и передача коклюша младенцам. вакцина
2010 г.; 29:11-6; PMID: 21034823; http://dx.doi. org/10.1016/j.vaccine.2010.10.029 [бесплатная статья PMC] [PubMed] [Google Scholar]
org/10.1016/j.vaccine.2010.10.029 [бесплатная статья PMC] [PubMed] [Google Scholar]
63.
Вендельбо А.М., Ван Ри А., Салмасо С., Инглунд Дж.А. Длительность иммунитета против коклюша после естественного заражения или вакцинации. Педиатр Infect Dis J
2005 г.; 24 (прил.): S58-61; PMID:15876927; http://dx.doi.org/10.1097/01.inf.0000160914.59160.41 [PubMed] [Google Scholar]
64.
Хан Ф.Н., Лин М., Хинкль С.Дж., Франклин П., Лютер Р., Вудрафф Ф., Хенсон К., Люкенбилл М., Гутьеррес М., Чжу Б.П. Изучение анамнеза прививок методом «случай-контроль» в отношении риска коклюша во время вспышки среди школьников. Педиатр Infect Dis J
2006 г.; 25:1132-6; PMID: 17133158; http://dx.doi.org/10.1097/01.inf.0000245099.01427.93 [PubMed] [Google Scholar]
65.
Klein NP, Bartlett J, Rowhani-Rahbar A, Fireman B, Baxter R. Снижение защиты после пятой дозы бесклеточной коклюшной вакцины у детей. N Engl J Med
2012 г.; 367:1012-9; PMID: 22970945; http://dx.doi.org/10.1056/NEJMoa1200850 [PubMed] [Google Scholar]
66.
Misegades LK, Winter K, Harriman K, Talarico J, Messonnier NE, Clark TA, Martin SW. Ассоциация детского коклюша с получением 5 доз коклюшной вакцины по времени с момента последней дозы вакцины, Калифорния, 2010 г. JAMA
2012 г.; 308:2126-32; PMID: 23188029; http://dx.doi.org/10.1001/jama.2012.14939 [PubMed] [Google Scholar]
67.
Витт М.А., Кац П.Х., Витт Д.Дж. Неожиданно ограниченная стойкость иммунитета после бесклеточной вакцинации против коклюша у подростков во время вспышки в Северной Америке. Клин заразить Dis
2012 г.; 54:1730-5; PMID: 22423127; http://dx.doi.org/10.1093/cid/cis287 [PubMed] [Google Scholar]
68.
Tartof SY, Lewis M, Kenyon C, White K, Osborn A, Liko J, Zell E, Martin S, Messonnier NE, Clark TA и др..
Снижение иммунитета к коклюшу после 5 доз DTaP. Педиатрия
2013; 131:e1047-52; PMID: 23478868; http://dx.doi.org/10.1542/peds.2012-1928 [PubMed] [Google Scholar]
69.
Кляйн Н.П., Бартлетт Дж., Пожарный Б., Роухани-Рахбар А., Бакстер Р.
Сравнительная эффективность бесклеточных и цельноклеточных коклюшных вакцин у подростков.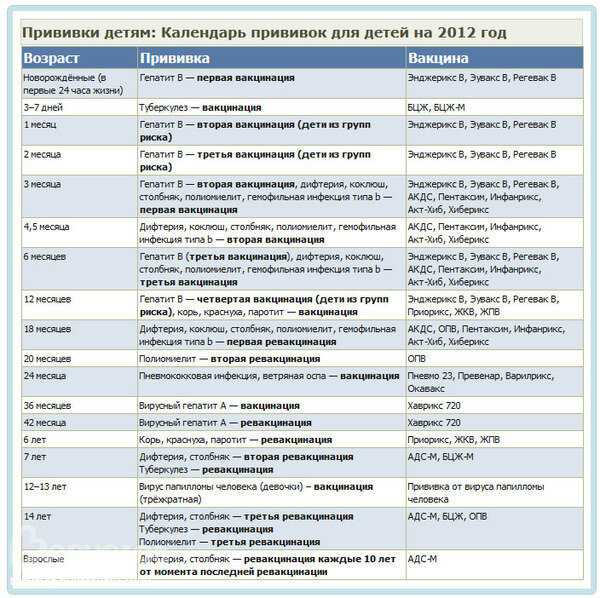 Педиатрия
Педиатрия
2013; 131:e1716-22. [PubMed] [Академия Google]
70.
Шеридан С.Л., Уэр Р.С., Гримвуд К., Ламберт С.Б. Количество и порядок введения цельноклеточных коклюшных вакцин в младенчестве и защита от болезней. ДЖАМА
2012 г.; 308:454-6; PMID: 22851107; http://dx.doi.org/10.1001/jama.2012.6364 [PubMed] [Google Scholar]
71.
Лико Дж., Робисон С.Г., Чеслак П.Р. Праймирование цельноклеточной вакциной против бесклеточного коклюша. N Engl J Med
2013; 368:581-2; PMID: 23388023; http://dx.doi.org/10.1056/NEJMc1212006 [PubMed] [Google Scholar]
72.
Центры по контролю и профилактике заболеваний (CDC). Обновленные рекомендации по использованию противостолбнячного анатоксина, редуцированного дифтерийного анатоксина и бесклеточной коклюшной вакцины (Tdap) у беременных женщин — Консультативный комитет по практике иммунизации (ACIP), 2012 г. MMWR Morb Mortal Wkly Rep
2013; 62:131-5; PMID: 23425962 [Бесплатная статья PMC] [PubMed] [Google Scholar]
73.
Бакстер Р., Бартлетт Дж. , Роухани-Рахбар А., Пожарный Б., Кляйн Н.П. Эффективность коклюшных вакцин для подростков и взрослых: исследование случай-контроль. БМЖ
, Роухани-Рахбар А., Пожарный Б., Кляйн Н.П. Эффективность коклюшных вакцин для подростков и взрослых: исследование случай-контроль. БМЖ
2013; 347:f4249; PMID: 23873919; http://dx.doi.org/10.1136/bmj.f4249 [PubMed] [Google Scholar]
Детская вакцина АКДС может обеспечивать перекрестный иммунитет к COVID-19
- Скачать PDF Копия
Автор Susha Cheriyedath, M.Sc.17 ноября 2020 г.
Количество случаев COVID-19 и их тяжесть сильно различаются в разных странах. COVID-19 также различается у разных людей в зависимости от таких факторов, как возраст, пол и сопутствующие заболевания. Однако фактором с наибольшей корреляцией между случаями и тяжестью COVID-19 является возраст. Исследования показали, что SARS-CoV-2 особенно опасен для пожилых людей, в то время как дети сравнительно менее подвержены влиянию вируса.
Большинство смертельных исходов от COVID-19 приходится на пожилых людей, при этом 90% жертв старше 70 лет, в то время как детское население в основном не поражается COVID-19. Хотя ожидается более значительное воздействие COVID-19 на пожилых людей, поскольку их иммунный ответ ослабевает с возрастом, вирулентность вируса, по-видимому, связана с непропорциональным иммунным ответом, и некоторым пациентам, по-видимому, помогают иммуномодулирующие препараты. Кроме того, неясно, как новорожденные и младенцы с незрелой адаптивной иммунной системой относительно защищены от COVID-19..
Хотя ожидается более значительное воздействие COVID-19 на пожилых людей, поскольку их иммунный ответ ослабевает с возрастом, вирулентность вируса, по-видимому, связана с непропорциональным иммунным ответом, и некоторым пациентам, по-видимому, помогают иммуномодулирующие препараты. Кроме того, неясно, как новорожденные и младенцы с незрелой адаптивной иммунной системой относительно защищены от COVID-19..
Изучение роли перекрестно-реактивного иммунитета от детских прививок в защите от COVID-19
Доцент Педро А. Рече с кафедры иммунологии и медицинского факультета Мадридского университета Комплутенсе, Испания, недавно исследовал потенциальную роль за счет перекрестно-реактивного иммунитета, полученного в результате вакцинации детей и воздействия других патогенов человека для защиты от COVID-19. Профессор Реш собрал пептиды, соответствующие SARS-CoV-2 в протеомах 25 патогенов человека и в антигенах вакцин. Они предсказали Т- и В-клеточную реактивность этих антигенов для выявления возможных перекрестно-реактивных эпитопов. Исследование опубликовано в журнале Границы иммунологии .
Исследование опубликовано в журнале Границы иммунологии .
Исследование: Потенциальный перекрестно-реактивный иммунитет к SARS-CoV-2 от обычных человеческих патогенов и вакцин. Изображение предоставлено: Катерина Кон / Shutterstock
Он обнаружил, что вирусы, подлежащие детской вакцинации, не имеют перекрестно-реактивных эпитопов для SARS-CoV-2, что показывает, что они не могут обеспечить защиту от COVID-19. Точно так же распространенные вирусы, такие как респираторный вирус, риновирус, вирус гриппа и некоторые вирусы герпеса, также являются плохими источниками перекрестно-реактивного иммунитета против SARS-CoV-2. Это доказывает, что иммунологическая память против этих вирусов не может играть защитную роль при COVID-19.. Однако Реш обнаружил, что комбинированные вакцины, такие как вакцина АКДС, используемые для лечения инфекционных заболеваний, дифтерии, столбняка и коклюша, могут быть значительными источниками перекрестно-реактивного иммунитета к SARS-CoV-2.
Решающая связь между вакцинацией АКДС и эпидемиологией COVID-19
Похожие статьи
- Здоровье матерей, плодов и детей зависит от материнской среды дети 8 или младше
- Тестирование ADOS не требуется для диагностики РАС педиатрами, специализирующимися на поведенческих исследованиях развития
Перекрестно-реактивные эпитопы DTP с SARS-CoV-2 включают большое количество эпитопов CD8 и CD4 T-клеток с широким охватом защиты и потенциально нейтрализующими эпитопами B-клеток при SARS -КоВ-2 S-белок. Во всем мире дети получают множественные прививки АКДС, в том числе 3–4 дозы в первый год жизни и 1 дозу в возрасте 4–6 лет. Ревакцинацию с низким содержанием антигена, называемую Tdap, также делают в 9 лет.–14 лет. Таким образом, дети могут быть защищены от SARS-CoV-2 за счет перекрестного реактивного иммунитета, обеспечиваемого этими множественными прививками АКДС.
«Эти результаты показывают, что перекрестный иммунитет, вызванный антигенами DT в комбинированных вакцинах DTP, вероятно, защищает детей и самых маленьких от COVID-19 во всем мире».
Результаты также показали, что вакцины MenB могут индуцировать значительный перекрестно-реактивный Т-клеточный иммунитет к SARS-CoV-2. Однако маловероятно, что они защитят детей от SARS-CoV-2, потому что вакцины против менингококка B были внедрены совсем недавно, да и то не везде. Напротив, комбинированные вакцины АКДС широко доступны по всему миру с 19 века.40с.
Тяжесть течения COVID-19 в разных странах может быть связана с различиями в их программах вакцинации АКДС
По словам профессора Рече, эти данные указывают на то, что перекрестный реактивный иммунитет, обеспечиваемый комбинированными вакцинами АКДС, вероятно, является причиной относительной безопасности детей от COVID-19 по всему миру. Этот перекрестно-реактивный иммунитет со временем ослабевает у взрослых, что объясняет, почему случаи COVID-19 и их тяжесть увеличиваются с возрастом.
«Перекрестно-реактивный иммунитет, вызванный вакцинами АКДС, со временем ослабнет, что объясняет, почему COVID-19случаи и степень тяжести увеличивается с возрастом».
Глобальный кризис в области здравоохранения, вызванный пандемией COVID-19, побудил к огромным глобальным усилиям по разработке эффективной вакцины против SARS-CoV-2, на создание которой, вероятно, потребуются годы. Однако эти результаты свидетельствуют о том, что вакцинация АКДС, в частности вакцинация АКДС, может использоваться для защиты населения в целом от SARS-CoV-2 за счет использования перекрестно-реактивного иммунитета, вызываемого комбинированной вакциной.
Автор считает, что из-за гетерогенности вакцин АКДС COVID-19тяжесть и смертность в разных странах могут быть связаны с различиями в составе их вакцин АКДС и началом их программ вакцинации АКДС.
«Учитывая гетерогенность вакцин АКДС, наши результаты также показывают, что уровень смертности от COVID-19 и тяжесть течения в разных странах могут быть связаны с различиями в составе вакцин АКДС, схемами вакцинации и началом программ вакцинации АКДС».
Номер журнала:
- Рече Педро А.
 , Потенциальный перекрестно-реактивный иммунитет к SARS-CoV-2 от обычных человеческих патогенов и вакцин, Frontiers in Immunology, DOI=10.3389/fimmu.2020.586984, https://www.frontiersin.org/articles/ 10.3389/fimmu.2020.586984/полный
, Потенциальный перекрестно-реактивный иммунитет к SARS-CoV-2 от обычных человеческих патогенов и вакцин, Frontiers in Immunology, DOI=10.3389/fimmu.2020.586984, https://www.frontiersin.org/articles/ 10.3389/fimmu.2020.586984/полный
Опубликовано в: Новости здоровья детей | Новости медицинских исследований | Новости болезней/инфекций
Теги: В-клетка, CD4, Клетка, Дети, Коронавирусная болезнь COVID-19, Дифтерия, Наркотики, Эпидемиология, Глобальное здоровье, Иммунный ответ, Иммунология, Иммуномодулирующие, Инфекционные заболевания, Грипп, Медицина, Смертность, Пандемия, Коклюш, коклюш (коклюш), белок, исследования, респираторные заболевания, респираторный вирус, риновирус, SARS-CoV-2, Т-клетки, столбняк, вакцина, вирус
Комментарии (0)
- Скачать PDF Копировать
Используйте один из следующих форматов для ссылки на эту статью в своем эссе, статье или отчете:
APA
Cheriyedath, Susha.


/90/90.jpg)
 , Потенциальный перекрестно-реактивный иммунитет к SARS-CoV-2 от обычных человеческих патогенов и вакцин, Frontiers in Immunology, DOI=10.3389/fimmu.2020.586984, https://www.frontiersin.org/articles/ 10.3389/fimmu.2020.586984/полный
, Потенциальный перекрестно-реактивный иммунитет к SARS-CoV-2 от обычных человеческих патогенов и вакцин, Frontiers in Immunology, DOI=10.3389/fimmu.2020.586984, https://www.frontiersin.org/articles/ 10.3389/fimmu.2020.586984/полный