Содержание
Прививка адсм взрослым — побочные эффекты и противопоказания — шоубизнес и мода
Вакцина АДС-М – частный вариант прививки АКДС, содержащей компонент против коклюша. АДСМ применяется для возобновления и продления действия защитных сил организма, сформированных во время предыдущей активной иммунопрофилактики. Прививка АДСМ взрослым применяется как превентивная мера борьбы с серьезными заболеваниями. Бивалентность вакцины позволяет создавать устойчивость организма к нескольким возбудителям за один укол. В отличие от моновалентных, препарат помогает снизить побочные эффекты от многократного введения балластных веществ в тело человека.
Что такое прививка АДСМ
Расшифровка прививки АДСМ – анатоксин дифтерийно-столбнячный в малых дозах. От чего прививка: вакцина содержит достаточную для активизации иммунных процессов дозировку компонентов для устойчивого иммунитета к дифтерии и столбняку. Инфекции такого типа представляют большую опасность для человека – по причине отсутствия эффективных методов борьбы с ними.
Учитывайте, сколько действует прививка от столбняка и дифтерии. Активность защитного механизма, вследствие применения вакцинного препарата продолжается 10 лет, а для ее продления требуется проводить ревакцинацию. Заразиться дифтерией или столбняком можно при любых обстоятельствах. Группу риска составляют люди:
- занятые сельским хозяйством;
работающие в строительстве;
не проходившие ранее программу активной иммунопрофилактики.
- Как назвать щенка-мальчика
Апноэ — что это такое, лечение синдрома. Симптомы и причины апноэ и как лечить.
Прическа водопад с пошаговым плетением
Инструкция по применению вакцины АДСМ
Профилактика дифтерии и столбняка осуществляется только индивидуальными инструментами, которые сразу после введения инъекции должны утилизироваться. Вакцина производится в жидком виде и поставляется в ампулах или одноразовых шприцах. Достоинством последних является полное отсутствие консервантов, что помогает облегчить реакцию организма на препарат. Дифтерийный анатоксин в ампулах или уколах должен храниться в холодильнике.
Достоинством последних является полное отсутствие консервантов, что помогает облегчить реакцию организма на препарат. Дифтерийный анатоксин в ампулах или уколах должен храниться в холодильнике.
Для большого количества препарата характерно наличие вещества, угнетающего развитие микроорганизмов – ртутного соединения. Иммунопрофилактика прививкой АДСМ взрослым требует некоторой подготовки в виде очищения кишечника и временного ограничения количества потребляемой пищи. Рекомендуется придерживаться таких ограничительных мер пару дней до и после вакцинации.
Когда делают прививку от дифтерии и столбняка взрослым
Срок действия прививки составляет 10 лет, после чего нужно ревакцинироваться. Верхней возрастной границы иммунопрофилактики не существует. Рекомендуется делать прививку АДСМ взрослым вплоть до самых преклонных лет. Если человек пропустил очередную ревакцинацию, но не прошло больше 20 лет с момента введения последней прививки АДСМ, то для активации иммунитета вводится всего один укол от столбняка и дифтерии. Согласно установленному графику при условии наличия прививки АКДС вакцина АДСМ вводится в следующие сроки:
Согласно установленному графику при условии наличия прививки АКДС вакцина АДСМ вводится в следующие сроки:
Возраст
№ ревакцинации (r)
6-8 лет
r 2
14-16 лет
r 3
24-26 лет
r 4
Последующие этапы ревакцинации необходимо проходить с периодичностью в 10 лет
- Как выглядит грибок на ногах — стопах и ногтях
Лечение лекарственными препаратами поджелудочной железы при симптомах заболеваний
Жаркое по-домашнему из свинины без лука
Куда делают прививку
Адсорбированный дифтерийно-столбнячный анатоксин предполагает внутримышечное введение вакцины. Быстрое поступление состава в кровь вызовет активную реакцию иммунных клеток, что приведет к уничтожению активных компонентов прививки. В мышце же вакцина создает себе базу, с которой происходит медленное высвобождение препарата в кровь с формированием невосприимчивости к инфекциям. Для обеспечения внутримышечного введения АДСМ прививать пациентов рекомендуется:
В мышце же вакцина создает себе базу, с которой происходит медленное высвобождение препарата в кровь с формированием невосприимчивости к инфекциям. Для обеспечения внутримышечного введения АДСМ прививать пациентов рекомендуется:
- в бедро;
в плечо;
под лопатку.
Противопоказания
Прививка АДСМ относится к числу легких вакцин, но существуют некоторые ограничения при ее осуществлении. Перед проведением иммунопрофилактики врач должен обязательно измерить температуру и осмотреть горло пациента, независимо, ребенок это или старый человек. Любые воспалительные явления в период вакцинации являются противопоказанием для ее проведения. При острых формах иммунодефицита прививка используется только после положительного заключения врачебной комиссии. Иммунопрофилактические мероприятия могут откладываться по следующим причинам:
беременность;
иммунодефицит;
острая форма любой болезни;
аллергия;
Побочные эффекты и последствия вакцинации
Вакцина АДСМ может приводить к легкой или тяжелой реакции организма на препарат. Болевой синдром в области введения инъекции, образование уплотнения являются нормальными проявлениями иммунопрофилактики. Слабая либо сильная реактогенность прививки не является патологией и не исключает проведение последующих вакцинаций. Побочные эффекты и осложнения после прививки:
Болевой синдром в области введения инъекции, образование уплотнения являются нормальными проявлениями иммунопрофилактики. Слабая либо сильная реактогенность прививки не является патологией и не исключает проведение последующих вакцинаций. Побочные эффекты и осложнения после прививки:
- рвота;
температура;
снижение нервной активности;
расстройство пищеварения;
упадок сил;
анафилактический шок;
менингит;
энцефалит.
Отзывы о прививке АДС-М
Елена, 26 лет
Проходила очередную вакцинацию согласно установленному календарю прививок. Спустя несколько дней после инъекции пошел тяжелейший «откат» у организма. Последствия введения: проявилась накопительная аллергическая реакция на препарат, кожные покровы «усеяла» крапивница. Пришлось вызывать скорую и ставить супрастиновую капельницу.
Ольга, 30 лет
Дочке требовалась ревакцинация, на очереди находилась прививка r3 АДСМ в 14 лет плюс инъекция от полиомиелита. Использование сразу 2 препаратов не спровоцировало особых побочных эффектов у ребенка. Общая слабость и невысокая температура – основные последствия ревакцинации.
Использование сразу 2 препаратов не спровоцировало особых побочных эффектов у ребенка. Общая слабость и невысокая температура – основные последствия ревакцинации.
Марина, 25 лет
В прошлом году решила сделать прививку АДСМ как профилактику дифтерии и столбняка. Организм самым ужасным образом отреагировал на компоненты вакцины: непрекращающаяся рвота, мышечные спазмы, головная боль. Шишка не проходила долгое время и постоянно гноилась, мыться поэтому строго запрещалось.
Внимание! Информация, представленная в статье, носит ознакомительный характер. Материалы статьи не призывают к самостоятельному лечению. Только квалифицированный врач может поставить диагноз и дать рекомендации по лечению, исходя из индивидуальных особенностей конкретного пациента.
Источник: sovets.net
расшифровка, побочные эффекты, осложнения и противопоказания прививки адсм у детей и взрослых
Инфекционные заболевания — болезни, поражающие организм взрослого и ребёнка.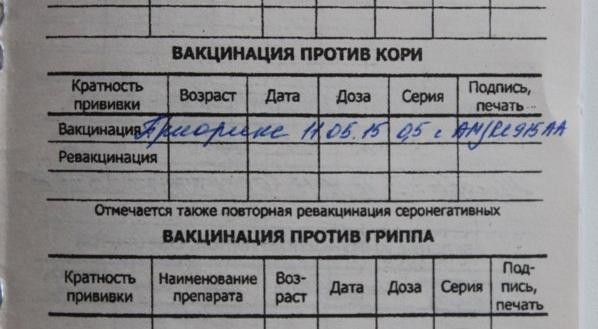 Оградить свою жизнь от тяжёлых болезней и летальных исходов может медицинская процедура — вакцинация. В графике прививания у детей в возрасте до 2 лет важное значение отводится прививке, блокирующей болезни: столбняк, дифтерию, коклюш (АКДС).
Оградить свою жизнь от тяжёлых болезней и летальных исходов может медицинская процедура — вакцинация. В графике прививания у детей в возрасте до 2 лет важное значение отводится прививке, блокирующей болезни: столбняк, дифтерию, коклюш (АКДС).
АКДС — вакцина идентичная по структуре АДСМ. Вакцина малой дозировки отличается от АКДС отсутствием компонента против коклюша. Введение комбинированного препарата АДСМ блокирует вирусные клетки, ограждая организм взрослого и ребёнка от опасных вирусных и инфекционных заболеваний.
Предназначение вакцины АДСМ
Расшифровка прививки АДСМ:
- А — адсорбированная
- Д — дифтерийно
- С — столбнячная
- М — малой дозы.
Вакцина выступает современным медицинским заменителем прививки АКДС. Адсорбированный коклюшно-дифтерийно-столбнячный заменитель вводится пациентам, у которых замечена неблагоприятная реакция на компонент «коклюш».
АДС в малой дозировке предназначена для повторных введений препарата, цель которого: активировать иммунитет или продлить его срок защиты от смертельных заболеваний — дифтерии, коклюша, столбняка.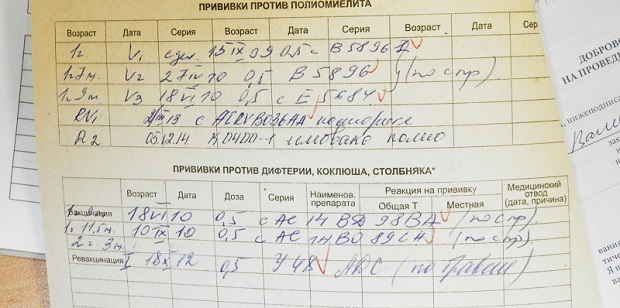 К ревакцинации подлежит группа людей старше 4 лет. Начиная с этого возраста, клетки коклюша стабилизируются и приравнивают шанс смертельного исхода к нулю. В состав препарата входят половина дозы анатоксинов столбняка и дифтерии.
К ревакцинации подлежит группа людей старше 4 лет. Начиная с этого возраста, клетки коклюша стабилизируются и приравнивают шанс смертельного исхода к нулю. В состав препарата входят половина дозы анатоксинов столбняка и дифтерии.
Непривитые дети возрастом до года при столкновении с паразитарными клетками коклюша молниеносно подхватывают заболевание. В таком случае редко что можно исправить, поскольку болезнь протекает молниеносно и приводит к гибели ребёнка.
К группе риска стоит отнести и взрослых людей, занятость или работоспособность которых связана с сельским хозяйством, строительством, отсутствием стартовой иммунопрофилактики.
Ревакцинация адсорбированным ДС препаратом охватывает не только детей возрастом до 14 лет, но и взрослых. Вакцина ставится каждые 10 лет людям, страдающими непереносимостью АКДС и АДС. При прохождении плановой прививки пациентам предлагают выбрать несколько вариантов ревакцинации:
При прохождении плановой прививки пациентам предлагают выбрать несколько вариантов ревакцинации:
- Отечественная адсорбированная коклюшно-дифтерийно-столбнячная.
- Зарубежная Imovax «D. T. Adult». Импортная вакцина после внутримышечного введения не вызывает побочных реакций и осложнений.
- Одновалентное привитие, направленное против болезней: столбняка и дифтерии (АС и АД).
Среди предложенных способов повторного привития самый безопасный — импортный препарат. В отличие от отечественных инъекций, он требует финансовых затрат. Imovax «D. T. Adult» не вызывает осложнений и непредвиденных реакций со стороны организма после введения. Более детальную адсм расшифровку пациент имеет право получить в медицинском учреждении на консультации у терапевта, педиатра, в прививочном кабинете, центре.
Влияние анатоксина
Основу вводимого препарата составляет компонент «анатоксин». Он не токсичен и безвреден для организма человека, его цель — сохранить иммуногенный эффект. После инъекции клетки возбудителя прекращают развитие в организме, вырабатывая антитела для защиты иммунитета от столбняка, дифтерии.
После инъекции клетки возбудителя прекращают развитие в организме, вырабатывая антитела для защиты иммунитета от столбняка, дифтерии.
Адсорбированный дифтерийно-столбнячный препарат включает в себя два компонента анатоксина против нескольких смертельных болезней, по этой причине инъекцию считают бивалентной или поливалентной. Для лучшего усвоения введённого препарата вакцину создают из чистых биологических веществ, позволяя консервантам попасть в организм один раз. Главное преимущество поливалентного введения — два препарата вводятся одним разом, что снижает количество уколов.
Иммунизация среди взрослых и детей
Прививка адс-м ставится детям начиная с младенчества. Ею прививают детей, плохо переносящих АКДС, начиная с трехмесячного возраста. Первая иммунизация проходит в 3, затем в 4—6 месяцев. Вавершает комплексный цикл бустерная доза. Она закрепляет невосприимчивость болезней, вводится в возрасте полутора лет. Базовый комплекс из 4 прививок формирует детский иммунитет против столбняка, дифтерии.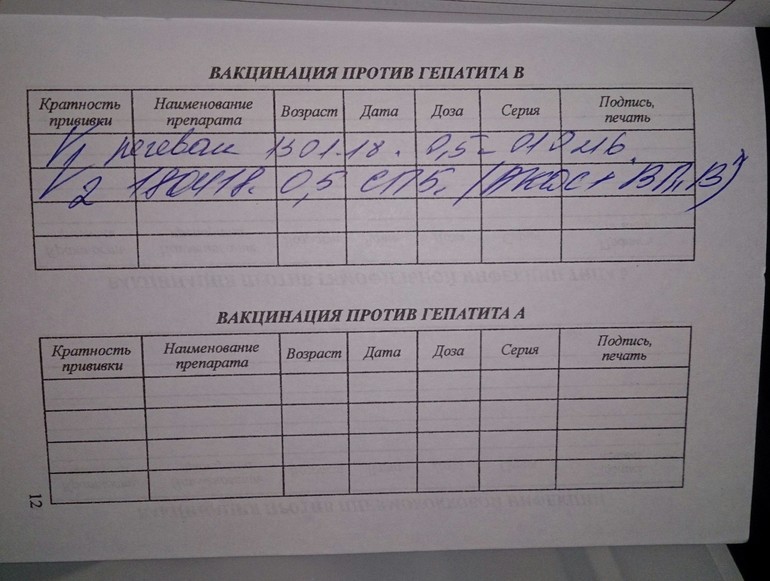
Последующие вакцины формата адс-м называются ревакцинацией, их цель — активировать иммунитет к возбудителям болезней. Затем до 6 лет родители могут быть спокойны за организм ребёнка. В возрасте 6 лет ребёнок должен пройти ревакцинацию (rv 2), которая будет поддерживать непереносимость от болезней в течение 10 последующих лет. По истечении 10 лет rv повторяется, меняя только нумерацию: например, в 6 лет ребёнок сделал rv 2, в возрасте 16 лет он обязан сделать rv 3. Так график ревакцинации будет повторяться каждые 10 лет.
Игнорировать, пропускать прививки не рекомендовано, поскольку просроченный срок rv снижает барьер защиты иммунитета.
Министерство Здравоохранение Р. Ф. для людей старше возраста 14 лет установило рамки проведения прививки rv:
Существуют группы людей, не вакцинирующихся путём адс-м в течение своей жизни. В таком случае необходимо пройти курс вакцинации: первое привитие, через месяц второе, через полгода третья прививка. При отсутствии rv интервалом в 20 лет врачи рекомендуют пациентам иммунизировать организм двумя дозами АДС-м с промежутком в один месяц.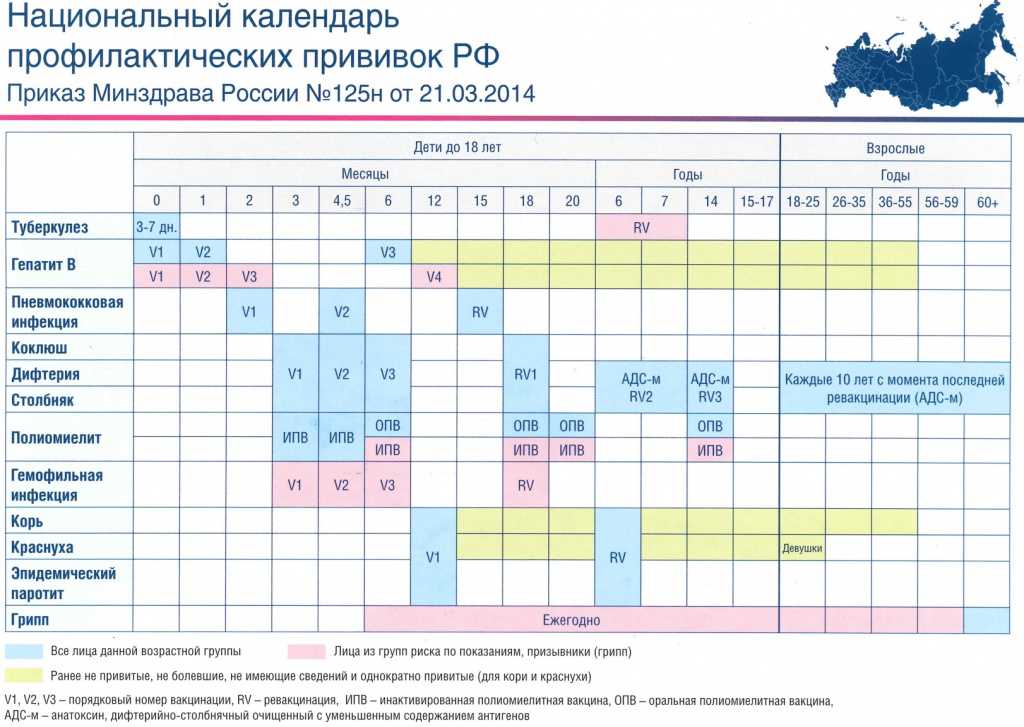
Границы для проведения последней инъекции нет. Она подходит всем возрастным категориям. Важно: перед прививкой пройти обследование у участкового врача, без его заключения инъекцию ставить запрещено.
Адсм расшифровка пугает родителей, не разбираясь в преимуществах вакцины, они сразу пишут отказ от прививки, не думая о последствиях при столкновении с возбудителем болезни.
Вакцинация в период беременности
Беременность — одно из основных противопоказаний к прививке Адс-м. Министерство Здравоохранения Российской Федерации настоятельно рекомендует женщинам, желающим забеременеть, привиться за два месяца до зачатия. В течение двух месяцев предохраняться, поскольку есть риск, что вакцина может негативно влиять на формирование плода.
Существуют и такие ситуации, когда женщина, сделав прививку, узнает, что она находится в положении. Какие бы ни были противопоказания вакцины, ничего не предпринимайте. Сообщите про поставленную инъекцию гинекологу и тщательно наблюдайтесь. Если гинеколог заметит проявление патологии, то беременность следует прервать.
Если гинеколог заметит проявление патологии, то беременность следует прервать.
Однако такое практикуется только на территории Российской Федерации. В США иная практика: адсорбированный коклюшно-дифтерийно-столбнячный укол ставится женщинам в положении на последних сроках. Медики это объясняют тем, что возбудители коклюша, дифтерии и столбняка мутировали и поражают детские организмы с рождения. Укол АКДС ставится детям не раньше двухмесячного возраста, чтобы оградить деток от ужасной болезни. Медики прививают беременных с целью передачи защиты от инфекции через плаценту.
Применение, место вакцинации, реакция
Профилактика иммунизации производится специализированными медицинскими инструментами, предназначенными для разового использования. Препарат выпускается в жидком виде и фасуется в ампулы для многократного использования и одноразовые шприцы. В 2017 предложили пациентам адс-м в разовых шприцах, в них отсутствуют консерванты. За счёт этого укол не вызывает осложнений со стороны организма.
В 2017 предложили пациентам адс-м в разовых шприцах, в них отсутствуют консерванты. За счёт этого укол не вызывает осложнений со стороны организма.
Перед инъекцией взрослым рекомендуется подготовить свой организм с целью снижения риска развития побочных реакций. Во-первых, нужно избегать длительных прогулок в массовых местах, во-вторых, не есть за 12 часов до вакцинации. В-третьих, не употреблять спиртные напитки за 3−5 дней до и после привития. По истечении 5 дней после введённой инъекции любителям спиртного рекомендуется употреблять спиртные напитки со слабым процентом спирта. Распространённые побочные эффекты прививки адсм у взрослых: аллергические проявления, менингит, анафилактический шок.
Детский организм — механизм, требующий детальной подготовки. «Куда делается вакцина и каковы её осложнения?» — главные вопросы, волнующие родителей. За три дня до привития подготовьте ребёнка. За два дня до и после вакцинации дайте ребёнку антигистаминные препараты, чтобы снизить риск аллергических реакций до минимума. Противоаллергическое средство согласуйте с участковым врачом, не прибегайте к самодеятельности.
Противоаллергическое средство согласуйте с участковым врачом, не прибегайте к самодеятельности.
Прививку делают внутримышечно, после введения препарата могут возникать незначительные последствия по причине активной выработки иммунитета на введённые компоненты. Родители должны быть готовы к тяжёлым реакциям организма ребёнка, например, к повышенной температуре. В таком случае детям рекомендуется дать жаропонижающие препараты, содержащие парацетамол.
Часто у детей после вакцины может болеть место инъекции, вызывая уплотнение, покраснение, отёчность, чувство жара. Такая реакция пройдёт самостоятельно в течение 14 дней. А также могут проявляться болевые ощущения, мешающие вести привычный образ жизни. Ни в коем случае нельзя греть место укола, перегрев может спровоцировать нагноение.
К заметным симптомам после прививочного периода можно отнести:
- капризность;
- беспокойство;
- потеря полноценного сна;
- рвота;
- понос;
- отсутствие аппетита;
- упадок сил;
- в редких случаях заторможенность.

Противопоказания инъекции
Адс в малой дозировке практически не имеет противопоказаний к применению. Однако перед проведением запланированной иммунопрофилактики следует замерить температуру тела, осмотреть горло для выявления воспалительных процессов, которые могут стать возбудителями анафилактического шока.
Любой воспалительный процесс организма можно считать противопоказанием к применению. А также иммунопрофилактические процедуры могут быть отменены по ряду причин: период беременности и лактации у женщин, воспалительные процессы любой болезни, аллергические реакции (отёк Квинке, крапивница), иммунодефицит, индивидуальная непереносимость препарата или его компонентов, чрезмерно тяжёлые последствия на прошлую иммунопрофилактику. Перед каждой иммунопрофилактикой в обязательном порядке нужно консультироваться с медицинским сотрудником на установление факта «можно или нельзя проходить пациенту иммунное повышение».
Re — вакцинация важна для девушек в возрасте от 16 до 26 лет, она укрепляет иммунитет женского организма, обеспечивая защиту в период беременности.
Процесс проведения укола
Профилактика организма должна осуществляться исключительно в стерильных условиях, медицинский сотрудник обязан соблюдать все антисептические инструкции. Перед уколом медработник должен проверить целостность инструментов, срок годности вводимой ампулы. Пациент после процедуры обязан выполнять рекомендации врача: не растирать место укола, подождать 30 минут — этого времени хватает, чтобы проследить аллергические реакции организма.
Адсорбированный дифтерийно-столбнячный препарат ограничивает людей разновозрастных рамок от заболеваний, предрасположенных к летальному исходу. Его профилактика обязательна начиная с младенчества (3, 4−6 месяцев). После достижения 14 лет она должна проводиться строго по графику каждые 10 лет. Иммунопрофилактика адс-м не требует особой подготовки и не наносит организму вреда.
youtube.com/embed/ZNF30lRf-TY» allowfullscreen=»allowfullscreen»/>
- Автор: chebo
- Распечатать
Оцените статью:
(0 голосов, среднее: 0 из 5)
Поделитесь с друзьями!
Два различных метода инокуляции выявили относительную независимость накопления ДОН в зернах пшеницы от степени тяжести заболевания на колосе после заражения фузариозом
1. Бай Г., Шанер Г. Управление и устойчивость пшеницы и ячменя к фузариозу колоса. Анну. Преподобный Фитопат. 2004; 42: 135–161. doi: 10.1146/annurev.phyto.42.040803.140340. [PubMed] [CrossRef] [Google Scholar]
2. Шампейл А., Доре Т., Фурбет Дж. Фузариоз колоса: эпидемиологическое происхождение влияния культурных методов на атаки гнили колоса и производство микотоксинов фузариозом в пшенице зерна. Растение.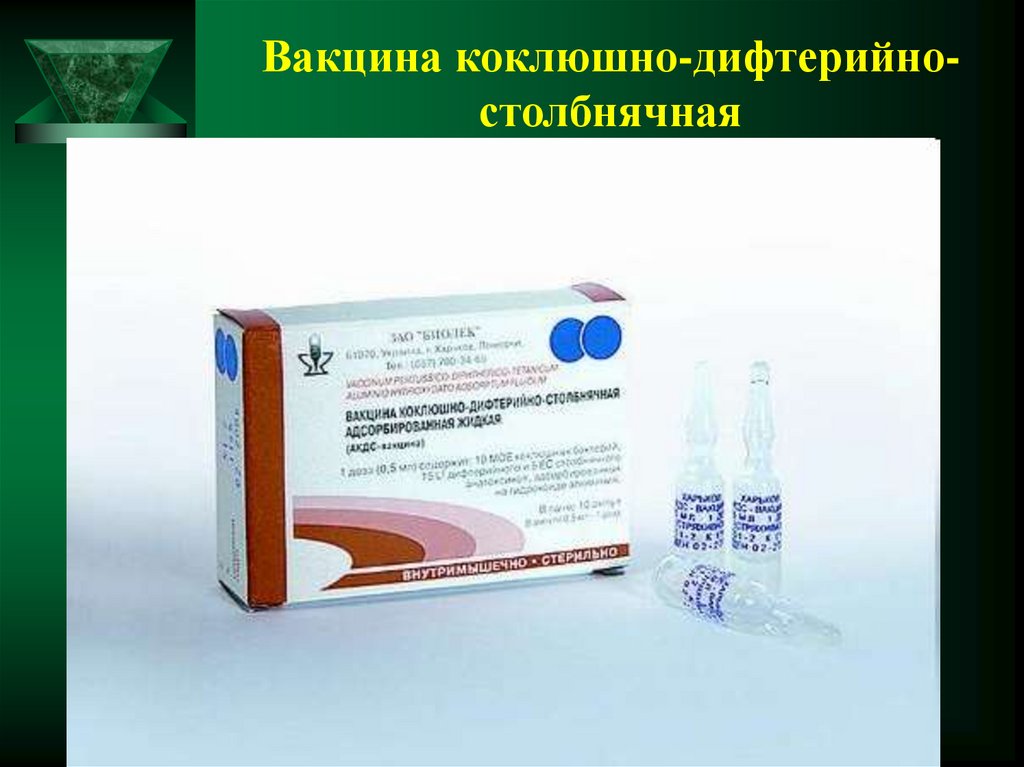 науч. 2004;166:1389–1415. doi: 10.1016/j.plantsci.2004.02.004. [CrossRef] [Google Scholar]
науч. 2004;166:1389–1415. doi: 10.1016/j.plantsci.2004.02.004. [CrossRef] [Google Scholar]
3. Местерхази А. Типы и компоненты устойчивости к фузариозу пшеницы. Растение. Порода. 1995; 114: 377–386. doi: 10.1111/j.1439-0523.1995.tb00816.x. [CrossRef] [Google Scholar]
4. Пестка Ю.Ю., Смолинский А.Т. Дезоксиниваленол: токсикология и потенциальное воздействие на человека. Дж. Токсикол. Окружающая среда. Здоровье Часть B. 2005; 8: 39–69. doi: 10.1080/10937400590889458. [PubMed] [CrossRef] [Академия Google]
5. Куадио Дж. Х., Мобио Т. А., Бодримон И., Муха С., Дано С. Д., Креппи Э. Э. Сравнительное исследование цитотоксичности и окислительного стресса, вызванного дезоксиниваленолом, зеараленоном или фумонизином B1, в линии клеток кишечника человека Caco-2. Токсикология. 2005; 213:56–65. doi: 10.1016/j.tox.2005.05.010. [PubMed] [CrossRef] [Google Scholar]
6. Агриопулу С., Стамателопулу Э., Варзакас Т. Достижения в области возникновения, важности и стратегии контроля микотоксинов: профилактика и детоксикация в пищевых продуктах. Еда. 2020;9:137. doi: 10.3390/foods9020137. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Еда. 2020;9:137. doi: 10.3390/foods9020137. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
7. Pestka J.J. Дезоксиниваленол: токсичность, механизмы и риски для здоровья животных. Аним. Кормовая наука. Технол. 2007; 137: 283–298. doi: 10.1016/j.anifeedsci.2007.06.006. [CrossRef] [Google Scholar]
8. Kolf-Clauw M., Castellote J., Joly B., Bourges-Abella N., Raymond-Letron I., Pinton P., Oswald I.P. Разработка культуры эксплантата тощей кишки свиньи для изучения желудочно-кишечной токсичности микотоксина дезоксиниваленола: гистопатологический анализ. Токсикол. В пробирке. 2009 г.;23:1580–1584. doi: 10.1016/j.tiv.2009.07.015. [PubMed] [CrossRef] [Google Scholar]
9. Соброва П., Адам В., Васаткова А., Беклова М., Земан Л., Кизек Р. Деоксиниваленол и его токсичность. междисциплинарный Токсикол. 2010;3:94–99. doi: 10.2478/v10102-010-0019-x. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
10. Shi J., Liu X., Qiu J., Ji F., Xu J., Dong F.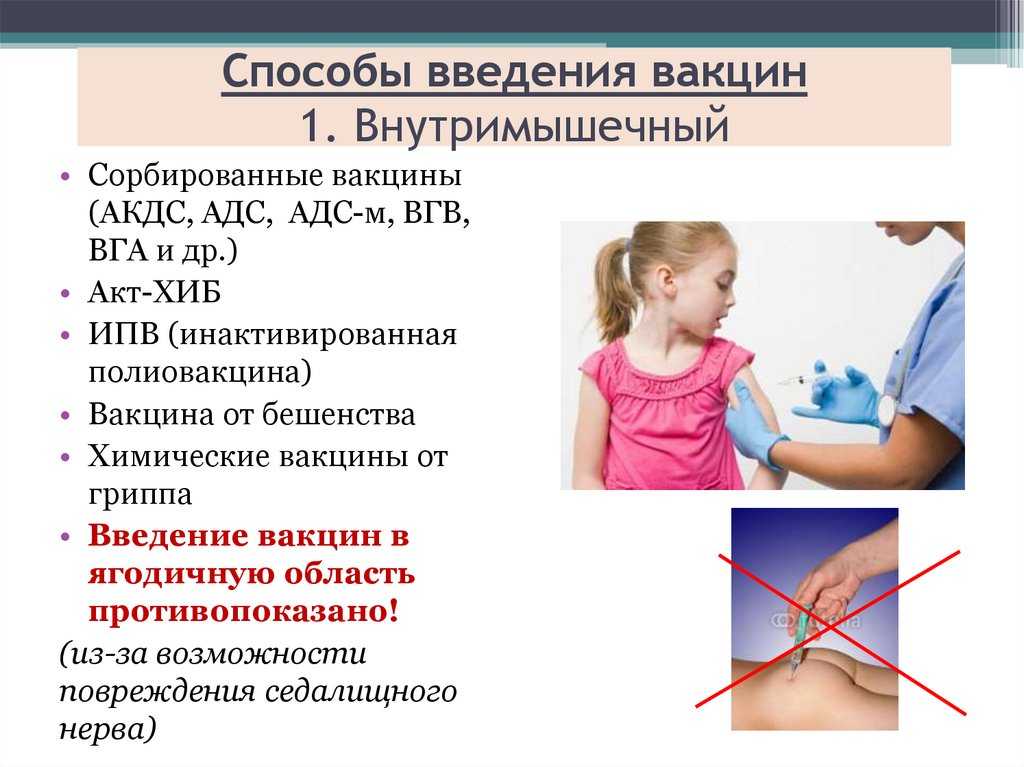 , Yin X., Ran J. Загрязнение пшеницы дезоксиниваленолом и борьба с ним. науч. Агр. Грех. 2014;47:3641–3654. [Академия Google]
, Yin X., Ran J. Загрязнение пшеницы дезоксиниваленолом и борьба с ним. науч. Агр. Грех. 2014;47:3641–3654. [Академия Google]
11. МакМаллен М., Бергстром Г., Де Вольф Э., Дилл-Маки Р., Хершман Д., Шейнер Г., Ван Сэнфорд Д. Объединенные усилия по борьбе с врагом пшеницы и ячменя: фузариозом колосьев . Растение. Дис. 2012; 96:1712–1728. doi: 10.1094/PDIS-03-12-0291-FE. [PubMed] [CrossRef] [Google Scholar]
12. Биндер Э., Тан Л., Чин Л., Хэндл Дж., Ричард Дж. Встречаемость микотоксинов в товарах, кормах и кормовых ингредиентах во всем мире. Аним. Кормовая наука. Технол. 2007; 137: 265–282. doi: 10.1016/j.anifeedsci.2007.06.005. [Перекрестная ссылка] [Академия Google]
13. Cui L., Selvaraj J.N., Xing F., Zhao Y., Zhou L., Liu Y. Небольшое исследование дезоксиниваленола в пшенице, зараженной фузариозом, в бассейне реки Янцзы-Хуайхэ в Китае. Пищевой контроль. 2013; 30: 469–473. doi: 10.1016/j.foodcont.2012.08.011. [CrossRef] [Google Scholar]
14. Бутиньи А.-Л. , Ришар-Форже Ф., Барро К. Естественные механизмы устойчивости злаков к накоплению Fusarium trichothecenes. Евро. Дж. Плант. Патол. 2008; 121:411–423. doi: 10.1007/s10658-007-9266-x. [Перекрестная ссылка] [Академия Google]
, Ришар-Форже Ф., Барро К. Естественные механизмы устойчивости злаков к накоплению Fusarium trichothecenes. Евро. Дж. Плант. Патол. 2008; 121:411–423. doi: 10.1007/s10658-007-9266-x. [Перекрестная ссылка] [Академия Google]
15. Далл’Эрта А., Чирлини М., Далл’Аста М., Дель Рио Д., Галаверна Г., Далл’Аста С. Маскированные микотоксины эффективно гидролизуются микробиотой толстой кишки человека с высвобождением их агликонов. хим. Рез. Токсикол. 2013;26:305–312. doi: 10.1021/tx300438c. [PubMed] [CrossRef] [Google Scholar]
16. Nagl V., Schwartz H., Krska R., Moll W.-D., Knasmüller S., Ritzmann M., Adam G., Berthiller F. Метаболизм замаскированный микотоксин дезоксиниваленол-3-глюкозид у крыс. Токсикол. лат. 2012; 213:367–373. doi: 10.1016/j.toxlet.2012.07.024. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
17. Nagl V., Woechtl B., Schwartz-Zimmermann H.E., Hennig-Pauka I., Moll W.-D., Adam G., Berthiller F. Метаболизм замаскированного микотоксина дезоксиниваленол-3-глюкозида у свиней. Токсикол. лат. 2014; 229:190–197. doi: 10.1016/j.toxlet.2014.06.032. [PubMed] [CrossRef] [Google Scholar]
Токсикол. лат. 2014; 229:190–197. doi: 10.1016/j.toxlet.2014.06.032. [PubMed] [CrossRef] [Google Scholar]
18. Tan Y., Zhu R., Wu A., Liu N. Основные типы замаскированных микотоксинов и современные методологические достижения для их обнаружения. науч. Грех. Чим. 2016; 46: 251–256. doi: 10.1360/N032015-00205. [Перекрестная ссылка] [Академия Google]
19. Bai G., Kolb F.L., Shaner G., Domier L.L. Маркеры полиморфизма длины амплифицированных фрагментов, связанные с основным локусом количественного признака, контролирующим устойчивость пшеницы к парше. Фитопатология. 1999; 89: 343–348. doi: 10.1094/PHYTO.1999.89.4.343. [PubMed] [CrossRef] [Google Scholar]
20. Уолдрон Б.Л., Морено-Севилья Б., Андерсон Дж.А., Стэк Р.В., Фроберг Р.К. RFLP Картирование QTL устойчивости пшеницы к фузариозу. Обрезать. науч. 1999; 39: 805–811. doi: 10.2135/cropsci1999.0011183X003
0032x. [CrossRef] [Google Scholar]
21. Bai G., Plattner R., Desjardins A., Kolb F., McIntosh R.A. Устойчивость к фузариозу и накоплению дезоксиниваленола в пшенице. Растение. Порода. 2001; 120:1–6. doi: 10.1046/j.1439-0523.2001.00562.x. [CrossRef] [Google Scholar]
Растение. Порода. 2001; 120:1–6. doi: 10.1046/j.1439-0523.2001.00562.x. [CrossRef] [Google Scholar]
22. Лемменс М., Шольц У., Бертиллер Ф., Далл’Аста С., Кутник А., Шумахер Р., Адам Г., Бюрстмайр Х., Акос М., Крска Р. и др. Способность детоксицировать микотоксин дезоксиниваленол колокализуется с основным количественным локусом признаков устойчивости к фузариозу пшеницы. Мол. Растение. Взаимодействие микробов. 2005;18:1318–1324. дои: 10.1094/МПМИ-18-1318. [PubMed] [CrossRef] [Google Scholar]
23. Геддес Дж., Юдес Ф., Такер Дж. Р., Легге В. Г., Селинджер Л. Оценка методов инокуляции инфекции и продукции дезоксиниваленола ячменем Fusarium graminearumon. Может. Дж. Плант. Патол. 2008; 30:66–73. doi: 10.1080/07060660809507497. [CrossRef] [Google Scholar]
24. Mesterházy A., Lehoczki-Krsjak S., Varga M., Szabó-Hever Á., Tóth B., Lemmens M. Селекция на устойчивость к FHB через ядра, поврежденные фузариозом, и накопление дезоксиниваленола как а также способы инокуляции озимой пшеницы. Агр. науч. 2015;6:970–1002. doi: 10.4236/as.2015.69094. [CrossRef] [Google Scholar]
Агр. науч. 2015;6:970–1002. doi: 10.4236/as.2015.69094. [CrossRef] [Google Scholar]
25. Zhang M.Y., Li M.A., Zhu M.S., Li L., He X., Sun Z., Li T. Базальная инъекция междоузлий позвоночника (BRII): новый метод инокуляции для оценки пшеницы устойчивость к фузариозной пятнистости. Фитопатология. 2021 doi: 10.1094/PHYTO-11-20-0488-R. [PubMed] [CrossRef] [Google Scholar]
26. Джаятилаке Д.В., Бай Г.Х., Донг Ю.Х. Новый локус количественного признака устойчивости к фузариозу колоса в хромосоме 7А пшеницы. Теор. заявл. Жене. 2011;122:1189–1198. doi: 10.1007/s00122-010-1523-2. [PubMed] [CrossRef] [Google Scholar]
27. Ю Дж.-Б., Бай Г.-Х., Цай С.-Б., Донг Ю.-Х., Бан Т. Новый фузариоз колоса- устойчивые источники из азиатской зародышевой плазмы пшеницы. Обрезать. науч. 2008;48:1090–1097. doi: 10.2135/cropsci2007.10.0554. [CrossRef] [Google Scholar]
28. Местерхази А., Барток Т., Мироча С.Г., Комороци Р. Природа устойчивости пшеницы к фузариозу колоса и роль дезоксиниваленола в селекции. Растение. Порода. 1999; 118: 97–110. дои: 10.1046/j.1439-0523.1999.118002097.х. [CrossRef] [Google Scholar]
Растение. Порода. 1999; 118: 97–110. дои: 10.1046/j.1439-0523.1999.118002097.х. [CrossRef] [Google Scholar]
29. Ma H.X., Zhang K.M., Gao L., Bai G.H., Chen H.G., Cai Z.X., Lu W.Z. Локусы количественных признаков устойчивости к фузариозу и накоплению дезоксиниваленола в пшенице Ваншуйбай в полевых условиях. Растение. Патол. 2006; 55: 739–745. doi: 10.1111/j.1365-3059.2006.01447.x. [CrossRef] [Google Scholar]
30. Kang Z., Buchenauer H. Иммуноцитохимическая локализация токсинов фузариоза в инфицированных колосьях пшеницы с помощью Fusarium culmorum . Физиол. Мол. Растение. Патол. 1999; 55: 275–288. doi: 10.1006/pmpp.1999.0233. [CrossRef] [Google Scholar]
31. Kang Z., Buchenauer H. Ультраструктурное и иммуноцитохимическое исследование развития патогенов и реакции хозяина на устойчивые и восприимчивые колосья пшеницы, инфицированные Fusarium culmorum . Физиол. Мол. Растение. Патол. 2000; 57: 255–268. doi: 10.1006/pmpp.2000.0305. [CrossRef] [Google Scholar]
32. Liu S., Hall M.D., Griffey C.A., McKendry A.L. Мета-анализ QTL, связанного с устойчивостью пшеницы к фузариозу. Обрезать. науч. 2009 г.;49:1955–1968. doi: 10.2135/cropsci2009.03.0115. [CrossRef] [Google Scholar]
Liu S., Hall M.D., Griffey C.A., McKendry A.L. Мета-анализ QTL, связанного с устойчивостью пшеницы к фузариозу. Обрезать. науч. 2009 г.;49:1955–1968. doi: 10.2135/cropsci2009.03.0115. [CrossRef] [Google Scholar]
33. Zheng T., Hua C., Li L., Sun Z., Yuan M., Bai G., Humphreys G., Li T. Интеграция обнаружения мета-QTL с omics : На пути к молекулярной селекционной платформе для повышения устойчивости пшеницы к фузариозу. Обрезать. J. 2020 doi: 10.1016/j.cj.2020.10.006. [CrossRef] [Google Scholar]
34. Buerstmayr H., Steiner B., Hartl L., Griesser M., Angerer N., Lengauer D., Miedaner T., Schneider B., Lemmens M. Молекулярное картирование QTL. на устойчивость к фузариозу яровой пшеницы. II. Устойчивость к проникновению и распространению грибков. Теор. заявл. Жене. 2003; 107: 503–508. doi: 10.1007/s00122-003-1272-6. [PubMed] [CrossRef] [Академия Google]
35. Schweiger W., Steiner B., Vautrin S., Nussbaumer T., Siegwart G., Zamini M., Jungreithmeier F., Gratl V., Lemmens M. , Mayer K.F.X., et al. Подавленная рекомбинация и уникальные гены-кандидаты в дивергентном гаплотипе, кодирующем Fhb1 , основной локус устойчивости к фузариозу пшеницы. Теор. заявл. Жене. 2016; 129:1607–1623. doi: 10.1007/s00122-016-2727-x. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
, Mayer K.F.X., et al. Подавленная рекомбинация и уникальные гены-кандидаты в дивергентном гаплотипе, кодирующем Fhb1 , основной локус устойчивости к фузариозу пшеницы. Теор. заявл. Жене. 2016; 129:1607–1623. doi: 10.1007/s00122-016-2727-x. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
36. Li G., Zhou J., Jia H., Gao Z., Fan M., Luo Y., Zhao P., Xue S. , Ли Н., Юань Ю. и др. Мутация богатого гистидином гена кальций-связывающего белка в пшенице придает устойчивость к фузариозу. Нац. Жене. 2019;51:1106–1112. doi: 10.1038/s41588-019-0426-7. [PubMed] [CrossRef] [Google Scholar]
37. Su Z., Bernardo A., Tian B., Chen H., Wang S., Ma H., Cai S., Liu D., Zhang D., Ли Т. и др. Делеционная мутация в TaHRC придает Fhb1 устойчивость к фузариозу пшеницы. Нац. Жене. 2019;51:1099–1105. doi: 10.1038/s41588-019-0425-8. [PubMed] [CrossRef] [Google Scholar]
38. Рават Н., Памфри М., Лю С., Чжан С., Тивари В.К., Андо К., Трик Х.Н., Бокус В.В., Ахунов Э. , Андерсон Дж.А., и другие. Пшеница Fhb1 кодирует химерный лектин с агглютининовыми доменами и порообразующим токсиноподобным доменом, придающим устойчивость к фузариозной гнили. Нац. Жене. 2016;48:1576–1580. doi: 10.1038/ng.3706. [PubMed] [CrossRef] [Google Scholar]
, Андерсон Дж.А., и другие. Пшеница Fhb1 кодирует химерный лектин с агглютининовыми доменами и порообразующим токсиноподобным доменом, придающим устойчивость к фузариозной гнили. Нац. Жене. 2016;48:1576–1580. doi: 10.1038/ng.3706. [PubMed] [CrossRef] [Google Scholar]
39. Де Лубресс Н.Г., Прохорова И.В., Холткамп В., Роднина М.В., Юсупова Г., Юсупов М. Структурные основы ингибирования эукариотической рибосомы. Нац. Клеточная биол. 2014; 513:517–522. doi: 10.1038/nature13737. [PubMed] [CrossRef] [Академия Google]
40. Пестка Ю.Ю. Дезоксиниваленол: механизмы действия, воздействие на человека и токсикологическая значимость. Арка Токсикол. 2010; 84: 663–679. doi: 10.1007/s00204-010-0579-8. [PubMed] [CrossRef] [Google Scholar]
41. Далл’Аста С., Далл’Эрта А., Мантовани П., Масси А., Галаверна Г. Наличие дезоксиниваленола и дезоксиниваленол-3-глюкозида в твердой пшенице. World Mycotoxin J. 2013;6:83–91. doi: 10.3920/WMJ2012.1463. [CrossRef] [Google Scholar]
42. Audenaert K., De Boevre M., Vanheule A., Callewaert J., Bekaert B., Höfte M., De Saeger S., Haesaert G. Глюкозилирование микотоксинов в коммерческих сортах пшеницы : Влияние на сопротивление до Fusarium graminearum в лабораторных и полевых условиях. Пищевой контроль. 2013; 34: 756–762. doi: 10.1016/j.foodcont.2013.06.019. [CrossRef] [Google Scholar]
Audenaert K., De Boevre M., Vanheule A., Callewaert J., Bekaert B., Höfte M., De Saeger S., Haesaert G. Глюкозилирование микотоксинов в коммерческих сортах пшеницы : Влияние на сопротивление до Fusarium graminearum в лабораторных и полевых условиях. Пищевой контроль. 2013; 34: 756–762. doi: 10.1016/j.foodcont.2013.06.019. [CrossRef] [Google Scholar]
43. Yang X., Pan Y., Singh P.K., He X., Ren Y., Zhao L., Zhang N., Cheng S., Chen F. Полногеномные исследования ассоциативное исследование устойчивости китайской мягкой пшеницы к фузариозной гнили. Завод БМК. биол. 2019;19:153. doi: 10.1186/s12870-019-1758-2. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
44. Фарбер О., Кадмон Р. Оценка альтернативных подходов к биоклиматическому моделированию с особым акцентом на расстояние Махаланобиса. Экол. Модель. 2003; 160:115–130. doi: 10.1016/S0304-3800(02)00327-7. [Перекрестная ссылка] [Академия Google]
45. Ю Дж.-Б., Бай Г.-Х., Цай С.-Б., Бан Т. Маркерная характеристика азиатских линий пшеницы на устойчивость к фузариозу. Теор. заявл. Жене. 2006; 113: 308–320. doi: 10.1007/s00122-006-0297-z. [PubMed] [CrossRef] [Google Scholar]
Теор. заявл. Жене. 2006; 113: 308–320. doi: 10.1007/s00122-006-0297-z. [PubMed] [CrossRef] [Google Scholar]
46. Li T., Luo M., Zhang D., Wu D., Li L., Bai G. Эффективные маркерные аллели, связанные с устойчивостью 2-го типа к фузариозной гнили в полях. Порода. науч. 2016;66:350–357. doi: 10.1270/jsbbs.15124. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
47. Mao X., Hua C., Yang L., Zhang Y., Sun Z., Li L., Li T. Влияние селена на фузариоз пшеницы и накопление DON зависели от соединения селена. Токсины. 2020;12:573. doi: 10.3390/toxins12090573. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
48. McLachlan G.J. Расстояние Махаланобиса. Резонанс. 1999; 4: 20–26. doi: 10.1007/BF02834632. [CrossRef] [Google Scholar]
49. Бернардо А.Н., Ма Х., Чжан Д., Бай Г. Однонуклеотидный полиморфизм в области хромосомы пшеницы, содержащей Fhb1 для устойчивости к фузариозу. Мол. Порода. 2012; 29: 477–488. doi: 10.1007/s11032-011-9565-y. [CrossRef] [Google Scholar]
[CrossRef] [Google Scholar]
50. Su Z., Jin S., Zhang D., Bai G. Разработка и валидация диагностических маркеров для региона Fhb1 , основного QTL для определения устойчивости пшеницы к фузариозу. Теор. заявл. Жене. 2018;131:2371–2380. doi: 10.1007/s00122-018-3159-6. [PubMed] [CrossRef] [Google Scholar]
Ответ на прививку Fusarium culmorum ячменю
[1] Bai G.H., Desjardins AE & Plattner R.D. 2002. Дезоксиниваленол, не продуцирующий Fusarium graminearum, вызывает первичное заражение, но не вызывает распространения болезни в колосьях пшеницы. Микопатология 153: 91–98. http://dx.doi.org/10.1023/A:101441932355010.1023/A:1014419323550Search in Google Scholar
[2] Buerstmayr H., Legzdina L., Steiner B. & Lemmens M. 2004. Вариация устойчивости к Fusarium head гниль ярового ячменя. Евфитика 137: 279–290. http://dx.doi.org/10.1023/B:EUPH.0000040440.99352.b910.1023/B:EUPH.0000040440.99352.b9Поиск в Google Scholar
[3] Campbell K.A.G. и Липпс П.Е. 1999. Распределение ресурсов: источники изменчивости в питомниках для скрининга фузариозной гнили. Фитопатология 88: 1078–1086. 10.1094/PHYTO.1998.88.10.1078Поиск в Google Scholar
1999. Распределение ресурсов: источники изменчивости в питомниках для скрининга фузариозной гнили. Фитопатология 88: 1078–1086. 10.1094/PHYTO.1998.88.10.1078Поиск в Google Scholar
пабмед
[4] Купер Б., Скоглунд Л., Аскельсон С. и Ван Хорн Дж. 2004. Практический опыт селекции ярового шестирядного солодового ячменя на фузариоз и ДОН с использованием различных методов селекции. В: Труды 2-го Международного симпозиума по фузариозной гнили, 1, Орландо, США, 11–15 декабря, стр. 44–48. Поиск в Google Академии
[5] Franckowiak J., Zhang B.X., Horsley R.D., Steffenson B.J., Smith K.J. и Нит С.М. 2004. Оценка ячменя в Китае на устойчивость к фузариозу. В: Труды 2-го Международного симпозиума по фузариозной гнили, 1, Орландо, США, 11–15 декабря, с. 58. Поиск в Google Scholar
[6] Гагкаева Т.Ю., Левитин М.М., Зуев Е.В. и Терентьева И.А. 2002. Оценка генетических ресурсов устойчивости к фузариозу пшеницы и ячменя с Дальнего Востока России. Дж. Заявл. Генетика 43А: 229–234.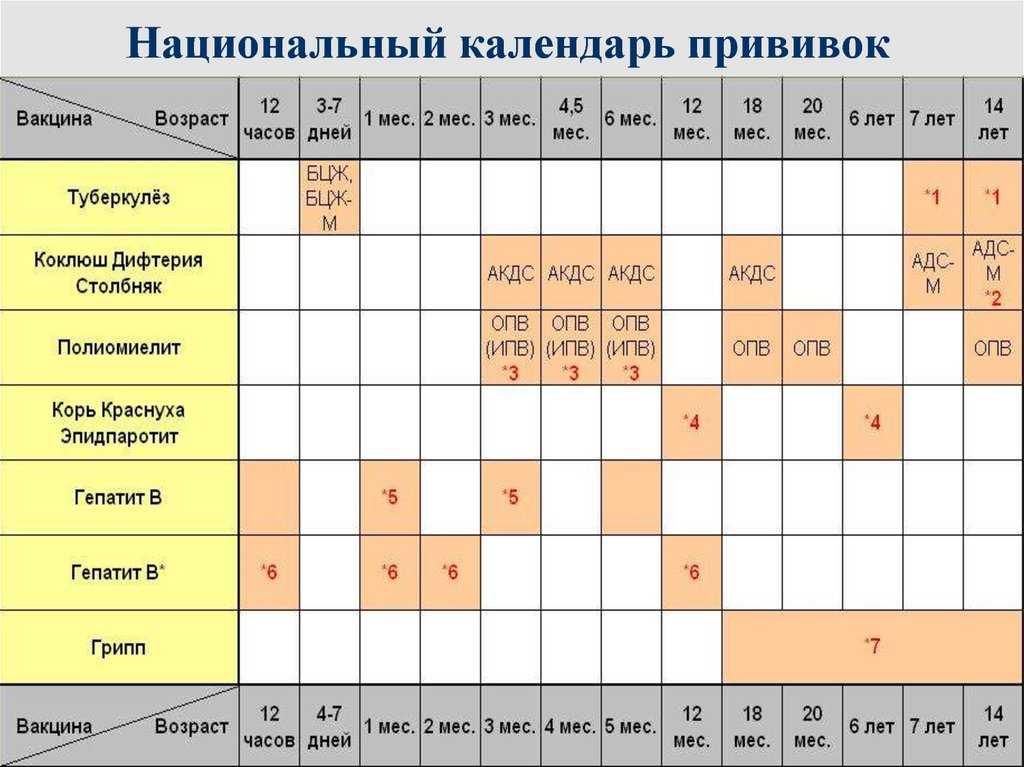 Поиск в Google Scholar
Поиск в Google Scholar
[7] Galtier P. 1998. Биологическая судьба микотоксинов у животных. Преподобный Мед.Вет. 149: 549–554. Поиск в Google Scholar
[8] Hýsek J., Vach M., Brožová J., Sychrová E., Civínova M., Nedilník J. & Hrubý J. 2002. Влияние применения минеральных удобрений с биопрепаратом Supresivit (Trichoderma harzianum) на здоровье и урожайность различных культур. Арка фитопат. Защита растений. 35: 115–124. http://dx.doi.org/10.1080/0323540021421110.1080/03235400214211Поиск в Google Scholar
[9] Ittu M., Grabarkiewicz-Szczęsna J., Kostecki M. & Goliński P. 2000. Накопление дезоксиниваленола и другие симптомы парши у шести румынских генотипов пшеницы, инокулированных Fusarium graminearum. Микологические рез. 16: 15–22. 10.1007/BF02946102Поиск в Google Scholar
пабмед
[10] Jansen D., Wettstein C., Schäfer W., Kogel K.H., Felk A. & Maier J. 2005. Модели заражения ячменя и колосьев пшеницы, инокулированных диким типом и геном триходиенсинтазы, нарушенным Fusarium graminearum.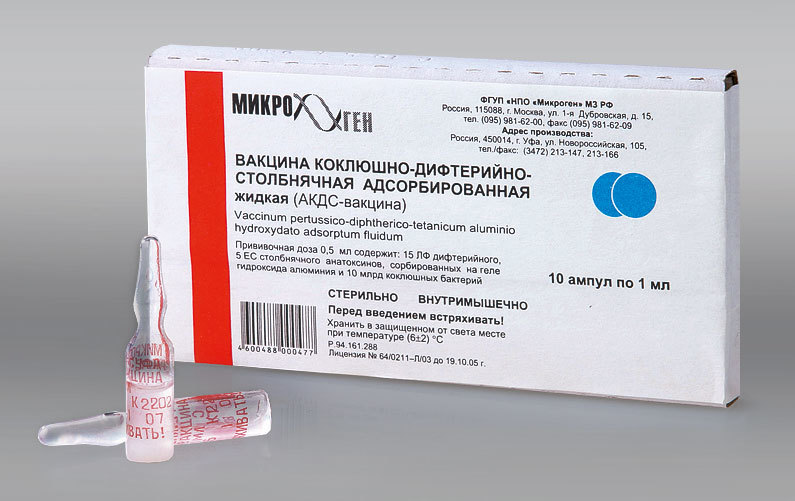 проц. Натл. акад. науч. США 102: 16892–16897. http://dx.doi.org/10.1073/pnas.050846710210.1073/pnas.0508467102Поиск в Google Scholar
проц. Натл. акад. науч. США 102: 16892–16897. http://dx.doi.org/10.1073/pnas.050846710210.1073/pnas.0508467102Поиск в Google Scholar
пабмед
ПабМед Центральный
[11] Джонс Р.К. 2000. Оценка фузариозной гнили пшеницы и ячменя в ответ на обработку фунгицидами. Завод Дис. 84: 1021–1030. 10.1094/PDIS.2000.84.9.1021Поиск в Google Scholar
пабмед
[12] Коттапалли Б., Вольф-Холл К.Е. и Шварц П.Б. 2005. Оценка обработки газообразным озоном и перекисью водорода для снижения выживаемости Fusarium в пивоваренном ячмене. Дж. Пищевая защита. 6: 1236–1240. 10.4315/0362-028X-68.6.1236Поиск в Google Scholar
пабмед
[13] Лемменс М., Шольц У., Бертиллер Ф., Далласта С., Кутник А., Шумахер Р., Адам Г., Бюрстмайр Х., Местерхази А., Крска Р. и Ракенбауэр П. 2005 ● Способность детоксицировать микотоксин дезоксиниваленол колонизирует основной количественный локус признаков устойчивости к фузариозному ожогу пшеницы. Мол. Взаимодействие растительных микробов. 12: 1318–1324. 10.1094/MPMI-18-1318Поиск в Google Scholar
Мол. Взаимодействие растительных микробов. 12: 1318–1324. 10.1094/MPMI-18-1318Поиск в Google Scholar
пабмед
[14] Лян Г.Х.Л., Хейн Э.Л. и Уолтер Т.Л. 1966. Оценки различных взаимодействий с окружающей средой в тестах на урожайность трех мелких зерен и их значение для селекционных программ. Растениеводство. 6: 135–139. 10.2135/cropsci1966.0011183X000600020009xПоиск в Google Scholar
[15] Лю В., Лангсет В., Скиннес Х., Элен О.Н. и Сундхейм Л. 1997. Сравнение показателей визуальной гнили, уровней заражения семян и выработки дезоксиниваленола для оценки устойчивости злаков, инокулированных Fusarium culmorum. Евро. Дж. Плант Патол. 103: 589–595. http://dx.doi.org/10.1023/A:100869321365610.1023/A:1008693213656Search in Google Scholar
[16] McCallum B.D., Tekauz A. & Gilbert J. 2001. Вегетативная совместимость среди изолятов Fusarium graminearum (Gibberella from zeae) колосья ячменя на юге Манитобы. Может. Дж. Плант Патол. 23: 83–87. 10.1080/07060660109506913Поиск в Google Scholar
[17] Местерхази А. 1997. Методология проверки устойчивости и селекции против фузариозной гнили и результаты селекции. Зерновые рез. коммун. 25: 631–637. 10.1007/BF03543801Search in Google Scholar
1997. Методология проверки устойчивости и селекции против фузариозной гнили и результаты селекции. Зерновые рез. коммун. 25: 631–637. 10.1007/BF03543801Search in Google Scholar
[18] Mesterházy A. 2002. Роль дезоксиниваленола в агрессивности Fusarium graminearum и F. culmorum и в устойчивости к фузариозной гнили. Евро. Дж. Плант Патол. 108: 675–684. http://dx.doi.org/10.1023/A:102063111406310.1023/A:1020631114063Поиск в Google Scholar
[19] Миллер Дж. Д., Янг Дж. К. и Сэмпсон Д. Р. 1985. Дезоксиниваленол и устойчивость к фузариозу яровых злаков. Дж. Фитопат. 113: 359–367. 10.1111/j.1439-0434.1985.tb04837.xSearch in Google Scholar
[20] Mielniczuk E., Kiecana I. & Perkowski J. 2004. Восприимчивость генотипов овса к инфекции Fusarium crookwellense Burgess, Nelson and Toussoun и накоплению микотоксинов . Биология 59: 809–816. Поиск в Google Scholar
[21] Парри Д.В., Дженкинсон П. и Маклеод Л. 1995. Фузариоз колоса (парша) мелкозерновых злаков — обзор. Завод Патол. 44: 207–238. 10.1111/j.1365-3059.1995.tb02773.xSearch in Google Scholar
44: 207–238. 10.1111/j.1365-3059.1995.tb02773.xSearch in Google Scholar
[22] Perkowski J., Pavlová A., Šrobárová A., Stachowiak J. & Golinski P. 2002. Биосинтез трихотеценов группы B в сортах пшеницы после инокуляции колосьев с изолятами Fusarium culmorum. Биология 57: 765–771. Поиск в Google Scholar
[23] Радд Дж. К., Хосли Р. Д., МакКендри А. Л. и Элиас Э. М. 2001. Гены устойчивости растений-хозяев к фузариозной гнили. Растениеводство. 41: 620–627. 10.2135/cropsci2001.413620xПоиск в Google Scholar
[24] Шредер Х.В. и Кристенсен Дж.Дж. 1963. Факторы, влияющие на устойчивость пшеницы к парше, вызываемой Gibberella zeae. Фитопатология 53: 831–838. Поиск в Google Scholar
[25] Snijders CHA & Perkowski J. 1990. Влияние гнили, вызванной Fusarium culmorum, на содержание токсинов и массу зерен пшеницы. Фитопатология 80: 566–570. 10.1094/Phyto-80-566Search in Google Scholar
[26] Шип В., Тварук Л. Хрпова Й., Сикорова С., Лейшова Л., Куэра Л. и Овесна Дж. 2004. Влияние фузариозного ожога на микотоксины содержание в зерне сортов ярового ячменя. Чех Я. Жене. Порода растений. 40:91–101. 10.17221/3705-CJGPBSearch in Google Scholar
2004. Влияние фузариозного ожога на микотоксины содержание в зерне сортов ярового ячменя. Чех Я. Жене. Порода растений. 40:91–101. 10.17221/3705-CJGPBSearch in Google Scholar
[27] Вивар Х.Е., Гилкрист Л., Хейс П., Цзунчжэнь Л., Стеффенсон Б., Франко Дж. и Генри М. 1997. Ячмень, устойчивый к парше головок, для соложения и пищевых продуктов. Зерновые рез. коммун. 25: 693–697. 10.1007/BF03543815Search in Google Scholar
[28] Yu G. & Franckowiak J.D. 2004. Оценка восточноазиатских сортов ячменя на устойчивость к фузариозу. В: Труды 2-го Международного симпозиума по фузариозной гнили, 1, Орландо, США, 11–15 декабря, стр. 214–216. Поиск в Google Академии
[29] Урреа К. А., Хорсли Р. Д. и Стеффенсон Б. Дж. 2002. Наследуемость устойчивости к фузариозу и накоплению дезоксиниваленола от образца ячменя. Растениеводство. 42: 1404–1408. 10.2135/cropsci2002.1404Поиск в Google Scholar
[30] Urrea C.A., Horsley R.D., Steffenson B.J. & Schwarz P.B. 2005. Агрономические характеристики, качество солода и устойчивость к болезням линий гермоплазмы ячменя с частичной устойчивостью к фузариозу колоса.