Содержание
Призываем всех заботливых родителей привить детей вакциной против полиомиелита
19 октября, на очередном оперативном совещании главный врач ГБУЗ СО «Тавдинская ЦРБ» Гонцов Д.А. довел до собравшихся информацию о важности и необходимости вакцинации детского населения против полиомиелита. По информации Дмитрия Александровича, в Тавдинском городском округе, по причине отказа родителей, не привиты около 60 детей.
Дмитрий Александрович рассказал всю важность и значимость вакцинации, так как полиомиелит – опасная вирусная инфекция способная привести к параличу и, как следствие, к инвалидности и смерти. Прививка – единственное эффективное средство предупреждения этой болезни. В связи с прибытием на территорию Российской Федерации беженцев и переселенцев из неблагополучных по полиомиелиту территории, возникает важность и значимость вакцинопрофилактики.
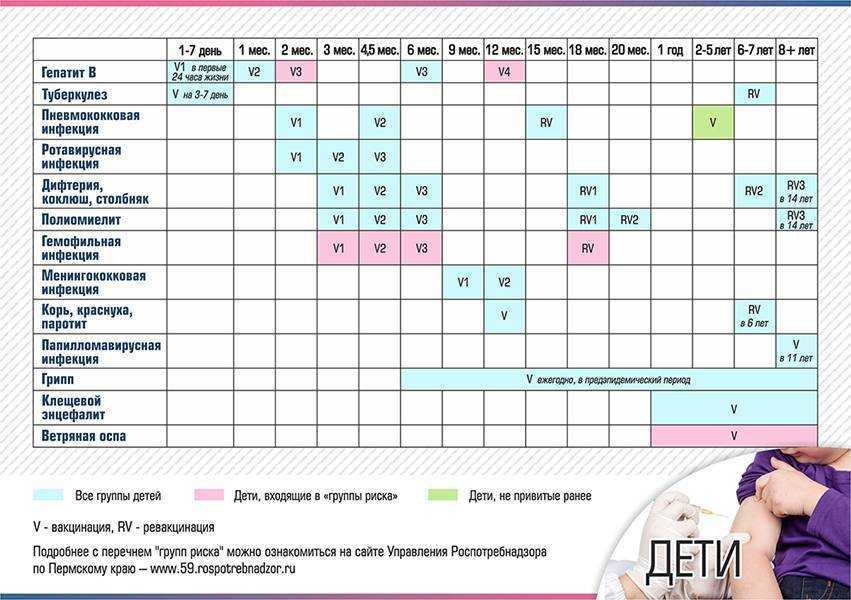
Вакцинация проводится в соответствие с национальным календарем прививок – начиная с 3-х месячного возраста и далее с интервалом в 1,5-2 месяца (в 4. 5 и 6 месяцев). Всего 3 раза, обычно совместно с АКДС. В 18 месяцев проводится первая ревакцинация против полиомиелита, в 20 месяцев – вторая, а третья – в возрасте 14 лет.
5 и 6 месяцев). Всего 3 раза, обычно совместно с АКДС. В 18 месяцев проводится первая ревакцинация против полиомиелита, в 20 месяцев – вторая, а третья – в возрасте 14 лет.
Существует два вида вакцин от полиомиелита – ОПВ и ИПВ. Они обе защищают от всех трех существующих форм вируса полиомиелита. В случае заболевания полиомиелитом иммунитет формируется лишь к одному типу вируса (вызвавшему болезнь), поэтому все равно следует продолжать вакцинацию препаратом ИПВ.
ОПВ – оральная живая вакцина против полиомиелита (содержит живые, но ослабленные вирусы) и применяется в виде капель в рот. После закапывания формирование иммунитета происходит в кишечнике – там вакцинный вирус поселяется и размножается, но не наносит вреда организму. В результате образуются антитела, которые распознают и уничтожают дикие вирусы полиомиелита. Кроме того, в ответ на прививку в организме начинает синтезироваться интерферон, создавая защиту от гриппа и ОРВИ.
Маленьким детям до года препарат капают на корень языка, а детям постарше на небные миндалины. Далее, в течение часа, ребенок не должен ни есть, ни пить. Если сразу после введения ОПВ произошло срыгивание, процедуру необходимо повторить.
Далее, в течение часа, ребенок не должен ни есть, ни пить. Если сразу после введения ОПВ произошло срыгивание, процедуру необходимо повторить.
Реакция организма на введение ОПВ
Изредка бывает небольшое незначительное повышение температуры (не более 37,5 градусов).
У совсем маленьких детей иногда наблюдается небольшое расстройство стула, сохраняющееся 1-2 дня и не требующее лечения (следует исключить кишечную инфекцию, совпавшую по времени с прививкой).
Противопоказания к прививке ОПВ
Противопоказано введение ОПВ детям, имеющим врожденный иммунодефицит или находящимся в контакте с человеком, у которого выявлено иммунодефицитное состояние. Для них существует опасность возникновения вакциноассоциированного полиомиелита (заболевания, вызванного вакцинным вирусом).
Не разрешено делать прививку детям, контактирующим с беременными женщинами. В таких случаях можно применять только вакцину ИПВ, которая не способна привести к таким последствиям.
Если после предыдущего введения ОПВ наблюдались неврологические осложнения, то это тоже является противопоказанием к применению данной вакцины.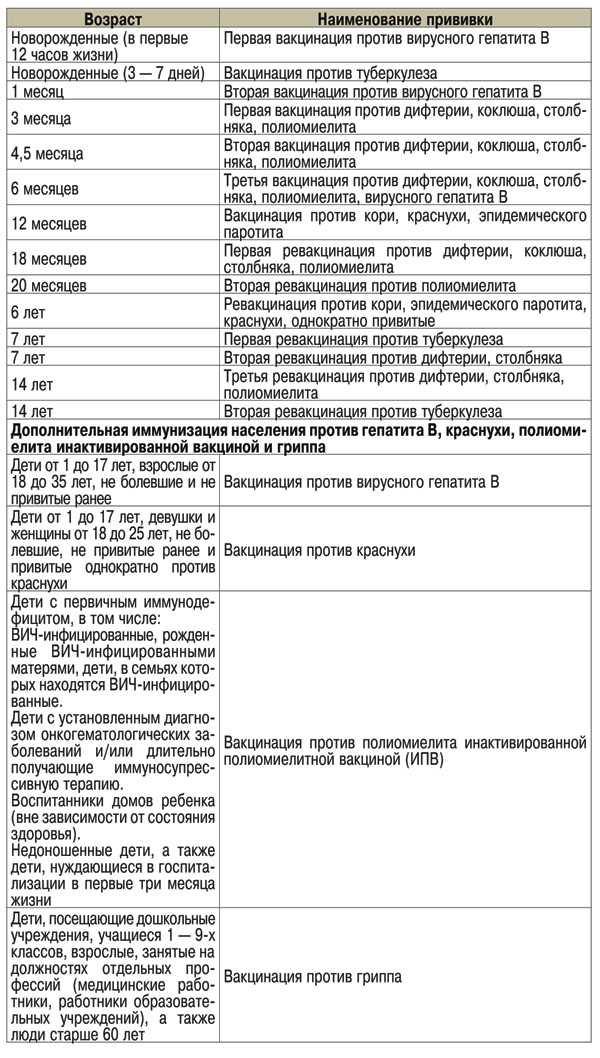
Инактивированная полиомиелитная вакцина — ИПВ
В ее составе имеются не живые, а убитые вирусы полиомиелита. Прививка производится путем инъекции. Детям до 18 месяцев ИПВ вводится подкожно под лопатку, в плечо или внутримышечно в бедро, детям постарше – в плечо. Это более удобная в применении вакцина, но она во много раз дороже, чем ОПВ и пока не производится в нашей стране.
Она также входит в состав комбинированной вакцины ТЕТРАКОК (АКДС+ИПВ).
Ребенок может быть привит ИПВ по желанию родителей на коммерческих условиях.
Реакции на введение полиомиелитной инактивированной вакцины имеют очень незначительную частоту. Они могут иметь вид отека, покраснения и болезненности в месте введения, которые появляются в течение двух суток после прививки и продолжаются до 48 часов. Еще реже бывает непродолжительное повышение температуры.
Нельзя ставить прививку если:
Ребенок болен и у него повышена температура
Имеется аллергия на стрептомицин, неомицин, полимиксин В или компоненты, входящие в состав вакцины
LA Composition du Vaccin Difhtérie Tétanos poliomyéleite
La Diphterie
LE Vaccin Est Compure. [3] Препарат, адсорбирующийся на поверхности алюминия для улучшения иммуногенности. Il существует sous deux formes, валентность D (à 30UI) для вакцинации детей < 10 и валентность d (à 2UI) для вакцинации детей > 10 ans. Il n’existe pas de вакцина моновалентная D, доступная во Франции. Существует вакцина DT, доступная по требованию врача на заводе-изготовителе SANOFI PASTEUR, поставляемая в форме комплекта, входящего в состав антиполиомиелитной вакцины. [2]
[3] Препарат, адсорбирующийся на поверхности алюминия для улучшения иммуногенности. Il существует sous deux formes, валентность D (à 30UI) для вакцинации детей < 10 и валентность d (à 2UI) для вакцинации детей > 10 ans. Il n’existe pas de вакцина моновалентная D, доступная во Франции. Существует вакцина DT, доступная по требованию врача на заводе-изготовителе SANOFI PASTEUR, поставляемая в форме комплекта, входящего в состав антиполиомиелитной вакцины. [2]
Le Tétanos
LE Vaccin EST COMITUSE DE L’Anatoxine Tétanique Inactivée Dans Le Formol. Препарат адсорбируется гидроксидом или фосфатом алюминия. [3]
La Poliomeélite
Le Vaccin inactivé est préparé à partir de trois souches de pololie-virus (40ui d’ontigènes d de la souche i ou ou ou mahoney, 8ui de la ii ii mef1 32 UI de la III ou Saukett). Les souchesviruses sontculivéessur des lignéescellulaires продолжает Vero (isolées à partir de cellules épithéliales de reinde de single vert). Elles неактивны по форме. Пероральная вакцина (источник вируса полиомиелита Сэбина) сыворотки prochainement заброшена в l’échelle mondiale par l’OMS en faveur du vaccin inactive. [4]
Elles неактивны по форме. Пероральная вакцина (источник вируса полиомиелита Сэбина) сыворотки prochainement заброшена в l’échelle mondiale par l’OMS en faveur du vaccin inactive. [4]
Композиция DES Vaccins Disponibles [1], [5]
Источники
Base de données publique des médicaments — rechercher un médicament — ANSM [Интернет]. [цитируется 25 мая 2022 г.]. Доступен по адресу: http://m.base-donnees-publique.medicaments.gouv.fr/#!accueil
DT VAX, Вакцина дифтерическая и противостолбнячная адсорбированная (суспензия для инъекций, многодозовая во флаконе) — Разрыв запасов — ANSM: Национальное агентство по безопасности лекарственных средств и продукции здравоохранения [Интернет]. [цитируется 25 мая 2022 г.]. Доступен по адресу: http://ansm.sante.fr/S-informer/Informations-de-securite-Ruptures-de-stock-des-medicaments/DT-VAX-Vaccin-diphterique-et-tetanique-adsorbe-Suspension-injectable -en-flacon-multidose-Rupture-de-stock
May_2014_DTP_final_FR.
 pdf [Интернет]. [цитируется 25 мая 2022 г.]. Доступен по адресу: http://www.who.int/vaccine_safety/initiative/tools/May_2014_DTP_final_FR.pdf?ua=1
pdf [Интернет]. [цитируется 25 мая 2022 г.]. Доступен по адресу: http://www.who.int/vaccine_safety/initiative/tools/May_2014_DTP_final_FR.pdf?ua=1 May_2014_Polio_final_FR.pdf [Интернет]. [цитируется 25 мая 2022 г.]. Доступен по адресу: http://www.who.int/vaccine_safety/initiative/tools/May_2014_Polio_final_FR.pdf?ua=1
Вакцины — MesVaccins.net [Интернет]. [цитируется 25 мая 2022 г.]. Доступен по адресу: https://www.mesvaccins.net/web/vaccines
- Письмо П. БАЛДИСЯКА, Ф. БЕРТРАНА и Ж. ЛЕГРАНА, релекция доктора А. ТИЛЛИ
Адреса: 20399
IMOVAX ПОЛИОМИЕЛИТ — MesVaccins.
 net
net
Вакцина доступна.
Описание
Вакцина полиомиелитная неактивная.
класс
Inerte
— Entier inactive
Форма и презентация
Суспензия для инъекций в предварительном приготовлении.
IMOVAX POLIO представляет собой прозрачную и бесцветную суспензию.
Природа и содержание внешней эмболии
- 0,5 мл суспензии для инъекций в форме премпли (verre de type I) муни д’ун бушон-поршень (бромбутил или хлорбутил или хлорбромбутил).
Boîte de 1 ou de 20. - 0,5 мл суспензии для инъекций в предварительном наборе (verre de type I) муни с бушон-поршнем (бромбутил или хлорбутил или хлорбромбутил), с наконечником-крышкой, с 1 и 2 отдельными кончиками.

Бот де 1.
Рекламодатели для коммерческих презентаций.
Сочинение
Единая доза (0,5 мл), состав:
1. Антиген
- Вирус полиомиелита 1 неактивный тип 1 (суш Махони): 40 UD 2, 3
- Вирус полиомиелита 1 неактивный тип 2 (например, MEF-1): 8 UD 2, 3
- Вирус полиомиелита 1 неактивный тип 3 (суш Saukett): 32 UD 2, 3
1: продукция на ячейках Vero;
2 : UD = Unité антиген D;
3 : количество антигена, эквивалентное определению, соответствующему иммунохимическому методу.
2. Вспомогательные вещества
- 2-феноксиэтанол (су-ла-форма одного раствора 2-феноксиэтанола до 50 % в этаноле)
- Этанол (2 мг)
- Формальдегид
- Milieu 199 de Hanks (sans rouge de phénol: меланж комплекс аминов кислот [без фенилаланина — 12,5 мкг], минералы, витамины и другие компоненты [comme le глюкоза], добавка полисорбата 80, разбавленный водой для инъекций)
- Кислота хлоргидрик или гидроксид натрия для регулировки pH
IMOVAX POLIO содержит следы неомицина, стрептомицина и полимиксина B (рубрика «Противопоказания»).
Се вакцина соответствует спецификациям европейской фармакопеи и рекомендациям OMS.
Показания
Эта вакцина является показанной для профилактики полиомиелита у детей, детей и взрослых, а также при прививке, проведенной на спуске.
IMOVAX POLIO используется в соответствии с применимыми официальными рекомендациями.
Позология
1. Детское население
Схема, соответствующая французским рекомендациям:
- 2 инъекции à deux mois d’intervalle, une à l’age de 2 mois et une à l’age de 4 mois (прививка) suivies d’un premier rappel à l’age de 11 mois.
Другие схемы posologiques соответствуют национальным рекомендациям en vigueur et à appliquer selon les recommandations de l’OMS selon les cas:
- в течение 6 месяцев или в течение 2 месяцев, удобному для администратора 3 последовательные дозы по 0,5 мл IMOVAX POLIO в или два раза в интервале времени первый спуск от 6 до 12 месяцев после последней дозы;
- Вакцина против полиомиелита пероральная живая (трехвалентная, двухвалентная или моновалентная ОПВ) используется в рамках программы плановой вакцинации, IMOVAX POLIO peut être utilisé en Association (co-administration) ou de façon séquentielle avec OPV, соответствие рекомендациям de l’OMS et en Accord avec les recommandations nationales en vigueur.

Les rappels suivants éventuels (во время детства, во время подросткового возраста и во взрослом возрасте) doivent être administrés conformément aux nationales en vigueur.
2. Взрослое население
Схема, соответствующая французским рекомендациям:
- chez l’adulte non vacciné, il convient d’adistrer 2 последовательные дозы по 0,5 мл à deux mois d’intervalle suivies d’un premier rappel 8 до 12 месяцев после первой дозы.
Другие схемы posologiques соответствуют национальным рекомендациям en vigueur et à appliquer selon les recommandations de l’OMS selon les cas :
- chez l’adulte non vacciné, il convient d’administrer 2 дозы по 0,5 мл один за другим, предпочтительно, deux mois d’intervalle suivies d’premier rappel 6 до 12 месяцев после последней дозы.
Les rappels suivants éventuels doivent être administrés conformémentaux aux recommandations nationales en vigueur.
Режим управления
Администрация по факту внутримышечного введения (IM) de preférence, ou sous-cutanée (SC).
Внутримышечная инъекция, предпочтительнее в передне-латеральную сторону лица, а также в дельтовидную мышцу ребенка, подростка и взрослого.
Противопоказания
Повышенная чувствительность к активным веществам или вспомогательным веществам, упомянутым в рубрике «Композиция», или ко всем вакцинным веществам, содержащим вещества, такие как неомицин, стрептомицин и полимиксин B.
Противопоказания к транзиторной прививке от всеобщей вакцинации: в случае болезни или эпидемии, в отличие от вакцинации.
Mises en garde et précautions d’emploi
Трасабилите
Afin d’améliorer la traçabilité des produits biologiques, le nom et le numero de lot du produit administré doivent être clairement enregistrés.
Ne pas injector par voie intravasculaire: s’assurer que l’aiguille ne pénètre pas dans un vaisseau sanguin.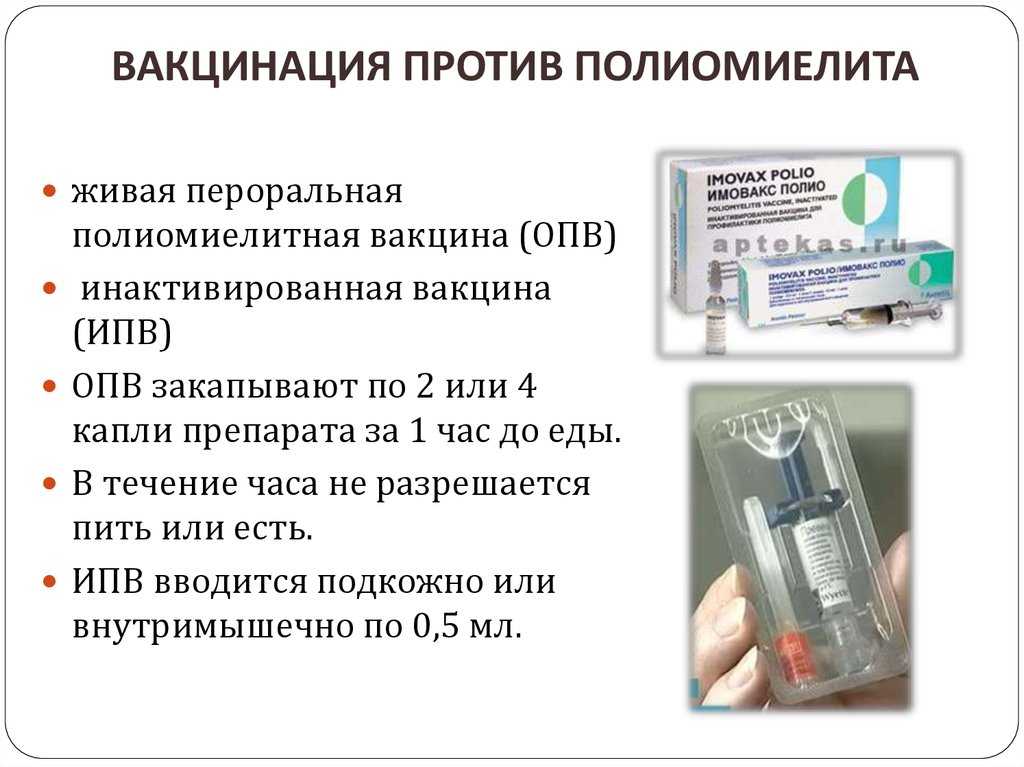
Comme tout вакцина для инъекций, IMOVAX POLIO doit être administré avec précaution en cas de тромбоцитопения или проблем с коагуляцией car l’injection intramusculaire peut engenrer un saignement chez ces sujets.
Comme pour tout вакцина для инъекций, одобренная с медицинской точки зрения, является доступной для немедленного использования и подлежит наблюдению за анафилактической реакцией, редко наблюдаемой после введения вакцины.
Иммунодепрессант или уровень иммунодефицита, вызывающий снижение иммунного ответа на вакцину. Il est alors recommandé d’attendre la fin du traitement pour vacker ou de s’assurer de la bonne protection du sujet. Néanmoins, la вакцинация де sujets présentant une хроническая иммунодепрессия, Telle qu’une инфекция par le VIH, est recommandée si la maladie sous-jacente permet une réponse en anticorps, même limitée.
IMOVAX POLIO peut également être recommandé chez les sujets pour lesquels le vaccin Oral est contre-indiqué, ainsi qu’en rappel pour les sujets préalablement vaccinés avec le оральная вакцина.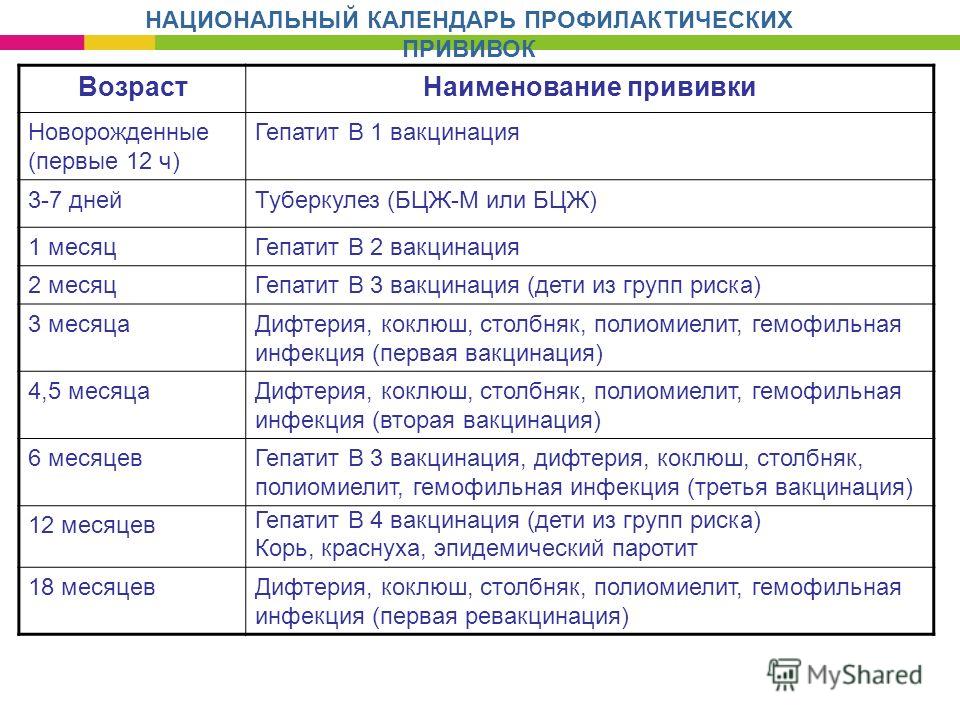
Le risque potentiel d’apnée avec nécessité de Observation Respiratoire Pendant 48-72 h doit être soigneusement pris en compte lors de l’administration des doses de primovaccation chez les grands prématurés (nés à 28 semaines de Grossesse ou Moins) et particulièrement chez ceux ayant des antécédents d’inmaturité respiratoire. En raison du benéfice élevé de la вакцинация chez ces nourrissons, l’administration ne doit pas être suspendue ou reportée.
Обморок (обморок), психогенная реакция на инъекцию с одной стороны, послеоперационный период, последующая вакцинация. Des mesures doivent être mises en place pour prévenir toute blessure due à l’évanouissement et prendre en charge les réactions syncopales.
IMOVAX POLIO, содержащий фенилалаланин, этанол и натрий
IMOVAX POLIO, содержащий 12,5 мкг фенилаланина в дозе 0,5 мл. Фенилаланин опасен для пациентов с фенилкетонурией (PCU), имеет редкую генетическую болезнь, характерную для накопления фенилаланина, что может привести к элиминированной коррекции.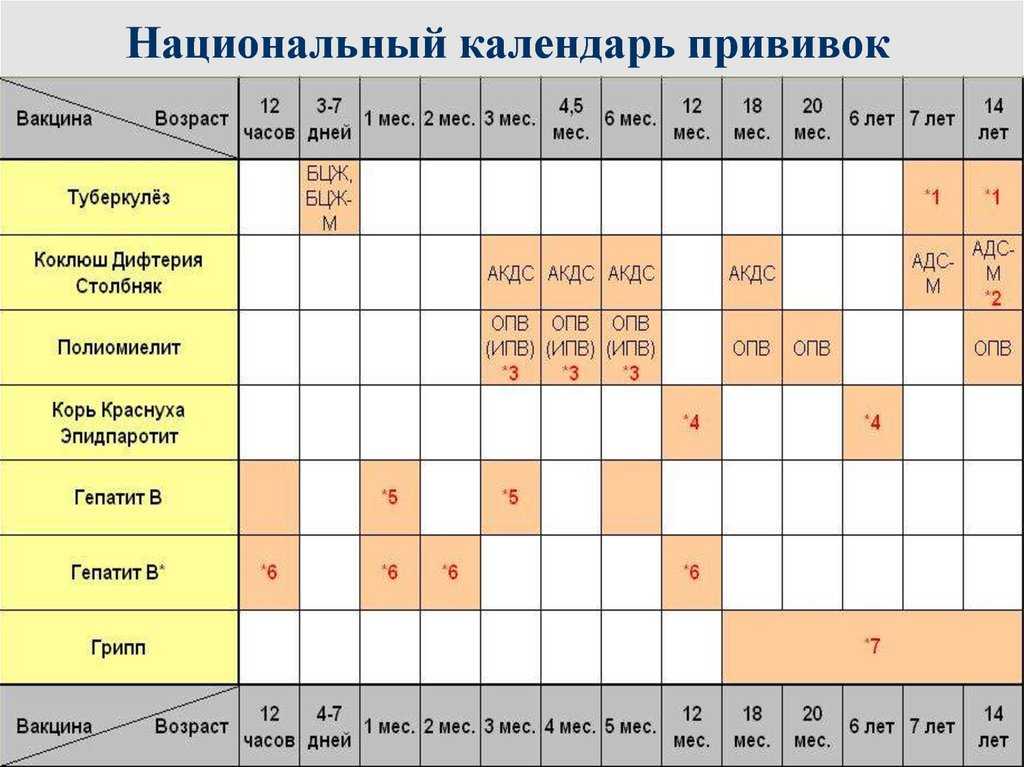
IMOVAX POLIO содержит 2 мг спирта (этанола) по 0,5 мл. La faible quantité d’alcool contenue dans ce médicament n’est pas восприимчивый d’entrainer d’effet примечательный.
IMOVAX POLIO содержит меньшее количество 1 ммоль (23 мг) натрия, номинальная доза, которая является незаменимой «без натрия».
Взаимодействия
Неудобный переход к администрированию IMOVAX POLIO au coours de la même séance de вакцинация с использованием других вакцин. En cas d’administration concomitante, des seringues différentes et des site d’injection séparés doivent être utilisés.
Гроссесс
Compte tenu des données cliniques, ce vaccin peut être prescrit Pendant la grassesse en cas de à à risque важная ситуация.
Фертилите
Aucune etude sur la fécondité n’a été réalisée.
Умиротворение
Возможное использование вакцины против коронавируса.
Нежелательные эффекты
1. Резюме нежелательных эффектов
Нежелательные эффекты в соответствии с классами терминологии MedDRA (по системе органов) и по частоте, выбранной по соглашению:
- очень часто: ≥ 10%;
- часто: ≥ 1% и 10%;
- част.: ≥ 0,1% и 1%;
- редко: ≥ 0,01% и 0,1%;
- три редкости: 0,01%;
- fréquence indéterminée ne peut être estimée sur la base des données disponibles.
Послеобеденные уведомления о спонтанных сообщениях, определенных нежелательных событиях и других случаях, связанных с использованием
Д’ИМОВАКС ПОЛИО. Les événements étant rapportés de façon volontaire à partir d’une населения de taille incertaine, il n’est pas toujours, возможный d’estimer de façon fiable leur frequence ou d’établir une отношения causale avec l’exposition au vaccin. Par conséquent, ces événements indésirables sont classés dans la catégorie de fréquence «Indéterminée».
Par conséquent, ces événements indésirables sont classés dans la catégorie de fréquence «Indéterminée».
Les événements listés ci-dessous ont été observés lors des études cliniques ou ont été rapportés spontanément après коммерциализации.
Нежелательные эффекты плюс частые реакции после введения вакцины, связанные с местными реакциями в месте инъекции (доулер, покраснение, отвердение) и сверхвысокой температурой 38,1 °C.
Заболевания системы иммунитета
- Неопределенная частота: реакция гиперчувствительности типа I на компоненты вакцины, тип крапивницы, ангионевротический отек, анафилактическая реакция или анафилактическая реакция на шок.
Заболевания психиатрические
- Неопределенная частота: ажитация, сонливость и раздражительность в первые дни после вакцинации и т. д.
непреодолимое ускорение.
Заболевания нервной системы
- Неопределенная частота: конвульсии (ассоциированные или не связанные с а-де-ла-фиевром) в дни, связанные с вакцинацией, головные боли,
paresthésies modérées et transoires (principalement des membres inférieurs) survenant dans les deux semaines après la
вакцинация.
Привязанность к воде и тканям sous-cutané
- Неопределенная частота: сыпь.
Заболевания опорно-двигательного аппарата и систем
- Неопределенная частота: умеренные и транзиторные артралгии и миалгии в дни после вакцинации.
Общие проблемы и аномалии в администрации
- Частые : douleur au site d’injection, fièvre superieure à 38,1 °C.
- Частые: rougeur au site d’injection.
- Peu frequent: уплотнение в месте инъекции.
- Неопределенная частота: лимфаденопатии, локальные реакции в месте инъекции типа отека, вызывающего наблюдение за 48
Heures suivant la вакцинация и др постоянный un ou deux jours.
Дополнительная информация, касающаяся отдельных групп населения
Apnée chez les grands prématurés (nés à 28 semaines de grassesse ou moins) voir rubrique «Mises en garde et précautions d’emploi».
2. Влияние на способность управлять транспортными средствами и использовать машины
Les effets sur l’aptitude à conduire des Vehicles et à utiliser des Machines n’ont pas été etudiés.
3. Сурдозировка
Без объекта.
4. Заявление о нежелательных действиях подозреваемых
La déclaration des effets indésirablesподозреваемые после авторизации дю Médicament est Importante. Elle permet une наблюдение продолжается du rapport benéfice/risque du médicament. Профессиональные работники в области здравоохранения объявляют о нежелательных подозреваемых действиях через национальную систему декларации: Национальное агентство по безопасности лекарственных средств и продуктов здравоохранения (ANSM) и центр региональных центров фармаконадзора — Интернет-сайт: www.signalement-sante.gouv.fr .
Фармакодинамика
Фармакотерапевтический класс: Вакцина против полиомиелита.
Код УВД: J07BF03.
Вакцина, приготовленная из части вируса полиомиелита типов 1, 2 и 3, культивируемых на клетках Vero, очищенная и неактивная на основе формальдегида.
Un mois après la primovacmination (3 дозы), les taux de séroprotection étaient de 100 % pour les poliomyélitiques вакцины типов 1, 3 и 99 % до 100 % литья типа 2.
Chez le nourrisson, la dose de rappel (4-я доза) является важным каналом повышения титров с уровнем серопротекции от 97,5 % до 100 % для 3 типов полиомиелитных вирусов.
Quatre à cinq ans après la dose de rappel, 94–99 % des sujets avaient des titres protecteurs.
Chez l’adulte primovacciné, une инъекции de rappel est suivie par une réponse anamnestique.
Ces données sont, pour la majorité, выпуски реальных исследований с вакцинами, содержащими полиомиелитные вакцины.
Иммунитет поддерживает подвеску в течение 5 дней после 4-х инъекций.
Сохранение
Продолжительность консервации: 3 ан.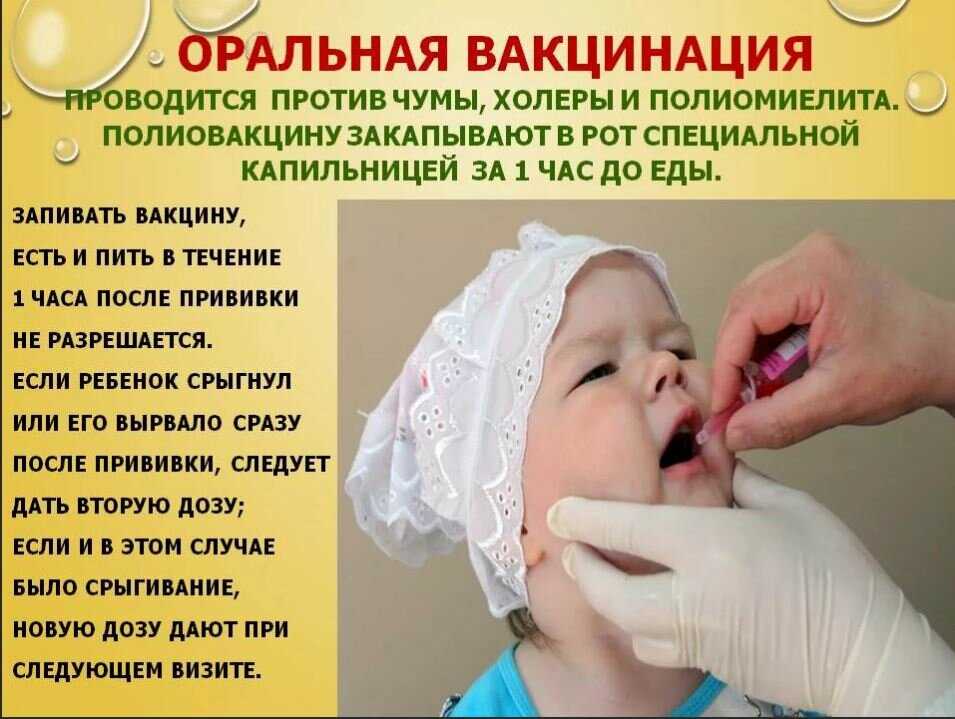
Консерватор в холодильнике (внутри + 2 °C и + 8 °C) и на свету.
Ne pas congeler.
Манипуляции
Проверка прозрачности и бесцветности вакцины. Ne pas utiliser si le produit представляет проблему с аспектом.
Pour les seringues sans aiguilletachée, l’aiguille doit être montée fermement sur la seringue en opérant une d’un quart de tour.
Tout produit non utilisé ou déchet doit être éliminé selon la réglementation en vigueur.
En l’absence d’études de compatibilité, ce médicament ne doit pas être mélange avec d’autres médicaments.
L’administration du vaccin doit être consignée par le médecin sur le carnet de вакцинация ou de santé avec le numéro de lot. Il peut aussi être inscrit par ле пациента или сына médecin сюр ип книжка де вакцинации électronique.
Рембурсмент
Remboursé par la Sécutité sociale на 65 %.

 pdf [Интернет]. [цитируется 25 мая 2022 г.]. Доступен по адресу: http://www.who.int/vaccine_safety/initiative/tools/May_2014_DTP_final_FR.pdf?ua=1
pdf [Интернет]. [цитируется 25 мая 2022 г.]. Доступен по адресу: http://www.who.int/vaccine_safety/initiative/tools/May_2014_DTP_final_FR.pdf?ua=1 

