Содержание
лиофилизат для приготовления суспензии для подкожного введения — Энциклопедия лекарств РЛС
Аналоги
Все формы выпуска, дозировки, регистрационные удостоверения, производители лекарства, характеристики препарата
Вакцина сибиреязвенная комбинированная (лиофилизат для приготовления суспензии для подкожного введения), инструкция по медицинскому применению РУ № ЛСР-009268/08
Дата последнего изменения: 27.04.2017
Содержание
- Действующее вещество
- ATX
- Фармакологическая группа
- Лекарственная форма
- Состав
- Описание лекарственной формы
- Фармакологические свойства
- Показания
- Противопоказания
- Способ применения и дозы
- Побочные действия
- Взаимодействие
- Форма выпуска
- Условия отпуска из аптек
- Условия хранения
- Срок годности
- Отзывы
Действующее вещество
Вакцина для профилактики сибирской язвы (Vaccine anthrax)
ATX
J07AC01 Сибиреязвенный антиген
Фармакологическая группа
Вакцины, сыворотки, фаги и анатоксины
Лекарственная форма
Лиофилизата для приготовления суспензии для подкожного введения
Состав
Вакцина сибиреязвенная комбинированная, лиофилизат для приготовления суспензии для подкожного введения представляет собой смесь живых спор вакцинного штамма Bacillus anthracis СТИ-1 (500 млн. спор в ампуле) и очищенного концентрированного протективного сибиреязвенного антигена (350 ИД50 для белых мышей в ампуле), адсорбированного на геле алюминия гидроксида (не более 25 мг в ампуле), стабилизатор: сахароза (0,2 г в ампуле).
спор в ампуле) и очищенного концентрированного протективного сибиреязвенного антигена (350 ИД50 для белых мышей в ампуле), адсорбированного на геле алюминия гидроксида (не более 25 мг в ампуле), стабилизатор: сахароза (0,2 г в ампуле).
Описание лекарственной формы
Пористая масса серовато-белого цвета.
Фармакологические свойства
Вакцина сибиреязвенная комбинированная обеспечивает формирование специфического иммунитета через 7 суток после прививки продолжительностью до 1 года.
Показания
Специфическая профилактика сибирской язвы у людей с 14-летнего возраста. Вакцинацию проводят в плановом порядке и по эпидемическим показаниям.
Плановым прививкам подлежат:
- лица, работающие с живыми культурами возбудителя сибирской язвы, с зараженными лабораторными животными или производящие исследования материалов, зараженных возбудителем сибирской язвы;
- лица, производящие убой скота, занятые заготовкой, сбором, хранением, транспортировкой, переработкой и реализацией сырья животного происхождения;
- лица, выполняющие следующие работы на энзоотичных по сибирской язве территориях:
- обслуживание общественного скота;
- сельскохозяйственные, агро- и гидромелиоративные, строительные и другие работы, связанные с выемкой и перемещением грунта;
- заготовительные, промысловые, геологические, изыскательные, экспедиционные.

Противопоказания
1. Острые инфекционные и неинфекционные заболевания — прививки проводят не ранее 1 месяца после выздоровления (ремиссии).
2. Первичные и вторичные иммунодефициты. При лечении стероидами, антиметаболитами, рентгенотерапией прививки проводят не ранее, чем через 6 месяцев после окончания терапии.
3. Злокачественные новообразования и злокачественные болезни крови.
4. Системные заболевания соединительной ткани.
5. Распространенные рецидивирующие болезни кожи.
6. Болезни эндокринной системы.
7. Беременность и период лактации.
В каждом отдельном случае при заболеваниях, не содержащихся в настоящем перечне, вакцинация проводится лишь по разрешению соответствующего врача-специалиста.
С целью выявления противопоказаний врач (фельдшер) в день прививки проводит опрос и осмотр прививаемых с обязательной термометрией.
Способ применения и дозы
Вакцинацию проводит средний медицинский персонал под руководством врача. Первичную иммунизацию проводят однократно подкожно шприцевым или безыгольным способами.
Первичную иммунизацию проводят однократно подкожно шприцевым или безыгольным способами.
Ревакцинацию проводят однократно. Первые три ревакцинации осуществляют ежегодно. Все последующие ревакцинации проводят один раз в два года.
Перед использованием каждую ампулу с вакциной тщательно просматривают. Не подлежит применению вакцина при повреждении целостности ампулы, изменении внешнего вида препарата (посторонние частицы, неразбившиеся комки и хлопья), отсутствии этикетки, истечении срока годности. Ампулу с вакциной протирают 70 % спиртом, надпиливают шейку ампулы, накрывают стерильным тампоном, отламывают надпиленный конец ампулы. С помощью стерильного шприца с иглой в ампулу вводят 5,0 мл растворителя — стерильного натрия хлорида раствора 0,9% и встряхивают до образования гомогенной суспензии серовато-белого цвета. Время растворения вакцины не должно превышать 5 мин. Растворенная вакцина, сохраняемая в асептических условиях, может быть использована в течение 4 ч.
1. Вакцинация шприцевым способом. Вакцину в объеме 0,5 мл вводят подкожно в область нижнего угла левой лопатки одноразовым шприцем. Кожу на месте инъекции обрабатывают 70% спиртом. Перед каждым отбором вакцины ампулу встряхивают. Место инъекции обрабатывают 5% настойкой йода.
Вакцину в объеме 0,5 мл вводят подкожно в область нижнего угла левой лопатки одноразовым шприцем. Кожу на месте инъекции обрабатывают 70% спиртом. Перед каждым отбором вакцины ампулу встряхивают. Место инъекции обрабатывают 5% настойкой йода.
2. Вакцинация безыгольным способом. Вакцину в объеме 0,5 мл вводят подкожно в область наружной поверхности верхней трети плеча безыгольным инъектором с протектором при строгом соблюдении инструкции по его применению. Место введения вакцины до и после инъекции обрабатывают как при шприцевом методе вакцинации.
Неиспользованная вакцина, использованные прививочные одноразовые шприцы и иглы подлежат обязательной инактивации автоклавированием при температуре (132±2) °С и давлении 2,0 кГс/м2 в течение 90 мин.
Части безыгольного инъектора, соприкасавшиеся с вакциной, погружают в 6% раствор перекиси водорода с добавлением 0,5% моющего средства типа «Прогресс» или «Астра» на 1 ч при температуре не ниже 50 °С. Раствор используют однократно. Затем проводят предстерилизационную обработку инъектора:
Затем проводят предстерилизационную обработку инъектора:
а) ополаскивание под проточной водой в течение 0,5 мин;
б) замачивание при полном погружении в моющий раствор при температуре 50°С на 15 мин. Рецептура 1 л моющего раствора: 17 г пергидроля (27,5 г 33% перекиси водорода), 5 г моющего средства и 978 мл воды;
в) мойка в моющем растворе при помощи ерша или ватно-марлевого тампона каждого предмета в течение 0,5 мин;
г) ополаскивание под проточной водой в течение 10 мин;
д) ополаскивание дистиллированной водой в течение 0,5 мин каждого предмета;
е) сушка до полного исчезновения влаги.
Стерилизацию частей безыгольного инъектора проводят автоклавированием при температуре (132±2)°С и давлении 2,0 кГс/м2 в течение 90 мин.
Побочные действия
Реакция на введение.
Прививки вакциной могут сопровождаться местными реакциями, интенсивность которых зависит от индивидуальных особенностей привитых. Через 24-48 ч после вакцинации на месте инъекции могут возникнуть болезненность, гиперемия, реже — инфильтрат диаметром до 50 мм.
Через 24-48 ч после вакцинации на месте инъекции могут возникнуть болезненность, гиперемия, реже — инфильтрат диаметром до 50 мм.
Побочное действие.
Может проявляться в первые сутки после прививки недомоганием, головной болью и повышением температуры тела до 38,5 °С.
Взаимодействие
Интервал между вакцинацией против сибирской язвы и введением других вакцин должен быть не менее одного месяца, а в отношении детских контингентов — не менее двух месяцев. Вакцина чувствительна к антибиотикам, в связи с чем иммунизация на фоне применения антибиотиков не допускается.
Форма выпуска
По 10 доз в ампуле, растворитель — натрия хлорида раствор 0,9 % — по 6 мл в ампуле.
Упаковка содержит 5 ампул вакцины, 5 ампул растворителя, инструкцию по применению и ампульный нож.
Условия отпуска из аптек
Для лечебно-профилактических и санитарно- профилактических учреждений.
Условия хранения
Хранят в соответствии с СП 3.3.2.1248-03 при температуре от 0 до 8 °С в недоступном для детей месте.
Транспортируют в соответствии с СП 3.3.2.1248-03 при температуре от 0 до 8 °С.
Срок годности
Срок годности 3 года. Препарат с истекшим сроком годности применению не подлежит.
Отзывы
«Ветеринария.рф»: Олег Скляров: «Причиной осложнений может быть не вакцина, а нарушение правил ее применения»
Источник: Ветеринария.рф
Споры сибирской язвы – особо опасной зоонозной инфекции – устойчивы к высокой температуре, могут сохраняться в почве долгое время. Для профилактики заболевания в России проводится массовая вакцинация сельскохозяйственных животных. У основной их части создается напряженный иммунитет, однако у коз и некоторых других животных фиксируются поствакцинальные осложнения. Сотрудники Всероссийского государственного Центра качества и стандартизации лекарственных средств для животных и кормов (ВГНКИ) приступают к исследованию, которое позволит повысить безопасность и эффективность иммунизации. О задачах и деталях предстоящей работы нам рассказал заведующий лабораторией качества и стандартизации бактерийных лекарственных средств ФГБУ «ВГНКИ», доктор ветеринарных наук Олег Скляров.
– Олег Дмитриевич, какая вакцина против сибирской язвы применяется сегодня?
– Вакцина против сибирской язвы сельскохозяйственных животных (крупного и мелкого рогатого скота, лошадей, ослов, верблюдов, оленей, свиней, пушных зверей) живая, жидкая или сухая различных отечественных производителей, а также ассоциированная вакциной против сибирской язвы и эмфизематозного карбункула – для крупного рогатого скота.
– Насколько часто фиксируются случаи поствакцинальных осложнений?
– Периодически в адрес ВГНКИ поступают данные о случаях поствакцинальных осложнений у сельскохозяйственных животных в результате профилактической иммунизации против сибирской язвы. Эта информация касается преимущественно коз, иногда лошадей и крупного рогатого скота. В частности, Комитет ветеринарии города Москвы и Главное управление ветеринарии Московской области сообщали о пяти таких случаях в 2013 году, о четырех – в 2014-м и девяти – в 2015-м. Были зафиксированы факты осложнений после вакцинации у коз в селе Васильевка Воронежской области, у пяти голов крупного рогатого скота в Бурятии (четыре из них погибли), у четырех коз в Павлово-Посадском районе Московской области, где одно животное погибло.
– Кто фиксирует случаи осложнений после вакцинации?
– Как правило, подобные случаи регистрируются сотрудниками территориальных управлений Россельхознадзора или управлений ветеринарии субъектов. Они же или сами владельцы пострадавших животных доводят эту информацию до производителя вакцины.
Кроме того, после принятия закона «О защите прав потребителей» разбирательство по таким случаям ведется между владельцем и организацией-производителем препарата. ВГНКИ может участвовать и участвует в проведении арбитражных испытаний образцов препарата с мест применения. Мы контролируем образцы вакцины этой же серии, отобранные из архива производителя в соответствии с требованиями нормативных документов, регламентирующих качество препаратов.
– Всегда ли удается точно установить причину осложнений?
– Не всегда просто это сделать, поскольку причиной может быть вовсе не вакцина, а нарушение порядка ее применения, прописанного в инструкции к препарату. Например, если проводится иммунизация клинически больных животных или животных с латентной формой болезни. Бывает, что не учитываются возрастные ограничения при иммунизации либо вакцинируют в холодное время года.
Бывает, что не учитываются возрастные ограничения при иммунизации либо вакцинируют в холодное время года.
– Насколько совершенны методики контроля безвредности вакцин?
– Согласно требованиям нормативных документов и ГОСТ Р 52616-2006 «Вакцина против сибирской язвы животных из штамма 55-ВНИИВВиМ живая» контроль сибиреязвенных вакцин по показателю качества «безвредность» проводится на кроликах. По данным испытаний рекламационных и архивных образцов вакцин, а также образцов, проверенных нашей организацией за последние пять лет в рамках лекарственного мониторинга и выборочного контроля качества лекарственных средств, вакцины по показателю «безвредность» практически всегда соответствовали требованиям нормативных документов. Это предполагает использование при проверке вакцин на безвредность другой модели животных, например, овец и (или) коз, что, кстати, регламентировано Руководством по диагностическим тестам и вакцинам Международного эпизоотического бюро. Конечно, это отразится на стоимости контроля и цене вакцины.
– Что послужило предпосылкой для новой научно-исследовательской работы в этом направлении?
– Проблема с иммунным статусом коз, возникающая в результате вакцинации животных против сибирской язвы и иногда приводящая к их гибели, вызывает недовольство владельцев. Периодически поступают рекламации и сообщения о случаях поствакцинальных осложнений. Поэтому встал вопрос о необходимости совершенствования методики контроля качества сибиреязвенных вакцин. Научно-техническая комиссия Россельхознадзора утвердила программу и этапы научно-исследовательской работы, цель которой – повышение эффективности и безопасности сибиреязвенной вакцины, применяемой в России.
– Какие задачи планируется решить в рамках данной работы?
– Прежде всего предстоит определить чувствительность коз различных пород к сибиреязвенным вакцинам отечественных производителей с учётом местных и общих реакций организма в поствакцинальный период. Также необходимо установить оптимальную иммунизирующую дозу и разработать схему иммунизации коз против сибирской язвы. При этом будут учитываться результаты изучения чувствительности животных к культурам разных вакцинных штаммов. Еще одна задача – совершенствовать методику контроля качества сибиреязвенных вакцин по показателю «безвредность».
При этом будут учитываться результаты изучения чувствительности животных к культурам разных вакцинных штаммов. Еще одна задача – совершенствовать методику контроля качества сибиреязвенных вакцин по показателю «безвредность».
– Сколько времени отводится для решения этих задач?
– Выполнение работы запланировано на период с 2019 по 2021 годы. Ответственным ее исполнителем является заместитель заведующего лабораторией качества и стандартизации бактерийных лекарственных средств ФГБУ «ВГНКИ», кандидат ветеринарных наук, доцент Лусине Гамлетовна Цатурян, которая специализируется на изучении этого зооноза. В работе будут участвовать научные и младшие сотрудники этой лаборатории.
Ученым предстоит осуществлять мониторинг содержания титра антител в крови вакцинированных животных. В испытаниях примут участие представители всех пород коз, которые встречаются на территории нашей страны.
– Как будут использоваться полученные результаты?
– По окончании научно-исследовательской работы будет предложена оптимальная схема иммунизации коз, других животных против сибирской язвы и даны соответствующие методические рекомендации. Полученные результаты послужат основанием для внесения изменений в ГОСТ Р 52616-2006, а также в нормативные документы производителей вакцин с учетом их согласия. Исследование, направленное на повышение эффективности и безопасности сибиреязвенных вакцин, должно помочь преодолеть нежелание владельцев вакцинировать животных против сибирской язвы, а также их недоверие к ветеринарным врачам.
Полученные результаты послужат основанием для внесения изменений в ГОСТ Р 52616-2006, а также в нормативные документы производителей вакцин с учетом их согласия. Исследование, направленное на повышение эффективности и безопасности сибиреязвенных вакцин, должно помочь преодолеть нежелание владельцев вакцинировать животных против сибирской язвы, а также их недоверие к ветеринарным врачам.
Стоит отметить, что эта актуальная проблема должна быть решена максимально оперативно. Причем ее решение зависит не только от специалистов ВГНКИ, но и производителей вакцин, ветеринарных служб страны независимо от их ведомственной подчиненности, а также от владельцев животных. Необходимы совместные усилия всех заинтересованных сторон. Бездействие будет способствовать сохранению риска возникновения новых сибиреязвенных очагов со всеми присущими этому негативными последствиями.
GAO: Военные прививки от сибирской язвы вызвали множество реакций, побудили некоторых пилотов уйти
8 ноября 2002 г. (Новости CIDRAP) Обязательные прививки Пентагона от сибирской язвы вызвали негативную реакцию у большинства получателей и помогли многим военнослужащим резерва ВВС и Национальной гвардии ВВС перейти в другие подразделения или покинуть армию в период с 1998 по 2000 год, согласно опросу. Генеральным бухгалтерским управлением Конгресса (GAO).
(Новости CIDRAP) Обязательные прививки Пентагона от сибирской язвы вызвали негативную реакцию у большинства получателей и помогли многим военнослужащим резерва ВВС и Национальной гвардии ВВС перейти в другие подразделения или покинуть армию в период с 1998 по 2000 год, согласно опросу. Генеральным бухгалтерским управлением Конгресса (GAO).
Опрос показал, что у 85% военнослужащих, получивших прививку от сибирской язвы, были побочные реакции, что намного выше, чем 30%, заявленные производителем в 2000 году, когда проводился опрос. Шестнадцать процентов респондентов либо уволились из армии, либо изменили свой статус, по крайней мере частично, из-за программы вакцинации.
Программа «похоже, отрицательно сказалась на ВВС Национальной гвардии и резерве ВВС с точки зрения удержания необходимого опытного персонала», — говорится в отчете, опубликованном в конце октября. GAO рекомендовало Министерству обороны (DoD) создать программу активного наблюдения за реакциями на вакцины.
В 1998 году Министерство обороны запустило программу вакцинации всех военнослужащих против сибирской язвы. В 2000 году программа была сокращена до нескольких избранных единиц из-за нехватки вакцины из-за того, что производителю было трудно получить разрешение Управления по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) на свою работу после реконструкции завода. В январе 2002 года FDA наконец одобрило новую систему производства. В мае прошлого года Министерство обороны объявило, что снова активизирует программу вакцинации, но прививки потребуются только персоналу, который находится более 15 дней в зонах повышенного риска.
Хотя опрос был проведен в 2000 году, до террористических атак и атак сибирской язвы в сентябре и октябре 2001 года и до утверждения FDA изменений в производстве, GAO считает, что результаты «все еще актуальны и полезны» как мера эффективности программы вакцинации. говорится в отчете.
Опрос был направлен на случайную выборку из 1253 сотрудников охраны и запаса, выбранных для представления всех пилотов и членов летных экипажей, включая вакцинированный и непривитый персонал. Опрос привлек 67% ответивших; Считается, что процентные результаты точны в пределах плюс-минус 5 баллов.
Опрос привлек 67% ответивших; Считается, что процентные результаты точны в пределах плюс-минус 5 баллов.
Опрос показал, что в период с сентября 1998 г. по сентябрь 2000 г. «около 16 процентов пилотов и членов летного состава караула и резерва были (1) переведены в другое подразделение (в основном на нелетные позиции, чтобы избежать или отсрочить получение прививок от сибирской язвы) ( 2) переведены в неактивное состояние или (3) уволены с военной службы», — говорится в сообщении. «Кроме того, примерно каждый пятый (18 процентов) из тех, кто в 2000 году еще состоял или приписан к части, — то есть те, кто еще не изменил свой статус, — заявили о своей готовности уйти в ближайшем будущем. которые уже ушли, и те, кто заявил о своем намерении уйти, оценили AVIP [Программу вакцинации против сибирской язвы] как ключевой фактор в своем решении уйти или изменить свое участие».
По результатам опроса GAO подсчитало, что к сентябрю 2000 г. 37% членов летных экипажей получили по крайней мере одну прививку от сибирской язвы (по схеме из шести доз). 85% вакцинированных сообщили о побочных реакциях, и каждая прививка вызывала среднее из четырех и более реакций. Почти пятая часть реакций была классифицирована как системная, а пятая из них длилась более недели. В отчете говорится, что на момент опроса на вкладыше к вакцине частота побочных реакций составляла около 30%, а частота системных реакций — 0,2%.
85% вакцинированных сообщили о побочных реакциях, и каждая прививка вызывала среднее из четырех и более реакций. Почти пятая часть реакций была классифицирована как системная, а пятая из них длилась более недели. В отчете говорится, что на момент опроса на вкладыше к вакцине частота побочных реакций составляла около 30%, а частота системных реакций — 0,2%.
«Такие заметные отклонения от данных, прилагаемых к продукту, предполагают возможность изменения состава вакцины по сравнению с вакциной, первоначально одобренной в 1970 году», — говорится в отчете. В нем не обсуждается, может ли более новая вакцина, произведенная на обновленном заводе корпорации BioPort в Лансинге, штат Мичиган, быть более безопасной, чем вакцина, произведенная до реконструкции.
В отчете отмечается, что два краткосрочных военных исследования побочных эффектов вакцины, одно в Корее и одно на Гавайях, дали результаты, аналогичные выводам GAO, и показали, что реакции гораздо чаще встречаются у женщин, чем у мужчин. В отчете говорится, что с 2000 года вкладыш к продукту был пересмотрен, чтобы включить в него результаты этих и других недавних исследований.
В отчете говорится, что с 2000 года вкладыш к продукту был пересмотрен, чтобы включить в него результаты этих и других недавних исследований.
В других выводах опрос показал, что только около 40% членов экипажа были удовлетворены информацией, предоставленной Министерством обороны о программе вакцинации. По оценкам GAO, 77% членов не стали бы принимать вакцину, если бы у них был выбор.
В отчете рекомендуется, чтобы Пентагон разработал программу активного мониторинга реакции на вакцину. Система сообщений о побочных эффектах вакцин (VAERS) доступна для вакцинированных, но это «пассивная» система, основанная на добровольных сообщениях. В отчете говорится, что многие военнослужащие, у которых были реакции на вакцину, не сообщали о них в VAERS или своим поставщикам медицинских услуг Министерства обороны США.
Министерство обороны, когда его пригласили прокомментировать проект отчета GAO, не согласилось с рекомендацией о создании программы активного наблюдения. Департамент процитировал заявление Института медицины в своем отчете о вакцине за март 2002 г. о том, что специальные программы мониторинга не кажутся необходимыми, несмотря на опасения военнослужащих. Но GAO ответило в отчете, что IOM фактически рекомендовало Министерству обороны использовать данные VAERS для выработки гипотез для дальнейшего изучения, а также проводить «специальный мониторинг реакции населения на все вакцины на основе единиц».
Департамент процитировал заявление Института медицины в своем отчете о вакцине за март 2002 г. о том, что специальные программы мониторинга не кажутся необходимыми, несмотря на опасения военнослужащих. Но GAO ответило в отчете, что IOM фактически рекомендовало Министерству обороны использовать данные VAERS для выработки гипотез для дальнейшего изучения, а также проводить «специальный мониторинг реакции населения на все вакцины на основе единиц».
Министерство обороны также отметило, что показатели увольнения пилотов из вооруженных сил были одинаковыми до и после начала программы вакцинации против сибирской язвы в 1998 году. Кроме того, Пентагон заявил, что в отчете не сравниваются показатели текучести летных экипажей, наблюдаемые в опросе, с нормальными или ожидаемыми показателями. .
Но GAO заявило, что военные чиновники не предоставили данных, подтверждающих утверждение о том, что показатели разделения пилотов остались прежними после начала программы вакцинации.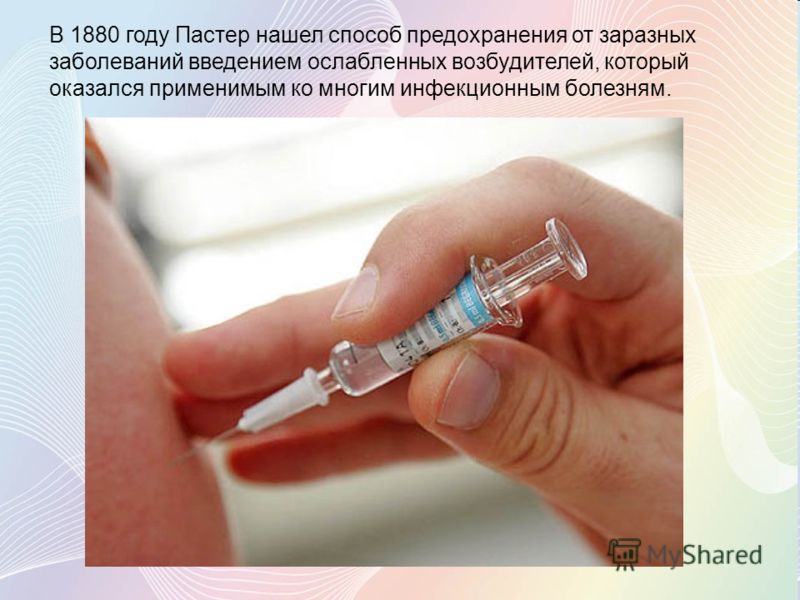 Кроме того, в отчете говорится, что опрос касался всех «изменений статуса», что является более широкой категорией, чем увольнение. Хотя показатели увольнения могли быть одинаковыми до и после появления программы вакцинации, «очевидно, что потери среди наиболее опытных пилотов (на базах, где внедрялась AVIP) в результате изменения статуса на некоторых базах были значительными, что привело к потере очень опытной рабочей силы», — говорится в отчете.
Кроме того, в отчете говорится, что опрос касался всех «изменений статуса», что является более широкой категорией, чем увольнение. Хотя показатели увольнения могли быть одинаковыми до и после появления программы вакцинации, «очевидно, что потери среди наиболее опытных пилотов (на базах, где внедрялась AVIP) в результате изменения статуса на некоторых базах были значительными, что привело к потере очень опытной рабочей силы», — говорится в отчете.
Смотрите также:
Полный текст отчета GAO «Вакцина против сибирской язвы: обследование GAO гвардейских и резервных пилотов и экипажей»
http://www.gao.gov/new.items/d02445.pdf
Вакцина против сибирской язвы: Информация о лекарствах MedlinePlus
Чтобы использовать функции обмена на этой странице, включите JavaScript.
Сибирская язва — серьезное заболевание, которое может поражать как животных, так и людей.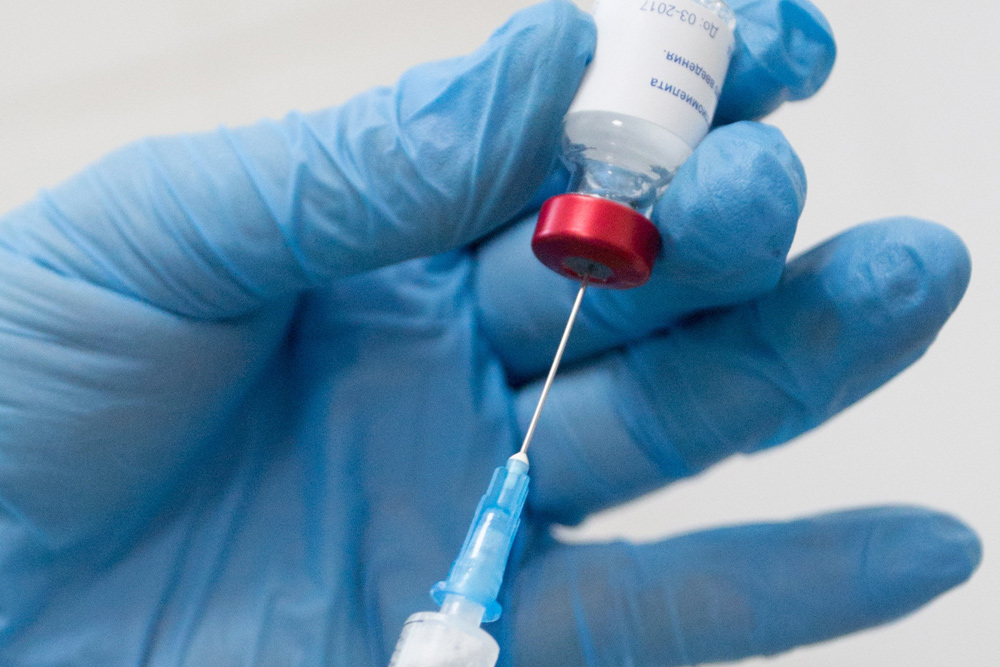 Его вызывают бактерии под названием Bacillus anthracis . Люди могут заразиться сибирской язвой при контакте с инфицированными животными, шерстью, мясом или шкурами.
Его вызывают бактерии под названием Bacillus anthracis . Люди могут заразиться сибирской язвой при контакте с инфицированными животными, шерстью, мясом или шкурами.
Кожная сибирская язва. В своей наиболее распространенной форме сибирская язва представляет собой кожное заболевание, вызывающее кожные язвы и обычно лихорадку и усталость. До 20% этих случаев заканчиваются летальным исходом при отсутствии лечения.
Желудочно-кишечная сибирская язва. Эта форма сибирской язвы может возникнуть в результате употребления в пищу сырого или недоваренного инфицированного мяса. Симптомы могут включать лихорадку, тошноту, рвоту, боль в горле, боль в животе и отек, а также увеличение лимфатических узлов. Желудочно-кишечная форма сибирской язвы может привести к заражению крови, шоку и смерти.
Вдыхание сибирской язвы. Эта форма сибирской язвы возникает при вдыхании B. anthracis и является очень серьезной. Первые симптомы могут включать боль в горле, умеренную лихорадку и мышечные боли. В течение нескольких дней за этими симптомами следуют тяжелые проблемы с дыханием, шок и часто менингит (воспаление оболочек головного и спинного мозга). Эта форма сибирской язвы требует госпитализации и агрессивного лечения антибиотиками. Часто это фатально.
Первые симптомы могут включать боль в горле, умеренную лихорадку и мышечные боли. В течение нескольких дней за этими симптомами следуют тяжелые проблемы с дыханием, шок и часто менингит (воспаление оболочек головного и спинного мозга). Эта форма сибирской язвы требует госпитализации и агрессивного лечения антибиотиками. Часто это фатально.
Вакцина против сибирской язвы защищает от сибирской язвы. Вакцина, используемая в Соединенных Штатах, не содержит клеток B. anthracis и не вызывает сибирской язвы. Вакцина против сибирской язвы была лицензирована в 1970 г. и повторно лицензирована в 2008 г.
На основании ограниченных, но достоверных данных вакцина защищает как от кожного (кожного), так и от ингаляционного сибирской язвы.
Вакцина против сибирской язвы рекомендуется для некоторых лиц в возрасте от 18 до 65 лет, которые могут подвергаться воздействию большого количества бактерий
B. anthracis на работе, в том числе:
- некоторые работники лабораторий или восстановителей
- некоторые люди, имеющие дело с животными или продуктами животного происхождения
- некоторые военнослужащие, как определено Министерством обороны
Эти люди должны получить пять доз вакцины (в мышцу): первая доза при выявлении риска потенциального заражения , а остальные дозы через 4 недели и 6, 12 и 18 месяцев после первой дозы.
Для постоянной защиты необходимы ежегодные бустерные дозы.
Если доза не введена в назначенное время, серию не нужно начинать заново. Возобновите серию, как только это станет практически возможным.
Вакцина против сибирской язвы также рекомендуется для непривитых людей, подвергшихся воздействию сибирской язвы в определенных ситуациях. Эти люди должны получить три дозы вакцины (подкожно), причем первую дозу как можно скорее после заражения, а вторую и третью дозы вводят через 2 и 4 недели после первой.
- Любой, у кого была серьезная аллергическая реакция на предыдущую дозу вакцины против сибирской язвы, не должен получать еще одну дозу.
- Любой, у кого есть тяжелая аллергия на какой-либо компонент вакцины, не должен получать дозу. Сообщите своему врачу, если у вас есть какие-либо серьезные аллергии, включая латекс.
- Если у вас когда-либо был синдром Гийена-Барра (СГБ), ваш лечащий врач может порекомендовать вам не проходить вакцинацию против сибирской язвы.

- Если у вас заболевание средней или тяжелой степени, ваш врач может попросить вас подождать, пока вы не выздоровеете, чтобы получить вакцину. Люди с легким заболеванием обычно могут быть вакцинированы.
- Вакцинация может быть рекомендована беременным женщинам, подвергшимся воздействию сибирской язвы и подверженным риску развития ингаляционного заболевания. Кормящим матерям можно безопасно делать вакцину против сибирской язвы.
Как и любое лекарство, вакцина может вызвать серьезную проблему, например сильную аллергическую реакцию.
Сибирская язва — очень серьезное заболевание, и риск серьезного вреда от вакцины крайне мал.
- Болезненность на руке, куда был сделан укол (примерно у 1 человека из 2)
- Покраснение на руке, где был сделан укол (примерно у 1 из 7 мужчин и у 1 из 3 женщин)
- Зуд на коже рука, в которую был сделан укол (примерно 1 из 50 мужчин и 1 из 20 женщин)
- Припухлость на руке, куда был сделан укол (примерно 1 из 60 мужчин и 1 из 16 женщин)
- Синяк на руке, где был сделан укол (примерно 1 из 25 мужчин и 1 из 22 женщин)
- Мышечные боли или временное ограничение движения рук (примерно 1 из 14 мужчин и 1 из 10 женщин)
- Головные боли (примерно 1 из 25 мужчин и 1 из 12 женщин)
- Усталость (примерно 1 из 15) мужчины, примерно 1 из 8 женщин)
- Серьезная аллергическая реакция (очень редко — реже одного раза на 100 000 доз).

Как и в случае любой вакцины, сообщалось о других серьезных проблемах. Но среди реципиентов вакцины против сибирской язвы это происходит не чаще, чем среди непривитых людей.
Нет никаких доказательств того, что вакцина против сибирской язвы вызывает долгосрочные проблемы со здоровьем.
Независимые гражданские комитеты не обнаружили, что вакцинация против сибирской язвы является фактором необъяснимых заболеваний среди ветеранов войны в Персидском заливе.
- Любое необычное состояние, такое как тяжелая аллергическая реакция или высокая температура. Если возникала тяжелая аллергическая реакция, то в течение от нескольких минут до часа после укола. Признаки серьезной аллергической реакции могут включать затрудненное дыхание, слабость, охриплость или свистящее дыхание, учащенное сердцебиение, крапивницу, головокружение, бледность или отек горла.
- Позвоните врачу или немедленно направьте человека к врачу.
- Сообщите своему врачу, что произошло, дату и время, когда это произошло, и когда была сделана прививка.

- Попросите своего поставщика услуг сообщить о реакции, заполнив форму Системы отчетности о побочных эффектах вакцины (VAERS). Вы также можете подать этот отчет через веб-сайт VAERS по адресу http://vaers.hhs.gov/index или по телефону 1-800-822-7967. VAERS не дает медицинских консультаций.
В соответствии с Законом о ПОДГОТОВКЕ была создана федеральная программа «Программа возмещения ущерба в связи с контрмерами» для оказания помощи в оплате медицинского обслуживания и других конкретных расходов определенных лиц, у которых наблюдается серьезная реакция на эту вакцину.
Если у вас есть реакция на вакцину, ваша возможность подать в суд может быть ограничена законом. Для получения дополнительной информации посетите веб-сайт программы по адресу www.hrsa.gov/countermeasurescomp или позвоните по телефону 1-888-275-4772.
- Спросите своего врача или другого поставщика медицинских услуг. Они могут дать вам вкладыш в упаковку вакцины или предложить другие источники информации.






