Содержание
Пневмококковая вакцина у детей и молодых людей с хронической болезнью почек | Нефрология Диализ Трансплантация
Фильтр поиска панели навигации
Нефрология Диализная трансплантацияЭтот выпускЖурналы ERAНефрологияКнигиЖурналыOxford Academic
Термин поиска мобильного микросайта
Закрыть
Фильтр поиска панели навигации
Нефрология Диализная трансплантацияЭтот выпускЖурналы ERAНефрологияКнигиЖурналыOxford Academic
Термин поиска на микросайте
Расширенный поиск
Статья журнала
А. Фухшубер,
А. Фухшубер
Ищите другие работы этого автора на:
Оксфордский академический
пабмед
Google ученый
О. Кюнемунд,
Кюнемунд,
О. Кюнемунд
Ищите другие работы этого автора на:
Оксфордский академический
пабмед
Google ученый
Б. Кит,
Б. Кит
Ищите другие работы этого автора на:
Оксфордский академический
пабмед
Google ученый
Р. Люттикен,
Р. Люттиккен
Ищите другие работы этого автора на:
Оксфордский академический
пабмед
Google ученый
Д. Михалк,
Д. Михалк
Ищите другие работы этого автора на:
Оксфордский академический
пабмед
Google ученый
У. Керфельд
Керфельд
У. Керфельд
Ищите другие работы этого автора на:
Оксфордский академический
пабмед
Google ученый
Нефрология Диализная трансплантация , том 11, выпуск 3, март 1996 г., страницы 468–473, https://doi.org/10.1093/ndt/11.3.468
Опубликовано:
01 марта 1996 г.
История статьи
Получено:
26 июля 1995 г.
Принято:
23 октября 1995 г.
Опубликовано:
01 марта 1996 г.
Фильтр поиска панели навигации
Нефрология Диализная трансплантацияЭтот выпускЖурналы ERAНефрологияКнигиЖурналыOxford Academic
Термин поиска мобильного микросайта
Закрыть
Фильтр поиска панели навигации
Нефрология Диализная трансплантацияЭтот выпускЖурналы ERAНефрологияКнигиЖурналыOxford Academic
Термин поиска на микросайте
Расширенный поиск
Фон.
Пневмококковая вакцинация рекомендована детям старше 2 лет с ослабленным иммунитетом, включая пациентов с хроническим заболеванием почек. Однако эффект вакцинации и ревакцинации изменчив, а показания к иммунизации являются предметом споров.
Методы.
Сорок детей и молодых взрослых с хроническими заболеваниями почек (включая идиопатический нефротический синдром, хроническую почечную недостаточность, больных, находящихся на диализе и после трансплантации) вакцинированы 23-валентной пневмококковой вакциной. Эффективность вакцины оценивали путем измерения титров антител до и через 4 недели, 6 месяцев и 12 месяцев после вакцинации. Через 1 год после первой вакцинации проведена ревакцинация 22 пациентам.
Результаты.
Достаточный иммунный ответ, определяемый как не менее чем четырехкратное повышение титров поствакцинальных антител и титр антител >200, наблюдался у 83% пациентов через 4 недели после вакцинации, но только у 68% через 6 месяцев и у 48 % через 1 год. Ревакцинация вызвала значительный иммунный ответ у 11 из 22 пациентов (50%) с последующим быстрым снижением уровня антител в течение 6 месяцев. Обе прививки переносились хорошо.
Ревакцинация вызвала значительный иммунный ответ у 11 из 22 пациентов (50%) с последующим быстрым снижением уровня антител в течение 6 месяцев. Обе прививки переносились хорошо.
Выводы.
Имеющаяся в настоящее время вакцина не имеет серьезных побочных эффектов и эффективна в отношении создания значительного иммунного ответа. Уровень антител следует контролировать у вакцинированных пациентов с хроническими заболеваниями почек, учитывая их быстрое снижение уже через 6 месяцев после вакцинации. Оценка эффективности ревакцинации у этих больных требует дальнейших исследований.
почечная недостаточность, Streptococcus pneumoniae, вакцинация
Этот контент доступен только в формате PDF.
© 1996 Европейская ассоциация диализа и трансплантации – Европейская ассоциация почек
Раздел выпуска:
Оригинальные статьи
Скачать все слайды
Реклама
Цитаты
Альтметрика
Дополнительная информация о метриках
Оповещения по электронной почте
Оповещение об активности статьи
Предварительные уведомления о статьях
Оповещение о новой проблеме
Получайте эксклюзивные предложения и обновления от Oxford Academic
Ссылки на статьи по телефону
Последний
Самые читаемые
Самые цитируемые
Факторы, влияющие на показатели трансплантации почки: исследование из реестра ERA
Отдаленные исходы и прогностические факторы выживаемости пациентов с АНЦА-ассоциированным васкулитом
Тенденции частоты трансплантаций почек в Европе: исследование из реестра ERA
Анализ событий безопасности при лечении рака с помощью дапродуктата по сравнению с обычными стимуляторами эритропоэза – апостериорный анализ исследований ASCEND-ND и ASCEND-D
Потребление лития с пищей, отторжение трансплантата и смертность у реципиентов почечного трансплантата
Объявление
FDA рассмотрит 15-валентную пневмококковую вакцину Merck для детей
Роуз Уэлдон
Источник/раскрытие информации
Источник:
Пресс-релиз.
Раскрытие информации:
Бейнс работает в Merck.
Вы успешно добавили оповещения. Вы получите электронное письмо, когда будет опубликован новый контент.
Щелкните здесь, чтобы управлять оповещениями по электронной почте
Нам не удалось обработать ваш запрос. Пожалуйста, повторите попытку позже. Если у вас по-прежнему возникает эта проблема, свяжитесь с нами по адресу [email protected].
Компания Merck объявила в среду, что FDA приняло для приоритетного рассмотрения заявку на получение дополнительной лицензии на биологические препараты Vaxneuvance, 15-валентной пневмококковой конъюгированной вакцины компании, предназначенной для использования у младенцев и детей.
Вакцина, ранее известная как V114, была одобрена FDA в июле для взрослых. Предотвращает инвазивные заболевания, вызванные Streptococcus pneumoniae серотипы 1, 3, 4, 5, 6А, 6В, 7F, 9V, 14, 18С, 19А, 19F, 22F, 23F и 33F.
В рамках обзора эффекты вакцины будут изучаться у детей в возрасте от 6 недель до 17 лет.
«Vaxneuvance обладает потенциалом для обеспечения значимой защиты от инвазивной пневмококковой инфекции у детей и младенцев путем воздействия на штаммы или серотипы пневмококка, которые вносят значительный вклад в бремя болезни, включая серотип 3, и расширения охвата дополнительными болезнетворными серотипами, 22F и 33F, которые не включены в пневмококковую конъюгированную вакцину, доступную в настоящее время для этой группы населения», — главный медицинский директор Merck 9.0282 Roy Baynes, M D, PhD , , говорится в пресс-релизе. «Мы рассчитываем на сотрудничество с FDA США, поскольку оно рассматривает вопрос о том, что станет первым новым вариантом вакцинации против пневмококка у детей более чем за десятилетие».
Компания Merck заявила, что заявление было поддержано результатами клинических исследований фазы 2 и фазы 3 в педиатрической популяции.
«Эти исследования поддерживают потенциальное использование Vaxneuvance в различных клинических условиях, включая иммунизацию младенцев и детей ясельного возраста, а также особых групп населения с повышенным риском пневмококковой инфекции, таких как дети с ВИЧ-инфекцией или серповидно-клеточной анемией». он сказал.
Первоначальное одобрение FDA вакцины для взрослых было основано на данных семи рандомизированных двойных слепых клинических исследований, которые показали, что вакцина не уступает 13-валентной пневмококковой конъюгированной вакцине (PCV13) в отношении 13 общих серотипов. По словам Merck, иммунный ответ был выше, чем у PCV13, для серотипа 3 и для двух серотипов, уникальных для Vaxneuvance, 22F и 33F.
Рандомизированные контролируемые исследования по оценке клинической эффективности препарата Ваксневанс по сравнению с ПКВ13 не проводились.
Ссылка:
Мерк. Компания Merck объявляет об одобрении Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США Vaxneuvance (пневмококковая 15-валентная конъюгированная вакцина) для профилактики инвазивной пневмококковой инфекции у взрослых в возрасте 18 лет и старше, вызванной 15 серотипами.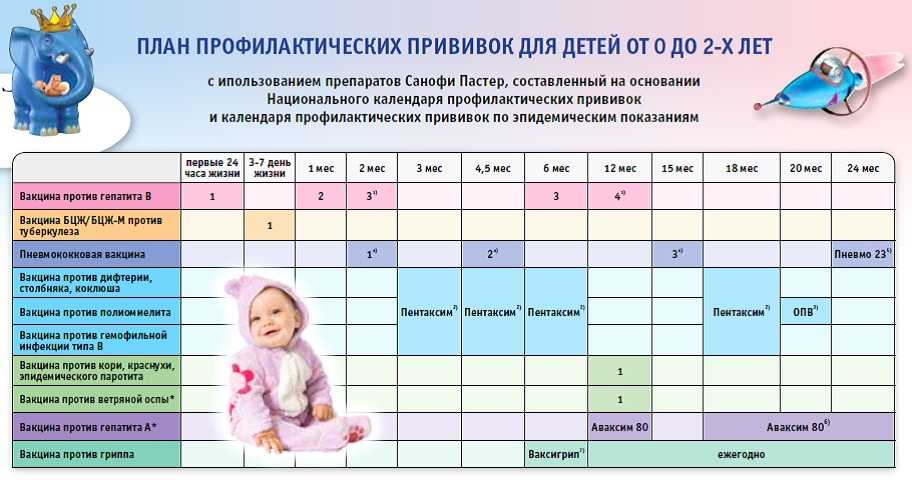

 Fuchshuber, O. Kühnemund, B. Keuth, R. Lütticken, D. Michalk, U. Querfeld, Пневмококковая вакцина у детей и молодых людей с хроническим заболеванием почек, Нефрология Диализ Трансплантация , Том 11, Выпуск 3, март 1996 г., страницы 468–473, https://doi.org/10.1093/ndt/11.3.468
Fuchshuber, O. Kühnemund, B. Keuth, R. Lütticken, D. Michalk, U. Querfeld, Пневмококковая вакцина у детей и молодых людей с хроническим заболеванием почек, Нефрология Диализ Трансплантация , Том 11, Выпуск 3, март 1996 г., страницы 468–473, https://doi.org/10.1093/ndt/11.3.468