Содержание
Полезная информация | Министерство здравоохранения Калининградской области
Энтеровирусные инфекции представляют собой большую группу заболеваний, вызываемых кишечными вирусами (энтеровирусами). Эти вирусы имеют множество различных видов, и с каждым годом открывается все больше новых представителей. Заболеваемость характеризуется летне-осенней сезонностью, причем пик инфицирования приходится на июль – август. В последнее время во всем мире нередко наблюдаются крупные вспышки заболеваемости (в основном, среди детей). Рекомендации по профилактике энтеровирусной инфекции помогут предотвратить опасные последствия, которыми грозит эта болезнь.
Как передается энтеровирусная инфекция?
Существует два механизма передачи — воздушно-капельный (при кашле, чихании, разговоре) и фекально-оральный (пищевой, водный, контактно-бытовой). «Входными воротами» инфекции являются слизистые оболочки верхних дыхательных путей и пищеварительного тракта. Восприимчивость к энтеровирусным инфекциям у человека высока в любом возрасте.
Восприимчивость к энтеровирусным инфекциям у человека высока в любом возрасте.
Опасность энтеровирусной инфекции
Энтеровирусы могут нанести большой вред организму. Запущенные формы приводят к тяжелым заболеваниям с поражением важных органов и систем организма, что может послужить причиной инвалидности и даже летального исхода. В основном, это касается поражения вирусами нервной системы. Последствием энтеровирусной инфекции при асептическом серозном менингите, энцефалите и менингоэнцефалите может стать отек головного мозга. При бульбарных нарушениях возможны тяжелые аспирационные пневмонии. Респираторная форма иногда осложняется вторичной бактериальной пневмонией, крупом. Кишечная форма опасна тяжелым обезвоживанием организма, а энтеровирусное поражение глаз грозит слепотой.
Прививка от энтеровирусной инфекции
К сожалению, вакцины от энтеровирусной инфекции пока не существует. Сегодня ученые работают над этим вопросом, но существование большого количества видов возбудителей не позволяет разработать вакцину, способную защитить одновременно от всех групп энтеровирусов. В настоящее время проводится лишь вакцинация от полиомиелита – заболевания, вызываемого несколькими типами энтеровируса. После перенесенной энтеровирусной инфекции образуется пожизненный иммунитет. Однако иммунитет является сероспицефичным, т.е. образуется только к тому типу вируса, которым переболел человек. От других разновидностей энтеровирусов он защитить не может.
В настоящее время проводится лишь вакцинация от полиомиелита – заболевания, вызываемого несколькими типами энтеровируса. После перенесенной энтеровирусной инфекции образуется пожизненный иммунитет. Однако иммунитет является сероспицефичным, т.е. образуется только к тому типу вируса, которым переболел человек. От других разновидностей энтеровирусов он защитить не может.
Меры профилактики энтеровирусной инфекции
Говоря о профилактике энтеровирусной инфекции, в первую очередь следует понимать санитарные правила, соблюдение которых предотвращает инфицирование и распространение инфекции. Перечислим наиболее важные из них:
1. Проведение мероприятий по контролю загрязнения объектов окружающей среды канализационными отходами, благоустройство источников водоснабжения.
2. Изоляция больных, тщательная дезинфекция их вещей и предметов гигиены.
3. Употребление для питья только качественной кипяченой или бутилированной воды, пастеризованного молока.
4. Тщательное мытье фруктов, ягод, овощей перед употреблением в пищу.
5. Защита продуктов от насекомых, грызунов.
6. Соблюдение правил личной гигиены.
7. Разделочный инвентарь (ножи, доски) для сырых и готовых продуктов должен быть отдельным.
8. Не покупать продукты в местах несанкционированной торговли.
9. Купаться только в разрешенных местах, не заглатывать воду во время водных процедур.
Людям, контактировавшим с инфицированными больными, для профилактики
энтеровирусной инфекции могут назначаться лекарственные препараты группы
интерферона.
Энтеровирусная инфекция — Профилактика заболеваний и ЗОЖ — Бюджетное учреждение Ханты-Мансийского автономного округа — Югры
памятка для населения
Энтеровирусные инфекции — это группа острых инфекционных болезней, вызываемых кишечными вирусами (энтеровирусами), характеризующаяся лихорадкой и многообразными клиническими симптомами.
Энтеровирусы (их более 80 типов) довольно быстро погибают при температурах свыше 50°С (при 60°С — за 6-8 мин.
Наиболее интенсивное выделение возбудителя происходит в первые дни болезни. Доказана высокая контагиозность (заразность) энтеровирусов.
Вирус обнаруживают в крови, моче, носоглотке и фекалиях за несколько дней до появления клинических симптомов; инфицированные лица наиболее опасны для окружающих в ранние периоды инфекции, когда возбудитель выделяется из организма в наибольших концентрациях.
Инкубационный (скрытый) период энтеровирусной инфекции варьируется от 2 — х до 35 дней, в среднем — до 2 — х недель.
Источником инфекции является только человек. Инфекция передается воздушно-капельным (от больных), контактно-бытовым (от вирусоносителей), пищевым и водным путем. Заболевание распространено повсеместно. В странах умеренного климата характерна сезонность с повышением заболеваемости в конце лета и в начале осени. Заболевают преимущественно дети и лица молодого возраста. Заболевания наблюдаются в виде спорадических случаев, локальных вспышек (чаще в детских коллективах) и в виде крупных эпидемий, поражающих отдельные регионы и даже страны.
Факторами передачи инфекции служат вода, овощи, загрязненные энтеровирусами в результате применения необезвреженных сточных вод при их поливе. Также вирус может передаваться через грязные руки, игрушки и другие объекты внешней среды.
Человек, в организм которого проник энтеровирус, чаще становится носителем, или переносит заболевание в легкой форме.
Способность энтеровирусов воздействовать на многие органы человека вызывает большое разнообразие клинических форм инфекции. Могут поражаться практически все органы и ткани организма: нервная, сердечно-сосудистая и бронхолегочная системы, желудочно-кишечный тракт, а также почки, глаза, мышцы, кожа, слизистая полости рта, печень, эндокринные органы. Одним из наиболее серьезных и нередко регистрируемых форм энтеровирусной инфекции является серозный менингит, характеризующийся сильной головной болью, повышением температуры до 38-39°С, болями в затылочных мышцах, светобоязнью, рвотой.
Методы специфической профилактики (вакцинация) против энтеровирусных инфекций не разработаны. Однако одним из методов борьбы с энтеровирусными инфекциями является вакцинация против полиомиелита, так как вакцинный штамм вируса обладает подавляющим действием на энтеровирус.
Меры неспецифической профилактики энтеровирусной инфекции: 5 простых правил профилактики кишечных инфекций:
При первых признаках заболевания необходимо немедленно обращаться за медицинской помощью, не заниматься самолечением. |
Энтеровирус 71
Болезнь рук, ящура (HFMD) впервые была зарегистрирована в Новой Зеландии в 1957 г.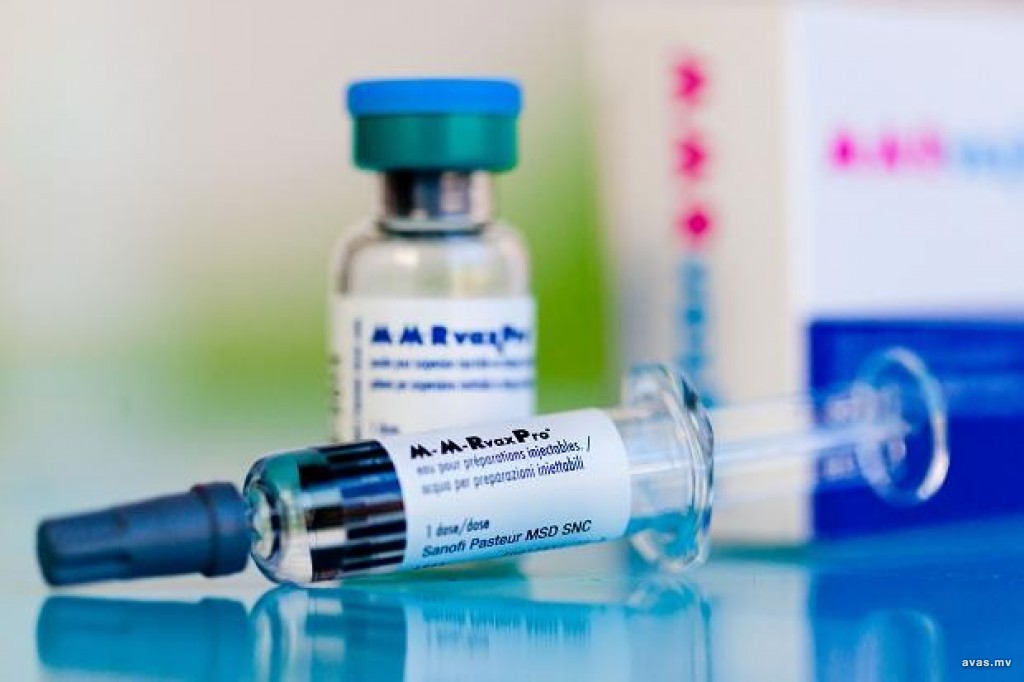 и встречается в основном у детей младшего возраста с пиком заболеваемости примерно в возрасте 2 лет. Возбудителями HFMD являются пикорнавирусы, чаще всего энтеровирусы человека вида А, в основном вирусы Коксаки А и энтеровирусы А71 (EV71). Пикорнавирусы принадлежат к Picornaviridae, семейству небольших безоболочечных вирусов с одноцепочечным РНК-геномом с положительным смыслом, состоящим примерно из 7500 нуклеотидов.
и встречается в основном у детей младшего возраста с пиком заболеваемости примерно в возрасте 2 лет. Возбудителями HFMD являются пикорнавирусы, чаще всего энтеровирусы человека вида А, в основном вирусы Коксаки А и энтеровирусы А71 (EV71). Пикорнавирусы принадлежат к Picornaviridae, семейству небольших безоболочечных вирусов с одноцепочечным РНК-геномом с положительным смыслом, состоящим примерно из 7500 нуклеотидов.
EV71 был впервые выделен из фекалий женщины, страдающей энцефалитом, в 1969 году в Калифорнии. Однако ретроспективное исследование, проведенное в Нидерландах, показало, что вирус мог появиться еще в 1963 году; это открытие согласуется с сообщениями о возможных всемирных эпидемиях EV71 в конце двадцатого века, во всем мире и с эпидемиями в Азии, Европе и Америке. Вирус EV71 вызывает ряд эффектов от бессимптомной инфекции и легкой формы HFMD до неврологических заболеваний с тяжелыми осложнениями со стороны центральной нервной системы и сердечно-легочной недостаточностью. В тяжелых случаях смертность может быть высокой, особенно у детей в возрасте 5 лет и младше. EV71 считается самым тяжелым нейротоксическим энтеровирусом, и тяжелое заболевание EV71 стало серьезной проблемой общественного здравоохранения в Китае.
В тяжелых случаях смертность может быть высокой, особенно у детей в возрасте 5 лет и младше. EV71 считается самым тяжелым нейротоксическим энтеровирусом, и тяжелое заболевание EV71 стало серьезной проблемой общественного здравоохранения в Китае.
Изоляты EV71 могут быть сгруппированы в соответствии с их геномной последовательностью как минимум в восемь геногрупп (A–H), но принадлежат к одному серотипу. Геногруппы B и C представляют наибольший интерес из-за их частоты выделения и влияния на заболевания в Восточной Азии, и каждая из них может быть подразделена на пять подгеногрупп (C1–C5 и B1–B5). C4, безусловно, является основной геногруппой, циркулирующей в Китае, в то время как B4, B5 и C5 встречаются в других азиатских странах. Напротив, штаммы геногрупп C1 и C2 преимущественно встречаются в Европе, где тяжелое заболевание встречается редко. В 2011 г. Региональное бюро ВОЗ для стран Западной части Тихого океана выпустило Руководство по клиническому ведению и ответным мерам общественного здравоохранения на кисту, ящуру (HFMD) для поддержки лечения, профилактики и контроля HFMD.
Вакцины против энтеровируса 71
На сегодняшний день в Китае лицензированы три вакцины против EV71, все с использованием штаммов геногруппы C4. Эффективность этих трех вакцин после иммунизации двумя дозами колеблется от 90,0% до 97,4% после одного года наблюдения до 95,1% после двухлетнего наблюдения. Вакцины-кандидаты, содержащие геногруппы B4 и B5, находятся в разработке в других странах, но еще не достигли стадии лицензирования. Другие вакцины, такие как рекомбинантные и другие формы субъединичных вакцин, векторные вакцины, вакцины на основе вирусоподобных частиц, находятся на ранней стадии разработки. Кроме того, рассматривается разработка вакцин против Коксаки А16, А6 и А10 с целью разработки комбинированных/поливалентных вакцин.
Стандартизация вакцин против энтеровируса
Письменные стандарты
В 2019 и 2020 годах ВОЗ организовала совещание рабочей группы и неофициальную консультацию для обзора текущего состояния разработки и регулирования вакцин против энтеровируса 71 и разработала Рекомендации ВОЗ для обеспечения качества, безопасности и эффективности вакцин против энтеровируса 71 (инактивированных). Этот документ содержит руководство для НРО и производителей по производственному процессу, а также по доклиническим и клиническим аспектам, чтобы гарантировать качество, безопасность и эффективность вакцин против энтеровируса 71 (инактивированных) для профилактического применения.
Этот документ содержит руководство для НРО и производителей по производственному процессу, а также по доклиническим и клиническим аспектам, чтобы гарантировать качество, безопасность и эффективность вакцин против энтеровируса 71 (инактивированных) для профилактического применения.
Рекомендации по обеспечению качества, безопасности и эффективности вакцин против энтеровируса 71 (инактивированных), Приложение 3, TRS № 1030. Первый международный стандарт ВОЗ для анти-EV71 сыворотки (человеческой) (код NIBSC 14/140) с присвоенным значением 1000 МЕ/ампула для стандартизации диагностических тестов для использования в исследованиях серопревалентности и для оценки иммунитета.

Международный каталог эталонных препаратов
Стандартизация вакцин >
Связанные темы здравоохранения
Вакцины против энтеровируса A71 – PMC
1. Alexander J.P., Jr., Baden L., Pallansch M.A., Anderson L.J. . Дж. Заразить. Дис. 1994; 169: 905–908. doi: 10.1093/infdis/169.4.905. [PubMed] [CrossRef] [Google Scholar]
2. Ooi M.H., Wong S.C., Lewthwaite P., Cardosa M.J., Solomon T. Клинические особенности, диагностика и лечение энтеровируса 71. Lancet Neurol. 2010;9: 1097–1105. doi: 10.1016/S1474-4422(10)70209-X. [PubMed] [CrossRef] [Google Scholar]
[PubMed] [CrossRef] [Google Scholar]
3. Lee K.Y. Энтеровирусная инфекция 71 и неврологические осложнения. Корейский Дж. Педиат. 2016;59:395–401. doi: 10.3345/kjp.2016.59.10.395. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Неврологические осложнения и отдаленные последствия энтеровируса А71. Дж. Биомед. науч. 2019;26:57. дои: 10.1186/с12929-019-0552-7. [PMC бесплатная статья] [PubMed] [CrossRef] [Google Scholar]
5. Puenpa J., Wanlapakorn N., Vongpunsawad S., Poovorawan Y. История вспышек энтеровируса A71 и молекулярная эпидемиология в Азиатско-Тихоокеанском регионе. Дж. Биомед. науч. 2019;26:75. doi: 10.1186/s12929-019-0573-2. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
6. Никонов О.С., Черных Е.С., Гарбер М.Б., Никонова Е.Ю. Энтеровирусы: классификация, вызываемые ими заболевания и подходы к созданию противовирусных препаратов. Биохимия. 2017;82:1615–1631. дои: 10.1134/S0006297917130041. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
7. Kung Y.A., Hung C.T., Liu Y.C., Shih S.R. Обновленная информация о разработке вакцин против энтеровируса 71. Мнение эксперта. биол. тер. 2014; 14:1455–1464. doi: 10.1517/14712598.2014.935330. [PubMed] [CrossRef] [Google Scholar]
Kung Y.A., Hung C.T., Liu Y.C., Shih S.R. Обновленная информация о разработке вакцин против энтеровируса 71. Мнение эксперта. биол. тер. 2014; 14:1455–1464. doi: 10.1517/14712598.2014.935330. [PubMed] [CrossRef] [Google Scholar]
8. Чанг Ю.К., Чен К.Х., Чен К.Т. Болезни рук, ящура и герпангина, вызванные инфекциями энтеровируса A71: обзор молекулярной эпидемиологии энтеровируса A71, патогенеза и текущей разработки вакцины. Преподобный Инст. Мед. Троп. Сан-Паулу. 2018;60:e70. дои: 10.1590/s1678-9946201860070. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
9. Chen B.S., Lee HC, Lee K.M., Gong Y.N., Shih S.R. Энтеровирусы и энцефалиты. Фронт. микробиол. 2020;11:261. doi: 10.3389/fmicb.2020.00261. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
10. Lin J.Y., Kung Y.A., Shih S.R. Противовирусные препараты и вакцины от энтеровируса А71. Дж. Биомед. науч. 2019;26:65. doi: 10.1186/s12929-019-0560-7. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
11. Ши С.Р., Столлар В., Ли М.Л. Факторы хозяина в репликации энтеровируса 71. Дж. Вирол. 2011; 85: 9658–9666. doi: 10.1128/ОВИ.05063-11. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Ши С.Р., Столлар В., Ли М.Л. Факторы хозяина в репликации энтеровируса 71. Дж. Вирол. 2011; 85: 9658–9666. doi: 10.1128/ОВИ.05063-11. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
12. Wang X., An Z., Huo D., Jia L., Li J., Yang Y., Liang Z., Wang Q. , Wang H. Эффективность вакцины против энтеровируса A71 в предотвращении заражения энтеровирусом A71 среди пациентов с заболеваниями рук, ящура и рта, находящихся под медицинским наблюдением, Пекин, Китай. Гум. Вакцина. Иммунотер. 2019;15:1183–1190. дои: 10.1080/21645515.2019.1581539. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
13. Minor PD. Ликвидация полиомиелита, прекращение вакцинации и повторное появление болезни. Нац. Преподобный Микробиолог. 2004; 2: 473–482. doi: 10.1038/nrmicro906. [PubMed] [CrossRef] [Google Scholar]
14. Zhou Y., Li J.X., Jin P.F., Wang Y.X., Zhu F.C. Энтеровирус 71: цельновирионная инактивированная вакцина против энтеровируса 71. Эксперт Преподобный Вакцина. 2016; 15:803–813. doi: 10.1080/14760584.2016.1191357. [PubMed] [CrossRef] [Академия Google]
2016; 15:803–813. doi: 10.1080/14760584.2016.1191357. [PubMed] [CrossRef] [Академия Google]
15. Mao Q.Y., Wang Y., Bian L., Xu M., Liang Z. Вакцина EV71, новый инструмент для борьбы со вспышками ящура и кистей рук (HFMD) Expert Rev. Vaccin. 2016;15:599–606. doi: 10.1586/14760584.2016.1138862. [PubMed] [CrossRef] [Google Scholar]
16. Bek E.J., Hussain K.M., Phuektes P., Kok C.C., Gao Q., Cai F., Gao Z., McMinn P.C. Вакцина, инактивированная формалином, вызывает перекрестный защитный иммунитет у мышей, моделирующих инфекцию энтеровируса человека 71. вакцина. 2011; 29:4829–4838. doi: 10.1016/j.vaccine.2011.04.070. [PubMed] [CrossRef] [Академия Google]
17. Dong C., Liu L., Zhao H., Wang J., Liao Y., Zhang X., Na R., Liang Y., Wang L., Li Q. Иммунопротекция, вызванная энтеровирусом типа 71 экспериментальная инактивированная вакцина на мышах и макаках-резусах. вакцина. 2011;29:6269–6275. doi: 10.1016/j.vaccine.2011.06.044. [PubMed] [CrossRef] [Google Scholar]
18. Chong P., Liu C.C., Chow Y.H., Chou A.H., Klein M. Обзор вакцин против энтеровируса 71. клин. Заразить. Дис. Выключенный. Опубл. Заразить. Дис. соц. Являюсь. 2015;60:797–803. doi: 10.1093/cid/ciu852. [PubMed] [CrossRef] [Академия Google]
Chong P., Liu C.C., Chow Y.H., Chou A.H., Klein M. Обзор вакцин против энтеровируса 71. клин. Заразить. Дис. Выключенный. Опубл. Заразить. Дис. соц. Являюсь. 2015;60:797–803. doi: 10.1093/cid/ciu852. [PubMed] [CrossRef] [Академия Google]
19. Zhu F., Xu W., Xia J., Liang Z., Liu Y., Zhang X., Tan X., Wang L., Mao Q., Wu J., et al. Эффективность, безопасность и иммуногенность вакцины против энтеровируса 71 в Китае. Н. англ. Дж. Мед. 2014; 370:818–828. doi: 10.1056/NEJMoa1304923. [PubMed] [CrossRef] [Google Scholar]
20. Liang Z., Mao Q., Gao Q., Li X., Dong C., Yu X., Yao X., Li F., Yin W., Ли К. и др. Установление национальных стандартов Китая в отношении содержания антигена и реакции нейтрализующих антител для оценки вакцин против энтеровируса 71 (EV71). вакцина. 2011;29: 9668–9674. doi: 10.1016/j.vaccine.2011.10.018. [PubMed] [CrossRef] [Google Scholar]
21. Li R., Liu L., Mo Z., Wang X., Xia J., Liang Z., Zhang Y., Li Y., Mao Q., Ван Дж. и др. Инактивированная вакцина против энтеровируса 71 у здоровых детей. Н. англ. Дж. Мед. 2014; 370:829–837. doi: 10.1056/NEJMoa1303224. [PubMed] [CrossRef] [Google Scholar]
Н. англ. Дж. Мед. 2014; 370:829–837. doi: 10.1056/NEJMoa1303224. [PubMed] [CrossRef] [Google Scholar]
22. Zhu F.C., Meng F.Y., Li J.X., Li XL., Mao Q.Y., Tao H., Zhang Y.T., Yao X., Chu K., Chen Q.H., et al. Эффективность, безопасность и иммунология инактивированной квасцово-адъювантной вакцины против энтеровируса 71 у детей в Китае: многоцентровое, рандомизированное, двойное слепое, плацебо-контролируемое исследование фазы 3. Ланцет. 2013;381:2024–2032. дои: 10.1016/S0140-6736(13)61049-1. [PubMed] [CrossRef] [Google Scholar]
23. Wei M., Meng F., Wang S., Li J., Zhang Y., Mao Q., Hu Y., Liu P., Shi N., Тао Х. и др. Двухлетняя эффективность, иммуногенность и безопасность вакцины Vigoo Enterovirus 71 у здоровых китайских детей: рандомизированное открытое исследование. Дж. Заразить. Дис. 2017;215:56–63. doi: 10.1093/infdis/jiw502. [PubMed] [CrossRef] [Google Scholar]
24. Hu Y., Zeng G., Chu K., Zhang J., Han W., Zhang Y., Li J., Zhu F. Пятилетняя стойкость иммунитета после иммунизации инактивированной вакциной энтеровируса 71 типа (EV71) у здоровых детей: дополнительное наблюдение. Гум. Вакцина. Иммунотер. 2018;14:1517–1523. дои: 10.1080/21645515.2018.1442997. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Гум. Вакцина. Иммунотер. 2018;14:1517–1523. дои: 10.1080/21645515.2018.1442997. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
25. Lei D., Griffiths E., Martin J. Заседание рабочей группы ВОЗ по разработке рекомендаций ВОЗ по обеспечению качества, безопасности и эффективности энтеровируса 71 вакцина. вакцина. 2020; 38: 4917–4923. doi: 10.1016/j.vaccine.2020.05.001. [Статья PMC бесплатно] [PubMed] [CrossRef] [Google Scholar]
, и другие. Отбор и характеристика вакцинного штамма для разработки вакцины против энтеровируса 71. вакцина. 2012;30:703–711. doi: 10.1016/j.vaccine.2011.11.087. [PubMed] [CrossRef] [Академия Google]
27. Chong P., Hsieh S.Y., Liu C.C., Chou A.H., Chang J.Y., Wu S.C., Liu S.J., Chow Y.H., Su I.J., Klein M. Производство вакцин-кандидатов EV71. Гум. Вакцина. Иммунотер. 2012; 8: 1775–1783. doi: 10.4161/hv.21739. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
28. Cheng A., Fung C.P., Liu C.C., Lin Y.T., Tsai HY, Chang S. C., Chou AH, Chang J.Y., Jiang R.H., Hsieh Y.C., и другие. Рандомизированное открытое исследование фазы I для оценки безопасности и иммуногенности вакцины против энтеровируса 71. вакцина. 2013;31:2471–2476. doi: 10.1016/j.vaccine.2013.03.015. [PubMed] [CrossRef] [Академия Google]
C., Chou AH, Chang J.Y., Jiang R.H., Hsieh Y.C., и другие. Рандомизированное открытое исследование фазы I для оценки безопасности и иммуногенности вакцины против энтеровируса 71. вакцина. 2013;31:2471–2476. doi: 10.1016/j.vaccine.2013.03.015. [PubMed] [CrossRef] [Академия Google]
29. Чоу А.Х., Лю К.С., Чан С.П., Го М.С., Се С.Ю., Ян В.Х., Чао Х.Дж., Ву С.Л., Хуан Дж.Л., Ли М.С., и др. Пилотное производство высокоэффективных и стабильных вакцин-кандидатов против энтеровируса 71. ПЛОС ОДИН. 2012;7:e34834. doi: 10.1371/journal.pone.0034834. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
30. Чоу А.Х., Лю К.С., Чанг Дж.Ю., Цзян Р., Се Ю.К., Цао А., Ву С.Л., Хуан Дж.Л., Фунг С.П., Се С.М. , и другие. Инактивированная формалином вакцина-кандидат EV71 индуцировала перекрестно-нейтрализующие антитела против субгенотипов B1, B4, B5 и C4A у взрослых добровольцев. ПЛОС ОДИН. 2013;8:e79783. doi: 10.1371/journal.pone.0079783. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
31. Huang L.M., Chiu CH, Chiu N.C., Lin C.Y., Li M.T., Kuo T.Y., Weng Y.J., Hsieh E.F., Tai I.C. Иммуногенность, безопасность, перекрестная реакция и иммунная персистенция инактивированной вакцины против энтеровируса А71 у детей в возрасте от двух месяцев до 11 лет на Тайване. вакцина. 2019; 37: 1827–1835. doi: 10.1016/j.vaccine.2019.02.023. [PubMed] [CrossRef] [Google Scholar]
Huang L.M., Chiu CH, Chiu N.C., Lin C.Y., Li M.T., Kuo T.Y., Weng Y.J., Hsieh E.F., Tai I.C. Иммуногенность, безопасность, перекрестная реакция и иммунная персистенция инактивированной вакцины против энтеровируса А71 у детей в возрасте от двух месяцев до 11 лет на Тайване. вакцина. 2019; 37: 1827–1835. doi: 10.1016/j.vaccine.2019.02.023. [PubMed] [CrossRef] [Google Scholar]
32. In H.J., Lim H., Lee J.A., Kim H.J., Kim J.W., Hyeon J.Y., Yeo S.G., Lee J.W., Yoo J.S., Choi Y.K., et al. Инактивированная вакцина против ящура с использованием штамма энтеровируса 71 (C4a), выделенного от корейского пациента, вызывает сильный иммуногенный ответ у мышей. ПЛОС ОДИН. 2017;12:e0178259. doi: 10.1371/journal.pone.0178259. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
33. Huang S.W., Cheng D., Wang J.R. Энтеровирус A71: вирулентность, антигенность и генетическая эволюция на протяжении многих лет. Дж. Биомед. науч. 2019;26:81. doi: 10.1186/s12929-019-0574-1. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
34. Fujii K., Sudaka Y., Takashino A., Kobayashi K., Kataoka C., Suzuki T., Iwata-Yoshikawa N., Kotani О., Ами Ю., Симидзу Х. и др. Аминокислотный остаток VP1 145 энтеровируса 71 является ключевым остатком для его прикрепления к рецептору и устойчивости к нейтрализующим антителам во время инфекции яванских обезьян. Дж. Вирол. 2018;92 doi: 10.1128/ОВИ.00682-18. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Fujii K., Sudaka Y., Takashino A., Kobayashi K., Kataoka C., Suzuki T., Iwata-Yoshikawa N., Kotani О., Ами Ю., Симидзу Х. и др. Аминокислотный остаток VP1 145 энтеровируса 71 является ключевым остатком для его прикрепления к рецептору и устойчивости к нейтрализующим антителам во время инфекции яванских обезьян. Дж. Вирол. 2018;92 doi: 10.1128/ОВИ.00682-18. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
35. Nishimura Y., Lee H., Hafenstein S., Kataoka C., Wakita T., Bergelson J.M., Shimizu H. Enterovirus 71 связывается с PSGL -1 на лейкоцитах: VP1-145 действует как молекулярный переключатель для управления взаимодействием с рецептором. PLoS Патог. 2013;9:e1003511. doi: 10.1371/journal.ppat.1003511. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
36. Yeh M.T., Wang S.W., Yu CK, Lin K.H., Lei HY, Su IJ, Wang J.R. Один нуклеотид в стволовой петле II 5′- нетранслируемая область способствует вирулентности энтеровируса 71 у мышей. ПЛОС ОДИН. 2011;6:e27082. doi: 10.1371/journal.pone.0027082. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
doi: 10.1371/journal.pone.0027082. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
37. Chang C.K., Wu S.R., Chen Y.C., Lee KJ, Chung N.H., Lu YJ, Yu S.L., Liu C.C., Chow Y.H. Мутации в VP1 и 5′-UTR влияют на вирулентность энтеровируса 71. науч. Отчет 2018; 8: 6688. doi: 10.1038/s41598-018-25091-7. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
38. Арита М., Нагата Н., Ивата Н., Ами Ю., Судзаки Ю., Мизута К., Ивасаки Т., Сата Т. , Wakita T., Shimizu H. Ослабленный штамм энтеровируса 71, принадлежащий к генотипу а, показал широкий спектр антигенности с ослабленной нейровирулентностью у яванских макаков. Дж. Вирол. 2007;81:9386–9395. doi: 10.1128/ОВИ.02856-06. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
39. Sadeghipour S., Bek E.J., McMinn P.C. Устойчивые к рибавирину мутанты энтеровируса человека 71 проявляют фенотип с высокой точностью репликации во время роста в клеточной культуре. Дж. Вирол. 2013; 87: 1759–1769. doi: 10. 1128/ОВИ.02139-12. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
1128/ОВИ.02139-12. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
40. Meng T., Kwang J. Аттенуация энтеровируса человека 71 вариант с высокой точностью репликации в AG129мышей. Дж. Вирол. 2014; 88: 5803–5815. doi: 10.1128/ОВИ.00289-14. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
41. Tsai Y.H., Huang S.W., Hsieh W.S., Cheng C.K., Chang C.F., Wang Y.F., Wang J.R. Энтеровирус A71, содержащий кодон-деоптимизированный VP1 и высокоточный Полимераза как кандидат в вакцины нового поколения. Дж. Вирол. 2019;93:e02308-18. doi: 10.1128/ОВИ.02308-18. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
42. Yee P.T.I., Tan S.H., Ong K.C., Tan K.O., Wong K.T., Hassan S.S., Poh C.L. Разработка живых аттенуированных вакцинных штаммов энтеровируса 71, обеспечивающих защиту от летального заражения у мышей. науч. Респ. 2019 г.;9:4805. doi: 10.1038/s41598-019-41285-z. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
43. Zhao D. , Sun B., Sun S., Fu B., Liu C., Liu D., Chu Y., Ma Y. , Бай Л., Ву Ю. и др. Характеристика вирусоподобных частиц энтеровируса человека71, используемых в качестве вакцинных антигенов. ПЛОС ОДИН. 2017;12:e0181182. doi: 10.1371/journal.pone.0181182. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
, Sun B., Sun S., Fu B., Liu C., Liu D., Chu Y., Ma Y. , Бай Л., Ву Ю. и др. Характеристика вирусоподобных частиц энтеровируса человека71, используемых в качестве вакцинных антигенов. ПЛОС ОДИН. 2017;12:e0181182. doi: 10.1371/journal.pone.0181182. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
44. Qian C., Liu X., Xu Q., Wang Z., Chen J., Li T., Zheng Q., Yu H. , Гу Ю., Ли С. и др. Недавний прогресс в универсальности вирусоподобных частиц. Вакцины (Базель) 2020;8:139. doi: 10.3390/vaccines8010139. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
45. Chung Y.C., Huang J.H., Lai C.W., Sheng HC, Shih S.R., Ho M.S., Hu Y.C. Экспрессия, очистка и характеристика вирусоподобных частиц энтеровируса-71. Мировой Ж. Гастроэнтерол. 2006; 12: 921–927. doi: 10.3748/wjg.v12.i6.921. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
46. Hu Y.C., Hsu J.T., Huang J.H., Ho M.S., Ho Y.C. Формирование энтеровирусоподобных агрегатов частиц рекомбинантными бакуловирусами, коэкспрессирующими P1 и 3CD, в клетках насекомых. Биотехнолог. лат. 2003;25:919–925. doi: 10.1023/A:1024071514438. [PubMed] [CrossRef] [Google Scholar]
Биотехнолог. лат. 2003;25:919–925. doi: 10.1023/A:1024071514438. [PubMed] [CrossRef] [Google Scholar]
Нейтрализующие антитела к энтеровирусу типа 71 в сыворотке макак, иммунизированных вирусоподобными частицами EV71. вакцина. 2012;30:1305–1312. doi: 10.1016/j.vaccine.2011.12.081. [PubMed] [CrossRef] [Google Scholar]
48. Rudd P.M., Elliott T., Cresswell P., Wilson I.A., Dwek R.A. Гликозилирование и иммунная система. Наука. 2001;291: 2370–2376. doi: 10.1126/science.291.5512.2370. [PubMed] [CrossRef] [Google Scholar]
49. Хякумура М., Уолш Р., Тайсен-Андерсен М., Кингстон Н.Дж., Ла М., Лу Л., Ловреч Г., Пакер Н.Х., Локарнини С., Неттер Х. Дж. Модификация плотности гликанов, связанных с аспарагином, для конструирования вирусоподобных частиц вируса гепатита В с повышенной иммуногенностью. Дж. Вирол. 2015;89:11312–11322. doi: 10.1128/ОВИ.01123-15. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
50. Zhang C., Ku Z., Liu Q., Wang X., Chen T., Ye X. , Li D., Jin X. , Huang Z. Высокопродуктивное производство рекомбинантных вирусоподобных частиц энтеровируса 71 в Pichia pastoris и их защитная эффективность против орального вирусного заражения у мышей. вакцина. 2015;33:2335–2341. doi: 10.1016/j.vaccine.2015.03.034. [PubMed] [CrossRef] [Академия Google]
, Li D., Jin X. , Huang Z. Высокопродуктивное производство рекомбинантных вирусоподобных частиц энтеровируса 71 в Pichia pastoris и их защитная эффективность против орального вирусного заражения у мышей. вакцина. 2015;33:2335–2341. doi: 10.1016/j.vaccine.2015.03.034. [PubMed] [CrossRef] [Академия Google]
51. Li H.Y., Han J.F., Qin C.F., Chen R. Вирусоподобные частицы энтеровируса 71, полученные из Saccharomyces cerevisiae, сильно вызывают защитные иммунные реакции у мышей. вакцина. 2013;31:3281–3287. doi: 10.1016/j.vaccine.2013.05.019. [PubMed] [CrossRef] [Google Scholar]
. Рекомбинантная адено-вакцина, экспрессирующая частицы, подобные энтеровирусу 71, против болезни рук, ящура и рта. PLoS Негл. Троп. Дис. 2015;9:e0003692. doi: 10.1371/journal.pntd.0003692. [Статья бесплатно PMC] [PubMed] [CrossRef] [Google Scholar]
53. Yan Q., Wu L., Chen L., Qin Y., Pan Z., Chen M. Вакцины на основе вируса везикулярного стоматита, экспрессирующие EV71 вирусоподобные частицы вызывают сильный иммунный ответ и защищают новорожденных мышей от летальных исходов. вакцина. 2016; 34:4196–4204. doi: 10.1016/j.vaccine.2016.06.058. [PubMed] [CrossRef] [Google Scholar]
вакцина. 2016; 34:4196–4204. doi: 10.1016/j.vaccine.2016.06.058. [PubMed] [CrossRef] [Google Scholar]
54. Вентарола Д., Бордоне Л., Сильверберг Н. Обновленная информация о ящуре. клин. Дерматол. 2015;33:340–346. doi: 10.1016/j.clidermatol.2014.12.011. [PubMed] [CrossRef] [Академия Google]
55. Zhang W., Dai W., Zhang C., Zhou Y., Xiong P., Wang S., Ye X., Liu Q., Zhou D., Huang Z. Основанный на вирусоподобных частицах Четырехвалентная вакцина против ящура и кистей рук вызывает широкий и сбалансированный защитный иммунитет. Эмердж. микробы заражают. 2018;7:94. doi: 10.1038/s41426-018-0094-1. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
56. Wu C.N., Lin Y.C., Fann C., Liao N.S., Shih S.R., Ho M.S. Защита новорожденных мышей от летальной инфекции энтеровирусом 71 путем пассивной иммунизации субъединичными вакцинами VP1 и инактивированным вирусом. вакцина. 2001;20:895–904. doi: 10.1016/S0264-410X(01)00385-1. [PubMed] [CrossRef] [Google Scholar]
57. Zhou S.L., Ying XL, Han X., Sun X.X., Jin Q., Yang F. Характеристика белка энтеровируса 71 VP1 как кандидата на вакцину. Дж. Мед. Вирол. 2015; 87: 256–262. doi: 10.1002/jmv.24018. [PubMed] [CrossRef] [Google Scholar]
Zhou S.L., Ying XL, Han X., Sun X.X., Jin Q., Yang F. Характеристика белка энтеровируса 71 VP1 как кандидата на вакцину. Дж. Мед. Вирол. 2015; 87: 256–262. doi: 10.1002/jmv.24018. [PubMed] [CrossRef] [Google Scholar]
58. Мэн Т., Колпе А.Б., Кинер Т.К., Чоу В.Т., Кванг Дж. Отображение VP1 на поверхности бакуловируса и его иммуногенность против гетерологичных штаммов энтеровируса человека 71 у мышей. ПЛОС ОДИН. 2011;6:e21757. doi: 10.1371/journal.pone.0021757. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
59. Wang X., Dong K., Long M., Lin F., Gao Z., Wang L., Zhang Z., Chen X., Dai Y., Wang H., et al. Индукция ответа антител с высоким титром с использованием вирусоподобных частиц на основе HIV gag-EV71 VP1, обладающих способностью защищать новорожденных мышей, зараженных летальной дозой энтеровируса 71. Arch. Вирол. 2018; 163:1851–1861. doi: 10.1007/s00705-018-3797-7. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
60. Han X., Ying XL, Zhou S. L., Han T., Huang H., Jin Q., Yang F., Sun Q.Y., Sun X.X. Характеристика полипротеина Р1 энтеровируса 71, экспрессируемого в Pichia pastor, в качестве вакцины-кандидата. Гум. Вакцина. Иммунотер. 2014;10:2220–2226. дои: 10.4161/hv.29123. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
L., Han T., Huang H., Jin Q., Yang F., Sun Q.Y., Sun X.X. Характеристика полипротеина Р1 энтеровируса 71, экспрессируемого в Pichia pastor, в качестве вакцины-кандидата. Гум. Вакцина. Иммунотер. 2014;10:2220–2226. дои: 10.4161/hv.29123. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
61. Fournillier A., Wychowski C., Boucreux D., Baumert T.F., Meunier J.C., Jacobs D., Muguet S., Depla E. , Inchauspe G. Индукция специфического иммунного ответа белка оболочки вируса гепатита С E1 может быть усилена мутацией сайтов N-гликозилирования. Дж. Вирол. 2001;75:12088–12097. doi: 10.1128/ОВИ.75.24.12088-12097.2001. [ Бесплатная статья PMC ] [ PubMed ] [ CrossRef ] [ Google Scholar ]
Модификации гликопротеина оболочки вируса иммунодефицита человека повышают иммуногенность при генетической иммунизации. Дж. Вирол. 2002; 76: 5357–5368. doi: 10.1128/ОВИ.76.11.5357-5368.2002. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
63. Фу Д.Г., Алонсо С., Фун М. С., Рамачандран Н.П., Чоу В.Т., Пох К.Л. Идентификация нейтрализующих линейных эпитопов капсидного белка VP1 энтеровируса 71 с использованием синтетических пептидов. Вирус рез. 2007; 125:61–68. doi: 10.1016/j.virusres.2006.12.005. [PubMed] [CrossRef] [Google Scholar]
С., Рамачандран Н.П., Чоу В.Т., Пох К.Л. Идентификация нейтрализующих линейных эпитопов капсидного белка VP1 энтеровируса 71 с использованием синтетических пептидов. Вирус рез. 2007; 125:61–68. doi: 10.1016/j.virusres.2006.12.005. [PubMed] [CrossRef] [Google Scholar]
64. Фу Д.Г., Алонсо С., Чоу В.Т., Пох К.Л. Пассивная защита от летальной инфекции энтеровируса 71 у новорожденных мышей за счет нейтрализации антител, индуцированных синтетическим пептидом. Микробы. Заразить. 2007;9: 1299–1306. doi: 10.1016/j.micinf.2007.06.002. [PubMed] [CrossRef] [Google Scholar]
65. Liu J.N., Wang W., Duo J.Y., Hao Y., Ma C.M., Li W.B., Lin S.Z., Gao X.Z., Liu X.L., Xu Y.F., et al. Комбинированные пептиды энтеровируса человека 71 защищают от вирусной инфекции у мышей. вакцина. 2010; 28:7444–7451. doi: 10.1016/j.vaccine.2010.08.080. [PubMed] [CrossRef] [Google Scholar]
66. Aw-Yong K.L., Sam I.C., Koh M.T., Chan Y.F. Иммунодоминантные эпитопы IgM и IgG, распознаваемые антителами, индуцированными у пациентов с энтеровирусом A71-ассоциированным заболеванием рук, ящура. ПЛОС ОДИН. 2016;11:e0165659. doi: 10.1371/journal.pone.0165659. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
ПЛОС ОДИН. 2016;11:e0165659. doi: 10.1371/journal.pone.0165659. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
67. Xu L., He D., Li Z., Zheng J., Yang L., Yu M., Yu H., Chen Y. , Que Y., Shih J.W., et al. Защита от летального заражения энтеровирусом 71 у мышей с помощью рекомбинантной вакцины-кандидата, содержащей эпитоп с широкой перекрестной нейтрализацией в петле EF VP2. Тераностика. 2014; 4: 498–513. doi: 10.7150/thno.7457. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
68. Huo C., Yang J., Lei L., Qiao L., Xin J., Pan Z. Ядерные частицы вируса гепатита B, содержащие множественные эпитопы обеспечивают защиту от энтеровируса 71 и вируса Коксаки A16 у мышей. вакцина. 2017; 35:7322–7330. doi: 10.1016/j.vaccine.2017.10.101. [PubMed] [CrossRef] [Академия Google]
69. Jiang L., Fan R., Sun S., Fan P., Su W., Zhou Y., Gao F., Xu F., Kong W., Jiang C. Новый эпитоп EV71 VP3 в норовирусе Вектор частицы P проявляет нейтрализующую активность и защиту in vivo у мышей. вакцина. 2015;33:6596–6603. doi: 10.1016/j.vaccine.2015.10.104. [PubMed] [CrossRef] [Google Scholar]
вакцина. 2015;33:6596–6603. doi: 10.1016/j.vaccine.2015.10.104. [PubMed] [CrossRef] [Google Scholar]
70. Mustafa S., Abd-Aziz N., Saw W.T., Liew S.Y., Yusoff K., Shafee N. Рекомбинантный энтеровирус 71 Вирусный белок 1, слитый с укороченным вирусом болезни Ньюкасла NP (NPt) белок-носитель. Вакцины (Базель) 2020; 8:742. дои: 10.3390/вакцин8040742. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Антителозависимая усиленная инфекция энтеровируса 71 in vitro и in vivo. Вирол. Дж. 2011; 8:106. doi: 10.1186/1743-422X-8-106. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
72. Wang X., Peng W., Ren J., Hu Z., Xu J., Lou Z., Li X., Yin W. , Shen X., Porta C., et al. Механизм сенсора-адаптера для снятия оболочки энтеровируса со структур EV71. Нац. Структура Мол. биол. 2012;19: 424–429. doi: 10.1038/nsmb.2255. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
73. Pardi N., Hogan M.J., Porter F.W., Weissman D. мРНК-вакцины — новая эра в вакцинологии.

 , при 100°С — мгновенно), быстро разрушаются под воздействием хлорсодержащих препаратов, ультрафиолетового облучения, при высушивании, кипячении. Тем не менее, при температуре 37°С вирусы могут сохранять жизнеспособность в течение 50-65 дней, длительно сохраняются в воде. В замороженном состоянии активность энтеровирусов сохраняется в течение многих лет, при хранении в обычном холодильнике (+4° — +6°С) — в течение нескольких недель, а при комнатной температуре — на протяжении нескольких дней. Они выдерживают многократное замораживание и оттаивание без потери активности. Резервуаром и источником инфекции является больной человек или инфицированный бессимптомный носитель вируса.
, при 100°С — мгновенно), быстро разрушаются под воздействием хлорсодержащих препаратов, ультрафиолетового облучения, при высушивании, кипячении. Тем не менее, при температуре 37°С вирусы могут сохранять жизнеспособность в течение 50-65 дней, длительно сохраняются в воде. В замороженном состоянии активность энтеровирусов сохраняется в течение многих лет, при хранении в обычном холодильнике (+4° — +6°С) — в течение нескольких недель, а при комнатной температуре — на протяжении нескольких дней. Они выдерживают многократное замораживание и оттаивание без потери активности. Резервуаром и источником инфекции является больной человек или инфицированный бессимптомный носитель вируса.
 Около 85% случаев заболеваний протекает бессимптомно, в 12-14% диагностируются легкие формы заболевания, и только 1-3% имеют тяжелое течение. Особую опасность энтеровирусные инфекции представляют для лиц со сниженным иммунитетом.
Около 85% случаев заболеваний протекает бессимптомно, в 12-14% диагностируются легкие формы заболевания, и только 1-3% имеют тяжелое течение. Особую опасность энтеровирусные инфекции представляют для лиц со сниженным иммунитетом. Поэтому следует обязательно прививаться в рамках национального календаря прививок, в который включена иммунизация против полиомиелита.
Поэтому следует обязательно прививаться в рамках национального календаря прививок, в который включена иммунизация против полиомиелита.