Содержание
Столбняк, дифтерия и коклюш — Институт безопасности вакцин
Рек. ACIP | Болезнь | Вакцина | Источники и ссылки | ВИС (DTaP) ВИС (Tdap) ВИС (Td) | Модули ВОЗ
Рекомендации Консультативного комитета по практике иммунизации (ACIP)
Младенцы и дети
• Все младенцы без противопоказаний должны получить три дозы детской комбинированной вакцины против столбняка, дифтерии и коклюша (аббревиатура: DTaP; торговые названия: Daptacel®, Infanrix®) вводят в возрасте 2, 4 и 6 месяцев.
• Четвертую дозу следует вводить через 6–12 месяцев после третьей дозы, предпочтительно в возрасте от 15 до 18 месяцев.
• Пятая доза рекомендуется в возрасте от 4 до 6 лет.
Подростки и взрослые
• Одна доза бустерной вакцины против столбняка, дифтерии и коклюша (аббревиатура: Tdap; торговые названия: Boostrix®, Adacel®) должна быть введена всем подросткам в возрасте от 11 до 18 лет.
• Вакцину Tdap также следует вводить всем подросткам и взрослым, которые никогда ранее ее не получали, особенно если в ближайшем будущем они будут контактировать с новорожденными [1–3].
Для получения дополнительной информации
• Рекомендации ACIP: https://www.cdc.gov/vaccines/hcp/acip-recs/vacc-specific/tdap-td.html
• Графики прививок: http://www. cdc.gov/vaccines/schedules/index.html
Важная информация для акушеров
- Обычно рекомендуется одна доза Tdap в течение каждой беременности, предпочтительно между 27 и 36 неделями беременности.
- Если мать не вакцинирована во время беременности и никогда не получала вакцину Tdap, вакцину следует ввести ей сразу после родов [1-3].
Болезнь
Дифтерия вызывается токсином аэробной грамположительной бактерии Corynebacterium diphtheria . Инкубационный период обычно составляет 2-5 дней. Дифтерия может поражать почти любую слизистую оболочку, но чаще всего поражает глотку и миндалины. Заболевание начинается коварно с легких симптомов, таких как недомогание, боль в горле, субфебрильная температура и анорексия. Мембрана формируется и расширяется в течение 2-3 дней, потенциально вызывая обструкцию дыхательных путей, а иногда приводит к коме и смерти в течение 6-10 дней. Осложнения дифтерии в основном связаны с токсином, а наиболее частыми осложнениями, помимо дыхательной обструкции, являются паралич и миокардит.
Мембрана формируется и расширяется в течение 2-3 дней, потенциально вызывая обструкцию дыхательных путей, а иногда приводит к коме и смерти в течение 6-10 дней. Осложнения дифтерии в основном связаны с токсином, а наиболее частыми осложнениями, помимо дыхательной обструкции, являются паралич и миокардит.
Столбняк вызывается экзотоксином анаэробной грамположительной спорообразующей бактерии Clostridium tetani. Споры могут годами выживать в суровых условиях и широко распространены в фекалиях животных и почве. Обычно микроорганизм попадает в организм человека через разрез на коже, после чего споры прорастают, а токсины распространяются по кровеносной и лимфатической системам, воздействуя на нейротрансмиттеры и вызывая мышечные сокращения и спазмы. Инкубационный период составляет в среднем 8 дней, но колеблется от 3 до 21 дня. Наиболее распространенным типом заболевания является генерализованный столбняк, который обычно начинается с тризма челюсти и завершается частыми спазмами, длящимися до месяца. Столбняк приводит к летальному исходу примерно в 11% случаев, даже при наличии интенсивной терапии; вероятность летального исхода у людей, которые никогда не были вакцинированы, в два раза выше. Столбняк новорожденных, хотя и редко встречающийся в США, может возникнуть, когда младенцы рождаются у матерей с недостаточным иммунитетом к столбняку, обычно в результате инфицирования незажившей культи пуповины. Поскольку это патоген окружающей среды, защита сообщества (также известная как «коллективный иммунитет») отсутствует.
Столбняк приводит к летальному исходу примерно в 11% случаев, даже при наличии интенсивной терапии; вероятность летального исхода у людей, которые никогда не были вакцинированы, в два раза выше. Столбняк новорожденных, хотя и редко встречающийся в США, может возникнуть, когда младенцы рождаются у матерей с недостаточным иммунитетом к столбняку, обычно в результате инфицирования незажившей культи пуповины. Поскольку это патоген окружающей среды, защита сообщества (также известная как «коллективный иммунитет») отсутствует.
Коклюш, также известный как коклюш, является высококонтагиозным заболеванием, вызываемым аэробной грамотрицательной палочковидной бактерией Bordetella pertussis . Инкубационный период коклюша чаще всего составляет 7-10 дней. Заболевание начинается с насморка, чихания, субфебрилитета и легкого кашля. Этот кашель постепенно становится более сильным, прогрессируя в частые приступы многочисленного быстрого кашля через 1-2 недели. Эти приступы кашля (пароксизмы) приводят к характерному коклюшу при попытках вдохнуть. Эти приступы кашля обычно продолжаются в течение 1-6 недель, но могут сохраняться до 10 недель. Младенцы подвергаются наибольшему риску осложнений, связанных с коклюшем. Наиболее частым осложнением и причиной большинства смертельных случаев, связанных с коклюшем, является пневмония. Раньше коклюш был существенной причиной смерти детей в США, но с момента введения вакцины заболеваемость коклюшем снизилась более чем на 80%. Однако в последние несколько десятилетий заболеваемость коклюшем снова постепенно увеличивается [1].
Эти приступы кашля обычно продолжаются в течение 1-6 недель, но могут сохраняться до 10 недель. Младенцы подвергаются наибольшему риску осложнений, связанных с коклюшем. Наиболее частым осложнением и причиной большинства смертельных случаев, связанных с коклюшем, является пневмония. Раньше коклюш был существенной причиной смерти детей в США, но с момента введения вакцины заболеваемость коклюшем снизилась более чем на 80%. Однако в последние несколько десятилетий заболеваемость коклюшем снова постепенно увеличивается [1].
Вакцина
Бесклеточные коклюшные вакцины являются инактивированными, субъединичными вакцинами и доступны только в сочетании с дифтерийным и столбнячным анатоксинами. Вакцина DTaP (торговые названия: Daptacel®, Infanrix®) одобрена для детей в возрасте от шести недель до 7 лет. Вакцина Tdap (торговые названия: Boostrix®, Adacel®) содержит уменьшенное количество антигена для дифтерии и коклюша и одобрена для лиц в возрасте от 10 до 64 лет (Boostrix®) или от 11 до 64 лет (Adacel®) [1].
Эффективность вакцины: Полная первичная серия из 3 доз дифтерийного анатоксина и столбнячного анатоксина приводит к предполагаемой клинической эффективности 95% и 100% соответственно. Эффективность бесклеточного коклюшного компонента вакцин DTaP, лицензированных в США, оценивается в 84% в краткосрочной перспективе (т. е. в течение 3 лет после завершения серии). Антительный ответ на одну дозу Tdap у взрослых аналогичен таковому у младенцев после трех доз DTaP [1, 5, 6]. Младенцы, рожденные матерями, иммунизированными во время беременности, имеют от 50 до 100% титров коклюшных антител своих матерей [7].
Однако со временем иммунитет ослабевает. К десяти годам после вакцинации уровень противостолбнячного антитоксина у некоторых людей снижается ниже минимального защитного уровня. Особую озабоченность вызывает ослабление иммунитета от бесклеточной коклюшной вакцины. Это одна из основных причин вакцинации Tdap во время каждой беременности [1].
Безопасность вакцины: Местные реакции, включая боль, покраснение и отек, возникают у 20–40% младенцев после первых трех доз DTaP. Самокупирующаяся лихорадка выше 101°F возникает у 3-5% реципиентов DTaP. Сообщалось об обширном отеке конечности в месте инъекции, усилении местных реакций и лихорадке после четвертой или пятой дозы DTaP. Системные реакции от умеренных до тяжелых, такие как лихорадка выше 105 ° F, фебрильные судороги, постоянный плач, продолжающийся более 3 часов, и гипотонические гипореактивные эпизоды возникают менее чем в 1 из 10 000 доз DTaP [1].
Самокупирующаяся лихорадка выше 101°F возникает у 3-5% реципиентов DTaP. Сообщалось об обширном отеке конечности в месте инъекции, усилении местных реакций и лихорадке после четвертой или пятой дозы DTaP. Системные реакции от умеренных до тяжелых, такие как лихорадка выше 105 ° F, фебрильные судороги, постоянный плач, продолжающийся более 3 часов, и гипотонические гипореактивные эпизоды возникают менее чем в 1 из 10 000 доз DTaP [1].
Местные реакции возникают у 21-66% взрослых после Tdap. Лихорадка выше 100,4 ° F возникает у 1,4% реципиентов Tdap. После вакцинации иногда возникают легкие системные реакции, такие как головная боль или сонливость. Помимо очень редких случаев анафилаксии, вакцинация Tdap не вызывала серьезных побочных эффектов*. Тяжелая аллергическая реакция (например, анафилаксия) на предыдущую дозу или компонент вакцины является противопоказанием для дальнейшей вакцинации Tdap [1].
Вакцины, которые могут вызывать лихорадку, также могут редко вызывать фебрильные судороги. Фебрильные судороги являются распространенным и, как правило, доброкачественным заболеванием детского возраста, возникающим у 2-5% детей в какой-то момент в течение первых пяти лет их жизни. По оценкам, фоновая частота фебрильных судорог составляет 240–480 на 100 000 человеко-лет у детей в возрасте до пяти лет, хотя эта частота значительно зависит от возраста, генетики, сопутствующих заболеваний и факторов риска окружающей среды. Простые фебрильные судороги не имеют долгосрочных последствий, за исключением, возможно, повышенного риска рецидива [8-11]. См. Вызывают ли вакцины судороги? резюме для более подробной информации.
Фебрильные судороги являются распространенным и, как правило, доброкачественным заболеванием детского возраста, возникающим у 2-5% детей в какой-то момент в течение первых пяти лет их жизни. По оценкам, фоновая частота фебрильных судорог составляет 240–480 на 100 000 человеко-лет у детей в возрасте до пяти лет, хотя эта частота значительно зависит от возраста, генетики, сопутствующих заболеваний и факторов риска окружающей среды. Простые фебрильные судороги не имеют долгосрочных последствий, за исключением, возможно, повышенного риска рецидива [8-11]. См. Вызывают ли вакцины судороги? резюме для более подробной информации.
Поскольку сообщалось об обмороках среди подростков, получающих прививки, подростки-реципиенты всегда должны получать вакцину сидя, а не на виду у других, ожидающих вакцинации, и находиться под наблюдением в течение 15 минут сразу после вакцинации [12-15].
Противопоказания и меры предосторожности: Тяжелая аллергическая реакция (например, анафилаксия) на предыдущую дозу или компонент вакцины является противопоказанием для дальнейшей вакцинации DTaP и Tdap. Другим противопоказанием для обеих вакцин является энцефалопатия в течение 7 дней после предыдущей вакцинации без идентифицируемой альтернативной причины. Текущее острое заболевание средней и тяжелой степени является мерой предосторожности при любой вакцинации.
Другим противопоказанием для обеих вакцин является энцефалопатия в течение 7 дней после предыдущей вакцинации без идентифицируемой альтернативной причины. Текущее острое заболевание средней и тяжелой степени является мерой предосторожности при любой вакцинации.
Меры предосторожности при АКДС включают следующие проявления в течение 48 часов после предыдущей вакцинации: эпизод гипотонической гипореактивности, который представляет собой внезапный эпизод отсутствия реакции и вялости [4], лихорадку выше 105°F или постоянный, безутешный плач, продолжающийся более 3 часов . Другие меры предосторожности включают судороги в течение 3 дней после предыдущей вакцинации или нестабильное прогрессирующее неврологическое расстройство.
Меры предосторожности при Tdap включают наличие в анамнезе синдрома Гийена-Барре в течение 6 недель после предыдущей вакцинации, содержащей столбнячный анатоксин, или наличие в анамнезе тяжелой местной реакции сразу после предыдущей вакцинации, содержащей столбнячный или дифтерийный анатоксин [1].
Соображения во время беременности:
Одна доза Tdap обычно рекомендуется во время каждой беременности, предпочтительно между 27 и 36 неделями беременности.
Если мать не вакцинирована во время беременности и никогда не получала вакцину Tdap, вакцину следует ввести ей сразу после родов [16, 17].
Вакцинация Tdap во время беременности помогает защитить младенцев от коклюша. Новорожденные и младенцы в первые несколько месяцев жизни зависят от трансплацентарно приобретенных материнских коклюшных антител и профилактики заражения от близких контактов для защиты от коклюша, поскольку активная иммунизация младенца не начинается до 2-месячного возраста и требуется несколько доз. индуцировать защиту от коклюша у большинства младенцев. Почти все случаи смерти от коклюша происходят в первые несколько месяцев жизни, чаще всего до получения рутинной вакцинации младенцев против коклюша [16, 17].
Было показано, что материнская вакцинация Tdap эффективна для предотвращения заболевания коклюшем у младенцев при ее использовании в рамках крупномасштабной вакцинации в Соединенном Королевстве [18].
Большой объем данных свидетельствует о безопасности вакцины Tdap как для беременных женщин, так и для их еще не родившихся детей [16, 17, 19, 20]. Прием Tdap во время беременности не связан с повышенным риском гипертензивных нарушений беременности или преждевременных или малоразмерных для гестационного возраста (SGA) родов [21]. Недавняя вакцинация против столбняка не увеличивает риск неблагоприятных исходов после вакцинации Tdap во время беременности [22]. Одновременное введение Tdap и противогриппозных вакцин во время беременности не связано с более высоким риском неблагоприятных исходов по сравнению с последовательной вакцинацией [23].
* Серьезное нежелательное явление определяется Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) как результат «любого из следующих исходов: смерть, опасное для жизни нежелательное явление, госпитализация в стационаре или продление существующей госпитализации, стойкое или значительная нетрудоспособность или существенное нарушение способности вести нормальную жизнедеятельность или врожденная аномалия/врожденный дефект.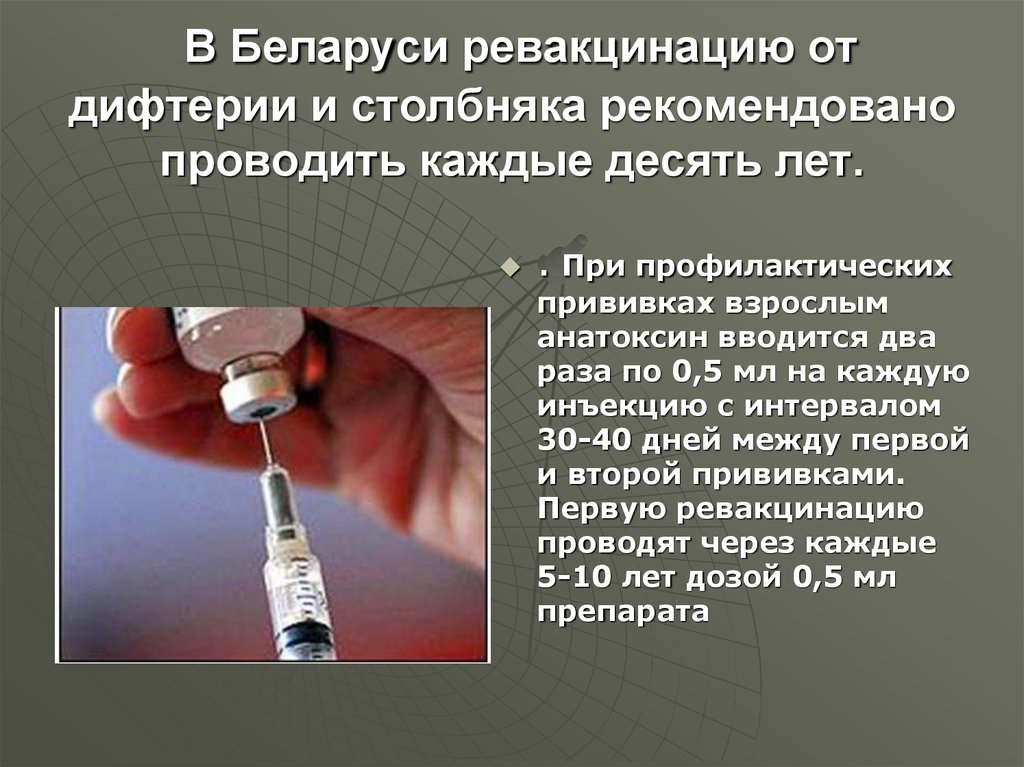 Важные медицинские события, которые могут не привести к смерти, быть опасными для жизни или потребовать госпитализации, могут считаться серьезными, если на основании соответствующего медицинского заключения они могут поставить под угрозу пациента или субъекта и могут потребовать медицинского или хирургического вмешательства для предотвращения одного из исходов. перечисленных в этом определении». Это определение можно найти в Разделе 21, §312.32 Электронного свода федеральных правил
Важные медицинские события, которые могут не привести к смерти, быть опасными для жизни или потребовать госпитализации, могут считаться серьезными, если на основании соответствующего медицинского заключения они могут поставить под угрозу пациента или субъекта и могут потребовать медицинского или хирургического вмешательства для предотвращения одного из исходов. перечисленных в этом определении». Это определение можно найти в Разделе 21, §312.32 Электронного свода федеральных правил
Источники и ссылки
Это краткое изложение преимущественно основано на опубликованных рекомендациях Консультативного комитета по практике иммунизации (ACIP) и учебнике CDC под названием «Эпидемиология и Профилактика вакциноуправляемых заболеваний, также известная как «Розовая книга». Каждое резюме начинается с рекомендаций ACIP, комитета из 15 экспертов, который консультирует Центры по контролю и профилактике заболеваний (CDC) и публикует исчерпывающие заявления об использовании отдельных вакцин, включая информацию о бремени болезни, которую предотвращает вакцина. эффективность вакцины, безопасность вакцины, показания, меры предосторожности, противопоказания и другую важную информацию. С рекомендациями ACIP по отдельным вакцинам можно ознакомиться по адресу www.cdc.gov/vaccines/hcp/acip-recs/index.html. IVS дополнил информацию во многих разделах другими недавними публикациями. IVS берет на себя ответственность за содержание.
эффективность вакцины, безопасность вакцины, показания, меры предосторожности, противопоказания и другую важную информацию. С рекомендациями ACIP по отдельным вакцинам можно ознакомиться по адресу www.cdc.gov/vaccines/hcp/acip-recs/index.html. IVS дополнил информацию во многих разделах другими недавними публикациями. IVS берет на себя ответственность за содержание.
1. Эпидемиология и профилактика вакциноуправляемых заболеваний. В: Hamborsky J KA, Wolfe S ed. 13 изд. Вашингтон, округ Колумбия: Центры по контролю и профилактике заболеваний; 2015.
2. Обновленные рекомендации по использованию столбнячного анатоксина, редуцированного дифтерийного анатоксина и бесклеточной коклюшной (Tdap) вакцины Консультативного комитета по практике иммунизации, 2010 г. MMWR Morb Mortal Wkly Rep. 2011;60(1):13-5.
3. Лян Дж.Л., Тивари Т., Моро П., Мессонье Н.Е., Рейнгольд А., Сойер М., Кларк Т.А. Профилактика коклюша, столбняка и дифтерии с помощью вакцин в США: рекомендации Консультативного комитета по практике иммунизации (ACIP). MMWR Recomm Rep 2018;67(2):1–44.
MMWR Recomm Rep 2018;67(2):1–44.
4. Золотой МС. Гипотонически-гипореактивные эпизоды после вакцинации против коклюша: повод для беспокойства? Препарат Саф. 2002;25(2):85-90.
5. Фултон Т.Р., Фадке В.К., Оренштейн В.А., Хинман А.Р., Джонсон В.Д., Омер С.Б. Защитный эффект современных коклюшных вакцин: систематический обзор и метаанализ. Клин Инфекция Дис. 2016;62(9):1100-10.
6. Чжан Л., Прич С.О., Аксельссон И., Гальперин С.А. Бесклеточные вакцины для профилактики коклюша у детей. Кокрановская система базы данных, ред. 2014(9):Cd001478.
7. Ван Рие А., Вендельбо А.М., Инглунд Дж.А. Роль материнских коклюшных антител у младенцев. Pediatr Infect Dis J. 2005;24(5 Suppl):S62-5.
8. (ААП) ААОП. Нейродиагностическая оценка ребенка с простыми фебрильными судорогами. Педиатрия. 2011;127(2):389-94.
9. (ААП) ААОП. Фебрильные судороги: клиническое руководство по долгосрочному ведению ребенка с простыми фебрильными судорогами. Педиатрия. 2008;121(6):1281-6.
10. Bonhoeffer J, Menkes J, Gold MS, de Souza-Brito G, Fisher MC, Halsey N, et al. Генерализованный судорожный припадок как нежелательное явление после иммунизации: определение случая и рекомендации по сбору, анализу и представлению данных. вакцина. 2004;22(5-6):557-62.
Bonhoeffer J, Menkes J, Gold MS, de Souza-Brito G, Fisher MC, Halsey N, et al. Генерализованный судорожный припадок как нежелательное явление после иммунизации: определение случая и рекомендации по сбору, анализу и представлению данных. вакцина. 2004;22(5-6):557-62.
11. Це А., Ценг Х.Ф., Грин С.К., Веллоцци С., Ли Г.М. Идентификация сигналов и оценка риска фебрильных судорог у детей после введения трехвалентной инактивированной вакцины против гриппа в рамках Проекта передачи данных по безопасности вакцин, 2010–2011 гг. вакцина. 2012;30(11):2024-31.
12. Kroger 13. Обморок после вакцинации – США, январь 2005 г. – июль 2007 г. MMWR Morb Mortal Wkly Rep. 2008;57(17):457-60.
14. Браун М.М., Патриарка П.А., Элленберг С.С. Обморок после иммунизации. Arch Pediatr Adolesc Med. 1997;151(3):255-9.
15. Bernard DM, Cooper Robbins SC, McCaffery KJ, Scott CM, Skinner SR. Эффект домино: реакция девочек-подростков на вакцинацию против вируса папилломы человека. Мед J Aust. 2011;194(6):297-300.
16. Заключение Комитета ACOG № 566: Новые данные об иммунизации и беременности: вакцинация против столбняка, дифтерии и коклюша. Акушерство Гинекол. 2013;121(6):1411-4.Общие рекомендации по иммунизации — рекомендации Консультативного комитета по практике иммунизации (ACIP). MMWR Recomm Rep. 2011;60(2):1-64.
17. Обновленные рекомендации по использованию противостолбнячного анатоксина, редуцированного дифтерийного анатоксина и бесклеточной коклюшной вакцины (Tdap) у беременных женщин – Консультативный комитет по практике иммунизации (ACIP), 2012 г. MMWR Morb Mortal Wkly Rep. 2013;62(7): 131-5.
18. Amirthalingam G, Campbell H, Ribeiro S, Fry NK, Ramsay M, Miller E, et al. Устойчивая эффективность программы иммунизации матерей против коклюша в Англии через 3 года после введения. Клин Инфекция Дис. 2016;63(доп.4):S236-s43.
19. Макмиллан М., Кларк М., Паррелла А., Фелл Д.Б., Амирталингам Г., Маршалл Х.С. Безопасность вакцинации против столбняка, дифтерии и коклюша во время беременности: систематический обзор. Акушерство Гинекол. 2017;129(3): 560-73.
Акушерство Гинекол. 2017;129(3): 560-73.
20. Kharbanda EO, Vazquez-Benitez G, Lipkind HS, Klein NP, Cheetham TC, Naleway AL, et al. Вакцинация матерей Tdap: охват и неотложные результаты безопасности в канале данных по безопасности вакцин, 2007–2013 гг. вакцина. 2016;34(7):968-73.
21. Kharbanda EO, Vazquez-Benitez G, Lipkind HS, Klein NP, Cheetham TC, Naleway A, et al. Оценка связи вакцинации матери против коклюша с акушерскими событиями и исходами родов. Джама. 2014;312(18):1897-904.
22. Sukumaran L, McCarthy NL, Kharbanda EO, McNeil MM, Naleway AL, Klein NP, et al. Ассоциация вакцинации Tdap с острыми событиями и неблагоприятными исходами родов среди беременных женщин с предшествующими вакцинациями против столбняка. Джама. 2015;314(15):1581-7.
23. Sukumaran L, McCarthy NL, Kharbanda EO, Weintraub ES, Vazquez-Benitez G, McNeil MM, et al. Безопасность столбнячного анатоксина, редуцированного дифтерийного анатоксина и бесклеточных вакцин против коклюша и гриппа при беременности. Акушерство Гинекол. 2015;126(5):1069-74.
Акушерство Гинекол. 2015;126(5):1069-74.
Темы для обсуждения
Темы для обсуждения
| Шаг 1: Выработайте сочувствие и доверие |
|
| Шаг 2. Кратко расскажите о конкретных проблемах, если таковые имеются |
| Шаг 3: Поворот к риску заболевания |
|
| Этап 4: Сообщение об эффективности вакцины |
|
| Шаг 5: Дайте сильную и персонализированную рекомендацию |
|



