Содержание
Приложение 25. Ежегодный список всех зарегистрированных случаев полиомиелита и острых вялых параличей (ОВП) (Рекомендуемый образец) \ КонсультантПлюс
- Главная
- Документы
- Приложение 25. Ежегодный список всех зарегистрированных случаев полиомиелита и острых вялых параличей (ОВП) (Рекомендуемый образец)
Санитарные правила, утв. данным документом, действуют до 1 сентября 2027 года.
Постановление Главного государственного санитарного врача РФ от 28.01.2021 N 4
(ред. от 25.05.2022)
«Об утверждении санитарных правил и норм СанПиН 3.3686-21 «Санитарно-эпидемиологические требования по профилактике инфекционных болезней»
(вместе с…
Приложение 25
к СП 3.3686-21
Рекомендуемый образец
ЕЖЕГОДНЫЙ СПИСОК
ВСЕХ ЗАРЕГИСТРИРОВАННЫХ СЛУЧАЕВ ПОЛИОМИЕЛИТА
И ОСТРЫХ ВЯЛЫХ ПАРАЛИЧЕЙ (ОВП)
в ______________________________
(субъект Российской Федерации)
ЭПИД N | Фамилия, имя, отчество (последнее при наличии) | Пол | Дата (4) | Возраст | Дата (4) | Количество прививок против полиомиелита | Даты (4) | Локал | Темп. | Быстрое Начало | Асимм | Дата (4) | Рез. | Лаб N | Лаб результаты | Окон | Клинический | ||||||||
рожден | начала пар. | план. | допол | последн. прививки | регистр | расслед | Ф1 | Ф2 | парал | парал | ПО | ПО | Ф1 | Р1 | Р2 | Р3 | НПЭВ | клас. | диагноз | ||||||
(1) | (2) | (3) | (5) | (6) | (7) | (8) | (9) | (10) | (11) | (12) | (13) | (14) | (15) | (16) | (17) | (18) | (19) | (20) | (21) | (22) | (22) | (22) | (23) | (24) | (25) |
Список всех зарегистрированных случаев полиомиелита и ОВП (продолжение) | |||||||||||||||||||||||||
(1) | Индивидуальный идентификационный номер (эпидномер). | ||||||||||||||||||||||||
(2) | Фамилия, имя, отчество (последнее при наличии) указываются сокращенно | ||||||||||||||||||||||||
(3) | Пол (1 = муж, 2 = жен, 9 = не известно). | ||||||||||||||||||||||||
(4) | Даты: день/месяц/год (ДД/ММ/ГГГГ). 4-значный формат года. | ||||||||||||||||||||||||
(5) | Дата рождения. Дата рождения или возраст должны представляться при первой регистрации, даже предварительной. | ||||||||||||||||||||||||
(6) | Возраст (количество полных лет). Обязательно, если не известна дата рождения. Для детей до 1 года жизни указывается «0», до двух лет — «1» и далее аналогичным образом. | ||||||||||||||||||||||||
Представляется | |||||||||||||||||||||||||
при регистрации. | |||||||||||||||||||||||||
(7) | Дата начала паралича. | ||||||||||||||||||||||||
(8) | Число доз ОПВ (любой полиовирусной вакцины), полученных в ходе плановой иммунизации по данным прививочной документации или «со слов» | ||||||||||||||||||||||||
(9) | Число дополнительных доз ОПВ | ||||||||||||||||||||||||
(10) | Дата получения последней дозы полиовакцины | ||||||||||||||||||||||||
(11) | Дата первого сообщения о случае в органы общественного здравоохранения | ||||||||||||||||||||||||
(12) | Дата эпидемиологического расследования органами общественного здравоохранения | ||||||||||||||||||||||||
(13) | Дата взятия первого образца стула от этого больного | ||||||||||||||||||||||||
(14) | Дата взятия второго образца стула от этого больного | ||||||||||||||||||||||||
(15) | Место паралича: 0 = только лицо, 1 = конечности, 2 = конечности и дыхательные мышцы (бульбарный), 3 = только бульбарный, 4 = конечности и лицо, 9 = не известно. | ||||||||||||||||||||||||
Обязательно при первичной регистрации, даже если данные предварительные | |||||||||||||||||||||||||
(16) | Наличие повышенной температуры в начале паралича: 1 = да, 2 = нет, 9 = не известно | ||||||||||||||||||||||||
(17) | Быстрое начало паралича (в течение 4 календарных дней): 1 = да, 2 = нет, 9 = не известно | ||||||||||||||||||||||||
(18) | Асимметрия параличей: 1 = да, 2 = нет, 9 = не известно | ||||||||||||||||||||||||
(19) | Дата повторного клинического осмотра | ||||||||||||||||||||||||
(20) | Результат повторного клинического осмотра через 60 календарных дней: 1 = остаточные параличи, 2 = нет остаточных параличей, 3 = потерян для наблюдения, 4 = умер | ||||||||||||||||||||||||
до повторного осмотра | |||||||||||||||||||||||||
(21) | Лабораторный номер для первого образца стула | ||||||||||||||||||||||||
(22) | Изолированы полиовирусы (Р1 = Тип 1; Р2 = Тип 2; Р3 = Тип 3): 1 = да, дикий, 2 = да, вакцинный, 3 = да, внутритиповая дифференциация не завершена, 4 = смесь — дикий/вакцинный, 5 = не изолирован, 6 = образцы не исследованы | ||||||||||||||||||||||||
(23) | Изолированы энтеровирусы: 1 = да, 2 = нет, 3 = образцы не исследованы | ||||||||||||||||||||||||
(24) | Окончательная классификация: | ||||||||||||||||||||||||
0 = не ОВП (спастические или хронические параличи или изолированные параличи лицевых нервов), | |||||||||||||||||||||||||
1 = подтвержденный полиомиелит (клинически или вирусологически), | |||||||||||||||||||||||||
2 = полиомиелит отвергнут, | |||||||||||||||||||||||||
3 = совместимый с полиомиелитом (по классификации ВОЗ), | |||||||||||||||||||||||||
4 = совместимый с полиомиелитом, возможно вакциноассоциированный, | |||||||||||||||||||||||||
5 = подтвержденный вакциноассоциированный, | |||||||||||||||||||||||||
6 = рассмотрен комитетом экспертов, классификация отложена до получения дополнительных клинических данных | |||||||||||||||||||||||||
(25) | Заключительный клинический диагноз: | ||||||||||||||||||||||||
0 = не ОВП: изолированные параличи лицевых нервов любой природы, спастические или хронические параличи, менингит, кома и иные | |||||||||||||||||||||||||
1 = Полиомиелит | |||||||||||||||||||||||||
2 = Полирадикулонейропатия/Синдром Гийена-Барре/Ландри, | |||||||||||||||||||||||||
3 = Миелит, | |||||||||||||||||||||||||
4 = Травматическая нейропатия, другие мононейропатии | |||||||||||||||||||||||||
5 = Опухоль спинного мозга (острая компрессия спинного мозга, вызванная новообразованием, гематомой, абсцессом) или другие новообразования, | |||||||||||||||||||||||||
6 = Периферическая нейропатия вследствие инфекции (дифтерия, боррелиоз) или интоксикации (тикозы, укус змеи, отравления тяжелыми металлами или инсектицидами), | |||||||||||||||||||||||||
7 = другие неспецифические неврологические заболевания, | |||||||||||||||||||||||||
8 = системные заболевания или нарушения метаболизма, заболевания мышц или костей, | |||||||||||||||||||||||||
9 = параличи неизвестной этиологии или неизвестный диагноз | |||||||||||||||||||||||||
Изолированные параличи лицевых нервов (если есть) должны иметь «локализацию паралича (16) = 0, «Окончательную классификацию = 0», «Заключительный клинический диагноз = 0» | |||||||||||||||||||||||||
Все случаи, у которых указаны «Локализация паралича = 0» и/или «Окончательная классификация = 0» не должны включаться в общее число случаев ОВП по итогам отчетного года и использоваться для расчета уровня заболеваемости ОВП, при этом в данный список они включаются | |||||||||||||||||||||||||
Приложение 24. Ежемесячный отчет о регистрации полиомиелита и острых вялых параличей и вирусологических исследованиях на полио и энтеровирусы (Рекомендуемый образец)
Ежемесячный отчет о регистрации полиомиелита и острых вялых параличей и вирусологических исследованиях на полио и энтеровирусы (Рекомендуемый образец)
Приложение 26. Направление на лабораторное (вирусологическое) исследование проб фекалий от больного полиомиелитом, острым вялым параличом (Рекомендуемый образец)
нОПВ2 – ГИЛП
Чтобы лучше справиться с меняющимся риском циркулирующего полиовируса вакцинного происхождения 2 типа (цПВВП2), партнеры ГИЛП вместе со странами внедряют инновационный инструмент – новую оральную полиомиелитную вакцину 2 типа (нОПВ2). Вакцина представляет собой модифицированную версию моновалентной ОПВ типа 2 (мОПВ2), которая, как показали клинические испытания, обеспечивает сравнимую защиту от полиовируса, будучи более генетической стабильностью и с меньшей вероятностью связанной с появлением цПВВП2 в условиях низкого иммунитета. Это означает, что nOPV2 может стать важным инструментом, помогающим более устойчиво останавливать вспышки.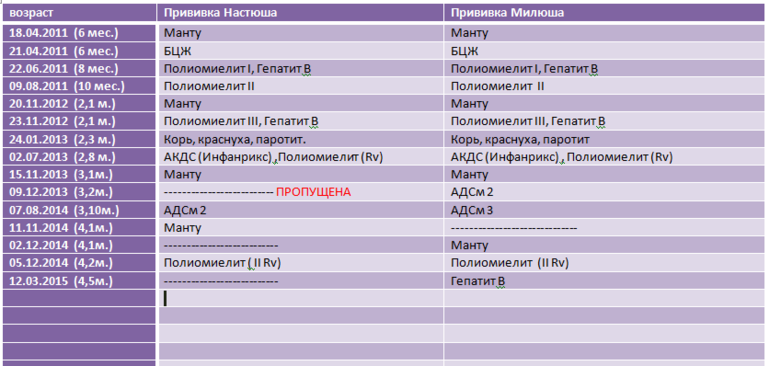
нОПВ2 внедряется в соответствии с процедурой Перечня использования в чрезвычайных ситуациях ВОЗ (EUL), чтобы обеспечить ее быструю доступность в полевых условиях. Даже после соблюдения строгих критериев EUL в отношении безопасности и иммуногенности эффективность nOPV2 в полевых условиях тщательно отслеживается в соответствии со стандартами EUL, и сбор данных продолжается с конечной целью предварительной квалификации ВОЗ и полного лицензирования.
Основные ресурсы
Обзор документов, информационных бюллетеней и часто задаваемых вопросов
Информационный бюллетень ГИЛП нОПВ2-цПВВП2 | Английский | французский |
Часто задаваемые вопросы по нОПВ2 | Английский | французский | арабский |
Краткое техническое описание nOPV2 | Английский | французский | Русский | португальский |
Информационный бюллетень PATH: Разработка новых вакцин против полиомиелита | Английский |
анимационное видео nOPV2 | Английский | французский | португальский | испанский | арабский | сомалийский | урду | пушту | Дари | фарси |
Инфографика процедуры включения ВОЗ в список для использования в чрезвычайных ситуациях | Английский | французский |
Научные исследования и данные по нОПВ2
Клиническое резюме новой оральной полиомиелитной вакцины типа 2 (нОПВ2) |Английский | французский | арабский | португальский | Русский |
Научные публикации по нОПВ2:
- Генетическая и фенотипическая стабильность полиовируса, выделенного от младенцев, получивших новые пероральные вакцины против полиомиелита типа 2 или Сэбина типа 2 в Панаме: анализ двух клинических испытаний ( The Lancet Microbe )
- Новый инструмент для искоренения древнего зла: история новой оральной вакцины против полиомиелита типа 2 (2022 Lancet Infectious Diseases публикация)
- Оценка стабильности аттенуированной вакцины Сэбина и двух новых пероральных вакцин против полиомиелита типа 2 у детей (2022 Вакцины npj , публикация )
- Глобальный консультативный комитет по безопасности вакцин, 17 сентября 2021 г.
 – Принципы использования вакцины nOPV2 (январь 2022 г., Еженедельный эпидемиологический бюллетень ВОЗ, публикация )
– Принципы использования вакцины nOPV2 (январь 2022 г., Еженедельный эпидемиологический бюллетень ВОЗ, публикация ) - Оценка генетических изменений и нейровирулентности выделенных вирусов Сэбина и новых вирусов пероральной полиомиелитной вакцины типа 2 (2021 npj Вакцины публикация)
- Разработка живой аттенуированной вакцины против полиомиелита для предотвращения возврата к вирулентности (публикация Cell Host & Microbe , 2020 г.)
- Разработка новой оральной вакцины против полиомиелита для окончательной ликвидации с использованием деоптимизации кодонов (публикация npj Vaccines , 2020 г.)
- Безопасность и иммуногенность двух новых кандидатов на пероральную полиомиелитную вакцину типа 2 по сравнению с моновалентной пероральной полиомиелитной вакциной типа 2 у здоровых взрослых: два клинических испытания (2020 г. Ланцет публикация)
- Безопасность и иммуногенность двух новых кандидатов на пероральную вакцину против полиомиелита типа 2 в сравнении с моновалентной пероральной вакциной против полиомиелита типа 2 у детей и младенцев: два клинических испытания (2020 , публикация Lancet )
- Безопасность и иммуногенность двух новых живых аттенуированных моновалентных (серотип 2) пероральных полиовирусных вакцин у здоровых взрослых: двойное слепое одноцентровое исследование фазы 1 (публикация Lancet , 2019 г.
 )
) - Варианты завершения полиомиелита: будут ли у нас необходимые вакцины ? (2019 Lancet комментарий)
- Полиополис (переписка 2019 г. в The Lancet )
- Полиополис: расширение границ научных инноваций для искоренения болезней (публикация Future Microbiology 2019 г.)
- Вакцинация против полиомиелита: прошлое, настоящее и будущее (публикация Future Microbiology 2015 г.)
- Реакция кишечных антител на две новые живые аттенуированные пероральные вакцины против полиомиелита типа 2 у здоровых взрослых в Бельгии (публикация Journal of Infectious Diseases, 2021 г.)
Нормативные документы
Отчет ВОЗ об оценке качества нОПВ2 | Английский | французский |
Вакцина против полиомиелита – новая оральная (нОПВ) моновалентная, тип 2 | Английский |
Обзор требований к использованию нОПВ2 согласно EUL
Дополнительные технические руководства по внедрению нОПВ2 (холодовая цепь, надзор и т.
 д.)
д.)
Руководство по обращению с вакцинами nOPV2 | Английский | французский | Русский | португальский |
Обращение с вакциной nOPV2 | Английский | французский | Русский | португальский |
Руководство по надзору за nOPV2 | Английский | французский | Русский | португальский |
Руководство по безопасности nOPV2 | Английский | французский | Русский | португальский |
nOPV2 Руководство по AESI | Английский | французский | Русский | португальский |
ГИЛП обучение реагированию на вспышки полиомиелита | Английский |
Внедрение нОПВ2 в ответ на вспышку полиомиелита: Руководство по надзору | Английский | французский |
Заявление о позиции ГИЛП: использование новой оральной полиомиелитной вакцины типа 2 в связи со сроком годности 12 месяцев или меньше | Английский |
Новая оральная полиомиелитная вакцина типа 2 (nOPV2), связанное с вакциной событие (VRE) План реагирования | Английский | французский | арабский | португальский |
Руководство по развитию ПВИЭ для стран | Английский | французский | португальский |
Стратегическое руководство ЮНИСЕФ по коммуникациям C4D для реагирования на вспышки, включая nOPV2 | Английский |
Пакет информационно-пропагандистских материалов для мер реагирования на вспышки цПВВП и нОПВ2 Введение | Английский |
Полевое руководство по борьбе с дезинформацией о вакцинах | Английский |
Рекомендации Исполнительного комитета ВОЗ и СКГЭ в отношении нОПВ2
Основные моменты совещания Стратегической консультативной группы экспертов (СКГЭ) по иммунизации 4–7 октября 2021 г. |английский |
|английский |
Концепция первоначального использования nOPV2, одобренная SAGE | Английский | французский |
Решение Исполнительного совета ВОЗ, призывающее государства-члены ускорить процессы выдачи разрешений на ввоз и использование нОПВ2 на основании ее перечня для использования в чрезвычайных ситуациях – февраль 2020 г. | Английский| французский|
Рекомендации SAGE — совещание в октябре 2021 г. (еженедельный эпидемиологический отчет) — на английском и французском языках
Рекомендации SAGE — совещание в июне 2021 г. (еженедельный эпидемиологический отчет) — на английском и французском языках Французский
Рекомендации SAGE, совещание, апрель 2020 г. (еженедельный эпидемиологический отчет) – английский и французский языки
Рекомендации SAGE, совещание, октябрь 2019 г. (еженедельный эпидемиологический отчет), – английский и французский языки
Центр СМИ
- Независимые эксперты советуют перейти к следующему этапу использования новой пероральной полиомиелитной вакцины типа 2
- Страны готовятся раз и навсегда изгнать все формы полиомиелита из Африки
- Рекомендации по отчетности о вспышках полиовируса | Английский | французский |
- Новая пероральная вакцина против полиомиелита типа 2 (nOPV2) получила промежуточную рекомендацию по применению в чрезвычайных ситуациях
- Рекомендация о выдаче разрешения на использование срочной вакцины для новой вакцины
- Специальный выпуск новостей о полиомиелите — май 2020 г.

Дополнительные ресурсы и обновленная информация
- Стратегия ответных мер на циркулирующий полиовирус вакцинного происхождения типа 2 на 2020–2021 | Английский |
- Рабочая группа по нОПВ2:
- Техническое задание
- Информационный лист
- Подкомитет GACVS по новой безопасности OPV2
Циркулирующий полиовирус вакцинного происхождения типа 2 (цПВВП2)
- Дом/
- Новости о вспышках болезней /
- Товар/
- Циркулирующий полиовирус вакцинного происхождения типа 2 (цПВВП2) – Алжир
Краткая информация о вспышке
8 июля 2022 г. ВОЗ получила уведомление о случае циркулирующего полиовируса вакцинного происхождения типа 2 (цПВВП2) с острым вялым параличом (ОВП) в провинции Таманрассет на юге Алжира. Это первый случай цПВВП2, выявленный в стране. Местные органы здравоохранения проводят полевое расследование и активный поиск дополнительных случаев ОВП; также запланирована кампания реактивной иммунизации.
Описание вспышки
8 июля 2022 г. через Глобальную лабораторную сеть полиомиелита (GPLN) в Алжире было сообщено о случае циркулирующего полиовируса вакцинного происхождения типа 2 (цПВВП2) в Алжире. Случай представляет собой ребенка в возрасте до двух лет из провинции Таманрассет, южный Алжир, с началом острого вялого паралича (ОВП) 11 апреля 2022 года. Образцы кала дали положительный результат на цПВВП2 в Институте Пастера в Алжире и были подтверждены Институтом Пастера в Париже. . Анализ геномной последовательности показывает, что выделенный вирус генетически связан с вирусом, ранее выделенным в Кано, Нигерия. Ребенок не получал никаких доз вакцины против полиомиелита и в анамнезе не выезжал за пределы провинции Таманрассет.
Это первый случай цПВВП2, выявленный в Алжире, где, согласно оценкам охвата иммунизацией ВОЗ-ЮНИСЕФ за 2021 г., охват Pol3 (третья доза полиомиелитной вакцины) составил 91%, а IPV1 (одна доза инактивированной полиомиелитной вакцины) охват составил 94%.
Эпидемиология Полиомиелит
Полиомиелит является высокоинфекционным заболеванием, которое в основном поражает детей в возрасте до пяти лет, вызывая необратимый паралич (приблизительно 1 из 200 инфекций) или смерть (2-10% парализованных).
Вирус передается от человека к человеку, в основном фекально-оральным путем или, реже, обычным переносчиком (например, зараженной водой или пищей) и размножается в кишечнике, откуда может проникнуть в нервную системы и вызвать паралич.
Инкубационный период обычно составляет 7–10 дней, но может варьироваться от 4 до 35 дней. До 90% инфицированных либо бессимптомны, либо имеют легкие симптомы, и болезнь обычно остается нераспознанной.
Полиовирус вакцинного происхождения представляет собой хорошо задокументированный штамм полиовируса, мутировавший из штамма, изначально содержащегося в пероральной полиомиелитной вакцине (ОПВ). ОПВ содержит живую ослабленную форму полиовируса, который размножается в кишечнике в течение ограниченного периода времени, тем самым вырабатывая иммунитет за счет накопления антител. В редких случаях при размножении в желудочно-кишечном тракте штаммы ОПВ генетически изменяются и могут распространяться в сообществах, которые не полностью вакцинированы против полиомиелита, особенно в районах с плохой гигиеной, плохой санитарией или перенаселенностью. Чем ниже популяционный иммунитет, тем дольше выживает этот вирус и тем больше генетических изменений он претерпевает.
В редких случаях при размножении в желудочно-кишечном тракте штаммы ОПВ генетически изменяются и могут распространяться в сообществах, которые не полностью вакцинированы против полиомиелита, особенно в районах с плохой гигиеной, плохой санитарией или перенаселенностью. Чем ниже популяционный иммунитет, тем дольше выживает этот вирус и тем больше генетических изменений он претерпевает.
В очень редких случаях вирус вакцинного происхождения может генетически измениться в форму, вызывающую паралич, как и дикий полиовирус – это то, что известно как полиовирус вакцинного происхождения (ПВВП). Обнаружение ПВВП по крайней мере в двух разных источниках с интервалом не менее двух месяцев, которые генетически связаны, демонстрируя признаки передачи в сообществе, следует классифицировать как «циркулирующий» полиовирус вакцинного происхождения типа 2 (цПВВП2). Циркулирующий полиовирус вакцинного происхождения типа 2 (цПВВП2) продолжает поражать различные регионы мира, особенно Африканский регион.
Меры общественного здравоохранения
- Усилен надзор для активного поиска дополнительных случаев ОВП в непосредственной близости от выявленного случая.
- В сотрудничестве с GPLN было начато подробное полевое расследование для определения масштабов циркуляции вируса (в том числе, возможно, в соседних странах).
- Подготовлен план реагирования в соответствии с пересмотренными СОП по реагированию на вспышку международной вспышки полиомиелита.
- Запланирована кампания реактивной иммунизации.
Оценка рисков ВОЗ
ВОЗ считает, что сохраняется высокий риск международного распространения цПВВП2 из-за сохраняющегося субоптимального иммунитета, пробелов в эпиднадзоре и крупномасштабных перемещений населения. Риск усугубляется снижением показателей иммунизации в связи с продолжающейся пандемией COVID-19.
Нынешний изолят в Алжире связан с вирусом, происходящим из Кано, Нигерия, что свидетельствует о возможности международного распространения этого заболевания.
Рекомендации ВОЗ
Важно, чтобы все страны, особенно те, которые часто путешествуют и контактируют со странами и районами, пораженными полиомиелитом, усилили эпиднадзор за случаями ОВП и начали плановое расширение эпиднадзора за окружающей средой, чтобы быстро выявлять любой новый завоз вируса и способствовать быстрому отклик. Страны, территории и районы также должны поддерживать одинаково высокий охват плановой иммунизацией на районном уровне, чтобы свести к минимуму последствия любого занесения нового вируса.
Организация ВОЗ по международным поездкам и здоровью рекомендует, чтобы все лица, совершающие поездки в районы, пораженные полиомиелитом, были полностью вакцинированы против полиомиелита. Жители (и посетители на срок более 4 недель) из зараженных районов должны получить дополнительную дозу пероральной полиомиелитной вакцины (ОПВ) или инактивированной полиомиелитной вакцины (ИПВ) в течение периода от четырех недель до 12 месяцев после поездки.
На основании рекомендаций Чрезвычайного комитета, созванного в соответствии с Международными медико-санитарными правилами (2005 г. ), риск международного распространения полиовируса остается чрезвычайной ситуацией в области общественного здравоохранения, имеющей международное значение (ЧСЗМЗ). На страны, затронутые передачей полиовируса, распространяются Временные рекомендации. Для выполнения Временных рекомендаций, изданных в рамках ЧСЗМЗ, любая страна, зараженная полиовирусом, должна объявить вспышку чрезвычайной ситуацией в области общественного здравоохранения, обеспечить вакцинацию жителей и лиц, прибывающих в течение длительного времени, и ограничить в пункте отъезда поездки лиц, у которых есть не были привиты или не могут подтвердить прививочный статус.
), риск международного распространения полиовируса остается чрезвычайной ситуацией в области общественного здравоохранения, имеющей международное значение (ЧСЗМЗ). На страны, затронутые передачей полиовируса, распространяются Временные рекомендации. Для выполнения Временных рекомендаций, изданных в рамках ЧСЗМЗ, любая страна, зараженная полиовирусом, должна объявить вспышку чрезвычайной ситуацией в области общественного здравоохранения, обеспечить вакцинацию жителей и лиц, прибывающих в течение длительного времени, и ограничить в пункте отъезда поездки лиц, у которых есть не были привиты или не могут подтвердить прививочный статус.
ВОЗ не рекомендует каких-либо ограничений на поездки и/или торговлю в Алжир на основании имеющейся информации об этом текущем событии.
Дополнительная информация
- Глобальная инициатива по ликвидации полиомиелита (ГИЛП)
- Глобальная сеть лабораторий по полиомиелиту (ГСПЛ)
- Информационный бюллетень ВОЗ по полиомиелиту
- Оценки ВОЗ/ЮНИСЕФ национального охвата иммунизацией
- Международные поездки и здоровье
- Стандартные операционные процедуры: реагирование на случай или вспышку полиовируса, версия 3.

Чрезвычайная ситуация в области общественного здравоохранения 9 ГИЛП0040

 в начале
в начале Присваивается при первичной регистрации.
Присваивается при первичной регистрации. Представляется при первой регистрации, даже если данные предварительные.
Представляется при первой регистрации, даже если данные предварительные.
 – Принципы использования вакцины nOPV2 (январь 2022 г., Еженедельный эпидемиологический бюллетень ВОЗ, публикация )
– Принципы использования вакцины nOPV2 (январь 2022 г., Еженедельный эпидемиологический бюллетень ВОЗ, публикация ) )
)