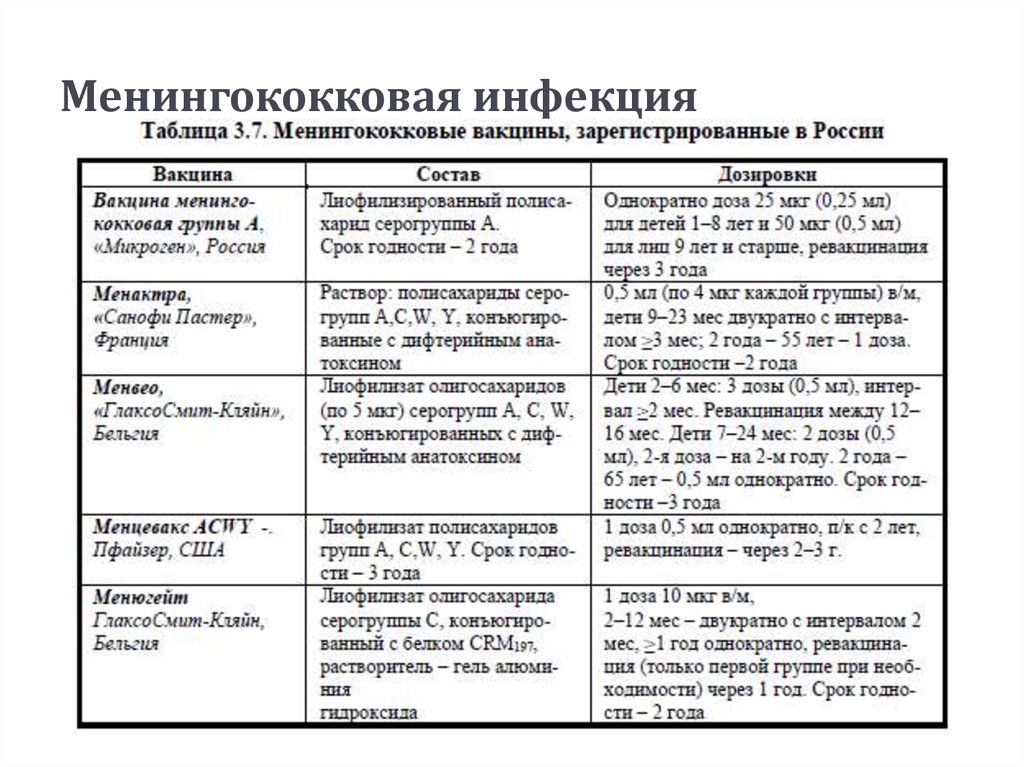
Содержание
Полисахаридная менингококковая вакцина А+С — инструкция по применению, дозы, побочные действия, отзывы о препарате Полисахаридная менингококковая вакцина А+С: — Энциклопедия лекарств РЛС
Описание препарата Полисахаридная менингококковая вакцина А+С (лиофилизат для приготовления суспензии для внутримышечного и подкожного введения, 0.5 мл/доза) основано на официальной инструкции, утверждено компанией-производителем в 1998 году
Дата согласования: 31.07.1998
Содержание
- Действующее вещество
- ATX
- Фармакологическая группа
- Нозологическая классификация (МКБ-10)
- Состав и форма выпускa
- Фармакологическое действие
- Характеристика
- Фармакологическое действие
- Фармакодинамика
- Показания
- Противопоказания
- Применение при беременности и кормлении грудью
- Способ применения и дозы
- Побочные действия
- Меры предосторожности
- Особые указания
- Условия хранения
- Срок годности
- Отзывы
Действующее вещество
Вакцина для профилактики менингококковых инфекций (Vaccine meningococcae)
ATX
J07AH01 Менингококка A антиген полисахаридный очищенный
Фармакологическая группа
Вакцины, сыворотки, фаги и анатоксины
Нозологическая классификация (МКБ-10)
Список кодов МКБ-10
Состав и форма выпускa
1 доза лиофилизированного порошка для приготовления инъекционного раствора полисахаридной вакцины для профилактики менингококковой инфекции серогрупп А и С содержит очищенных лиофилизированных полисахаридов Neisseria meningitidis серогрупп А и С по 50 мкг, лактозы q. s. для лиофилизации; во флаконах по 1 дозе в комплекте с растворителем в шприце по 0,5 мл или во флаконах по 10, 20 и 50 доз в комплекте с растворителем во флаконах по 5, 10 и 25 мл соответственно, в картонной коробке 1 комплект (1, 20 и 50 доз) или 10 комплектов (10 доз). Растворитель содержит натрия хлорида 4,15 мг, двухосновного натрия фосфата 0,065 мг, одноосновного натрия фосфата 0,023 мг, воды для инъекций q.s. до 0,5 мл.
s. для лиофилизации; во флаконах по 1 дозе в комплекте с растворителем в шприце по 0,5 мл или во флаконах по 10, 20 и 50 доз в комплекте с растворителем во флаконах по 5, 10 и 25 мл соответственно, в картонной коробке 1 комплект (1, 20 и 50 доз) или 10 комплектов (10 доз). Растворитель содержит натрия хлорида 4,15 мг, двухосновного натрия фосфата 0,065 мг, одноосновного натрия фосфата 0,023 мг, воды для инъекций q.s. до 0,5 мл.
Фармакологическое действие
Фармакологическое действие —
иммуностимулирующее.
Формирует активный специфический иммунитет к менингококкам (Neisseria meningitidis) серогрупп А и C.
Характеристика
Полисахаридная вакцина для профилактики менингококковой инфекции серогрупп А и C.
Формирует активный специфический иммунитет к менингококкам (Neisseria meningitidis) серогрупп А и C.
Фармакодинамика
Вакцина индуцирует иммунитет (сохраняется в течение 3 лет после вакцинации) только против менингита, вызываемого менингококками серогрупп А и С; не обеспечивает защиты от гнойных менингитов иной этиологии: менингококков группы B, Haemophilus influenzae, Streptococcus pneumoniae и др.
Показания
Профилактика цереброспинального менингита менингококковой этиологии серогрупп А и С (в эндемичных районах или в случае эпидемии).
Противопоказания
Гиперчувствительность, острые инфекционные заболевания, прогрессирующие заболевания (острые или хронические). Детский возраст (до 18 мес) во внеэпидемический период.
Применение при беременности и кормлении грудью
Вакцинация в период беременности и лактации может проводиться в случае высокого риска инфицирования (безвредность вакцинопрофилактики менингококковой инфекции серогрупп А и С у беременных женщин не установлена).
Способ применения и дозы
П/к или в/м, однократная инъекция взрослым или детям, начиная с 18-месячного возраста. Перед употреблением лиофилизат вакцины растворяют с помощью входящего в комплект растворителя.
Побочные действия
В течение первых 3 дней после вакцинации иногда (чаще у детей, чем у взрослых) появляется незначительное покраснение в месте инъекции, гипертермия (быстро проходящая после приема антипиретиков), раздражительность, слабость.
Меры предосторожности
Вакцинация грудных детей старше 3 мес возможна в случае их контакта с лицами, инфицированными менингококком. Всю разведенную вакцину немедленно используют; шприц (упаковочный) после использования уничтожают.
Особые указания
При проведении массовой вакцинации возможно использование безыгольных инжекторов.
Условия хранения
При температуре 2–8 °C (в холодильнике).
Хранить в недоступном для детей месте.
Срок годности
3 года.
Не применять по истечении срока годности, указанного на упаковке.
Менактра Вакцина менингококковая, раствор для внутримышечного введения, 0.5 мл, 1 шт.
Вакцинации подлежат дети достигшие 9-месячного возраста.
Дети в возрасте от 9 до 18 мес.
Большая часть зарегистрированных местных и общих реакций, наблюдавшихся в течение 7 дней после вакцинации, были легкими и продолжались менее 3 сут.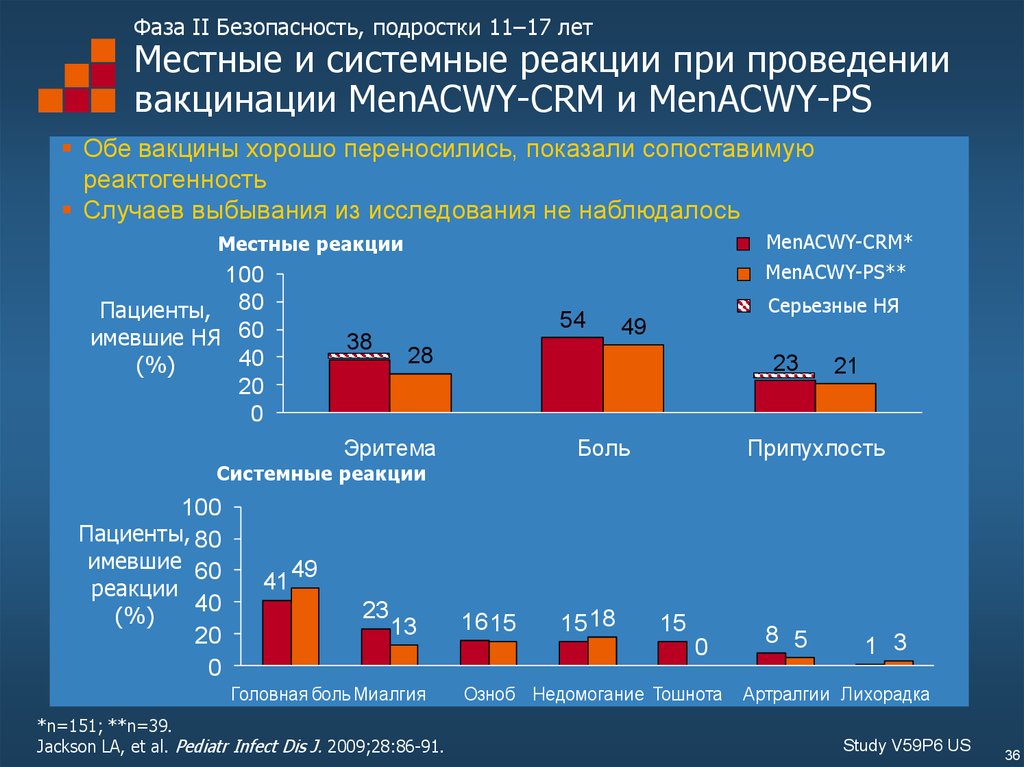 Кроме этого, отмечены следующие побочные эффекты:
Кроме этого, отмечены следующие побочные эффекты:
- Со стороны нервной системы: очень часто — сонливость;
- Со стороны пищеварительной системы: очень часто — потеря аппетита; очень часто или часто — рвота.
- Общие расстройства и нарушения в месте введения: очень часто — болезненность, эритема в месте инъекции, отек в месте инъекции, раздражительность, аномальный плач, лихорадка.
Дети в возрасте от 2 до 10 лет
Большая часть зарегистрированных местных и общих реакций, наблюдавшихся в течение 7 дней после вакцинации, были легкими. Кроме этого, отмечены следующие нарушения:
- Со стороны нервной системы: очень часто или часто — сонливость.
- Со стороны пищеварительной системы: очень часто или часто — снижение аппетита; очень часто — диарея; часто — рвота.
- Со стороны кожи и подкожных тканей: часто — сыпь, крапивница.
- Со стороны костно-мышечной системы: часто — артралгия.
- Общие расстройства и нарушения в месте введения: очень часто — болезненность и уплотнение в месте инъекции; очень часто или часто — раздражительность, покраснение в месте инъекции, отек в месте инъекции, лихорадка.

Лица в возрасте 11-55 лет
Большая часть зарегистрированных местных и общих реакций, наблюдавшихся в течение 7 дней после вакцинации, были легкими. Кроме этого, отмечены следующие нарушения:
- Со стороны нервной системы: очень часто — головная боль.
- Со стороны пищеварительной системы: очень часто или часто — снижение аппетита, диарея; часто — рвота.
- Со стороны кожи и подкожных тканей: часто — сыпь.
- Со стороны костно-мышечной системы: очень часто — артралгия.
- Общие расстройства и нарушения в месте введения: очень часто — боль, уплотнение, покраснение и отек в месте инъекции, повышенная утомляемость, общее недомогание; часто — озноб, лихорадка.В постмаркетинговый период дополнительно получена информация о следующих нежелательных явлениях после введения препарата (в настоящее время частота развития данных явлений и их причинно-следственная связь с применением вакцины Менактра не может быть определена):
- Со стороны иммунной системы: реакции гиперчувствительности, такие как анафилактический шок, анафилактоидные реакции, стридорозное дыхание, затруднение при дыхании, отек верхних дыхательных путей, крапивница, покраснение кожи, кожный зуд, снижение АД.

- Со стороны нервной системы: синдром Гийена-Барре (СГБ), парестезии, потеря сознания (обусловленная нарушениями регуляции со стороны вегетативной нервной системы), головокружение, судороги, паралич лицевого нерва, острый рассеянный энцефаломиелит, поперечный миелит.
- Со стороны костно-мышечной системы: миалгия.
Постмаркетинговое исследование
Риск СГБ после введения вакцины Менактра оценивался в рамках проводившегося в США ретроспективного когортного исследования, в котором использовалась электронная база данных медицинского обслуживания 9 578 688 пациентов в возрасте 11-18 лет, из которых 1 431 906 (15%) получили вакцину Менактра. Ни один из пациентов, описанных в 72 сообщениях о медицински подтвержденных случаях СГБ, не получил вакцину Менактра в течение 42 дней до начала развития симптомов. Еще 129 потенциальных случаев СГБ не были медицински подтверждены или были исключены из анализа вследствие отсутствия или недостаточности медицинской информации. В рамках анализа, учитывавшего отсутствовавшие данные, оцененный дополнительный риск СГБ варьировал от 0 до 5 дополнительных случаев СГБ на 1 000 000 привитых в течение 6 недель после вакцинации.
В рамках анализа, учитывавшего отсутствовавшие данные, оцененный дополнительный риск СГБ варьировал от 0 до 5 дополнительных случаев СГБ на 1 000 000 привитых в течение 6 недель после вакцинации.
Исследования на животных не выявили отрицательного действия вакцины Менактра на течение беременности и фето-эмбрионального развития плода, процесс родов и постнатальное развитие. В связи с тем, что исследований вакцины у беременных женщин не проводилось, а постмаркетинговый опыт ее применения ограничен, введение вакцины беременным женщинам рекомендуется только в случае крайней необходимости, как например, во время вспышки менингококковой инфекции, перед поездкой в эндемичный район, и только после оценки соотношения пользы и риска вакцинации.
В настоящее время неизвестно, способны ли активные вещества, входящие в состав вакцины, проникать в грудное молоко. Однако ранее было показано, что антитела к полисахаридам обнаруживаются у молодых мышей, находившихся на грудном вскармливании.
В исследованиях на мышах не было продемонстрировано неблагоприятного влияния на постнатальное развитие потомства, получавшего материнские антитела с молоком и выработка которых была индуцирована введением вакцины Менактра. В то же время, эффекты у детей первого года жизни, матери которых были иммунизированы вакциной Менактра в период грудного вскармливания, не исследовались. Перед принятием решения об иммунизации кормящей женщины, необходимо оценить риски и пользу данной иммунизации.
В то же время, эффекты у детей первого года жизни, матери которых были иммунизированы вакциной Менактра в период грудного вскармливания, не исследовались. Перед принятием решения об иммунизации кормящей женщины, необходимо оценить риски и пользу данной иммунизации.
Обзор менингококковых вакцин с обновленной информацией об иммунизации взрослых
Обзор
. 2014;10(4):995-1007.
doi: 10.4161/hv.27739.
Epub 2014 5 февраля.
Йорго С Захлание
1
, Моза М Хаммади
1
, Соха Т Ганем
2
, Гассан С. Дбайбо
1
Принадлежности
- 1 Центр исследований инфекционных заболеваний; Отделение детских инфекционных заболеваний; отделение педиатрии и подростковой медицины; Медицинский центр Американского университета Бейрута; Бейрут, Ливан.

- 2 Педиатрическое отделение; больница общего профиля Макассед; Бейрут, Ливан.
PMID:
24500529
PMCID:
PMC4896590
DOI:
10.4161/хв.27739
Бесплатная статья ЧВК
Обзор
Yorgo C Zahlanie et al.
Hum Вакцина Иммунотер.
2014.
Бесплатная статья ЧВК
. 2014;10(4):995-1007.
doi: 10. 4161/hv.27739.
4161/hv.27739.
Epub 2014 5 февраля.
Авторы
Йорго С Захлание
1
, Моза М Хаммади
1
, Соха Т Ганем
2
, Гассан С. Дбайбо
1
Принадлежности
- 1 Центр исследований инфекционных заболеваний; Отделение детских инфекционных заболеваний; отделение педиатрии и подростковой медицины; Медицинский центр Американского университета Бейрута; Бейрут, Ливан.
- 2 Педиатрическое отделение; больница общего профиля Макассед; Бейрут, Ливан.
PMID:
24500529
PMCID:
PMC4896590
DOI:
10.
 4161/хв.27739
4161/хв.27739
Абстрактный
Менингококковая инфекция представляет собой серьезное и глобально угрожающее жизни заболевание. На шесть серогрупп (A, B, C, W-135, X и Y) приходится большая часть менингококковой инфекции во всем мире. Менингококковые полисахаридные вакцины были внедрены несколько десятилетий назад и привели к снижению бремени болезни. Однако полисахаридные вакцины имеют ряд ограничений, включая низкую иммуногенность у младенцев и детей ясельного возраста, кратковременную защиту, отсутствие иммунологической памяти, незначительное влияние на носоглоточное носительство и наличие гипореактивности после повторных доз. Химическая конъюгация простых полисахаридных вакцин может устранить эти недостатки. Менингококковые конъюгированные вакцины включают четырехвалентные вакцины (MenACWY-DT, MenACWY-CRM и MenACWY-TT), а также моновалентные вакцины А и С. Было показано, что эти конъюгированные вакцины вызывают сильный иммунный ответ у взрослых. В этом обзоре рассматриваются различные аспекты менингококковой инфекции, ограничения, связанные с полисахаридными вакцинами, различные конъюгированные вакцины с учетом их иммуногенности и реактогенности у взрослых, а также текущие рекомендации для взрослых.
В этом обзоре рассматриваются различные аспекты менингококковой инфекции, ограничения, связанные с полисахаридными вакцинами, различные конъюгированные вакцины с учетом их иммуногенности и реактогенности у взрослых, а также текущие рекомендации для взрослых.
Ключевые слова:
менингококковая энцефалопатия; взрослые люди; менингококковая конъюгированная вакцина; менингококковая инфекция; менингококковая полисахаридная вакцина; рекомендации.
Похожие статьи
Вакцина MenACWY-TT для активной иммунизации против инвазивной менингококковой инфекции.
Папаевангелоу В., Спиридис Н.
Папаевангелоу В. и др.
Эксперт Rev Вакцины. 2012 май; 11(5):523-37. doi: 10.1586/erv.12.32.
Эксперт Rev Вакцины. 2012.PMID: 22827239Обзор.
Профилактика и борьба с менингококковой инфекцией: рекомендации Консультативного комитета по практике иммунизации (ACIP).

Кон А.С., Макнейл Дж.Р., Кларк Т.А., Ортега-Санчес И.Р., Бриер Э.З., Мейснер Х.К., Бейкер С.Дж., Мессонье Н.Е.; Центры по контролю и профилактике заболеваний (CDC).
Кон А.С. и соавт.
MMWR Recomm Rep. 2013 Mar 22;62(RR-2):1-28.
MMWR Recomm Rep. 2013.PMID: 23515099
Иммуногенность и иммунная память неадъювантной четырехвалентной менингококковой гликоконъюгированной вакцины у детей раннего возраста.
Perrett KP, Snape MD, Ford KJ, John TM, Yu LM, Langley JM, McNeil S, Dull PM, Ceddia F, Anemona A, Halperin SA, Dobson S, Pollard AJ.
Перретт К.П. и др.
Pediatr Infect Dis J. 2009 Mar; 28(3):186-93. doi: 10.1097/INF.0b013e31818e037d.
Pediatr Infect Dis J. 2009.PMID: 19209097
Клиническое испытание.
Безопасность и иммуногенность бустерной дозы менингококковой (группы A, C, W и Y) полисахаридной конъюгированной вакцины против дифтерийного анатоксина.

Робертсон К.А., Гринберг Д.П., Хедрик Дж., Пичичеро М., Декер М.Д., Сондерс М.
Робертсон, Калифорния, и соавт.
вакцина. 2016 17 октября; 34 (44): 5273-5278. doi: 10.1016/j.vaccine.2016.09.003. Epub 2016 15 сентября.
вакцина. 2016.PMID: 27642132
Клиническое испытание.
Обновление клинического опыта применения четырехвалентной менингококковой конъюгированной вакцины ACWY-CRM.
Кешаван П., Пеллегрини М., Вадивелу-Печай К., Ниссен М.
Кешаван П. и др.
Эксперт Rev Вакцины. 2018 Октябрь; 17 (10): 865-880. дои: 10.1080/14760584.2018.1521280. Epub 2018 27 сентября.
Эксперт Rev Вакцины. 2018.PMID: 30198805
Обзор.
Посмотреть все похожие статьи
Цитируется
Вакцины для предотвращения менингита: исторические перспективы и будущие направления.

Олдерсон М.Р., Уэлш Дж.А., Риган К., Ньюхаус Л., Бхат Н., Марфин А.А.
Олдерсон М.Р. и соавт.
Микроорганизмы. 2021 7 апреля; 9 (4): 771. doi: 10.3390/microorganisms9040771.
Микроорганизмы. 2021.PMID: 33917003
Бесплатная статья ЧВК.Обзор.
Иммуногенность и безопасность четырехвалентной конъюгированной вакцины против менингококкового анатоксина столбняка (MenACYW-TT) у взрослых в возрасте 56 лет и старше: рандомизированное исследование фазы II.
Кирстейн Дж., Пина М., Пан Дж., Джорданов Э., Дингра М.С.
Кирстейн Дж. и соавт.
Hum Вакцина Иммунотер. 2020 2 июня; 16 (6): 1299-1305. дои: 10.1080/21645515.2020.1733868. Epub 2020 1 апр.
Hum Вакцина Иммунотер. 2020.PMID: 32233961
Бесплатная статья ЧВК.Клиническое испытание.
Перекрестная реактивность с бразильскими штаммами Neisseria meningitidis B после иммунизации везикулами наружной мембраны.

Trzewikoswki de Lima G, Portilho AI, De Gaspari E.
Trzewikoswki de Lima G, et al.
Вакцины The Adv Immunother. 2019 11 декабря; 7:2515135519894825. дои: 10.1177/2515135519894825. Электронная коллекция 2019.
Вакцины The Adv Immunother. 2019.PMID: 31853514
Бесплатная статья ЧВК.Вакцинный антиген NHBA серогруппы B Bexsero Neisseria meningitidis представляет собой высокоаффинный белок, связывающий хондроитинсульфат.
Мубайва Т.Д., Хартли-Тассел Л.Е., Семченко Э.А., Дэй С.Дж., Дженнингс М.П., Сейб К.Л.
Мубайва Т.Д. и соавт.
Научный представитель 2018 г. 25 апреля; 8 (1): 6512. doi: 10.1038/s41598-018-24639-x.
Научный представитель 2018.PMID: 29695781
Бесплатная статья ЧВК.Прогресс на пути к глобальной борьбе с Neisseria meningitidis: вакцины 21 века, текущие рекомендации и проблемы для будущей разработки вакцин.

Дретлер А.В., Руфаэль Н.Г., Стивенс Д.С.
Дретлер А.В. и др.
Hum Вакцина Иммунотер. 2018 4 мая; 14 (5): 1146-1160. дои: 10.1080/21645515.2018.1451810. Эпаб 2018 9 мая.
Hum Вакцина Иммунотер. 2018.PMID: 29543582
Бесплатная статья ЧВК.Обзор.
Просмотреть все статьи «Цитируется по»
Типы публикаций
термины MeSH
вещества
По каким причинам не делать прививку от менингита?
Наличие вакцины против менингита безопасно и сопряжено с минимальными побочными эффектами или рисками. Однако могут быть ситуации, когда человеку не следует делать прививку или откладывать вакцинацию.
Вакцина против менингита защищает человека от инфекций, которые могут вызвать опасные для жизни заболевания или постоянную инвалидность.
По данным Национальной ассоциации менингита (NMA), около 600–1000 человек в Соединенных Штатах ежегодно заболевают менингококковой инфекцией, разновидностью бактериального менингита, и 10–15% этих людей умирают в результате.
По данным NMA, количество людей с менингококковой инфекцией значительно сократилось за последние годы, потому что больше людей получили вакцины против менингита. Несмотря на это, каждый пятый подросток в США остается незащищенным.
В этой статье рассказывается о вакцине против менингита, для кого она предназначена, а также о ее рисках и возможных побочных эффектах.
Узнайте больше о вакцине против менингита здесь.
Менингококковая вакцина, также называемая вакциной против менингита, защищает от Бактерии Neisseria meningitides . Эта бактерия имеет шесть типов: A, B, C, W, X и Y. Другое название этих подгрупп — серогруппы.
Когда бактерии проникают в организм, они могут поражать кровоток и вызывать сепсис. Он также может поражать мозговые оболочки, ткани, окружающие головной и спинной мозг, вызывая менингит.
Менингококковый менингит — это тяжелое и опасное для жизни состояние, которое может привести к смерти в течение нескольких часов. Другие типы менингита могут по-прежнему вызывать неблагоприятные последствия для здоровья, но могут быть менее серьезными.
По данным Всемирной организации здравоохранения (ВОЗ), примерно 1 из 10 человек с бактериальным менингитом умирает, а у 1 из 5 человек возникают долговременные осложнения, включая потерю слуха и умственную отсталость.
В США доступны два типа вакцин против менингита: менингококковая конъюгатная (MenACWY) и менингококковая В (MenB). Первая вакцина защищает от менингококковых бактерий типов A, C, W и Y. Вторая защищает от менингококковых бактерий типа B.
Обе прививки эффективно защищают людей от различных штаммов бактерий, вызывающих менингит.
Хотя любой человек может заразиться менингококковой инфекцией, Центры по контролю и профилактике заболеваний (CDC) указывают, что дети в возрасте до 1 года и люди в возрасте 16–23 лет наиболее подвержены заражению.
Узнайте о последствиях менингита здесь.
Как и любое лекарство, вакцина против менингита может вызывать побочные эффекты. Тем не менее, они, как правило, легкие и обычно проходят в течение нескольких дней.
Mild side effects include:
- redness or soreness at the site of injection
- muscle pain
- tiredness
- headache
- muscle or joint pain
- nausea
- diarrhea
- fever or chills
Although some люди могут испытывать боль в месте инъекции или даже потерять сознание после вакцинации, серьезные побочные эффекты, такие как тяжелые аллергические реакции, серьезные травмы или смерть, возникают крайне редко.
Хотя есть сообщения о том, что вакцина может вызвать синдром Гийена-Барре (СГБ), два обширных исследования показали, что это было совпадением и что нет никакой связи между менингококковой конъюгированной вакциной и СГБ.
Узнайте больше о распространенных побочных эффектах прививок здесь.
Согласно CDC, людям с определенными заболеваниями не следует делать определенные прививки или ждать, пока их врач не сообщит им, что это безопасно. К ним относятся те, кто:
- имели опасную для жизни реакцию на предыдущую дозу вакцины против менингита
- имели сильную аллергию на какой-либо ингредиент вакцины
- имели среднетяжелое или тяжелое заболевание
- беременны или кормили грудью
Люди с легкими заболеваниями, такими как простуда, можно сделать прививку. Точно так же беременные или кормящие грудью люди с повышенным риском заражения менингококковой инфекцией могут получить эти вакцины.
Узнайте о возможных долгосрочных последствиях менингита здесь.
CDC рекомендует делать прививку от менингита. Руководящие принципы предполагают, что все дети получают вакцину MenACWY в возрасте 11–12 лет, а ревакцинацию — в 16 лет. Предпочтительный возраст для введения вакцины MenB — 16–18 лет, но люди до 23 лет также могут получить пользу от вакцинации.
Тем не менее, все лица с повышенным риском заражения менингококковой инфекцией должны пройти вакцинацию. К ним относятся люди, которые:
- имеют дефицит компонента комплемента, редкое иммунное заболевание
- принимают ингибиторы комплемента, такие как Ultomiris
- имеют поврежденную или удаленную селезенку
- имеют серповидноклеточную анемию
- имеют ВИЧ
- живут в районе с высоким бременем болезни, например, в странах Африки к югу от Сахары
- поедет в страны, где это заболевание распространено или имеет место вспышка менингококковой инфекции
Узнайте больше о менингите здесь.
Младенцы и дети
Младенцы в возрасте 2 месяцев могут быть вакцинированы, если они подвержены риску заражения. В частности, они могут получить вакцину MenACWY в возрасте от 2 месяцев до 10 лет и вакцину MenB для детей от 10 лет и старше.
Родители и лица, осуществляющие уход за младенцами и детьми, могут поговорить со своими врачами, чтобы обсудить, когда и целесообразна ли вакцинация.
Узнайте больше о менингите у новорожденных здесь.
Подростки и подростки
Эксперты в области здравоохранения рекомендуют вакцину MenACWY для детей в возрасте от 11 до 12 лет, ревакцинацию, когда им исполняется 16 лет, и подростков в возрасте от 11 до 18 лет, если они не вакцинированы.
Узнайте больше о менингите у детей здесь.
Взрослые
Помимо причин, упомянутых выше, некоторые состояния повышают риск заражения взрослых менингококковой инфекцией. К ним относятся:
- микробиолог, контактировавший с бактериями
- не прошедшие вакцинацию
- первокурсник колледжа, который будет жить в общежитии
- новобранец
Узнайте больше о менингите у взрослых здесь.
Человек может получить вакцину в местных медицинских центрах, аптеках, общественных клиниках, частных клиниках, департаментах здравоохранения и общественных местах, таких как школы и религиозные центры.
В соответствии с положениями Закона о доступном медицинском обслуживании планы Health Insurance Marketplace и большинство частных страховых планов покрывают менингококковую вакцину, а также некоторые другие вакцины.


 4161/хв.27739
4161/хв.27739