Содержание
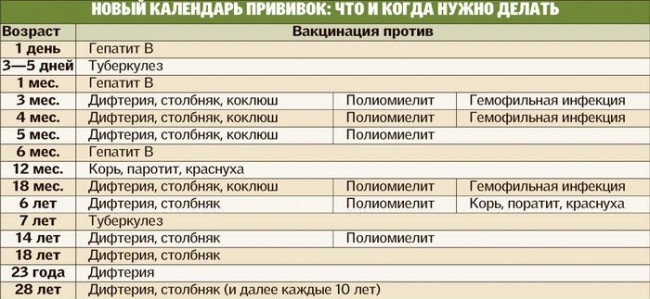
Вакцина Пентаксим — показания, противопоказания, преимущества
Вакцинация против гемофильной палочки рекомендована до 5 лет. В более старшем возрасте прививаться против данной инфекции нецелесообразно
Статью подготовила заведующая детской клиникой, педиатр Юлия Александровна Ермолаева
Каковы отличия пентаксима от других аналогичных вакцин?
Пентаксим – многокомпонентная вакцина. Вакцина Пентаксим предназначена для иммунизации против коклюша, дифтерии, столбняка, полиомиелита, гемофильной палочки. За одну инъекцию одномоментно вводится вакцина сразу против 5 инфекций. В упаковке данного препарата находится шприц с готовой вакциной АКДС и флакон с лиофилизатом против гемофильной палочки типа b. Таким образом, при желании можно ставить отдельно АКДС без гемофильной палочки.
Пентаксим, так же, как и Инфанрикс, вызывает меньше побочных и нежелательных явления в сравнении с отечественной АКДС-вакциной. Объяснением тому является содержание бесклеточного коклюшного компонента, отсутствие консерванта – мертиолята в вакцинах импортного производства. В АКДС-вакцине содержатся цельные коклюшные микробные клетки, вызывающие сильнейшую иммунную реакцию, проявляющуюся в виде повышения температуры, местных и общих аллергических проявлениях и др.
В АКДС-вакцине содержатся цельные коклюшные микробные клетки, вызывающие сильнейшую иммунную реакцию, проявляющуюся в виде повышения температуры, местных и общих аллергических проявлениях и др.
Но наличие меньшей реактогенности ацеллюлярных вакцин сопровождается менее эффективным и непродолжительно сформированным иммунитетом в сопоставлении с клеточными вакцинами (результаты крупномасштабных исследований).
Вакцина Пентаксим в своем составе содержит инактивированный вирус полиомиелита, что является обязательным условием первых вакцинаций против полиомиелитной инфекции. Начало вакцинации с живой полиомиелитной вакцины в виде капель влечет за собой риск развития вакцино-ассоциируемого полиомиелита в 1-4% случаев.
Сроки вакцинации
Вакцинация Пентаксим проводится в следующие сроки: в 3 месяца, 4,5 месяцев, 6 месяцев. Первая ревакцинация проводится через 12 месяцев после введения третьей дозы. В случае нарушения графика вакцинации интервалы между введениями сохраняются: для вакцинации 45 дней, ревакцинация также проводится через 12 мес.
До какого возраста нужно прививать против гемофильной инфекции?
Вакцинация против гемофильной палочки рекомендована до 5 лет. В более старшем возрасте прививаться против данной инфекции нецелесообразно, даже при отсутствии лабораторно подтвержденных заболеваний этой этиологии. К 6 годам у ребенка формируется естественный иммунитет ребенка на гемофильную палочку в ходе постоянной встречи с этим микробом в окружающей среде.
Можно ли проводить курс вакцинации против коклюша, дифтерии столбняка разными вакцинами?
Да. Все вакцины взаимозаменяемы.
Какую вакцину лучше выбрать для постановки?
Для формирования достаточного иммунитета и снижения количества местных прививочных реакций схема вакцинации должна включать, как цельноклеточные, так и бесклеточные вакцины. Для лучшей переносимости и формирования стойкого иммунитета наши педиатрыа рекомендуют в качестве первой вакцинации использовать АКДС-вакцину российского производства, являющейся цельноклеточной, а дальнейшие вакцинации проводить менее реактогенными вакцинами – бесклеточными (Инфанрикс, Пентаксим).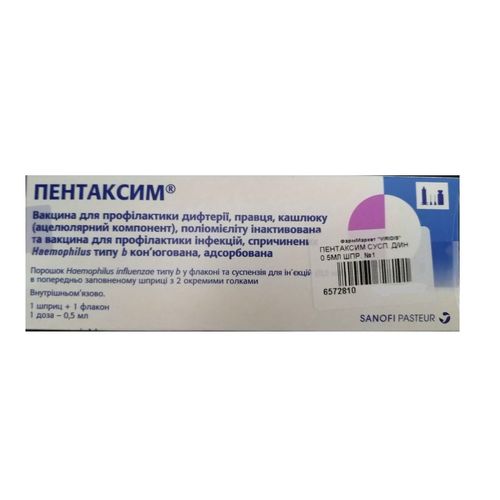
Противопоказания для постановки Пентаксима
- Прогрессирующая энцефалопатия, сопровождающаяся судорогами или без таковых.
- Энцефалопатия неясной этиологии, развившаяся в течение 7 дней после введения любой вакцины (цельноклеточной или ацеллюлярной), содержащей антигены Bordetella pertussis.
- Сильная реакция, развившаяся в течение 48 ч после предыдущей иммунизации вакциной, содержащей коклюшный компонент: температура тела равная или превышающая 40 °С, синдром длительного необычного плача (дольше 3 ч), фебрильные и афебрильные судороги, гипотонический-гипореактивный синдром.
- Гиперчувствительность на предыдущее введение дифтерийной, столбнячной, коклюшной вакцин, вакцин против полиомиелита или инфекции, вызываемой Haemophilus influenzae (гемофильная палочка) тип b.
- Установленная гиперчувствительность к любому компоненту вакцины, а также глютаральдегиду, неомицину, стрептомицину и полимиксину В.
- Заболевание, сопровождающиеся повышением температуры тела, острое инфекционное или хроническое заболевание в стадии обострения.
 Вакцинацию проводят через 2-4 недели после выздоровления или в период реконвалесценции или ремиссии.
Вакцинацию проводят через 2-4 недели после выздоровления или в период реконвалесценции или ремиссии. - При нетяжелых ОРВИ, острых кишечных заболеваниях и т.д. прививки проводят сразу после нормализации температуры.
Какие побочные эффекты после введения Пентаксима?
Побочные явления на введения Пентаксима бывают в виде местных и системных реакций.
Местные реакции проявляются как покраснение, отек, болезненность в месте постановки вакцины. Системная реакция характеризуется повышением температуры, раздражительностью, нарушением сна, беспокойством, плачем, потерей аппетита, рвотой, диареей, легкими проявлениями ОРЗ.
Осложнения после вакцинации Пентаксим
- Анафилактический шок является крайне редким осложнением. Возникает чаще после повторного введения вакцины в течение первых нескольких минут, реже – через 3-4 часа.
- Афебрильные судороги – судороги на фоне нормальной температуры тела с потерей сознания.
 Очень часто афебрильные судороги являются первым проявлением эпилепсии. Определить принадлежность судорог к эпилепсии или поствакцинальному осложнению не представляется возможным, поэтому при предшествующей вакцинации судорожный синдром расценивается как осложнение.
Очень часто афебрильные судороги являются первым проявлением эпилепсии. Определить принадлежность судорог к эпилепсии или поствакцинальному осложнению не представляется возможным, поэтому при предшествующей вакцинации судорожный синдром расценивается как осложнение.
Вакцинация против дифтерии, столбняка, коклюша
Вакцинопрофилактика инфекционных заболеваний осуществляется в соответствии с Национальным календарем профилактических прививок, установленным Постановлением Министерства здравоохранения Республики Беларусь от 18 июля 2012 г. № 106 (далее – Национальный календарь). Согласно Национальному календарю детям с 3 месяцев проводятся профилактические прививки против дифтерии, столбняка и коклюша. В учреждениях здравоохранения Республики Беларусь для иммунизации против дифтерии, столбняка, коклюша имеется АКДС-вакцина.
АКДС (Россия) является адсорбированной коклюшно-дифтерийно-столбнячной вакциной для профилактики коклюша, дифтерии и столбняка у детей от 3-х месяцев до 3 лет 11 месяцев 29 дней.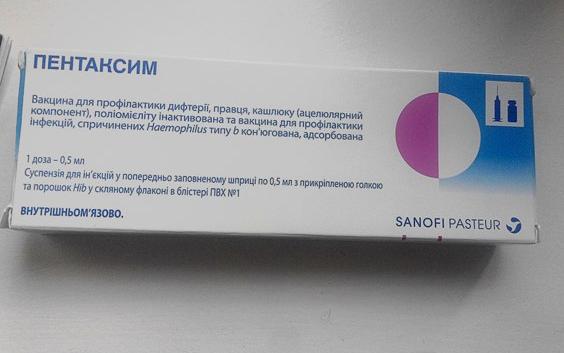 В своем составе вакцина АКДС содержит дифтерийный и столбнячный анатоксины, и инактивированный (корпускулярный) возбудитель коклюша (Bordetella pertussis).
В своем составе вакцина АКДС содержит дифтерийный и столбнячный анатоксины, и инактивированный (корпускулярный) возбудитель коклюша (Bordetella pertussis).
Показания к применению. Первичная вакцинация против дифтерии, столбняка и коклюша у детей с 3 месяцев до 3 лет 11 месяцев 29 дней. Курс первичной иммунизации вакциной АКДС состоит из 3 доз вакцины, вводимых согласно Национальному календарю профилактических прививок РБ в 3, 4 и 5 месяцев жизни; ревакцинацию проводят в 18 месяцев.
Способ применения. Способ применения вакцины АКДС — вводится внутримышечно. У детей обычно в четырехглавую мышцу бедра (средняя треть бедра), а у более старших детей в дельтовидную мышцу (плечо). Инъекция в ягодицу в настоящее время не практикуется. Допустимо подкожное введение. Внутривенное введение категорически противопоказано.
Применение препарата АКДС совместно с другими вакцинами. Вакцину АКДС можно вводить одновременно со всеми препаратами из национального календаря профилактических прививок в один день, в разные участки тела, за исключением вакцины БЦЖ. Применение вакцины АКДС совместно с другими прививками не влияет на их иммуногенность (способность выработки иммунитета). Переносимость вакцин не ухудшается, количество побочных реакций не возрастает. АКДС можно применять для завершения курса вакцинации, начатого другими вакцинами против коклюша, дифтерии и столбняка, равно как и для ревакцинации при необходимости. Все вакцины национального календаря прививок РБ взаимозаменяемы.
Применение вакцины АКДС совместно с другими прививками не влияет на их иммуногенность (способность выработки иммунитета). Переносимость вакцин не ухудшается, количество побочных реакций не возрастает. АКДС можно применять для завершения курса вакцинации, начатого другими вакцинами против коклюша, дифтерии и столбняка, равно как и для ревакцинации при необходимости. Все вакцины национального календаря прививок РБ взаимозаменяемы.
Возможные побочные реакции. У части привитых в первые двое суток могут развиваться кратковременные общие (повышение температуры, недомогание) и местные (болезненность, гиперемия, отечность) реакции. В редких случаях могут развиться осложнения: судороги (обычно связанные с повышением температуры, эпизоды пронзительного крика, аллергические реакции, крапивница, полиморфная сыпь, отек Квинке). Учитывая возможность развития аллергических реакций немедленного типа у особо чувствительных детей, за привитыми необходимо обеспечить медицинское наблюдение в течение 30 минут.
Противопоказания к применению. Противопоказаниями к вакцинации являются прогрессирующие заболевания нервной системы, афебрильные судороги в анамнезе, развитие на предшествующее введение АКДС-вакцины сильной реакции (повышение температуры выше 40°С, в месте введения вакцины — отек и гиперемия свыше 8 см в диаметре). Стабильные проявления аллергического заболевания (локализованные кожные проявления, скрытый бронхоспазм и т.п.) не являются противопоказанием к вакцинации, которая может быть проведена на фоне соответствующей терапии. Детей, родившихся с весом менее 2 кг, прививают при нормальном физическом и психомоторном развитии; отставание в весе не является основанием к отсрочке вакцинации.
Дополнительные сведения. Детей, перенесших острые заболевания, прививают не ранее, чем через 4 недели после выздоровления; при легких формах респираторных заболеваний (ринит, легкая гиперемия зева и т.д.) прививка допускается через 2 недели после выздоровления. Больных хроническими заболеваниями прививают по достижении стойкой ремиссии (не менее 4 недель).
Больных хроническими заболеваниями прививают по достижении стойкой ремиссии (не менее 4 недель).
Синдром острой ВИЧ-инфекции, имитирующий побочные эффекты вакцинации против COVID-19: клинический случай | Исследования и лечение СПИДа
- Отчет о болезни
- Открытый доступ
- Опубликовано:
- Юлиан Трибельхорн 1 ,
- Стефани Хашка 1 ,
- Феликс Гессе 1 ,
- Йоханна Эрбер 1 ,
- Simon Weidlich 1 ,
- Marcel Lee 1 ,
- Dieter Hoffmann 2 ,
- Josef Eberle 3 &
- …
- Christoph D.
 Spinner 1
Spinner 1
Исследования и лечение СПИДа
том 18 , Номер статьи: 78 (2021)
Процитировать эту статью
32 тыс. обращений
756 Альтметрический
Сведения о показателях
Abstract
Исходная информация
Симптомы первичной ВИЧ-инфекции, включая лихорадку, сыпь и головную боль, неспецифичны и часто описываются как гриппоподобные. COVID-19Побочные эффекты вакцинации, такие как лихорадка, которая возникает у 10% людей после вакцинации против COVID-19, могут еще более затруднить диагностику острой ВИЧ-инфекции.
Описание случая
26-летний мужчина поступил с лихорадкой и головной болью после вакцинации против COVID-19. Первоначально считалось, что симптомы являются побочными эффектами вакцины. Диагностическое обследование было проведено из-за сохраняющейся лихорадки и головной боли > 72 часов после вакцинации, и у него была диагностирована острая ВИЧ-инфекция II стадии по Фибиху через 3 недели после незащищенного анального полового акта с другим мужчиной.
Заключение
Тщательный анамнез является ключом к оценке индивидуального риска первичной ВИЧ-инфекции у пациентов с гриппоподобными симптомами. Ранняя диагностика и начало антиретровирусной терапии связаны с лучшим прогнозом и ограничивают передачу заболевания.
Исходная информация
Сероконверсия ВИЧ описывает начальный иммунный ответ развития антител, специфичных к вирусу иммунодефицита человека (ВИЧ), которые обычно обнаруживаются через 22–24 дня после заражения (таблица 1). Фибиг и др. [1] разделили процесс сероконверсии ВИЧ на шесть стадий в зависимости от соотношения антитело-антиген и вирусной нагрузки ВИЧ в крови. Эта классификация позволяет точно описать пациентов с первичной ВИЧ-инфекцией. В 89% случаев процесс сероконверсии сопровождается симптомами, известными как сероконверсионная болезнь ВИЧ [2]. Симптомы часто включают недомогание, головную боль, лихорадку, генерализованную лимфаденопатию, диарею и сыпь. В тяжелых случаях у пациентов могут возникать менингеальные симптомы, требующие госпитализации. Общие симптомы сероконверсии ВИЧ неспецифичны и часто описываются как гриппоподобные, что затрудняет различие между сероконверсионной болезнью ВИЧ и широким спектром других состояний, включая побочные эффекты вакцин. Во время COVID-19В период массовой вакцинации в рамках продолжающейся пандемии COVID-19 побочные эффекты вакцины следует учитывать при дифференциальной диагностике при условии, что пациент был недавно вакцинирован. Побочные эффекты вакцины против COVID-19 включают утомляемость, покраснение, лихорадку, артралгию и головную боль и могут напоминать симптомы сероконверсионной болезни ВИЧ, что затрудняет диагностику ВИЧ [3].
Фибиг и др. [1] разделили процесс сероконверсии ВИЧ на шесть стадий в зависимости от соотношения антитело-антиген и вирусной нагрузки ВИЧ в крови. Эта классификация позволяет точно описать пациентов с первичной ВИЧ-инфекцией. В 89% случаев процесс сероконверсии сопровождается симптомами, известными как сероконверсионная болезнь ВИЧ [2]. Симптомы часто включают недомогание, головную боль, лихорадку, генерализованную лимфаденопатию, диарею и сыпь. В тяжелых случаях у пациентов могут возникать менингеальные симптомы, требующие госпитализации. Общие симптомы сероконверсии ВИЧ неспецифичны и часто описываются как гриппоподобные, что затрудняет различие между сероконверсионной болезнью ВИЧ и широким спектром других состояний, включая побочные эффекты вакцин. Во время COVID-19В период массовой вакцинации в рамках продолжающейся пандемии COVID-19 побочные эффекты вакцины следует учитывать при дифференциальной диагностике при условии, что пациент был недавно вакцинирован. Побочные эффекты вакцины против COVID-19 включают утомляемость, покраснение, лихорадку, артралгию и головную боль и могут напоминать симптомы сероконверсионной болезни ВИЧ, что затрудняет диагностику ВИЧ [3].
Таблица 1. Стадии маркеров ВИЧ/диагностических тестов на ранней стадии инфекции, как описано Fiebig et al.
Полноразмерный стол
Мы описываем случай сероконверсионного заболевания ВИЧ, которое первоначально было ошибочно диагностировано как побочный эффект вакцины против COVID-19, чтобы проиллюстрировать сходство между общими побочными эффектами вакцины против COVID-19 и диагностическим процессом, необходимым для дифференциации этих двух состояний.
История болезни
Через день после получения первой дозы вакцины против COVID-19 с мРНК-1273 (Moderna Biotech, Кембридж, Массачусетс, США) у 26-летнего немца развилась лихорадка, озноб и головная боль. В последующие дни у него появились сыпь, головокружение и тошнота, кульминацией которых стал единичный синкопальный эпизод через 8 дней после вакцинации, как показано на рис. 1. Пациента направили в ближайшую местную больницу, так как его симптомы подозревались в связи с вакциноассоциированные побочные эффекты. Ему дали анальгетики и жидкость, и симптомы быстро исчезли. Подробный сбор сексуального анамнеза выявил эпизод незащищенного анального полового акта с другим мужчиной 23 днями ранее. Впоследствии он дал положительный результат на ВИЧ с помощью иммуноферментного анализа, связанного с p24 / ab-ферментом четвертого поколения (ELISA). Пациент был направлен в наш третичный медицинский центр для дальнейшего обследования и начала лечения.
Ему дали анальгетики и жидкость, и симптомы быстро исчезли. Подробный сбор сексуального анамнеза выявил эпизод незащищенного анального полового акта с другим мужчиной 23 днями ранее. Впоследствии он дал положительный результат на ВИЧ с помощью иммуноферментного анализа, связанного с p24 / ab-ферментом четвертого поколения (ELISA). Пациент был направлен в наш третичный медицинский центр для дальнейшего обследования и начала лечения.
Рис. 1
Хронология истории облучения пациента, клинической картины и диагноза. Симптомы и события, описанные в этом клиническом случае, показаны на временной шкале, измеряемой в днях с момента заражения. События обозначены красными полосами, а положительные результаты теста обозначены зелеными полосами. Симптомы и продолжительность персистенции показаны синими столбиками разного оттенка
Увеличенное изображение
При поступлении пациент жаловался на легкую головную боль, общую слабость и сохраняющуюся гиперемию кожи. Биохимический анализ крови показал повышенный уровень С-реактивного белка (СРБ) (2,0 мг/дл; контроль: < 0,5 мг/дл), а гематология показала лимфоцитопению (2,49).Г/л), с количеством Т-клеток CD4 284 клеток/мкл и соотношением CD4/CD8 0,2. Он был повторно протестирован на ВИЧ с использованием скринингового теста (комбинация антигенов/антител к ВИЧ, выполненная в компании Abbott Architect, Чикаго, Иллинойс, США) и иммуноблота на ВИЧ (recomLine HIV-1 и HIV-2 от Mikrogen, Neuried, Германия). Скрининговый тест был реактивным, но ВИЧ-специфический вестерн-блоттинг был отрицательным, и ВИЧ-специфические антитела не были обнаружены. Тестирование полимеразной цепной реакции (ПЦР) на ВИЧ в режиме реального времени (Эбботт, Чикаго, Иллинойс, США) выявило высокую вирусную нагрузку 49≥817 530 копий/мл, что подтверждает диагноз острой ВИЧ-инфекции II стадии по Фибигу, как показано в таблице 1. Коинфекция SARS-CoV-2 была многократно исключена с помощью ПЦР на SARS-CoV-2 (TaqMan™-ПЦР, проведенная на Roche cobas ® 6800, Базель, Швейцария).
Биохимический анализ крови показал повышенный уровень С-реактивного белка (СРБ) (2,0 мг/дл; контроль: < 0,5 мг/дл), а гематология показала лимфоцитопению (2,49).Г/л), с количеством Т-клеток CD4 284 клеток/мкл и соотношением CD4/CD8 0,2. Он был повторно протестирован на ВИЧ с использованием скринингового теста (комбинация антигенов/антител к ВИЧ, выполненная в компании Abbott Architect, Чикаго, Иллинойс, США) и иммуноблота на ВИЧ (recomLine HIV-1 и HIV-2 от Mikrogen, Neuried, Германия). Скрининговый тест был реактивным, но ВИЧ-специфический вестерн-блоттинг был отрицательным, и ВИЧ-специфические антитела не были обнаружены. Тестирование полимеразной цепной реакции (ПЦР) на ВИЧ в режиме реального времени (Эбботт, Чикаго, Иллинойс, США) выявило высокую вирусную нагрузку 49≥817 530 копий/мл, что подтверждает диагноз острой ВИЧ-инфекции II стадии по Фибигу, как показано в таблице 1. Коинфекция SARS-CoV-2 была многократно исключена с помощью ПЦР на SARS-CoV-2 (TaqMan™-ПЦР, проведенная на Roche cobas ® 6800, Базель, Швейцария). Пациент был выписан без каких-либо симптомов, и ему была начата антиретровирусная терапия биктегравиром/эмтрицитабином/тенофовиром алафенамидом.
Пациент был выписан без каких-либо симптомов, и ему была начата антиретровирусная терапия биктегравиром/эмтрицитабином/тенофовиром алафенамидом.
Обсуждение и заключение
Этот клинический случай иллюстрирует, как симптомы острой ВИЧ-инфекции могут быть ошибочно приняты за побочные эффекты COVID-19.вакцинация, особенно в текущий период массовой вакцинации против COVID-19 в условиях продолжающейся пандемии. Учитывая сходство симптомов, включая утомляемость, лихорадку, эритему, головную боль и сонливость, первичную ВИЧ-инфекцию можно легко не заметить, а симптомы острой ВИЧ-инфекции можно ошибочно отнести к побочным эффектам вакцины. Во время диагностического обследования подробный сбор анамнеза, в том числе опрос о недавнем сексуальном поведении, является ключом к оценке риска заражения ВИЧ. Факторы или индикаторы риска включают незащищенный половой акт, наличие других инфекций, передающихся половым путем, употребление инъекционных наркотиков, инъекции нестерильным инструментом, случайные уколы иглой, нестерильные порезы или прокалывания. Особенно в группах высокого риска, таких как мужчины, имеющие половые контакты с мужчинами, работники коммерческого секса и потребители инъекционных наркотиков, пациенты, сообщающие о гриппоподобных симптомах, должны всегда расспрашиваться об их недавнем сексуальном поведении и истории употребления наркотиков, чтобы выявить в анамнезе возможный ВИЧ. воздействие и последующее тщательное диагностическое тестирование на недавнюю ВИЧ-инфекцию. Язвы в полости рта и потеря массы тела обладают самой высокой специфичностью, в то время как лихорадка и сыпь являются лучшими независимыми предикторами первичной ВИЧ-инфекции, поэтому эти симптомы особенно важно учитывать [6].
Особенно в группах высокого риска, таких как мужчины, имеющие половые контакты с мужчинами, работники коммерческого секса и потребители инъекционных наркотиков, пациенты, сообщающие о гриппоподобных симптомах, должны всегда расспрашиваться об их недавнем сексуальном поведении и истории употребления наркотиков, чтобы выявить в анамнезе возможный ВИЧ. воздействие и последующее тщательное диагностическое тестирование на недавнюю ВИЧ-инфекцию. Язвы в полости рта и потеря массы тела обладают самой высокой специфичностью, в то время как лихорадка и сыпь являются лучшими независимыми предикторами первичной ВИЧ-инфекции, поэтому эти симптомы особенно важно учитывать [6].
Несмотря на то, что тестирование на ВИЧ очень надежно в диагностике инфекции из-за высокой чувствительности скрининговых тестов на ВИЧ и высокой специфичности подтверждающего тестирования в соответствии с заранее определенными рекомендациями, все еще существуют пробелы в диагностике ранней инфекции [7]. Такие пробелы могут легко привести к пропуску диагноза острой ВИЧ-инфекции, особенно если симптомы появляются после вакцинации. Хотя в диагностике для ранней диагностики был достигнут значительный прогресс, задержка между заражением и реактивацией скрининговых тестов на ВИЧ четвертого поколения составляет примерно 17–21 день (или 22–24 дня с помощью скрининговых тестов третьего поколения) (таблица 1). До подтверждения реактивного скринингового теста требуется еще 14 дней, чтобы дать время для образования достаточного количества ВИЧ-специфических антител для достижения заданных критериев (3/3 положительных антител против: p24, gp41, gp120). Эти диагностические пробелы позволяют легко отказаться от предварительного диагноза первичной ВИЧ-инфекции, если результат скринингового теста не подтверждается первичным подтверждающим тестом.
Хотя в диагностике для ранней диагностики был достигнут значительный прогресс, задержка между заражением и реактивацией скрининговых тестов на ВИЧ четвертого поколения составляет примерно 17–21 день (или 22–24 дня с помощью скрининговых тестов третьего поколения) (таблица 1). До подтверждения реактивного скринингового теста требуется еще 14 дней, чтобы дать время для образования достаточного количества ВИЧ-специфических антител для достижения заданных критериев (3/3 положительных антител против: p24, gp41, gp120). Эти диагностические пробелы позволяют легко отказаться от предварительного диагноза первичной ВИЧ-инфекции, если результат скринингового теста не подтверждается первичным подтверждающим тестом.
Возможные последствия ошибочного диагноза первичной ВИЧ-инфекции очень серьезные. Упуская возможность ранней диагностики и лечения, инфицированные люди могут столкнуться с прогрессированием заболевания, что приведет к худшему исходу. Исследование START показало, что раннее начало лечения снижает риск событий, связанных с синдромом приобретенного иммунодефицита (СПИД), на 72% и не связанных со СПИДом событий на 39% [8]. Раннее начало антиретровирусной терапии (АРТ) также ограничивает резервуар ВИЧ и обеспечивает оптимальное восстановление иммунитета, что обеспечивает наилучший возможный результат [9].].
Раннее начало антиретровирусной терапии (АРТ) также ограничивает резервуар ВИЧ и обеспечивает оптимальное восстановление иммунитета, что обеспечивает наилучший возможный результат [9].].
Кроме того, игнорирование диагноза на стадии первичной ВИЧ-инфекции упускает возможность предотвратить передачу ВИЧ другим людям. Концентрация РНК ВИЧ достигается на ранних стадиях инфекции примерно во время сероконверсии, что делает этих людей особенно заразными. Бреннер и др. [10] подсчитали, что примерно половина случаев передачи ВИЧ происходит на ранней стадии инфекции, что делает раннюю диагностику и лечение мощным инструментом предотвращения распространения ВИЧ.
В заключение, в этом отчете о клиническом случае подчеркивается возможность неправильной интерпретации симптомов и результатов тестов на ранней стадии ВИЧ-инфекции из-за одновременной вакцинации против COVID-19 и пробелов в диагностике ранних инфекций, что позволяет легко ошибочно приписать симптомы побочным эффектам, связанным с вакциной. .
.
Доступность данных и материалов
Все данные, полученные или проанализированные в ходе этого исследования, включены в эту опубликованную статью.
Сокращения
- СПИД:
Синдром приобретенного иммунодефицита
- АРТ:
Антиретровирусная терапия
- COVID-19:
Коронавирусная болезнь
- CRP:
С-реактивный белок
- ИФА:
Иммуноферментный анализ
- ВИЧ:
Вирус иммунодефицита человека
- МСМ:
Мужчины, имеющие половые контакты с мужчинами
- ПКР:
Полимеразная цепная реакция
Ссылки
- «>
Сантанджело Х. Острая сероконверсия ВИЧ-инфекции в условиях амбулаторного лечения. Практика медсестры. 2001;26(4):48, 51–4, 6.
Google ученый
Ананд П., Стахель В.П. Обзор безопасности вакцин мРНК Covid-19: обзор. Пациент Саф Сург. 2021;15(1):20.
Артикул
Google ученый
Коэн М.С., Шоу Г.М., МакМайкл А.Дж., Хейнс Б.Ф. Острая инфекция ВИЧ-1. N Engl J Med. 2011;364(20):1943–54.
Артикул
КАСGoogle ученый
«>Hecht FM, Busch MP, Rawal B, Webb M, Rosenberg E, Swanson M, et al. Использование лабораторных тестов и клинических симптомов для выявления первичной ВИЧ-инфекции. СПИД. 2002;16(8):1119–29.
Артикул
Google ученый
Beelaert G, Fransen K. Оценка быстрого и простого скринингового анализа на ВИЧ четвертого поколения для качественного обнаружения антигена p24 ВИЧ и/или антител к ВИЧ-1 и ВИЧ-2. Дж. Вироловые методы. 2010;168(1–2):218–22.
Артикул
КАСGoogle ученый
Исследовательская группа INSIGHT START, Лундгрен Д.
 Д., Бабикер А.Г., Гордин Ф., Эмери С., Грунд Б. и др. Начало антиретровирусной терапии при ранней бессимптомной ВИЧ-инфекции. N Engl J Med. 2015;373(9): 795–807.
Д., Бабикер А.Г., Гордин Ф., Эмери С., Грунд Б. и др. Начало антиретровирусной терапии при ранней бессимптомной ВИЧ-инфекции. N Engl J Med. 2015;373(9): 795–807.Артикул
Google ученый
Hocqueloux L, Avettand-Fenoel V, Jacquot S, Prazuck T, Legac E, Melard A, et al. Длительная антиретровирусная терапия, начатая во время первичной инфекции ВИЧ-1, является ключом к достижению как низких резервуаров ВИЧ, так и нормального количества Т-клеток. J Антимикробная химиотерапия. 2013;68(5):1169–78.
Артикул
КАСGoogle ученый
Бреннер Б.Г., Роджер М., Рути Дж.П., Мойзи Д., Нтемгва М., Матте С. и др. Высокая частота событий прямой передачи после острой/ранней инфекции ВИЧ-1. J заразить дис. 2007;195 (7): 951–9.
Артикул
КАСGoogle ученый
Fiebig EW, Wright DJ, Rawal BD, Garrett PE, Schumacher RT, Peddada L, et al. Динамика виремии ВИЧ и сероконверсии антител у доноров плазмы: значение для диагностики и стадирования первичной ВИЧ-инфекции. СПИД. 2003; 17 (13): 1871–189.
Артикул
Google ученый
Фасенте С.Н., Гребе Э., Пилчер К.Д., Буш М.П., Мерфи Г., Велте А. Предполагаемые даты обнаруживаемой инфекции (EDDI) как улучшение стадирования Фибига для определения ВИЧ-инфекции. Эпидемиол инфекции. 2020;148: e53.
Артикул
КАС
Google ученый
Ссылки на скачивание
Благодарности
Неприменимо.
Финансирование
Финансирование открытого доступа организовано и разрешено Projekt DEAL. Непригодный.
Информация об авторе
Авторы и организации
Отделение внутренних болезней II, Университетская клиника Рехтс дер Изар, Медицинский факультет Мюнхенского технического университета, Ismaninger-Straße 22, 93675, Мюнхен, Германия
Джулиан Трибельхорн, Стефани Хашка, Феликс Гессе, Йоханна Эрбер, Саймон Вайдлих, Марсель Ли и Кристоф Д. Спиннер
Институт вирусологии, Медицинский факультет Мюнхенского технического университета, Мюнхен, Германия
Дитер Хоффманн
Институт Макса фон Петтенкофера, Немецкий национальный справочный центр ретровирусов при Мюнхенском университете Людвига-Максимилиана, Мюнхен, Германия
Йозеф Эберле
Авторы
- Джулиан Трибельхорн
Просмотр публикаций автора
Вы также можете искать этого автора в
PubMed Google Scholar - Stefanie Haschka
Просмотр публикаций автора
Вы также можете искать этого автора в
PubMed Google Scholar - Felix Hesse
Просмотр публикаций автора
Вы также можете искать этого автора в
PubMed Google Академия - Johanna Erber
Посмотреть публикации автора
Вы также можете искать этого автора в
PubMed Google Scholar - Simon Weidlich
Просмотр публикаций автора
Вы также можете искать этого автора в
PubMed Google Scholar - Marcel Lee
Просмотр публикаций автора
Вы также можете искать этого автора в
PubMed Google Scholar - Дитер Хоффманн
Просмотр публикаций автора
Вы также можете искать этого автора в
PubMed Google Scholar - Josef Eberle
Просмотр публикаций автора
Вы также можете искать этого автора в
PubMed Google Scholar - Christoph D.
 Spinner
SpinnerПросмотр публикаций автора
Вы также можете искать этого автора в
PubMed Google Scholar
Вклады
Все авторы внесли свой вклад в диагностику и лечение пациентов. Эта статья была в основном написана JT и курировалась CDS. Все авторы прочитали и одобрили окончательный вариант рукописи.
Автор, ответственный за переписку
Юлиан Трибельхорн.
Декларация этики
Одобрение этики и согласие на участие
Неприменимо.
Согласие на публикацию
От пациента было получено письменное информированное согласие на публикацию данного клинического случая. Копия письменного согласия доступна для ознакомления редактору этого журнала.
Конкурирующие интересы
Кристоф Спиннер сообщает о грантах, личных вознаграждениях и нефинансовой поддержке со стороны AbbVie; гранты, личные сборы и нефинансовая поддержка от Apeiron; гранты, личные гонорары от B. Braun Melsungen, гранты от Cepheid, личные гонорары от Formycon, гранты, личные гонорары и нефинансовая поддержка от Gilead Sciences; гранты и личные гонорары от Eli Lilly; гранты, личные гонорары и нефинансовая поддержка от Janssen-Cilag; личные сборы от партнеров Molecular, гранты, личные сборы и нефинансовая поддержка со стороны GSK/ViiV Healthcare; гранты, личные гонорары и нефинансовая поддержка от MSD, помимо представленной работы. Саймон Вейдлих сообщает о личных гонорарах и нефинансовой поддержке со стороны Gilead Sciences и Janssen-Cilag. Никаких дополнительных конкурирующих интересов со стороны авторов этой статьи.
Braun Melsungen, гранты от Cepheid, личные гонорары от Formycon, гранты, личные гонорары и нефинансовая поддержка от Gilead Sciences; гранты и личные гонорары от Eli Lilly; гранты, личные гонорары и нефинансовая поддержка от Janssen-Cilag; личные сборы от партнеров Molecular, гранты, личные сборы и нефинансовая поддержка со стороны GSK/ViiV Healthcare; гранты, личные гонорары и нефинансовая поддержка от MSD, помимо представленной работы. Саймон Вейдлих сообщает о личных гонорарах и нефинансовой поддержке со стороны Gilead Sciences и Janssen-Cilag. Никаких дополнительных конкурирующих интересов со стороны авторов этой статьи.
Дополнительная информация
Примечание издателя
Springer Nature остается нейтральной в отношении юрисдикционных претензий в опубликованных картах и институциональной принадлежности.
Права и разрешения
Открытый доступ Эта статья находится под лицензией Creative Commons Attribution 4.0 International License, которая разрешает использование, совместное использование, адаптацию, распространение и воспроизведение на любом носителе или в любом формате при условии, что вы укажете авторство оригинальный автор(ы) и источник, предоставьте ссылку на лицензию Creative Commons и укажите, были ли внесены изменения. Изображения или другие сторонние материалы в этой статье включены в лицензию Creative Commons на статью, если иное не указано в кредитной строке материала. Если материал не включен в лицензию Creative Commons статьи, а ваше предполагаемое использование не разрешено законом или выходит за рамки разрешенного использования, вам необходимо получить разрешение непосредственно от правообладателя. Чтобы просмотреть копию этой лицензии, посетите http://creativecommons.org/licenses/by/4.0/. Отказ Creative Commons от права на общественное достояние (http://creativecommons.org/publicdomain/zero/1.0/) применяется к данным, представленным в этой статье, если иное не указано в кредитной линии данных.
Изображения или другие сторонние материалы в этой статье включены в лицензию Creative Commons на статью, если иное не указано в кредитной строке материала. Если материал не включен в лицензию Creative Commons статьи, а ваше предполагаемое использование не разрешено законом или выходит за рамки разрешенного использования, вам необходимо получить разрешение непосредственно от правообладателя. Чтобы просмотреть копию этой лицензии, посетите http://creativecommons.org/licenses/by/4.0/. Отказ Creative Commons от права на общественное достояние (http://creativecommons.org/publicdomain/zero/1.0/) применяется к данным, представленным в этой статье, если иное не указано в кредитной линии данных.
Перепечатки и разрешения
Об этой статье
SARS-CoV-2 и ВИЧ-1 — история о двух вакцинах
SARS-CoV-2 и ВИЧ-1 — история о двух вакцинах
Скачать PDF
Ваша статья скачана
Карусель с тремя слайдами одновременно.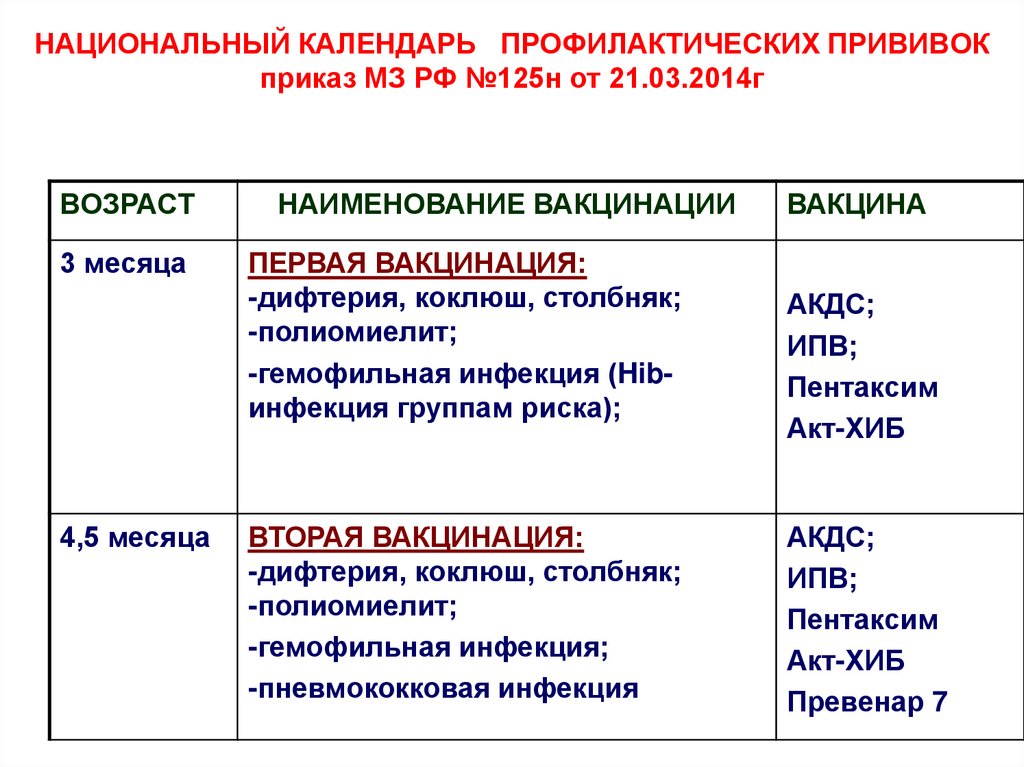 Используйте кнопки «Назад» и «Далее» для перехода по трем слайдам за раз или кнопки с точками в конце для перехода по трем слайдам за раз.
Используйте кнопки «Назад» и «Далее» для перехода по трем слайдам за раз или кнопки с точками в конце для перехода по трем слайдам за раз.
Скачать PDF
- Комментарий
- Опубликовано:
- Бартон Ф. Хейнс
ORCID: orcid.org/0000-0002-7643-9023 1
Обзоры природы Иммунология
том 21 , страницы 543–544 (2021)Процитировать эту статью
31 тыс.
 обращений
обращений10 цитирований
319 Альтметрический
Сведения о показателях
Субъекты
- Белковые вакцины
- Трансляционные исследования
Быстрая разработка вакцин против COVID-19 и их развертывание менее чем за год — это научный и медицинский триумф, который поднял ключевой вопрос. Почему у нас есть несколько вакцин против SARS-CoV-2, но нет ни одной вакцины против ВИЧ-1?
Вакцины являются основным средством профилактики инфекционных заболеваний, и их использование повышает выживаемость, защищает сообщества от новых инфекционных агентов и повышает производительность общества. Основным компонентом вакциноиндуцированного защитного иммунитета для большинства вирусных инфекций являются нейтрализующие антитела, хотя ненейтрализующие антитела и CD8 + Т-клетки могут повысить защитную эффективность вакцины. В декабре 2019 г. ВОЗ была уведомлена о кластере вирусной пневмонии неизвестного происхождения, а в январе 2020 г. был опубликован первый проект генома вируса-возбудителя SARS-CoV-2. К концу 2020 г. -2 вакцины были разработаны. Два из них показали эффективность ~ 95% в предотвращении симптоматического COVID-19 в испытаниях эффективности фазы III и получили одобрение FDA для развертывания в соответствии с разрешением на использование в чрезвычайных ситуациях до конца года. Напротив, четыре десятилетия назад, летом 1981 были описаны первые люди с так называемым синдромом приобретенного иммунодефицита (СПИД), а в 1983 году был выделен этиологический агент СПИДа, ВИЧ-1. 1 вакцина. Критический вопрос: «Почему вакцина против SARS-CoV-2 была изготовлена так быстро, а вакцина против ВИЧ-1 была так сложна?»? Ответ лежит в иммунобиологии взаимодействия вирусов с их хозяевами.
Основным компонентом вакциноиндуцированного защитного иммунитета для большинства вирусных инфекций являются нейтрализующие антитела, хотя ненейтрализующие антитела и CD8 + Т-клетки могут повысить защитную эффективность вакцины. В декабре 2019 г. ВОЗ была уведомлена о кластере вирусной пневмонии неизвестного происхождения, а в январе 2020 г. был опубликован первый проект генома вируса-возбудителя SARS-CoV-2. К концу 2020 г. -2 вакцины были разработаны. Два из них показали эффективность ~ 95% в предотвращении симптоматического COVID-19 в испытаниях эффективности фазы III и получили одобрение FDA для развертывания в соответствии с разрешением на использование в чрезвычайных ситуациях до конца года. Напротив, четыре десятилетия назад, летом 1981 были описаны первые люди с так называемым синдромом приобретенного иммунодефицита (СПИД), а в 1983 году был выделен этиологический агент СПИДа, ВИЧ-1. 1 вакцина. Критический вопрос: «Почему вакцина против SARS-CoV-2 была изготовлена так быстро, а вакцина против ВИЧ-1 была так сложна?»? Ответ лежит в иммунобиологии взаимодействия вирусов с их хозяевами.
ВИЧ-1, член группы Retroviridae и SARS-CoV-2, коронавирус подрода Sarbecovirus, представляют собой одноцепочечные РНК-вирусы с положительным смыслом. Однако основное различие между SARS-CoV-2 и ВИЧ-1 заключается в том, что большинство людей, инфицированных SARS-CoV-2, избавляются от вируса, а люди с ВИЧ-1 — нет. Это связано с тем, что SARS-CoV-2 является медленно мутирующим, неинтегрирующимся вирусом, и хозяин может полагаться на вторичный иммунный ответ, вызванный вакциной, на чистые инфицированные SARS-CoV-2 клетки. Напротив, ВИЧ-1 интегрируется в геном хозяина в течение примерно 72 часов после передачи. К тому времени, когда развивается первичный иммунный ответ на ВИЧ-1, возникает необратимая инфекция с латентно инфицированным CD4 9.0014 + Т-клеточный резервуар с включенной провирусной двухцепочечной ДНК. Таким образом, для успешной вакцины против ВИЧ-1 во время передачи должны присутствовать высокие уровни защитных нейтрализующих антител, чтобы полностью предотвратить заражение, что представляет собой очень высокую планку 2 .
Мишенью нейтрализующих антител к SARS-CoV-2 является рецептор-связывающий домен (RBD) гликопротеина шипа (S), тогда как мишенью нейтрализующих антител к ВИЧ-1 является гликопротеин оболочки (Env). Оба типа нейтрализующих антител блокируют связывание вирионов с их рецепторами — ангиотензинпревращающим ферментом 2 для SARS-CoV-2 и молекулой CD4 для ВИЧ-1. Все COVID-19вакцины, испытанные в фазе III, индуцировали нейтрализующие антитела, нацеленные на белок S, и обладают высокой степенью защиты от симптоматического заболевания. У обезьян коррелятами защиты являются прежде всего нейтрализующие антитела 3 . Традиционные первичные или первичные и бустерные схемы вакцинации с иммуногенами S-гликопротеина оказались чрезвычайно успешными в качестве вакцин против COVID-19 (рис. 1). Предыдущая работа над спайковым белком 4 ближневосточного респираторного синдрома, над модифицированной мРНК, заключенной в липидные наночастицы 5 , а также на платформах и методах исследования вакцины против ВИЧ-1 6 — все они позволили быстро разработать вакцину против COVID-19.
Рис. 1: Разработка вакцины против SARS-CoV-2 и ВИЧ-1.
Ат, антитело; bnAb, широко нейтрализующее антитело.
Изображение полного размера
В отношении ВИЧ-1 в испытаниях эффективности вакцины были протестированы две основные стратегии: индукция CD8 + Т-клеток, которые убивают ВИЧ-1-инфицированные клетки, и индукция ненейтрализующих антител, которые защищают от передачи ВИЧ-1 с помощью противовирусных эффекторных функций, опосредованных Fc-рецептором-γ (FcRγ). Подобно антителам, нейтрализующим SARS-CoV-2, ненейтрализующие антитела к ВИЧ-1 легко индуцируются любым из ряда мономеров или открытых тримеров Env ВИЧ-1. Однако из семи испытаний эффективности вакцины против ВИЧ-1, проведенных на сегодняшний день, шесть потерпели неудачу. Седьмой, названный RV144, который был проведен в Таиланде армией США, показал минимальную защиту ~ 31%, а ненейтрализующие антитела с FcRγ-опосредованными противовирусными эффекторными функциями служили коррелятами снижения риска передачи 7 . Два дополнительных испытания эффективности, направленные на индукцию защитных ненейтрализующих антител, нацеленных на Env, и ответы Т-клеток продолжаются, с надеждой, что они продемонстрируют степень защиты.
Два дополнительных испытания эффективности, направленные на индукцию защитных ненейтрализующих антител, нацеленных на Env, и ответы Т-клеток продолжаются, с надеждой, что они продемонстрируют степень защиты.
Тем не менее, конечной целью разработки вакцины против ВИЧ-1 является индукция антител широкого нейтрализующего действия (bnAb) 8 . В то время как антитела, нейтрализующие SARS-CoV-2, легко индуцируются в течение примерно 10 дней после появления симптомов COVID-19 и в течение 2 недель после вакцинации, bnAb к ВИЧ-1 нелегко индуцируются ни вакцинацией, ни инфекцией и появляются только в очень высокие уровни примерно у 10% людей, инфицированных ВИЧ-1, после нескольких лет инфицирования. Препятствиями для индукции bnAb ВИЧ-1 являются наличие плотного и слабо иммуногенного гликанового щита Env, молекулярная мимикрия эпитопов Env, вызывающая перекрестную реакцию антител с человеческими белками, и вариабельные участки петли в Env, которые могут индуцировать конкурирующие неиммуногенные эпитопы. защитные антитела. Что наиболее важно, bnAb ВИЧ-1 обладают необычными чертами, такими как аутореактивность, длинные участки, определяющие комплементарность третьей тяжелой цепи (HCDR3), и обогащены редкими соматическими мутациями — все это делает предшественники bnAb либо очень редкими из-за делеции иммунной толерантности, либо трудно активируемыми. 9,10 .
защитные антитела. Что наиболее важно, bnAb ВИЧ-1 обладают необычными чертами, такими как аутореактивность, длинные участки, определяющие комплементарность третьей тяжелой цепи (HCDR3), и обогащены редкими соматическими мутациями — все это делает предшественники bnAb либо очень редкими из-за делеции иммунной толерантности, либо трудно активируемыми. 9,10 .
Эти необычные свойства bnAb к ВИЧ-1 обусловили необходимость стратегии разработки вакцины против ВИЧ-1, в первую очередь нацеленной на редкие наивные В-клеточные предшественники bnAb для расширения пула предшественников bnAb. Далее, последовательные тримеры Env должны быть специально разработаны для отбора промежуточных членов B-клеточной линии bnAb, имеющих редкие мутации антител, необходимые для созревания bnAb 8,9,10 (рис. 1). Кроме того, чтобы избежать ускользания вируса-основателя ВИЧ-1, успешная вакцина против ВИЧ-1 должна индуцировать линии В-клеток к нескольким из семи сайтов связывания bnAb на Env ВИЧ-1. Значение успешного нацеливания на зародышевую линию и последовательного дизайна иммуногена ВИЧ-1 выходит за рамки создания долгожданной вакцины против ВИЧ-1. Изучение правил безопасного управления линиями В-клеток bnAb должно улучшить разработку других сложных в производстве вакцин, а также извлечь уроки в отношении предотвращения нежелательных иммунных реакций, таких как выработка патогенных аутоантител.
Значение успешного нацеливания на зародышевую линию и последовательного дизайна иммуногена ВИЧ-1 выходит за рамки создания долгожданной вакцины против ВИЧ-1. Изучение правил безопасного управления линиями В-клеток bnAb должно улучшить разработку других сложных в производстве вакцин, а также извлечь уроки в отношении предотвращения нежелательных иммунных реакций, таких как выработка патогенных аутоантител.
Работа над вакциной против SARS-CoV-2 потребовала экстраординарных ресурсов и беспрецедентного глобального сотрудничества. Научные и медицинские успехи вакцин против COVID-19 в настоящее время внушают новое чувство неотложности этой самой сложной работы по разработке вакцины против ВИЧ-1.
История изменений
04 августа 2021 г.
Опубликована коррекция в эту статью: https://doi.org/10.1038/S41577-021-00604-0
13 декаб к этой статье был опубликован: https://doi.org/10.1038/s41577-021-00671-3
Ссылки
- «>
МакМайкл, А. Дж., Борроу, П., Томарас, Г. Д., Гунетиллеке, Н. и Хейнс, Б. Ф. Иммунный ответ при острой инфекции ВИЧ-1: ключи к разработке вакцины. Нац. Преподобный Иммунол. 10 , 11–23 (2010).
Артикул
КАСGoogle ученый
McMahan, K. et al. Корреляты защиты от SARS-CoV-2 у макак-резусов. Природа 590 , 630–634 (2021).
Артикул
КАСGoogle ученый
Corbett, K.S. et al. Разработка мРНК-вакцины против SARS-CoV-2 стала возможной благодаря готовности прототипа патогена. Природа 586 , 567–571 (2020).
Артикул
КАСGoogle ученый
«>Семповски Г. Д., Сондерс К. О., Ачарья П., Вихе К. Дж. и Хейнс Б. Ф. Готовность к пандемии: разработка вакцин и терапевтических антител против COVID-19. Cell 181 , 1458–1463 (2020).
Артикул
КАСGoogle ученый
Томарас, Г. Д. и Плоткин, С. А. Комплексные иммунные корреляты защиты в испытаниях эффективности вакцины против ВИЧ-1. Иммунол. 275 , 245–261 (2017).
Артикул
КАСGoogle ученый
Хейнс, Б. Ф., Бертон, Д. Р. и Маскола, Дж. Р. Многочисленные роли антител, широко нейтрализующих ВИЧ. Науч. Перевод мед.
 11 , eaaz2686 (2019).
11 , eaaz2686 (2019).Артикул
КАСGoogle ученый
Haynes, B. F. & Verkoczy, L. Хозяин-контроль нейтрализующих антител к ВИЧ. Наука 344 , 588–589 (2014).
Артикул
Google ученый
Haynes, B.F., Kelsoe, G., Harrison, S.C. & Kepler, T.B. Дизайн иммуногена B-клеток при разработке вакцины против ВИЧ-1 в качестве тематического исследования. Нац. Биотехнолог. 30 , 423–433 (2012).
Артикул
КАСGoogle ученый
Сетте А. и Кротти С. Адаптивный иммунитет к SARS-CoV-2 и COVID-19. Cell 184 , 861–880 (2021).
Артикул
КАС
Google ученый
Парди, Н., Хоган, М.Дж. и Вайсман, Д. Последние достижения в технологии мРНК-вакцины. Курс. мнение Иммунол. 65 , 14–20 (2020).
Артикул
КАС
Google ученый
Скачать ссылки
Благодарности
B.F.H. поддерживается NIH, NIAID, Отделом СПИДа NIAID, грантом UM1 AI144371 Консорциумом по разработке вакцины против ВИЧ/СПИДа. Автор выражает благодарность К. Сондерс за предоставление изображений иммуногенов ВИЧ-1 на рис. 1.
Информация об авторе
Авторы и организации
Институт человеческих вакцин Дьюка и факультеты медицины и иммунологии Медицинской школы Университета Дьюка, Дарем, Северная Каролина, США
Barton F.
 Haynes
Haynes
Авторы
- Barton F. Haynes Посмотреть 900 публикаций
Вы также можете искать этого автора в
PubMed Google Scholar
Автор, ответственный за переписку
Бартон Ф. Хейнс.
Декларации этики
Конкурирующие интересы
B.F.H. имеет поданные и находящиеся на рассмотрении патенты на конструкции белков шипов коронавируса, состав и способы их использования (патенты США № 63/147,998; 63/149,541; 63/167,390), композиции, содержащие модифицированные оболочки ВИЧ (патент США PCT/US 2018/034,772), и композиции, содержащие оболочки ВИЧ, для индукции антител к ВИЧ (предварительная заявка на патент США 62/739,701).
Права и разрешения
Перепечатка и разрешения
Об этой статье
Эту статью цитирует
Стратегии для вакцин против ВИЧ-1, которые индуцируют нейтрализующие антитела широкого спектра действия
- Бартон Ф.

- Бартон Ф.

 Вакцинацию проводят через 2-4 недели после выздоровления или в период реконвалесценции или ремиссии.
Вакцинацию проводят через 2-4 недели после выздоровления или в период реконвалесценции или ремиссии. Очень часто афебрильные судороги являются первым проявлением эпилепсии. Определить принадлежность судорог к эпилепсии или поствакцинальному осложнению не представляется возможным, поэтому при предшествующей вакцинации судорожный синдром расценивается как осложнение.
Очень часто афебрильные судороги являются первым проявлением эпилепсии. Определить принадлежность судорог к эпилепсии или поствакцинальному осложнению не представляется возможным, поэтому при предшествующей вакцинации судорожный синдром расценивается как осложнение. Spinner 1
Spinner 1  Д., Бабикер А.Г., Гордин Ф., Эмери С., Грунд Б. и др. Начало антиретровирусной терапии при ранней бессимптомной ВИЧ-инфекции. N Engl J Med. 2015;373(9): 795–807.
Д., Бабикер А.Г., Гордин Ф., Эмери С., Грунд Б. и др. Начало антиретровирусной терапии при ранней бессимптомной ВИЧ-инфекции. N Engl J Med. 2015;373(9): 795–807. Spinner
Spinner обращений
обращений 11 , eaaz2686 (2019).
11 , eaaz2686 (2019). Haynes
Haynes