Содержание
Вакцинация во Всеволожске для детей и взрослых
Ребенок должен быть защищен от всего, от чего может быть защищен
(Всемирная организация здравоохранения)
Вакцинопрофилактика – один из наиболее благотворных вкладов медицинской науки в общественное здравоохранение. Благодаря ей в развитых странах частота ряда инфекционных заболеваний (дифтерия, корь, паротит, врождённая краснуха, гемофильная инфекция типа В) снизилась многократно, а по оспе и полиомиелиту – до нулевой и спорадической. В определённой мере человечество обязано ей увеличением продолжительности жизни, неотягощённой инфекционными болезнями.
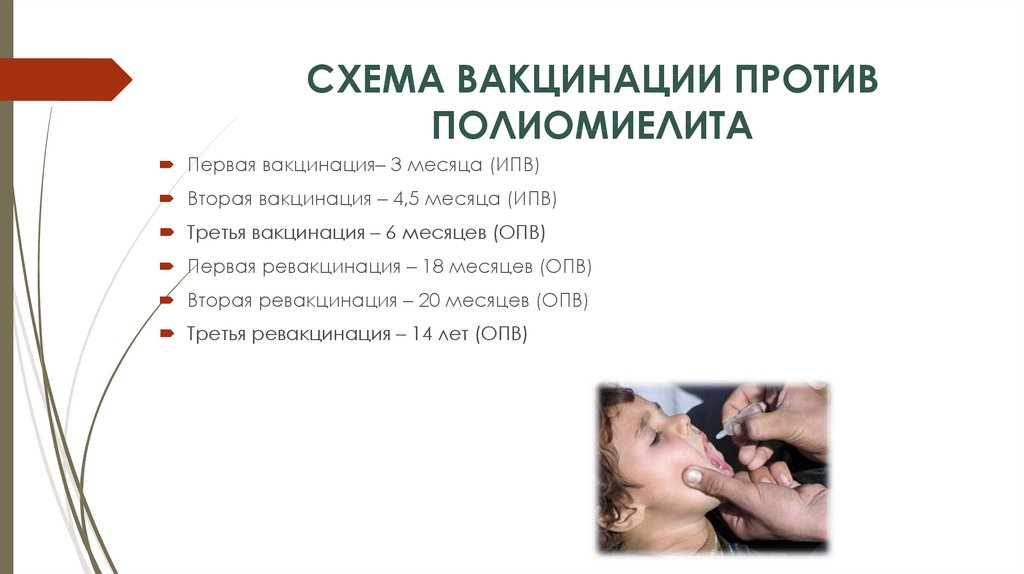
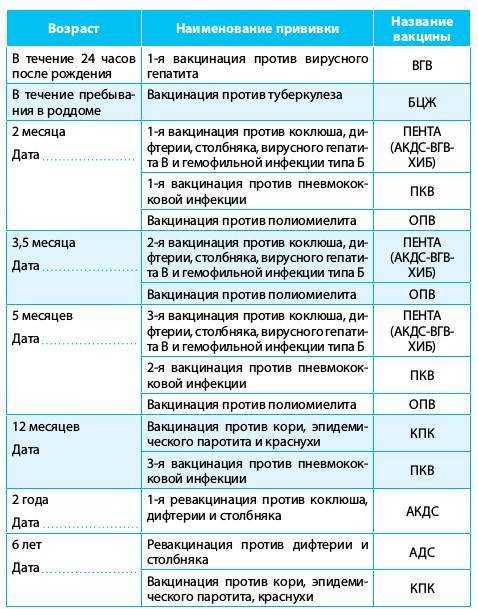
Профилактические прививки в каждой стране производят по своему календарю, который разрабатывают, исходя из эпидемической ситуации в стране, наличия соответствующих вакцин, уровня организации здравоохранения.
Последние изменения в наш календарь прививок были внесены в декабре 2011 года.
В нем содержится информация о возрасте, в котором необходимо сделать прививку, а также о группах детей, которым может быть необходима дополнительная вакцинация или изменение ее схемы.
Нужно помнить, что каждый ребенок индивидуален, и решение, о сроке прививки и вакцине, принимает курирующий ребенка врач-педиатр.
Кроме плановых профилактических прививок (по национальному календарю), существуют дополнительные вакцины, которые можно рекомендовать разным возрастным группам:
— так, перед поступлением в детский сад можно сделать прививку против гемофильной и пневомококковой инфекции– это позволит защитить вашего малыша от частых ОРЗ, отитов, пневмоний;
— перед школой — к перечисленному списку можно добавить еще вакцинацию против ветряной оспы, т.к. старшие дети ее тяжелее переносят;
— перед весеннее — летним сезоном – вакцинация против гепатита А и клещевого энцефалита (т.к. территория Санкт-Петербурга и Ленинградской области эндемична по данному заболеванию),
В настоящее время существует большой выбор вакцин разных производителей, которые зарекомендовали себя как эффективные и безопасные. Можно выбрать моно- (против одной инфекции) или комбинированные вакцины.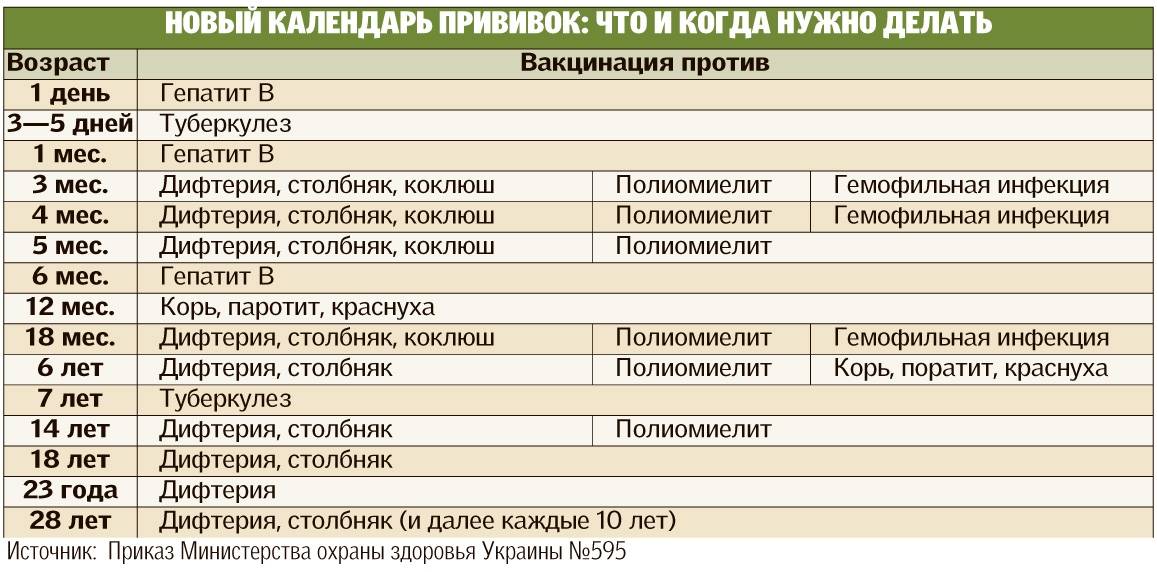
|
Наименование прививки
|
Используемые вакцины
|
|
Вакцинация против вирусного гепатита В
|
Эувакс, Регевак В, Энджерикс В, Комбиотекс
|
|
Вакцинация против туберкулеза
|
БЦЖ, БЦЖ-М
|
|
Вакцинация против дифтерии, коклюша, столбняка
|
АКДС, АДС-М, Инфанрикс, Пентаксим, Тетраксим
|
|
Вакцинация против гемофильной инфекции
|
Пентаксим, АКТ-ХИБ, Хиберикс
|
|
Вакцинация против полиомиелита
|
ОПВ, ИПВ, Полиорикс, Тетраксим
|
|
Вакцинация против кори, краснухи, эпидемического паротита
|
Вакцина против кори, краснухи, паротита, Приорикс
|
|
Вакцинация против пневмококковой инфекции
|
Пневмо-23, Превенар
|
|
Вакцинация против ветряной оспы
|
Вариликс
|
|
Вакцинация против вирусного гепатита А
|
ГЕП-А-ин-ВАК, Аваксим
|
|
Вакцинация против клещевого энцефалита
|
ФСМЕ-ИММУН, ФСМЕ-ИММУН Джуниор, Энцепур
|
Необходимо вспомнить о противопоказаниях к вакцинации, существуют:
— Истинные – настоящие противопоказания, перечисленные в инструкции к вакцинам и в руководящих документах
— Ложные – противопоказаниями не являются, но в силу каких-либо причин, таковыми считаются (перинатальная энцефалопатия, реакция на вакцинацию у кого-то из членов семьи)
— Временные – например, при острых заболеваниях и обострении хронических
— Постоянные – противопоказания, которые со временем снять невозможно.
Наличие или отсутствие противопоказаний определяет врач-педиатр, наблюдающий ребенка.
Итак, ребенок осмотрен педиатром, вакцина выбрана, мама и малыш доблестно выдержали инъекцию, что теперь?
Необходимо соблюдать все рекомендации врача.
Не вводить новые продукты в рацион за несколько дней до и после прививок.
Если ребенок себя чувствует хорошо и у него нет температуры — можно гулять, то же самое касается и купания (исключение составляет проба Манту).
В каких случаях необходимо обратиться к педиатру:
– если у Вашего ребенка высокая температура
— ребенок выглядит бледным, вялым, или наоборот, очень беспокойный
— плачет более трех часов подряд
— ребенок плачет странным, отличным от обычного, высоким голосом
— ребенок дрожит, вздрагивает, или у него судороги
— ребенок пассивный или заторможенный
— ребенок отказывается от еды и питья
О развитии осложнений
Вакцины изготавливаются из микроорганизмов или бывают синтетическими. Факт, что прививка может содержать части микроорганизмов или даже ослабленных живых микробов, которые могут вызвать заболевание у ребенка, очень пугает родителей.
Факт, что прививка может содержать части микроорганизмов или даже ослабленных живых микробов, которые могут вызвать заболевание у ребенка, очень пугает родителей.
Нужно помнить, что биологический материал, из которого изготавливают прививки, проходит тщательные проверки, и потому риск развития активной формы болезни после вакцинации ничтожно мал. Для изготовления вакцин не используются активные патогенные микроорганизмы, а только их фрагменты или сильно ослабленные или убитые штаммы.
Практически все вакцины вызывают такие побочные реакции как незначительное повышение температуры, болезненность и припухлость на месте введения — это нормальная (нормэргическая) реакция на вакцинацию. Эти реакции столь кратковременны и безобидны, что их просто нельзя сравнивать с риском самой болезни, против которой был привит ребенок.
|
Вакцинация (профилактическая прививка) является одним из видов медицинских вмешательств (п. Гражданин, один из родителей или иной законный представитель несовершеннолетнего в возрасте до 15 лет или больного наркоманией несовершеннолетнего в возрасте до 16 лет, законный представитель лица, признанного недееспособным, вправе отказаться от вакцинации (ч. 3 ст. 20 Закона N 323-ФЗ; п. 1 ст. 5, п. 2 ст. 11 Закона от 17.09.1998 N 157-ФЗ). Законными представителями несовершеннолетних являются, в частности, родители, усыновители, опекуны или попечители. Законными представителями лиц, признанных судом недееспособными, являются опекуны (п. 1 ст. 26, п. 1 ст. 28, п. 2 ст. 29, п. 1 ст. 32 ГК РФ; п. 1 ст. 64 СК РФ). Отказ от проведения медицинского вмешательства, в том числе профилактических прививок, содержится в медицинской документации гражданина и оформляется в виде документа на бумажном носителе либо формируется в форме электронного документа, подписанного гражданином (одним из родителей или иным законным представителем) с использованием усиленной квалифицированной электронной подписи или простой электронной подписи посредством применения ЕСИА, а также медицинским работником с использованием усиленной квалифицированной электронной подписи. При этом отказ от вакцинации одного из родителей (иного законного представителя) может быть в форме электронного документа при наличии в медицинской документации пациента сведений о его законном представителе (ч. 7 ст. 20 Закона N 323-ФЗ; п. п. 1, 3 ст. 5 Закона N 157-ФЗ; Письмо Минздрава России от 13.07.2015 N 24-2/3048428-1510). При отказе от медицинского вмешательства гражданину, одному из родителей или иному законному представителю указанных выше лиц в доступной форме должны быть разъяснены возможные последствия такого отказа (ч. 4 ст. 20 Закона N 323-ФЗ; п. 1 ст. 5 Закона N 157-ФЗ).
Последствия отказа от вакцинации Отсутствие профилактических прививок влечет (п. 2 ст. 5 Закона N 157-ФЗ; п. 5.7 Правил, утв. Постановлением Главного государственного санитарного врача РФ от 22.10.2013 N 60; Письмо Минздрава России от 09.11.2017 N 15-2/3111843-28319): • запрет на выезд в страны, пребывание в которых, в соответствии с международными медико-санитарными правилами либо международными договорами РФ, требует конкретных профилактических прививок; • временный отказ в приеме в образовательные и оздоровительные учреждения в случае возникновения массовых инфекционных заболеваний или при угрозе возникновения эпидемий (т. • отказ в приеме граждан на работы или отстранение граждан от работ, выполнение которых связано с высоким риском заболевания инфекционными болезнями. Перечень работ, выполнение которых связано с высоким риском заболевания инфекционными болезнями и требует обязательного проведения профилактических прививок, утверждается федеральным органом исполнительной власти, уполномоченным Правительством РФ. Кроме того, медицинская организация вправе обратиться в суд с административным исковым заявлением о защите интересов несовершеннолетнего или лица, признанного в установленном порядке недееспособным, в случае отказа законного представителя от медицинского вмешательства, необходимого для спасения жизни (ч. 5 ст. 20 Закона N 323-ФЗ; п.
Противопоказания для вакцинации В список противопоказаний к вакцинации включены следующие состояния (п. 3.1 МУ 3.3.1.1095-02, утв. Главным государственным санитарным врачом РФ 09.01.2002):
Острые инфекционные и неинфекционные заболевания, обострение хронических заболеваний являются временными противопоказаниями для проведения прививок. Плановые прививки проводятся через две – четыре недели после выздоровления или в период ремиссии. При нетяжелых ОРВИ, острых кишечных заболеваниях и других заболеваниях прививки проводятся сразу после нормализации температуры (таблица N 1 МУ 3.3.1.1095-02). Наличие или отсутствие противопоказаний к использованию той или иной вакцины относится к сфере специальных медицинских знаний и должно проверяться перед каждой предполагаемой вакцинацией по отношению к каждому пациенту. Наличие противопоказания не означает, что в случае проведения прививки у вакцинированного обязательно возникнет осложнение, речь идет лишь о повышении риска неблагоприятной реакции, что, однако, должно рассматриваться как препятствие к проведению вакцинации в большинстве случаев (п. 3.
| ||||||||||||||||||||||||
Пероральная вакцина против полиомиелита влияет на иммунный ответ на вакцинацию БЦЖ. Естественный эксперимент
1. Colditz GA, Brewer TF, Berkey CS, Wilson ME, Burdick E, et al. Эффективность вакцины БЦЖ в профилактике туберкулеза. Метаанализ опубликованной литературы. ДЖАМА. 1994; 271: 698–702. [PubMed] [Google Scholar]
2. Прекрасная физкультура. Изменение защиты БЦЖ: последствия гетерологичного иммунитета и для него. Ланцет. 1995; 346: 1339–45. [PubMed] [Google Scholar]
3. Marchant A, Goetghebuer T, Ota MO, Wolfe I, Cesay SJ, et al. У новорожденных развивается иммунный ответ Th2-типа на вакцинацию Mycobacterium bovis bacillus Calmette-Guérin. Дж Иммунол. 1999;163:2249–55. [PubMed] [Google Scholar]
4. Ota MO, Vekemans J, Schlegel-Haueter SE, Fielding K, Sanneh M, et al. Влияние Mycobacterium bovis бациллы Кальметта-Герена на реакцию антител и цитокинов на неонатальную вакцинацию человека.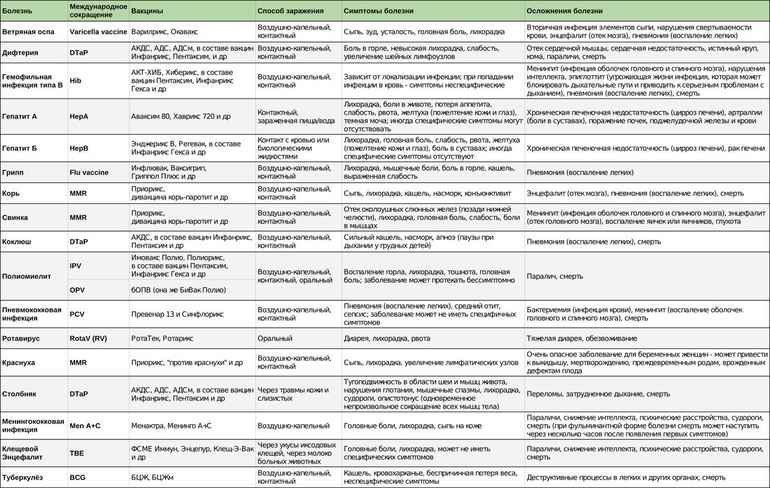 Дж Иммунол. 2002; 168: 919–25. [PubMed] [Google Scholar]
Дж Иммунол. 2002; 168: 919–25. [PubMed] [Google Scholar]
5. Benn CS, Diness BR, Roth A, Nante E, Fisker AB, et al. Влияние 50 000 МЕ витамина А, введенного с вакциной БЦЖ, на смертность младенцев в Гвинее-Бисау: рандомизированное плацебо-контролируемое исследование. БМЖ. 2008; 336:1416–20. [Бесплатная статья PMC] [PubMed] [Google Scholar]
6. Динесс Б.Р., Фискер А.Б., Рот А., Язданбахш М., Сартоно Э. и соавт. Влияние добавок с высокими дозами витамина А на иммунный ответ на вакцину Bacille Calmette-Guerin. Am J Clin Nutr. 2007; 86: 1152–9. [PubMed] [Google Scholar]
7. Benn CS, Fisker AB, Rodrigues A, Ravn H, Sartono E, et al. Влияние оральной полиомиелитной вакцины, вводимой БЦЖ при рождении, на детскую смертность в зависимости от пола в Гвинее-Бисау. Естественный эксперимент. ПЛОС ОДИН. 2008;3(12):e4056. [Бесплатная статья PMC] [PubMed] [Google Scholar]
8. Eriksson M, Sartono E, Martins CL, Balé C, Garly ML, et al. Сравнение продукции цитокинов ex vivo в венозной и капиллярной крови. Клин Эксп Иммунол. 2007; 150:469–76. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Клин Эксп Иммунол. 2007; 150:469–76. [Бесплатная статья PMC] [PubMed] [Google Scholar]
9. Bouros D, Zeros G, Panaretos C, Vassilatos C, Siafakas N. Метод пальпации против пера для измерения туберкулиновой реакции кожи (проба Манту). Грудь. 1999; 99: 416–9. [PubMed] [Google Scholar]
10. Garly ML, Bale C, Martins CL, Baldé MA, Hedegaard KL, et al. Вакцинация БЦЖ среди младенцев из Западной Африки связана с меньшей анергией туберкулина и дифтерийно-столбнячного антигена. вакцина. 2001; 20: 468–74. [PubMed] [Академия Google]
11. Баррос А.Дж., Хираката В.Н. Альтернативы логистической регрессии в перекрестных исследованиях: эмпирическое сравнение моделей, непосредственно оценивающих коэффициент распространенности. БМС Мед Рез Методол. 2003;3:21. [Бесплатная статья PMC] [PubMed] [Google Scholar]
12. Lalor MK, Ben-Smith A, Gorak-Stolinska P, Weir RE, Floyd S, et al. Популяционные различия в иммунных реакциях на вакцинацию против бациллы Кальметта-Герена в младенчестве. J заразить Dis. 2009; 199: 795–800. [Бесплатная статья PMC] [PubMed] [Google Scholar]
J заразить Dis. 2009; 199: 795–800. [Бесплатная статья PMC] [PubMed] [Google Scholar]
13. Günther J, Haas W, Von Boehmer H. Подавление ответов Т-клеток посредством конкуренции за фактор роста Т-клеток (интерлейкин 2). Евр Дж Иммунол. 1982; 12: 247–9. [PubMed] [Google Scholar]
14. Stockinger B, Kassiotis G, Bourgeois C. Память Т-клеток CD4. Семин Иммунол. 2004; 16: 295–303. [PubMed] [Google Scholar]
15. Vekemans J, Ota MO, Wang EC, Kidd M, Borysiewicz LK, et al. Реакция Т-клеток на вакцины у младенцев: дефект продукции IFNgamma после пероральной вакцинации против полиомиелита. Клин Эксп Иммунол. 2002;127:495–8. [Бесплатная статья PMC] [PubMed] [Google Scholar]
16. Klein NP, Gans HA, Sung P, Yasukawa LL, Jhonson J, et al. Реакция Т-клеток недоношенных детей на инактивированную вакцину против полиомиелита. J заразить Dis. 2010;201:214–22. [PubMed] [Google Scholar]
17. Анурадха Б., Рах С.С., Исхак М., Мурти К.Дж.Р., Валлури В.Л. Генотип +874 низкого продуцента интерферона-γ чрезмерно представлен у детей, не отвечающих на лечение Bacillus Calmette-Guirin. Pediatr Infect Dis J. 2008;27:325–9. [PubMed] [Академия Google]
Pediatr Infect Dis J. 2008;27:325–9. [PubMed] [Академия Google]
18. Купер А.М., Далтон Д.К., Стюарт Т.А., Гриффин Дж.П., Рассел Д.Г. и соавт. Диссеминированный туберкулез у мышей с нарушенным геном гамма-интерферона. J Эксперт Мед. 1993;178:2243–7. [Бесплатная статья PMC] [PubMed] [Google Scholar]
19. Flynn JL, Chan J, Triebold KJ, Dalton DK, Stewart TA, et al. Существенная роль гамма-интерферона в устойчивости к инфекции Mycobacterium tuberculosis . J Эксперт Мед. 1993; 178:2249–54. [Бесплатная статья PMC] [PubMed] [Google Scholar]
20. Jouanguy E, Altare F, Lamhammedi S, Revy P, Emile JF, et al. Дефицит интерферон-гамма-рецептора у младенца с фатальной инфекцией бациллой Кальметта-Герена. N Engl J Med. 1996; 335: 1956–61. [PubMed] [Google Scholar]
21. Newport MJ, Huxley CM, Huston S, Hawrylowicz CM, Oostra BA, et al. Мутация в гене рецептора гамма-интерферона и восприимчивость к микобактериальной инфекции. N Engl J Med. 1996; 335:1941–9. [PubMed] [Google Scholar]
22. Аль-Аттия Р., Мустафа А.С., Абаль А.Т., Мади Н.М., Андерсен П. Восстановление микобактериальной антиген-индуцированной пролиферации и интерферон-гамма-ответов в мононуклеарных клетках периферической крови больных туберкулезом при эффективном химиотерапия. FEMS Immunol Med Microbiol. 2003;38:249–56. [PubMed] [Google Scholar]
Аль-Аттия Р., Мустафа А.С., Абаль А.Т., Мади Н.М., Андерсен П. Восстановление микобактериальной антиген-индуцированной пролиферации и интерферон-гамма-ответов в мононуклеарных клетках периферической крови больных туберкулезом при эффективном химиотерапия. FEMS Immunol Med Microbiol. 2003;38:249–56. [PubMed] [Google Scholar]
23. Hirsch CS, Toossi Z, Othieno C, Johnson JL, Schwander SK, et al. Подавленные Т-клеточные интерферон-гамма-ответы при туберкулезе легких: анализ основных механизмов и модулирование с помощью терапии. J заразить Dis. 1999; 180:2069–73. [PubMed] [Google Scholar]
24. Marchant A, Amedei A, Azzurri A, Vekemans J, Benagiano M, et al. Поляризация PPD-специфического Т-клеточного ответа больных туберкулезом с профиля Th0 на профиль Th2 после успешной антимикобактериальной терапии или кондиционирования in vitro интерфероном-альфа или интерлейкином-12. Am J Respir Cell Mol Biol. 2001; 24: 187–9.4. [PubMed] [Google Scholar]
25. Allende LM, López-Goyanes A, Paz-Artal E, Corell A, García-Pérez MA, et al.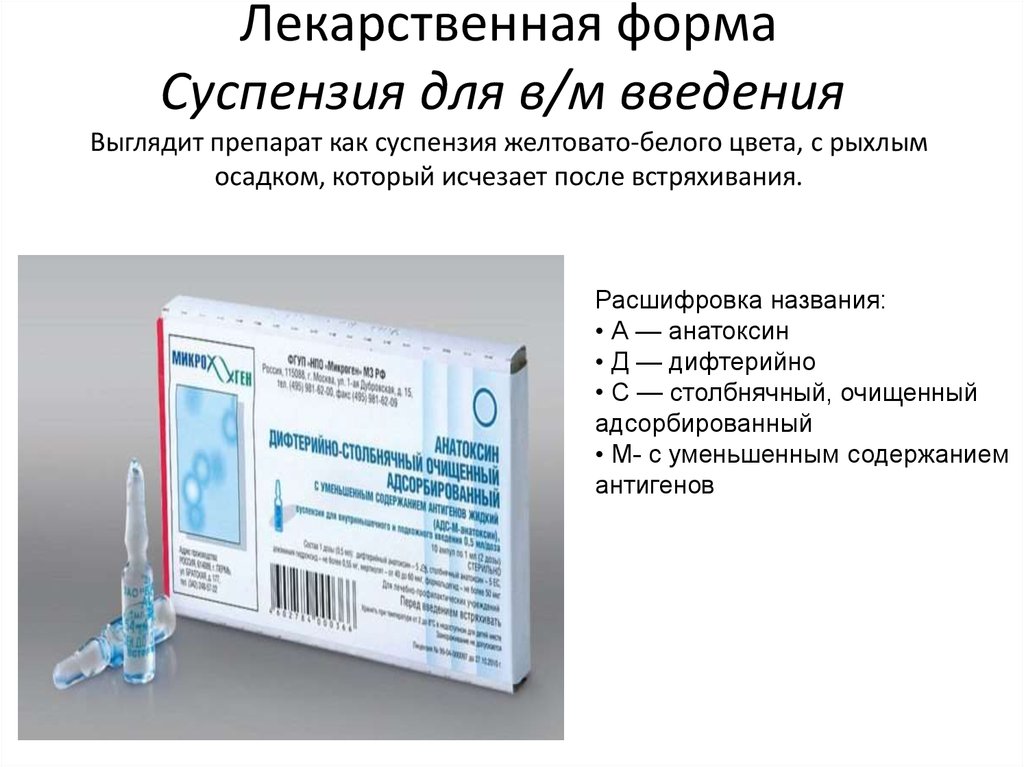 Точковая мутация в домене рецептора гамма-интерферона 1 провоцирует выраженный иммунодефицит. Клин Диагн Лаб Иммунол. 2001; 8: 133–137. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Точковая мутация в домене рецептора гамма-интерферона 1 провоцирует выраженный иммунодефицит. Клин Диагн Лаб Иммунол. 2001; 8: 133–137. [Бесплатная статья PMC] [PubMed] [Google Scholar]
26. Cunningham JA, Kellner JD, Bridge PJ, Trevenen CL, Mcleod DR, et al. Диссеминированная инфекция бациллой Кальметта-Герена у младенца с новой делецией в гене рецептора интерферона-гамма. Int J Tuberc Lung Dis. 2000;4:791–4. [PubMed] [Google Scholar]
27. Дорман С.Е., Холланд С.М. Мутация в сигнально-трансдуцирующей цепи рецептора интерферона-гамма и восприимчивость к микобактериальной инфекции. Джей Клин Инвест. 1998; 101: 2364–9. [Бесплатная статья PMC] [PubMed] [Google Scholar]
28. Dogan E, Erkoc R, Sayarlioglu H, Uzun K. Результаты туберкулинового кожного теста и феномен бустера в двухэтапном туберкулиновом кожном тесте у пациентов, находящихся на гемодиализе. Рен Фэйл. 2005; 27: 425–8. [PubMed] [Академия Google]
Ранняя эволюция оральной полиовирусной вакцины обусловлена сильным положительным отбором и узкими местами передачи
Асеведо А.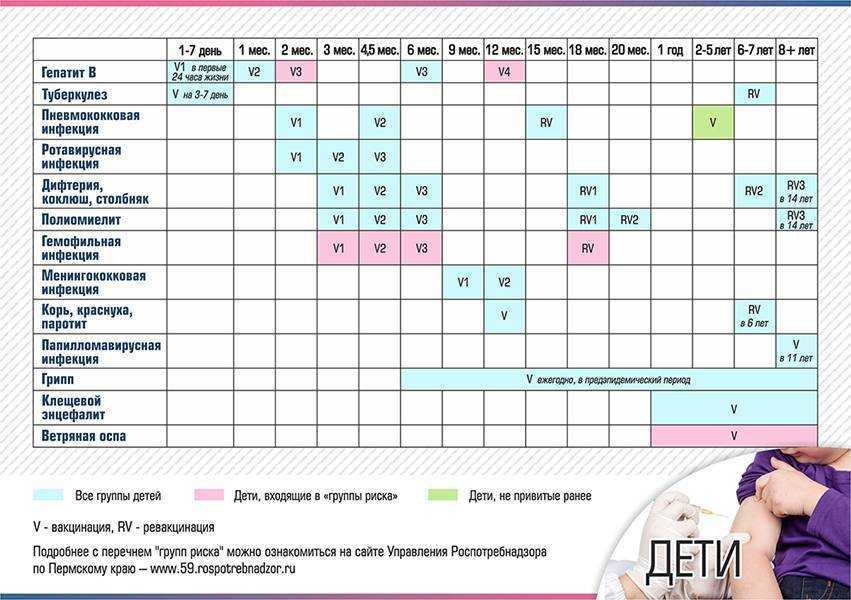 , Бродский Л., Андино Р. Мутационные и приспособленные ландшафты РНК-вируса, выявленные в результате секвенирования популяции. Природа. 2014; 505: 686–690. [Бесплатная статья PMC] [PubMed] [Google Scholar]
, Бродский Л., Андино Р. Мутационные и приспособленные ландшафты РНК-вируса, выявленные в результате секвенирования популяции. Природа. 2014; 505: 686–690. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Алам Н., Али Т., Раззак А., Рахман М., Захирул Хак М., Саха С.К., Ахмед А., Сардер А.М., Мойнуддин Хайдер М., Юнус М. Система наблюдения за здоровьем и демографией (HDSS) в Матлабе, Бангладеш. Междунар. Дж. Эпидемиол. 2017;46:809–816. [PubMed] [Google Scholar]
Avanzino BC, Jue H., Miller C.M., Cheung E., Fuchs G., Fraser CS Молекулярный механизм аттенуации вакцинного штамма полиовируса Sabin. Дж. Биол. хим. 2018;293:15471–15482. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Blake I.M., Pons-Salort M., Molodecky N.A., Diop O.M., Chenoweth P., Bandyopadhyay A.S., Zaffran M., Sutter R.W., Grassly N.C. Обнаружение полиовируса типа 2 после глобальный отказ от трехвалентной пероральной вакцины. Н. англ. Дж. Мед. 2018;379: 834–845. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Boot HJ, Sonsma J.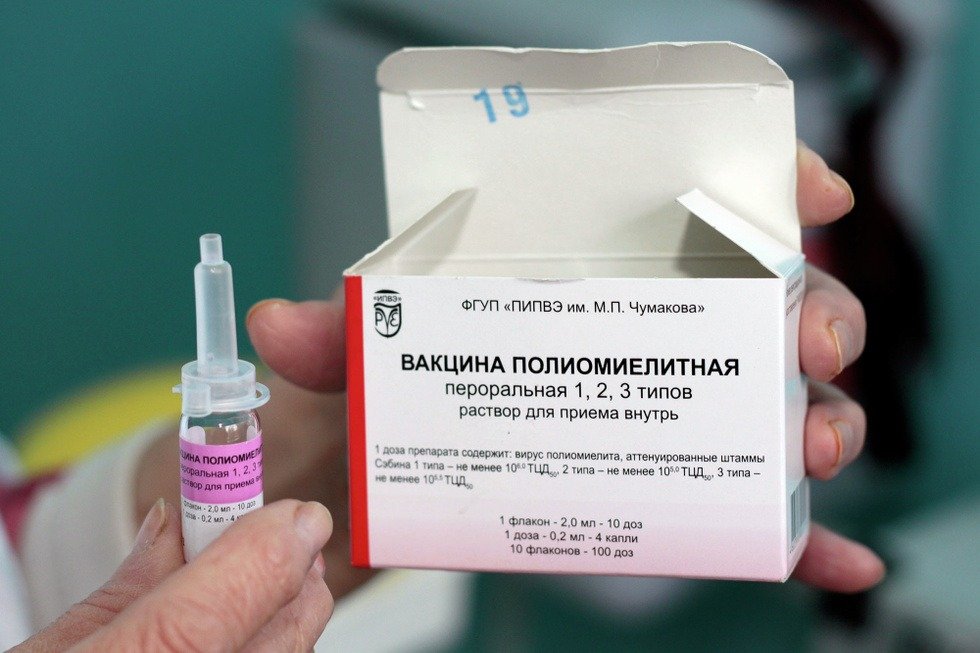 , van Nunen F., Abbink F., Kimman T.G., Buisman A.M. Детерминанты мутагенеза моновалентной оральной полиомиелитной вакцины у привитых пожилых людей. вакцина. 2007; 25:4706–4714. [PubMed] [Google Scholar]
, van Nunen F., Abbink F., Kimman T.G., Buisman A.M. Детерминанты мутагенеза моновалентной оральной полиомиелитной вакцины у привитых пожилых людей. вакцина. 2007; 25:4706–4714. [PubMed] [Google Scholar]
Bull J.J., Smithson M.W., Nuismer S.L. Трансмиссивные вирусные вакцины. Тенденции микробиол. 2018;26:6–15. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Бернс К.С., Диоп О.М., Саттер Р.В., Кью О.М. Полиовирусы вакцинного происхождения. Дж. Заразить. Дис. 2014;210(Приложение 1):S283–S293. [PubMed] [Google Scholar]
Burns C.C., Shaw J., Jorba J., Bukbuk D., Adu F., Gumede N., Pate M.A., Abanida EA, Gasasira A., Iber J. Множественные независимые появления полиовирусов вакцинного происхождения типа 2 во время крупной вспышки в Северной Нигерии. Дж. Вирол. 2013; 87: 4907–4922. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Деббинк К., Маккроун Дж.Т., Петри Дж.Г., Траскон Р., Джонсон Э., Мантло Э.К., Монто А.С., Лауринг А.С. Вакцинация оказывает минимальное влияние на внутрихозяинное разнообразие вирусов гриппа h4N2. PLoS Патог. 2017;13:e1006194. [Бесплатная статья PMC] [PubMed] [Google Scholar]
PLoS Патог. 2017;13:e1006194. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Дедепсидис Э., Каракасилиотис И., Паксимади Э., Кириакопулоу З., Комиотис Д., Маркулатос П. Обнаружение необычной мутации в области VP1 разного происхождения. -изоляты полиовируса вакцины Сэбина. Гены вирусов. 2006; 33: 183–191. [PubMed] [Google Scholar]
Dinis J.M., Florek N.W., Fatola O.O., Moncla L.H., Mutschler J.P., Charlier O.K., Meece J.K., Belongia EA, Friedrich T.C. Глубокое секвенирование выявляет потенциальные антигенные варианты с низкой частотой у людей, инфицированных вирусом гриппа А. Дж. Вирол. 2016;90:3355–3365. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Долан П.Т., Уитфилд З.Дж., Андино Р. Механизмы и концепции динамики и эволюции популяции РНК-вируса. Анну. Преподобный Вирол. 2018;5:69–92. [PubMed] [Google Scholar]
Долан П.Т., Уитфилд З.Дж., Андино Р. Картирование эволюционного потенциала РНК-вирусов. Клеточный микроб-хозяин. 2018;23:435–446. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Duintjer Tebbens RJD, Pallansch M. A., Kim JH, Burns C.C., Kew O.M., Oberste M.S., Diop O.M., Wassilak S.G.F., Cochi S.L., Thompson K.M. Эволюция оральной полиовирусной вакцины и идеи, относящиеся к моделированию рисков, связанных с циркулирующими полиовирусами вакцинного происхождения (цПВВП) Risk Anal. 2013; 33: 680–702. [Бесплатная статья PMC] [PubMed] [Google Scholar]
A., Kim JH, Burns C.C., Kew O.M., Oberste M.S., Diop O.M., Wassilak S.G.F., Cochi S.L., Thompson K.M. Эволюция оральной полиовирусной вакцины и идеи, относящиеся к моделированию рисков, связанных с циркулирующими полиовирусами вакцинного происхождения (цПВВП) Risk Anal. 2013; 33: 680–702. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Эдгар Р.К. MUSCLE: множественное выравнивание последовательностей с высокой точностью и высокой пропускной способностью. Нуклеиновые Кислоты Res. 2004; 32: 1792–1797. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Елена С.Ф., Санхуан Р., Бордерия А.В., Тернер П.Е. Узкие места передачи и эволюция приспособленности быстро развивающихся РНК-вирусов. Заразить. Жене. Эвол. 2001; 1:41–48. [PubMed] [Google Scholar]
Famulare M., Chang S., Iber J., Zhao K., Adeniji J.A., Bukbuk D., Baba M., Behrend M., Burns C.C., Oberste M.S. Реверсия вакцины Сэбина в полевых условиях: всесторонний анализ изолятов полиовируса, подобного Сэбину, в Нигерии. Дж. Вирол. 2016;90: 317–331. [Статья бесплатно PMC] [PubMed] [Google Scholar]
Дж. Вирол. 2016;90: 317–331. [Статья бесплатно PMC] [PubMed] [Google Scholar]
Famulare M., Selinger C., McCarthy K.A., Eckhoff P.A., Chabot-Couture G. Оценка стабильности ликвидации полиомиелита после отмены оральной вакцины против полиомиелита. PLoS биол. 2018;16:e2002468. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Фитцсиммонс В.Дж., Вудс Р.Дж., Маккроун Дж.Т., Вудман А., Арнольд Дж.Дж., Йеннавар М., Эванс Р., Кэмерон К.Е., Лоринг А.С. Компромисс между скоростью и точностью определяет скорость мутаций и вирулентность РНК-вируса. PLoS биол. 2018;16:e2006459. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Геогеган Дж. Л., Холмс Э. К. Эволюционная вирусология в 40 лет. Генетика. 2018;210:1151–1162. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Герстунг М., Байзель К., Рехштайнер М., Уайлд П., Шрамл П., Мох Х., Беренвинкель Н. Надежное обнаружение субклональных однонуклеотидных вариантов в популяции опухолевых клеток. Нац. коммун. 2012;3:811. [PubMed] [Google Scholar]
[PubMed] [Google Scholar]
Грубо Н.Д., Гангаварапу К., Квик Дж., Маттесон Н.Л., Де Хесус Дж.Г., Мейн Б.Дж., Тан А.Л., Пол Л.М., Брэкни Д.Е., Гревал С. Основанная на ампликоне система секвенирования для точного измерение разнообразия вирусов внутри хозяина с использованием PrimalSeq и iVar. Геном биол. 2019;20:8. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Гутьеррес Б., Эскалера-Замудио М., Пибус О.Г. Параллельная молекулярная эволюция и адаптация у вирусов. Курс. мнение Вирол. 2019;34:90–96. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Холубар М., Саху М.К., Хуанг С., Мохамед-Хадли А., Лю Ю., Вагонер Дж.Дж., Трой С.Б., Гарсия-Гарсия Л., Феррейра-Рейес Л., Мальдонадо Ю. Глубокое секвенирование требует модификации ОТ-ПЦР в реальном времени для серотип-специфического обнаружения полиовирусов. Дж. Вирол. Методы. 2019;264:38–43. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Дженкинс Х.Е., Эйлуорд Р.Б., Гасасира А., Доннелли К.А., Мванза М., Корандер Дж. , Гарнье С., Шовин С., Абанида Э., Пейт М.А. циркулирующего полиовируса вакцинного происхождения в Нигерии. Н. англ. Дж. Мед. 2010; 362:2360–2369. [PubMed] [Google Scholar]
, Гарнье С., Шовин С., Абанида Э., Пейт М.А. циркулирующего полиовируса вакцинного происхождения в Нигерии. Н. англ. Дж. Мед. 2010; 362:2360–2369. [PubMed] [Google Scholar]
Джорба Дж., Кампаньоли Р., Де Л., Кью О. Калибровка нескольких молекулярных часов полиовируса, охватывающих расширенный эволюционный диапазон. Дж. Вирол. 2008; 82: 4429–4440. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Karlsson Hedestam G.B.K., Fouchier R.A.M., Phogat S., Burton D.R., Sodroski J., Wyatt R.T. Проблемы выявления нейтрализующих антител к ВИЧ-1 и к вирусу гриппа. Нац. Преподобный Микробиолог. 2008; 6: 143–155. [PubMed] [Google Scholar]
Кью О., Моррис-Глазго В., Ландаверде М., Бернс С., Шоу Дж., Гариб З., Андре Дж., Блэкман Э., Фриман С.Дж., Джорба Дж. Вспышка полиомиелита в Эспаньоле, связанного с циркулирующим полиовирусом вакцинного происхождения типа 1. Наука. 2002; 296: 356–359.. [PubMed] [Google Scholar]
Кью О., Палланш М. Разрыв последних цепочек передачи полиовируса: прогресс и проблемы в глобальной ликвидации полиомиелита. Анну. Преподобный Вирол. 2018;5:427–451. [PubMed] [Google Scholar]
Анну. Преподобный Вирол. 2018;5:427–451. [PubMed] [Google Scholar]
Кью О.М., Саттер Р.В., де Гурвилль Э.М., Даудл В.Р., Палланш М.А. Полиовирусы вакцинного происхождения и стратегия завершения глобальной ликвидации полиомиелита. Анну. Преподобный Микробиолог. 2005; 59: 587–635. [PubMed] [Google Scholar]
Килпатрик Д.Р., Ибер Дж.К., Чен К., Чинг К., Ян С.Дж., Де Л., Мандельбаум М.Д., Эмери Б., Кампаньоли Р., Бернс К.С. Праймеры для секвенирования VP1, специфичные для серотипа полиовируса. Дж. Вирол. Методы. 2011; 174:128–130. [PubMed] [Академия Google]
Konopka-Anstadt J.L., Campagnoli R., Vincent A., Shaw J., Wei L., Wynn N.T., Smithee S.E., Bujaki E., Te Yeh M., Laassri M. Разработка новой пероральной полиовирусной вакцины для конец игры эрадикации с помощью деоптимизации кодонов. Вакцины NPJ. 2020;5:26. [PMC free article] [PubMed] [Google Scholar]
Кряжимский С., Плоткин Ю.Б. Популяционная генетика dN/dS. Генетика PLoS. 2008;4:e1000304. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Langmead B.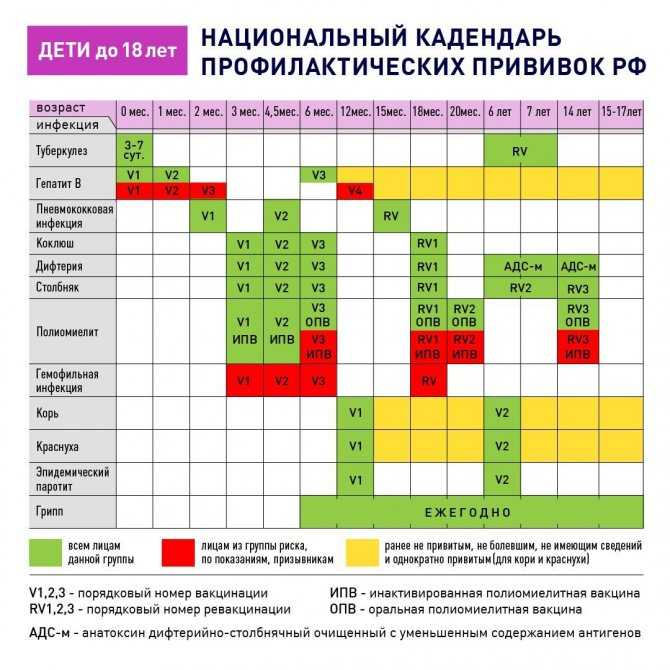 , Salzberg S.L. Быстрое выравнивание с промежутками чтения с Bowtie 2. Nat. Методы. 2012;9: 357–359. [Бесплатная статья PMC] [PubMed] [Google Scholar]
, Salzberg S.L. Быстрое выравнивание с промежутками чтения с Bowtie 2. Nat. Методы. 2012;9: 357–359. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Lauring A.S. Вирусное разнообразие внутри хозяина: окно в вирусную эволюцию. Анну. Преподобный Вирол. 2020; 7: 63–81. [PubMed] [Google Scholar]
Леким С., Фонтейн А., Ар Гуй М., Молтини-Конклуа И., Ламбрехтс Л. Генетический дрейф, очищающий отбор и генотип вектора формируют генетическое разнообразие вируса денге внутри хозяина у комаров. Генетика PLoS. 2016;12:e1006111. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Левек Н., Семлер Б.Л. Перспектива репликации полиовируса в 21 веке. PLoS Патог. 2015;11:e1004825. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Ли Х., Хэндсакер Б., Вайсокер А., Феннелл Т., Руан Дж., Гомер Н., Март Г., Абекасис Г., Дурбин Р., Подгруппа обработки данных проекта 1000 Genome Выравнивание последовательностей/формат карты и SAMTools. Биоинформатика. 2009;25:2078–2079. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Макадам А.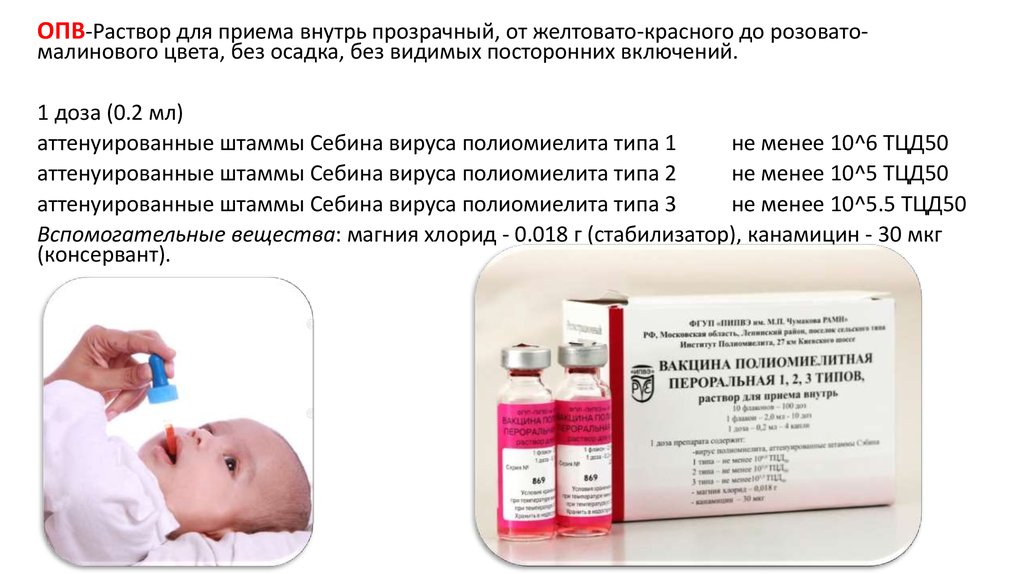 Дж., Поллард С.Р., Фергюсон Г., Данн Г., Скьюс Р., Алмонд Дж.В., Майнор П.Д. 5′-некодирующая область вакцинного штамма полиовируса 2 содержит детерминанты аттенуации и температурной чувствительности. Вирусология. 1991;181:451–458. [PubMed] [Google Scholar]
Дж., Поллард С.Р., Фергюсон Г., Данн Г., Скьюс Р., Алмонд Дж.В., Майнор П.Д. 5′-некодирующая область вакцинного штамма полиовируса 2 содержит детерминанты аттенуации и температурной чувствительности. Вирусология. 1991;181:451–458. [PubMed] [Google Scholar]
Макадам А.Дж., Поллард С.Р., Фергюсон Г., Скуче Р., Вуд Д., Алмонд Дж.В., Майнор П.Д. Генетическая основа аттенуации вакцинного штамма полиовируса Сэбина типа 2 у приматов. Вирусология. 1993; 192:18–26. [PubMed] [Google Scholar]
Маклин Г.Р., О’Рейли К.М., Грассли Н.К., Эдмундс В.Дж., Мах О., Кришнан Р.С.Г., Вурман А., Вертефей Дж.Ф., Абдельвахаб Дж., Гумеде Н. Эволюция эпидемиологии полиовируса серотипа 2 после отмены оральной вакцины против полиомиелита 2 типа. Наука. 2020; 368: 401–405. [PubMed] [Академия Google]
Мартин М. Cutadapt удаляет последовательности адаптера из высокопроизводительных считываний секвенирования. EMBnet J. 2011; 17:10–12. [Google Scholar]
McCrone J.T., Lauring A.S. Измерения внутрихозяинного вирусного разнообразия чрезвычайно чувствительны к систематическим ошибкам в определении вариантов. Дж. Вирол. 2016;90:6884–6895. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Дж. Вирол. 2016;90:6884–6895. [Бесплатная статья PMC] [PubMed] [Google Scholar]
McCrone J.T., Woods R.J., Martin E.T., Malosh R.E., Monto A.S., Lauring A.S. Стохастические процессы ограничивают эволюцию вируса гриппа внутри и между хозяевами. электронная жизнь. 2018;7:e35962. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Montmayeur A.M., Ng T.F.F., Schmidt A., Zhao K., Magaña L., Iber J., Castro C.J., Chen Q., Henderson E., Ramos E. Высокопроизводительное секвенирование полиовирусов нового поколения. Дж. Клин. микробиол. 2017;55:606–615. [PMC free article] [PubMed] [Google Scholar]
Музыченко А.Р., Липская ГЮ Г.Ю., Маслова С.В., Свиткин Ю.В., Пилипенко Е.В., Ноттай Б.К., Кью О.М., Агол В.И. Связанные мутации в 5′-нетранслируемой области штаммов полиовируса Сэбина во время пассажей in vivo: структурные и функциональные последствия. Вирус рез. 1991;21:111–122. [PubMed] [Google Scholar]
Неверов А., Чумаков К. Массивно-параллельное секвенирование для мониторинга генетической согласованности и контроля качества живых вирусных вакцин. проц. Натл. акад. науч. США. 2010;107:20063–20068. [Бесплатная статья PMC] [PubMed] [Google Scholar]
проц. Натл. акад. науч. США. 2010;107:20063–20068. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Парамесваран П., Шарлебуа П., Теллез Ю., Нуньес А., Райан Э.М., Мальбеф С.М., Левин Дж.З., Леннон Н.Дж., Бальмаседа А., Харрис Э. Геном Широкие паттерны внутричеловеческого разнообразия вируса денге обнаруживают связи с вирусной филогенетической кладой и межхозяинным разнообразием. Дж. Вирол. 2012; 86: 8546–8558. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Патель В., Фергюсон М., Майнор П.Д. Антигенные сайты полиовируса 2 типа. Вирусология. 1993; 192: 361–364. [PubMed] [Google Scholar]
Понс-Салорт М., Молодецки Н.А., О’Рейли К.М., Вадуд М.З., Сафдар Р.М., Этсано А., Ваз Р.Г., Джафари Х., Грассли Н.К., Блейк И.М. Популяционный иммунитет против серотипа- 2 полиомиелит, приведший к глобальному отказу от пероральной вакцины против полиомиелита: пространственно-временное моделирование данных эпиднадзора. ПЛОС Мед. 2016;13:e1002140. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Рен Р. Б., Мосс Э.Г., Раканиелло В.Р. Идентификация двух детерминант, которые ослабляют вакцинородственный полиовирус 2 типа. Дж. Вирол. 1991; 65: 1377–1382. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Б., Мосс Э.Г., Раканиелло В.Р. Идентификация двух детерминант, которые ослабляют вакцинородственный полиовирус 2 типа. Дж. Вирол. 1991; 65: 1377–1382. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Robinson C.M., Jesudhasan P.R., Pfeiffer J.K. Связывание бактериального липополисахарида повышает стабильность вириона и способствует адаптации кишечного вируса к окружающей среде. Клеточный микроб-хозяин. 2014;15:36–46. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Sahoo M.K., Holubar M., Huang C., Mohamed-Hadley A., Liu Y., Wagoner J.J., Troy SB, Garcia-Garcia L., Ferreyra-Reyes Л., Мальдонадо Ю. Обнаружение новых полиовирусов, связанных с вакцинами, путем глубокого секвенирования. Дж. Клин. микробиол. 2017;55:2162–2171. [Бесплатная статья PMC] [PubMed] [Google Scholar]
van der Sanden S., Pallansch M.A., van de Kassteele J., El-Sayed N., Sutter R.W., Koopmans M., van der Avoort H. Выделение вакцинных вирусов с повышенной антигенной и генетической дивергенцией после вакцинации новорожденных с моновалентная пероральная вакцина против полиомиелита 1 типа.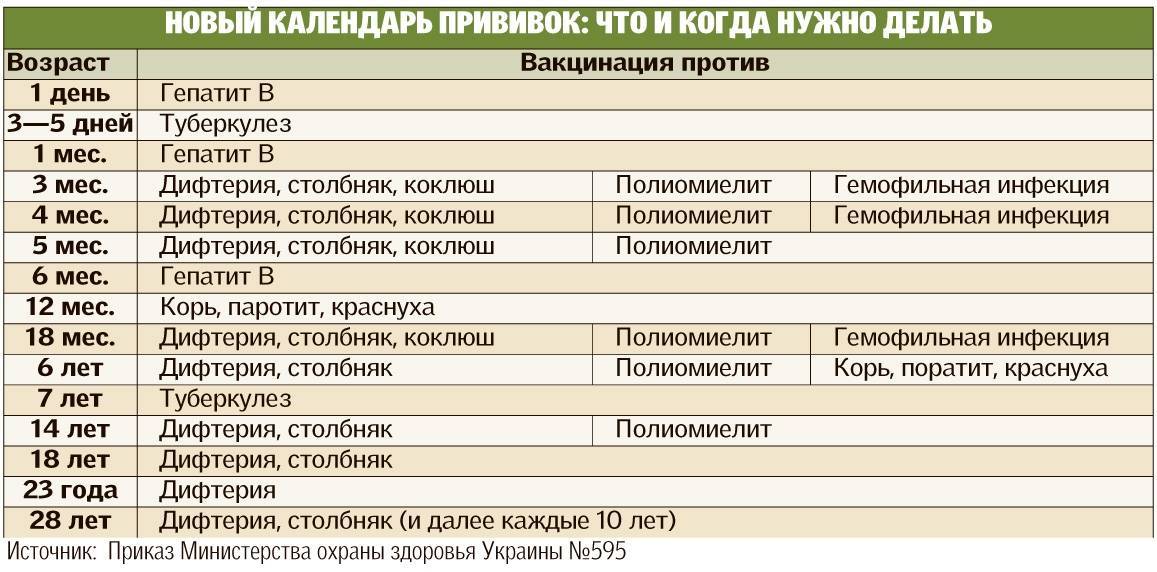 Дж. Вирол. 2009; 83: 8693–8704. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Дж. Вирол. 2009; 83: 8693–8704. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Санхуан Р., Небот М.Р., Кирико Н., Мански Л.М., Белшоу Р. Скорость вирусных мутаций. Дж. Вирол. 2010; 84: 9733–9748. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Сарси Э., Серрес А., Тинди Ф., Шарейр А., Нг С., Николя М., Веттер Э., Бонневей Т., Абачин Э., Маллет Л. Количественное определение низкочастотных ревертантов в пероральной полиовирусной вакцине с использованием секвенирования следующего поколения. Дж. Вирол. Методы. 2017; 246:75–80. [PubMed] [Google Scholar]
Шоу Дж., Джорба Дж., Чжао К., Ибер Дж., Чен К., Аду Ф., Адениджи А., Букбук Д., Баба М., Хендерсон Э. Динамика эволюция полиовирусных нейтрализующих антигенных участков и других функциональных доменов капсида во время крупной и продолжительной вспышки. Дж. Вирол. 2018;92:e01949-17. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Собель Леонард А.С., Вайсман Д.Б., Гринбаум Б., Гедин Э., Кёлле К. Оценка размера узкого места передачи на основе данных глубокого секвенирования патогенов с применением к человеческому гриппу А вирус. Дж. Вирол. 2017;91:e00171-17. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Дж. Вирол. 2017;91:e00171-17. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Стерн А., Йе М.Т., Зингер Т., Смит М., Райт К., Линг Г., Нильсен Р., Макадам А., Андино Р. Эволюционная путь к вирулентности РНК-вируса. Клетка. 2017;169: 35–46.e19. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Танючи М., Фамуларе М., Заман К., Уддин М.Дж., Апфилл-Браун А.М., Ахмед Т., Саха П., Хак Р., Бандйопадхьяй А.С., Модлин J.F. Передача полиовируса типа 2 в сообществе после прекращения применения трехвалентной оральной вакцины против полиомиелита в Бангладеш: открытое кластерное рандомизированное исследование и модельное исследование. Ланцет Инфекция. Дис. 2017;17:1069–1079. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Валесано А.Л., Фитцсиммонс В.Дж., Маккроун Дж.Т., Петри Дж.Г., Монто А.С., Мартин Э.Т., Лауринг А.С. Вирусы гриппа В демонстрируют более низкое разнообразие внутри хозяина, чем вирусы гриппа А в организме человека. Дж. Вирол. 2020;94:e01710–e01719. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Wassilak S.

 5 ст. 2 Закона от 21.11.2011 N 323-ФЗ; ст. 1 Закона от 17.09.1998 N 157-ФЗ).
5 ст. 2 Закона от 21.11.2011 N 323-ФЗ; ст. 1 Закона от 17.09.1998 N 157-ФЗ).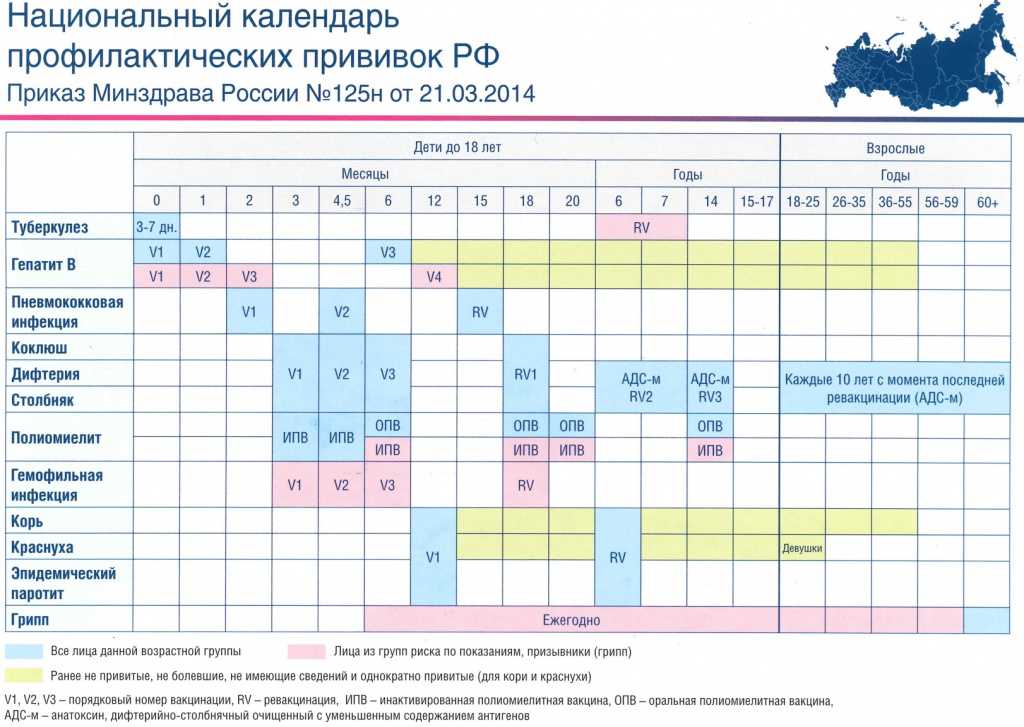
 е. если такой угрозы нет, оформить ребенка в образовательное учреждение возможно при отсутствии прививок). При этом дети, не прошедшие туберкулинодиагностику, допускаются в детские учреждения только при наличии заключения врача-фтизиатра об отсутствии заболевания;
е. если такой угрозы нет, оформить ребенка в образовательное учреждение возможно при отсутствии прививок). При этом дети, не прошедшие туберкулинодиагностику, допускаются в детские учреждения только при наличии заключения врача-фтизиатра об отсутствии заболевания;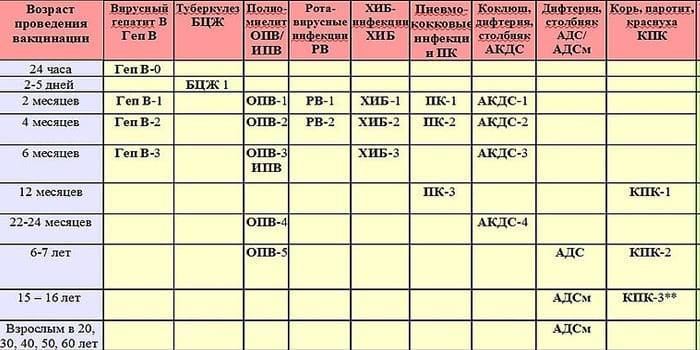 9 ч. 3 ст. 1, ч. 5 ст. 23, ст. 285.1 КАС РФ).
9 ч. 3 ст. 1, ч. 5 ст. 23, ст. 285.1 КАС РФ). п. 1 и 2, не имеют
п. 1 и 2, не имеют 2 МУ 3.3.1.1095-02).
2 МУ 3.3.1.1095-02).