Содержание
Пентаксим — профилактика дифтерии | Медицинский центр Доверие
Вакцина для профилактики дифтерии и столбняка адсорбированная, коклюша ацеллюлярная, полиомиелита инактивированная, инфекции, вызываемой Haemophilusinfluenzae тип b конъюгированная.
О составе: содержит антигены дифтерийного и столбнячного анатоксина, компоненты клеточной стенки возбудителя коклюша, инактивированный вирус полиомиелита 1,2,3 типов и капсульные полисахариды гемофильной палочки тип b. В отличие от цельноклеточных вакцин (АКДС) такой способ производства позволяет значительно снизить реактогенность вакцины Пентаксим®. Одним уколом иммунизирует ребенка против коклюша, дифтерии, столбняка, полиомиелита. И заболеваний, вызываемых гемофильной палочкой (менингит, септицемия, пневмония, эпиглотит и др.). Производитель: SANOFI PASTEUR, S.A., Франция.
Показания к применению:
Рекомендована для профилактики коклюша, дифтерии и столбняка, полиомиелита, инвазивной инфекции, вызываемой Haemophilus influenzae тип b у детей от 3-х месяцев до 3 лет 11 месяцев 29 дней.
Допускается вакцинация и ревакцинация детей, которые ранее были иммунизированы несколькими дозами бесклеточной или цельноклеточной коклюшно-дифтерийно-столбнячной вакцины. При условии продолжающейся вакцинации или ревакцинации от полиомиелита.
Совместимость с другими вакцинами: совместима со всеми препаратами из национального календаря профилактических прививок в один день, в разные участки тела, кроме вакцины БЦЖ. Пентаксим® можно применять для продолжения и завершения курса вакцинации, начатого другими вакцинами против коклюша, дифтерии, столбняка, полиомиелита и гемофильной инфекции. Все вакцины национального календаря прививок России взаимозаменяемы.
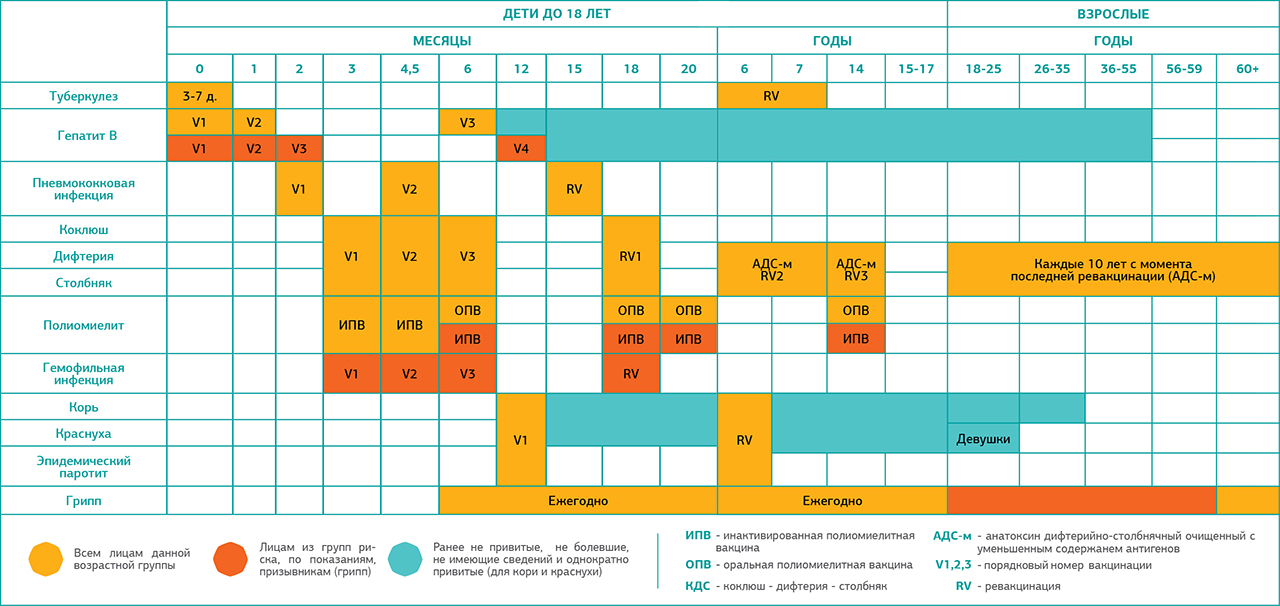
Схема вакцинации: состоит из 3 вакцинаций – в 3, 4,5 и 6 месяцев жизни. Ревакцинацию проводят в 18 месяцев. Допускается индивидуальная схема иммунизации. Важно соблюдать сроки вакцинации. Если прошло больше времени, то заново вакцинацию не возобновляют. Гемофильный компонент вакцины Пентаксим® для детей старше года вводится однократно.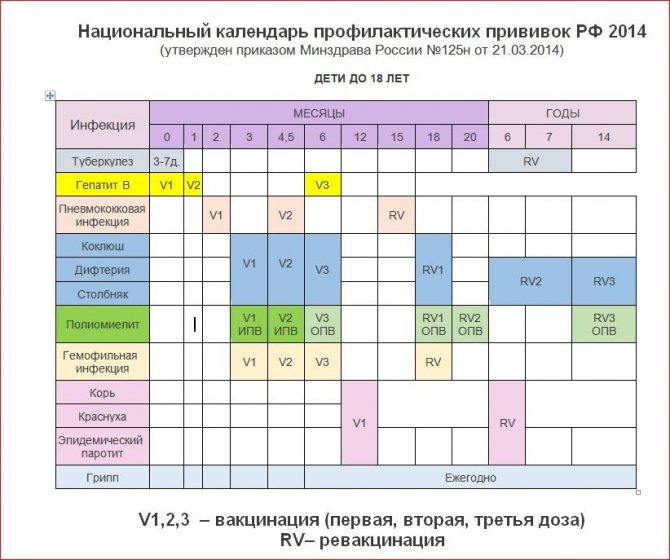 Поэтому, как только ребенку старше года проводится инъекция вакцины Пентаксим® с гемофильным компонентом, то она является последней для иммунизации от гемофильной инфекции. Дальнейшая профилактика дифтерии, коклюша, столбняка и полиомиелита вакциной Пентаксим® у ребенка старше года проводится без гемофильного компонента.
Поэтому, как только ребенку старше года проводится инъекция вакцины Пентаксим® с гемофильным компонентом, то она является последней для иммунизации от гемофильной инфекции. Дальнейшая профилактика дифтерии, коклюша, столбняка и полиомиелита вакциной Пентаксим® у ребенка старше года проводится без гемофильного компонента.
Перед вакцинацией обязателен осмотр педиатра и сдача анализов крови и мочи. Вакцинация проводится только здоровым детям. Пентаксим® не формирует иммунитета против инфекции, вызываемой другими серотипами Haemophilus influenzae. А также против менингитов и пневмоний иной этиологии.
Вводится внутримышечно. У детей раннего возраста в четырехглавую мышцу бедра (средняя треть бедра). У детей старше в дельтовидную мышцу (плечо). Допустимо подкожное введение. Внутривенное введение противопоказано.
Противопоказания:
- прогрессирующая энцефалопатия, сопровождающаяся судорогами или без таковых; энцефалопатия, развившаяся в течение 7 дней после введения любой вакцины, содержащей антигены Bordetella pertussis;
- сильная реакция в течение 48 ч после предыдущей вакцинации вакциной, содержащей коклюшный компонент;
- аллергическая реакция, развившаяся после предыдущего введения вакцины
- для профилактики дифтерии, столбняка, коклюша, полиомиелита и вакцины для профилактики инфекции, вызываемой Haemophilus influenzae типа b
- подтвержденная системная реакция гиперчувствительности к любому ингредиенту вакцины.
 А также глютаральдегиду, неомицину, стрептомицину и полимиксину В;
А также глютаральдегиду, неомицину, стрептомицину и полимиксину В; - заболевания, сопровождающиеся повышением температуры тела, острые проявления инфекционного заболевания или обострение хронического заболевания.
Вместе или раздельно: – вакарта
Прививки – вводить вместе или раздельно
Выбранные вакцины:
с рождения
+
с рождения
+
с рождения
Выбрать заново
Варианты сочетания выбранных вакцин
Можно ли вводить их в один и тот же день?
Да, можно
Можно вводить в тот же день в разные участки тела.
Выбранные вакцины содержат компоненты против одинакового заболевания. Проверьте, нет ли ошибки в выборе вакцин.
Сколько ждать, если вводить в разные дни?
Можно в любой другой день
Не нужно ждать какое-то определенное количество дней от одной прививки, чтобы привиться другой.
Следующую прививку можно вводить в любой день, хоть на следующий день.
Вместе с уже выбранными вакцинами можно сочетать еще – выберите вакцину
+ H-B-Вакс-II+ HB-Вакс Про+ Аваксим-160+ Аваксим-80+ Адасель+ Адасель Полио+ АДС Биолик+ АДС-м Биолик+ АДС-м Индия+ АКДС Биолик+ АКДС Индия+ АктХиб+ Альгавак+ Амбирикс+ Афлуриа Квадривалент+ Бексеро+ Бивак Полио+ Бубо-Кок+ Бустрикс+ Бустрикс Полио+ БЦЖ SSI Дания+ БЦЖ USP+ БЦЖ Болгария+ БЦЖ Индия+ БЦЖ Польша+ Вакселис+ Ваксигрипп+ Ваксигрипп Тетра+ Вакта+ Варивакс+ Варилрикс+ Верораб+ Вианвак+ Виваксим+ Гардасил+ Гардасил 9+ Гексаксим+ Гексион+ Гепатирикс+ Гриппол Плюс+ Даптасель+ ДжиСи Флю+ ДжиСи Флю Квадривалент+ Дифтет ДТ+ Зоставакс+ Иксиаро+ Имовакс Полио+ Имовакс Рабиес+ Индираб+ Инфанрикс+ Инфанрикс Гекса+ Инфанрикс ИПВ+ Инфанрикс ИПВ Hib+ Инфанрикс Пента+ Инфлувак+ Инфлувак Тетра+ Инфлусплит Тетра+ Ипол+ ИФ-Вакс+ Квадрасель+ Кинрикс+ Клещ-Э-вак+ Коваксис+ Менактра+ Менвео+ Мениторикс+ ММР-II+ ММР ВаксПро+ НеисВак-C+ Нименрикс+ ПедваксХиб+ Педиарикс+ Пентабио+ Пентавак+ Пентаксим+ Пентасель+ Пента Хиб+ Пневмовакс 23+ Полимилекс+ Полиовакцина SSI+ Полио Сабин+ Превенар-13+ Приорикс+ Приорикс Тетра+ ПроКвад+ РабАверт+ Рабипур+ Регевак-B+ Рекомбивакс HB+ Репевакс+ Ротавак+ Ротарикс+ РотаТек+ Синфлорикс+ Совигрипп+ Стамарил+ Твинрикс+ Тенивак+ Тетраксим+ ТикоВак Джуниор (ФСМЕ-Иммун детская)+ ТикоВак (ФСМЕ-Иммун)+ Тифим ВИ+ Триаксис+ Тримовакс+ Труменба+ Ультрикс Квадри+ Фендрикс+ Флуад+ Флуарикс Тетра (Квадри)+ Флюблок Квадривалент+ Флюенц Тетра+ Флюзон Квадривалент+ ФлюЛаваль Квадривалент+ Флю-М+ ФлюМист Квадривалент+ Флю-М Тетра+ Флюсельвакс Квадривалент+ Хаврикс-1440+ Хаврикс-720+ Хиберикс+ Церварикс+ Шингрикс+ Энджерикс-B взрослый+ Энджерикс-B детский+ Энцевир+ Энцепур+ Энцепур детский+ Эувакс-B
Горизонтальный список вакцин прокручивается вправо-влево сенсорно или колесиком мыши.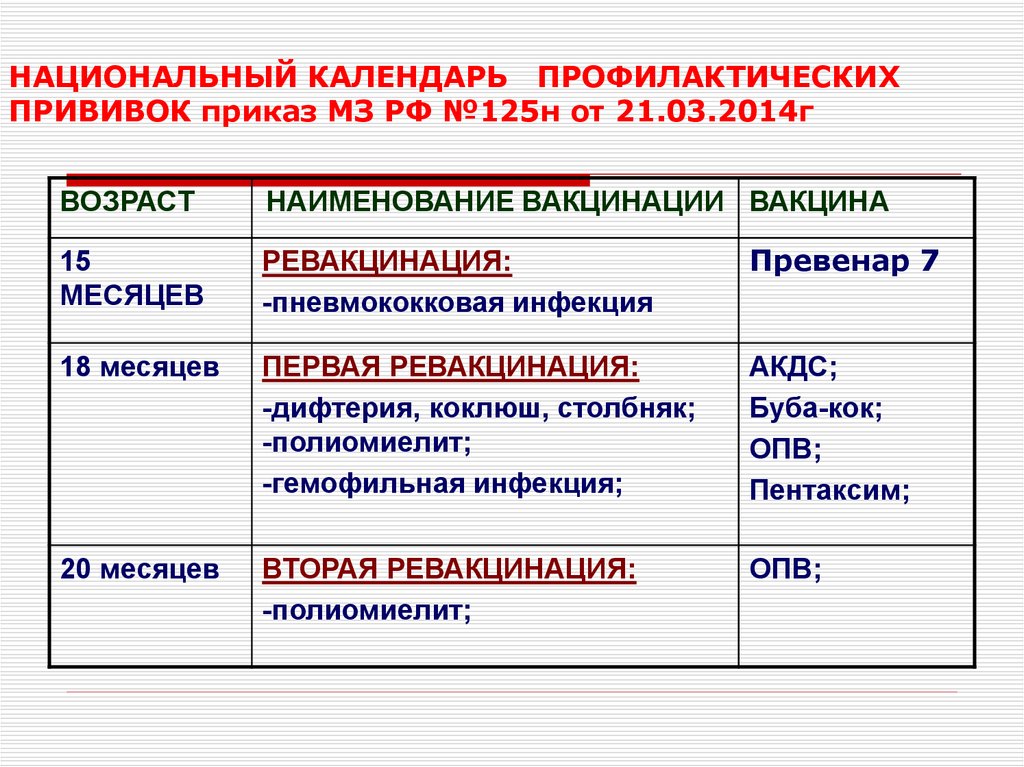
Вакцинация – это просто.
Заведите личный календарь прививок
Защита вашей семьи – в ваших руках.
Вакарта – вакцинальная карта
Индивидуальный ГРАФИК прививок онлайн
Учетная запись регистрируется на ваше имя. После регистрации можно добавлять других членов семьи.
Ваши имя и фамилия:
Ваша дата рождения:
12345678910111213141516171819202122232425262728293031
январяфевралямартаапрелямаяиюняиюляавгустасентябряоктябряноябрядекабря
202220212020201920182017201620152014201320122011201020092008200720062005200420032002200120001999199819971996199519941993199219911990198919881987198619851984198319821981198019791978197719761975197419731972197119701969196819671966196519641963196219611960195919581957195619551954195319521951195019491948194719461945194419431942194119401939193819371936193519341933193219311930192919281927192619251924192319221921192019191918191719161915191419131912191119101909190819071906190519041903190219011900
Страна вашего календаря прививок:
— укажите —AfghanistanÅland IslandsAlbaniaAlgeriaAmerican SamoaAndorraAngolaAnguillaAntarcticaAntigua and BarbudaArgentina⚑ ArmeniaAruba⚑ AustraliaAustria⚑ AzerbaijanBahamasBahrainBangladeshBarbados⚑ BelarusBelgiumBelizeBeninBermudaBhutanBolivia, Plurinational State ofBonaire, Sint Eustatius and SabaBosnia and HerzegovinaBotswanaBouvet IslandBrazilBritish Indian Ocean TerritoryBrunei DarussalamBulgariaBurkina FasoBurundiCambodiaCameroonCanadaCape VerdeCayman IslandsCentral African RepublicChadChileChinaChristmas IslandCocos (Keeling) IslandsColombiaComorosCongoCongo, the Democratic Republic of theCook IslandsCosta RicaCôte d’IvoireCroatiaCubaCuraçaoCyprusCzech Republic⚑ DenmarkDjiboutiDominicaDominican RepublicEcuadorEgyptEl SalvadorEquatorial GuineaEritrea⚑ EstoniaEthiopiaFalkland Islands (Malvinas)Faroe IslandsFiji⚑ Finland⚑ FranceFrench GuianaFrench PolynesiaFrench Southern TerritoriesGabonGambia⚑ Georgia⚑ GermanyGhanaGibraltarGreeceGreenlandGrenadaGuadeloupeGuamGuatemalaGuernseyGuineaGuinea-BissauGuyanaHaitiHeard Island and McDonald IslandsHoly See (Vatican City State)HondurasHong KongHungaryIceland⚑ IndiaIndonesiaIran, Islamic Republic ofIraq⚑ IrelandIsle of Man⚑ IsraelItalyJamaicaJapanJerseyJordan⚑ KazakhstanKenyaKiribatiKorea, Democratic People’s Republic ofKorea, Republic ofKuwait⚑ KyrgyzstanLao People’s Democratic Republic⚑ LatviaLebanonLesothoLiberiaLibyaLiechtenstein⚑ LithuaniaLuxembourgMacaoMacedonia, the former Yugoslav Republic ofMadagascarMalawiMalaysiaMaldivesMaliMaltaMarshall IslandsMartiniqueMauritaniaMauritiusMayotteMexicoMicronesia, Federated States of⚑ Moldova, Republic ofMonacoMongoliaMontenegroMontserratMoroccoMozambiqueMyanmarNamibiaNauruNepalNetherlandsNew Caledonia⚑ New ZealandNicaraguaNiger⚑ NigeriaNiueNorfolk IslandNorthern Mariana Islands⚑ NorwayOmanPakistanPalauPalestinian Territory, OccupiedPanamaPapua New GuineaParaguayPeruPhilippinesPitcairn⚑ PolandPortugalPuerto RicoQatarRéunionRomania⚑ Russian FederationRwandaSaint BarthélemySaint Helena, Ascension and Tristan da CunhaSaint Kitts and NevisSaint LuciaSaint Martin (French part)Saint Pierre and MiquelonSaint Vincent and the GrenadinesSamoaSan MarinoSao Tome and PrincipeSaudi ArabiaSenegalSerbiaSeychellesSierra LeoneSingaporeSint Maarten (Dutch part)SlovakiaSloveniaSolomon IslandsSomalia⚑ South AfricaSouth Georgia and the South Sandwich IslandsSouth SudanSpainSri LankaSudanSurinameSvalbard and Jan MayenSwaziland⚑ SwedenSwitzerlandSyrian Arab RepublicTaiwan, Province of ChinaTajikistanTanzania, United Republic ofThailandTimor-LesteTogoTokelauTongaTrinidad and TobagoTunisia⚑ TurkeyTurkmenistanTurks and Caicos IslandsTuvaluUganda⚑ Ukraine⚑ United Arab Emirates⚑ United Kingdom⚑ United StatesUnited States Minor Outlying IslandsUruguay⚑ UzbekistanVanuatuVenezuela, Bolivarian Republic ofViet NamVirgin Islands, BritishVirgin Islands, U.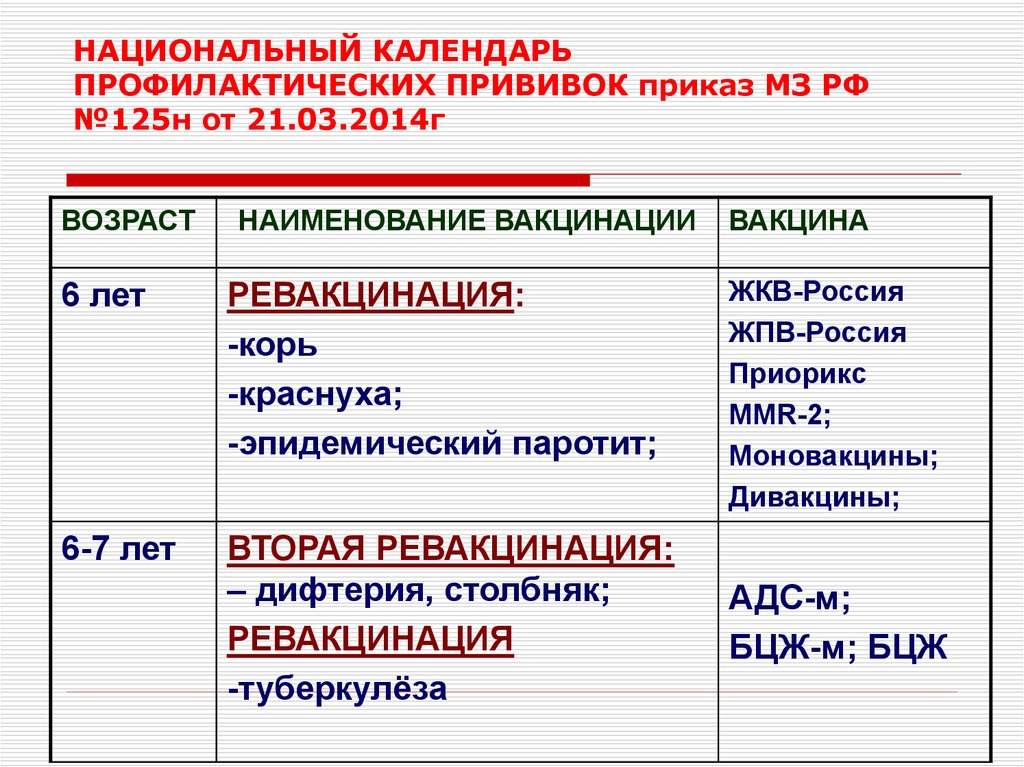 S.Wallis and FutunaWestern SaharaYemenZambiaZimbabwe
S.Wallis and FutunaWestern SaharaYemenZambiaZimbabwe
Далее
Ваш пол:
муж.жен.
Ваш e-mail:
Ваш пароль:
Промокод, если есть:
Подтвердите, что вы человек, а не бот:
Подтвердить согласие с Политикой конфиденциальности и защиты персональных данных
Регистрация возможна только при согласии с указанными условиями конфиденциальности
Вам будет отправлен емейл для подтверждения. Если не видите письма, проверьте спам-папку.
Ваш логин:
Пароль:
Не удается войти?
Забыли пароль?
Доступное составление индивидуального графика вакцинации на основе международных рекомендаций.
Также возможны напоминания на нужный день, рекомендации по прививкам беременных, сохранение серий вакцин.
Для каждой вакцины есть своя страница с подробной информацией.
Есть предложения или заметили ошибку?
Напишите через facebook или telegram. Опишите ошибку, прикрепив скриншот.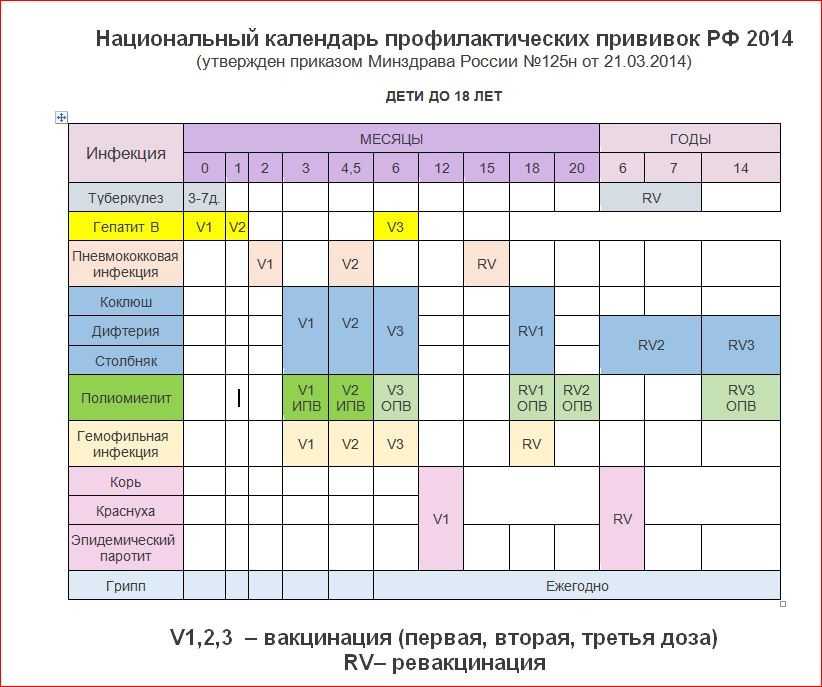
Степан Бегларян
Оплата на сайте vakarta.com осуществляется за возможность использования платных функций:
- возможность внесения новой информации о прививках — а именно даты прививки и типа вакцинного препарата
- и отключения рекламного компонента
Оплата предоставляет доступ аккаунта к указанному функционалу Вакарты сроком на 1 год
Оплата возможна на любую сумму из приведенных, которую пользователь Вакарты выбирает самостоятельно:
- 139 грн или 189 грн или 289 грн – в Украине;
- 7,9 $ или 11,9 $ или 18,9 $ – в других странах.
Доступ к платным функциям Вакарты устанавливается с момента оплаты на срок, указанный во время выбора варианта оплаты.
Введение записей о прививках, индивидуальный график вакцинации предусматривают гипотетический случай.
Никаких дополнительных ограничений по использованию других функций сервиса нет. Сохранение истории вакцинации, информация о прививочных препаратах, рекомендации беременным, оповещения предоставляются бесплатно.
Оплата производится платежными картами Visa, Mastercard
WayForPay (UA) / Monobank (UA) / FastSpring (Global) / Google Billing (android app)
При самостоятельном удалении пользователем своего аккаунта или в других случаях средства не возвращаются, услуга считается оказанной.
Получатель средств — автор и разработчик vakarta.com
Степан Бегларян, педиатр и иммунолог
ФЛП ИПН 3322009838
Тел.: +380944909759
E-mail: [email protected]
Привет! Я Коди — талисман вакарты и просто веселый котик.
Меня как мягкую игрушку подарила автору вакарты его жена. И теперь я Коди. Живу здесь и делаю приятнее все эти программные коды и сложные названия прививок.
Еще у вакарты есть для вас код специального назначения. Это личный промокод для бесплатного продления полного доступа. Поищите в настройках, промокод где-то там.
Передаю вашей семье наилучшие пожелания — быть здоровыми! А вакарта в этом поможет.
Живими атенуйованими є вакцини проти:
- туберкульозу (БЦЖ)
- кору, епідемічного паротиту, краснухи (КПК)
- вітряної віспи
- оральна поліомієлітну вакцина (ОПВ, через рот)
- ротавірусної інфекції (через рот)
- жовтої лихоманки
- а також натуральної віспи, туляремії, бруцельозу, сибірської виразки.

Такі вакцини проходять процес атенуації — ослаблення мікроорганізму із зниженням вірулентності при збереженні вихідної антигенності.
Живі атенуйовані вакцини не вводять вагітним (про всяк випадок) та при наявності деяких імунодефіцитних станів.
Про імунодефіцити можна почитати тут: Імунодефіцити — наскільки це серйозно.
Для виявлення підозри на первинний імунодефіцит у дитини можна пройти онлайн-тест.
При підозрі на імунодефіцит потрібна обов’язкова консультація лікаря-імунолога. При деяких із цих захворювань живі вакцини протипоказані, натомість показані всі додаткові неживі (інактивовані) вакцини.
Всім іншим людям вводити живі вакцини безпечно.
Особливістю живих вакцин є те, що ін’єкційні живі вакцини можуть впливати одна на одну. Тому дві ін’єкційні живі вакцини потібно вводити або з різницею в 1 місяць, або в один і той самий день.
А неживі (інактивовані) вакцини можна вводити з будь-якою іншою (живою чи неживою) вакциною як завгодно, в той самий день чи будь-який інший день.
Так само пероральні (через рот) живі вакцини не впливають на будь-які інші (живі чи неживі) вакцини, тому їх теж можна вводити з іншими вакцинами як завгодно, в той самий день чи будь-який інший день.
Вместе или по отдельности: – Вакарта
Учетная запись зарегистрирована на ваше имя. После регистрации вы сможете добавлять других членов семьи.
Ваше имя и фамилия:
Дата вашего рождения:
12345678910111213141516171819202122232425262728293031
ЯнвФевМарАпрМайИюнИюльАвгСентОктНоя Дек
20222021202020192018201720162015201420132012201120102009200820072006200520042003200220012000199919981997199619951994199319921992
91988198719861985198419831982198119801979197819771976197519741973197219711970196919681967196619651964196319621961196019591958195719561955195419531952195119501949194819471946194519441943194219411940193919381937193619351934193319321931193019291928192719261925192419231922192119201919191819171916191519141913191219111910190919081907190619051904190319021
00
— choose —AfghanistanÅland IslandsAlbaniaAlgeriaAmerican SamoaAndorraAngolaAnguillaAntarcticaAntigua and BarbudaArgentina⚑ ArmeniaAruba⚑ AustraliaAustria⚑ AzerbaijanBahamasBahrainBangladeshBarbados⚑ BelarusBelgiumBelizeBeninBermudaBhutanBolivia, Plurinational State ofBonaire, Sint Eustatius and SabaBosnia and HerzegovinaBotswanaBouvet IslandBrazilBritish Indian Ocean TerritoryBrunei DarussalamBulgariaBurkina FasoBurundiCambodiaCameroonCanadaCape VerdeCayman IslandsCentral African RepublicChadChileChinaChristmas IslandCocos (Keeling) IslandsColombiaComorosCongoCongo, the Democratic Republic of theCook IslandsCosta RicaCôte d’IvoireCroatiaCubaCuraçaoCyprusCzech Republic⚑ DenmarkDjiboutiDominicaDominican RepublicEcuadorEgyptEl SalvadorEquatorial GuineaEritrea⚑ EstoniaEthiopiaFalkland Islands (Malvinas)Faroe IslandsFiji⚑ Finland⚑ FranceFrench GuianaFrench PolynesiaFrench Southern TerritoriesGabonGambia⚑ Georgia⚑ GermanyGhanaGibraltarGreeceGreenlandGrenadaGuadeloupeGuamGuatemalaGuernsey GuineaGuinea-BissauGuyanaHaitiHeard Island and McDonald IslandsHoly See (Vatican City State)HondurasHong KongHungaryIceland⚑ IndiaIndonesiaIran, Islamic Republic ofIraq⚑ IrelandIsle of Man⚑ IsraelItalyJamaicaJapanJerseyJordan⚑ KazakhstanKenyaKiribatiKorea, Democratic People’s Republic ofKorea, Republic ofKuwait⚑ KyrgyzstanLao People’s Democratic Republic⚑ LatviaLebanonLesothoLiberiaLibyaLiechtenstein⚑ LithuaniaLuxembourgMacaoMacedonia, the former Yugoslav Republic ofMadagascarMalawiMalaysiaMaldivesMaliMaltaMarshall IslandsMartiniqueMauritaniaMauritiusMayotteMexicoMicronesia, Federated States of⚑ Moldova, Republic ofMonacoMongoliaMontenegroMontserratMoroccoMozambiqueMyanmarNamibiaNauruNepalNetherlandsNew Caledonia⚑ New ZealandNicaraguaNiger⚑ NigeriaNiueNorfolk IslandNorthern Mariana Islands⚑ NorwayOmanPakistanPalauPalestinian Territory, OccupiedPanamaPapua New GuineaParaguayPeruPhilippinesPitcairn⚑ PolandPortugalPuerto RicoQatarRéunionRomania⚑ Russian FederationRwandaSaint BarthélemySai nt Helena, Ascension and Tristan da CunhaSaint Kitts and NevisSaint LuciaSaint Martin (French part)Saint Pierre and MiquelonSaint Vincent and the GrenadinesSamoaSan MarinoSao Tome and PrincipeSaudi ArabiaSenegalSerbiaSeychellesSierra LeoneSingaporeSint Maarten (Dutch part)SlovakiaSloveniaSolomon IslandsSomalia⚑ South AfricaSouth Georgia and the South Sandwich IslandsSouth SudanSpainSri LankaSudanSurinameSvalbard and Jan MayenSwaziland⚑ SwedenSwitzerlandSyrian Arab RepublicTaiwan, Province of ChinaTajikistanTanzania, United Republic ofThailandTimor-LesteTogoTokelauTongaTrinidad and TobagoTunisia⚑ TurkeyTurkmenistanTurks and Caicos IslandsTuvaluUganda⚑ Ukraine⚑ United Arab Emirates⚑ United Kingdom⚑ United StatesUnited States Minor Outlying IslandsUruguay⚑ UzbekistanVanuatuVenezuela, Bolivarian Republic ofViet NamVirgin Islands, BritishVirgin Islands , США Уоллис и ФутунаЗападная СахараЙеменЗамбияЗимбабве
Следующий
Ваш пол:
мужчина женщина
Ваш адрес электронной почты:
Ваш пароль:
Промокод, если есть:
Подтвердите, что вы человек, а не бот:
Подтвердите согласие с Политикой конфиденциальности и защиты персональных данных
Регистрация возможна только при согласии с указанными условиями конфиденциальности
Вы получите подтверждение по электронной почте. Если сообщение не отображается, проверьте папку со спамом.
Если сообщение не отображается, проверьте папку со спамом.
ВАКЦИНА АБКДС-ИПВ//ПРП~Т: ОБЗОР 16-ЛЕТНЕГО ОПЫТА КЛИНИЧЕСКОГО ПРИМЕНЕНИЯ | Плоткин
1. Международный банк реконструкции и развития. Доклад о мировом развитии, 1993 г.: Инвестиции в здоровье http://files.dcp2. org/pdf/WorldDevelopmentReport1993.
2. Chandran A., Watt J.P., Santosham M. Вакцины против Haemophilus influenz ae. В: Вакцины. 5-е издание. Плоткин С.А., Оренштейн В., Оффит П.А. (ред.). США, Saunders Co., PA, 2008. — С. 157–175.
3. Эдвардс К., Декер М. Вакцины против коклюша. В: Вакцины. 5-е издание. Плоткин С. Оренштейн В., Оффит П.А. (ред.). США, Saunders Co., PA, 2008. — С. 467–517.
4. Peltola H. Заболевание Haemophilus influenzae типа b в мире в начале 21 века: глобальный анализ бремени болезни через 25 лет после использования полисахаридной вакцины и десятилетие после появления конъюгатов // Клин. микробиол. Изд. — 2000 г.; 13 (2): 302–317.
5. Vitek C.R., Wharton M. Токсоид дифтерии. В: Вакцины. 5-е издание. Плоткин С.А., Оренштейн В., Оффит П.А. (ред.). США, Saunders Co., PA, 2008. — С. 139–155.
Токсоид дифтерии. В: Вакцины. 5-е издание. Плоткин С.А., Оренштейн В., Оффит П.А. (ред.). США, Saunders Co., PA, 2008. — С. 139–155.
6. Василак С.Г., Ропер М.Х., Крецингер К., Оренштейн В.А. Столбнячный анатоксин. В: Вакцины. 5-е издание. Плоткин С.А., Оренштейн В., Оффит П.А. (ред.). США, Saunders Co., PA, 2008. — С. 139–155.
7. Всемирная организация здравоохранения. Глобальное видение и стратегия иммунизации www.who.int/vaccines-documents/DocsPDF05/GIVS_Final_EN.pdf
8. Эдвардс К.М., Декер М.Д. Комбинированные вакцины: надежды и проблемы // Педиатр. Заразить. Дис. Дж. — 1994; 13 (5): 805–839.
9. Пичичеро М.Е. Новые комбинированные вакцины // Педиатр. клин. Север. Являюсь. — 2000 г.; 47 (2): 407–426.
10. Обаро С.К., Палмер А. Вакцины для детей: политика, политика и бедность // Вакцины. — 2003 г.; 21 (13–14): 1423–1431.
11. Андре Ф. Э., Буй Р., Бок Х. Л. и др. Вакцинация значительно снижает заболеваемость, инвалидность, смертность и несправедливость во всем мире // Бюлл. Всемирный орган здравоохранения. — 2008 г.; 86 (2): 140–146.
Всемирный орган здравоохранения. — 2008 г.; 86 (2): 140–146.
12. Aristegui J., Usonis V., Coovadia H. et al. Содействие расширенной программе ВОЗ по иммунизации: клинический профиль комбинированной вакцины против дифтерии, столбняка, коклюша, гепатита В и гемофильной палочки типа b // Int. Дж. Заразить. Дис. — 2003 г.; 7 (2): 143–151.
13. Декер М.Д. Принципы педиатрических комбинированных вакцин и практические вопросы, связанные с применением в клинической практике // Педиатр. Заразить. Дис. Ж. — 2001; 20 (11 Дополнение): S10–S18.
14. Декер М., Богартс Х., Эдвардс К. Комбинированные вакцины. В: Вакцины. 5-е издание. Плоткин С.А., Оренштейн В., Оффит П.А. (ред.). США, Saunders Co., PA, 2008. — С. 1069–1101.
15. Watt J.P., Wolfson L.J., O’Brien K.L. et al. Бремя болезней, вызванных Haemophilus influenzae типа b, у детей в возрасте до 5 лет: глобальные оценки // Lancet. — 2009 г.; 374 (9693): 903–911.
16. Всемирная организация здравоохранения. Документ с изложением позиции по дифтерии // Wkly Epidemiol. Рек. — 2006 г.; 81 (3): 24–32.
Рек. — 2006 г.; 81 (3): 24–32.
17. Всемирная организация здравоохранения. Документ с изложением позиции по столбняку // Wkly Epidemiol. Рек. — 2010 г.; 81 (20): 198–208.
18. Всемирная организация здравоохранения. Инактивированная полиомиелитная вакцина после прекращения пероральной полиомиелитной вакцины // Wkly Epidemiol. Рек. — 2006 г.; 81 (15): 137–144.
19. Глобальная инициатива по ликвидации полиомиелита. Еженедельный бюллетень о диком полиовирусе www.polioeradication.org/Dataandmonitoring/Poliothisweek.aspx
20. Центры по контролю и профилактике заболеваний. Рекомендуемый график иммунизации детей // MMWR. — 2001 г.; 50 (1): 1–3.
21. Центры по контролю и профилактике заболеваний. Обновленная информация о полиовирусах вакцинного происхождения — во всем мире // MMWR. — 2007 г.; 56 (38): 996–1001.
22. Heymann D.L., Sutter R.W., Aylward R.B. Глобальный призыв к новым вакцинам против полиомиелита // Nature. — 2005 г.; 434 (7034): 699–700.
23. Кью О.М., Саттер Р.В., де Гурвиль Э.М. и соавт. Полиовирусы вакцинного происхождения и завершающая стратегия глобальной ликвидации полиомиелита // Annu. Преподобный Микробиолог. — 2005 г.; 59: 587–635.
24. Всемирная организация здравоохранения. Внедрение инактивированной полиовакцины в странах, использующих пероральную полиомиелитную вакцину // Wkly Epidemiol. Рек. — 2003 г.; 78 (28): 241–252.
25. Всемирная организация здравоохранения. Полиовирусы вакцинного происхождения — обновленная информация // Wkly Epidemiol. Рек. — 2006 г.; 81 (42): 398–404.
26. Всемирная организация здравоохранения. Стратегический план Глобальной инициативы по ликвидации полиомиелита на 2004–2008 гг. www.polioeradication.org/content/publications/2004stratplan.pdf
Рекомендации 2-го Национального консультативного совещания Индийской академии педиатрии (IAP) по ликвидации полиомиелита и совершенствованию плановой иммунизации // Индийская педиатр. — 2008 г.; 45 (5): 367–378.
28. Центры по контролю и профилактике заболеваний. Профилактика полиомиелита в США. Обновленные рекомендации Консультативного комитета по практике иммунизации // MMWR. — 2000 г.; 49: 1–22.
29. Боннет М.С., Датта А. Мировой опыт применения инактивированной полиовакцины // Вакцины. — 2008 г.; 26 (39): 4978–4983.
30. Decker M.D., Edwards K.M., Steinhoff M.C. et al. Сравнение 13 бесклеточных коклюшных вакцин: побочные реакции // Педиатрия. — 1995; 96 (3 часть 2): 557–566.
31. Pichichero M.E., Deloria M.A., Rennels M.B. et al. Сравнение безопасности и иммуногенности 12 бесклеточных коклюшных вакцин и одной цельноклеточной коклюшной вакцины, вводимой четвертой дозой у детей в возрасте от 15 до 20 месяцев // Педиатрия. — 1997 г.; 100 (5): 772–788.
32. Beutels P., Bonanni P., Tormans G. et al. Экономическая оценка всеобщей вакцинации против коклюша в Италии // Вакцины. — 1999 г.; 17 (19): 2400–2409.
33. Ekwueme D.U., Strebel P.M., Hadler S. C. et al. Экономическая оценка использования бесклеточной вакцины против дифтерии, столбняка и коклюша или вакцины против дифтерии, столбняка и цельноклеточного коклюша в США, 1997 // Арх. Педиатр. Подросток Мед. — 2000 г.; 154 (8): 797–803.
C. et al. Экономическая оценка использования бесклеточной вакцины против дифтерии, столбняка и коклюша или вакцины против дифтерии, столбняка и цельноклеточного коклюша в США, 1997 // Арх. Педиатр. Подросток Мед. — 2000 г.; 154 (8): 797–803.
34. Tormans G., Van Doorslaer E., Van Damme P., Clara R., Schmitt H.J. Экономическая оценка профилактики коклюша цельноклеточной и бесклеточной вакциной в Германии // Eur. Дж. Педиатр. — 1998 г.; 157 (5): 395–401.
35. Thisyakorn U., Montellano M., Ortiz E., Lane A. Обзор схем введения вакцины против гепатита B у младенцев. Представлено на 5-м Азиатском конгрессе детских инфекционных заболеваний. Тайбэй, Тайвань, 2010 г.
36. Всемирная организация здравоохранения. Вакцины, прошедшие предварительную квалификацию Организации Объединенных Наций www.who.int/immunization_standards/vaccine_quality/PQ_vaccine_list_en/en/index.html
37. Capeding M. R., Cadorna-Carlos J., Book-Montellano M., Ortiz E. Иммуногенность и безопасность DTaP–IPV // Комбинированная вакцина PRPT, вводимая с вакциной против гепатита B: рандомизированное открытое исследование. Бык // Всемирный орган здравоохранения. — 2008 г.; 86 (6): 443–451.
Бык // Всемирный орган здравоохранения. — 2008 г.; 86 (6): 443–451.
38. Dutta A.K., Verghese V.P., Pemde H.K. et al. Иммуногенность и безопасность пятивалентной конъюгированной вакцины против дифтерии, столбняка, бесклеточного коклюша, инактивированного полиовируса, гемофильной палочки типа В (Пентаксим) с вакциной против гепатита В // Индийская педиатр. — 2009 г.; 46 (11): 975–982.
39. Madhi S.A., Cutland C., Jones S., Ortiz E. Устойчивость антител после первичной вакцинации и иммуногенность/безопасность DTaP–IPV // Бустерная вакцина PRPT у детей в возрасте от 18 до 19 месяцев в Южной Африке/Программы и Тезисы докладов 26-го Конгресса педиатров Международной педиатрической ассоциации. Johannesburg, South Africa, 2010.
40. Madhi S.A., Cutland C., Jones S., Ortiz E. Иммуногенность и безопасность бесклеточного коклюша, дифтерии, столбняка, инактивированного полиовируса, Hib-конъюгированной комбинированной вакцины (Pentaxim™) и моновалентная вакцина против гепатита В в возрасте 6, 10 и 14 месяцев у детей раннего возраста в Южной Африке // S.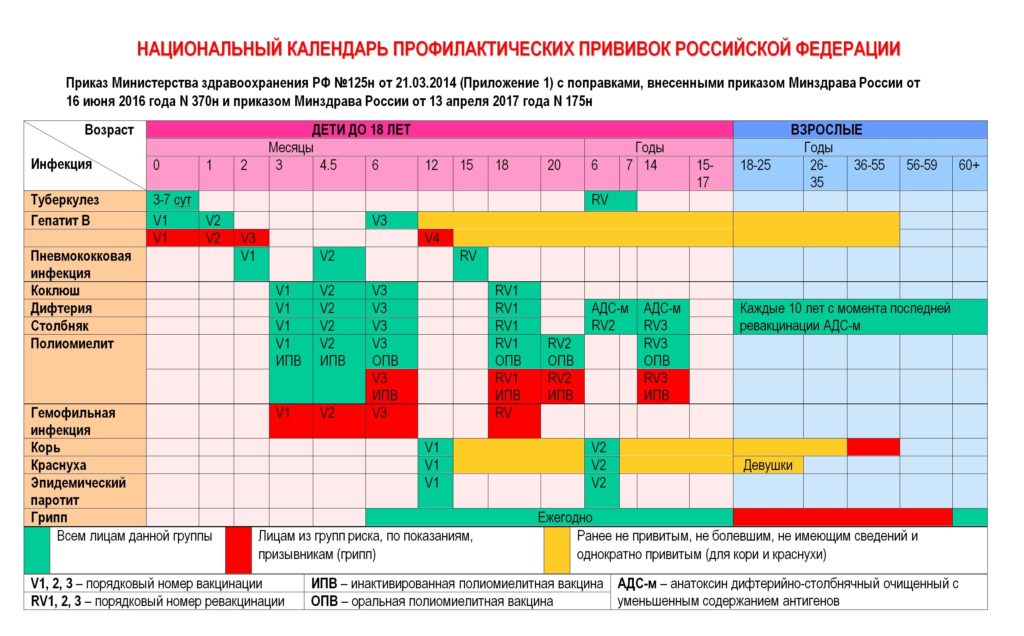 Afr. Мед. Ж. — 2011; 101: 126–131.
Afr. Мед. Ж. — 2011; 101: 126–131.
41. Kanra G., Silier T., Yurdakok K. et al. Изучение иммуногенности комбинированной вакцины против дифтерии, столбняка, бесклеточного коклюша, инактивированной полиомиелитной вакцины, используемой для восстановления лиофилизированной вакцины против Haemophilus influenzae типа b (DTaP-IPV // PRP-T), вводимой одновременно с вакциной против гепатита B в два, три и четыре года месяцев жизни // Вакцина. — 1999 г.; 18 (9–10): 947–954.
42. Li R.C., Li F.X., Li Y.P. et al. Иммуногенность и безопасность пятивалентной бесклеточной коклюшной комбинированной вакцины, включающей дифтерию, столбняк, инактивированный полиовирус и конъюгированный полисахарид Haemophilus influenzae типа b, для первичной вакцинации детей грудного возраста в возрасте 2, 3, 4 или 3, 4, 5 месяцев в Китае // Вакцины. — 2011 г.; 29(10): 1913–1920 гг.
43. Langue J., David T., Roussel F. et al. Безопасность и иммуногенность вакцин DTaP-IPV и Act-Hib, вводимых вместе или раздельно детям в возрасте 2, 3 и 4 месяцев / Программы и тезисы 15-го ежегодного собрания Европейского общества детских инфекционных болезней.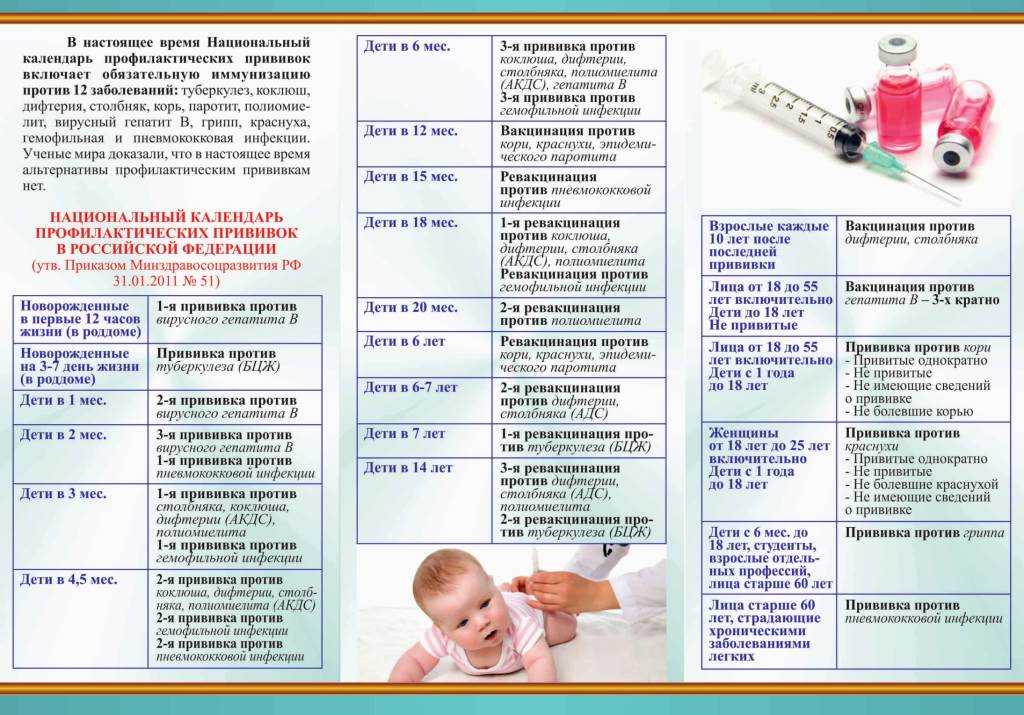 Paris, France, 1997.
Paris, France, 1997.
44. Mallet E., Hoffenbach A., Salomon H. et al. Первичная иммунизация комбинированной бесклеточной вакциной DTaP-IPV-Act-HIB в возрасте 2–3–4 или 2–4–6 месяцев/Программы и тезисы 14-го Европейского общества детских инфекционных болезней. Элиснор, Дания, 19 лет96.
45. Reinert P., Boucher J., Pines E. et al. Первичная или бустерная иммунизация вакциной DTaP-IPV, вводимой либо в комбинации, либо в сочетании с вакциной Haemophilus influenzae типа b (Act-Hib): крупномасштабное исследование безопасности / Программы и тезисы 15-го ежегодного собрания Европейского общества педиатрических инфекционистов Болезни. Париж, Франция, 1997 год.
46. Лагос Р., Котлофф К., Хоффенбах А. и соавт. Клиническая приемлемость и иммуногенность пятивалентной парентеральной комбинированной вакцины, содержащей дифтерийный, столбнячный, бесклеточный коклюшный, инактивированный полиомиелитный и конъюгированные антигены Haemophilus influenzae типа b, у двух-, четырех- и шестимесячных чилийских детей // Педиатр. Заразить. Дис. Дж. — 1998; 17 (4): 294–304.
Заразить. Дис. Дж. — 1998; 17 (4): 294–304.
47. Малле Э., Фабр П., Пайнс Э. и др. Иммуногенность и безопасность новой жидкой шестивалентной комбинированной вакцины в сравнении с раздельным введением референтных лицензированных вакцин у детей раннего возраста // Педиатр. Заразить. Дис. Дж. — 2000; 19 (12): 1119–1127.
48. Carlsson R.M., Claesson B.A., Selstam U. et al. Безопасность и иммуногенность комбинированной дифтерийно-столбнячно-бесклеточной коклюшно-инактивированной полиомиелитной вакцины и вакцины против Haemophilus influenzae типа b, вводимой в возрасте 2–4–6–13 или 3–5–12 месяцев // Педиатр. Заразить. Дис. Дж. — 1998; 17 (11): 1026–1033.
49. Carlsson R.M., Claesson B.A., Fagerlund E. et al. Персистенция антител у пятилетних детей, получивших в младенчестве пятивалентную комбинированную вакцину // Педиатр. Заразить. Дис. Ж. — 2002; 21 (6): 535–541.
50. Thisyakorn U., Pancharoen C., Chuenkitmongkol S., Ortiz E. Иммуногенность и безопасность ревакцинации DTaP–IPV // PRP–T вакцина (Пентаксим) на втором году жизни у тайских детей, примированных бесклеточным коклюшная комбинированная вакцина // Southeast Asian J.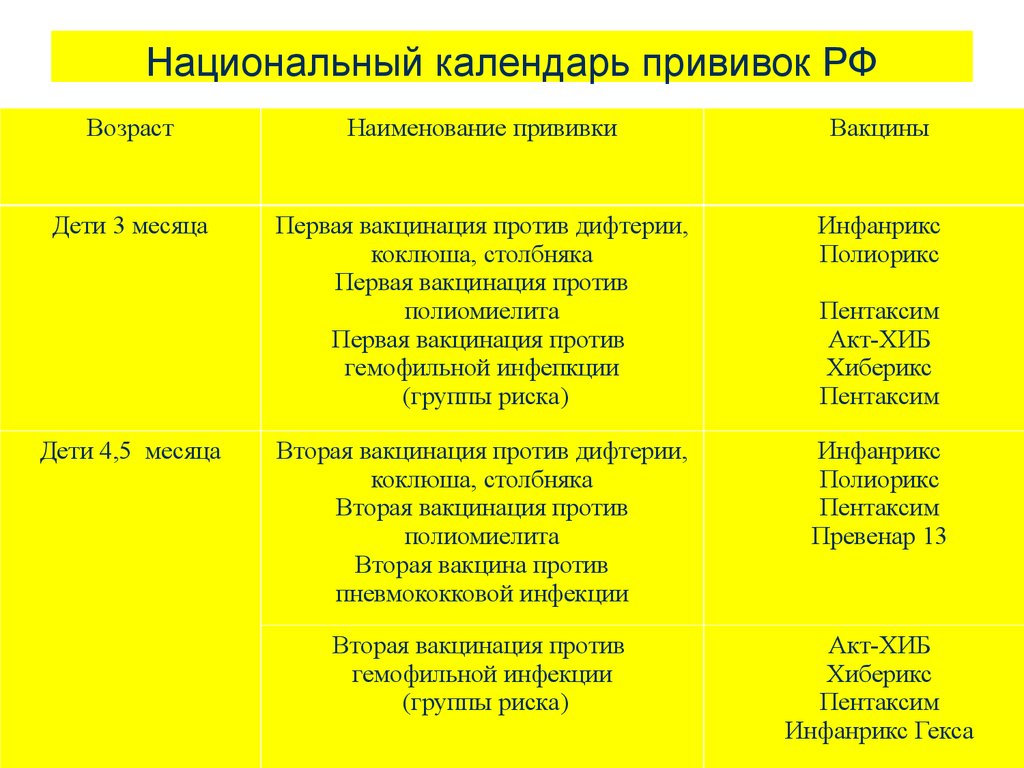 Trop. Мед. Здравоохранение. — 2009 г.; 40 (2): 282–294.
Trop. Мед. Здравоохранение. — 2009 г.; 40 (2): 282–294.
51. Thisyakorn U., Chotpitayasunondh T., Pancharoen C. et al. Оценка бесклеточного коклюша, дифтерии, столбняка, инактивированного полиовируса, Hib-конъюгированной комбинированной вакцины (Пентаксим) в возрасте 2, 4 и 6 месяцев плюс вакцина против гепатита В при рождении, в возрасте 2 и 6 месяцев у младенцев в Таиланде / / Юго-Восточная Азия Дж. Троп. Мед. Здравоохранение. — 2010 г.; 41 (2): 450–462.
52. Инглунд Дж. А., Декер М. Д., Эдвардс К. М. и соавт. Бесклеточная и цельноклеточная коклюшные вакцины в качестве бустерных доз: многоцентровое исследование // Педиатрия. — 1994; 93 (1): 37–43.
53. Всемирная организация здравоохранения. Документ с изложением позиции по коклюшу // Wkly Epidemiol. Рек. — 2010 г.; 85 (40): 385–400.
54. Le Saux N., Barrowman N.J., Moore D.L. et al. Снижение числа госпитализаций по поводу фебрильных судорог и сообщений об эпизодах гипотонической чувствительности, поступивших в отделения неотложной помощи больниц после перехода на бесклеточную коклюшную вакцину в Канаде: отчет IMPACT // Pediatrics. — 2003 г.; 112 (5): 348.
— 2003 г.; 112 (5): 348.
55. Collins C.L., Salt P., Mc Carthy N. et al. Иммуногенность и безопасность низкодозовой комбинированной вакцины против дифтерии, столбняка и бесклеточного коклюша с инактивированной или пероральной полиомиелитной вакциной в качестве дошкольной бустерной вакцины у детей в Великобритании // Вакцина. — 2004 г.; 22 (31–32): 4262–4269.
56. Langue J., Matisse N., Pacoret P. et al. Персистенция антител в возрасте 5–6 лет у детей, получивших первичную серию прививок пятивалентной цельноклеточной коклюшной вакциной и первую ревакцинацию пятивалентной бесклеточной коклюшной вакциной: иммуногенность и переносимость второй ревакцинации четырехвалентной бесклеточной вакциной в 5–6 лет // Вакцина. — 2004 г.; 22 (11–12): 1406–1414.
57. Малле Э., Матисс Н., Матье Н. и др. Персистенция антител против дифтерии, столбняка, коклюша, полиомиелита и гемофильной палочки типа b (Hib) у детей 5–6 лет после первичной вакцинации и первой ревакцинации пятивалентной комбинированной бесклеточной коклюшной вакциной: иммуногенность и переносимость четырехвалентной комбинированной бесклеточной коклюшной вакцины вакцина, вводимая в качестве второй бустерной дозы // Вакцина.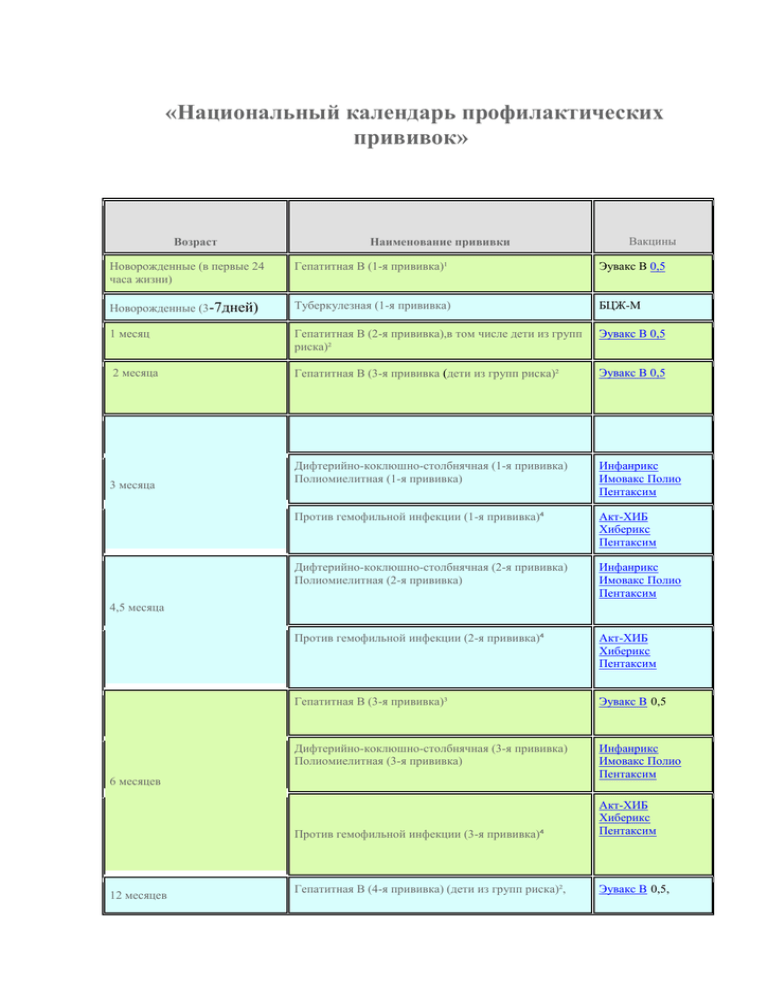 — 2004 г.; 22 (11–12): 1415–1422.
— 2004 г.; 22 (11–12): 1415–1422.
58. Плоткин С. А. Корреляты защиты, индуцируемой вакцинацией // Клин. Вакцина Иммунол. — 2010 г.; 17 (7): 1055–1065.
59. Карлссон Р. М., Тролльфорс Б. Борьба с коклюшем — уроки, извлеченные из 10-летней программы эпиднадзора в Швеции // Вакцина. — 2009 г.; 27 (42): 5709–5718.
60. Okada K., Ohashi Y., Matsuo F. et al. Эффективность бесклеточной коклюшной вакцины у японских детей в неэпидемический период: парное исследование случай-контроль // Эпидемиол. Заразить. — 2009 г.; 137 (1): 124–130.
61. Всемирная организация здравоохранения. Валидация элиминации столбняка новорожденных в отдельных штатах — Индия // Wkly Epidemiol. Рек. — 2008 г.; 83 (21): 185–192.
62. Видор Э., Плоткин С. А. Иммуногенность двухкомпонентной (ПТ и ФГА) бесклеточной коклюшной вакцины в различных сочетаниях // Гум. вакцина. — 2008 г.; 4 (5): 328–340.
63. Dutta A., Verghese V.P., Pemde H.K. et al. Персистенция антител после первичной вакцинации, иммуногенность и безопасность вакцины DTaP–IPV // ревакцинация PRPT в возрасте от 18 до 19 летмесячного возраста у индийских младенцев / Программы и тезисы 3-го Азиатско-Тихоокеанского конгресса педиатров. Shanghai, China, 2009.
Shanghai, China, 2009.
64. Li R.C., Li F.X., Li Y.P. et al. Персистенция антител в возрасте 18–20 месяцев после первичной вакцинации здоровых детей комбинированной вакциной АКДС–ИПВ // ПРРТ в сравнении с отдельными вакцинами (АКДС, ПРРТ и ИПВ) и иммуногенность и безопасность ревакцинации в Китайской Народной Республике /Программы и тезисы 5-го Азиатского конгресса детских инфекционистов. Тайбэй, Тайвань, 2010 г.
65. Gustafsson L., Hessel L., Storsaeter J., Olin P. Длительное наблюдение за шведскими детьми, вакцинированными бесклеточными коклюшными вакцинами в возрасте 3, 5 и 12 месяцев, указывает на необходимость ревакцинации в возрасте 5 лет. до 7 лет // Педиатрия. — 2006 г.; 118 (3): 978–984.
66. Thisyakorn U., Chotpitayasunondh T., Pancharoen C. et al. Персистенция антител после первичной вакцинации и иммуногенность / безопасность ревакцинации DTaPIPV // PRPT в возрасте от 18 до 19 месяцев у тайских младенцев / Программы и тезисы 6-го Конгресса Всемирного общества детских инфекционных болезней.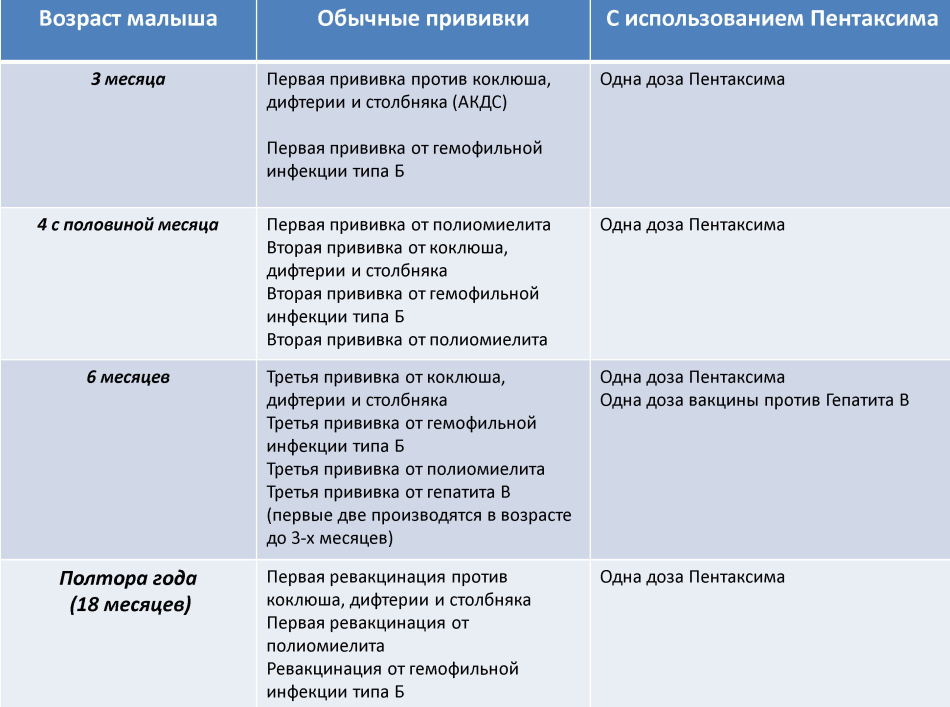 Буэнос-Айрес, Аргентина, 2009 г..
Буэнос-Айрес, Аргентина, 2009 г..
67. Zhang L., Prietsch S. O. M., Axelsson I., Halperin S. Бесклеточные вакцины для профилактики коклюша у детей // Cochrane Database Syst. Изд. — 2011 г.; 1: CD001478.
68. Джефферсон Т., Рудин М., Ди Пьетрантонж С. Систематический обзор эффектов коклюшных вакцин у детей // Вакцины. — 2003 г.; 21 (17–18): 2003–2014 гг.
69. Desauziers E., Hessel L., Decker M.D. et al. Систематический обзор эффектов коклюшных вакцин у детей // Вакцины. — 2004 г.; 22 (21–22): 2681–2684.
70. Симондон Ф. Систематический обзор эффектов коклюшных вакцин у детей // Вакцины. — 2004 г.; 22 (23–24): 2965.
71. Gustafsson L., Hallander H. O., Olin P. et al. Контролируемое испытание двухкомпонентной бесклеточной, пятикомпонентной бесклеточной и цельноклеточной коклюшной вакцины // N. Engl. Дж. Мед. — 1996 г.; 334 (6): 349–355.
72. Бонмарин И., Леви-Брюль Д., Барон С. и др. Эпиднадзор за коклюшем во французских больницах: результаты 10-летнего периода // Euro Surveill. — 2007 г.; 12 (1): 6.
— 2007 г.; 12 (1): 6.
73. Olin P., Hallander H. O. Заметное снижение заболеваемости коклюшем после возобновления вакцинации против коклюша в Швеции // Euro Surveill. — 1999 г.; 4 (12): 128–129.
74. Ренди-Вагнер П., Паульке-Коринек М., Станек Г. и соавт. Влияние программы ревакцинации подростков и взрослых на эпидемиологию коклюша в Австрии // Педиатр. Заразить. Дис. Ж. — 2007; 26 (9): 806–810.
75. Лизе Дж. Г., Стоянов С., Петерс А. Продолжительность эффективности после первичной иммунизации бесклеточной коклюшной вакциной Байкен (Трипедия)/Программы и тезисы 43-й Межнаучной конференции по противомикробным препаратам и химиотерапии. Чикаго, Иллинойс, США, 2003 г.
76. Liese J.G., Meschievitz C.K., Harzer E. et al. Эффективность двухкомпонентной бесклеточной коклюшной вакцины у детей раннего возраста // Педиатр. Заразить. Дис. Дж. — 1997; 16 (11): 1038–1044.
77. Шведский институт по контролю за инфекционными заболеваниями. Эпиднадзор за коклюшем в Швеции с расширенным последующим наблюдением за когортами, иммунизированными бесклеточными коклюшными вакцинами, 2009 г. Приложение 2 к одиннадцатилетнему отчету www.smittskyddsinstitutet.se/upload/Publikationer/11-y-report-app202-SPMSD.pdf
Приложение 2 к одиннадцатилетнему отчету www.smittskyddsinstitutet.se/upload/Publikationer/11-y-report-app202-SPMSD.pdf
78. Ренди-Вагнер П., Кунди М., Миколасек А. и соавт. Больничный активный эпиднадзор за детским коклюшем в Австрии с 1996 к 2003 г.: оценки заболеваемости и вакциноэффективности цельноклеточной и бесклеточной вакцины // Вакцины. — 2006 г.; 24 (33–34): 5960–5965.
79. Hviid A., Stellfeld M., Andersen P.H. et al. Влияние плановой вакцинации коклюшным анатоксином в Дании // Вакцина. — 2004 г.; 22 (27–28): 3530–3534.
80. Хвиид А. Постлицензионная эпидемиология вакцинации детей: опыт Дании // Expert Rev Vaccines. — 2006 г.; 5 (5) 6 641–649.
81. Ватанабэ М., Нагаи М. Бесклеточные вакцины против коклюша в Японии: прошлое, настоящее и будущее // Эксперт Rev. Вакцины. 2005 г.; 4 (2): 173–184.
82. Liese J.G., Stojanov S., Froeschle J. et al. Долгосрочная эффективность бесклеточной коклюшной вакцины Байкен (Трипедия) / Программы и тезисы 40-й Межнаучной конференции по антимикробным препаратам и химиотерапии.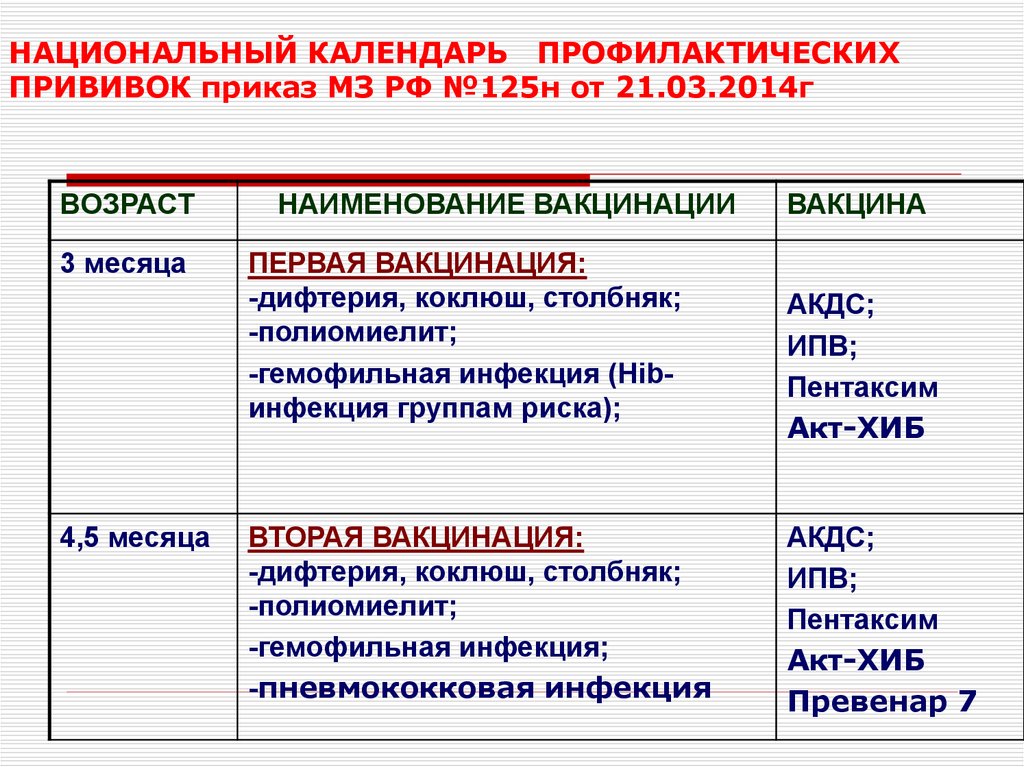 Торонто, Канада, 2000.
Торонто, Канада, 2000.
83. Bisgard K.M., Rhodes P., Connelly B.L. et al. Эффективность коклюшной вакцины среди детей в возрасте от 6 до 59 месяцев в США, 1998–2001 гг. // Педиатрия. — 2005 г.; 116 (2): e285–e294.
84. Эскола Дж., Уорд Дж., Даган Р. и соавт. Комбинированная вакцинация конъюгатом Haemophilus influenzae типа b и дифтерийно-столбнячно-коклюшной, содержащей бесклеточный коклюш // Lancet. — 1999; 354 (9195): 2063–2068.
85. Hoppenbrouwers K., Kanra G., Roelants M. et al. Примирующий эффект, иммуногенность и безопасность конъюгата гемофильной палочки типа b и столбнячного анатоксина (PRP-T) и комбинированной вакцины против дифтерии, столбняка и бесклеточного коклюша (DTaP), вводимых младенцам в Бельгии и Турции // Вакцина. — 1999 г.; 17 (7–8): 875–886. 86. Гринберг Д. П., Доемланд М., Беттингер Дж. А. и соавт. Эпидемиология коклюша и Haemophilus influenzae типа b в Канаде с использованием исключительно детской комбинированной вакцины против дифтерии-столбняка-бесклеточного коклюша-инактивированного полиовируса-Haemophilus influenzae типа b и противостолбнячной-дифтерийно-бесклеточной коклюшной вакцины подростков-взрослых: последствия для профилактики заболеваний в США // Педиатр.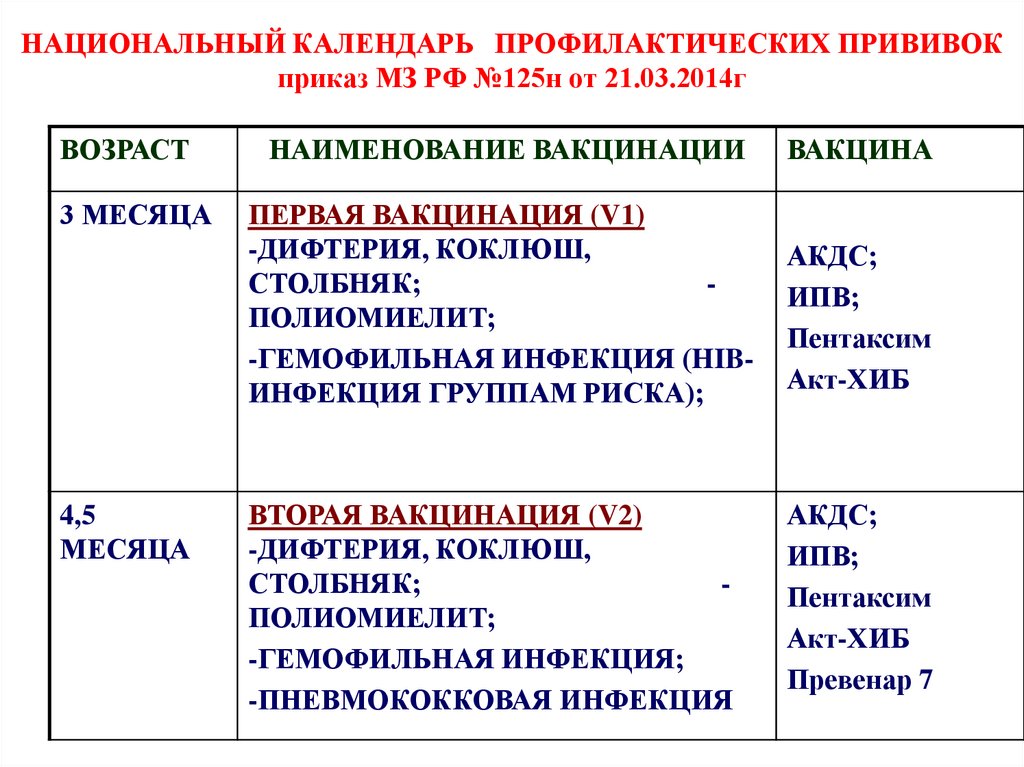 Заразить. Дис. Дж. — 2009 г.; 28 (6): 521–528.
Заразить. Дис. Дж. — 2009 г.; 28 (6): 521–528.
86. Kalies H., Verstraeten T., Grote V. et al. Четыре с половиной года наблюдения за эффективностью комбинированных вакцин дифтерийно-столбнячный анатоксин-бесклеточный коклюш/гемофильная палочка типа b и дифтерийно-столбнячный анатоксин-бесклеточный коклюш-инактивированный полиовирус/H. influenzae типа b в Германии // Педиатр. Заразить. Дис. Ж. — 2004; 23 (10): 944–950.
87. Schmitt H.J., von Kries R., Hassenpflug B. et al. Заболевание, вызываемое гемофильной палочкой типа b: влияние и эффективность комбинированных вакцин против дифтерии, столбняка, бесклеточного коклюша (инактивированного полиовируса) / H. influenzae типа b // Педиатр. Заразить. Дис. Ж. — 2001; 20 (8): 767–774.
88. Cruces R.P., Donoso F.A., Camacho A.J. et al. Инвазивные инфекции, вызванные Haemophilus influenzae типа b, после введения конъюгированной вакцины по расширенной программе иммунизации // Чили. Преподобный Чилена. Инфектол. — 2006 г.; 23 (1): 50–54.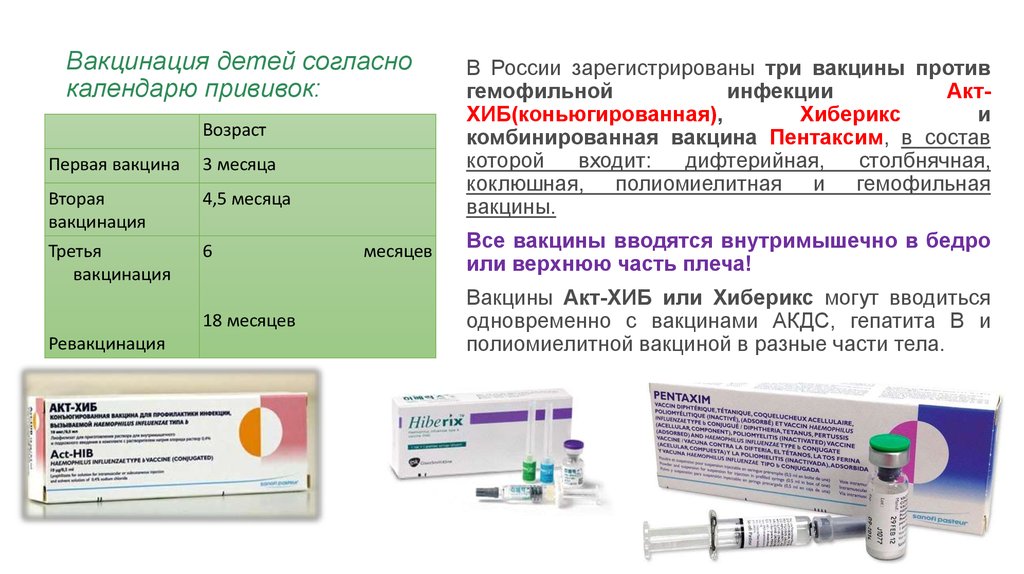
89. Келли Д. Ф., Моксон Э. Р., Поллард А. Дж. Конъюгированные вакцины против гемофильной палочки типа b // Иммунология. — 2004 г.; 113 (2): 163–174.
90. Cameron C., Pebody R. Введение пневмококковой конъюгированной вакцины в британскую программу иммунизации детей и изменения в календарях менингита C и Hib // Euro Surveill. — 2006 г.; 11 (3): E060302.
91. Ladhani S., Heath P.T., Slack M.P. et al. Неэффективность конъюгированной вакцины против Haemophilus influenzae серотипа b в двенадцати странах с установленными национальными программами иммунизации детей // Clin. микробиол. Заразить. — 2010 г.; 16 (7): 948–954.
92. Всемирная организация здравоохранения. Конъюгированные вакцины против гемофильной палочки типа b — документ с изложением позиции ВОЗ // Wkly Epidemiol. Рек. — 2006 г.; 81 (47): 445–452.
93. Garpenholt O., Hugosson S., Fredlund H. et al. Инвазивное заболевание, вызванное Haemophilus influenzae типа b, в течение первых шести лет общей вакцинации шведских детей // Acta Paediatr.

 А также глютаральдегиду, неомицину, стрептомицину и полимиксину В;
А также глютаральдегиду, неомицину, стрептомицину и полимиксину В;