Содержание
Вакцина Коревая платно в Москве
О вакцине
Вакцина коревая культуральная живая — это ослабленная вакцина от кори, производство Россия.
График вакцинации
Коревая вакцина инструкция
Национальный календарь профилактических прививок предусматривает двукратную вакцинацию против кори:
- в 12 месяцев и в 6 лет (с 4 до 6 лет по данным CDC).
При догоняющей вакцинации минимальный интервал между прививками в РФ составляет 3 месяца (1 месяц по данным CDC).
Подросткам и взрослым показана вакцинация, если они не болели и не были привиты ранее. Для большинства взрослых достаточно одной дозы вакцины. Взрослые из групп риска прививаются дважды: учащиеся образовательных учреждений, медицинские работники, международные путешественники и др.
Дети, путешествующие в другие страны, могут получить нулевую дозу вакцины против кори начиная с 6-месячного возраста, а затем с 12 месяцев двукратно вакцинироваться по календарю.
Экстренная вакцинация проводится в течение 72 часов после контакта с корью.
Противопоказания
- Тяжелая аллергическая реакция на предыдущую дозу или на компоненты вакцины, в т.ч. на неомицин.
- Беременность и планирование беременности в течение месяца после вакцинации,
- Тяжелые иммунодефициты, связанные с онкологическими
заболеваниями, иммуносупрессивной терапией, ВИЧ-инфекцией и др.
Не рекомендована вакцинация при острых инфекциях и обострении хронических заболеваний. При ОРВИ и кишечных инфекциях вакцинацию лучше отложить до нормализации температуры тела.
Возможные реакции
После вакцинации возможны местные реакции (покраснение, боль и отек в месте инъекции), а также кратковременное ухудшение самочувствия (подъем температуры тела, беспокойство). Эти реакции возникают редко и самостоятельно проходят в течение 1–3 дней.
На живые вакцины могут развиваться отсроченные реакции, напоминающие течение болезни в малой форме. Они не представляют опасности для здоровья и не заразны для окружающих.
Через 7-14 дней после вакцинации против кори у 5% вакцинируемых появляется кореподобная сыпь и поднимается температура тела.
Эти реакции проходят самостоятельно и не требуют лечения.
Совместимость с другими вакцинами
Вакцина сочетается со всеми вакцинами календаря профилактических прививок (кроме БЦЖ), поэтому прививку можно делать одномоментно с другими вакцинами в разные участки тела.
Прививаться другой живой вакциной можно через 1 месяц, для неживых вакцин ограничений по интервалам нет
Хочу получить консультацию о вакцинации
ОТПРАВИТЬ
Нажимая на кнопку, вы соглашаетесь с Политикой
конфиденциальности
расшифровка, что это такое, инструкция, реакция
СодержаниеСвернутьРазвернуть
- Прививка ОПВ — что это такое?
- Описание инструкции по применению вакцины ОПВ
- Противопоказания и меры предосторожности
- Возможные осложнения
- Сроки вакцинации
- Как подготовиться к вакцинации ОПВ
- Реакция на вакцину ОПВ
В российский национальный календарь прививок входят вакцинации против более десяти инфекционных заболеваний. От чего делают прививку ОПВ и какие препараты используют для этой цели? Так обозначается вакцинация против опасного вирусного заболевания — полиомиелита, или детского спинномозгового паралича, до недавнего времени регистрируемого по всему земному шару.
От чего делают прививку ОПВ и какие препараты используют для этой цели? Так обозначается вакцинация против опасного вирусного заболевания — полиомиелита, или детского спинномозгового паралича, до недавнего времени регистрируемого по всему земному шару.
Так что это такое — прививка ОПВ? Эта аббревиатура расшифровывается как «оральная полиомиелитная вакцина» или полиовакцина. Слово «оральная» означает, что препарат вводят через рот. Давайте выясним всё об этой прививке.
Прививка ОПВ — что это такое?
В настоящее время на территории нашей страны разрешён только один препарат для оральной прививки. Это «Вакцина полиомиелитная пероральная 1, 2, 3 типов (ОПВ)». Она выпускается российским производителем ФГУП «Институт полиомиелита и вирусных энцефалитов им. М.П. Чумакова РАМН».
В составе вакцины ОПВ содержится живой вирус полиомиелита. Он был получен в 1950 годах американским исследователем Альбертом Сэйбином в результате длительного культивирования дикого штамма на культуре клеток обезьян. Особенность этого типа полиовируса в том, что он хорошо приживается и размножается в кишечнике, но не способен поражать клетки нервной ткани. Тогда как полевой, или дикий полиовирус опасен именно тем, что вызывает гибель нейронов спинного мозга — отсюда идут параличи и нарушение нервной деятельности.
Особенность этого типа полиовируса в том, что он хорошо приживается и размножается в кишечнике, но не способен поражать клетки нервной ткани. Тогда как полевой, или дикий полиовирус опасен именно тем, что вызывает гибель нейронов спинного мозга — отсюда идут параличи и нарушение нервной деятельности.
Вакцинный вирус включает в себя три разновидности — 1, 2, 3 серотипы, которые полностью перекрывают дикие штаммы полиовируса. По необходимости могут выпускать моновалентные препараты, содержащие только один тип вируса — их применяют для борьбы с заболеванием в очагах инфекции.
Кроме вируса, в состав вакцины входят антибиотики, не позволяющие размножаться в питательной среде бактериям — полимицин, неомицин, стрептомицин. Об этом следует знать тем, у кого в анамнезе есть аллергия на данные антибактериальные средства.
Вакцина Сэйбина широко применяется по всему миру и является единственной живой вакциной против полиовируса. Во многом благодаря ей большинство развитых стран на сегодняшний день объявлены ВОЗ зоной, свободной от полиомиелита. С 2002 года такой зоной был объявлен Европейский регион, в том числе и страны СНГ.
С 2002 года такой зоной был объявлен Европейский регион, в том числе и страны СНГ.
В календаре прививок против полиомиелита значатся две вакцины — ОПВ и ИПВ. В чём разница между ними? ИПВ — это инактивированная полиовакцина, которая содержит убитый (инактивированный) вирус. Её вводят при помощи инъекции. В то время как вакцина ОПВ содержит живой вирус полиомиелита и делается она перорально.
До 2010 года в России делалась вакцинация против полиомиелита при помощи исключительно инактивированных вакцин — это позволяла благополучная эпидемиологическая обстановка. Но в 2010 году в сопредельном Таджикистане произошла вспышка заболевания, а в России от полиомиелита умер один человек. В результате этого было принято решение о смешанной вакцинации. На первом году жизни детям вводят инактивированную полиомиелитную вакцину («Имовакс полио», «Полиорикс»), затем три дозы живой вакцины. Ревакцинация в старшем возрасте проводится только живой вакциной ОПВ.
Иногда можно встретить аббревиатуру: прививка r2 ОПВ — что это такое? Так обозначается вторая ревакцинация оральной полиовакциной, которую делают в возрасте 20 месяцев. А что за прививка r3 ОПВ? Соответственно, это ревакцинация №3, которую проводят детям в 14 лет.
А что за прививка r3 ОПВ? Соответственно, это ревакцинация №3, которую проводят детям в 14 лет.
Описание инструкции по применению вакцины ОПВ
По инструкции вакцина ОПВ предназначена для применения у детей в возрасте от трёх месяцев до 14 лет. В очагах инфекции вакцина может вводиться новорождённым непосредственно в родильных домах. Взрослых вакцинируют при въезде в неблагополучную зону.
Куда делают прививку ОПВ? Её вводят орально, то есть через рот.
Вакцина представляет собой жидкость розового цвета, расфасованную во флаконы по 25 доз (5 мл). Разовая доза равна 4 каплям, или 0,2 мл. Её забирают при помощи специальной пипетки или шприца и капают на корень языка грудничкам или на нёбные миндалины детям старшего возраста. Процедура введения вакцины должна проводиться таким образом, чтобы не провоцировать повышенное слюноотделение, срыгивание и рвоту. Если такая реакция все же произошла, то ребёнку вводят ещё одну дозу вакцины. Дело в том, что вирус должен «усвоиться» слизистой оболочкой ротовой полости и попасть в миндалины. Оттуда он проникает в кишечник и размножается, вызывая выработку иммунитета. Если вирус при внесении вышел со рвотой или его смыло слюной, то вакцинация будет неэффективна. При попадании в желудок вирус также обезвреживается желудочным соком и не достигает нужной цели. Если ребёнок срыгнул и после повторного нанесения вируса, то третий раз введение вакцины не повторяют.
Оттуда он проникает в кишечник и размножается, вызывая выработку иммунитета. Если вирус при внесении вышел со рвотой или его смыло слюной, то вакцинация будет неэффективна. При попадании в желудок вирус также обезвреживается желудочным соком и не достигает нужной цели. Если ребёнок срыгнул и после повторного нанесения вируса, то третий раз введение вакцины не повторяют.
ОПВ можно делать одновременно с другими вакцинами. Исключение составляют БЦЖ и вакцинные препараты, вводимые орально — например, «Ротатек». На выработку иммунитета к другим заболеваниям ОПВ не влияет и никак не сказывается на переносимость вакцин ребёнком.
Противопоказания и меры предосторожности
Нельзя вводить вакцину ОПВ в следующих случаях:
- иммунодефицитные состояния, в том числе ВИЧ, онкологические заболевания;
- если в ближайшем окружении ребёнка есть люди с ослабленным иммунитетом, а также беременные женщины;
- при неврологических осложнениях на предыдущие прививки ОПВ;
- под контролем врача проводят прививку при заболеваниях желудка и кишечника.

Респираторные инфекции, повышенная температура, другие незначительные ослабления иммунитета ребёнка требуют полного излечения перед введением ОПВ.
Поскольку ОПВ — вакцина, содержащая живой вирус, активно размножающийся в организме, то в течение некоторого времени привитый ребёнок может заражать неиммунных людей. В связи с этим прививка ОПВ требует соблюдения определённых правил при её применении, в других случаях её необходимо заменять на инактивированную вакцину.
- Если в семье есть дети в возрасте до 1 года, непривитые от полиомиелита (или дети, имеющие медотвод от вакцины), прививку лучше делать ИПВ.
- При проведении массовой вакцинации ОПВ, непривитых детей изолируют от коллектива на срок от 14 до 30 дней.
Также ОПВ в некоторые сроки заменяют на ИПВ в закрытых детских дошкольных учреждениях (детские дома, специализированные интернаты для детей, дома ребёнка), противотуберкулёзных санаториях, стационарных отделениях больниц.
Возможные осложнения
В очень редких случаях — примерно в одном на 750 000 — ослабленный вирус в вакцине ОПВ претерпевает изменения в организме и возвращается к типу, который может парализовать нервные клетки. Этот побочный эффект получил название ВАПП — вакциноассоциированный полиомиелит. ВАПП является грозным осложнением вакцины ОПВ.
Наиболее высок риск развития такого осложнения после первой вакцинации, меньше — после второй. Именно поэтому первые две прививки делают инактивированными вакцинами — от них ВАПП не развивается, а защита вырабатывается. У ребёнка, дважды привитого ИПВ, риск развития вакцинной инфекции практически отсутствует.
Первая реакция в случае появления ВАПП возникает с 5 по 14 день после введения капель. Осложнения на прививку ОПВ могут быть у людей с иммунодефицитом. Тогда ослабленная иммунная система не вырабатывает антител, защищающих от вируса, и он беспрепятственно размножается, вызывая серьёзное заболевание. Поэтому прививки живыми вакцинами в этом случае противопоказаны.
Поэтому прививки живыми вакцинами в этом случае противопоказаны.
Сроки вакцинации
По национальному календарю прививок вакцинацию против полиомиелита проводят в следующие сроки:
- в 3 и 4,5 месяца ребёнку делают инъекцию ИПВ;
- в 6 месяцев — живую ОПВ;
- первая ревакцинация ОПВ в 18 месяцев;
- вторая ревакцинация — в 20 месяцев;
- третья ревакцинация, последняя — прививка ОПВ в 14 лет.
Таким образом, ревакцинация ОПВ проводится трижды.
При желании родителей ребёнка вакцинации против полиомиелита, могут быть сделаны с применением инактивированных вакцин, на личные средства пациента.
Как подготовиться к вакцинации ОПВ
Вакцина ОПВ от полиомиелита требует подготовки к прививке. Обязателен осмотр у педиатра, оценка риска заражения других членов семьи (дети, беременные женщины) вакцинным вирусом.
Для того чтобы вакцина лучше усвоилась, ребёнка нельзя кормить и поить в течение одного часа до и после прививки.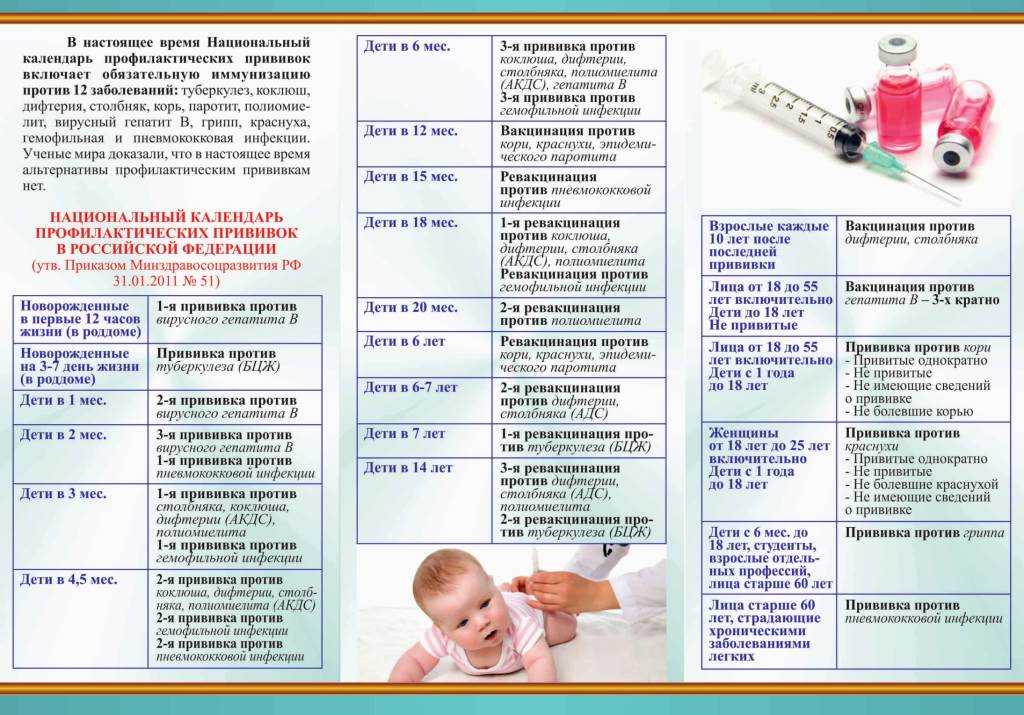
Реакция на вакцину ОПВ
Реакция на прививку ОПВ обычно не выражена — дети переносят её легко. В день прививки с ребёнком можно гулять, купать его и жить обычным распорядком.
Побочные действия прививки ОПВ могут проявляться небольшим расстройством стула (жидкий или учащённый) в течение нескольких дней после вакцинации, которое проходит без какого-либо вмешательства. Также, возможно, проявление слабых аллергических реакций — сыпи на коже. Иногда возникает тошнота, однократная рвота.
Температура после прививки ОПВ — нехарактерная реакция. Обычно она связана с другими факторами.
Подведём итоги всего вышесказанного. Прививка ОПВ — расшифровка определяется как «оральная полиовакцина». Это вакцина, содержащая живой вирус полиомиелита, вводится она капельками в рот. Нужна ли прививка от полиомиелита — решать в первую очередь родителям. Но нужно учесть, что медики не сомневаются в пользе массовой вакцинации, которая позволила в относительно короткие сроки (с 1960 годов по 1990-е) свести к минимуму проявление такого опасного заболевания, как полиомиелит. Даже в странах, которые уже в течение десятилетий свободны от болезни, вакцинацию от полиомиелита не прекращают. Чтобы исключить ВАПП и циркуляцию вакцинного вируса в популяции, там перешли на полный цикл использования инактивированных вакцин. В случае стабилизации эпидемиологической обстановки в России — планируется поступить так же.
Даже в странах, которые уже в течение десятилетий свободны от болезни, вакцинацию от полиомиелита не прекращают. Чтобы исключить ВАПП и циркуляцию вакцинного вируса в популяции, там перешли на полный цикл использования инактивированных вакцин. В случае стабилизации эпидемиологической обстановки в России — планируется поступить так же.
Реакция на оральную полиомиелитную вакцину у младенцев, находящихся на грудном вскармливании, с недоеданием и диареей
- Список журналов
- Рукописи авторов HHS
- PMC4936916
Вакцина. Авторская рукопись; доступно в PMC 2016 7 июля.
Опубликовано в окончательной редакции как:
Вакцина. 2014 16 января; 32(4): 478–482.
2014 16 января; 32(4): 478–482.
Published online 2013 Dec 2. doi: 10.1016/j.vaccine.2013.11.056
PMCID: PMC4936916
NIHMSID: NIHMS613588
PMID: 24300591
, a , b , b , B , C , B , B , B , A , A , A , D , D , D D , D , D D , D , D D , D , D D0028 , e и b, *
Информация об авторе Информация об авторских правах и лицензии Отказ от ответственности Причины этого недостаточно понятны. Мы проверили факторы риска плохой реакции на ОПВ у младенцев из городских трущоб Дакки, Бангладеш. Снижение реакции нейтрализации сыворотки на ОПВ, но не неэффективность внутримышечно вводимых вакцин, ассоциировалось с недоеданием, диареей и меньшей продолжительностью грудного вскармливания.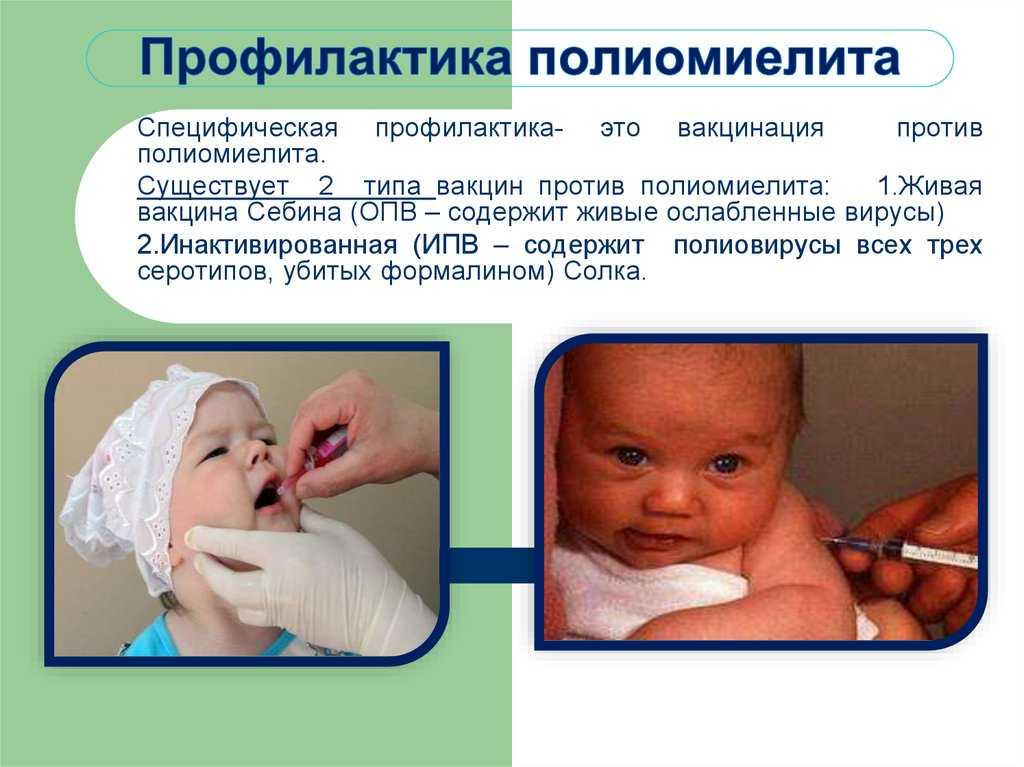 Дети с недоеданием (WAZ <-2) имели значительно более низкие титры OPV 3 ( р = 0,029). У детей, у которых было 2 или более эпизодов диареи в течение первых месяцев жизни, вероятность неудачи ОПВ была более чем в два раза выше, чем у детей, у которых был 1 эпизод диареи или не было диареи ( p = 0,0245). Напротив, каждый дополнительный месяц при исключительно грудном вскармливании был связан с увеличением титра ОПВ-3 на 0,41 ( р = 0,0072) и 0,16 ( р = 0,0065) при 25-м и 50-м процентилях титров ОПВ-3 соответственно. Эти данные согласуются с дефектом в индукции иммунитета в кишечнике к ОПВ, но не к парентеральным вакцинам, дефекту, который может частично поддаваться вмешательству путем поощрения исключительно грудного вскармливания.
Дети с недоеданием (WAZ <-2) имели значительно более низкие титры OPV 3 ( р = 0,029). У детей, у которых было 2 или более эпизодов диареи в течение первых месяцев жизни, вероятность неудачи ОПВ была более чем в два раза выше, чем у детей, у которых был 1 эпизод диареи или не было диареи ( p = 0,0245). Напротив, каждый дополнительный месяц при исключительно грудном вскармливании был связан с увеличением титра ОПВ-3 на 0,41 ( р = 0,0072) и 0,16 ( р = 0,0065) при 25-м и 50-м процентилях титров ОПВ-3 соответственно. Эти данные согласуются с дефектом в индукции иммунитета в кишечнике к ОПВ, но не к парентеральным вакцинам, дефекту, который может частично поддаваться вмешательству путем поощрения исключительно грудного вскармливания.
Пероральная вакцина против полиомиелита менее эффективна у детей в развивающихся странах [1]. По оценкам, эффективность трехвалентной ОПВ на дозу составляет 50% в США и только 21% в Индии [2]. Точно так же пероральная ротавирусная вакцина была вдвое менее эффективной в предотвращении тяжелой ротавирусной инфекции [3,4]. Гипотезы более низкой эффективности пероральной вакцинации в развивающихся странах включают недоедание, диарейные заболевания и экологическую энтеропатию [5–12]. Считается, что экологическая энтеропатия часто встречается у детей в развивающихся странах и патологически характеризуется укорочением ворсинок с увеличением интраэпителиальных лимфоцитов в тонкой кишке [9].–12]. Имеется мало данных об эффективности пероральных вакцин у детей с экологической энтеропатией, но было замечено, что ОПВ менее эффективна, если ее вводить во время эпизодов диареи [13]. Это свидетельствовало о потенциальной связи кишечной инфекции и энтеропатии с неэффективностью вакцины и побудило нас проверить такую связь у младенцев в Дакке, Бангладеш.
Гипотезы более низкой эффективности пероральной вакцинации в развивающихся странах включают недоедание, диарейные заболевания и экологическую энтеропатию [5–12]. Считается, что экологическая энтеропатия часто встречается у детей в развивающихся странах и патологически характеризуется укорочением ворсинок с увеличением интраэпителиальных лимфоцитов в тонкой кишке [9].–12]. Имеется мало данных об эффективности пероральных вакцин у детей с экологической энтеропатией, но было замечено, что ОПВ менее эффективна, если ее вводить во время эпизодов диареи [13]. Это свидетельствовало о потенциальной связи кишечной инфекции и энтеропатии с неэффективностью вакцины и побудило нас проверить такую связь у младенцев в Дакке, Бангладеш.
2.1. Продольная когорта рождения
Изучаемые дети были из городских трущоб Мирпур Тана в Дакке, Бангладеш. Субъекты были определены путем переписи беременных женщин в сообществе, проведенной обученными полевыми исследователями. Детей регистрировали в течение первой недели после рождения, начиная с января 2008 г. , а затем посещали домохозяйства два раза в неделю до достижения ими возраста одного года. Всего в когорту, получившую ОПВ (любое количество доз), вошли 435 детей. 314 детей получили не менее трех доз ОПВ к 12 месяцам, из них 258/314 получили 3 дозы к 6-месячному возрасту. Среднее количество доз было 3, а нижняя и верхняя квартили были 3 и 4 соответственно. Диарею определяли как три случая жидкого или неоформленного стула в течение 24 часов или по отчету матери у младенцев, находящихся на грудном вскармливании, в возрасте до одного года. Исключительно грудное вскармливание определялось ежемесячным отчетом матери о потреблении ее ребенком грудного молока без добавок (включая воду, но исключая лекарства). Исследование было одобрено комитетами по исследованиям и этике Международного центра исследований диарейных заболеваний, Бангладеш, Дакка, и Советом по институциональному обзору Университета Вирджинии. Было два предыдущих сообщения от этой когорты о кишечных инфекциях [14,15].
, а затем посещали домохозяйства два раза в неделю до достижения ими возраста одного года. Всего в когорту, получившую ОПВ (любое количество доз), вошли 435 детей. 314 детей получили не менее трех доз ОПВ к 12 месяцам, из них 258/314 получили 3 дозы к 6-месячному возрасту. Среднее количество доз было 3, а нижняя и верхняя квартили были 3 и 4 соответственно. Диарею определяли как три случая жидкого или неоформленного стула в течение 24 часов или по отчету матери у младенцев, находящихся на грудном вскармливании, в возрасте до одного года. Исключительно грудное вскармливание определялось ежемесячным отчетом матери о потреблении ее ребенком грудного молока без добавок (включая воду, но исключая лекарства). Исследование было одобрено комитетами по исследованиям и этике Международного центра исследований диарейных заболеваний, Бангладеш, Дакка, и Советом по институциональному обзору Университета Вирджинии. Было два предыдущих сообщения от этой когорты о кишечных инфекциях [14,15].
2.
 2. Антропометрия
2. Антропометрия
Вес и рост детей оценивали с помощью электронных весов и длинных досок с точностью до 10 г и 1 мм соответственно (SECA Gmbh & Co, Гамбург, Германия). Регистрировали среднее значение двух последовательных измерений. Они были преобразованы в массу тела к возрасту (WAZ) и длину тела к возрасту (LAZ) с использованием стандартов роста детей Многоцентрового эталонного исследования роста ВОЗ [16]. Недостаток веса определялся как WAZ <-2, а задержка роста как LAZ <-2.
2.3. История вакцинации и иммуногенность
Истории иммунизации были получены от матерей младенцев, и в анализ были включены только дети, получившие не менее трех прививок ОПВ. Сывороточные нейтрализующие антитела к штаммам полиомиелита 1–3 типа измеряли в CDC, Атланта, как описано ранее [17,18]. Во всех анализах OPV использовали титр log 2 . Уровни сывороточных IgG против столбняка, кори и дифтерии выражали в МЕ/мл и измеряли с помощью ИФА в соответствии с инструкциями производителя (Virion/Serion GmbH, Германия).
2.4. Статистический анализ
Ответ на пероральную вакцину против полиомиелита измеряли по нейтрализующим антителам в сыворотке у детей, получивших рекомендуемые минимум три дозы ОПВ в возрасте 6 месяцев (для измерения ответа на вакцину в течение 6 месяцев) или 12 месяцев (для измерения ответа на вакцину в течение 12 месяцев). ). Неэффективность вакцины определяли как титр менее 1:8 (log 2 [титр] < 3). Критерий Колмогорова-Смирнова использовали для оценки связи задержки роста с ОПВ и системным ответом на вакцину. Грудное вскармливание было протестировано как потенциальная переменная окружающей среды из-за его способности предотвращать кишечную инфекцию и способствовать развитию иммунной системы младенцев. Исключительно грудное вскармливание определялось как отсутствие прикорма какой-либо пищей или жидкостью, кроме грудного молока. Другие независимые предикторы включали статус питания в возрасте 6 месяцев (нормальный вес по сравнению с недостаточным весом), количество эпизодов диареи в течение первых 6 месяцев, а также доход семьи.
Принимая во внимание асимметричное распределение измерения титра ОПВ и цензурирование нижнего и верхнего пределов (2,5 и 10,5 соответственно по шкале log 2 ), была использована квантильная регрессия для оценки прогностического эффекта независимых переменных при непрерывном ответе ОПВ через 12 месяцев. В отличие от линейной регрессии, квантильная регрессия не предполагает распределения и более надежна при обработке экстремальных значений и выбросов, поэтому коэффициенты регрессии не изменяются в зависимости от ограничения переменной отклика для большинства процентилей. Из-за беспокойства по поводу потенциально ослабленного эффекта цензурированных показателей титра квантильная регрессия проводилась только для 25-го и 50-го процентилей ответа ОПВ. Кроме того, обобщенная линейная модель с GEE (т. е. продольная логистическая регрессия) использовалась для повторных неудач ОПВ через 6 и 12 месяцев. Повторные анализы неудач ОПВ через 6 и 12 месяцев моделируют взаимосвязь ковариат с ответом с течением времени и учитывают внутрисубъектные корреляции, и, таким образом, потенциально более эффективны, чем отдельные анализы в каждый момент времени. Статистическая значимость в этом исследовании была установлена на уровне p < 0,05, и все зарегистрированные значения p были двусторонними. Все анализы проводились с использованием SAS версии 9.3 (Институт SAS, Кэри, Северная Каролина).
Статистическая значимость в этом исследовании была установлена на уровне p < 0,05, и все зарегистрированные значения p были двусторонними. Все анализы проводились с использованием SAS версии 9.3 (Институт SAS, Кэри, Северная Каролина).
Мы проверили сниженную иммуногенность ОПВ в продольной проспективной когорте детей, наблюдаемых от рождения до одного года в городских трущобах Дакки, Бангладеш. Средний размер семьи составлял 5 человек, ежемесячный доход семьи составлял 6000 така (примерно 80 долларов США), а 40% матерей не имели никакого образования. Средняя продолжительность исключительно грудного вскармливания составляла примерно 4 месяца. Недостаточность питания присутствовала у 16% детей при рождении и у одной трети детей в возрасте 12 месяцев, что измерялось показателем массы тела для возраста (WAZ) <-2 (дополнительная таблица 1).
Неэффективность ОПВ типа 3 (log 2 [титр нейтрализующих антител в сыворотке] < 3) составила 13,6 и 7,3% для детей, получивших не менее 3 доз ОПВ в возрасте 6 и 12 месяцев соответственно. Напротив, частота неудач для вирусов типа 1 и 2 была ниже, как и ожидалось из предыдущего опыта с этой вакциной (дополнительная рис. 1). Поэтому наши анализы были сосредоточены на титре OPV 3.
Напротив, частота неудач для вирусов типа 1 и 2 была ниже, как и ожидалось из предыдущего опыта с этой вакциной (дополнительная рис. 1). Поэтому наши анализы были сосредоточены на титре OPV 3.
Недоедание, измеряемое как масса тела для данного возраста, более чем на 2 стандартных отклонения ниже нормы ВОЗ (WAZ < -2), обратно ассоциировалось с титром ОПВ 3 в возрасте 12 месяцев ( н = 314; р = 0,0289) (). Напротив, реакция антител на внутримышечно введенные вакцины против кори, столбняка и дифтерии у недоедающих младенцев не отличалась (). Число преждевременных родов не измерялось, поэтому влияние преждевременных родов на ответ на ОПВ неизвестно. HAZ ≥-2 через 6 месяцев оказался положительно связанным с титром OPV 3 через 12 месяцев, хотя он был лишь незначительно значимым для 50-го процентиля ( p = 0,07) и статистически не значим для 25-го процентиля ( p = 0,07).0013 p = 0,45) (данные не показаны).
Открыть в отдельном окне
Реакция на оральную полиомиелитную вакцину типа 3 и парентеральную вакцину у детей с нормальным питанием и детей с истощением. Титры сывороточных нейтрализующих антител в ответ на ОПВ типа 3 и парентерально вводимые вакцины в возрасте 12 месяцев у детей с оценкой WAZ <-2 сравнивались с титрами с WAZ >-2 в возрасте 6 месяцев ( n = 314 p = 0,0289 для ОПВ, n = 435 и p = NS для ответов на вакцины против дифтерии, столбняка и кори; критерий порядка рангов Колмогорова-Смирнова).
Титры сывороточных нейтрализующих антител в ответ на ОПВ типа 3 и парентерально вводимые вакцины в возрасте 12 месяцев у детей с оценкой WAZ <-2 сравнивались с титрами с WAZ >-2 в возрасте 6 месяцев ( n = 314 p = 0,0289 для ОПВ, n = 435 и p = NS для ответов на вакцины против дифтерии, столбняка и кори; критерий порядка рангов Колмогорова-Смирнова).
Исключительно грудное вскармливание положительно ассоциировалось с титром ОПВ 3 через 12 месяцев, что определялось методом квантильной регрессии (). В частности, прогнозировалось, что при 25-м и 50-м процентилях титра 3 ОПВ каждый дополнительный месяц исключительно грудного вскармливания будет увеличивать титр 3 ОПВ на 0,36 (95% доверительный интервал (ДИ): 0,16–0,57, p = 0,0006) и 0,13 ( 95% ДИ: 0,02–0,23, p = 0,019) соответственно.
Открыть в отдельном окне
Связь исключительно грудного вскармливания с реакцией на пероральную полиомиелитную вакцину типа 3 (на уровне 25-го и 50-го процентилей). Из-за неравномерного распределения показателя титра 3 ОПВ (первый квартиль и медиана 7,83 и 9,67 соответственно) был проведен квантильный регрессионный анализ для оценки прогностического эффекта исключительно грудного вскармливания на титр 3 ОПВ в возрасте 12 месяцев ( n = 314). ). Продолжительность исключительно грудного вскармливания достоверно предсказывала увеличение показателя титра ОПВ, при этом эффект был более выражен в первом квартиле.
Из-за неравномерного распределения показателя титра 3 ОПВ (первый квартиль и медиана 7,83 и 9,67 соответственно) был проведен квантильный регрессионный анализ для оценки прогностического эффекта исключительно грудного вскармливания на титр 3 ОПВ в возрасте 12 месяцев ( n = 314). ). Продолжительность исключительно грудного вскармливания достоверно предсказывала увеличение показателя титра ОПВ, при этом эффект был более выражен в первом квартиле.
Результаты многопараметрической квантильной регрессии для непрерывного титра OPV типа 3 суммированы в . Независимые переменные в этом исследовании включали эпизоды диареи, WAZ в 6 месяцев, продолжительность исключительно грудного вскармливания в первые 6 месяцев и доход семьи. Традиционная линейная регрессия для титра OPV 3 моделирует влияние независимых переменных на условное среднее значение титра OPV 3; однако, поскольку у большинства детей наблюдался серо-ответ, а распределение титров ОПВ-3 было асимметричным с первым квартилем и средними значениями 7,83 и 9. 67, нижние условные квантили более важны для ответа на такие вопросы, как влияние этих независимых переменных на титр ОПВ 3 по-разному у детей с низкими титрами и у детей со средними титрами, у которых ОПВ неэффективна. Таким образом, наш регрессионный анализ был сосредоточен на подгонке условных квантилей титра OPV 3 на уровне 25-го и 50-го процентилей. Скорректированный анализ показал, что как недоедание в возрасте 6 месяцев, так и более короткое исключительно грудное вскармливание в течение первых 6 месяцев жизни были отрицательно связаны с титром ОПВ, и эффекты были сильнее в первом квартиле. По сравнению с детьми, страдающими от недоедания, у нормальных детей было 2,35 (95% ДИ: 0,66–4,03, p = 0,0065) и 1,11 (95% ДИ: 0,31–1,90, p = 0,0063) более высокий титр 3 ОПВ соответствует 25-му и 50-му процентилю ответа ОПВ соответственно. Более того, каждый дополнительный месяц исключительно грудного вскармливания был связан с увеличением титра ОПВ 3 на 0,4 (95% ДИ: 0,11–0,71, p = 0,0072) и 0,16 (95% ДИ: 0,05–0,28, p = 0,0065).
67, нижние условные квантили более важны для ответа на такие вопросы, как влияние этих независимых переменных на титр ОПВ 3 по-разному у детей с низкими титрами и у детей со средними титрами, у которых ОПВ неэффективна. Таким образом, наш регрессионный анализ был сосредоточен на подгонке условных квантилей титра OPV 3 на уровне 25-го и 50-го процентилей. Скорректированный анализ показал, что как недоедание в возрасте 6 месяцев, так и более короткое исключительно грудное вскармливание в течение первых 6 месяцев жизни были отрицательно связаны с титром ОПВ, и эффекты были сильнее в первом квартиле. По сравнению с детьми, страдающими от недоедания, у нормальных детей было 2,35 (95% ДИ: 0,66–4,03, p = 0,0065) и 1,11 (95% ДИ: 0,31–1,90, p = 0,0063) более высокий титр 3 ОПВ соответствует 25-му и 50-му процентилю ответа ОПВ соответственно. Более того, каждый дополнительный месяц исключительно грудного вскармливания был связан с увеличением титра ОПВ 3 на 0,4 (95% ДИ: 0,11–0,71, p = 0,0072) и 0,16 (95% ДИ: 0,05–0,28, p = 0,0065). ) в 25-м и 50-м процентилях соответственно. Ни количество эпизодов диареи, ни доход семьи не были значимо связаны с продолжительным титром ОПВ типа 3 в этом многопараметрическом анализе. Мы пришли к выводу, что более низкая иммуногенность, но не неэффективность вакцины ОПВ типа 3, была связана с недоеданием и более короткой продолжительностью исключительно грудного вскармливания. Неэффективность вакцины ОПВ типа 3 была связана с диареей, как обсуждается ниже.
) в 25-м и 50-м процентилях соответственно. Ни количество эпизодов диареи, ни доход семьи не были значимо связаны с продолжительным титром ОПВ типа 3 в этом многопараметрическом анализе. Мы пришли к выводу, что более низкая иммуногенность, но не неэффективность вакцины ОПВ типа 3, была связана с недоеданием и более короткой продолжительностью исключительно грудного вскармливания. Неэффективность вакцины ОПВ типа 3 была связана с диареей, как обсуждается ниже.
Таблица 1
Связь независимых переменных с титрами непрерывной пероральной полиовакцины типа 3 через 12 месяцев a .
| Характеристики | Регрессия 25-го квантиля | 50-я квантильная регрессия | ||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Эффект | 95% CI | P -Value | 95% CI | 9 | 95% CI | -PA| 95% CI | -PA | 95% CI | -PA | 95% CI | -PA | 95% CI | 95% | 95% | . |  0199 0199 3.73 | (1.21, 6.25) | 0.0039 | 8.54 | (7.53, 9.55) | <.0001 | | ||||
| ≥2 diarrhea episodes in 1st 6 months | −0.23 | (−1.26, 0. 80) | 0.6599 | −0.17 | (−0.66, 0.33) | 0.5116 | ||||||||||||||||||||
| WAZ ≥−2 at 6 months | 2. 35 35 | (0.66, 4.03) | 0.0065 | 1.11 | (0,31, 1,90) | 0,0063 | ||||||||||||||||||||
| Breastfeeding duration in 1st 6 months | 0.41 | (0.11, 0.71) | 0.0072 | 0.16 | (0.05, 0.28) | 0.0065 | ||||||||||||||||||||
| Family income (1000 Taka) b | 0. 05 05 | (−0.05, 0.15) | 0.3717 | −0.03 | (−0.08, 0.02) | 0.2159 | ||||||||||||||||||||
Open in a separate window
a Type 3 titer at 12 months возраста анализировали как непрерывный результат в квантильной регрессии ( н = 314).
b Доход семьи был стандартизирован в 1000 така, так что ожидаемый эффект интерпретировался как изменение титров типа 3 на каждые 1000 така (один така равен примерно 0,013 доллара США).
Мы также проверили прогностический эффект переменных окружающей среды, связанный с вероятностью повторного отсутствия сероконверсии в тип 3 в возрасте 6 и 12 месяцев, определяемый как log 2 [титр] < 3. Многофакторная продольная логистическая регрессия показала что диарея в первые 6 месяцев жизни в значительной степени связана с риском неудачи ОПВ-3. По сравнению с теми, у кого был 1 эпизод диареи или не было диареи, дети, у которых было 2 или более эпизодов диареи в течение 1-го месяца жизни, имели отношение шансов (ОШ) = 2,35 для неудачи (9).5% ДИ: 1,12–4,94, p = 0,0245) (дополнительная таблица 2). Диарея не зависела от низкой массы тела при рождении (ранее было показано, что она является фактором риска диареи в этой когорте (14)) в качестве предиктора неэффективности ОПВ. Доход семьи, по-видимому, был незначительно связан с неудачей ОПВ, поскольку каждые 1000 така увеличивали вероятность неудачи ОПВ на 12% (ОШ = 0,88, 95% ДИ: 0,77–1,01, p = 0,0599).
Многофакторная продольная логистическая регрессия показала что диарея в первые 6 месяцев жизни в значительной степени связана с риском неудачи ОПВ-3. По сравнению с теми, у кого был 1 эпизод диареи или не было диареи, дети, у которых было 2 или более эпизодов диареи в течение 1-го месяца жизни, имели отношение шансов (ОШ) = 2,35 для неудачи (9).5% ДИ: 1,12–4,94, p = 0,0245) (дополнительная таблица 2). Диарея не зависела от низкой массы тела при рождении (ранее было показано, что она является фактором риска диареи в этой когорте (14)) в качестве предиктора неэффективности ОПВ. Доход семьи, по-видимому, был незначительно связан с неудачей ОПВ, поскольку каждые 1000 така увеличивали вероятность неудачи ОПВ на 12% (ОШ = 0,88, 95% ДИ: 0,77–1,01, p = 0,0599).
Наиболее важным результатом этого исследования является связь сниженной иммуногенности вируса ОПВ типа 3 с недостаточным питанием, более короткой продолжительностью исключительно грудного вскармливания и диареей. В противоположность этому, эти три переменные не влияли на иммуногенность вакцин, вводимых внутримышечно. Таким образом, это исследование бедных младенцев в Бангладеш указывает на специфический дефект иммунного ответа на пероральную вакцину против полиомиелита. Примечательно, что характеристики, связанные с недостаточной эффективностью ОПВ, являются уникальными для условий развивающихся стран, где до 40% детей недоедают, диарея является основной причиной смерти, а продолжительность грудного вскармливания неоптимальна [19].,20].
В противоположность этому, эти три переменные не влияли на иммуногенность вакцин, вводимых внутримышечно. Таким образом, это исследование бедных младенцев в Бангладеш указывает на специфический дефект иммунного ответа на пероральную вакцину против полиомиелита. Примечательно, что характеристики, связанные с недостаточной эффективностью ОПВ, являются уникальными для условий развивающихся стран, где до 40% детей недоедают, диарея является основной причиной смерти, а продолжительность грудного вскармливания неоптимальна [19].,20].
Давно признано, что ОПВ менее иммуногенна в развивающихся странах. Например, вспышки паралитического полиомиелита имели место в развивающихся странах, несмотря на высокий процент иммунизированных детей, при этом оценки иммуногенности однократной дозы трехвалентной ОПВ менее чем вдвое меньше, чем в развитых странах [1,2]. Это нарушение иммунного ответа на ОПВ в развивающихся странах было преодолено путем введения детям до 10 доз, хотя это обременительно для системы общественного здравоохранения. Ценность этого исследования заключается в том, что оно указывает на недоедание и диарею, проблемы, которые несоразмерно затрагивают детей в развивающихся странах, в качестве возможных объяснений. Он также предлагает потенциальные возможности для повышения эффективности ОПВ, что может включать увеличение продолжительности исключительно грудного вскармливания и улучшение питания.
Ценность этого исследования заключается в том, что оно указывает на недоедание и диарею, проблемы, которые несоразмерно затрагивают детей в развивающихся странах, в качестве возможных объяснений. Он также предлагает потенциальные возможности для повышения эффективности ОПВ, что может включать увеличение продолжительности исключительно грудного вскармливания и улучшение питания.
Взаимодействие с ОПВ при грудном вскармливании изучалось в прошлом. Работа, проведенная в развитых странах, показала, что у детей, находящихся на грудном вскармливании, реакция нейтрализующих антител в сыворотке крови на ОПВ была выше, чем у детей, находящихся на искусственном вскармливании [21,22]. Воздержание от грудного вскармливания во время иммунизации (для проверки противоположной гипотезы о том, что антитела IgA к полиомиелиту материнского грудного молока могут мешать вакцинации ОПВ) не влияло на титры ОПВ [23]. Таким образом, совокупность данных как по развивающимся (данный отчет), так и по развитым странам согласуется с тем, что грудное вскармливание выгодно для иммуногенности ОПВ.
Обнадеживает то, что исследование иллюстрирует потенциальные вмешательства для улучшения эффективности ОПВ. Например, пропаганда исключительно грудного вскармливания может представлять собой легко реализуемое вмешательство. Сниженная иммуногенность ОПВ, а не вакцин против кори, дифтерии или столбняка, также свидетельствует о том, что очевидный кишечный барьер для иммунизации можно преодолеть с помощью парентеральной вакцинации.
Дополнение
Нажмите здесь для просмотра. (1.2M, pdf)
Мы благодарим семьи Мирпура за их участие и поддержку исследования. Роланд Саттер, Уолтер Оренштейн, Пирей Огра, Том Брюэр, Крис Уилсон, Ник Грассли и Джейкоб Джон были бесценными источниками советов. Мы благодарим Уильяма С. Хендли, Йитинга Чжана, Шарлу Л. Макдональд и Дебору Д. Мур за проведение реакции нейтрализующих антител сыворотки. При поддержке NIH Grant AI-43596 и Фондом Билла и Мелинды Гейтс.
Дополнительный материал, относящийся к этой статье, можно найти в онлайн-версии по адресу http://dx. doi.org/10.1016/j.vaccine.2013.11.056.
doi.org/10.1016/j.vaccine.2013.11.056.
Конфликт интересов : Авторы заявляют об отсутствии конфликта интересов.
1. Grassly NC, Jafari H, Bahl S, et al. Бессимптомная полиовирусная инфекция дикого типа в Индии среди детей, которым ранее была сделана пероральная вакцинация против полиомиелита. J заразить дис. 2010; 201:1535–43. [PubMed] [Академия Google]
2. Grassly NC, Fraser C, Wenger J, et al. Новые стратегии ликвидации полиомиелита в Индии. Наука. 2006; 314:1150–3. [PubMed] [Google Scholar]
3. Zaman K, Anh DD, Victor JC, et al. Эффективность пятивалентной ротавирусной вакцины против тяжелого ротавирусного гастроэнтерита у младенцев в развивающихся странах Азии: рандомизированное двойное слепое плацебо-контролируемое исследование. Ланцет. 2010; 376: 615–23. [PubMed] [Google Scholar]
4. Madhi SA, Cunliffe NA, Steele D, et al. Влияние ротавирусной вакцины человека на тяжелую диарею у африканских младенцев. N Engl J Med. 2010;362:289–98. [PubMed] [Google Scholar]
[PubMed] [Google Scholar]
5. Парашар У.Д., Гласс Р.И. Ротавирусные вакцины — первые вопросы об успехе остаются под вопросом. N Engl J Med. 2009; 360:1063–5. [PubMed] [Google Scholar]
6. Джон Дж.Т. Оральная вакцинация против полиомиелита у детей в тропиках. II. Реакция антител на вакциновирусную инфекцию. Am J Эпидемиол. 1975; 102: 414–21. [PubMed] [Google Scholar]
7. Zaman K, Sack DA, Yunus M, et al. Успешное совместное введение вакцины против ротавируса человека и пероральной полиовирусной вакцины бангладешским младенцам по 2-дозовой схеме в возрасте 12 и 16 недель. вакцина. 2009 г.;27:1333–9. [PubMed] [Google Scholar]
8. Panter-Brick C, Lunn PG, Langford RM, et al. Пути, ведущие к раннему замедлению роста: исследование важности повреждения слизистой оболочки и иммуностимуляции в различных социально-экономических группах в Непале. Брит Джей Нутр. 2009; 101: 558–67. [PubMed] [Google Scholar]
9. Korpe P, Petri WA, Jr Экологическая энтеропатия: критические последствия плохо изученного состояния. Тренды Мол Мед. 2012;18:328–36. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Тренды Мол Мед. 2012;18:328–36. [Бесплатная статья PMC] [PubMed] [Google Scholar]
10. Veitch AM, Kelly P, Zulu IS, et al. Тропическая энтеропатия: гиперпластическая энтеропатия, опосредованная Т-клетками. Eur J Гастроэнтерол Гепатол. 2001; 13:1175–81. [PubMed] [Google Scholar]
11. Campbell DI, Murch SH, Elia M, et al. Хроническая энтеропатия, опосредованная Т-клетками, у детей из сельских районов Западной Африки: связь с состоянием питания и функцией тонкой кишки. Педиатр рез. 2003; 54: 306–11. [PubMed] [Google Scholar]
12. Papasavvas E, Pistilli M, Reynolds G, et al. Отсроченная потеря контроля над уровнем липополисахаридов в плазме после прерывания терапии у хронически инфицированных ВИЧ-1 пациентов. СПИД. 2009 г.;23:369–75. [Бесплатная статья PMC] [PubMed] [Google Scholar]
13. Myaux JA, Unicomb L, Besser RE, et al. Влияние диареи на гуморальный ответ на пероральную вакцинацию против полиомиелита. Pediatr Infect Dis J. 1996; 15: 204–9. [PubMed] [Google Scholar]
14. Mondal D, Minak J, Alam M, et al. Вклад кишечной инфекции, измененной барьерной функции кишечника и недостаточности питания матерей в недоедание младенцев в Бангладеш. Клин Инфекция Дис. 2012;54:185–92. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Mondal D, Minak J, Alam M, et al. Вклад кишечной инфекции, измененной барьерной функции кишечника и недостаточности питания матерей в недоедание младенцев в Бангладеш. Клин Инфекция Дис. 2012;54:185–92. [Бесплатная статья PMC] [PubMed] [Google Scholar]
15. Korpe PS, Liu Y, Siddique A, et al. Проспективное когортное исследование паразитоспецифических антител к грудному молоку и защиты от кишечной протозойной инфекции у младенцев в Бангладеш, находящихся на грудном вскармливании. Клин Инфекция Дис. 2013;56:988–92. [Бесплатная статья PMC] [PubMed] [Google Scholar]
16. Всемирная организация здравоохранения. Многоцентровое исследование эталонов роста ВОЗ (МИЭР) Интернет: http://www.who.int/childgrowth/mgrs/en/ (по состоянию на 13 января 2013 г.).
17. ВОЗ Совместная исследовательская группа по оральным и инактивированным вакцинам против полиомиелита. Комбинированная иммунизация младенцев пероральными и инактивированными вакцинами против полиомиелита: результаты рандомизированного исследования в Гамбии, Омане и Таиланде. J заразить дис. 1997;175:S215–27. [PubMed] [Google Scholar]
J заразить дис. 1997;175:S215–27. [PubMed] [Google Scholar]
18. Отчет неофициальной консультации ВОЗ по анализу антител, нейтрализующих полиомиелит, Нэшвилл, 5–6 декабря 1991 г. Женева: Всемирная организация здравоохранения; 1991. Расширенная программа иммунизации. [Google Scholar]
19. Petri WA, Jr, Miller M, Binder HJ, et al. Кишечные инфекции, диарея и их влияние на функцию и развитие. Джей Клин Инвест. 2008; 118:1277–90. [Бесплатная статья PMC] [PubMed] [Google Scholar]
20. Sutter RW, John TJ, Jain H, et al. Иммуногенность двухвалентной пероральной вакцины против полиомиелита типов 1 и 3: рандомизированное двойное слепое контролируемое исследование. Ланцет. 2010; 376:1682–8. [PubMed] [Академия Google]
21. Пикеринг Л.К., Гранофф Д.М., Эриксон Дж.Р. и соавт. Модуляция иммунной системы грудным молоком и детской смесью, содержащей нуклеотиды. Педиатрия. 1998; 101: 242–9. [PubMed] [Google Scholar]
22. Hahn-Zoric M, Fulconis F, Minoli I, et al. Реакция антител на парентеральные и пероральные вакцины снижается при использовании обычных и низкобелковых смесей по сравнению с грудным вскармливанием. Acta Pediatr Scand. 1990;79:42. [PubMed] [Google Scholar]
Реакция антител на парентеральные и пероральные вакцины снижается при использовании обычных и низкобелковых смесей по сравнению с грудным вскармливанием. Acta Pediatr Scand. 1990;79:42. [PubMed] [Google Scholar]
23. John TJ, Devarajan LV, Luther L, et al. Влияние грудного вскармливания на сероответ младенцев на пероральную вакцинацию против полиомиелита. Педиатрия. 1976;57:47–53. [PubMed] [Академия Google]
Вакцинация и грудное вскармливание | JAMA
Вакцинация и грудное вскармливание | ДЖАМА | Сеть ДЖАМА
[Перейти к навигации]
Эта проблема
- Скачать PDF
- Полный текст
Поделиться
Твиттер
Фейсбук
Эл. адрес
адрес
LinkedIn- Процитировать это
- Разрешения
Артикул
19 ноября 1982 г.
Роберт Ким-Фарли, MD, MPH ; Эдвард Бринк, MD ; Уолтер Оренштейн, MD ; и другие
Кеннет Барт, MD, MPH
Принадлежности автора
Центры по контролю за заболеваниями Атланты
ДЖАМА. 1982;248(19):2451-2452. дои: 10.1001/jama.1982.033301
019
Полный текст
Абстрактный
В редакцию.—
В недавней книге для врачей, медсестер и другого медицинского персонала правильно указано, что вакцины против дифтерии, столбняка, коклюша (АКДС), краснухи, эпидемического паротита и кори следует вводить детям, находящимся на грудном вскармливании, в установленное время.


 адрес
адрес