Содержание
Осложнения во время химиотерапии. Нейтропения
Во время химиотерапии у пациента обычно возникают осложнения разной степени выраженности. Опытный врач обязательно объяснит, как избежать побочных эффектов лечения или снизить их интенсивность, но есть вещи, о которых нужно помнить всегда.
Нейтропения — это снижение количества циркулирующих в крови нейтрофилов, подвида лейкоцитов (белых кровяных клеток), которые отвечают за непосредственный контакт с инфекционным возбудителем и его уничтожение. Другими словами, нейтрофилы — это защита нашего организма.
Нейтропения при химиотерапии возникает из-за повреждения быстроделящихся клеток костного мозга и, как следствие, недостаточного количества нейтрофилов в крови. В целом это нормальный процесс — костный мозг восполняет дефицит, но глубина и длительность нейтропении зависит от множества факторов: в большей степени от режима химиотерапии, возраста пациента и его сопутствующей патологии.
Количество нейтрофилов обычно начинает снижаться примерно через неделю после начала каждого цикла химиотерапии. Уровень нейтрофилов достигает нижней точки через 7-14 дней после лечения. Это явление носит название «надир» и является точкой наибольшего риска по развитию инфекции. Затем количество нейтрофилов снова начинает расти — костный мозг возобновляет нормальную выработку нейтрофилов. Но для достижения нормального уровня может потребоваться 3-4 недели.
Уровень нейтрофилов достигает нижней точки через 7-14 дней после лечения. Это явление носит название «надир» и является точкой наибольшего риска по развитию инфекции. Затем количество нейтрофилов снова начинает расти — костный мозг возобновляет нормальную выработку нейтрофилов. Но для достижения нормального уровня может потребоваться 3-4 недели.
Снижение абсолютного числа нейтрофилов (АЧН) ниже 0,5 тыс/мкл (нижний порог нормы 2 тыс/мкл) чревато риском развития инфекции, в том числе и тяжелой. И чем старше пациент, тем выше риск.
Одно из самых важных и потенциально опасных осложнений химиотерапии — фебрильная нейтропения. Ее можно избежать, если знать, что делать.
При нейтропении системная реакция организма на инфекцию чаще всего сначала ограничена лихорадкой. Вот почему важно регулярно сдавать общий анализ крови в процессе химиотерапии и следить за температурой тела. Если при химиотерапии возникло повышение температуры выше 38°C на фоне снижения АЧН ниже 0,5 тыс/мкл, нужно незамедлительно сообщить об этом лечащему врачу, начать лечение антибиотиками широкого спектра и гранулоцитарными колониестимулирующими факторами.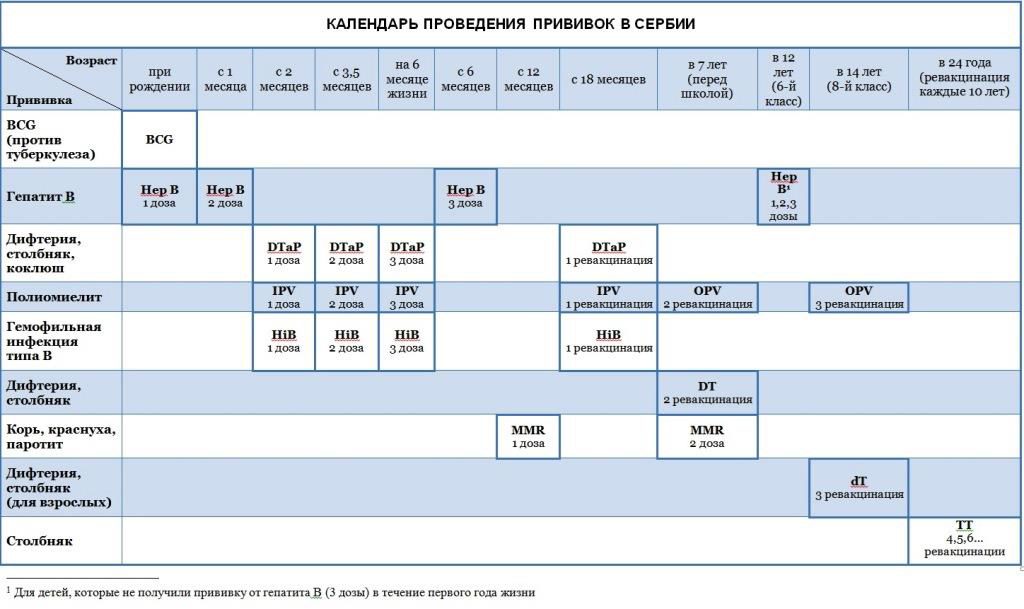
Ранее считалось, то все пациенты в таком состоянии должны быть госпитализированы. Сегодня есть определенные прогностические калькуляторы, которые определяют возможность лечиться амбулаторно, но с четкими рекомендациями по мониторингу состояния.
Фебрильная нейтропения — это опасное состояние, которое без лечения может осложниться сепсисом и даже летальным исходом.
1. Нейтропения может угрожать жизни.
В России статистика по нейтропении, возникающей вследствие проведения химиотерапии, не ведется. Но в США, где анализируют эти данные, нейтропения становится причиной госпитализации 60 000 онкологических пациентов ежегодно. Каждый 14-й пациент умирает от осложнений, связанных с этим состоянием.
2. Дни повышенного риска.
Нейтропения может развиться через 7-12 дней после начала каждого цикла химиотерапии.
3. Почему вы находитесь в зоне риска развития нейтропении?
Химиотерапия убивает как ненормальные (раковые), так и нормальные (в том числе ответственные за иммунитет) клетки в вашем организме. Когда это случается, риск развития инфекционного заболевания увеличивается.
Когда это случается, риск развития инфекционного заболевания увеличивается.
4. Инфекции при нейтропении могут быстро прогрессировать.
Контролируйте температуру тела. Немедленно свяжитесь с врачом, если на фоне химиотерапии у вас поднялась температура выше 38°С.
Если предполагается госпитализация, обязательно сообщите врачам, что у вас онкологическое заболевание и вы проходите химиотерапию.
5. Как вы можете предотвратить инфекцию:
- чаще мойте руки;
- поговорите с врачом о необходимости вакцинации от гриппа;
- принимайте ванну или душ каждый день, используйте нейтральный (без отдушек) лосьон для тела, чтобы снизить риск сухости кожи и появления на ней трещин;
- спросите своего врача, что нужно делать, если количество белых кровяных телец (лейкоцитов и, самое главное, — нейтрофилов) сильно снизится.
Автор:
Абсалямов Руслан Ильдарович
врач-онколог
Удар по лимфоцитам: COVID вызывает длительные сбои работы иммунитета | Статьи
Ученые из КНР предупреждают: многие переболевшие коронавирусом пациенты могут столкнуться с проблемами восстановления иммунитета. У части из них наблюдается снижение уровня лимфоцитов в крови, число которых не достигает нормы даже через 11 недель после выздоровления. Хроническое повреждение этих иммунных клеток чаще всего вызывает ВИЧ. Однако российские специалисты говорят, что, в отличие от вируса иммунодефицита человека, SARS-CoV-2 не способен размножаться в лимфоцитах. Поэтому описанные нарушения работы защитной системы организма могут носить длительный, но не перманентный характер.
У части из них наблюдается снижение уровня лимфоцитов в крови, число которых не достигает нормы даже через 11 недель после выздоровления. Хроническое повреждение этих иммунных клеток чаще всего вызывает ВИЧ. Однако российские специалисты говорят, что, в отличие от вируса иммунодефицита человека, SARS-CoV-2 не способен размножаться в лимфоцитах. Поэтому описанные нарушения работы защитной системы организма могут носить длительный, но не перманентный характер.
Атака на защитников
Ученые из Института вирусологии Уханя опубликовали препринт научной статьи, в которой говорится о проведенном исследовании воздействия коронавируса на лимфоциты, — клетки крови, отвечающие за иммунитет.
Как сказано в аннотации к препринту, лимфопения (временное или стойкое снижение уровня лимфоцитов в крови. — «Известия») является типичным симптомом у пациентов с COVID-19. Ученые изучили состояние 55 выздоровевших от коронавирусной инфекции людей, чтобы узнать, как меняется со временем количество иммунных клеток в их крови.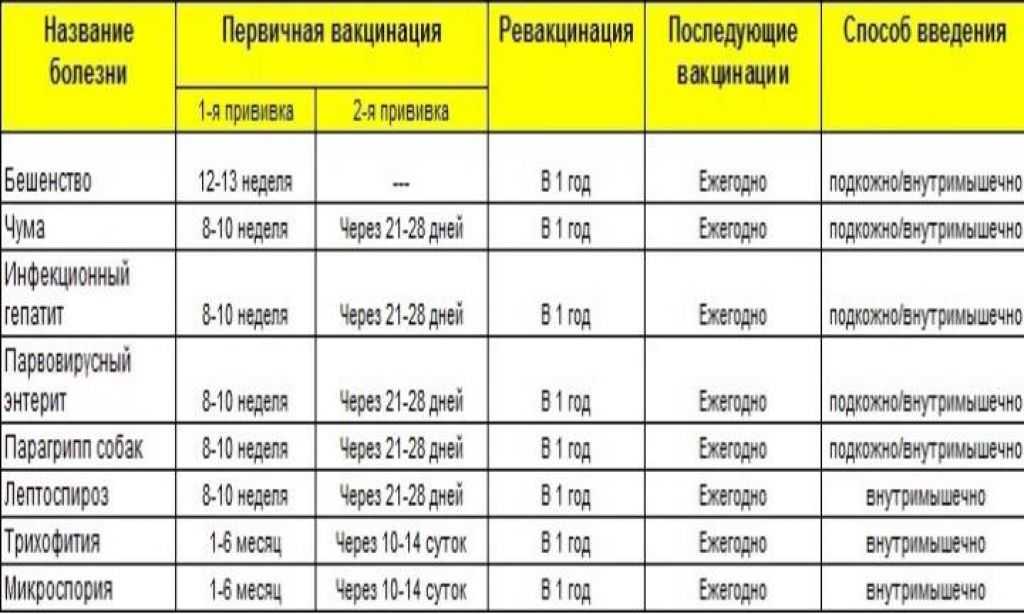
Фото: REUTERS/Manuel Claure
«У пациентов с COVID-19 всё еще наблюдались значительные фенотипические изменения в лимфоцитах после клинического выздоровления через 4–11 недель. Это говорит о том, что инфекция SARS-CoV-2 глубоко влияет на лимфоциты и приводит к длительным потенциальным дисфункциям», — сказано в тексте.
Причем пациенты не показали даже тенденции к восстановлению числа лимфоцитов в течение всего периода наблюдения. Российские ученые подтверждают, что стойкое снижение уровня лимфоцитов в крови может быть следствием перенесенного вирусного заболевания. Однако механизмы, вызывающие потерю отдельных популяций иммунных клеток, пока еще хорошо не изучены, сообщил «Известиям» младший научный сотрудник лаборатории экспериментальной хирургии и онкологии Курского государственного медицинского университета Давид Наимзада.
— Известно, что их перманентная потеря может вызываться не только хроническими инфекциями, — пояснил ученый.
Бойцы невидимого фронта
Сама по себе лимфопения встречается при различных патологических состояниях: вследствие длительной вирусной инфекции, иммунодефицита, патологий костного мозга и т. д. Наиболее частым инфекционным заболеванием, вызывающим снижение лимфоцитов, является СПИД, при котором разрушаются пораженные ВИЧ CD4 Т-клетки (CD4 расшифровываются как cluster of differentiation, — это особая группа Т-клеток, а именно Т-хелперов, которые помогают другим клеткам уничтожать инфицирующие организмы). Однако в этом случае повреждения иммунной системы носят хронический характер.
д. Наиболее частым инфекционным заболеванием, вызывающим снижение лимфоцитов, является СПИД, при котором разрушаются пораженные ВИЧ CD4 Т-клетки (CD4 расшифровываются как cluster of differentiation, — это особая группа Т-клеток, а именно Т-хелперов, которые помогают другим клеткам уничтожать инфицирующие организмы). Однако в этом случае повреждения иммунной системы носят хронический характер.
Фото: ИЗВЕСТИЯ/Павел Бедняков
В случае же с коронавирусом речь идет о хоть и длительной, но обратимой дисфункции иммунитета. Когда человек заражается новым патогеном, в его организме происходит экспансия лимфоцитов. Это своего рода солдаты, которые должны бороться с вредоносным вирусом, пояснил «Известиям» руководитель лаборатории геномной инженерии МФТИ (вуз— участник проекта «5-100») Павел Волчков.
— А после инфекции в организме происходит «демобилизация», так как такое количество активированных Т-клеток и В-клеток уже не нужно, подчеркнул эксперт. — После активации иммунные клетки живут недолго, а затем исчезают либо становятся «клетками памяти».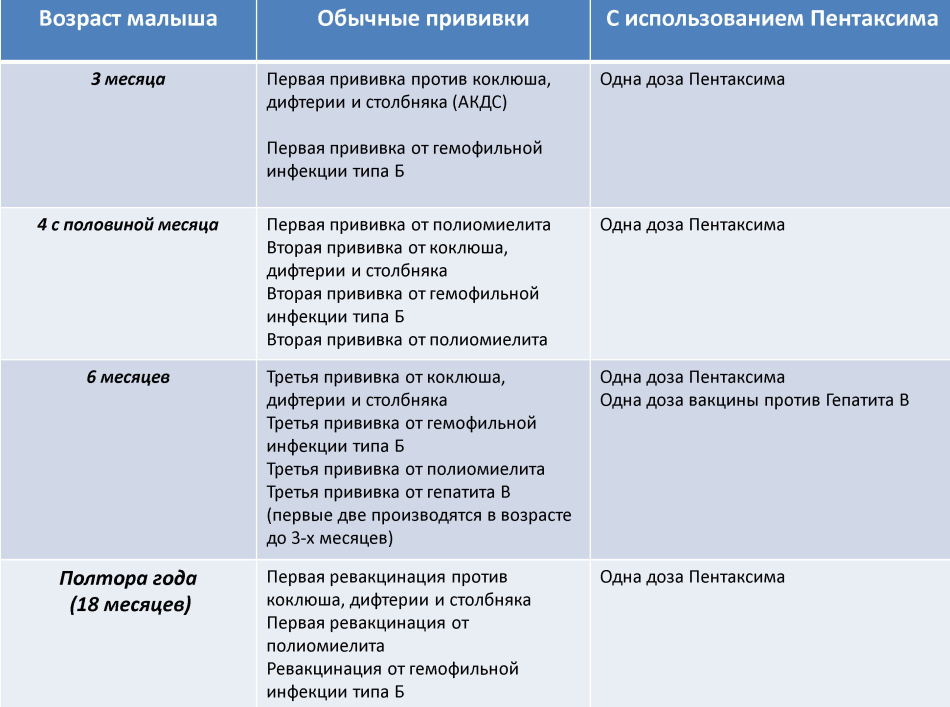 Это мы и называем иммунитетом. Система так устроена, что во время отправки солдат-лимфоцитов «в запас» могут обнаруживаться небольшие колебания в их количестве. Но потом провал будет восстановлен новыми клетками.
Это мы и называем иммунитетом. Система так устроена, что во время отправки солдат-лимфоцитов «в запас» могут обнаруживаться небольшие колебания в их количестве. Но потом провал будет восстановлен новыми клетками.
Иммунная дисфункция
О том, что коронавирус способен поражать клетки иммунитета, ранее сообщали китайские ученые из Фуданьского университета. В апреле этого года в ведущем мировом научном журнале Nature была опубликована их работа, в которой утверждалось, что в лабораторных условиях SARS-Cov-2 способен заражать Т-лимфоциты. Однако позже статья была отозвана самими авторами — выяснилось, что им следовало использовать первичные Т-клетки вместо лабораторных линий для достоверного результата.
— В данной статье было написано, что некоторые коронавирусы, например MERS (ближневосточный респираторный синдром), способны вызывать гибель клеток иммунной системы, запуская определённый каскад биохимических реакций, — рассказал «Известиям» заместитель директора по научной работе ИФХЭ РАН Олег Батищев..jpg) — Для SARS-Cov-2 четких подтверждений такой возможности пока не обнаружено. Ни один из коронавирусов в отличие от ВИЧ не может размножаться в иммунных клетках.
— Для SARS-Cov-2 четких подтверждений такой возможности пока не обнаружено. Ни один из коронавирусов в отличие от ВИЧ не может размножаться в иммунных клетках.
Фото: ИЗВЕСТИЯ/Сергей Коньков
Как подчеркнул эксперт, MERS приводил к более высокой смертности, чем COVID-19, отчасти из-за угнетения иммунного ответа.
— Лимфоциты поражают ВИЧ, вирусы герпеса и некоторые другие вирусы, — сообщил «Известиям» заведующий лабораторией биотехнологии и вирусологии Новосибирского государственного университета Сергей Нетесов. — Из-за этого иммунный ответ на инфекцию может замедляться или быть неполноценным.
Что касается коронавируса, то сейчас главное — это тщательное изучение инфекционного процесса в организме пациентов, что даст наиболее важные данные о выработке полноценного иммунного ответа или сложностях в этом процессе, считает эксперт.
Не путать с ВИЧ
Некоторые специалисты уже сравнивали коронавирус нового типа с ВИЧ и даже говорили об их сходстве. В частности, лауреат Нобелевской премии 2008 года, французский вирусолог Люк Монтанье заявлял о лабораторном происхождении COVID-19 и о том, что его геном содержит в себе элементы ВИЧ. Однако позже эти идеи подверглись жесткой критике со стороны научного сообщества.
В частности, лауреат Нобелевской премии 2008 года, французский вирусолог Люк Монтанье заявлял о лабораторном происхождении COVID-19 и о том, что его геном содержит в себе элементы ВИЧ. Однако позже эти идеи подверглись жесткой критике со стороны научного сообщества.
— При ВИЧ-инфекции поражаются клетки иммунной системы. Причем их инфицирование является основным способом репликации вируса иммунодефицита человека, — сказала «Известиям» сотрудник научно-клинического отдела МГЦ СПИД и Международного центра вирусологии РУДН Елена Белова.
Для коронавируса такая возможность не доказана. Поэтому COVID-19 и ВИЧ — это принципиально разные патогены.
Фото: ИЗВЕСТИЯ/Сергей Коньков
— COVID-19 — это вирус, вызывающий острую, а значит, краткосрочную инфекцию, — пояснил Павел Волчков. — На сегодняшний день нет ни одного случая коронавируса, который бы перешел из острой фазы в хроническую, то есть стал жить в организме человека. Данный патоген поражает фактически все органы и ткани, в силу того что рецепторы на поверхности клеток, за которые он цепляется, находятся практически на всех типах тканей. По этой причине он теоретически может инфицировать и клетки иммунной системы, что действительно может вызывать их гибель.
По этой причине он теоретически может инфицировать и клетки иммунной системы, что действительно может вызывать их гибель.
ВИЧ — это вирус, вызывающий хроническую инфекцию именно иммунной системы, никаких других тканей он не поражает. Говоря точнее, вирус инфицирует и живет исключительно в CD4 T-клетках, рассказал эксперт.
Что касается препринта ученых из Уханя, то они в выводах к своей статье проводят параллель со СПИДом и гепатитом С. Также исследователи утверждают, что им еще предстоит выяснить, как долго будут длиться фенотипические изменения и потенциальные дисфункции лимфоцитов у выздоровевших пациентов.
Нейтропения как нежелательное явление после вакцинации: результаты рандомизированных клинических испытаний на здоровых взрослых и систематический обзор
1. Reading R. Риск иммунной тромбоцитопенической пурпуры после иммунизации детей против кори, эпидемического паротита и краснухи. Ребенок: уход, здоровье и развитие. 2008;34(4):548–. 10.1111/j.1365-2214. 2008.00864_6.x [CrossRef] [Google Scholar]
2008.00864_6.x [CrossRef] [Google Scholar]
2. O’Leary ST, Glanz JM, McClure DL, Akhtar A, Daley MF, Nakasato C, et al.
Риск развития иммунной тромбоцитопенической пурпуры после вакцинации у детей и подростков. Педиатрия. 2012;129(2): 248–55. Эпублик от 11.01.2012. 10.1542/пед.2011-1111. [PubMed] [CrossRef] [Google Scholar]
3. Haddy TB, Rana SR, Castro O. Доброкачественная этническая нейтропения: каково нормальное абсолютное количество нейтрофилов?
Журнал лабораторной и клинической медицины. 1999;133(1):15–22. Epub 1999/06/29. 10.1053/lc.1999.v133.a94931. [PubMed] [CrossRef] [Google Scholar]
4. Reed WW, Diehl LF. Лейкопения, нейтропения и снижение уровня гемоглобина у здоровых чернокожих американцев. Архив внутренней медицины. 1991;151(3):501–5. Эпб 1991/03/01. . [PubMed] [Google Scholar]
5. Bain BJ. Этнические и половые различия в общем и дифференциальном количестве лейкоцитов и количестве тромбоцитов. Журнал клинической патологии. 1996;49(8):664–6. Эпб 1996/08/01. ; Центральный PMCID PubMed: PMCPmc500612. [Бесплатная статья PMC] [PubMed] [Google Scholar]
; Центральный PMCID PubMed: PMCPmc500612. [Бесплатная статья PMC] [PubMed] [Google Scholar]
6. фон Фитингхофф С., Лей К. Гомеостатическая регуляция количества нейтрофилов в крови. Журнал иммунологии (Балтимор, Мэриленд: 1950). 2008;181(8):5183–8. Эпублик 2008/10/04. ; Центральный PMCID PubMed: PMCPmc2745132. [Бесплатная статья PMC] [PubMed] [Google Scholar]
7. Райх Д., Ноллс М.А., Као В.Х., Акылбекова Е.Л., Тандон А., Паттерсон Н. и соавт.
Снижение количества нейтрофилов у лиц африканского происхождения связано с регуляторным вариантом гена рецептора антигена Даффи для хемокинов. Генетика PLoS. 2009;5(1):e1000360 Epub 2009/01/31. 10.1371/журнал.pgen.1000360
[PMC free article] [PubMed] [CrossRef] [Google Scholar]
8. Shoenfeld Y, Ben-Tal O, Berliner S, Pinkhas J. Исход бактериальной инфекции у субъектов с доброкачественной семейной лейкопенией (BFL). Биомед Фармаколог. 1985;39(1):23–6. Эпб 1985/01/01. . [PubMed] [Google Scholar]
9. Gerke C, Colucci AM, Giannelli C, Sanzone S, Vitali CG, Sollai L, et al.
Производство вакцины Shigella sonnei на основе обобщенных модулей мембранных антигенов (GMMA), 1790GAHB. ПлоС один. 2015;10(8):e0134478 Epub 2015/08/08. 10.1371/journal.pone.0134478 ; Центральный PMCID PubMed: PMCPmc4527750. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
10. Администрация FUSFaD. Шкала оценки токсичности для здоровых взрослых добровольцев и подростков, участвующих в клинических испытаниях профилактических вакцин.
11. Дурбин А.П., Уайтхед С.С., Шаффер Д., Элвуд Д., Ванионек К., Тумар Б. и соавт.
Однократная доза вакцины-кандидата DENV-1 rDEN1Delta30 является сильно иммуногенной и индуцирует устойчивость ко второй дозе в рандомизированном исследовании. PLoS игнорирует тропические болезни. 2011;5(8):e1267 Epub 2011/08/11. 10.1371/journal.pntd.0001267 ; Центральный PMCID PubMed: PMCPmc3149013. [Статья бесплатно PMC] [PubMed] [CrossRef] [Google Scholar]
12. Morrison D, Legg TJ, Billings CW, Forrat R, Yoksan S, Lang J. Новая четырехвалентная вакцина против лихорадки денге хорошо переносится и иммуногенна против всех 4 серотипы у взрослых, ранее не инфицированных флавивирусами. Журнал инфекционных болезней. 2010;201(3):370–7. Эпублик 12.01.2010. 10.1086/649916 . [PubMed] [CrossRef] [Google Scholar]
Журнал инфекционных болезней. 2010;201(3):370–7. Эпублик 12.01.2010. 10.1086/649916 . [PubMed] [CrossRef] [Google Scholar]
13. Cunningham CK, Wara DW, Kang M, Fenton T, Hawkins E, McNamara J, et al.
Безопасность двух оболочечных вакцин рекомбинантного вируса иммунодефицита человека типа 1 (ВИЧ-1) у новорожденных, рожденных от ВИЧ-1-инфицированных женщин. Клинические инфекционные заболевания: официальное издание Американского общества инфекционистов. 2001;32(5):801–7. Эпб 2001/03/07. 10.1086/319215. [PubMed] [CrossRef] [Google Scholar]
14. Kotloff KL, Corretti M, Palmer K, Campbell JD, Reddish MA, Hu MC, et al.
Безопасность и иммуногенность рекомбинантной мультивалентной стрептококковой вакцины группы А у здоровых взрослых: исследование фазы 1. Джама. 2004;292(6):709–15. Эпублик 12.08.2004. 10.1001/jama.292.6.709. [PubMed] [CrossRef] [Google Scholar]
15. Ellis RD, Mullen GE, Pierce M, Martin LB, Miura K, Fay MP, et al.
Фаза 1 исследования вакцины-кандидата против малярии на стадии крови AMA1-C1/Alhydrogel с CPG 7909 с использованием двух разных составов и интервалов дозирования.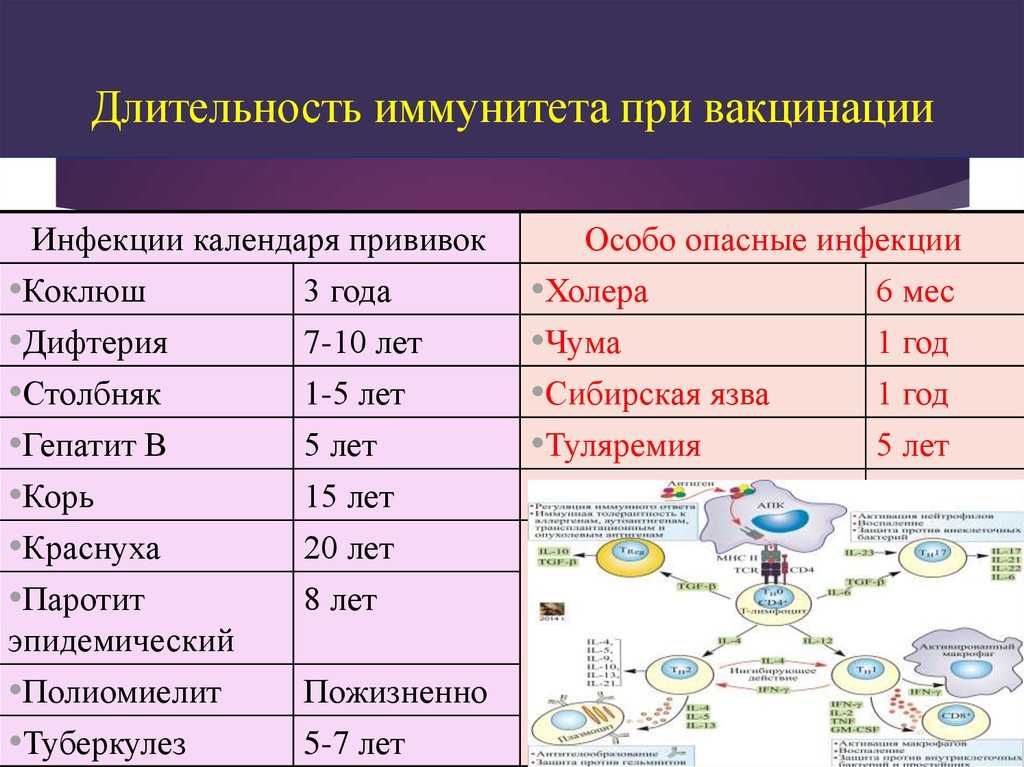 вакцина. 2009;27(31):4104–9. Эпб 2009/05/05. 10.1016/j.vaccine.2009.04.077; Центральный PMCID PubMed: PMCPmc2722923. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
вакцина. 2009;27(31):4104–9. Эпб 2009/05/05. 10.1016/j.vaccine.2009.04.077; Центральный PMCID PubMed: PMCPmc2722923. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
16. Duncan CJ, Sheehy SH, Ewer KJ, Douglas AD, Collins KA, Halstead FD, et al.
Влияние вакцины белок-в-адъюванте AMA1-C1/Alhydrogel+CPG 7909 на скорость размножения малярийных паразитов у инфицированных добровольцев. PloS one. 2011;6(7):e22271 Epub 2011/07/30. 10.1371/journal.pone.0022271 ; Центральный PMCID PubMed: PMCPmc3142129. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
17. Шелдон Э.А., Шварц Х., Цзян К., Джардина П.С., Перес Дж.Л. Фаза 1 рандомизированного открытого исследования с активным контролем для оценки безопасности двухвалентной вакцины rLP2086 против менингококка серогруппы B у здоровых взрослых. Вакцины для человека и иммунотерапевтические препараты. 2012;8(7):888–95. Эпублик 2012/07/27. 10.4161/хв.19983 . [PubMed] [CrossRef] [Google Scholar]
18. McFarland EJ, Johnson DC, Muresan P, Fenton T, Tomaras GD, McNamara J, et al.
Вакцина против ВИЧ-1 вызывала иммунный ответ у новорожденных от матерей, инфицированных ВИЧ-1. СПИД (Лондон, Англия). 2006;20(11):1481–9. Эпублик 19.07.2006. 10.1097/01.помощ.0000237363.33994.45 . [PubMed] [CrossRef] [Google Scholar]
19. Diyye TN, Ndiaye BP, Dieng AB, Fall M, Brittain N, Vermaak S, et al.
Две дозы противотуберкулезной вакцины-кандидата MVA85A субъектам, ранее не получавшим антиретровирусную терапию (АРТ), обеспечивают иммуногенность, сравнимую с одной дозой у субъектов, получающих АРТ+. ПлоС один. 2013;8(6):e67177 Epub 2013/07/11. 10.1371/journal.pone.0067177 ; Центральный PMCID PubMed: PMCPmc3696007. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
20. Durbin AP, McArthur J, Marron JA, Blaney JE Jr., Thumar B, Wanionek K, et al.
Живая аттенуированная вакцина против лихорадки денге серотипа 1 rDEN1Delta30 является безопасной и высокоиммуногенной для здоровых взрослых добровольцев. Вакцины для человека. 2006;2(4):167–73. Эпубликовано 03.10. 2006. . [PubMed] [Google Scholar]
2006. . [PubMed] [Google Scholar]
21. Edelman R, Wasserman SS, Bodison SA, Putnak RJ, Eckels KH, Tang D, et al.
Испытание фазы I 16 составов четырехвалентной живой аттенуированной вакцины против лихорадки денге. Американский журнал тропической медицины и гигиены. 2003;69(6 Дополнение): 48–60. Эпублик 27 января 2004 г. . [PubMed] [Google Scholar]
22. Jaoko W, Nakwagala FN, Anzala O, Manyonyi GO, Birungi J, Nanvubya A, et al.
Безопасность и иммуногенность рекомбинантных низкодозированных вакцин-кандидатов против ВИЧ-1 А, векторизованных плазмидной ДНК pTHr или модифицированным вирусом осповакцины Анкара (MVA) у людей в Восточной Африке. вакцина. 2008;26(22):2788–95. Эпб 2008/04/29. 10.1016/j.vaccine.2008.02.071. [PubMed] [CrossRef] [Google Scholar]
23. Karron RA, Talaat K, Luke C, Callahan K, Thumar B, Dilorenzo S, et al.
Оценка двух живых аттенуированных холодоадаптированных вакцин против гриппа H5N1 у здоровых взрослых. вакцина. 2009 г.;27(36):4953–60. Эпб 2009/06/23. 10.1016/j.vaccine.2009.05.099. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
10.1016/j.vaccine.2009.05.099. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
24. Kitchener S, Nissen M, Nasveld P, Forrat R, Yoksan S, Lang J, et al.
Иммуногенность и безопасность двух составов живой аттенуированной четырехвалентной вакцины против денге у здоровых взрослых австралийцев. вакцина. 2006;24(9):1238–41. Эпублик 11.10.2005. 10.1016/j.vaccine.2005.09.029. [PubMed] [CrossRef] [Google Scholar]
25. McArthur JH, Durbin AP, Marron JA, Wanionek KA, Thumar B, Pierro DJ, et al.
Фаза I клинической оценки rDEN4Delta30-200,201: живой аттенуированной вакцины-кандидата против лихорадки денге 4, предназначенной для снижения гепатотоксичности. Американский журнал тропической медицины и гигиены. 2008;79(5): 678–84. Эпб 05.11.2008. ; Центральный PMCID PubMed: PMCPmc2590927. [Бесплатная статья PMC] [PubMed] [Google Scholar]
26. Ouedraogo A, Tiono AB, Kargougou D, Yaro JB, Ouedraogo E, Kabore Y, et al.
Фаза 1b рандомизированного, контролируемого, двойного слепого исследования с повышением дозы для оценки безопасности, реактогенности и иммуногенности циркумспорозоитной малярийной вакцины на основе аденовируса типа 35 у здоровых взрослых жителей Буркина-Фасо в возрасте от 18 до 45 лет. ПлоС один. 2013;8(11):e78679 Epub 2013/11/19. 10.1371/journal.pone.0078679; Центральный PMCID PubMed: PMCPmc3823848. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
ПлоС один. 2013;8(11):e78679 Epub 2013/11/19. 10.1371/journal.pone.0078679; Центральный PMCID PubMed: PMCPmc3823848. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
27. Sun W, Cunningham D, Wasserman SS, Perry J, Putnak JR, Eckels KH, et al.
Клинические испытания фазы 2 трех составов четырехвалентной живой аттенуированной вакцины против денге у взрослых, ранее не инфицированных флавивирусом. Вакцины для человека. 2009;5(1):33–40. Эпублик 2008/08/02. . [PubMed] [Google Scholar]
28. Talaat KR, Karron RA, Callahan KA, Luke CJ, DiLorenzo SC, Chen GL, et al.
Живая аттенуированная вакцина против вируса гриппа H7N3 хорошо переносится и иммуногенна в испытаниях фазы I на здоровых взрослых. вакцина. 2009 г.;27(28):3744–53. Эпб 2009/05/26. 10.1016/j.vaccine.2009.03.082; Центральный PMCID PubMed: PMCPmc2771405. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
29. Chuang I, Sedegah M, Cicatelli S, Spring M, Polhemus M, Tamminga C, et al.
Вакцина против малярии с примированием ДНК/аденовирусом, кодирующая P. falciparum CSP и AMA1, индуцирует стерильную защиту, связанную с клеточно-опосредованным иммунитетом. ПлоС один. 2013;8(2):e55571 Epub 2013/03/05. 10.1371/journal.pone.0055571 ; Центральный PMCID PubMed: PMCPmc3573028. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
falciparum CSP и AMA1, индуцирует стерильную защиту, связанную с клеточно-опосредованным иммунитетом. ПлоС один. 2013;8(2):e55571 Epub 2013/03/05. 10.1371/journal.pone.0055571 ; Центральный PMCID PubMed: PMCPmc3573028. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
30. Sedegah M, Tamminga C, McGrath S, House B, Ganeshan H, Lejano J, et al.
Аденовирусная 5-векторная вакцина P. falciparum, экспрессирующая CSP и AMA1. Часть A: безопасность и иммуногенность у серонегативных взрослых. ПлоС один. 2011;6(10):e24586 Epub 2011/10/18. 10.1371/journal.pone.0024586 ; Центральный PMCID PubMed: PMCPmc3189181. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
31. Watanaveeradej V, Simasathien S, Nisalak A, Endy TP, Jarman RG, Innis BL, et al.
Безопасность и иммуногенность четырехвалентной живой аттенуированной вакцины против денге у младенцев, не инфицированных флавивирусами. Американский журнал тропической медицины и гигиены. 2011;85(2):341–51. Эпб 2011/08/05. 10.4269/ajtmh.2011.10-0501 ; Центральный PMCID PubMed: PMCPmc3144835. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
10.4269/ajtmh.2011.10-0501 ; Центральный PMCID PubMed: PMCPmc3144835. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
32. Chang LJ, Dowd KA, Mendoza FH, Saunders JG, Sitar S, Plummer SH, et al.
Безопасность и переносимость вакцины с частицами, подобными вирусу чикунгуньи, у здоровых взрослых: фаза 1 испытания с повышением дозы. Ланцет. 2014;384(9959):2046–52. Эпб 2014/08/19. 10.1016/s0140-6736(14)61185-5 . [PubMed] [CrossRef] [Google Scholar]
33. Njuguna IN, Ambler G, Reilly M, Ondondo B, Kanyugo M, Lohman-Payne B, et al.
PedVacc 002: рандомизированное клиническое испытание фазы I/II вакцины MVA.HIVA, вводимой младенцам, рожденным от матерей, инфицированных вирусом иммунодефицита человека типа 1, в Найроби. вакцина. 2014;32(44):5801–8. Эпублик 2014/09/01. 10.1016/j.vaccine.2014.08.034; Центральный PMCID PubMed: PMCPmc4414927. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
34. Durbin AP, Wright PF, Cox A, Kagucia W, Elwood D, Henderson S, et al.
Живая аттенуированная химерная вакцина rWN/DEN4Delta30 хорошо переносится и иммуногенна у здоровых взрослых добровольцев, ранее не получавших флавивирусы. вакцина. 2013;31(48):5772–7. Эпб 2013/08/24. 10.1016/j.vaccine.2013.07.064; Центральный PMCID PubMed: PMCPmc3833717. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
35. Sun W, Edelman R, Kanesa-Thasan N, Eckels KH, Putnak JR, King AD, et al.
Вакцинация добровольцев моновалентными и четырехвалентными живыми аттенуированными вакцинами-кандидатами против лихорадки денге. Американский журнал тропической медицины и гигиены. 2003; 69 (6 Дополнение): 24–31. Эпублик 27 января 2004 г. . [PubMed] [Google Scholar]
36. Capeding RZ, Luna IA, Bomasang E, Lupisan S, Lang J, Forrat R, et al.
Живая аттенуированная четырехвалентная вакцина против лихорадки денге у детей, подростков и взрослых в стране, эндемичной по лихорадке денге: рандомизированное контролируемое исследование фазы I на Филиппинах. вакцина. 2011;29(22): 3863–72. Эпублик от 12.04.2011. 10.1016/j.vaccine.2011.03.057. [PubMed] [CrossRef] [Google Scholar]
Эпублик от 12.04.2011. 10.1016/j.vaccine.2011.03.057. [PubMed] [CrossRef] [Google Scholar]
37. Durbin AP, McArthur JH, Marron JA, Blaney JE, Thumar B, Wanionek K, et al.
rDEN2/4Delta30(ME), живая аттенуированная химерная вакцина против лихорадки денге серотипа 2, безопасна и обладает высокой иммуногенностью у здоровых взрослых, ранее не болевших денге. Вакцины для человека. 2006;2(6):255–60. Эпублик 16.11.2006. . [PubMed] [Google Scholar]
38. Vardas E, Kaleebu P, Bekker LG, Hoosen A, Chomba E, Johnson PR, et al.
Исследование фазы 2 для оценки безопасности и иммуногенности рекомбинантной вакцины против ВИЧ типа 1 на основе аденоассоциированного вируса. Исследования СПИДа и ретровирусы человека. 2010;26(8):933–42. Эпб 2010/07/30. 10.1089/помощь.2009.0242. [PubMed] [CrossRef] [Google Scholar]
39. Kanesa-thasan N, Smucny JJ, Hoke CH, Marks DH, Konishi E, Kurane I, et al.
Безопасность и иммуногенность аттенуированных рекомбинантных рекомбинантных вирусов японского энцефалита и поксвирусов вакцин NYVAC-JEV и ALVAC-JEV у неиммунных и невосприимчивых к осповакцине людей. вакцина. 2000;19(4–5):483–91. Эпублик 2000/10/12. . [PubMed] [Google Scholar]
вакцина. 2000;19(4–5):483–91. Эпублик 2000/10/12. . [PubMed] [Google Scholar]
40. Gershon AA, Levin MJ, Weinberg A, Song LY, LaRussa PS, Steinberg SP, et al.
Фаза I-II исследования живой аттенуированной вакцины против вируса ветряной оспы для повышения иммунитета у детей, инфицированных вирусом иммунодефицита человека, ранее болевших ветряной оспой. Журнал детских инфекционных болезней. 2009 г.;28(7):653-5. Эпб 2009/06/30. 10.1097/INF.0b013e3181998f06; Центральный PMCID PubMed: PMCPmc2868313. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
41. Линдоу Дж. К., Дурбин А. П., Уайтхед С. С., Пирс К. К., Кармолли М. П., Киркпатрик Б. Д. Вакцинация добровольцев живыми аттенуированными вирусами денге в низких дозах приводит к серотип-специфическим иммунологическим и вирусологическим профилям. вакцина. 2013;31(33):3347–52. Эпублик 2013/06/06. 10.1016/j.vaccine.2013.05.075; Центральный PMCID PubMed: PMCPmc3777849. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
42. Siberry GK, Williams PL, Lujan-Zilbermann J, Warshaw MG, Spector SA, Decker MD, et al.
Siberry GK, Williams PL, Lujan-Zilbermann J, Warshaw MG, Spector SA, Decker MD, et al.
Фаза I/II, открытое исследование безопасности и иммуногенности менингококковой (группы A, C, Y и W-135) полисахаридной конъюгированной вакцины против дифтерийного анатоксина у подростков, инфицированных вирусом иммунодефицита человека. Журнал детских инфекционных болезней. 2010;29(5):391–6. Эпб 2010/05/01. 10.1097/INF.0b013e3181c38f3b ; Центральный PMCID PubMed: PMCPmc2868314. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
43. Siberry GK, Warshaw MG, Williams PL, Spector SA, Decker MD, Jean-Philippe P, et al.
Безопасность и иммуногенность четырехвалентной менингококковой конъюгированной вакцины у детей в возрасте от 2 до 10 лет, инфицированных вирусом иммунодефицита человека. Журнал детских инфекционных болезней. 2012;31(1):47–52. Эпублик 12.10.2011. 10.1097/INF.0b013e318236c67b; Центральный PMCID PubMed: PMCPmc3252429. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
44. Wright PF, Ankrah S, Henderson SE, Durbin AP, Speicher J, Whitehead SS, et al.
Wright PF, Ankrah S, Henderson SE, Durbin AP, Speicher J, Whitehead SS, et al.
Оценка безопасности и иммуногенности химерного вируса Лангата/денге 4 в качестве живой ослабленной вакцины против клещевого энцефалита у здоровых взрослых добровольцев. вакцина. 2008; 26(7):882–9.0. Эпублик 22 января 2008 г. 10.1016/j.vaccine.2007.12.015; Центральный PMCID PubMed: PMCPmc2254188. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
45. Sanchez V, Gimenez S, Tomlinson B, Chan PK, Thomas GN, Forrat R, et al.
Врожденный и адаптивный клеточный иммунитет у неинфицированных флавивирусов людей, реципиентов живой аттенуированной вакцины против лихорадки денге серотипа 3, полученной в клетках Vero (VDV3). вакцина. 2006;24(23):4914–26. Эпб 2006/04/25. 10.1016/j.vaccine.2006.03.066. [PubMed] [CrossRef] [Академия Google]
46. Karita E, Ketter N, Price MA, Kayitenkore K, Kaleebu P, Nanvubya A, et al.
Гематологические и биохимические референтные интервалы, полученные на основе CLSI, для здоровых взрослых жителей восточной и южной частей Африки. ПлоС один. 2009;4(2):e4401
ПлоС один. 2009;4(2):e4401
10.1371/journal.pone.0004401
[Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Нейтропения как побочное явление после вакцинации: результаты рандомизированных клинических испытаний на здоровых взрослых и систематический обзор
Обзор
. 4 августа 2016 г .; 11 (8): e0157385.
doi: 10.1371/journal.pone.0157385.
Электронная коллекция 2016.
Винсент Мутури-Киой
1
, Дэвид Льюис
2
, Одиль Лоне
3
, Герт Леру-Роэлс
4
, Алессандра Анемона
1
, Пьер Лулерг
3
, Кэролайн Л. Бодинхэм
2
, Аннелис Эрсенс
4
, Никола Грот
5
, Аллан Сол
1
, Аудино Подда
1
Принадлежности
- 1 Институт глобального здравоохранения вакцин Новартис, Сиена, Италия.

- 2 Центр клинических исследований Суррея, Университет Суррея, Гилфорд, Соединенное Королевство.
- 3 Université Paris Descartes, Sorbonne Paris cité и Inserm CIC 1417, F-CRIN I-Reivac, Assistance Publique Hôpitaux de Paris, CIC Cochin-Pasteur, Париж, Франция.
- 4 Гентский университет и университетская больница, Гент, Бельгия.
- 5 Novartis Vaccines & Diagnostics, Сиена, Италия.
PMID:
27490698
PMCID:
PMC4974007
DOI:
10.
 1371/журн.pone.0157385
1371/журн.pone.0157385
Бесплатная статья ЧВК
Обзор
Vincent Muturi-Kioi et al.
ПЛОС Один.
.
Бесплатная статья ЧВК
. 4 августа 2016 г .; 11 (8): e0157385.
doi: 10.1371/journal.pone.0157385.
Электронная коллекция 2016.
Авторы
Винсент Мутури-Киой
1
, Дэвид Льюис
2
, Одиль Лоне
3
, Герт Леру-Роэлс
4
, Алессандра Анемона
1
, Пьер Лулерг
3
, Кэролайн Л. Бодинхэм
Бодинхэм
2
, Аннелис Эрсенс
4
, Никола Грот
5
, Аллан Сол
1
, Аудино Подда
1
Принадлежности
- 1 Институт глобального здравоохранения вакцин Новартис, Сиена, Италия.
- 2 Центр клинических исследований Суррея, Университет Суррея, Гилфорд, Соединенное Королевство.
- 3 Université Paris Descartes, Sorbonne Paris cité и Inserm CIC 1417, F-CRIN I-Reivac, Assistance Publique Hôpitaux de Paris, CIC Cochin-Pasteur, Париж, Франция.
- 4 Гентский университет и университетская больница, Гент, Бельгия.

- 5 Novartis Vaccines & Diagnostics, Сиена, Италия.
PMID:
27490698
PMCID:
PMC4974007
DOI:
10.1371/журн.pone.0157385
Абстрактный
Задний план:
В контексте ранних испытаний вакцин, направленных на оценку профиля безопасности новых вакцин, часто сообщается об аномальных гематологических показателях, таких как нейтропения. Поэтому важно оценить, как следует планировать эти испытания, чтобы не упустить потенциально важные сигналы безопасности, а также понять последствия и клиническую значимость.
Методология:
Мы сообщаем и обсуждаем результаты пяти клинических испытаний (два с новой вакциной против шигелл на ранней стадии клинической разработки и три с лицензированными вакцинами), в которых до и после вакцинации оценивали абсолютное число нейтрофилов (АНЧ). Кроме того, мы провели систематический обзор литературы о случаях нейтропении, зарегистрированных во время испытаний вакцин, чтобы обсудить наши результаты в более общем контексте.
Основные выводы:
Как в наших клинических испытаниях, так и в обзоре литературы сообщалось о нескольких случаях нейтропении в первые две недели после вакцинации. Однако нейтропения, как правило, была преходящей и имела доброкачественный клинический исход после вакцинации либо несколькими новыми кандидатами, либо хорошо известными лицензированными вакцинами. Кроме того, реципиенты вакцины с нейтропенией часто имели более низкий исходный уровень АЧН, чем вакцинированные лица без нейтропении. Во многих случаях нейтропения возникала у лиц африканского происхождения, у которых, как известно, АЧН ниже, чем у жителей западных стран.
Во многих случаях нейтропения возникала у лиц африканского происхождения, у которых, как известно, АЧН ниже, чем у жителей западных стран.
Выводы:
Важно включить ANC и другие гематологические тесты в ранние испытания вакцин, чтобы выявить потенциальные сигналы безопасности. Поствакцинальная нейтропения не является чем-то необычным, обычно транзиторным и клинически доброкачественным, но во многих испытаниях вакцин нет графика отбора проб, позволяющего ее обнаружить. Учитывая этническую изменчивость уровня циркулирующих нейтрофилов, нормальные диапазоны с учетом этнической принадлежности следует использовать для определения критериев включения/исключения в исследование и классификации нежелательных явлений, связанных с нейтропенией.
Пробная регистрация:
ClinicalTrials.gov NCT02017899, NCT02034500, NCT01771367, NCT01765413, NCT02523287.
Заявление о конфликте интересов
Конкурирующие интересы: A. Anemona, NG, AS и AP работали в Novartis на момент проведения этих исследований и в настоящее время работают в GSK. ВМК был медицинским стажером в Novartis на момент проведения этих исследований и в настоящее время работает в GSK. Конкретные роли этих авторов сформулированы в разделе «вклад авторов». Это не меняет приверженности авторов политике PLOS ONE в отношении обмена данными и материалами.
Цифры
Рис. 1. Схема исследования H03_01TP и H03_02TP…
Рис. 1. Блок-схемы исследования H03_01TP и H03_02TP.
Рис. 1. Блок-схемы исследования H03_01TP и H03_02TP.
1. Блок-схемы исследования H03_01TP и H03_02TP.
Рис. 2. Схема исследования CRC305A и CRC305C…
Рис. 2. Блок-схемы исследования CRC305A и CRC305C.
Рис. 2. Блок-схемы исследования CRC305A и CRC305C.
Рис. 3. Блок-схема экспериментального исследования в Генте.
Рис. 3. Блок-схема экспериментального исследования в Генте.
Рис. 3. Блок-схема экспериментального исследования в Генте.
Рис. 4. Блок-схема поиска литературы.
4. Блок-схема поиска литературы.
Рис. 4. Блок-схема поиска литературы.
Рис. 4. Блок-схема поиска литературы.
Рис. 5. Абсолютное количество нейтрофилов при разных…
Рис. 5. Абсолютное количество нейтрофилов в разные моменты времени после вакцинации тремя дозами…
Рис. 5. Абсолютное количество нейтрофилов в разные моменты времени после вакцинации тремя дозами либо 1790GAHB, либо плацебо через 0, 1 и 2 месяца.
(A) Исследование H03_01TP. (B) Исследование H03_02TP. Красные точки обозначают субъектов, у которых абсолютное количество нейтрофилов было ниже лабораторного нормального диапазона по крайней мере в один момент времени после вакцинации. Исходные данные собираются во время скрининга добровольцев. Столбцы указывают медиану и межквартильный диапазон. В каждый момент времени точки, относящиеся к ANC у вакцинированных, находятся слева, а точки, относящиеся к ANC у реципиентов плацебо, — справа.
Исходные данные собираются во время скрининга добровольцев. Столбцы указывают медиану и межквартильный диапазон. В каждый момент времени точки, относящиеся к ANC у вакцинированных, находятся слева, а точки, относящиеся к ANC у реципиентов плацебо, — справа.
Рис. 6. Абсолютное количество нейтрофилов при разных…
Рис. 6. Абсолютное количество нейтрофилов в разные моменты времени после вакцинации в день 0.
(А…
Рис. 6. Абсолютное количество нейтрофилов в разные моменты времени после вакцинации в день 0.
(A и B) сезонный TIV с адъювантом. (C) сезонный TIV. (D) ослабленная живая вакцина против желтой лихорадки. (A, C и D) проводится стационарно. (Б) проводится амбулаторно. Красные точки обозначают субъектов, у которых абсолютное количество нейтрофилов было ниже лабораторного нормального диапазона по крайней мере в один момент времени после вакцинации. Столбцы указывают медиану и межквартильный диапазон.
Столбцы указывают медиану и межквартильный диапазон.
См. это изображение и информацию об авторских правах в PMC
Похожие статьи
Технология GMMA для разработки безопасных вакцин: метаанализ данных отдельных пациентов для оценки профиля безопасности вакцины Shigella sonnei 1790GAHB у здоровых взрослых с особым акцентом на нейтропению.
Де Рик И., Саракину Э., Накакана У., Чилио Г.Л., Ндиайе А., Велла В., Ауэрбах Дж., Гранада Дж.П., Конти В., Подда А.
Де Рик I и др.
Заразить Dis Ther. 2022 апр; 11 (2): 757-770. дои: 10.1007/s40121-022-00596-х. Epub 2022 3 февраля.
Заразить Dis Ther. 2022.PMID: 35118580
Бесплатная статья ЧВК.Профиль безопасности и иммунологические реакции новой вакцины против Shigella sonnei, вводимой внутримышечно, внутрикожно и интраназально: результаты двух параллельных рандомизированных клинических исследований фазы 1 на здоровых взрослых добровольцах в Европе.

Лоне О., Льюис Д. М., Анемона А., Лулерг П., Лихи Дж., Скир А. С., Могард А., Маркетти Э., Занкан С., Хуо З., Рондини С., Мархаба Р., Финко О., Мартин Л. Б., Ауэрбах Дж., Коэн Д., Саул А., Герке С., Подда А.
Лоней О. и др.
ЭБиоМедицина. 2017 авг; 22: 164-172. doi: 10.1016/j.ebiom.2017.07.013. Epub 2017 15 июля.
ЭБиоМедицина. 2017.PMID: 28735965
Бесплатная статья ЧВК.Клиническое испытание.
Клинические испытания пероральной живой вакцины-кандидата против Shigella sonnei, WRSS1, на взрослых тайцах.
Питисуттитхум П., Ислам Д., Чамнанчанунт С., Руамсап Н., Хантапура П., Кевкунвал Дж., Киттитракул С., Лувира В., Дхитават Дж., Венкатесан М.М., Мейсон С.Дж., Бодхидатта Л.
Питисуттитум П. и др.
Клин Вакцина Иммунол. 2016 5 июля; 23 (7): 564-75. doi: 10.1128/CVI.00665-15. Печать 2016 июль.
Клин Вакцина Иммунол. 2016.
2016.PMID: 27146000
Бесплатная статья ЧВК.Клиническое испытание.
Безопасность и иммуногенность потенциальной биоконъюгированной вакцины против Shigella flexneri 2a, вводимой здоровым взрослым: простое слепое рандомизированное исследование фазы I.
Риддл М.С., Камински Р.В., Ди Паоло С., Портер С.К., Гутьеррес Р.Л., Кларксон К.А., Вертс Х.Е., Дюплесси С., Кастеллано А., Алаймо С., Паолино К., Гормли Р., Гамбиллара Фонк В.
Риддл М.С. и др.
Клин Вакцина Иммунол. 2016 5 декабря; 23(12):908-917. doi: 10.1128/CVI.00224-16. Печать 2016 дек.
Клин Вакцина Иммунол. 2016.PMID: 27581434
Бесплатная статья ЧВК.Клиническое испытание.
Клинические испытания вакцин против шигелл: два шага вперед и шаг назад на долгом и трудном пути.

Левин М.М., Котлофф К.Л., Барри Э.М., Пасетти М.Ф., Штейн М.Б.
Левин М.М. и др.
Nat Rev Microbiol. 2007 г., июль; 5(7):540-53. DOI: 10.1038/nrmicro1662.
Nat Rev Microbiol. 2007.PMID: 17558427
Бесплатная статья ЧВК.Рассмотрение.
Посмотреть все похожие статьи
Цитируется
Редкое нежелательное явление после введения CoronaVac ® : нейтропения у реципиента почечного трансплантата.
Артан А.С., Демир Э., Гюллер Н., Туркмен А.
Артан А.С. и соавт.
Balkan Med J. 22 июля 2022 г .; 39 (4): 305–306. doi: 10.4274/balkanmedj.galenos.2022.2022-4-30.
Балкан Мед Ж. 2022.PMID: 35873917
Бесплатная статья ЧВК.Аннотация недоступна.
ВкДНК, полученная из В-клеток, после первичной вакцинации мРНК BNT162b2 предвосхищает В-клетки памяти и нейтрализующие антитела против SARS-CoV-2.

Фокс-Фишер И., Пиянзин С., Бриллер М., Ойкнин-Джиан Э., Альфи О., Бен-Ами Р., Перец А., Нейман Д., Очана Б.Л., Фридлих О., Дравши З., Клохендлер А., Магенхейм Дж., Шаре Д., Авраами Р., Рибак Ю., Талмон А., Рубин Л., Мильман Н., Сегев М., Фельдман Э., Таль Ю., Шен-Орр С.С., Глейзер Б., Шемер Р., Вольф Д., Дор Ю.
Фокс-Фишер I и др.
Мед (Нью-Йорк). 2022, 8 июля; 3(7):468-480.e5. doi: 10.1016/j.medj.2022.05.005. Epub 2022 19 мая.
Мед (Нью-Йорк). 2022.PMID: 35716665
Бесплатная статья ЧВК.Экспрессия шиповидного белка SARS-CoV-2 In Vitro и гематологические эффекты у мышей, вакцинированных AZD1222 (ChAdOx1 nCoV-19).
Стеббингс Р., Джонс С., Коттон П., Армор Г., Магуайр С., Скеллетт В., Танг К.М., Гудман Дж., Брэди Т., Такахаши В., Даунт А., Лапойнт Дж.М., Коэн Т.С.
Стеббингс Р. и соавт.
Фронт Иммунол. 2022 12 апр;13:836492. doi: 10.3389/fimmu.2022.836492. Электронная коллекция 2022.
doi: 10.3389/fimmu.2022.836492. Электронная коллекция 2022.
Фронт Иммунол. 2022.PMID: 35493482
Бесплатная статья ЧВК.На пути к четырехкомпонентной вакцине на основе ГММА против Shigella .
Миколи Ф., Накакана ООН, Берланда Скорца Ф.
Миколи Ф. и соавт.
Вакцины (Базель). 2022 18 февраля; 10 (2): 328. doi: 10.3390/vaccines10020328.
Вакцины (Базель). 2022.PMID: 35214786
Бесплатная статья ЧВК.Рассмотрение.
Технология GMMA для разработки безопасных вакцин: метаанализ данных отдельных пациентов для оценки профиля безопасности вакцины Shigella sonnei 1790GAHB у здоровых взрослых с особым акцентом на нейтропению.
Де Рик И., Саракину Э., Накакана У., Чилио Г.Л., Ндиайе А., Велла В., Ауэрбах Дж.
 , Гранада Дж.П., Конти В., Подда А.
, Гранада Дж.П., Конти В., Подда А.
Де Рик I и др.
Заразить Dis Ther. 2022 апр; 11 (2): 757-770. дои: 10.1007/s40121-022-00596-х. Epub 2022 3 февраля.
Заразить Dis Ther. 2022.PMID: 35118580
Бесплатная статья ЧВК.
Просмотреть все статьи «Цитируется по»
использованная литература
Чтение Р. Риск развития иммунной тромбоцитопенической пурпуры после иммунизации детей против кори, эпидемического паротита и краснухи. Ребенок: уход, здоровье и развитие. 2008;34(4):548–. 10.1111/j.1365-2214.2008.00864_6.x
—
DOI
О’Лири С.Т., Гланц Дж.М., МакКлюр Д.Л., Ахтар А.
 , Дейли М.Ф., Накасато С. и др. Риск развития иммунной тромбоцитопенической пурпуры после вакцинации у детей и подростков. Педиатрия. 2012;129(2):248–55. Эпублик от 11.01.2012. 10.1542/пед.2011-1111.
, Дейли М.Ф., Накасато С. и др. Риск развития иммунной тромбоцитопенической пурпуры после вакцинации у детей и подростков. Педиатрия. 2012;129(2):248–55. Эпублик от 11.01.2012. 10.1542/пед.2011-1111.—
DOI
—
пабмед
Haddy TB, Rana SR, Castro O. Доброкачественная этническая нейтропения: каково нормальное абсолютное число нейтрофилов? Журнал лабораторной и клинической медицины. 1999;133(1):15–22. Epub 1999/06/29. 10.1053/lc.1999.v133.a94931.
—
DOI
—
пабмед
Рид В.
 В., Дил Л.Ф. Лейкопения, нейтропения и снижение уровня гемоглобина у здоровых чернокожих американцев. Архив внутренней медицины. 1991;151(3):501–5. Эпб 1991/03/01. .
В., Дил Л.Ф. Лейкопения, нейтропения и снижение уровня гемоглобина у здоровых чернокожих американцев. Архив внутренней медицины. 1991;151(3):501–5. Эпб 1991/03/01. .—
пабмед
Бейн БЖ. Этнические и половые различия в общем и дифференциальном количестве лейкоцитов и количестве тромбоцитов. Журнал клинической патологии. 1996;49(8):664–6. Эпб 1996/08/01. ; Центральный PMCID PubMed: PMCPmc500612.
—
ЧВК
—
пабмед
Типы публикаций
термины MeSH
вещества
Грантовая поддержка
Эта работа была поддержана ЕВРОПЕЙСКОЙ КОМИССИЕЙ — Грант 261472 (STOPENTERICS) (http://stopenterics.


 1371/журн.pone.0157385
1371/журн.pone.0157385

 2016.
2016.

 doi: 10.3389/fimmu.2022.836492. Электронная коллекция 2022.
doi: 10.3389/fimmu.2022.836492. Электронная коллекция 2022. , Гранада Дж.П., Конти В., Подда А.
, Гранада Дж.П., Конти В., Подда А. , Дейли М.Ф., Накасато С. и др. Риск развития иммунной тромбоцитопенической пурпуры после вакцинации у детей и подростков. Педиатрия. 2012;129(2):248–55. Эпублик от 11.01.2012. 10.1542/пед.2011-1111.
, Дейли М.Ф., Накасато С. и др. Риск развития иммунной тромбоцитопенической пурпуры после вакцинации у детей и подростков. Педиатрия. 2012;129(2):248–55. Эпублик от 11.01.2012. 10.1542/пед.2011-1111. В., Дил Л.Ф. Лейкопения, нейтропения и снижение уровня гемоглобина у здоровых чернокожих американцев. Архив внутренней медицины. 1991;151(3):501–5. Эпб 1991/03/01. .
В., Дил Л.Ф. Лейкопения, нейтропения и снижение уровня гемоглобина у здоровых чернокожих американцев. Архив внутренней медицины. 1991;151(3):501–5. Эпб 1991/03/01. .