Содержание
«Я не знала, что корь настолько страшна»
«Они могут думать о своих детях, но не об окружающих»
В детском центре, куда ходил мой сын, корью заболел ребенок, и родители не поставили никого в известность. Они молча отболели и вернулись, видимо, ещё в инкубационный период, а так как Давид не был привит от кори, он эту болезнь подхватил. Резко подскочила температура и держалась 5 дней. Мы думали, что у него грипп. На шестой день он проснулся весь в сыпи, и я сразу поняла, что это корь. Мы вызвали скорую, я собрала вещи, так как понимала, что мы сейчас поедем в больницу. Фельдшер подтвердил диагноз, и нас увезли.
Я сразу написала в родительские чаты, так как врачи спросили, где мы были две недели назад. В это время мы были в детском центре и ходили на елку с садиком. В чате детского центра одна родительница написала: «Ой, мы тоже недавно переболели, вам главное полоскать горло». Когда мы прослушали её аудиозапись, все родители стали возмущаться, почему не предупредили, ведь это такое серьезное заболевание. Она ответила, что предупредила, но на самом деле ни руководство садика, ни воспитателя она не предупреждала, просто сказала, что ребенок простудился. Как я поняла, этот ребенок не лежал в больнице — ему несколько раз вызывали скорую и педиатра. Когда все родители начали ругаться, она стала оправдываться, что это была энтеровирусная корь. Я узнала у врачей, что такой кори не существует, и попросила эту маму рассказать, как прошла болезнь. Все симптомы указывали на то, что это была самая настоящая корь.
Она ответила, что предупредила, но на самом деле ни руководство садика, ни воспитателя она не предупреждала, просто сказала, что ребенок простудился. Как я поняла, этот ребенок не лежал в больнице — ему несколько раз вызывали скорую и педиатра. Когда все родители начали ругаться, она стала оправдываться, что это была энтеровирусная корь. Я узнала у врачей, что такой кори не существует, и попросила эту маму рассказать, как прошла болезнь. Все симптомы указывали на то, что это была самая настоящая корь.
В тот момент я осознала, что далеко не все родители ответственны. Они могут думать о своих детях, но не об окружающих. Я не могу защитить своих детей от таких родителей. Поэтому, когда в больнице нам предложили поставить прививку младшей дочери, я поняла, что момент упущен — Этери уже была с Давидом в контакте, когда он сильно болел. Если бы мы знали, что это корь, мы бы её огородили — вакцинировали и увезли к бабушке с дедушкой. У кори есть такое окно: за 4 дня до сыпи ребенок становится заразным, а после сыпи должно пройти ещё 4 дня.
У меня внутри бушевал ураган, но я прекрасно понимала, что ничего не добьюсь, даже наговорив этой маме всё, что о ней думаю. Но помимо злости на промолчавшую родительницу, мучило то, что я всё-таки совершила ошибку. Я винила себя за то, что мой ребенок заболел корью, потому что это я не поставила ему прививку. Я изучала, спрашивала, почему так происходит. Спрашивала у других родителей, почему они не ставят прививки. Во-первых, может быть, чтобы где-то оправдать себя и понять, правильно я поступала или нет. Я не знала, что корь настолько страшна. Нам говорят «корь, корь, корь», но от неё на самом деле большие последствия. Корь очень сильно стирает иммунную систему, и как бы я ни укрепляла её, вирус просто уничтожил всю эту работу. Конечно, многое зависит от организма, но от 11 до 79% иммунитета она стирает. И поэтому я пришла к выводу, что лучше всё-таки вакцинироваться. Конечно, вред может быть и от прививки — здесь как в лотерее. Но если ставить на чаши весов, что хуже — прививка (при этом ты ребенка подготавливаешь, оздоравливаешь и ставишь её в нужный момент) или корь, после которой ребенок восстанавливается три года, мой выбор очевиден. Сейчас у меня дети каждые две недели болеют — то температура, то насморк, то кашель, то ухо. Они сейчас очень слабые и быстро подхватывают вирусы.
Сейчас у меня дети каждые две недели болеют — то температура, то насморк, то кашель, то ухо. Они сейчас очень слабые и быстро подхватывают вирусы.
Я этого не знала. Ведь нас ругают из-за отказа ставить прививку, а почему — не объясняют. Летальные исходы от кори не сразу ведь происходят, чаще всего после того, как дети переболеют, иммунитет ослабевает, и они могут схватить пневмонию, менингит или что-то в этом роде. В течение первых трех лет после кори, если иммунитетом не заниматься, ребенок может погибнуть.
Пострадать не по-детски. Все, что нужно знать про корь
Пострадать не по-детски. Все, что нужно знать про корь
В 28 странах Европы и на всём Американском континенте от Канады до Мексики сложилась неблагополучная эпидемиологическая ситуация по кори. В Европе за год заболеваемость выросла в 4 раза. А в соседней с нами Украине – в десятки раз! Лишь в первом полугодии 2018‑го там было зарегистрировано более 20 тыс. заболевших, а от осложнений умерли 11 человек.
Существует масса заблуждений по поводу этой инфекции.
№ 1. Чтобы защититься от кори, достаточно мыть руки и обходить стороной тех, кто чихает, кашляет, а тем более покрыт сыпью.
На самом деле. Заболевший корью опасен для окружающих задолго до возникновения у него проявлений болезни. В последние дни инкубационного периода, когда больной активно выделяет в атмосферу вирус, никаких симптомов у него нет. Соответственно на этом этапе выявить корь практически невозможно. Да и в первые несколько дней заболевания корь протекает как банальная простуда: повышенная температура, кашель, насморк, иногда конъюнктивит. Сыпь появляется лишь на 5–6‑й день заболевания, и к этому моменту все вокруг, кто не имел прививок, уже наверняка заразились.
Тем не менее и в это время ещё есть шанс уберечься от болезни. Для этого людям, оказавшимся в контакте с заболевшим, нужно в течение 2–3 дней ввести живую вакцину от кори или готовый внутривенный иммуноглобулин, содержащий донорские антитела. Этот препарат получают из сыворотки крови людей, переболевших корью. Его действия хватит на 2–3 месяца, а потом для защиты от кори необходимо сделать прививку.
Этот препарат получают из сыворотки крови людей, переболевших корью. Его действия хватит на 2–3 месяца, а потом для защиты от кори необходимо сделать прививку.
№ 2. Прививать детей от кори не нужно. Во‑первых, привитые тоже болеют. А во‑вторых, уж лучше перенести эту инфекцию легко в детстве, чем болеть гораздо тяжелее уже будучи взрослыми.
На самом деле. Да, корью болеют и привитые. Но крайне редко. Практически это происходит лишь в двух случаях: либо если в атмосфере была очень высокая концентрация вируса, либо у привитого человека плохо сформировался иммунитет. Так бывает, если есть какие-то нарушения в работе иммунной системы или если прививка была проведена неправильно. Например, препарат был просрочен или хранился с нарушением температурного режима (поэтому важно вакцинироваться в надёжном месте), а также если не была соблюдена кратность введения вакцины. К слову, детей от кори прививают дважды: в 1 год и в 6 лет (хотя тех, кто родился до 2000 года, раньше прививали однократно).
Взрослые, а тем более пожилые люди, переносят корь, как правило, хуже, чем дети. Но всё же не стоит ради выработки естественного пожизненного иммунитета заражать ребёнка корью. Ведь трудно предсказать, как в конкретном случае будет протекать болезнь. Часто инфекцию сопровождают высокая температура, светобоязнь, боль, явления интоксикации и другие симптомы. Но самая главная опасность кори – это риск грозных осложнений, среди которых: энцефалит, менингит, пневмония. Именно от них, а не от самой кори погибают люди. Так стоит ли играть с болезнью в русскую рулетку?
Есть и ещё одна важная причина сделать прививку от кори. Особенно девочкам и женщинам. Ведь вакцина помогает защитить от болезни не только их самих, но и их будущих детей. Согласно нашему Национальному календарю, от кори у нас прививают годовалых малышей, тогда как заболевание наиболее опасно для младенцев. Хороший способ защитить кроху – кормить его грудным молоком, в котором содержатся материнские антитела к этой инфекции.
№ 3. Прививка вызывает у детей аутизм и другие нарушения. К тому же может спровоцировать заболевание корью. А вот естественным образом переболев этой инфекцией, можно укрепить иммунитет и стать невосприимчивым к аллергии, астме, экземе и даже к развитию опухолей.
На самом деле. Вакцина содержит живой, но ослабленный вирус кори. Её введение приводит к выработке антител, которые будут защищать от заболевания, а не провоцировать его развитие. Постпрививочные осложнения крайне редки. Обычно бывают лишь повышение температуры, слабость, незначительная сыпь.
Что касается аутизма и прочих заболеваний, то нет ни одного научного исследования, которое бы могло подтвердить эти домыслы. Как и нет объективных данных о защитной роли кори. А вот вред от таких мифов существует. И вполне объективный. Именно антипрививочными настроениями, широко распространёнными в Европе да и у нас, можно объяснить рост заболеваемости корью и другими опасными инфекциями в мире в последнее время.
№ 4. Корь крайне сложно отличить от других заболеваний, например, от скарлатины.
На самом деле. Корь, которая протекает типично, достаточно легко опознать. Для этого не надо ждать появления сыпи на теле, которая возникает лишь на 5–6‑е сутки болезни. Нужно заглянуть больному в рот – на внутренней поверхности щёк должны быть серо-белые пятна с алой каймой (пятна Бельского – Филатова – Коплика). После их исчезновения появляется сыпь на теле. Она всегда идёт сверху вниз: начинается с головы, через 2–3 дня спускается на туловище, а затем ещё через 2–3 дня – на ноги.
№ 5. При первых признаках кори нужно как можно быстрее принимать противовирусные и антибиотики.
На самом деле. Корь – вирусное заболевание, поэтому антибиотики принимать в этом случае не просто бессмысленно, но и вредно (лишний удар по ослабленному организму). Специфического лечения кори нет, борьба должна идти только с симптомами: жаром, кашлем, конъюнктивитом и другими. Антибиотики нужны, только если присоединилась бактериальная инфекция.
Антибиотики нужны, только если присоединилась бактериальная инфекция.
№ 6. Взрослые и дети, страдающие дефицитом витамина A, гораздо больше подвержены кори, чем те, у кого он в достатке.
На самом деле. Корь очень заразна. Вирус передаётся воздушно-капельным путём. И если рядом находится больной, то шанс заразиться для непривитого человека практически 100%, не важно, пьёт он витамины или нет. А вот приём витамина A для заболевшего полезен. Назначение высоких доз этого вещества (200 000 международных единиц) в первые дни кори достоверно снижает тяжесть болезни и риск осложнений.
Важно!
Плановая бесплатная вакцинация против кори проводится:
- Детям дважды – в возрасте 12 мес. и в 6 лет.
- Подросткам в 15–17 лет и взрослым до 35 лет: не привитым ранее и не болевшим корью – двукратно с интервалом не менее 3 месяцев между прививками.
По эпидемическим показаниям прививки бесплатно делают:
- независимо от возраста лицам из очагов заболевания корью;
- не болевшим и не привитым;
- привитым однократно.

Вакцины
24 апр. — 25 апр. 2018 г.
Малага, Испания
- Конференция
- {{Заголовок}}
- Европа
- {{Заголовок}}
Зарегистрируйтесь сейчас
осталось зарегистрироваться
- Обзор
- Повестка дня
- Дополнительная информация
- Путешествовать
- Регистрационные сборы
- Выставка и спонсорство
- Контакт
Основные моменты программы
Регуляторные спикеры подтверждены!
- Матс Велин
Агентство медицинской продукции, Швеция - Хайди Мейер, доктор философии
Институт Пауля Эрлиха - Gwenaël Ciréfice, PhD
Европейское управление качества лекарственных средств и здравоохранения, EDQM - Richard H.
 Siggers, PhD
Siggers, PhD
Управление биологических и генетических препаратов, Health Canada - Erika Pfeiler, PhD
CDER Отдел микробиологических оценок, US FDA
Обзор
Уважаемые коллеги,
Мы рады пригласить вас на конференцию 2018 PDA Europe Vaccines , которая состоится 24-25 апреля 2018 г.
На конференции будут рассмотрены новые тенденции в разработке вакцин и управлении жизненным циклом, включая (1) использование платформенных технологий, (2) предварительные знания, (3) разработка новых вакцин, включающих терапевтические вакцины и противораковые вакцины, и (4) рассмотрение сценариев ускоренной разработки. В этом контексте принципы «Качества по дизайну» в настоящее время внедрены в различные аспекты разработки вакцин и не только. На конференции будет представлен обзор применимости QbD в различных аспектах, с точки зрения продуктов, аналитики и процессов, а также соображений при управлении жизненным циклом, а также будут затронуты новые тенденции в области регулирования, такие как ICHQ12.
Мы стремимся продолжить обсуждение текущих тенденций в области ОМЦ и стратегий регулирования новых заболеваний, начатое несколько лет назад в рамках вакцины против лихорадки Эбола и с тех пор эволюционировавшее.
Мы с нетерпением ждем возможности приветствовать вас на этом специальном мероприятии PDA Europe в Испании в апреле следующего года!
С уважением, Председатели
Кристиана Кампа , председатель конференции, GSK Vaccines
Нэнси Каувенбергс , председатель конференции, МСД
Повестка дня
- вторник
- Среда
Tuesday, 24 April 2018
9:00
Welcome and Introduction
Kerstin Wilken, PDA Europe
Cristiana Campa, Conference Chair, GSK Vaccines
Nancy Cauwenberghs, Conference Chair, МСД9:10 — 11:15
Сессия 1: Нормативные новости
Модератор: Тьерри Гастино, Санофи9:10
Сближение нормативных требований в отношении вакцин и изменений после утверждения
Хайди Мейер, Paul-Ehrlich-Institut09:40
Гармонизированные подходы к управлению жизненным циклом вакцин
Richard H. Siggers, Управление биологических и генетических препаратов, Health Canada
Siggers, Управление биологических и генетических препаратов, Health Canada 10:10
Вакцины для человека в Европейской фармакопее: последние разработки
Gwenaël Ciréfice, Европейское управление качества лекарственных средств и здравоохранения, EDQM10:40
Вопросы и ответы, обсуждение11:15 – 11:45
Перерыв на кофе, постерная сессия и выставка11:45 — 13:30
Сессия 2: Платформенные технологии и новые продукты
Модератор: Керстин Уилкен, PDA Europe11:45
Новая противотуберкулезная вакцина на горизонте
Леандер Гроде, VPM12:10
Новое поколение вакцин на основе гликанов
Арне против Бонина, Vaxxilion12:35
Использование платформы и предшествующих знаний для продвижения разработки вакцин на основе аденовирусных векторов
Els van Deventer-Troost, Janssen J&J13:00
Разработка и оптимизация процессов производства вирусных платформ для экономичного и быстрого выпуска вакцин
Анисса Бумлик, Merck KGaA13:30 – 14:30
Обеденный перерыв, постерная сессия и выставка14:30 – 16:30
Сессия 3: Ускоренное развитие и предварительные знания
Модератор: Нэнси Каувенбергс, MSD14:30
Предыдущие знания – рекомендации по вакцинам
Матс Велин, MPA15:00
Стратегии ускорения для быстрого доступа пациентов к вакцинам
Амин Хан, Вакцины GSK15:30
Вакцина против вируса Эбола – тематическое исследование подходов к ускорению разработки процессов и исследований характеристик
Джозеф П. Калифано, МСД
Калифано, МСД 16:00
Вопросы и ответы, обсуждение16:30 – 17:00
Перерыв на кофе, постерная сессия и выставка17:00 – 18:30
Сессия 4: Риск-ориентированные подходы к аналитической разработке и дизайну помещений для вакцин
Модератор: Анник Вандеркаммен, GSK Vaccines17:00
Применение подхода QbD к аналитической стратегии — ключ к успеху
Томас Жак, Вакцины GSK17:30
Проблемы и возможности интеграции QbD в разработку и производство вакцин
Nausheen Rahman, Sanofi Pasteur18:00
Риск-ориентированные подходы к проектированию биофармацевтических предприятий
Кавита Рамалингам Айер, MSD18:30
End of Conference Day 119:30
Networking ReceptionWednesday, 25 April 2018
9:00
Welcome and Introduction
Kerstin Wilken, PDA Europe
Cristiana Campa, Председатель конференции, GSK Vaccines
Nancy Cauwenberghs, Стул для конференций, MSD9:05 — 11:05
Сессия 5. Развитие технических аспектов производства вакцин
Развитие технических аспектов производства вакцин
Модератор: Кристиана Кампа, GSK Vaccines9:05
Прогнозирование пирогенного содержания без моделей животных
Сара Валентини, GSK9:35
Проблема категоризации параметров процесса: комплексный процесс ранжирования
Джеффрой Гельдхоф, Вакцины GSK10:05
Валидация процесса и непрерывная проверка процесса стерилизации вакцин
Антон Мангольд, tempris
Александр Кассис, GSK Canada- 8
10:35
Предварительно заполняемые шприцы Критерии выбора вакцин: техническое сравнение нескольких типов шприцев
Лоран Жанмар, Вакцины GSK
Кристиан Хельбиг, SCHOTT11:05 – 11:35
Перерыв на кофе, постерная сессия и выставка11:35 – 13:15
Сессия 6: Инновационная последующая обработка вакцин
Модератор: Марта Фолмсби, PALL11:40
Путаница с фильтрацией в процессе проверки: текущие темы стерилизующей фильтрации в FDA/CDER
Erika Pfeiler, FDA США12:05
Понимание стерильной фильтрации вакцинных наносуспензий
John Welsh, PALL12:35
Осветление вирусных вакцин и векторов на основе фильтров
Юнесс Черради, Merck KGaA13:00
Вопросы и ответы, обсуждение13:15 – 14:15
Перерыв на обед, постерная сессия и выставка14:15 – 17:00
Сессия 7: Глобальные взгляды отрасли на текущее регулирование – перспективы на будущее
Модератор: Нэнси Каувенбергс, МСД14:15
Сложность управления изменениями после утверждения и новые подходы к регулированию: Актуальность для вакцин
Эндрю Деавин, Вакцины GSK
Тьерри Пастино 9090 San14:45
Нехватка вакцин – от слов к делу Точка зрения руководителей отдела качества вакцин
Андерс Винтер, Санофи Пастер
Марчелло Колао, Вакцины GSK15:15 – 15:45
Перерыв на кофе, постерная сессия и выставка15:45
Панельная дискуссия, вопросы и ответы – Основные моменты конференции: Возможности для разработки вакцин
Матс Велин, MPA
Хайди Мейер, PEI
Richard H. Siggers, Health Canada
Siggers, Health Canada
Gwenaël Ciréfice, EDQM16:30
Summary & End of Conference & Farewell
Cristiana Campa, Conference Chair, GSK Vaccines
Nancy Cauwenberghs, Conference Chair, MSD
Kerstin Wilken, PDA Europe
Дополнительная информация
Есть вопрос? У нас есть ответы
Свяжитесь с нами
Путешествия
ПОЖАЛУЙСТА, ПРОЧТИТЕ PDA не является аффилированным лицом и не имеет контрактов с какой-либо сторонней подрядной компанией, работающей с отелями. Если кто-либо, кроме PDA или отеля, выбранного PDA, свяжется с вами и предложит представить какое-либо мероприятие PDA, он этого не сделает. PDA рекомендует бронировать отель напрямую через официальный выбранный PDA отель, указанный на нашем веб-сайте.
Если кто-либо, кроме PDA или отеля, выбранного PDA, свяжется с вами и предложит представить какое-либо мероприятие PDA, он этого не сделает. PDA рекомендует бронировать отель напрямую через официальный выбранный PDA отель, указанный на нашем веб-сайте.
Как добраться
Самолетом
Скоро будет дополнительная информация.
На автомобиле
Более подробная информация появится в ближайшее время.
Другие варианты
Дополнительная информация появится позже.
Направления
Регистрационный сбор
Обычная цена
- В целях безопасности информации о вашей кредитной карте: пожалуйста, отправьте свои данные только по факсу
- Для упрощения регистрации обратите внимание на полезные советы в регистрационной форме
3 способа регистрации
- Онлайн-регистрация
- ФАКС: +49 30 436 55 08 66
- [электронная почта защищена]
Пожалуйста, не забудьте войти в систему, если вы уже являетесь членом PDA!
Если вы работаете в государственном учреждении или органе здравоохранения или в академической организации, пожалуйста, свяжитесь с г-жой Антье Петцхольд перед регистрацией.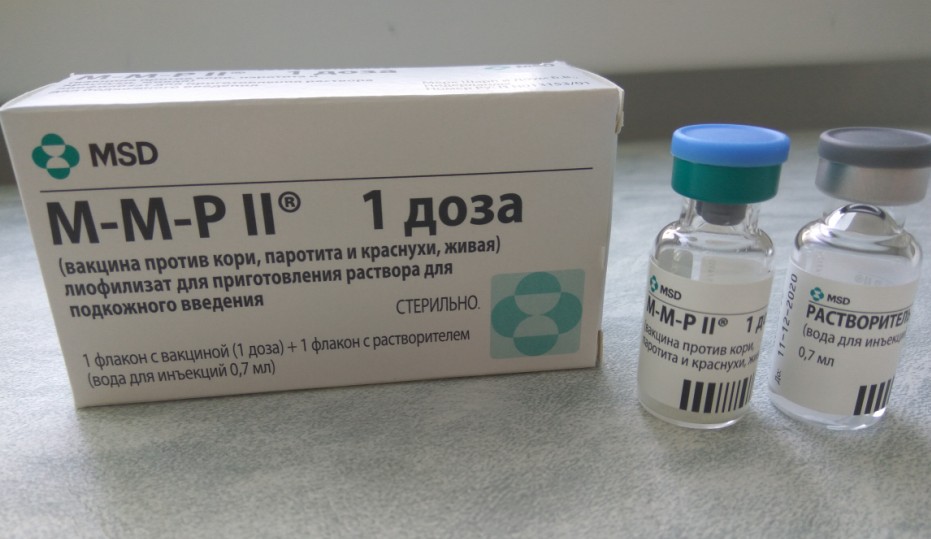 Она проверит ваш статус и зарегистрирует вас.
Она проверит ваш статус и зарегистрирует вас.
- Все заявки, связанные с получением визы, должны быть отправлены в PDA EU не позднее, чем за четыре недели до начала мероприятия. При более поздней регистрации PDA Europe не сможет помочь участникам в каких-либо визовых вопросах.
- Все расходы, возникающие в связи с визовыми вопросами, несут зарегистрированные лица. (Это относится, в частности, к расходам на подачу документов курьером.)
- Потенциальные участники должны быть клиентами судоходного агентства UPS и предоставить свой регистрационный номер клиента UPS в PDA EU (вместе с регистрацией).
Регистрационный сбор
Имеете ли вы право на получение скидки? Нужна помощь?
Член
By 4 March 2018
1.395 Euro
After 4 March 2018
1. 595 Euro
595 Euro
Nonmember
By 4 March 2018
1,695 Евро
После 4 марта 2018
1.895 EURO 9004
.0028
By 4 March 2018
700 Euro
After 4 March 2018
800 Euro
All fees given in Евро и без учета НДС (21%)
Контакт
Антье Петжолдт
Менеджер по регистрации, отделению и членству
Тел.: +49 (0) 30 43 655 08-10
Факс: +49(0) 30 43 655 08-66
Электронная почта
Избранные экспоненты
Мошенничество со списком участников по электронной почте
К сожалению, циркулируют электронные письма, предлагающие продать списки участников многих конференций и мероприятий PDA. Эти письма рассылают мошенники.
Эти письма рассылают мошенники.
Примечание : PDA не продает свои списки экспонентов или посетителей, и ни одна третья сторона не уполномочена распространять или продавать какие-либо списки, связанные с нашими мероприятиями. Заявления о том, что мы предлагаем наши списки участников, являются мошенническими. Если вы получаете электронные письма с предложением продать списки участников конференции PDA, не связывайтесь с отправителем и немедленно удалите сообщение.
Стать экспонентом
Хотите стать экспонентом? Узнайте о возможностях и преимуществах.
Информация о запросе
Информационные партнеры
Вакцины от рака поджелудочной железы — PMC
1. Американское онкологическое общество. Общество АС. Факты и цифры рака 2012. 2012 [Google Scholar]
2. Hruban RH, Goggins M, Parsons J, et al. Модель прогрессирования рака поджелудочной железы. Клин Рак Рез. 2000;6(8):2969–2972. [PubMed] [Google Scholar]
[PubMed] [Google Scholar]
3. Clark CE, Beatty GL, Vonderheide RH. Иммунонадзор за аденокарциномой поджелудочной железы: выводы из генетически модифицированных мышиных моделей рака. Рак Летт. 2009 г.;279(1):1–7. [PubMed] [Google Scholar]
4. Kubuschok B, Xie X, Jesnowski R, et al. Экспрессия антигенов рака яичка в клеточных линиях карциномы поджелудочной железы, аденокарциномы поджелудочной железы и хронического панкреатита. Инт Джей Рак. 2004;109(4):568–575. [PubMed] [Google Scholar]
5. Guerra C, Collado M, Navas C, et al. Воспаление, вызванное панкреатитом, способствует развитию рака поджелудочной железы, подавляя индуцированное онкогенами старение. Раковая клетка. 2011;19(6):728–739. [Бесплатная статья PMC] [PubMed] [Google Scholar]
6. Guerra C, Schuhmacher AJ, Canamero M, et al. Хронический панкреатит необходим для индукции аденокарциномы протоков поджелудочной железы онкогенами K-Ras у взрослых мышей. Раковая клетка. 2007;11(3):291–302. [PubMed] [Google Scholar]
7. Fridlender ZG, Sun J, Kim S, et al. Поляризация фенотипа ассоциированных с опухолью нейтрофилов по TGF-бета: «N1» против «N2» TAN. Раковая клетка. 2009;16(3):183–194. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Fridlender ZG, Sun J, Kim S, et al. Поляризация фенотипа ассоциированных с опухолью нейтрофилов по TGF-бета: «N1» против «N2» TAN. Раковая клетка. 2009;16(3):183–194. [Бесплатная статья PMC] [PubMed] [Google Scholar]
8. Грегори А.Д., Хоутон А.М. Опухолеассоциированные нейтрофилы: новые мишени для терапии рака. Рак рез. 2011;71(7):2411–2416. [PubMed] [Академия Google]
9. Nozawa H, Chiu C, Hanahan D. Инфильтрирующие нейтрофилы опосредуют начальное ангиогенное переключение в мышиной модели многостадийного канцерогенеза. Proc Natl Acad Sci U S A. 2006;103(33):12493–12498. [Бесплатная статья PMC] [PubMed] [Google Scholar]
10. Esposito I, Menicagli M, Funel N, et al. Воспалительные клетки способствуют возникновению ангиогенного фенотипа при аденокарциноме протоков поджелудочной железы. Джей Клин Патол. 2004;57(6):630–636. [Бесплатная статья PMC] [PubMed] [Google Scholar]
11. Albazaz R, Verbeke CS, Rahman SH, et al. Экспрессия циклооксигеназы-2 связана с тяжестью поражений PanIN: возможная связь между хроническим панкреатитом и раком поджелудочной железы. Панкреатология. 2005;5(4-5):361–369. [PubMed] [Google Scholar]
Панкреатология. 2005;5(4-5):361–369. [PubMed] [Google Scholar]
12. Maitra A, Ashfaq R, Gunn CR, et al. Экспрессия циклооксигеназы 2 при аденокарциноме поджелудочной железы и интраэпителиальной неоплазии поджелудочной железы: иммуногистохимический анализ с автоматизированной визуализацией клеток. Ам Джей Клин Патол. 2002;118(2):194–201. [PubMed] [Google Scholar]
13. Schmitz-Winnenthal FH, Volk C, Z’Graggen K, et al. Высокие частоты функциональных опухолереактивных Т-клеток в костном мозге и крови больных раком поджелудочной железы. Рак рез. 2005;65(21):10079–10087. [PubMed] [Google Scholar]
14. Fukunaga A, Miyamoto M, Cho Y, et al. CD8+ лимфоциты, инфильтрирующие опухоль, вместе с CD4+ лимфоцитами, инфильтрирующими опухоль, и дендритные клетки улучшают прогноз пациентов с аденокарциномой поджелудочной железы. Поджелудочная железа. 2004;28(1):e26–31. [PubMed] [Академия Google]
15. Acuto O, Michel F. CD28-опосредованная костимуляция: количественная поддержка передачи сигналов TCR. Нат Рев Иммунол. 2003;3(12):939–951. [PubMed] [Google Scholar]
Нат Рев Иммунол. 2003;3(12):939–951. [PubMed] [Google Scholar]
16. Цзоу В. Иммуносупрессивные сети в опухолевой среде и их терапевтическое значение. Нат Рев Рак. 2005;5(4):263–274. [PubMed] [Google Scholar]
17. Чжэн Л., Джаффи Э.М. Вакцинотерапия и иммунотерапия рака поджелудочной железы. В: Neoptolemos J, Urrutia R, Abbruzzese L и др., редакторы. Панкреатический рак. Нью-Йорк: Springer Science; 2010. С. 1269.–1318. [Google Scholar]
18. Корман А.Дж., Пеггс К.С., Эллисон Дж.П. Блокада контрольных точек в иммунотерапии рака. Ад Иммунол. 2006; 90: 297–339. [Бесплатная статья PMC] [PubMed] [Google Scholar]
19. Bierie B, Moses HL. Микроокружение опухоли: TGFbeta: молекулярный Джекил и Хайд рака. Нат Рев Рак. 2006;6(7):506–520. [PubMed] [Google Scholar]
20. Goggins M, Kern SE, Offerhaus JA, et al. Прогресс в генетике рака: уроки рака поджелудочной железы. Энн Онкол. 1999 г.;10(Приложение 4):4–8. [PubMed] [Google Scholar]
21. Harizi H, Gualde N. Ключевая роль PGE2 и IL-10 в перекрестной регуляции медиаторов воспаления, происходящих из дендритных клеток. Селл Мол Иммунол. 2006;3(4):271–277. [PubMed] [Google Scholar]
Ключевая роль PGE2 и IL-10 в перекрестной регуляции медиаторов воспаления, происходящих из дендритных клеток. Селл Мол Иммунол. 2006;3(4):271–277. [PubMed] [Google Scholar]
22. Bellone G, Turletti A, Artusio E, et al. Связанный с опухолью трансформирующий фактор роста-бета и интерлейкин-10 вносят вклад в системный иммунный фенотип Th3 у пациентов с карциномой поджелудочной железы. Ам Джей Патол. 1999;155(2):537–547. [Бесплатная статья PMC] [PubMed] [Google Scholar]
23. Апостолопулос В., Син П.С., Маккензи И.Ф. Иммунный ответ мыши на клетки, трансфицированные человеческим MUC1: иммунизация клеточными и синтетическими антигенами. Рак рез. 1994;54(19):5186–5193. [PubMed] [Google Scholar]
24. De Monte L, Reni M, Tassi E, et al. Инфильтрат внутриопухолевых Т-хелперов 2-го типа коррелирует с ассоциированной с раком продукцией стромального лимфопоэтина фибробластами тимуса и снижением выживаемости при раке поджелудочной железы. J Эксперт Мед. 2011;208(3):469–478. [Бесплатная статья PMC] [PubMed] [Google Scholar]
25. Чен Л. Ко-ингибиторные молекулы семейства B7-CD28 в контроле Т-клеточного иммунитета. Нат Рев Иммунол. 2004;4(5):336–347. [PubMed] [Google Scholar]
Чен Л. Ко-ингибиторные молекулы семейства B7-CD28 в контроле Т-клеточного иммунитета. Нат Рев Иммунол. 2004;4(5):336–347. [PubMed] [Google Scholar]
26. Лахеру Д., Джаффи Э.М. Иммунотерапия рака поджелудочной железы — наука, движущая клинический прогресс. Нат Рев Рак. 2005;5(6):459–467. [PubMed] [Google Scholar]
27. Argani P, Iacobuzio-Donahue C, Ryu B, et al. Мезотелин сверхэкспрессирован в подавляющем большинстве протоковых аденокарцином поджелудочной железы: идентификация нового маркера рака поджелудочной железы с помощью серийного анализа экспрессии генов (SAGE) Clin Cancer Res. 2001;7(12):3862–3868. [PubMed] [Академия Google]
28. Томас А.М., Сантарсьеро Л.М., Лутц Э.Р. и соавт. Мезотелин-специфические ответы CD8(+) Т-клеток свидетельствуют о перекрестном праймировании in vivo антигенпрезентирующими клетками у вакцинированных больных раком поджелудочной железы. J Эксперт Мед. 2004;200(3):297–306. [Бесплатная статья PMC] [PubMed] [Google Scholar]
29. Hassan R, Ebel W, Routhier EL, et al. Доклиническая оценка MORAb-009, химерного антитела, нацеленного на ассоциированный с опухолью мезотелин. Иммунитет против рака. 2007; 7:20. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Hassan R, Ebel W, Routhier EL, et al. Доклиническая оценка MORAb-009, химерного антитела, нацеленного на ассоциированный с опухолью мезотелин. Иммунитет против рака. 2007; 7:20. [Бесплатная статья PMC] [PubMed] [Google Scholar]
30. Le DT, Brockstedt DG, Nir-Paz R, et al. Живая аттенуированная вакцина против листерии (ANZ-100) и живая аттенуированная вакцина против листерии, экспрессирующая мезотелин (CRS-207), для лечения прогрессирующего рака: фаза I исследований безопасности и индукции иммунитета. Клин Рак Рез. 2012;18(3):858–868. [Бесплатная статья PMC] [PubMed] [Google Scholar]
31. Zheng L, Foley K, Huang L, et al. Зависимая от фосфорилирования тирозина 23 локализация аннексина А2 на клеточной поверхности необходима для инвазии и метастазирования рака поджелудочной железы. ПЛОС Один. 2011;6(4):e19390. [Бесплатная статья PMC] [PubMed] [Google Scholar]
32. Zheng L, Jaffee EM. Аннексин А2 является новой антигенной мишенью для иммунотерапии рака поджелудочной железы. Онкоиммунология. 2012;1(1):112–114. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Онкоиммунология. 2012;1(1):112–114. [Бесплатная статья PMC] [PubMed] [Google Scholar]
33. Iacobuzio-Donahue CA. Генетическая эволюция рака поджелудочной железы: уроки, извлеченные из проекта секвенирования генома рака поджелудочной железы. Кишка. 2012;61(7):1085–1094. [Бесплатная статья PMC] [PubMed] [Google Scholar]
34. Jones S, Zhang X, Parsons DW, et al. Основные сигнальные пути при раке поджелудочной железы человека, выявленные глобальным геномным анализом. Наука. 2008;321(5897): 1801–1806 гг. [Бесплатная статья PMC] [PubMed] [Google Scholar]
35. Segal NH, Parsons DW, Peggs KS, et al. Ландшафт эпитопов при раке молочной железы и колоректальном раке. Рак рез. 2008;68(3):889–892. [PubMed] [Google Scholar]
36. Шапиро Д., Тарин Б. Современные и новые методы лечения резистентного к кастрации рака предстательной железы. Эксперт Rev Anticancer Ther. 2012;12(7):951–964. [PubMed] [Google Scholar]
37. Gaudernack G. Перспективы вакцинотерапии рака поджелудочной железы. Best Pract Res Clin Gastroenterol. 2006;20(2):299–314. [PubMed] [Google Scholar]
Best Pract Res Clin Gastroenterol. 2006;20(2):299–314. [PubMed] [Google Scholar]
38. Melief CJ, van der Burg SH. Иммунотерапия установленного (пред) злокачественного заболевания синтетическими длиннопептидными вакцинами. Нат Рев Рак. 2008;8(5):351–360. [PubMed] [Google Scholar]
39. Gjertsen MK, Bakka A, Breivik J, et al. Вакцинация мутантными пептидами ras и индукция реактивности Т-клеток у пациентов с карциномой поджелудочной железы, несущих соответствующую мутацию RAS. Ланцет. 1995;346(8987):1399–1400. [PubMed] [Академия Google]
40. Gjertsen MK, Bjorheim J, Saeterdal I, et al. Цитотоксические CD4+ и CD8+ Т-лимфоциты, полученные при вакцинации пациента мутантным пептидом p21-ras (12Val), распознают 12Val-зависимые вложенные эпитопы, присутствующие в составе вакцинного пептида, и убивают аутологичные опухолевые клетки, несущие эту мутацию. Инт Джей Рак. 1997;72(5):784–790. [PubMed] [Google Scholar]
41. Jaffee EM. Иммунотерапия рака. Энн Н.Ю. Академия наук. 1999; 886: 67–72. [PubMed] [Google Scholar]
1999; 886: 67–72. [PubMed] [Google Scholar]
42. Dranoff G, Jaffee E, Lazenby A, et al. Вакцинация облученными опухолевыми клетками, сконструированными для секреции мышиного гранулоцитарно-макрофагального колониестимулирующего фактора, стимулирует сильный, специфический и длительный противоопухолевый иммунитет. Proc Natl Acad Sci U S A. 1993;90(8):3539–3543. [Бесплатная статья PMC] [PubMed] [Google Scholar]
43. Gjertsen MK, Buanes T, Rosseland AR, et al. Внутрикожная вакцинация пептидом ras с гранулоцитарно-макрофагальным колониестимулирующим фактором в качестве адъюванта: клинические и иммунологические ответы у пациентов с аденокарциномой поджелудочной железы. Инт Джей Рак. 2001;92(3):441–450. [PubMed] [Google Scholar]
44. Gilliam AD, Broome P, Topuzov EG, et al. Международное многоцентровое рандомизированное контролируемое исследование G17DT у больных раком поджелудочной железы. Поджелудочная железа. 2012;41(3):374–379. [PubMed] [Google Scholar]
45. Vonderheide RH, Hahn WC, Schultze JL, et al. Каталитическая субъединица теломеразы представляет собой широко экспрессируемый опухолеассоциированный антиген, распознаваемый цитотоксическими Т-лимфоцитами. Иммунитет. 1999;10(6):673–679. [PubMed] [Google Scholar]
Vonderheide RH, Hahn WC, Schultze JL, et al. Каталитическая субъединица теломеразы представляет собой широко экспрессируемый опухолеассоциированный антиген, распознаваемый цитотоксическими Т-лимфоцитами. Иммунитет. 1999;10(6):673–679. [PubMed] [Google Scholar]
46. Bernhardt SL, Gjertsen MK, Trachsel S, et al. Вакцинация теломеразным пептидом пациентов с нерезектабельным раком поджелудочной железы: исследование фазы I/II с увеличением дозы. Бр Дж Рак. 2006;95(11):1474–1482. [Бесплатная статья PMC] [PubMed] [Google Scholar]
47. Cole DJ, Wilson MC, Baron PL, et al. Фаза I исследования рекомбинантной вакцины против вируса коровьей оспы СЕА с поствакцинальным заражением пептидом СЕА. Гул Джин Тер. 1996;7(11):1381–1394. [PubMed] [Google Scholar]
48. Goydos JS, Elder E, Whiteside TL, et al. Фаза I испытаний синтетической вакцины на основе муцинового пептида. Индукция специфической иммунной реактивности у больных аденокарциномой. J Surg Res. 1996;63(1):298–304. [PubMed] [Google Scholar]
49. Kaufman HL, Kim-Schulze S, Manson K, et al. Вакцинотерапия на основе поксвируса для пациентов с распространенным раком поджелудочной железы. J Transl Med. 2007; 5:60. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Kaufman HL, Kim-Schulze S, Manson K, et al. Вакцинотерапия на основе поксвируса для пациентов с распространенным раком поджелудочной железы. J Transl Med. 2007; 5:60. [Бесплатная статья PMC] [PubMed] [Google Scholar]
50. Arlen PM, Gulley JL, Madan RA, et al. Доклинические и клинические исследования рекомбинантных поксвирусных вакцин для терапии рака. Критический преподобный Иммунол. 2007;27(5):451–462. [PubMed] [Google Scholar]
51. Сингх Р., Патерсон Ю. Listeria monocytogenes как вектор опухолеассоциированных антигенов для иммунотерапии рака. Эксперт Rev Вакцины. 2006;5(4):541–552. [PubMed] [Google Scholar]
52. Singh R, Dominiecki ME, Jaffee EM, et al. Слияние с Listeriolysin O и доставка Listeria monocytogenes повышает иммуногенность HER-2/neu и выявляет субдоминантные эпитопы у мышей FVB/N. Дж Иммунол. 2005;175(6):3663–3673. [PubMed] [Академия Google]
53. Brockstedt DG, Giedlin MA, Leong ML, et al. Противораковые вакцины на основе листерий, отличающие иммуногенность от токсичности. Proc Natl Acad Sci U S A. 2004;101(38):13832–13837. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Proc Natl Acad Sci U S A. 2004;101(38):13832–13837. [Бесплатная статья PMC] [PubMed] [Google Scholar]
54. Yoshimura K, Laird LS, Chia CY, et al. Живая аттенуированная Listeria monocytogenes эффективно лечит метастазы колоректального рака в печень и сильно усиливается за счет истощения регуляторных Т-клеток. Рак рез. 2007;67(20):10058–10066. [PubMed] [Академия Google]
55. Gilboa E. Противораковые вакцины на основе DC. Джей Клин Инвест. 2007;117(5):1195–1203. [Бесплатная статья PMC] [PubMed] [Google Scholar]
56. Lepisto AJ, Moser AJ, Zeh H, et al. Фаза I/II исследования импульсной аутологичной вакцины на основе дендритных клеток с пептидом MUC1 в качестве адъювантной терапии у пациентов с удаленными опухолями поджелудочной железы и желчевыводящих путей. Рак Тер. 2008; 6 (Б): 955–964. [Бесплатная статья PMC] [PubMed] [Google Scholar]
57. Kimura Y, Tsukada J, Tomoda T, et al. Клиническая и иммунологическая оценка иммунотерапии на основе дендритных клеток в сочетании с гемцитабином и/или S-1 у пациентов с распространенным раком поджелудочной железы.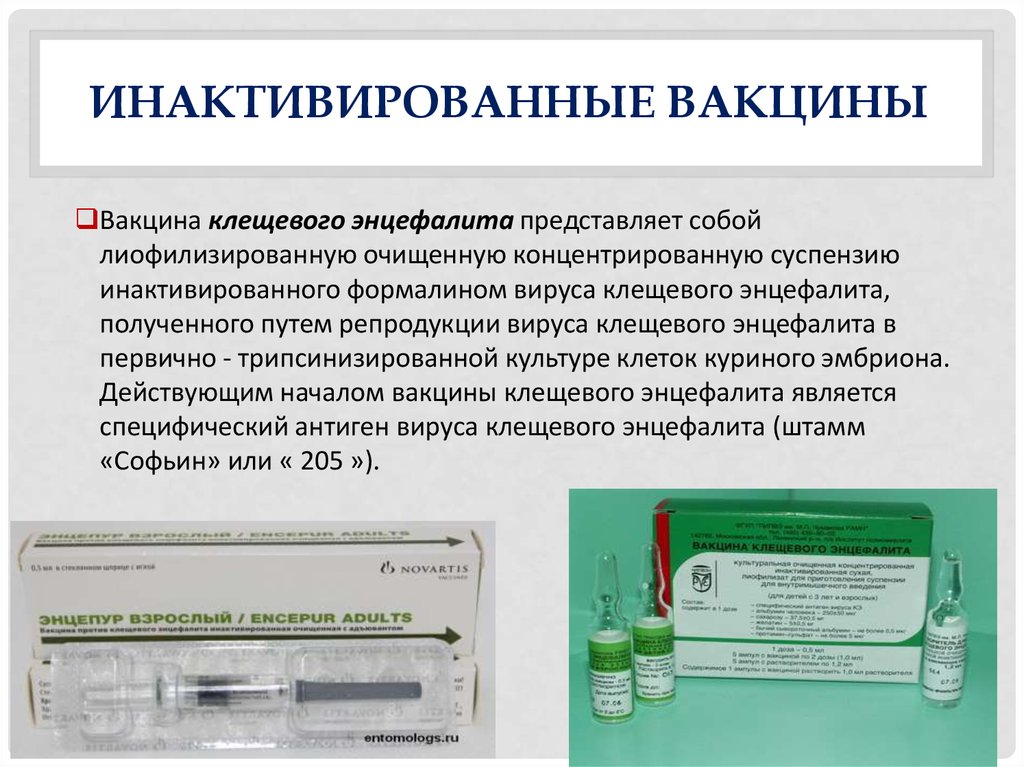 Поджелудочная железа. 2012;41(2):195–205. [PubMed] [Google Scholar]
Поджелудочная железа. 2012;41(2):195–205. [PubMed] [Google Scholar]
58. Simons JW, Jaffee EM, Weber CE, et al. Биоактивность аутологичных вакцин против облученного почечно-клеточного рака, полученных путем переноса гена гранулоцитарно-макрофагального колониестимулирующего фактора ex vivo. Рак рез. 1997;57(8):1537–1546. [Бесплатная статья PMC] [PubMed] [Google Scholar]
59. Немунайтис Дж. Вакцины против рака: GVAX, генная вакцина GM-CSF. Эксперт Rev Вакцины. 2005;4(3):259–274. [PubMed] [Google Scholar]
60. Hege KM, Jooss K, Pardoll D. Иммунотерапия раковых клеток с модифицированным геном GM-CSF: мышей и мужчин. Int Rev Immunol. 2006;25(5-6):321–352. [PubMed] [Академия Google]
61. Jaffee EM, Hruban RH, Biedrzycki B, et al. Новая аллогенная гранулоцитарно-макрофагальная колониестимулирующая опухолевая вакцина против рака поджелудочной железы: фаза I испытаний безопасности и иммунной активации. Дж. Клин Онкол. 2001;19(1):145–156. [PubMed] [Google Scholar]
62. Lutz E, Yeo CJ, Lillemoe KD, et al. Летально облученная аллогенная гранулоцитарно-макрофагальная колониестимулирующая фактор-секретирующая вакцина против аденокарциномы поджелудочной железы. Испытание фазы II безопасности, эффективности и иммунной активации. Энн Сург. 2011;253(2):328–335. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Lutz E, Yeo CJ, Lillemoe KD, et al. Летально облученная аллогенная гранулоцитарно-макрофагальная колониестимулирующая фактор-секретирующая вакцина против аденокарциномы поджелудочной железы. Испытание фазы II безопасности, эффективности и иммунной активации. Энн Сург. 2011;253(2):328–335. [Бесплатная статья PMC] [PubMed] [Google Scholar]
63. Laheru D, Lutz E, Burke J, et al. Аллогенная гранулоцитарно-макрофагальная колониестимулирующая иммунотерапия опухоли, секретирующая фактор, отдельно или последовательно с циклофосфамидом при метастатическом раке поджелудочной железы: пилотное исследование безопасности, осуществимости и иммунной активации. Клин Рак Рез. 2008;14(5):1455–1463. [Бесплатная статья PMC] [PubMed] [Google Scholar]
64. Ghiringhelli F, Menard C, Puig PE, et al. Метрономная схема циклофосфамида избирательно истощает CD4+CD25+ регуляторные Т-клетки и восстанавливает эффекторные функции Т- и NK у больных раком на терминальной стадии. Рак Иммунол Иммунотер. 2007;56(5):641–648. [PubMed] [Академия Google]
[PubMed] [Академия Google]
65. Mandell RB, Flick R, Staplin WR, et al. Технология alphaGal HyperAcute((R)): повышение иммуногенности противовирусных вакцин за счет использования естественной alphaGal-опосредованной зоонозной блокады. Зоонозы Общественное здравоохранение. 2009;56(6-7):391–406. [PubMed] [Google Scholar]
66. Hardacre JM, Mulcahy MF, Talamonti M, et al. Влияние сверхострой иммунотерапии в дополнение к стандартной адъювантной терапии резецированного рака поджелудочной железы на безрецидивную и общую выживаемость: предварительный анализ данных фазы II. Ежегодное собрание ASCO; 2010. [Google Академия]
67. Ascierto PA, Marincola FM, Ribas A. Моноклональные антитела против CTLA4: прошлое и будущее в клиническом применении. J Transl Med. 2011;9:196. [Бесплатная статья PMC] [PubMed] [Google Scholar]
68. Ribas A, Hanson DC, Noe DA, et al. Тремелимумаб (CP-675,206), цитотоксический антиген 4, ассоциированный с Т-лимфоцитами, блокирующий моноклональное антитело, в клинической разработке для пациентов с раком. Онколог. 2007;12(7):873–883. [PubMed] [Google Scholar]
Онколог. 2007;12(7):873–883. [PubMed] [Google Scholar]
69. Вебер Дж. Обзор: антитело против CTLA-4 ипилимумаб: тематические исследования клинического ответа и нежелательных явлений, связанных с иммунитетом. Онколог. 2007;12(7):864–872. [PubMed] [Академия Google]
70. Роял Р.Э., Леви С., Тернер К. и др. Испытание фазы 2 монотерапии ипилимумабом (анти-CTLA-4) при местно-распространенной или метастатической аденокарциноме поджелудочной железы. J Иммунотер. 2010;33(8):828–833. [Бесплатная статья PMC] [PubMed] [Google Scholar]
71. Le DT, Lutz E, Huang L, et al. Фаза Ib исследования ипилимумаба отдельно или в комбинации с аллогенными опухолевыми клетками поджелудочной железы, трансфицированными геном GM-CSF (вакцина) при раке поджелудочной железы. симпозиум по желудочно-кишечным ракам; 2012. [Google Академия]
72. Clark CE, Hingorani SR, Mick R, et al. Динамика иммунной реакции на рак поджелудочной железы от начала до инвазии. Рак рез. 2007;67(19):9518–9527. [PubMed] [Google Scholar]
[PubMed] [Google Scholar]
73. Beatty GL, Chiorean EG, Fishman MP, et al. Агонисты CD40 изменяют строму опухоли и проявляют эффективность против карциномы поджелудочной железы у мышей и людей. Наука. 2011;331(6024):1612–1616. [Бесплатная статья PMC] [PubMed] [Google Scholar]
74. Keir ME, Butte MJ, Freeman GJ, et al. PD-1 и его лиганды в толерантности и иммунитете. Анну Рев Иммунол. 2008; 26: 677–704. [PubMed] [Академия Google]
75. Brahmer JR, Tykodi SS, Chow LQ, et al. Безопасность и активность антитела против PD-L1 у пациентов с распространенным раком. N Engl J Med. 2012;366(26):2455–2465. [Бесплатная статья PMC] [PubMed] [Google Scholar]
76. Topalian SL, Hodi FS, Brahmer JR, et al. Безопасность, активность и иммунные корреляты антитела против PD-1 при раке. N Engl J Med. 2012;366(26):2443–2454. [Бесплатная статья PMC] [PubMed] [Google Scholar]
77. Шевач Е.М. Специальный обзор регуляторных Т-клеток: как я стал знатоком Т-супрессоров/регуляторных клеток. Иммунология. 2008;123(1):3–5. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Иммунология. 2008;123(1):3–5. [Бесплатная статья PMC] [PubMed] [Google Scholar]
78. Liyanage UK, Moore TT, Joo HG, et al. Преобладание регуляторных Т-клеток повышено в периферической крови и микроокружении опухоли у пациентов с аденокарциномой поджелудочной железы или молочной железы. Дж Иммунол. 2002;169(5):2756–2761. [PubMed] [Google Scholar]
79. Curiel TJ, Coukos G, Zou L, et al. Специфическое привлечение регуляторных Т-клеток при карциноме яичников способствует иммунной привилегии и предсказывает снижение выживаемости. Нат Мед. 2004;10(9):942–949. [PubMed] [Google Scholar]
80. Woo EY, Chu CS, Goletz TJ, et al. Регуляторные CD4(+)CD25(+) Т-клетки в опухолях пациентов с немелкоклеточным раком легкого на ранней стадии и раком яичников на поздней стадии. Рак рез. 2001;61(12):4766–4772. [PubMed] [Академия Google]
81. Hiraoka N, Onozato K, Kosuge T, et al. Преобладание FOXP3+ регуляторных Т-клеток увеличивается при прогрессировании аденокарциномы протоков поджелудочной железы и ее предраковых поражений. Клин Рак Рез. 2006;12(18):5423–5434. [PubMed] [Google Scholar]
Клин Рак Рез. 2006;12(18):5423–5434. [PubMed] [Google Scholar]
82. Huang CT, Workman CJ, Flies D, et al. Роль LAG-3 в регуляторных Т-клетках. Иммунитет. 2004;21(4):503–513. [PubMed] [Google Scholar]
83. Le DT, Jaffee EM. Модуляция регуляторных Т-клеток с использованием циклофосфамида в подходах к вакцинам: современная перспектива. Рак рез. 2012;72(14):3439–3444. [Бесплатная статья PMC] [PubMed] [Google Scholar]
84. Casares N, Pequignot MO, Tesniere A, et al. Каспазозависимая иммуногенность доксорубицин-индуцированной гибели опухолевых клеток. J Эксперт Мед. 2005; 202(12):1691–1701. [Бесплатная статья PMC] [PubMed] [Google Scholar]
85. Chu Y, Wang LX, Yang G, et al. Эффективность противоопухолевой вакцины, продуцирующей GM-CSF, после химиотерапии доцетакселом у мышей с установленной карциномой легких Льюис. J Иммунотер. 2006;29(4):367–380. [PubMed] [Академия Google]
86. Machiels JP, Reilly RT, Emens LA, et al. Циклофосфамид, доксорубицин и паклитаксел усиливают противоопухолевый иммунный ответ цельноклеточных вакцин, секретирующих гранулоциты/макрофагальные колониестимулирующие факторы, у HER-2/нейтолеризованных мышей. Рак рез. 2001;61(9):3689–3697. [PubMed] [Google Scholar]
Рак рез. 2001;61(9):3689–3697. [PubMed] [Google Scholar]
87. Plate JM, Plate AE, Shott S, et al. Влияние гемцитабина на иммунные клетки у пациентов с аденокарциномой поджелудочной железы. Рак Иммунол Иммунотер. 2005;54(9):915–925. [PubMed] [Академия Google]
88. Motoyoshi Y, Kaminoda K, Saitoh O, et al. Различные механизмы противоопухолевого действия низких и высоких доз циклофосфамида. Oncol Rep. 2006;16(1):141–146. [PubMed] [Google Scholar]
89. Lutsiak ME, Semnani RT, De Pascalis R, et al. Ингибирование функции CD4(+)25+ Т-регуляторных клеток, участвующей в усилении иммунного ответа при применении циклофосфамида в низких дозах. Кровь. 2005;105(7):2862–2868. [PubMed] [Google Scholar]
90. Ercolini AM, Ladle BH, Manning EA, et al. Рекрутирование латентных пулов высокоавидных CD8(+) Т-клеток к противоопухолевому иммунному ответу. J Эксперт Мед. 2005;201(10):1591–1602. [Бесплатная статья PMC] [PubMed] [Google Scholar]
91. Sistigu A, Viaud S, Chaput N, et al.

 Siggers, PhD
Siggers, PhD  Siggers, Управление биологических и генетических препаратов, Health Canada
Siggers, Управление биологических и генетических препаратов, Health Canada  Калифано, МСД
Калифано, МСД 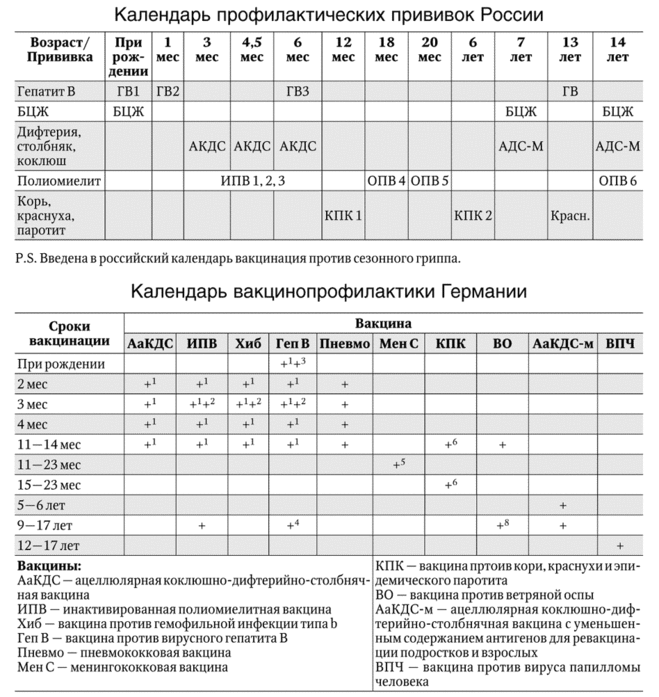 Развитие технических аспектов производства вакцин
Развитие технических аспектов производства вакцин  Siggers, Health Canada
Siggers, Health Canada