Содержание
Спасет ли прививка БЦЖ от Covid-19
В последнее время стала актуальной тема связи между коронавирусной инфекцией и БЦЖ вакциной. На сегодняшний день еще не разработана вакцина от коронавируса, однако есть некоторые интересные факты. Ученые из Нью-Йоркского университета опубликовали данные исследований, которые заставили многих задуматься. Они утверждают, что заболеваемость COVID-19 значительно выше на территории стран, которые отказались от обязательной вакцинации людей прививкой БЦЖ.
Есть также мнения, что все это выдумки, и не существует связи между БЦЖ, COVID-19. Так, все-таки, является ли вакцина БЦЖ сдерживающим фактором при коронавирусной инфекции?
Статистика распространения такого заболевания, как туберкулез, удручающая. Еще в 1993 году Всемирная Организация Здравоохранения отнесла туберкулез в группу опасных болезней с высокой контагиозностью. Только в 2017 году было зарегистрировано около 10-ти миллионов заболевших, из которых 1,6 миллиона умерли. Среди детей заболеваемость составила приблизительно 1 миллион, при этом в 230-ти тысячах случаев — с летальным исходом.
Вакцина имеет в своем составе ослабленного возбудителя бычьего туберкулеза и является единственным способом профилактики тяжелой патологии у человека. Несмотря на наличие противников данной прививки, другого варианта противостояния туберкулезу пока нет.
Согласно статистическим сведениям, bcg прививка позволяет предупредить развитие диссеминированной, легочной формы болезни у детей до 15-ти лет (при условии проведения вакцинации в роддоме).
В некоторых странах прививка не является обязательной, она делается детям из группы риска или в случае положительного результата кожного теста. На сегодня на территории 154 стран из 180 проводится вакцинация БЦЖ.
БЦЖ и COVID-19: совпадение? Не думаю
Ученые в Университете Нью-Йорка провели сравнение между уровнями заболеваемости коронавирусом в странах с разным обхватом людей, которым ранее была сделала bcg вакцина.
Виникли питання — проконсультуйтеся з лікарем
Для запису на консультацію телефонуйте або заповніть форму зворотнього зв’язку:
(050) 301-99-26
(067) 446-11-79
Заметим, что именно Италия, Испания, Америка, а также Нидерланды в прошлом столетии отказалась от вакцины БЦЖ. Некоторые страны внесли данную прививку в список необязательных. В итоге получаем всплеск коронавирусной инфекции на территориях этих государств. Что же касается стран постсоветского пространства, где риск заразиться туберкулезом выше, здесь вакцинация БЦЖ проводится каждому малышу еще в роддоме. В результате проведенной вакцинации организм иначе реагирует на коронавирусную инфекцию.
Некоторые страны внесли данную прививку в список необязательных. В итоге получаем всплеск коронавирусной инфекции на территориях этих государств. Что же касается стран постсоветского пространства, где риск заразиться туберкулезом выше, здесь вакцинация БЦЖ проводится каждому малышу еще в роддоме. В результате проведенной вакцинации организм иначе реагирует на коронавирусную инфекцию.
То же самое следует сказать об Индии, где прививка БЦЖ является обязательной с 1948 года. В стране с высокой плотностью населения, особенно в больших городах, низким уровнем санитарных условий, зафиксировано всего сто летальных исходов от COVID-19.
Даже если предположить о наличии погрешностей в статистических подсчетах, в СМИ нет информации о массовой смертности в Индии и большом количестве пациентов, которые находятся на искусственной вентиляции легких.
«Подопытный кролик» БЦЖ и хищник коронавирус
Казалось бы, обычная вакцина БЦЖ и COVID-19, как они связаны? Официально эпидемия коронавируса началась в декабре 2019 года на территории Китая. Начиная с конца января, инфекция начала распространяться по всему миру, массово поражая легочную ткань людей.
Начиная с конца января, инфекция начала распространяться по всему миру, массово поражая легочную ткань людей.
Всемирная Организация Здравоохранения в марте 2020 года признала нынешнюю эпидемию коронавируса пандемией. На тот момент было зарегистрировано около 4,6 тысяч летальных исходов на фоне COVID-19. Инфекция охватила более 110 стран.
По статусу на 3 апреля число инфицированных превысило 1 миллион на территории 180 стран мира. На этом фоне в некоторых регионах стран наблюдается вспышка заболевания со смертностью более 10%. Несмотря на это, всемирная статистика заболеваемости и смертности не имеет ужасающих цифр.
Ученые выдвинули предположение, что в странах, в которых раньше всего была введена в использование вакцина БЦЖ, заболеваемость COVID-19 значительно ниже в сравнении со странами, где БЦЖ не является обязательной прививкой.
В каких странах делают БЦЖ? На территории Ирана вакцинация проводится с 1984 года, поэтому на данный момент смертность в стране составляет почти 20 случаев на миллион человек. Что касается Японии, где БЦЖ используется с 1947 года, смертность в 100 раз ниже (0,28 случаев на миллион людей).
Что касается Японии, где БЦЖ используется с 1947 года, смертность в 100 раз ниже (0,28 случаев на миллион людей).
В Бразилии прививка введена в график обязательной вакцинации еще в 1920 году, поэтому смертность от COVID-19 у них составляет всего 0,0573 случаев на миллион человек.
Такая шумиха вокруг БЦЖ и коронавируса заставила ученых начать проведение исследований. Так, ученые из Германии разработали на основе БЦЖ новую вакцину (VPM1002), которая включает ослабленные бактерии, имеющие сходство с палочками Коха.
Они создавались путем генной модификации, что облегчило их распознавание иммунной системой. Вакцина также эффективна против злокачественной патологии мочевого пузыря. Теперь разработчики думают, как испытать прививку БЦЖ от коронавируса.
В свою очередь исследователи из Австралии объявили о старте проекта, в ходе которого будет оцениваться эффективность прививки БЦЖ при коронавирусной инфекции. Аналогичные исследования будут проводиться на территории Англии, Германии, Нидерландов. В Украине подобные исследования пока не проводятся.
В Украине подобные исследования пока не проводятся.
«БЦЖ — не вакцина от коронавируса». Может ли прививка от туберкулеза защитить от Covid-19
Ученые из Австралии, Нидерландов, Греции и Германии готовят клинические исследования, чтобы проверить, может ли противотуберкулезная прививка БЦЖ защитить от коронавируса. В австралийском Мельбурне собрали группу из 4 000 медицинских работников, которые работают с пациентами с Covid-19. Одной половине сделают прививку БЦЖ, другой — плацебо. Доктор биологических наук, иммунолог Дмитрий Купраш по просьбе «Правмира» объяснил, действительно ли БЦЖ может быть эффективна.
Группа ученых из Нью-Йоркского института технологий выпустила статью о предполагаемой пользе противотуберкулезной прививки БЦЖ при Covid-19. Исследователи заметили, что в странах, где прививки делают, как в Китае и России, ситуация со скоростью распространения коронавируса и летальностью отличается. Например, в Испании 124 летальных случая на миллион жителей, а в соседней с ней Португалии — 10, при этом Португалия отказалась от обязательной вакцинации против туберкулеза в 2017 году, а Испания — в 1981-м.
БЦЖ — вакцина, изготовленная из штамма ослабленной живой бычьей туберкулезной палочки (Mycobacterium bovis). Для взрослых она не очень эффективна, однако хорошо защищает от тяжелого течения туберкулеза у детей. В странах с высоким уровнем жизни дети и так не болеют туберкулезом, поэтому там от БЦЖ отказались. В странах с не такой благоприятной ситуацией, в том числе в России, где у ребенка действительно есть риск подхватить туберкулезную палочку, вакцинация обязательна.
Дмитрий Купраш
Дмитрий Купраш рассказывает, что еще в 80-х годах прошлого века научные исследования показали, что мыши и люди, которые получили вакцину БЦЖ, оказываются более устойчивы к большому спектру различных заболеваний, в частности к некоторым РНК-вирусам и гриппу. Сравнительно недавно ученые открыли врожденные лимфоидные клетки, это группа лимфоцитов, которые вовлечены в быстрое реагирование организма во время воспалительного процесса. Этот феномен, который называют врожденной иммунной памятью, только недавно начали исследовать на молекулярном и клеточном уровне. Дмитрий объясняет:
Дмитрий объясняет:
— Сам факт активного иммунного ответа на что-то организм запоминает, и следующий иммунный ответ на что-то другое может быть более эффективным. Возможно, вакцина БЦЖ это может сделать в случае с коронавирусом. Но надо понимать, что вряд ли это поможет тяжелым больным. Вакцинация БЦЖ не может дать специфического защитного иммунитета против коронавируса, там нет ничего молекулярно родственного, чтобы появились защитные антитела. Но, возможно, получится сопротивляемость организма увеличить. Поможет ли это защитить медиков, на самом деле неизвестно. Руководитель австралийских испытаний совершенно справедливо говорит, что проверить гипотезу можно, но гарантии нет никакой. Есть и такой момент: иммунная система детей не совсем зрелая, она устроена иначе, чем иммунная система взрослых, и может оказаться, что при вакцинации согласно календарю в детском возрасте БЦЖ будет давать защитный эффект, а взрослым не поможет.
Прививка безопасная, хуже точно не будет, но совершенно необязательно, что будет лучше.
По словам ученого, объяснений, почему в разных странах ситуация развивается по-разному, может быть множество. У коронавирусов яркий эффект так называемых супер-распространителей. Это проявляется и в новой эпидемии.
— Один человек, который по непонятному стечению обстоятельств заразил 100 человек, может резко изменить ход течения инфекции. Вполне может быть, что в Испании таких людей было, предположим, три, а в Португалии — ни одного, и это предопределило ход событий. Туристический поток, методика тестирования, методика подсчета статистики — может быть множество причин, почему цифры отличаются. Гипотеза с БЦЖ выглядит, конечно, впечатляюще, но пока на это надо смотреть с большой долей скепсиса, — говорит Дмитрий Купраш.
Первые результаты исследований, по словам Дмитрия, появятся только через несколько месяцев. Если гипотеза оправдает себя, то для России прогноз станет более благоприятным, однако это не повод отменять самоизоляцию. Также не следует бежать в поликлинику, чтобы делать повторную прививку — это создаст дополнительное напряжение в медицинском учреждении и повысит вероятность распространения инфекции.
Поскольку вы здесь…
У нас есть небольшая просьба. Эту историю удалось рассказать благодаря поддержке читателей. Даже самое небольшое ежемесячное пожертвование помогает работать редакции и создавать важные материалы для людей.
Сейчас ваша помощь нужна как никогда.
Подпишитесь на Правмир в
Выбор читателей «Правмира»
Подпишитесь на самые интересные материалы недели.
БЦЖ: история и современное применение противотуберкулезной вакцины — Pharma Technology Focus | Выпуск 112
Вакцины
Вакцина БЦЖ показала многообещающие результаты в текущих испытаниях Covid-19, что привело к предположению, что вакцину можно перепрофилировать для борьбы с вирусом. Чтобы узнать больше,
Darcy Jimenez рассказывает об истории вакцины против туберкулеза и ее разнообразных применениях сегодня.
I В 1921 году человеку впервые была введена противотуберкулезная вакцина Bacillus Calmette-Guérin (BCG). Вакцина была разработана французскими учеными Альбером Кальметтом и Камиллой Герен для защиты от туберкулеза легких, основной причины смерти в начале 19 века.00с.
Вакцина была разработана французскими учеными Альбером Кальметтом и Камиллой Герен для защиты от туберкулеза легких, основной причины смерти в начале 19 века.00с.
За сто лет, прошедших с момента ее первого применения, вакцина БЦЖ не только предотвратила бесчисленное количество смертей от туберкулеза, но и широко использовалась для защиты или лечения ряда других заболеваний. Прививка, составляющая основу Списка основных лекарственных средств Всемирной организации здравоохранения (ВОЗ), ежегодно делается примерно 100 миллионам детей во всем мире.
Чтобы узнать больше, мы рассмотрим историю вакцины и ее применение в современной медицине.
Вакцина против туберкулеза
Немецкий врач и микробиолог Роберт Кох впервые определил Mycobacterium tuberculosis ( M. tuberculosis ) как причину туберкулезной инфекции в 19 веке.
Позже была выдвинута гипотеза, что инфекция штаммом Mycobacterium bovis ( M. bovis ), обнаруженным у коров, может обеспечить защиту от туберкулеза человека. Испытания этого подхода привели к катастрофическим результатам, поскольку было обнаружено, что туберкулез крупного рогатого скота столь же вреден, как и человеческий штамм.
bovis ), обнаруженным у коров, может обеспечить защиту от туберкулеза человека. Испытания этого подхода привели к катастрофическим результатам, поскольку было обнаружено, что туберкулез крупного рогатого скота столь же вреден, как и человеческий штамм.
В 1904 году Кальметт выделил M. bovis из молока инфицированной коровы и вместе со своим помощником, ставшим партнером Гереном, работал над созданием ослабленной версии бактерии, которую можно было бы безопасно использовать в качестве вакцины. После 13 лет исследований был разработан аттенуированный штамм БЦЖ.
БЦЖ была принята Комитетом по здравоохранению Лиги Наций — предшественника ВОЗ — в 1928 году, но вакцина не получила широкого распространения до окончания Второй мировой войны.
Нетуберкулезные микобактерии
Было обнаружено, что противотуберкулезная вакцина обеспечивает некоторую защиту от проказы и язвы Бурули, других заболеваний, также вызываемых микобактериями.
По данным Всемирной организации здравоохранения, защитный эффект БЦЖ против проказы – инфекционного заболевания, которое может привести к поражению нервов, дыхательных путей, кожи и глаз – составляет от 20% до 80%.
Язва Бурули — относительно редкое заболевание, характеризующееся безболезненными открытыми ранами и чаще всего встречающееся в странах Африки к югу от Сахары и в Австралии. Исследования показали, что вакцинация БЦЖ может помочь защитить от язвы Бурули или отсрочить ее прогрессирование.
Иммунотерапия рака
БЦЖ является наиболее часто используемым иммунотерапевтическим средством для лечения рака мочевого пузыря на ранней стадии. С 1977 года вакцина используется в качестве стандарта лечения этого заболевания, ее часто вводят непосредственно в мочевой пузырь после операции, чтобы предотвратить рост или возвращение туда раковых клеток.
Механизм действия вакцины БЦЖ при этом показании неясен, но считается, что прививка вызывает местный иммунный ответ, который помогает бороться с опухолями в мочевом пузыре.
Вакцина также исследуется в качестве потенциальной терапии колоректального рака. Исследования показали, что БЦЖ может принести некоторую пользу в области лечения заболеваний, и американская биотехнологическая компания Vaccinogen в настоящее время испытывает противораковую вакцину с адъювантом БЦЖ для лечения рака толстой кишки II стадии.
Диабет 1-го типа
Ранние исследования показали, что БЦЖ может быть перспективным средством лечения аутоиммунных заболеваний, таких как диабет 1-го типа.
В 2018 году исследователи из Массачусетской больницы общего профиля обнаружили, что вакцинация БЦЖ привела к «длительному клинически и статистически значимому падению» уровня HbA1c (среднего уровня глюкозы в крови) в исследовании I фазы у людей с диабетом 1 типа. Дополнительные результаты этого года показали, среди прочего, что БЦЖ была особенно эффективной в снижении уровня HbA1c у участников в возрасте до 21 года.
Covid-19
В настоящее время проводится более 20 клинических испытаний, чтобы выяснить, можно ли перепрофилировать прививку БЦЖ для защиты от Covid-19 или снижения риска серьезного повреждения легких вирусом.
Одно исследование, проведенное исследователями из Национального института исследований туберкулеза при Индийском совете медицинских исследований, показало, что вакцина может уменьшить воспаление, вызванное Covid, у пожилых людей. Более ранние исследования, еще не прошедшие экспертную оценку, также показали, что вакцинация БЦЖ привела к снижению риска заражения Covid-19 на 68%.диагнозов и может служить профилактической мерой для тех, кто наиболее уязвим к вирусу.
Более ранние исследования, еще не прошедшие экспертную оценку, также показали, что вакцинация БЦЖ привела к снижению риска заражения Covid-19 на 68%.диагнозов и может служить профилактической мерой для тех, кто наиболее уязвим к вирусу.
Хотя в настоящее время БЦЖ не рекомендуется для использования в этом контексте, в случае успеха испытаний вакцина может стать альтернативным средством защиты от тяжелой формы Covid-19 в странах, где запасы вакцины против коронавируса ограничены.
В значительной степени подготовка к распространению вакцины будет означать изучение того, что уже было достигнуто.
«Я думаю, что отчасти это связано с моделированием — вы можете моделировать множество процессов логистики производства и распределения», — говорит Бойл. «Вы можете спланировать несколько сценариев «что, если», по крайней мере, определить слабые места в системе и какие факторы стресса могут вывести ее из строя. Затем, когда вы начинаете видеть источник стресса, вы уже знаете, что это вызовет сбой в системе, и у вас уже есть план на случай непредвиденных обстоятельств».
На практике это может означать реализацию региональной стратегии с некоторой избыточностью в цепочке поставок, обеспечивающей поддержку, если какая-то страна окажется в изоляции.
Эффективная доставка миллиардов доз вакцины по всему миру будет сопряжена с чрезвычайно сложными логистическими и программными препятствиями.
«Все хотят работать с минимальными уровнями запасов и максимальной экономической эффективностью, но сейчас мы задаемся вопросом: «Когда бережливое производство становится слишком бережливым?», — говорит Бойл. «Профиль риска этой позиции изменился, и люди собираются пересмотреть некоторые из своих целей. Речь идет об обеспечении устойчивости цепочки поставок и определении уровня риска, на который вы готовы пойти».
С появлением первых вакцин пришло время поставщикам логистических услуг, правительствам, авиакомпаниям и многим другим начать серьезную подготовку. Как подчеркивали выступавшие на телеконференции IATA, это грандиозное мероприятие, требующее тщательного планирования от каждой заинтересованной стороны.
«Эффективная доставка миллиардов доз вакцины всему миру будет сопряжена с чрезвычайно сложными логистическими и программными препятствиями на всем протяжении цепочки поставок», — сказал д-р Сет Беркли, генеральный директор Gavi, Vaccine Alliance. «Мы рассчитываем на сотрудничество с правительством, производителями вакцин и партнерами по логистике, чтобы обеспечить эффективное глобальное развертывание безопасной и доступной вакцины от Covid-19.вакцина».
Вакцинация БЦЖ для борьбы с туберкулезом
Abou-Zeid C, Smith I, Grange J, Steele J, Rook G (1986) Подразделение дочерних штаммов Bacille Calmette -Герена (БЦЖ) в соответствии с образцами секретируемого белка. J Gen Microbiol 132: 3047–3053
PubMed
КАС
Google Scholar
Armbruster C, Junker W, Vetter N, Jaksch G 11990) Диссеминированная инфекция Bacille Calmette-Guérin у больного СПИДом через 30 лет после вакцинации БЦЖ. J заразить Dis 162: 1216
J заразить Dis 162: 1216
Google Scholar
Aronson JD (1948) Защитная вакцинация против туберкулеза с социальными ссылками на вакцинацию БЦЖ. Am Rev Tuberc 58: 275–281
Google Scholar
Aronson JD, Dannenberg AM (1935) Влияние вакцинации БЦЖ на туберкулез в младенчестве и детстве. Am J Dis Child 50: 1117–1130
Google Scholar
Aronson JD, Aronson CF, Taylor HC (1958) Двадцатилетняя оценка вакцинации БЦЖ в борьбе с туберкулезом. Arch Intern Med 101: 881–893
CAS
Google Scholar
Ashley MJ, Siebenman CO (1967) Чувствительность кожи к туберкулину после вакцинации БЦЖ вакцинами с высоким и низким количеством жизнеспособных клеток. Can Med Assoc J 97: 1335–1338
PubMed
КАС
Google Scholar
Беттаг О. Л., Калузный А.А., Морс Д., Раднер Д.Б. (1964) Исследование БЦЖ в государственной школе для умственно отсталых. Dis Chest 45: 503–507
Л., Калузный А.А., Морс Д., Раднер Д.Б. (1964) Исследование БЦЖ в государственной школе для умственно отсталых. Dis Chest 45: 503–507
CrossRef
пабмед
КАС
Google Scholar
Blackwell JM (1988) Бактериальные инфекции. В: Wakelin D, Blackwell JM (eds) Генетика устойчивости к бактериальным и паразитарным инфекциям. Тейлор и Фрэнсис, Лондон
Google Scholar
Blin P, Delolme HG, Heyraud JD, Charpak Y, Sentilhes L (1986) Оценка защитного эффекта вакцинации БЦЖ методом случай-контроль в Яунде, Камерун. Бугорок 67: 283–288
CrossRef
КАС
Google Scholar
Blondon H, Guez T, Paul G, Truffot-Pernot C, Sicard D (1991) Аденит и вакцина БЦЖ 6 после вакцинации в рамках SIDA. Presse Med 20: 1091
PubMed
КАС
Google Scholar
Botttiger M, Romanus V, de Verdier C, Boman G (1982) Остеит и другие осложнения, вызванные генерализованным БЦЖ-итом. Acta Paediatr Scand 71: 471–478
Acta Paediatr Scand 71: 471–478
CrossRef
Google Scholar
Bunch-Christensen K (1977) Оценка вакцин БЦЖ у детей, влияние штамма и дозы. J Biol Стенд 5: 159–164
CrossRef
пабмед
КАС
Google Scholar
Calmette, Guérin (1908) Lait Nocard
Google Scholar
Центры по контролю и профилактике заболеваний (1985 г.) Распространенная инфекция Mycobacterium bovis в результате вакцинации БЦЖ пациента с синдромом приобретенного иммунодефицита. MMWR 34: 227–228
Google Scholar
Центры по контролю за заболеваниями (1988 г.) Рекомендации Консультативного комитета по практике иммунизации (ACIP). Использование вакцин БЦЖ для борьбы с туберкулезом: совместное заявление ACIP и Консультативного комитета по ликвидации туберкулеза. MMWR 37: 663–664, 669–675
MMWR 37: 663–664, 669–675
Google Scholar
Центры по контролю за заболеваниями (1991 г.) Вакцинация БЦЖ и детская ВИЧ-инфекция – Руанда, 1988–1990 гг. MMWR 40: 833–836
Google Scholar
Clemens JB, Chuong JJH, Feinstein AR (1983) Противоречие BCG: методологическая и статистическая переоценка. JAMA 249: 2361–2369
CrossRef
Google Scholar
Coetzee AM, Berjak J (1968) БЦЖ в профилактике туберкулеза у взрослого населения. Proc Mine Med Off Assoc 48: 41–53
PubMed
КАС
Google Scholar
Кольдиц Г., Брюэр Т., Берки С., Уилсон М., Бурдик Э., Файнберг Х., Мостеллер Ф. (1994) Эффективность вакцины БЦЖ в профилактике туберкулеза. JAMA 271: 698–702
пабмед
КАС
Google Scholar
Колебандерс Р. , Манн Дж. М., Фрэнсис Х., Била К., Изалей Л., Каконде Н., Кабаселе К., Ифото Л., Нзиламби Н., Куинн Т.С., Ван дер Гроен Г., Карран Дж., Веркаутерен Г., Пиот П. (1987) Оценка клинического случая синдрома приобретенного иммунодефицита в Африке. Ланцет 1: 492–494
, Манн Дж. М., Фрэнсис Х., Била К., Изалей Л., Каконде Н., Кабаселе К., Ифото Л., Нзиламби Н., Куинн Т.С., Ван дер Гроен Г., Карран Дж., Веркаутерен Г., Пиот П. (1987) Оценка клинического случая синдрома приобретенного иммунодефицита в Африке. Ланцет 1: 492–494
CrossRef
пабмед
КАС
Google Scholar
Comstock GW (1988) Идентификация эффективной вакцины против туберкулеза. Ам Рев Респир Дис 138: 479–480
ПабМед
КАС
Google Scholar
Comstock GW, Edward PQ (1972) Американский взгляд на вакцинацию БЦЖ, иллюстрированный результатами контролируемого испытания в Пуэрто-Рико. Scand J Respir Dis 53: 207–217
PubMed
КАС
Google Scholar
Comstock GW, Webster RG (1969) Исследования туберкулеза в округе Маскоги, Джорджия. VII. Двадцатилетняя оценка вакцинации БЦЖ школьников. Am Rev Respir Dis 100: 839–845
ПабМед
КАС
Google Scholar
Comstock, GW, Edwards LB, Nabangxang H (1971) Чувствительность к туберкулину через восемь-пятнадцать лет после вакцинации БЦЖ. Am Rev Respir Dis 103: 572–575
Am Rev Respir Dis 103: 572–575
PubMed
КАС
Google Scholar
Comstock GW, Livesay VT, Woolpert SF (1974) Оценка вакцинации БЦЖ среди детей в Перто-Рико. Am J Общественное здравоохранение 64: 283–291
Перекрёстная ссылка
пабмед
КАС
Google Scholar
Comstock GW, Woolpert SF, Livesay VT (1976) Исследования туберкулеза в округе Маскоги, Джорджия. Двадцатилетняя оценка клинических испытаний вакцинации БЦЖ. Представитель общественного здравоохранения 91: 276–280
PubMed
КАС
Google Scholar
Криспен Р. (1989) История БЦЖ и ее подштаммов. В: БЦЖ при поверхностном раке мочевого пузыря. EORTC Genitour Group Monogr 6: 35–50
Google Scholar
Dawodu AH (1985) Туберкулиновая конверсия после вакцинации БЦЖ у недоношенных детей. Acta Paediatr Scand 74: 564–567
Acta Paediatr Scand 74: 564–567
CrossRef
пабмед
КАС
Google Scholar
Эдвардс Л.Б., Гелтинг А.С. (1950) Исследования вакцин БЦЖ. Bull World Health Organ 3: 1–24
PubMed
КАС
Google Scholar
Ferguson RS, Simes AB (1949) Вакцинация БЦЖ индийских младенцев в Саскачеване. Бугорок 30: 511
CrossRef
Google Scholar
Fine PEM (1988) Вакцинация БЦЖ против туберкулеза и проказы. Br Med Bull 44: 691–703
PubMed
КАС
Google Scholar
Friedland IR (1990) Бустерный эффект повторного туберкулинового тестирования у детей и его связь с вакцинацией БЦЖ. S Afr Med J 77: 387–389
ПабМед
КАС
Google Scholar
Frimodt-Moller J, Acharyulu GS, Kesava Pillai K (1973) Наблюдения за защитным эффектом вакцинации БЦЖ среди сельского населения Южной Индии: четвертый отчет. Bull Int Union Tuberc 48: 40–49
Bull Int Union Tuberc 48: 40–49
PubMed
КАС
Google Scholar
Гарднер Л.В. (1932) История штамма R1 туберкулезной палочки. Ам Рев Туберк 25: 577–590
Google Scholar
Gheorghiu M, LaGrange PH (1983) Жизнеспособность, термостабильность и иммуногенность четырех вакцин БЦЖ, приготовленных из четырех разных штаммов БЦЖ. Энн Иммунол 134C: 125–147
CAS
Google Scholar
Grange JM, Gibson JA (1986) Изменение иммуногенности БЦЖ от штамма к штамму. Dev Biol Stand 58: 37–41
PubMed
Google Scholar
Грейндж Дж.М., Гибсон Дж., Осборн Т.В. (1983) Что такое БЦЖ? Бугорок 64: 129–139
CAS
Google Scholar
Guld J, Waaler H, Sundaresan TK, Kaufmann PC, Ten Dam HG (1968) Продолжительность индуцированной БЦЖ чувствительности к туберкулину у детей и ее неактуальность для ревакцинации. Bull World Health Organ 39: 829–836
Bull World Health Organ 39: 829–836
PubMed
КАС
Google Scholar
Хэнк Дж.А., Чан Дж.К., Эдвардс М.Л., Мюллер Д., Смит Д.В. (1981) Влияние вирулентности Mycobacterium tuberculosis на защиту, индуцированную Bacille-Calmette-Guérin у морских свинок. J Infect Dis 143: 734–738
CrossRef
пабмед
КАС
Google Scholar
Hart PD, Sutherland I (1977) Вакцины БЦЖ и палочки полевки в профилактике туберкулеза в подростковом и раннем взрослом возрасте. Мед Д 2:293–295
Перекрёстная ссылка
КАС
Google Scholar
Hart PD, Sutherland I, Thomas J (1967) Иммунитет, обеспечиваемый эффективными вакцинами БЦЖ и бациллами полевки, в связи с индивидуальными вариациями чувствительности к туберкулину и техническими вариациями вакцин. Бугорок 48: 201–210
CrossRef
Google Scholar
Hesselberg I (1972) Лекарственная устойчивость шведско-норвежского штамма БЦЖ. Bull World Health Organ 46: 503–507
Bull World Health Organ 46: 503–507
ПабМед
КАС
Google Scholar
Heyworth B (1977) Отсроченная гиперчувствительность к PPD-S после вакцинации БЦЖ у африканских детей – 18-месячное полевое исследование. Trans R Soc Trop Med Hyg 71: 251–253
CrossRef
пабмед
КАС
Google Scholar
Horwitz O, Bunch-Christensen K (1972) Корреляция между чувствительностью к туберкулину через 2 месяца и 5 лет среди вакцинированных БЦЖ субъектов. Бык Всемирный орган здравоохранения 47: 49–58
ПабМед
КАС
Google Scholar
Houde C, Dery P (1988) Mycobacterium bovis сепсис у младенца с инфекцией, вызванной вирусом иммунодефицита человека. Pediatr Infect Dis J 7: 810–812
CrossRef
пабмед
КАС
Google Scholar
Houston S, Fanning A, Soskolne CL (1990) Эффективность вакцинации бациллой Кальметта-Герена (БЦЖ) против туберкулеза: исследование случай-контроль среди индейцев Договора, Альберта, Канада. AM J Эпидемиол 340–348
AM J Эпидемиол 340–348
Google Scholar
Международный союз по борьбе с туберкулезом (1978 г.) Фенотипы штаммов посевной партии вакцины БЦЖ: результаты международного совместного исследования. Бугорок 59: 139–142
CrossRef
Google Scholar
Jespersen A (1971) Эффективность вакцин БЦЖ определялась на животных. Кандидатская диссертация, Копенгагенский университет
Google Scholar
Karalliedde S, Katugaha LP, Uragoda CG (1987) Туберкулиновая реакция шри-ланкийских детей после вакцинации БЦЖ при рождении. Бугорок 68: 33–38
CrossRef
пабмед
КАС
Google Scholar
Kathipari K, Seth V, Sinclair S, Arora NK, Kukreja N (1982) Клеточный иммунный ответ после вакцинации БЦЖ как определяющий фактор оптимального возраста вакцинации. Indian J Med Res 76: 508–511
PubMed
КАС
Google Scholar
Lallemant-Le Coeur S, Lallemant M, Cheynier D, Nzingoula S, Drucker J, Larouze B (1991) Иммунизация бациллой Кальметта-Герена у младенцев, рожденных от ВИЧ-1-серопозитивных матерей. СПИД 5: 195–199
СПИД 5: 195–199
CrossRef
пабмед
Google Scholar
Lefford MJ (1977) Индукция и экспрессия иммунитета после иммунизации БЦЖ. Infect Immun 18: 646–653
PubMed
КАС
Google Scholar
Lehmann HG, Engelhardt H, Freudenstein H, Hennessen W, Widmark R (1979) Вакцинация БЦЖ новорожденных, младенцев, школьников и подростков, часть I: исследования по определению дозы с использованием штамма БЦЖ 1331 Копенгаген. Dev Biol Stand 43: 127–132
PubMed
КАС
Google Scholar
Левин М.И., Сакетт М.Ф. (1946) Результаты иммунизации БЦЖ в Нью-Йорке. Am Rev Tuberc 53: 517–532
PubMed
КАС
Google Scholar
Levy FM, Conge GA, Pasquier JF, Mauss H, Dubos R, Schaedler R (1961) Влияние вакцинации БЦЖ на судьбу вирулентных туберкулезных бацилл у мышей. Am Rev Respir Dis 84: 28–36
Am Rev Respir Dis 84: 28–36
PubMed
КАС
Google Scholar
Lotte A, Wasz-Hockert O, Poisson N, Dumitrescu N, Verron M, Couvet E (1984) Осложнения БЦЖ. Adv Tuberc Res 21: 107–193
PubMed
КАС
Google Scholar
Lotte A, Wasz-Hockert O, Poisson N, Engbaek H, Landmann H, Quast U, Andrasofszky B, Lugosi L, Vadasz Mihailescu P, Pal D, Sudic D (1988) Второе исследование IUATLD осложнений, вызванных внутрикожным введением БЦЖ-вакцинация. Bull Int Union Tuberc Lung Dis 63: 47–59
PubMed
КАС
Google Scholar
Ламб, Р., Шоу Д. (1992) Вакцинация против Mycobacterium bovis (БЦЖ). Прогрессирующее заболевание у пациента, симптоматически инфицированного вирусом иммунодефицита человека. Med J Aust 156: 286–287
ПабМед
КАС
Google Scholar
MacKaness GB (1968) Иммунология противотуберкулезного иммунитета. Am Rev Resp Dis 97: 337
Am Rev Resp Dis 97: 337
PubMed
КАС
Google Scholar
MacKay A, Alcorn MJ, Macleod IM, Stack BHR, Macleod T, Laidlaw M, Millar JS, White RG (1980) Смертельная диссеминированная БЦЖ-инфекция у 18-летнего мальчика. Ланцет 2: 1332–1334
CrossRef
пабмед
КАС
Google Scholar
Манерикар С.С., Малавия А.Н., Сингх М.Б., Раджгопалан П., Кумар Р. (1976) Иммунный статус и вакцинация БЦЖ у новорожденных с задержкой внутриутробного развития. Clin Exp Immunol 26: 173–175
PubMed
КАС
Google Scholar
McMurray DN, Carlomagno MA, Mintzer CL, Tetzlaff CL (1985) Mycobacterium bovis Вакцина БЦЖ не защищает морских свинок с дефицитом белка от респираторного заражения вирулентным вирусом Микобактерии туберкулеза . Infect Immun 50: 555–559
PubMed
КАС
Google Scholar
Milstien JB, Gibson JJ (1990) Контроль качества вакцины БЦЖ ВОЗ: обзор факторов, которые могут влиять на эффективность и безопасность вакцины. Bull World Health Organ 68: 93–108
Bull World Health Organ 68: 93–108
PubMed
КАС
Google Scholar
Минникин Д.Е., Парлетт Дж.Х., Магнуссон М., Риделл М., Линд А. (1984) Миколевокислотные образцы представителей Mycobacterium bovis БЦЖ. J Gen Microbiol 130: 2733–2736
PubMed
КАС
Google Scholar
Myint TT, Yin Y, Yi MM, Aye HH (1985) Реакция на БЦЖ у детей, ранее вакцинированных БЦЖ. Энн Троп Педиатр 5: 29–31
PubMed
КАС
Google Scholar
Нинан Дж., Гримонпрез А., Бертонбой Г., Франсуа А., Корню Г. (1988) Диссеминированная БЦЖ при ВИЧ-инфекции. Arch Dis Child 63: 1268–1269
CrossRef
пабмед
КАС
Google Scholar
Nyboe J, Bunch-Christensen K (1966) Анализ различных препаратов БЦЖ у человека. Bull World Health Organ 35: 645–650
PubMed
КАС
Google Scholar
Osborn TW (1983) Изменения штаммов БЦЖ. Бугорок 64: 1–13
Бугорок 64: 1–13
CrossRef
пабмед
КАС
Google Scholar
Padungchan S, Konjanart S, Kasiratta S (1986) Эффективность вакцинации БЦЖ новорожденных против детского туберкулеза в Бангкоке. Bull World Health Organ 64: 247–258
PubMed
КАС
Google Scholar
Palmer CE, Long MW (1966) Влияние инфекции атипичными микобактериями на вакцинацию БЦЖ и туберкулез. Am Rev Respir Dis 94: 533–568
Google Scholar
Палмер К., Мейер С.Н. (1951) Исследовательский вклад программ вакцинации БЦЖ. I. Туберкулиновая аллергия как семейный признак. Представитель общественного здравоохранения 66: 259–276
CrossRef
пабмед
КАС
Google Scholar
Peltola H, Salmi I, Vahvanen V, Ahlqvist J (1984) Вакцинация БЦЖ как причина остеомиелита и подкожного абсцесса. Arch Dis Child 59: 157–161
Arch Dis Child 59: 157–161
CrossRef
пабмед
КАС
Google Scholar
Ray CS, Pringle D, Legg W, Mbengeranwa OL (1988) Лимфаденит, связанный с вакцинацией БЦЖ: отчет о вспышке в Хараре, Зимбабве. Cent Afr J Med 34: 281–286
PubMed
КАС
Google Scholar
Reynes J, Perez C, Lamaury I, Janbon F, Bertrand A (1989) Bacille Calmette-Guérin аденит через 30 лет после иммунизации у больного СПИДом. J Infect Dis 160: 727
CrossRef
пабмед
КАС
Google Scholar
Rodrigues L, Diwan V, Wheeler J (1993) Защитный эффект БЦЖ против туберкулезного менингита и милиарного туберкулеза: метаанализ. Int J Epidemiol 22: 1154–1158
CrossRef
пабмед
КАС
Google Scholar
Rook GAW, Bahr GM, Stanford JL (1981) Влияние двух различных форм клеточно-опосредованного ответа на микобактерии на защитную эффективность БЦЖ. Бугорок 62: 63–68
Бугорок 62: 63–68
CrossRef
пабмед
КАС
Google Scholar
Rosenthal SR (1980) Пути и методы введения. В: Rosenthal SR (ed) Вакцина БЦЖ: туберкулез — рак. ПСЖ, Литтлтон, глава 11,12
Google Scholar
Rosenthal SR, Loewinsohn E, Graham M, Liveright D, Thorne M, Johnson V (1961a) Вакцинация БЦЖ в семьях, больных туберкулезом. Am Rev Respir Dis 84: 690–704
CAS
Google Scholar
Rosenthal SR, Loewinsohn E, Graham M, Liveright D, Thorne M, Johnson V (1961b) Вакцинация БЦЖ против туберкулеза в Чикаго. Двадцатилетнее исследование статистически проанализировано. Педиатрия 28: 622–641
CAS
Google Scholar
Sergent E, Catanei A, Ducros-Rougebief H (1960) Предварительное противотуберкулезное средство par le BCG. Campagne controlee poursuivie a Alger depuis 1935. Troisieme note. Arch Inst Pasteur d’Algerile 38: 131–137
Troisieme note. Arch Inst Pasteur d’Algerile 38: 131–137
Google Scholar
Shaaban MA, Ati Abdul M, Bahr GM, Stanford JL, Lockwood DNJ, McManus IC (1990) Ревакцинация БЦЖ: ее влияние на кожные пробы у кувейтских старших школьников. Eur Respir J 3: 187–191
PubMed
КАС
Google Scholar
Шапиро С., Кук Н., Эванс Д., Уиллетт В., Фахардо И., Кох-Везер Д., Бергонзоли Г., Боланос О., Герроэро Р., Хеннекенс С. (1985) Исследование случай-контроль БЦЖ и детского туберкулеза в Кали, Колумбия. Int J Epidemiol 14: 441–446
CrossRef
пабмед
КАС
Google Scholar
Smith DW, (1985) Защитный эффект БЦЖ при экспериментальном туберкулезе. Adv Tuberc Res 22: 66–73
Google Scholar
Smith DW, McMurray DN, Wiegeshaus EH, Grover AA, Harding GE (1970)Взаимоотношения хозяин-паразит при экспериментальном туберкулезе.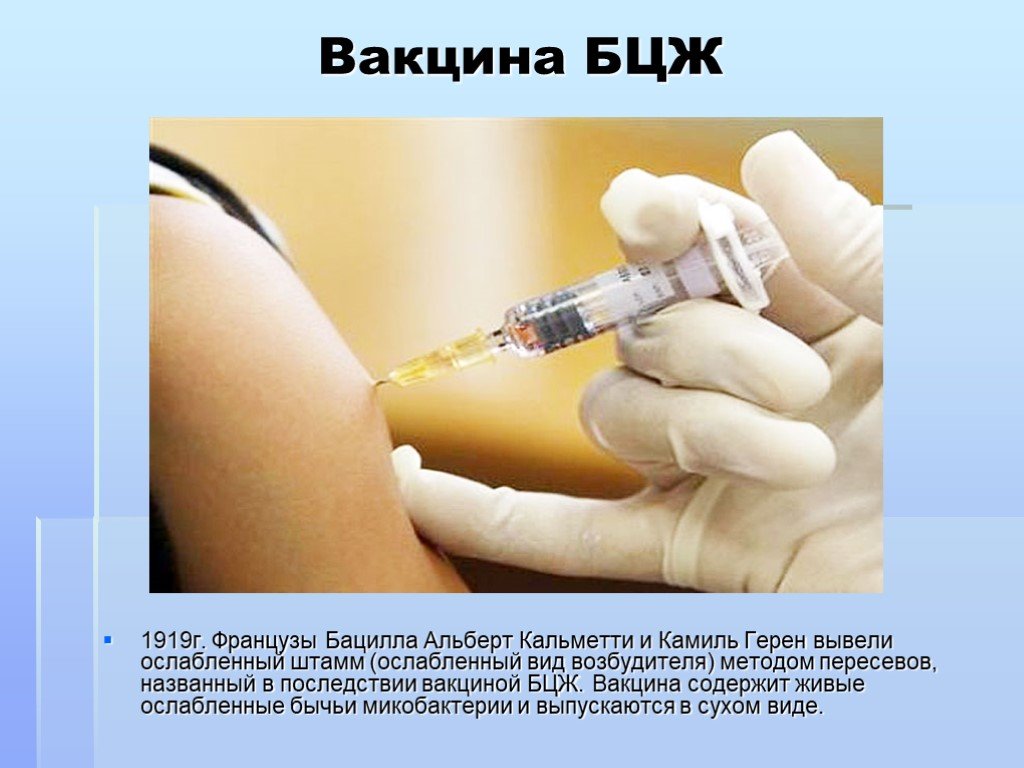 IV. Ранние явления в течении инфекции у вакцинированных и невакцинированных морских свинок. Ам Рев Респир Дис 102: 937–949
IV. Ранние явления в течении инфекции у вакцинированных и невакцинированных морских свинок. Ам Рев Респир Дис 102: 937–949
PubMed
КАС
Google Scholar
Smith E, Thybo S, Bennedsen J (1992) Инфекция Mycobacterium bovis у пациента со СПИДом: позднее осложнение вакцинации БЦЖ. Scand J Infect Dis 24: 109–110
CrossRef
пабмед
КАС
Google Scholar
Smith PG (1987) Исследование эффективности БЦЖ против туберкулеза методом случай-контроль. Bull Int Union Tuberc 62: 73–79
Google Scholar
Snider DE (1985) Bacille Calmette-Guérin вакцинация и туберкулиновые кожные пробы. JAMA 253: 3438–3439
Google Scholar
Stewart CJ (1968) Чувствительность кожи к PPD человека, птиц и БЦЖ после вакцинации БЦЖ. Бугорок 49: 84–91
CrossRef
пабмед
КАС
Google Scholar
Сазерленд I (1972) Письмо. Бугорок 53: 150–151
Бугорок 53: 150–151
CrossRef
КАС
Google Scholar
Tardieu M, Carriere JP, Truffot-Pernot C, Dupic Y (1988) Туберкулезный менингит, вызванный БЦЖ, у двух ранее здоровых детей. Ланцет 1: 440–441
CrossRef
пабмед
КАС
Google Scholar
Ten Dam HG, Pio A (1982) Патогенез туберкулеза и эффективность вакцинации. Бугорок 63: 225–233
Перекрёстная ссылка
пабмед
Google Scholar
Тиджани О., Амедом А., Тен Дам Х.Г. (1986) Защитный эффект вакцинации новорожденных БЦЖ против детского туберкулеза в африканском сообществе. Бугорок 67: 269–281
CrossRef
пабмед
КАС
Google Scholar
Tripathy SP (1987) Пятнадцатилетнее наблюдение за испытанием вакцины БЦЖ в Индии. Булл Инт Юнион Туберк 62: 69–72
Google Scholar
Vandiviere HM, Dworski M, Melvin I, Watson K, Begley J (1973)Эффективность бациллы Кальметта-Герена и резистентной к изониазиду бациллы Кальметта-Герена с химиопрофилактикой изониазидом и без нее со дня вакцинации. Am Rev Respir Dis 108: 301–313
Am Rev Respir Dis 108: 301–313
PubMed
КАС
Google Scholar
Weltman A, Rose D (1993) Безопасность вакцинации Bacille Calmette-Guérin при ВИЧ-инфекции и СПИДе. СПИД 7: 149–157
Перекрестная ссылка
пабмед
КАС
Google Scholar
Всемирная организация здравоохранения (1977 г.) Спонсируемый ВОЗ международный контроль качества вакцины БЦЖ. Серия технических отчетов ВОЗ 8
Google Scholar
Всемирная организация здравоохранения (1986 г.) Вакцинация новорожденных БЦЖ. Обоснование и руководящие принципы страновых программ. ВОЗ/ТБ/86.147
Google Scholar
Комитет экспертов Всемирной организации здравоохранения по биологической стандартизации (1985 г.) Требования к высушенной вакцине БЦЖ. Требования к биологическим веществам, № 11
Google Scholar
Всемирная организация здравоохранения/Международный союз по борьбе с туберкулезом (1989 г.
