Содержание
Инфанрикс® Гекса (Вакцина для профилактики дифтерии, столбняка, коклюша (бесклеточная), полиомиелита (инактивированная), гепатита В комбинированная, адсорбированная в комплекте с вакциной для профилактики инфекции, вызываемой Haemophilus influenzae тип b (Infanrix® hexa)
Инфанрикс® Гекса (Вакцина для профилактики дифтерии, столбняка, коклюша (бесклеточная), полиомиелита (инактивированная), гепатита В комбинированная, адсорбированная в комплекте с вакциной для профилактики инфекции, вызываемой Haemophilus influenzae тип b (суспензия для внутримышечного введения, 0.5 мл/доза), инструкция по медицинскому применению РУ № ЛП-№(000115)-(РГ-RU)
Дата последнего изменения: 15.01.2021
Содержание
- Действующее вещество
- ATX
- Нозологическая классификация (МКБ-10)
- Фармакологическая группа
- Лекарственная форма
- Состав
- Описание лекарственной формы
- Показания
- Противопоказания
- Применение при беременности и кормлении грудью
- Способ применения и дозы
- Побочные действия
- Взаимодействие
- Передозировка
- Особые указания
- Форма выпуска
- Условия отпуска из аптек
- Условия хранения
- Срок годности
- Заказ в аптеках Москвы
- Отзывы
Действующее вещество
Вакцина для профилактики дифтерии, коклюша, полиомиелита, столбняка и инфекций, вызываемых Haemophilus influenzae типа b (Diphtheria, tetanus, pertussis, polio and Haemophilus influenzae type b)
ATX
J07CA09 Вакцина против дифтерии, Haemophilus Influenzae B, коклюша, полиомиелита, столбняка, гепатита B
Нозологическая классификация (МКБ-10)
Список кодов МКБ-10
Фармакологическая группа
Вакцины, сыворотки, фаги и анатоксины
Лекарственная форма
Суспензия
для внутримышечного введения в комплекте с лиофилизатом для приготовления
суспензии для внутримышечного введения.
Состав
Чтобы получить доступ к скрытым полям, необходимо Войти
Описание лекарственной формы
Вакцина
для профилактики дифтерии, столбняка, коклюша (бесклеточная), полиомиелита
(инактивированная), гепатита B
комбинированная, адсорбированная: суспензия беловатого цвета, разделяющаяся при
отстаивании на бесцветную прозрачную жидкость и белый осадок, полностью
разбивающийся при встряхивании.
Вакцина
для профилактики инфекции, вызываемой Haemophilus
influenzae тип b, конъюгированная, адсорбированная:
лиофилизированный порошок или плотная масса белого цвета.
Восстановленный
раствор: непрозрачная жидкость, при отстаивании разделяющаяся на бесцветную
жидкость с образованием белого осадка, который легко ресуспендируется
встряхиванием.
Показания
Противопоказания
Применение при беременности и кормлении грудью
Способ применения и дозы
Побочные действия
Данные, полученные при проведении клинических исследований
Представленный
ниже профиль безопасности основан на данных, полученных более чем
у 16000 участников клинических исследований.
При
применении АаКДС и комбинированных вакцин, содержащих АаКДС-компоненты,
наблюдалось увеличение частоты местных реакций и лихорадки после назначения
ревакцинирующей дозы вакцины Инфанрикс® Гекса в 18 месяцев
жизни, по сравнению с курсом первичной иммунизации.
Нежелательные
реакции, представленные ниже, перечислены в соответствии с поражением
органов и систем органов и частотой встречаемости. Частота встречаемости
определяется следующим образом: очень часто
(≥1/10), часто
(≥1/100 и <1/10), нечасто
(≥1/1000 и <100), редко
(≥1/10000 и <1/1000), очень редко
(<1/10000, включая отдельные случаи). Категории частоты были сформированы
на основании клинических исследований препарата.
Частота встречаемости нежелательных реакций
Инфекционные и паразитарные заболевания
Нечасто: инфекции
верхних дыхательных путей.
Нарушения со стороны обмена веществ и питания
Очень часто:
потеря аппетита.
Нарушения психики
Очень часто: раздражительность,
необычный плач, беспокойство.
Часто: возбудимость.
Нарушения со стороны нервной системы
Нечасто: сонливость.
Очень редко:
судороги (на фоне повышенной температуры тела или без повышенной
температуры тела)3.
Нарушения со стороны дыхательной системы, органов грудной
клетки и средостения
Нечасто: кашель1.
Редко: бронхит.
Нарушения со стороны желудочно-кишечного тракта
Часто: рвота, диарея.
Нарушения со стороны кожи и подкожных тканей
Часто: зуд1.
Редко: сыпь.
Очень редко:
дерматит, крапивница1.
Общие расстройства и нарушения в месте введения
Очень часто: болезненности
покраснение, отек в месте инъекции (≤50 мм), повышение температуры
тела ≥38 °С, утомляемость.
Часто: отек в месте
инъекции (>50 мм)2, повышение температуры тела
>39,5 °С, уплотнение в месте инъекции.
Нечасто: диффузный отек
конечности, в которую была произведена инъекция, иногда с вовлечением
прилежащего сустава2.
Данные пострегистрационного наблюдения
При
наблюдении за массовым применением вакцины зарегистрированы следующие
нежелательные реакции:
Нарушения со стороны крови и лимфатической системы
Редко: лимфаденопатия,
тромбоцитопения.
Нарушения со стороны иммунной системы
Редко: аллергические
реакции (включая анафилактические и анафилактоидные реакции).
Нарушения со стороны нервной системы
Редко: коллапс или
шокоподобное состояние (гипотензивно-гипореспонсивный синдром)3.
Нарушения со стороны дыхательной системы, органов грудной
клетки и средостения
Редко: апноэ1
(см. сведения о применении у глубоко недоношенных детей (гестационный
сведения о применении у глубоко недоношенных детей (гестационный
возраст ≤28 недель в разделе «Особые указания»).
Нарушения со стороны кожи и подкожных тканей
Редко:
ангионевротический отек1.
Общие расстройства и нарушения в месте введения
Редко: выраженный
отек, отек всей конечности, в которую была произведена инъекция2,
пузырьки в месте введения вакцины.
1– наблюдается
только при применении других АаКДС-вакцин производства компании
«ГлаксоСмитКляйн».
2– у
детей, получивших в качестве курса первичной вакцинации бесклеточные коклюшные
вакцины, чаще развиваются местные реакции в виде припухлости после введения
ревакцинирующей дозы, чем у детей, которым первичная вакцинация
проводилась с использованием цельноклеточных вакцин. Такие реакции обычно
проходят, в среднем, через 4 дня.
3– анализ
данных пострегистрационного наблюдения позволяет сделать вывод о потенциально
повышенном риске развития судорог (на фоне повышенной температуры тела или без
повышенной температуры тела) и гипотензивно-гипореспонсивного синдрома при
совместном применении вакцины Инфанрикс® Гекса и вакцины
Превенар 13 (вакцина пневмококковая полисахаридная конъюгированная
адсорбированная, тринадцативалентная) по сравнению с применением только вакцины
Инфанрикс® Гекса.
Безопасность применения у недоношенных детей
В
рамках исследований курс первичной вакцинации был проведен с применением
вакцины Инфанрикс® Гекса у свыше 1000 недоношенных детей (родившиеся
в период с 24 по 36 недели гестации), ревакцинацию на втором
году жизни получили свыше 200 недоношенных детей. По данным
сравнительных исследований частота реакций, наблюдавшаяся у недоношенных и
доношенных детей, была одинакова.
Опыт, полученный в ходе использования вакцины против
гепатита B
Во
время пострегистрационного наблюдения после назначения вакцины против гепатита B
производства компании «ГлаксоСмитКляйн Байолоджикалз с.а.» у детей младше
2 лет были зарегистрированы следующие побочные явления
(причинно-следственная связь с вакцинацией не установлена): менингит,
синдром, напоминающий сывороточную болезнь, паралич, энцефалит, энцефалопатия,
нейропатия, синдром Гийена-Барре, неврит, снижение артериального давления,
васкулит, плоский лишай, многоформная эритема, артрит, мышечная слабость.
Взаимодействие
Передозировка
Передозировка
при использовании однодозовой упаковки маловероятна.
Особые указания
Форма выпуска
Суспензия
для внутримышечного введения в комплекте с лиофилизатом для приготовления
суспензии для внутримышечного введения, 0,5 мл (1 доза).
Вакцина для профилактики дифтерии, столбняка, коклюша
(бесклеточная), полиомиелита (инактивированная), гепатита B комбинированная, адсорбированная упакована:
по 0,5 мл (1 доза) суспензии в шприц нейтрального стекла
типа I (Евр.Ф.). Носик шприца укупорен колпачком из резины.
Вакцина для профилактики инфекции, вызываемой Haemophilus
influenzae тип b, конъюгированная, адсорбированная упакована: по
1 дозе
лиофилизата во флакон нейтрального стекла типа I (Евр.Ф.),
укупоренный пробкой из резины и алюминиевым колпачком под обкатку, снабженным
защитной отщелкивающейся пластиковой крышечкой.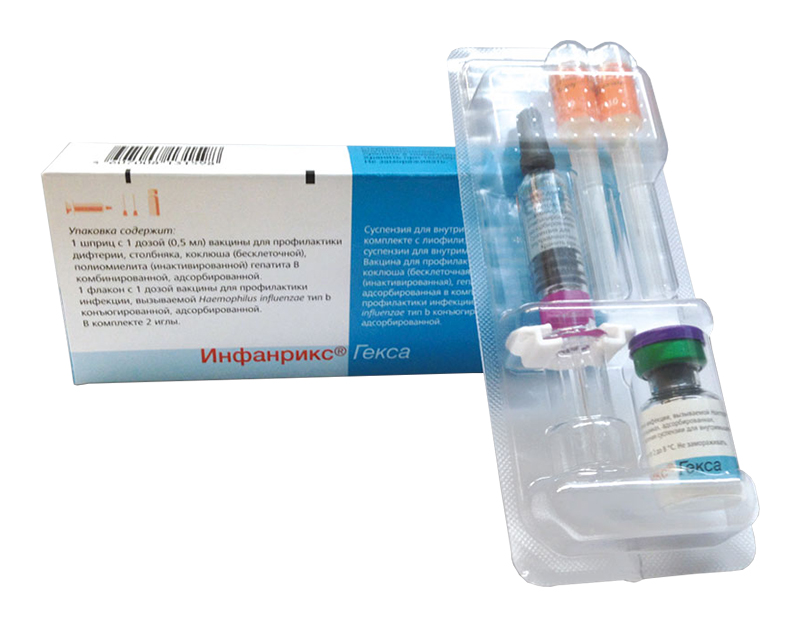
Комплектность
Для аптек
По
1 шприцу с суспензией и по 2 иглы (или без игл) в отдельных пластиковых
контейнерах в комплекте с 1 флаконом с лиофилизатом в блистере из
поливинилхлорида и закрытом пленкой из полиэтилентерефталата. По 1
блистеру вместе с инструкцией по применению в картонной пачке.
Для лечебно-профилактических учреждений
По
10 шприцев с суспензией и по 20 игл (или без игл) в мягкой контурной ячейковой
упаковке в комплекте с 10 флаконами с лиофилизатом и инструкцией
по применению в картонной коробке, снабженной встроенным картонным
разделителем с защитной перфорацией от несанкционированного вскрытия.
Условия отпуска из аптек
Условия хранения
Срок годности
Представленная информация о ценах на препараты не является предложением о продаже или покупке товара.
Информация предназначена исключительно для сравнения цен в стационарных аптеках, осуществляющих деятельность в
соответствии со статьей 55 Федерального закона «Об обращении лекарственных средств» от 12.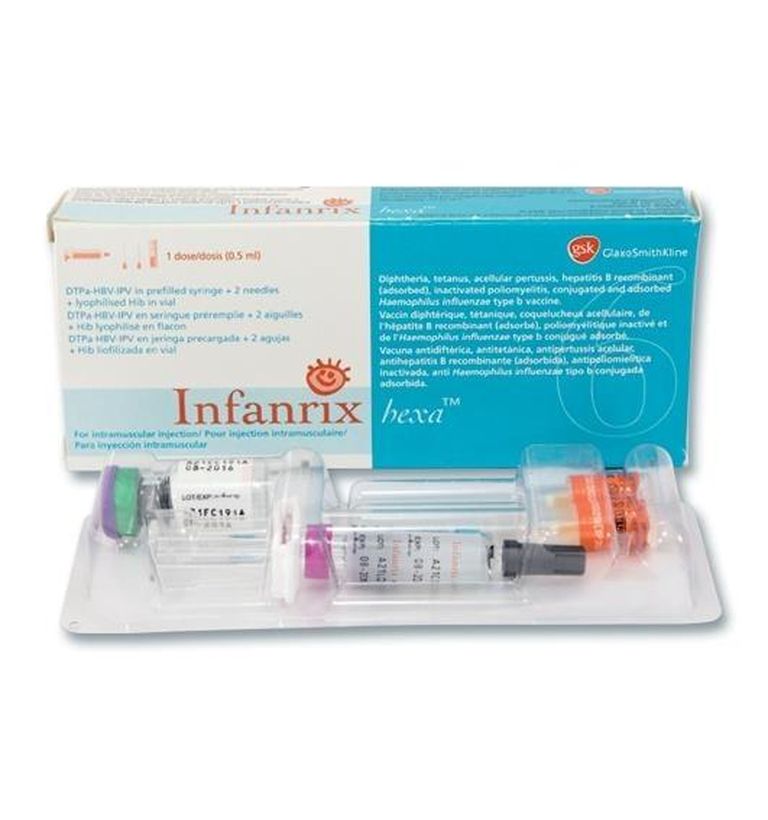 04.2010 № 61-ФЗ.
04.2010 № 61-ФЗ.
Вакцина Инфанрикс ГЕКСА — медицинский центр Бэби Плюс в Одинцово
Вакцина Инфанрикс ГЕКСА
Инфанрикс Гекса® представляет собой адсорбированную ацеллюлярную (то есть бесклеточную) коклюшно-дифтерийно-столбнячную вакцину, инактивированную полиомиелитную вакцину, рекомбинантную вакцину против вируса гепатита В и вакцину для профилактики заболеваний, вызываемых гемофильной палочкой (Haemophilus influenzae тип b).
Вакцина Инфанрикс ГЕКСА (GlaxoSmithKline, Бельгия) — это одна из самых современных комбинированных вакцин, которая применяется для профилактики сразу шести опасных инфекций.
Инфанрикс Гекса® представляет собой адсорбированную ацеллюлярную (то есть бесклеточную) коклюшно-дифтерийно-столбнячную вакцину, инактивированную полиомиелитную вакцину, рекомбинантную вакцину против вируса гепатита В и вакцину для профилактики заболеваний, вызываемых гемофильной палочкой (Haemophilus influenzae тип b).
При создании бесклеточной вакцины с помощью современных технологий в 30 раз удалось снизить количество белковых молекул в составе данной вакцины, что значительно уменьшает количество нежелательных реакций на прививку, без потери ее иммуногенности.
Показания к применению вакцины ИНФАНРИКС ГЕКСА
Вакцина Инфанрикс Гекса применяется у детей для профилактики таких заболеваний, как:
- дифтерия;
- столбняк;
- коклюш;
- полиомиелит;
- гепатит В;
- инвазивной инфекции, вызываемой Haemophilus influenzae тип b (менингит, септицемия, пневмония, эпиглотит и др.).
Кроме этого, Инфанрикс Гекса применяется для вакцинация и ревакцинация детей, которые ранее были иммунизированы несколькими дозами бесклеточной или цельноклеточной коклюшно-дифтерийно-столбнячной вакцины, и рекомбинантной вакцины против гепатита В, при условии продолжающейся вакцинации или ревакцинации от полиомиелита и гепатита В.
Режим дозирования и способ применения.
Рекомендуемое место для введения вакцины Инфанрикс Гекса — это средняя треть передненаружной поверхности бедра. Вакцина вводится глубоко внутримышечно при помощи шприц-дозы, снабженного специальной иглой, минимизирующей болевые ощущения, и предотвращающего повторное использование шприца. Разовая доза при введении составляет 0,5 мл.
Разовая доза при введении составляет 0,5 мл.
Иммунизация проводится в соответствии с национальным календарем профилактических прививок.
Схема вакцинации подбирается индивидуально для каждого ребенка с учетом его особенностей.
Получить консультацию по вопросам вакцинации, а так сделать необходимые профилактические прививки, можно, обратившись в медицинский центр «БЭБИ ПЛЮС», расположенный по адресу: Одинцовский район, п. ВНИИССОК, ул. Михаила Кутузова, д. 5а, 3 этаж.
Телефоны медицинского центра: 8 499 499 95 05 и 8 926 006 50 23
При этом не имеет значения где именно проживает ребенок. Для посещения педиатра и постановки вакцины необходимо на руках иметь прививочный сертификат (или амбулаторную карту), где содержится информация о сделанных ранее профилактических прививках, а при первичной вакцинации — дополнительно: результаты лабораторных исследований ( общий анализ крови, общий анализ мочи) и разрешение от невролога о том, что противопоказаний к вакцинации нет.
Вакцина Пентаксим
Дата публикации: 13.12.2018 17:05:24
Шестивалентная вакцина добавлена в программу «Вакцины для детей»
Миранда Хестер
Contemporary PEDS Journal , Том 37 № 4, Том 37, Выпуск 4 После единогласного голосования 3 Консультативного комитета
по практике иммунизации шестивалентная вакцина с адсорбированными дифтерийно-столбнячными анатоксинами и бесклеточным коклюшем, инактивированным полиовирусом, конъюгатом Haemophilus influenzae типа b (конъюгат менингококкового белка) и гепатитом B (HepB) (рекомбинантная) включена в федеральную программу «Вакцины для детей». .
Согласно выпуску Еженедельного отчета о заболеваемости и смертности Центров по контролю и профилактике заболеваний (CDC) от 7 февраля 2020 г. шестивалентная вакцина, содержащая дифтерийно-столбнячный анатоксин и бесклеточный коклюшный анатоксин (DTaP), адсорбирована, инактивированный полиовирус (ИПВ), конъюгат Haemophilus influenzae типа b (Hib) (конъюгат менингококкового белка) и вирус гепатита В (HepB) (рекомбинантный) – DTaP-IPV-Hib-HepB – включен в федеральную программу «Вакцины для детей». после единогласного голосования Консультативного комитета по практике иммунизации (ACIP). 1
после единогласного голосования Консультативного комитета по практике иммунизации (ACIP). 1
ACIP рассмотрел 6 исследований фазы III, в которых оценивали безопасность и иммуногенность вакцины DTaP-IPV-Hib-HepB, включая 2 исследования не меньшей эффективности, в которых приняли участие более 4200 детей, использующих график вакцинации США 2, 4 и 6 месяцев. Иммунологические ответы оценивали после третьей дозы вакцины. Исследования показали, что в целом измеренные антитела не уступали лицензированным вакцинам сравнения, за исключением 1 антигена коклюша. Однако критерию не меньшей эффективности соответствовали все коклюшные антигены при использовании второй измеренной конечной точки процентной доли, которая соответствовала предварительно определенному ответу на вакцину.
Было обнаружено, что профиль безопасности соответствует лицензированным компонентным вакцинам. Исследователи действительно обнаружили более высокий уровень лихорадки у реципиентов шестивалентной вакцины по сравнению с теми, кто получил пятивалентную вакцину (DTaP-IPV/Hib) (47,1–47,4% против 33,2–34,4% соответственно). Связанные с лихорадкой медицинские явления, такие как фебрильные судороги, возникали с одинаковой частотой в обеих группах.
Связанные с лихорадкой медицинские явления, такие как фебрильные судороги, возникали с одинаковой частотой в обеих группах.
Руководство по применению
Коклюш
Вакцина показана для использования в возрасте 2, 4 и 6 месяцев. Для профилактики дифтерии, столбняка и коклюша шестивалентную вакцину можно использовать для первых 3 доз, когда будет вводиться АКДС, но ее не следует использовать для повторных прививок в возрасте от 15 до 18 месяцев и от 4 до 6 лет. . Если шестивалентная вакцина вводится для любой из ревакцинаций, нет необходимости вводить дозу другой вакцины с АКДС, если соблюдены надлежащие интервалы между предыдущими дозами.
В случае ускоренного графика для обеспечения защиты от коклюша, серию можно начинать у младенцев в возрасте 6 недель, при этом вторую и третью дозы DTaP вводят не ранее, чем через 4 недели после предыдущей дозы. Поскольку рекомендуемый минимальный возраст для третьей дозы шестивалентной вакцины составляет 24 недели, что является минимальным возрастом для серии вакцин против гепатита В, шестивалентная вакцина не рекомендуется для третьей дозы при ускоренном графике.
Полиомиелит
Комбинированную вакцину можно использовать для первых 3 доз серии ИПВ, но она не показана для четвертой дозы. В случае, если вакцина случайно введена в качестве бустерной дозы, повторная доза другой вакцины с ИПВ не требуется, при условии соблюдения надлежащего интервала между предыдущими дозами.
Haemophilus influenzae тип b
При иммунизации против Hib для завершения первичной вакцинации потребуется 3 дозы вакцины, содержащей конъюгат Hib, если вакцина DTaP-IPV-Hib-HepB вводится для любой дозы. После завершения первичной серии шестивалентную вакцину не следует использовать для бустерных доз. При сохранении надлежащего интервала между предыдущими дозами нет необходимости вводить повторную дозу Hib-содержащей вакцины, если доза DTaP-IPV-Hib-HepB была случайно введена в качестве бустерной дозы.
Гепатит B
Вакцина не лицензирована для дозы при рождении. Его можно использовать для доз, вводимых в возрасте 6 недель и старше младенцам, матери которых являются отрицательными по поверхностному антигену гепатита В (HBsAg). Его также можно назначать младенцам в возрасте 6 недель и старше от матерей, у которых HBsAg-положительный или неизвестный HBsAg-статус. Если третья доза вакцины DTaP-IPV-Hib-HepB вводится ребенку до достижения им возраста 24 недель или старше, дополнительную дозу вакцины против гепатита B следует ввести, когда ребенку исполнится не менее 24 недель, с надлежащими интервалами для предыдущих вакцин. дозы.
Его также можно назначать младенцам в возрасте 6 недель и старше от матерей, у которых HBsAg-положительный или неизвестный HBsAg-статус. Если третья доза вакцины DTaP-IPV-Hib-HepB вводится ребенку до достижения им возраста 24 недель или старше, дополнительную дозу вакцины против гепатита B следует ввести, когда ребенку исполнится не менее 24 недель, с надлежащими интервалами для предыдущих вакцин. дозы.
Вакцина DTaP-IPV-Hib-HepB для детей, находящихся на контрольном календаре, может использоваться у детей в возрасте до 5 лет. Дозы не следует вводить с интервалами меньше, чем минимальные интервалы, указанные в Общем руководстве по передовой практике для иммунизации (см. Таблицу 3-1 в разделе «Сроки и интервалы введения иммунобиологических препаратов»).
Ссылки:
1. Oliver SE, Moore КЛ. Лицензирование дифтерийно-столбнячного анатоксина и бесклеточного коклюша, инактивированного полиовируса, Haemophilus influenzae конъюгат типа b и вакцина против гепатита b, а также руководство по применению у детей грудного возраста. MMWR Morb Mortal Wkly Rep . 2020;69(5):136-139.
MMWR Morb Mortal Wkly Rep . 2020;69(5):136-139.
Скачать Выпуск: Том 37 № 4
| ||||||||||

 пять детей в ЕС умерли в течение 24 часов после вакцинации. Четыре сообщения о необъяснимых смертях были получены из Германии и одно из Австрии (1). На сегодняшний день в Германии около 1,6 миллиона детей были привиты шестивалентными вакцинами. Это приводит к одному сообщению о необъяснимой смерти на 400 000 детей. Двое из умерших детей были в возрасте 4 или 5 месяцев, двое — в возрасте 17 месяцев и один — в возрасте 23 месяцев. Все были признаны здоровыми. Подозрения о том, что факторы риска, такие как семейный анамнез судорог, следует рассматривать как спусковой механизм для летальных исходов или что синдром внезапной детской смерти (СВДС) может иметь место, не подтвердились (1,2). СВДС обычно возникает в возрасте около 3 месяцев. В 90% случаев СВДС возникает в возрасте до 6 месяцев (3).
пять детей в ЕС умерли в течение 24 часов после вакцинации. Четыре сообщения о необъяснимых смертях были получены из Германии и одно из Австрии (1). На сегодняшний день в Германии около 1,6 миллиона детей были привиты шестивалентными вакцинами. Это приводит к одному сообщению о необъяснимой смерти на 400 000 детей. Двое из умерших детей были в возрасте 4 или 5 месяцев, двое — в возрасте 17 месяцев и один — в возрасте 23 месяцев. Все были признаны здоровыми. Подозрения о том, что факторы риска, такие как семейный анамнез судорог, следует рассматривать как спусковой механизм для летальных исходов или что синдром внезапной детской смерти (СВДС) может иметь место, не подтвердились (1,2). СВДС обычно возникает в возрасте около 3 месяцев. В 90% случаев СВДС возникает в возрасте до 6 месяцев (3).
