Прививка | ||||
Дифтерии Дифтерия: при инфекции в зеве образуются пленки, закрывающие дыхательные пути, и человек может задохнуться. Подробнее | Каждые 10 лет | Каждые 10 лет | ||
Столбняка Столбняк: токсин поражает нервную систему, приводя к сильным судорогам, иногда смерти. Подробнее | Каждые 10 лет | Каждые 10 лет | ||
Кори1 Корь легко передается от человека к человеку. Опасна осложнениями — отит, пневмония, воспаление головного мозга. Подробнее | До 35 лет включительно | До 35 лет включительно | Взрослые от 36 до 55 лет, относящие к группам риска | |
Краснухи Краснуха: основная опасность — заражение от детей беременных женщин и рождение у них детей с серьезными дефектами. Подробнее | Женщины до 25 лет, не болевшие и не привитые ранее | Женщины до 25 лет, не болевшие и не привитые ранее | ||
Гепатита В Гепатит В может приводить к развитию цирроза и рака печени. Вирус может передаваться во время родов, через кровь, через зараженные предметы. Подробнее | Взрослые от 18 до 55 лет, не привитые ранее; контактные лица из очагов заболевания, не болевшие, не привитые ранее и не имеющие сведений о профилактических прививках против гепатита В | Взрослые от 18 до 55 лет, не привитые ранее; контактные лица из очагов заболевания, не болевшие, не привитые ранее и не имеющие сведений о профилактических прививках против гепатита В | ||
Гриппа2 Грипп быстро распространяется от человека к человеку, может вызвать лихорадку, пневмонию, опасен осложнениями. Подробнее | Ежегодно группы риска1 | Ежегодно группы риска1 | ||
Пневмококковой инфекции3,4 Пневмококк — одна из причин пневмоний, гнойного менингита, отита. Менингит может привести к смертельному исходу. Подробнее | В соответствии с инструкцией по применению препаратов | В соответствии с инструкцией по применению препаратов | ||
Гепатита А3,5 Гепатит А передается через воду или пищу. Подробнее | В соответствии с инструкцией по применению препаратов | В соответствии с инструкцией по применению препаратов | ||
Менингококковой инфекции3,6 Менингококк — одна из частых причин менингита или сепсиса. Болезнь может унести жизнь ребенка за 24 часа. Подробнее | В соответствии с инструкцией по применению препаратов | В соответствии с инструкцией по применению препаратов | ||
Бешенства3,7 Бешенство — 100% cмертельное инфекционное заболевание, передается со слюной при укусе больного животного. Вакцинация должна проводиться сразу после укуса животного. Подробнее | В соответствии с инструкцией по применению препаратов | В соответствии с инструкцией по применению препаратов | ||
Бруцеллеза3,8 Бруцеллез развивается при употреблении в пищу сырых молочных продуктов и мяса от зараженных животных и приводит к множественному поражению органов. Подробнее | В соответствии с инструкцией по применению препаратов | В соответствии с инструкцией по применению препаратов | ||
Брюшного тифа3,9 Брюшной тиф развивается при употреблении продуктов, контактировавших с зараженной водой (молоко, салаты, овощи). Подробнее | В соответствии с инструкцией по применению препаратов | В соответствии с инструкцией по применению препаратов | ||
Ветряной оспы3,10 Ветряная оспа проявляется в виде зудящей сыпи (у детей) или болезненного опоясывающего герпеса (у взрослых). Подробнее | В соответствии с инструкцией по применению препаратов | В соответствии с инструкцией по применению препаратов | ||
Желтой лихорадки3,11 Желтая лихорадка — острая вирусная инфекция тропических стран с поражением внутренних органов, передающееся через укусы комаров. Подробнее | В соответствии с инструкцией по применению препаратов | В соответствии с инструкцией по применению препаратов | ||
Клещевого вирусного энцефалита3,12 Клещевой энцефалит передается при укусе инфицированного клеща, развивается менингит и/или энцефалит. Подробнее | В соответствии с инструкцией по применению препаратов | В соответствии с инструкцией по применению препаратов | ||
Лептоспироза3,13 Лептоспироз — острая инфекция с преимущественным поражением почек, печени и нервной системы. Подробнее | В соответствии с инструкцией по применению препаратов | В соответствии с инструкцией по применению препаратов | ||
Лихорадки Ку3,14 Лихорадка Ку: инфекция наблюдается на некоторых территориях, наиболее часто поражаются легкие. Подробнее | В соответствии с инструкцией по применению препаратов | В соответствии с инструкцией по применению препаратов | ||
Полиомиелита3,15 Полиомиелит может навсегда парализовать руки или ноги или даже дыхательные мышцы. Подробнее | В соответствии с инструкцией по применению препаратов | В соответствии с инструкцией по применению препаратов | ||
Сибирской язвы3,16 Сибирская язва — молниеносная особо опасная инфекция, возбудитель которой чаще всего проникает через поврежденную кожу. Подробнее | В соответствии с инструкцией по применению препаратов | В соответствии с инструкцией по применению препаратов | ||
Туляремии3,17 Туляремия — острое инфекционное заболевание. Заражение происходит при контакте с больными животными, через инфицированную воду и продукты, укусе клещей, комаров, блох. Подробнее | В соответствии с инструкцией по применению препаратов | В соответствии с инструкцией по применению препаратов | ||
Холеры3,18 Холера — острая кишечная инфекция с развитием сильной диареи и рвоты, что может привести к развитию обезвоживания, шока и смерти. Подробнее | В соответствии с инструкцией по применению препаратов | В соответствии с инструкцией по применению препаратов | ||
Чумы3,19 Чума — острая особо опасная инфекция, передающаяся от зараженных животных человеку через блох. Ранее смертность от этого заболевания достигала 99%. Подробнее | В соответствии с инструкцией по применению препаратов | В соответствии с инструкцией по применению препаратов | ||
Шигеллезов3,20 Шигеллез — острая кишечная инфекция, передается через воду, пищу и при контактах, проявляется выраженной болью в животе и диареей. Подробнее | В соответствии с инструкцией по применению препаратов | В соответствии с инструкцией по применению препаратов | ||
Эпидемического паротита3,21 Эпидемический паротит — сильный отек околоушных желез. Вирус у мальчиков может вызвать воспаление тканей яичка и дальнейшее бесплодие. Подробнее | В соответствии с инструкцией по применению препаратов | В соответствии с инструкцией по применению препаратов |
Обзор вакцины БЦЖ и других подходов к ликвидации туберкулеза
Обзор
. 2021 3 августа; 17 (8): 2454-2470.
дои: 10.1080/21645515.2021.1885280.
Epub 2021 26 марта.
Томас Чо
1
, Кристофер Хачадурян
1
, Хью Нгуен
1
, Яш Дара
1
, Шуна Юнг
1
, Вишванат Венкетараман
1
2
Принадлежности
- 1 Тихоокеанский колледж остеопатической медицины, Западный университет медицинских наук, Помона, Калифорния, США.

- 2 Высший колледж биомедицинских наук, Западный университет медицинских наук, Помона, Калифорния, США.
PMID:
33769193
PMCID:
PMC8475575
DOI:
10.1080/21645515.2021.1885280
Бесплатная статья ЧВК
Обзор
Томас Чо и соавт.
Hum Вакцина Иммунотер.
.
Бесплатная статья ЧВК
. 2021 3 августа; 17 (8): 2454-2470.
дои: 10.1080/21645515.2021.1885280.
Epub 2021 26 марта.
Авторы
Томас Чо
1
, Кристофер Хачадурян
1
, Хью Нгуен
1
, Яш Дара
1
, Шуна Юнг
1
, Вишванат Венкетараман
1
2
Принадлежности
- 1 Тихоокеанский колледж остеопатической медицины, Западный университет медицинских наук, Помона, Калифорния, США.
- 2 Высший колледж биомедицинских наук, Западный университет медицинских наук, Помона, Калифорния, США.

PMID:
33769193
PMCID:
PMC8475575
DOI:
10.1080/21645515.2021.1885280
Абстрактный
Несмотря на энергичные усилия по искоренению, туберкулез (ТБ) остается глобальным бременем для здравоохранения, которое непропорционально затрагивает более бедные и менее развитые страны. Единственная вакцина, одобренная для лечения туберкулеза, вакцина Bacillus Кальметта и Герена (БЦЖ) остается спорной, поскольку ее заявленная эффективность составляет от 0 до 80%. Тем не менее, были сделаны захватывающие открытия о механизме действия вакцины БЦЖ, которые позволяют предположить, что сегодня она играет важную роль в календаре иммунизации. Мы рассматриваем последние данные, свидетельствующие о том, что вакцина обеспечивает защиту как от туберкулезных, так и от нетуберкулезных возбудителей через недавно открытую иммунную систему, называемую обученным иммунитетом. Эффективность БЦЖ, по-видимому, также связана с ее влиянием на гранулоциты на уровне эпигенетических и гемопоэтических стволовых клеток, что мы подробно обсуждаем в этой статье. Мы также пишем о том, как разные штаммы вакцины БЦЖ вызывают разные иммунные реакции, предполагая, что одни штаммы БЦЖ более иммуногенны, чем другие. Наконец, в нашем обзоре рассматривается, как текущая вакцина переформулируется, чтобы сделать ее более эффективной, и отслеживается разработка вакцин против туберкулеза следующего поколения.
Мы рассматриваем последние данные, свидетельствующие о том, что вакцина обеспечивает защиту как от туберкулезных, так и от нетуберкулезных возбудителей через недавно открытую иммунную систему, называемую обученным иммунитетом. Эффективность БЦЖ, по-видимому, также связана с ее влиянием на гранулоциты на уровне эпигенетических и гемопоэтических стволовых клеток, что мы подробно обсуждаем в этой статье. Мы также пишем о том, как разные штаммы вакцины БЦЖ вызывают разные иммунные реакции, предполагая, что одни штаммы БЦЖ более иммуногенны, чем другие. Наконец, в нашем обзоре рассматривается, как текущая вакцина переформулируется, чтобы сделать ее более эффективной, и отслеживается разработка вакцин против туберкулеза следующего поколения.
Ключевые слова:
БЦЖ; противотуберкулезные вакцины; Тренированный иммунитет; Туберкулез.
Похожие статьи
Защита от туберкулеза с помощью вакцинации Бациллой Кальметта-Герена (БЦЖ): историческая перспектива.

Setiabudiawan TP, Reurink RK, Hill PC, Netea MG, van Crevel R, Koeken VACM.
Setiabudiawan TP, et al.
Мед (Нью-Йорк). 2022 14 января; 3(1):6-24. doi: 10.1016/j.medj.2021.11.006. Epub 2021 31 декабря.
Мед (Нью-Йорк). 2022.PMID: 355
Обзор.
Стратегии вакцинации БЦЖ против туберкулеза: обновления и перспективы.
Цюй М., Чжоу С., Ли Х.
Ку М и др.
Hum Вакцина Иммунотер. 2021 2 декабря; 17 (12): 5284-5295. дои: 10.1080/21645515.2021.2007711. Epub 2021 2 декабря.
Hum Вакцина Иммунотер. 2021.PMID: 34856853
Обзор.
Диетический пиридоксин контролирует эффективность витамин B6-ауксотрофной противотуберкулезной вакцины бациллы Кальметта-Герена ΔureC::hly Δpdx1 у мышей.
Генгенбахер М.
 , Фогельзанг А., Шурер С., Лазар Д., Кайзер П., Кауфманн С.Х.
, Фогельзанг А., Шурер С., Лазар Д., Кайзер П., Кауфманн С.Х.
Генгенбахер М. и соавт.
мБио. 3 июня 2014 г .; 5 (3): e01262-14. doi: 10.1128/mBio.01262-14.
мБио. 2014.PMID: 24895310
Бесплатная статья ЧВК.MTBVAC, живая противотуберкулезная вакцина, должна начать испытания эффективности через 100 лет после БЦЖ.
Мартин С., Маринова Д., Агило Н., Гонсало-Асенсио Х.
Мартин С. и др.
вакцина. 2021 8 декабря; 39(50):7277-7285. doi: 10.1016/j.vaccine.2021.06.049. Epub 2021 6 июля.
вакцина. 2021.PMID: 34238608
Клиническое испытание.
Будущий путь к разработке противотуберкулезной вакцины: усиление БЦЖ или переобучение с помощью новой субъединичной вакцины.
Гупта Н., Гарг С., Веди С., Кунимото Д.
 Ю., Кумар Р., Агравал Б.
Ю., Кумар Р., Агравал Б.
Гупта Н. и др.
Фронт Иммунол. 2018 16 окт;9:2371. doi: 10.3389/fimmu.2018.02371. Электронная коллекция 2018.
Фронт Иммунол. 2018.PMID: 30386336
Бесплатная статья ЧВК.
Посмотреть все похожие статьи
Цитируется
Индуцированный БЦЖ тренированный иммунитет усиливает бесклеточный ответ на вакцинацию против коклюша в исследовательском рандомизированном клиническом исследовании.
Гиллард Дж., Блок Б.А., Гарза Д.Р., Венкатасубраманян П.Б., Симонетти Э., Элевельд М.Дж., Берберс Г.А.М., ван Гагельдонк П.Г.М., Йостен И., де Грут Р., де Бри Л.С. М.Г., Диаватопулос Д.А.
Гиллард Дж. и др.
Вакцины NPJ. 2022 17 февраля; 7 (1): 21. doi: 10.1038/s41541-022-00438-4.
Вакцины NPJ. 2022.PMID: 35177621
Бесплатная статья ЧВК.
Типы публикаций
термины MeSH
вещества
Грантовая поддержка
- R15 HL143545/HL/NHLBI NIH HHS/США
О защите вакциной БЦЖ от COVID-19: обзор
1. Мизумото К., Кагая К., Заребски А., Чоуэлл Г. Оценка бессимптомной доли коронавирусной болезни 2019 г.Случаи (COVID-19) на борту круизного лайнера Diamond Princess, Йокогама, Япония, 2020 г. Евронадзор. 2020;25(10):2000180. doi: 10.2807/1560-7917.ES.2020.25.10.2000180. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Мизумото К., Кагая К., Заребски А., Чоуэлл Г. Оценка бессимптомной доли коронавирусной болезни 2019 г.Случаи (COVID-19) на борту круизного лайнера Diamond Princess, Йокогама, Япония, 2020 г. Евронадзор. 2020;25(10):2000180. doi: 10.2807/1560-7917.ES.2020.25.10.2000180. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
2. Bentivegna E, Luciani M, Spuntarelli V, Speranza M, Guerritore L, Sentimentale A, et al. Крайне тяжелый случай пневмонии COVID-19 выздоровел, несмотря на плохие прогностические показатели: дидактический отчет. SN Compr Clin Med. 2020;2(8):1204–1207. doi: 10.1007/s42399-020-00383-0. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
3. Dong Y, Mo X, Hu Y, Qi X, Jiang F, Jiang Z, Tong S. Эпидемиология COVID-19 среди детей в Китае. Педиатрия. 2020;145(6):e20200702. doi: 10.1542/peds.2020-0702. [PubMed] [CrossRef] [Google Scholar]
4. Kuchar E, Załęski A, Wronowski M, Krankowska D, Podsiadły E, Brodaczewska K, et al. Дети реже заражались SARS-CoV-2, чем взрослые, во время пандемии COVID-19 2020 года в Варшаве, Польша. Eur J Clin Microbiol Infect Dis. 2020: 1–7. 10.1007/с10096-020-04038-9. [Бесплатная статья PMC] [PubMed]
Eur J Clin Microbiol Infect Dis. 2020: 1–7. 10.1007/с10096-020-04038-9. [Бесплатная статья PMC] [PubMed]
5. Бродин П. Почему COVID-19 так легко протекает у детей? Акта Педиатр. 2020;109(6):1082–1083. doi: 10.1111/apa.15271. [PubMed] [CrossRef] [Google Scholar]
6. Bentivegna E, Sentimentale A, Luciani M, Speranza ML, Guerritore L, Martelletti P. Новая сероконверсия IgM и положительный тест RT-PCR после контакта с вирусом у переболевших COVID- 19 пациент. J Med Virol. 2021;93(1):97–98. doi: 10.1002/jmv.26160. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
7. Luciani M, Bentivegna E, Spuntarelli V, Lamberti PA, Cacioli G, Del Porto F, et al. Рецидивирующая пневмония COVID-19 на фоне химиотерапии: следствие ослабленного иммунитета? J Med Virol. 2020; 93: 1882–1884. doi: 10.1002/jmv.26701. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
8. Pai M, Behr MA, Dowdy D, Dheda K, Divangahi M, Boehme CC, Ginsberg A, Swaminathan S, Spigelman M, Getahun H, Menzies D, Равильоне М. Туберкулез. Праймеры Nat Rev Dis. 2016;2:16076. doi: 10.1038/nrdp.2016.76. [PubMed] [CrossRef] [Академия Google]
Туберкулез. Праймеры Nat Rev Dis. 2016;2:16076. doi: 10.1038/nrdp.2016.76. [PubMed] [CrossRef] [Академия Google]
9. Van Etten E, Stoffels K, Gysemans C, Mathieu C, Overbergh L. Регуляция гомеостаза витамина D: последствия для иммунной системы. Nutr Rev. 2008; 66 (suppl_2): S125–SS34. doi: 10.1111/j.1753-4887.2008.00096.x. [PubMed] [CrossRef] [Google Scholar]
10. Lalor MK, Floyd S, Gorak-Stolinska P, Weir RE, Blitz R, Branson K, Fine PE, Dockrell HM. Вакцинация БЦЖ: роль витамина D? ПЛОС Один. 2011;6(1):e16709. doi: 10.1371/journal.pone.0016709. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
11. Moorlag S, Arts R, Van Crevel R, Netea M. Неспецифические эффекты вакцины БЦЖ на вирусные инфекции. Клин Микробиол Инфект. 2019;25(12):1473–1478. doi: 10.1016/j.cmi.2019.04.020. [PubMed] [CrossRef] [Google Scholar]
12. Чумаков К., Бенн К.С., Ааби П., Коттилил С., Галло Р. Могут ли существующие живые вакцины предотвратить COVID-19? Наука. 2020;368(6496):1187–1188. doi: 10.1126/science.abc4262. [PubMed] [CrossRef] [Google Scholar]
doi: 10.1126/science.abc4262. [PubMed] [CrossRef] [Google Scholar]
13. Escobar LE, Molina-Cruz A, Barillas-Mury C. Защита вакциной БЦЖ от тяжелой коронавирусной болезни 2019(COVID-19) Proc Natl Acad Sci. 2020;117(30):17720–17726. doi: 10.1101/2020.05.05.20091975. [Статья бесплатно PMC] [PubMed] [CrossRef] [Google Scholar]
14. Arlehamn CSL, Sette A, Peters B. Отсутствие доказательств защиты вакцины БЦЖ от тяжелой формы COVID-19. Proc Natl Acad Sci. 2020;117(41):25203–25204. doi: 10.1073/pnas.2016733117. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
15. Hamiel U, Kozer E, Youngster I. Показатели SARS-CoV-2 у вакцинированных БЦЖ и невакцинированных молодых людей. Джама. 2020;323(22):2340–2341. дои: 10.1001/jama.2020.8189. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
16. Матюрин К.С., Мартенс Г.В., Корнфельд Х., Валлийский Р.М. Гетерологичный иммунитет, опосредованный Т-клетками CD4, между микобактериями и поксвирусами. Дж Вирол. 2009;83(8):3528–3539. doi: 10.1128/ОВИ.02393-08. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
2009;83(8):3528–3539. doi: 10.1128/ОВИ.02393-08. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
17. Kleinnijenhuis J, Quintin J, Preijers F, Joosten LA, Ifrim DC, Saeed S, et al. Бацилла Кальметта-Герена индуцирует NOD2-зависимую неспецифическую защиту от повторного заражения путем эпигенетического перепрограммирования моноцитов. Proc Natl Acad Sci. 2012;109(43): 17537–17542. doi: 10.1073/pnas.1202870109. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
18. Netea MG, Joosten LA, Latz E, Mills KH, Natoli G, Stunnenberg HG, et al. Тренированный иммунитет: программа врожденной иммунной памяти в норме и при болезни. Наука. 2016;352(6284):aaf1098. doi: 10.1126/science.aaf1098. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
19. Mantovani A, Netea MG. Тренировал врожденный иммунитет, эпигенетику и Covid-19. N Engl J Med. 2020;383(11):1078–1080. doi: 10.1056/NEJMcibr2011679. [PubMed] [CrossRef] [Google Scholar]
20. Trunz BB, Fine P, Dye C. Влияние вакцинации БЦЖ на детский туберкулезный менингит и милиарный туберкулез во всем мире: метаанализ и оценка экономической эффективности. Ланцет. 2006;367(9517):1173–1180. doi: 10.1016/S0140-6736(06)68507-3. [PubMed] [CrossRef] [Google Scholar]
Влияние вакцинации БЦЖ на детский туберкулезный менингит и милиарный туберкулез во всем мире: метаанализ и оценка экономической эффективности. Ланцет. 2006;367(9517):1173–1180. doi: 10.1016/S0140-6736(06)68507-3. [PubMed] [CrossRef] [Google Scholar]
21. Roy A, Eisenhut M, Harris R, Rodrigues L, Sridhar S, Habermann S, et al. Эффект вакцинации БЦЖ против инфекции Mycobacterium tuberculosis у детей: систематический обзор и метаанализ. бмж. 2014;349:g4643. doi: 10.1136/bmj.g4643. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
22. Luciani M, Bentivegna E, Spuntarelli V, Lamberti PA, Guerritore L, Chiappino D, et al. Коинфекция туберкулезной пневмонии и COVID-19 у пациента, вакцинированного бациллой Кальметта-Герена (БЦЖ): история болезни. SN Compr Clin Med. 2020;2(11):2419–2422. doi: 10.1007/s42399-020-00601-9. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
23. Aaby P, Roth A, Ravn H, Napirna BM, Rodrigues A, Lisse IM, Stensballe L, Diness BR, Lausch KR, Lund N, Biering -Соренсен С.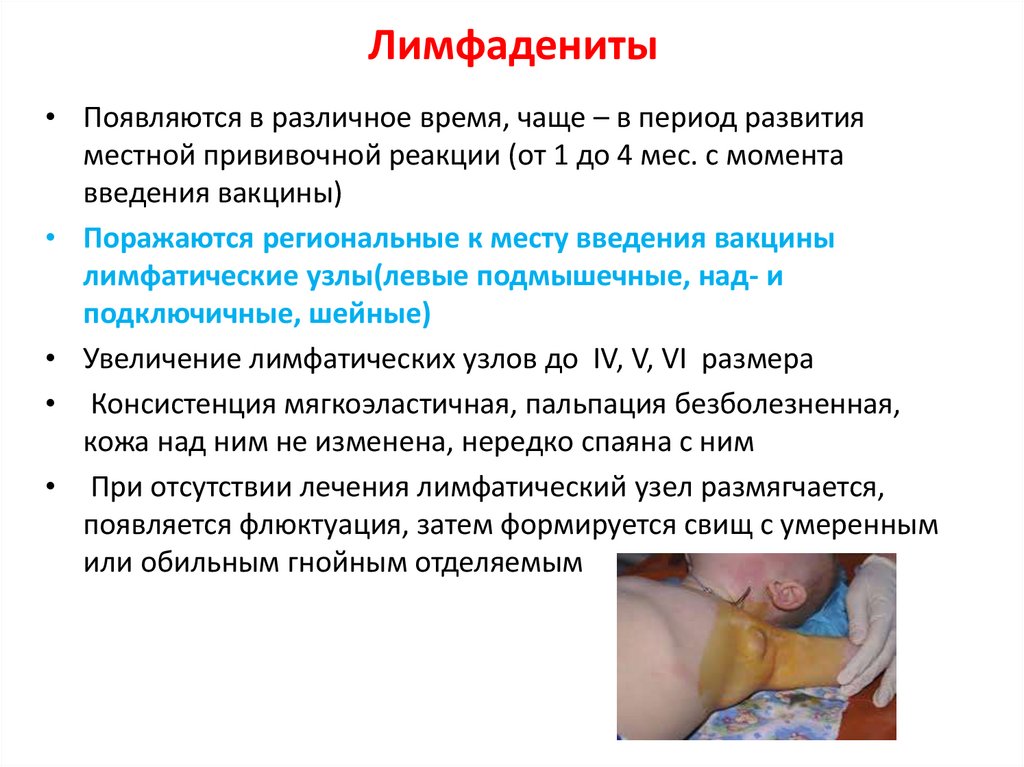 , Уиттл Х., Бенн К.С. Рандомизированное исследование вакцинации БЦЖ при рождении детей с низкой массой тела при рождении: положительный неспецифический эффект в неонатальном периоде? J заразить дис. 2011;204(2):245–252. дои: 10.1093/infdis/jir240. [PubMed] [CrossRef] [Google Scholar]
, Уиттл Х., Бенн К.С. Рандомизированное исследование вакцинации БЦЖ при рождении детей с низкой массой тела при рождении: положительный неспецифический эффект в неонатальном периоде? J заразить дис. 2011;204(2):245–252. дои: 10.1093/infdis/jir240. [PubMed] [CrossRef] [Google Scholar]
24. Wardhana DE, Sultana A, Mandang V, Jim E. Эффективность прививок Bacillus Calmette-Guerin для профилактики острой инфекции верхних дыхательных путей у пожилых людей. Акта Мед Индонес. 2011;43(3):185–190. [PubMed] [Google Scholar]
25. Leentjens J, Kox M, Stokman R, Gerretsen J, Diavatopoulos DA, van Crevel R, Rimmelzwaan GF, Pickkers P, Netea MG. Вакцинация БЦЖ повышает иммуногенность последующей вакцинации против гриппа у здоровых добровольцев: рандомизированное плацебо-контролируемое пилотное исследование. J заразить дис. 2015;212(12):1930–1938. doi: 10.1093/infdis/jiv332. [PubMed] [CrossRef] [Google Scholar]
26. Arts RJ, Moorlag SJ, Novakovic B, Li Y, Wang S-Y, Oosting M, et al. Вакцинация БЦЖ защищает человека от экспериментальной вирусной инфекции за счет индукции цитокинов, связанных с тренированным иммунитетом. Клеточный микроб-хозяин. 2018;23(1):89–100. е5. doi: 10.1016/j.chom.2017.12.010. [PubMed] [CrossRef] [Google Scholar]
Вакцинация БЦЖ защищает человека от экспериментальной вирусной инфекции за счет индукции цитокинов, связанных с тренированным иммунитетом. Клеточный микроб-хозяин. 2018;23(1):89–100. е5. doi: 10.1016/j.chom.2017.12.010. [PubMed] [CrossRef] [Google Scholar]
27. Usher NT, Chang S, Howard RS, Martinez A, Harrison LH, Santosham M, et al. Ассоциация вакцинации БЦЖ в детстве с последующим диагнозом рака: 60-летнее наблюдение за клиническим испытанием. JAMA Сеть открыта. 2019;2(9):e1912014-e. doi: 10.1001/jamanetworkopen.2019.12014. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
28. Guallar-Garrido S, Julián E. Bacillus Calmette-Guérin (BCG) терапия рака мочевого пузыря: обновление. ImmunoTargets Ther. 2020; 9:1–11. doi: 10.2147/ITT.S202006. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
29. Kühtreiber WM, Faustman DL. БЦЖ-терапия при сахарном диабете 1 типа: восстановление сбалансированного иммунитета и обмена веществ. Тенденции Эндокринол Метаб. 2019;30(2):80–92. doi: 10.1016/j.tem.2018.11.006. [PubMed] [CrossRef] [Google Scholar]
2019;30(2):80–92. doi: 10.1016/j.tem.2018.11.006. [PubMed] [CrossRef] [Google Scholar]
30. Sudre CH, Lee K, Lochlainn MN, Varsavsky T, Murray B, Graham MS, et al. Кластеры симптомов в Covid19: потенциальный инструмент клинического прогнозирования из приложения для изучения симптомов COVID. MedRxiv. 2020. 10.1101/2020.06.12.20129056. [Статья бесплатно PMC] [PubMed]
31. Бенн К.С., Фискер А.Б., Уиттл Х.К., Ааби П. Ревакцинация живыми аттенуированными вакцинами дает дополнительные благоприятные неспецифические эффекты на общую выживаемость: обзор. ЭБиоМедицина. 2016;10:312–317. doi: 10.1016/j.ebiom.2016.07.016. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
32. Biot C, Rentsch CA, Gsponer JR, Birkhäuser FD, Jusforgues-Saklani H, Lemaître F, et al. Существующие ранее БЦЖ-специфические Т-клетки улучшают внутрипузырную иммунотерапию рака мочевого пузыря. Sci Transl Med. 2012;4(137):137ra72-ra72. doi: 10.1126/scitranslmed.3003586. [PubMed] [CrossRef] [Google Scholar]
33. Организация WH. ВОЗ. Глобальный отчет Всемирной организации здравоохранения по туберкулезу. Всемирная организация здравоохранения; 2017.
Организация WH. ВОЗ. Глобальный отчет Всемирной организации здравоохранения по туберкулезу. Всемирная организация здравоохранения; 2017.
34. Немес Э., Гельденхейс Х., Розот В., Рутковски К.Т., Ратанджи Ф., Билек Н., Мабве С., Махете Л., Эразмус М., Тофи А., Муленга Х., Ханеком В.А., Селф С.Г., Беккер Л.Г., Райалл Р. , Гурунатан С., ДиазГранадос С., Андерсен П., Кроманн И., Эванс Т., Эллис Р.Д., Лэндри Б., Хоки Д.А., Хопкинс Р., Гинзберг А.М., Скриба Т.Дж., Хазерилл М., C-040-404 Исследовательская группа Профилактика инфекции M.tuberculosis с h5: вакцина IC31 или ревакцинация БЦЖ. N Engl J Med. 2018;379(2): 138–149. doi: 10.1056/NEJMoa1714021. [Статья PMC бесплатно] [PubMed] [CrossRef] [Google Scholar]
35. Кристенсен И., Файн П., Ааби П., Дженсен Х. Обычные прививки и выживание детей: последующее исследование в Гвинее-Бисау, Западная Африка. Комментарий: неожиданный вывод, который нуждается в подтверждении или отклонении. бмж. 2000;321(7274):1435–1438. doi: 10.1136/bmj.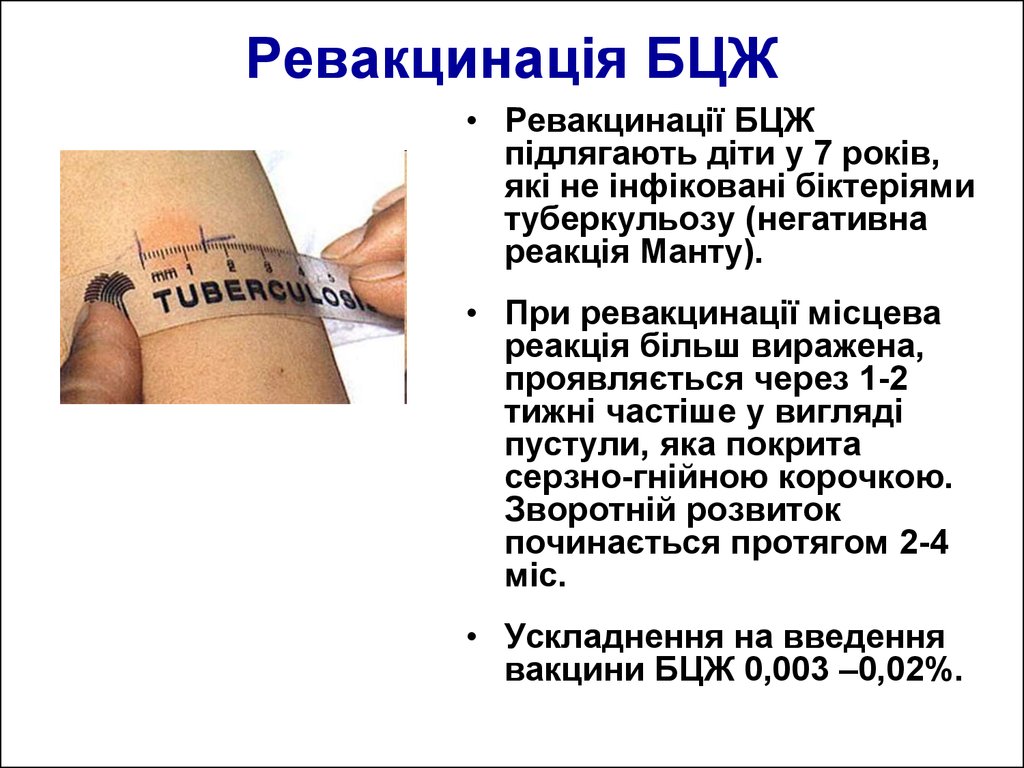 321.7274.1435. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
321.7274.1435. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
36. Roth AE, Benn CS, Ravn H, Rodrigues A, Lisse IM, Yazdanbakhsh M, et al. Влияние ревакцинации БЦЖ в раннем детстве на смертность: рандомизированное исследование в Гвинее-Бисау. бмж. 2010;340:c671. doi: 10.1136/bmj.c671. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
37. Дорадо И., Риос М., Перейра С., Кунья С., Ичихара М., Гоес Дж., Родригес Л.С., Бирренбах А.Л., Баррето М.Л. Частота побочных реакций на первую и вторую дозы вакцины БЦЖ: результаты крупного клинического исследования среди бразильских школьников. Int J Tuberc Lung Dis. 2003;7(4):399–402. [PubMed] [Google Scholar]
38. Giamarellos-Bourboulis EJ, Tsilika M, Moorlag S, Antonakos N, Kotsaki A, Domínguez-Andrés J, et al. ACTIVATE: рандомизированное клиническое исследование вакцинации БЦЖ против инфекции у пожилых людей. Клетка. 2020;183(2):315–23. e9. doi: 10.1016/j.cell.2020.08.051. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
39. Wickramasinghe D, Wickramasinghe N, Kamburugamuwa S A, Arambepola C, Samarasekera DN. Корреляция между иммунитетом от БЦЖ и заболеваемостью и смертностью от COVID-19. Тропические болезни, туристическая медицина и вакцины. 2020;6. 10.1186/с40794-020-00117-з. [Бесплатная статья PMC] [PubMed]
Wickramasinghe D, Wickramasinghe N, Kamburugamuwa S A, Arambepola C, Samarasekera DN. Корреляция между иммунитетом от БЦЖ и заболеваемостью и смертностью от COVID-19. Тропические болезни, туристическая медицина и вакцины. 2020;6. 10.1186/с40794-020-00117-з. [Бесплатная статья PMC] [PubMed]
40. Кумар А., Мишра С., Верма В., Вишвакарма Р.К., Камал В.К., Натх М., Пракаш К., Упадхьяй А.Д., Саху Дж.К. Глобальное влияние температуры окружающей среды и охвата вакцинацией БЦЖ на трансмиссивность и смертность от COVID-19. ПЛОС Один. 2020;15(10):e0240710. doi: 10.1371/journal.pone.0240710. [Статья PMC бесплатно] [PubMed] [CrossRef] [Google Scholar]
41. Клингер Д., Бласс И., Раппопорт Н., Линиал М. Значительное улучшение результатов COVID-19 в странах с более высоким охватом вакцинацией БЦЖ: многопараметрический анализ. Вакцина. 2020;8(3):378. doi: 10.3390/vaccines8030378. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
42. Berg MK, Yu Q, Salvador CE, Melani I, Kitayama S.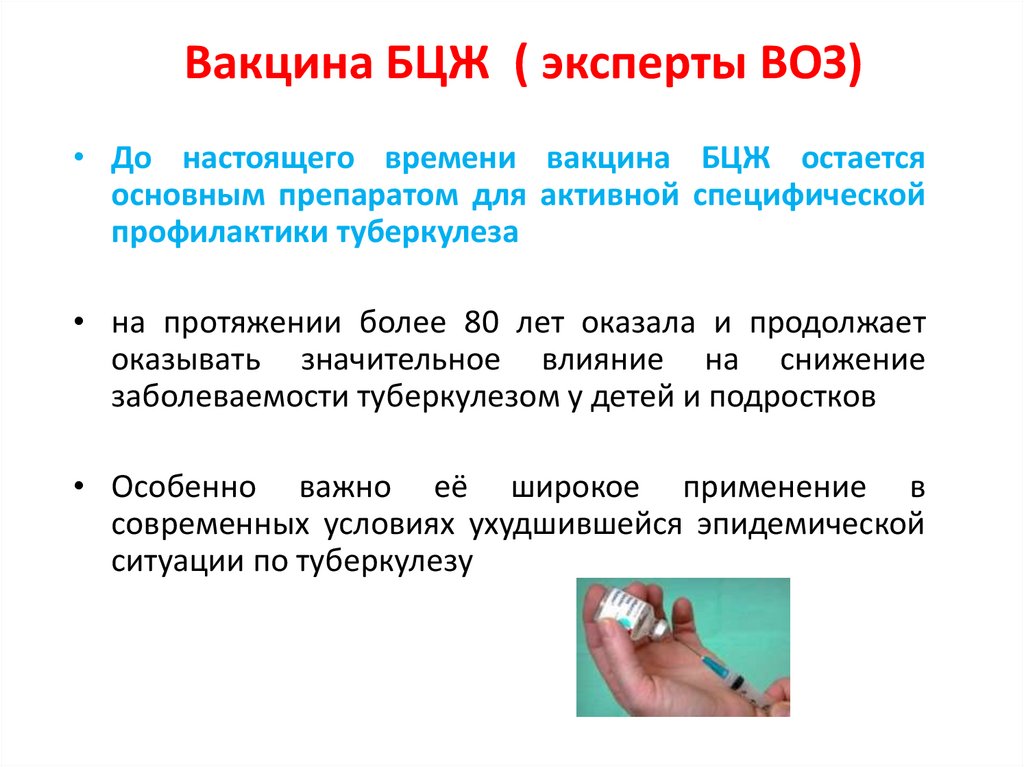 Обязательная вакцинация бациллой Кальметта-Герена (БЦЖ) предсказывает сглаженные кривые распространения COVID-19. Научная реклама 2020;6:eabc1463. doi: 10.1126/sciadv.abc1463. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Обязательная вакцинация бациллой Кальметта-Герена (БЦЖ) предсказывает сглаженные кривые распространения COVID-19. Научная реклама 2020;6:eabc1463. doi: 10.1126/sciadv.abc1463. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
43. Джой М., Малавика Б., Асирватам Э.С., Сударсанам Т.Д., Джеясилан Л. Связана ли БЦЖ со снижением заболеваемости COVID-19? Мета-регрессия глобальных данных из 160 стран. Клиническая эпидемиология и глобальное здоровье. 2020. 10.1016/j.cegh.2020.08.015. [Бесплатная статья PMC] [PubMed]
44. Миллер А., Реанделар М.Дж., Фаскильоне К., Руменова В., Ли И., Отазу Г.Х. Корреляция между политикой всеобщей вакцинации БЦЖ и снижением заболеваемости и смертности от COVID-19: эпидемиологическое исследование. MedRxiv. 2020. 10.1101/2020.03.24.20042937.
45. Szigeti R, Kellermayer D, Trakimas G, Kellermayer R. Эпидемиология БЦЖ поддерживает ее защиту от COVID-19? Слово предостережения. ПЛОС Один. 2020;15(10):e0240203. doi: 10.1371/journal.pone. 0240203. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
0240203. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
46. Wassenaar TM, Buzard GS, Newman DJ. Вакцинация БЦЖ в раннем возрасте не улучшает исходы COVID-19 у пожилых людей, согласно данным, представленным в национальных отчетах. Письма по прикладной микробиологии. 2020;71(5):498-505. 10.1111/лам.13365. [PubMed]
47. Hensel J, McAndrews KM, McGrail DJ, Dowlatshahi DP, LeBleu VS, Kalluri R. Защита от SARS-CoV-2 с помощью вакцинации БЦЖ не подтверждается эпидемиологическими анализами. Научный доклад 2020; 10 (1): 1–9. doi: 10.1038/s41598-020-75491-x. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
48. Мацуура Х., Фукуи М., Кавагути К. Снижает ли вакцинация против туберкулеза инфекцию covid-19?: нет доказательств разрыва регрессии и различий в различиях анализ. medRxiv. 2020. 10.1101/2020.04.13.20064287.
49. https://mapchart.net/world.html. 4 декабря 2020 г.
50. Хауэр Дж., Фишер У., Ауэр Ф., Боркхардт А. Региональная политика вакцинации БЦЖ в бывшей Восточной и Западной Германии может повлиять как на тяжесть SARS-CoV-2, так и на заболеваемость детской лейкемией. Лейкемия. 2020;34(8):2217–9. 10.1038/s41375-020-0871-4. [Бесплатная статья PMC] [PubMed]
Лейкемия. 2020;34(8):2217–9. 10.1038/s41375-020-0871-4. [Бесплатная статья PMC] [PubMed]
51. de Chaisemartin C, de Chaisemartin L. Bacille Calmette-Guérin Вакцинация в младенчестве не защищает от коронавирусной болезни 2019 г.(COVID-19): данные естественного эксперимента в Швеции. Клин Инфекция Дис. 2020. 10.1093/cid/ciaa1223. [Статья бесплатно PMC] [PubMed]
52. Киношита М., Танака М. Влияние плановой вакцинации детей БЦЖ на профилактику местного распространения COVID-19 в Японии. J заразить. 2020;81(4):625–633. doi: 10.1016/j.jinf.2020.08.013. [Статья PMC бесплатно] [PubMed] [CrossRef] [Google Scholar]
53. Moorlag SJ, van Deuren RC, van Werkhoven CH, Jaeger M, Debisarun P, Taks E, et al. Безопасность и COVID-19симптомы у лиц, недавно вакцинированных БЦЖ: ретроспективное когортное исследование. Сотовый представитель Мед. 2020;1(5):100073. doi: 10.1016/j.xcrm.2020.100073. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
54. Карабай О., Кёсе О., Токоглу А.


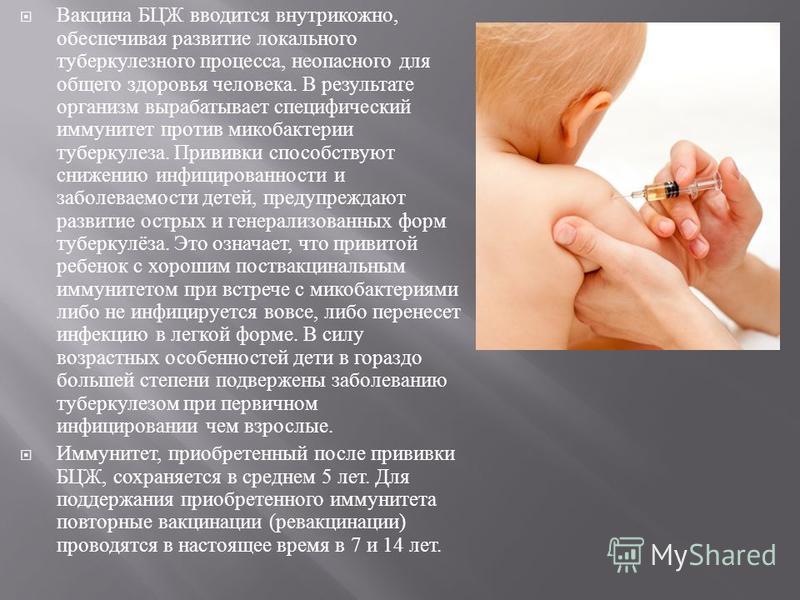
 Обычно проявляется желтухой и поражением печени. Период восстановления может занимать несколько месяцев.
Обычно проявляется желтухой и поражением печени. Период восстановления может занимать несколько месяцев. 


 При вспышках умирает до 60% зараженных.
При вспышках умирает до 60% зараженных. 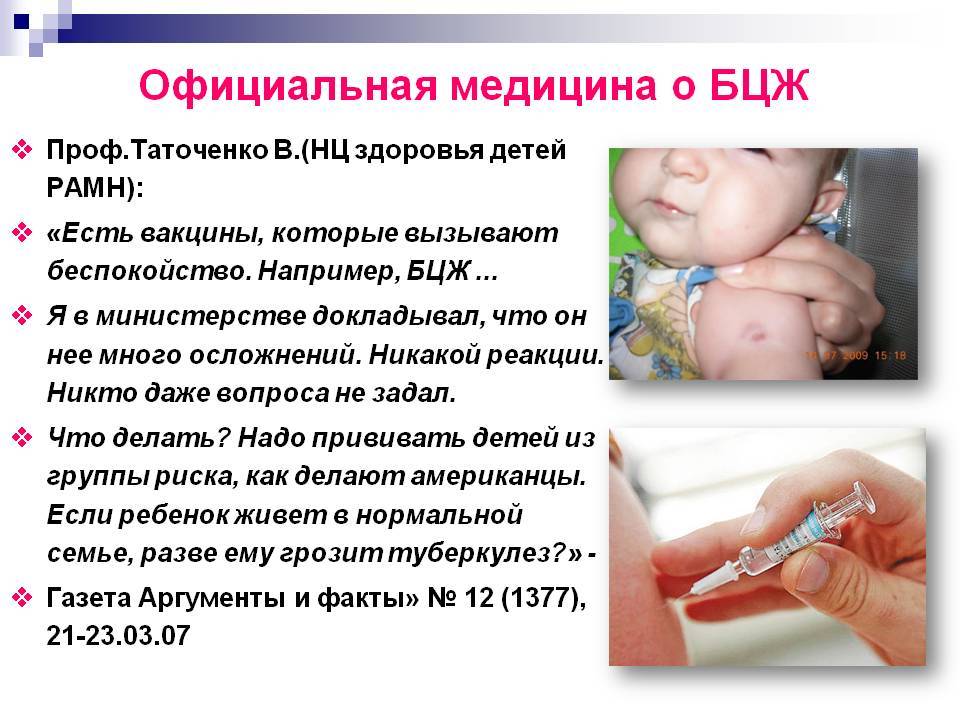 Заражение чаще происходит при сельскохозяйственных работах.
Заражение чаще происходит при сельскохозяйственных работах. 







 , Фогельзанг А., Шурер С., Лазар Д., Кайзер П., Кауфманн С.Х.
, Фогельзанг А., Шурер С., Лазар Д., Кайзер П., Кауфманн С.Х. Ю., Кумар Р., Агравал Б.
Ю., Кумар Р., Агравал Б.