💊 Состав препарата Вакцина туберкулезная для щадящей первичной иммунизации (БЦЖ-М) ✅ Применение препарата Вакцина туберкулезная для щадящей первичной иммунизации (БЦЖ-М) Сохраните у себя Поиск аналогов Взаимодействие Описание активных компонентов препарата Вакцина туберкулезная для щадящей первичной иммунизации (БЦЖ-М) Приведенная научная информация является обобщающей и не может быть использована для принятия Дата обновления: 2020.03.24 Владелец регистрационного удостоверения: ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России (филиал «МЕДГАМАЛ» ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России) Код ATX: J07AN (Вакцина для профилактики туберкулеза) Активное вещество: USP Фармакопея США Лекарственная форма
Форма выпуска, упаковка и состав |
| Лиофилизат для приготовления суспензии для внутрикожного введения | 1 амп. | 1 доза |
| живые микобактерии вакцинного штамма БЦЖ-1* | 500 мг | 25 мкг |
* — живые микобактерии вакцинного штамма БЦЖ-1 лиофилизированы в 1.5% растворе глутамината натрия.
Растворитель: р-р натрия хлорида 0.9% — 2 мл.
20 доз — ампулы (5) в комплекте с растворителем (амп. 5 шт.) — пачки картонные.
Клинико-фармакологическая группа:
Вакцина для профилактики туберкулеза
Фармако-терапевтическая группа:
МИБП-вакцина
Сохраните у себя
Вакцина БЦЖ-М детям — сделать прививку в Москве
Полностью защитить от заражения препарат не может, однако его применение позволяет нивелировать риск развития тяжелой формы болезни. Кроме того, пациенты после БЦЖ-М не сталкиваются с такими серьезными осложнениями, как туберкулез костей или суставов, туберкулезный менингит.
Кроме того, пациенты после БЦЖ-М не сталкиваются с такими серьезными осложнениями, как туберкулез костей или суставов, туберкулезный менингит.
Вакцина БЦЖ-М выпускается в Российской Федерации с 1986 года. Препарат разработан НИИ ЭМ имени Гамалеи. Клинические исследования неоднократно подтвердили безопасность средства. В среднем эффективность прививки среди новорожденных составляет 82%.
Состав препарата
В основе БЦЖ-М лежат бактерии вакцинного штамма. Для получения рабочего состава потребуется растворитель для инъекций.
Показания к применению
БЦЖ-М от туберкулеза применяются для:
- всех новорожденных
- недоношенных новорожденных, вес которых более 2000 грамм
- детей, которые ранее не прошли вакцинацию из-за наличия противопоказаний
Если БЦЖ-М не проведена в родильном доме, ребенка вакцинируют в течение 2 месяцев после рождения, в верхнюю треть плеча внутрикожно. Старше 2 месяцев – после проведения туберкулинодиагностики.
Старше 2 месяцев – после проведения туберкулинодиагностики.
Ревакцинация
Ревакцинация проводится в возрасте 7 лет при отрицательных результатах тубркулинодиагностики.
Побочные действия
Обычно пациенты хорошо переносят введение вакцины БЦЖ-М, побочные реакции возникают редко.
В течение 4-6 недель появляется инфильтрат до 5-10 мм с корочкой в центре либо пустула с необильным серозным отделяемым. За 2-4 месяца происходит образование рубчика 3-10 мм.
Осложнения, которые возникают, можно разделить на 4 группы:
- Локальные (как правило из-за нарушений техники введения)
- БЦЖ-инфекция
- Генерализованная БЦЖ-инфекция (при врожденном иммунодифиците)
- Пост-БЦЖ-синдром
Особые указания
Вводить БЦЖ-М нужно исключительно внутрикожно (при нарушении техники возникают осложнения). После вакцинации запрещено обрабатывать место инъекции дезрастворами, делать повязки, так как это значительно увеличивает вероятность нежелательных местных реакций.
После вакцинации запрещено обрабатывать место инъекции дезрастворами, делать повязки, так как это значительно увеличивает вероятность нежелательных местных реакций.
Противопоказания
Ограничением может стать:
- Низкая масса тела новорожденного (менее 2000 грамм)
- Острый инфекционный процесс
- Иммунодефицитное состояние
- ВИЧ (также у матери)
- Активный или перенесенный туберкулез
- Келоидный рубец на прошлое введение (для ревакцинации)
- Положительная или сомнительная реакция Манту или Диаскинтест (вакцинация не будет эффективной)
Взаимодействие с другими лекарственными препаратами
Детская прививка БЦЖ-М не проводится вместе с другими вакцинами. Иммунологического обоснования этого ограничения нет, такие меры нужны для недопущения контаминации, ведь при случайном подкожном/внутримышечном введении могут возникать осложнения.
Единственное исключение – вакцина от гепатита В, осуществимая в родильном доме.
Подготовка к вакцинации
Подготовка требуется детям старше 2 месяцев, не вакцинированным в роддоме. Заключается она в проведении реакции Манту.
Сделать прививку БЦЖ-М в Москве
Если вам нужно сделать прививку БЦЖ-М ребенку в Москве, вы всегда можете обратиться за этим в клинику «Наше время». Доктора предварительно осмотрят пациента, соберут анамнез, чтобы убедиться в отсутствии противопоказаний.
Только при положительном прохождении этого этапа ребенка допустят к вакцинации. Чтобы записаться на прием, вы можете позвонить администратору по телефону +7 (495) 481-40-04 или написать на WhatsApp. Также доступна система онлайн-записи.
Бацилла Кальметта-Герена — StatPearls
Непрерывное обучение
Бацилла Кальметта-Герена (БЦЖ) представляет собой живую аттенуированную форму вакцины Mycobacterium bovis, используемую для профилактики туберкулеза и других микобактериальных инфекций. Вакцина была разработана Кальметтом и Гереном и впервые была введена людям в 1921 году. БЦЖ — единственная вакцина против туберкулеза. Это наиболее широко применяемая вакцина, обычно входящая в план плановой иммунизации новорожденных. Вакцина БЦЖ также обеспечивает защиту от нетуберкулезных микобактериальных инфекций, таких как проказа и язва Бурули. В ходе этого мероприятия рассматривается механизм действия вакцины БЦЖ и подчеркивается роль межпрофессиональной команды в обучении пациентов методам профилактики туберкулеза.
Вакцина была разработана Кальметтом и Гереном и впервые была введена людям в 1921 году. БЦЖ — единственная вакцина против туберкулеза. Это наиболее широко применяемая вакцина, обычно входящая в план плановой иммунизации новорожденных. Вакцина БЦЖ также обеспечивает защиту от нетуберкулезных микобактериальных инфекций, таких как проказа и язва Бурули. В ходе этого мероприятия рассматривается механизм действия вакцины БЦЖ и подчеркивается роль межпрофессиональной команды в обучении пациентов методам профилактики туберкулеза.
Цели:
Опишите механизм действия вакцины БЦЖ.
Ознакомьтесь с показаниями для вакцины БЦЖ.
Обобщите клиническую значимость вакцины БЦЖ.
Объясните важность улучшения координации помощи между членами межпрофессиональной команды для улучшения результатов у пациентов, получающих вакцину БЦЖ.
Доступ к бесплатным вопросам с несколькими вариантами ответов по этой теме.
Введение
Бацилла Кальметта-Герена (БЦЖ) представляет собой живую аттенуированную форму вакцины Mycobacterium bovis, используемую для профилактики туберкулеза и других микобактериальных инфекций. Вакцина была разработана Кальметтом и Гереном и впервые была введена людям в 1921 году. БЦЖ — единственная вакцина против туберкулеза. Это наиболее широко применяемая вакцина, обычно входящая в план плановой иммунизации новорожденных. Вакцина БЦЖ также обеспечивает защиту от нетуберкулезных микобактериальных инфекций, таких как проказа и язва Бурули. Он также используется при лечении поверхностного рака мочевого пузыря.
Вакцина БЦЖ — достаточно безопасная вакцина, и она не вызывает серьезных осложнений. До микобактериальной инфекции индуцированная вакциной или приобретенная естественным путем инфекция может защитить от последующей инфекции, вызванной микобактериями, включая туберкулез.[1] Предшествующая инфекция нетуберкулезными микобактериями и Mycobacterium tuberculosis может обеспечить естественную защиту от туберкулезной инфекции.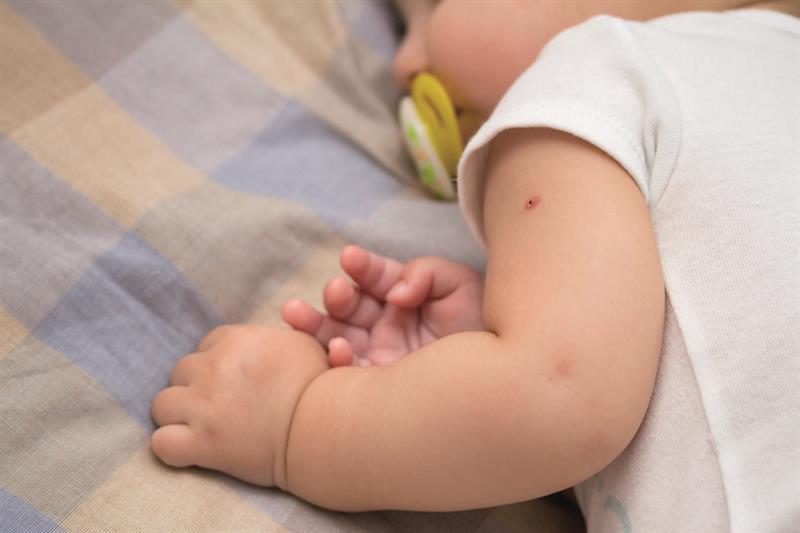 Защита от туберкулезной инфекции обычно обусловлена иммунным ответом на антигены микобактерий. Ранее содержал латентную инфекцию с Mycobacterium tuberculosis может обеспечить до 80 процентной защиты от заболевания при последующем воздействии.[4] У пациентов с предыдущим активным заболеванием существует повышенный риск рецидива активного туберкулеза из-за различных штаммов как у ВИЧ-неинфицированных, так и у ВИЧ-инфицированных пациентов. [5][6][7][8][9][10] Бацилла Кальметта-Герена (БЦЖ) связана со снижением детской смертности, не связанной с туберкулезом. Снижение детской смертности может быть связано с эпигенетическим перепрограммированием рецептора нуклеотид-связывающего домена олигомеризации (NOD2) [11][12][13][14].
Защита от туберкулезной инфекции обычно обусловлена иммунным ответом на антигены микобактерий. Ранее содержал латентную инфекцию с Mycobacterium tuberculosis может обеспечить до 80 процентной защиты от заболевания при последующем воздействии.[4] У пациентов с предыдущим активным заболеванием существует повышенный риск рецидива активного туберкулеза из-за различных штаммов как у ВИЧ-неинфицированных, так и у ВИЧ-инфицированных пациентов. [5][6][7][8][9][10] Бацилла Кальметта-Герена (БЦЖ) связана со снижением детской смертности, не связанной с туберкулезом. Снижение детской смертности может быть связано с эпигенетическим перепрограммированием рецептора нуклеотид-связывающего домена олигомеризации (NOD2) [11][12][13][14].
Вакцину БЦЖ можно вводить внутрикожно или внутрикожно. В настоящее время проводятся исследования респираторного введения с момента естественного заражения, и сенсибилизация к Mycobacterium tuberculosis у людей, как правило, происходит в дыхательной системе.
Показания
Группы, которые следует рассмотреть для вакцинации БЦЖ, включают
Дети: новорожденные и младенцы получают наибольшую пользу от вакцинации БЦЖ
Младенцы и дети до пяти лет с высоким риском заражения активным легочным ТБ.
Здоровые новорожденные [17]
Дети школьного возраста (от 7 до 14 лет), ранее не вакцинированные.[18]
Развитые страны: рассмотреть возможность вакцинации БЦЖ у младенцев и детей до 5 лет при следующих состояниях
[19]
[20]
Длительный контакт с пациентом с нелеченым, недостаточно леченным или устойчивым к изониазиду и рифампину M.tuberculosis, если отделение от такого контакта невозможно.
Воздействие МЛУ-ТБ
Рассмотрите возможность вакцинации путешественников, медицинских работников и лиц в сообществе, подвергшихся воздействию туберкулеза с множественной лекарственной устойчивостью (МЛУ-).

Вводить невакцинированным туберкулинотрицательным лицам.
Медицинские работники
Рутинная вакцинация медицинских работников не рекомендуется в Соединенных Штатах, поскольку уровень инфицирования туберкулезом низкий. Вакцина БЦЖ также влияет на результат туберкулиновой кожной пробы, которая используется для выявления инфекции Mycobacterium tuberculosis. У медицинских работников эффективность вакцинации БЦЖ не определена.[21] В районах с высокой частотой передачи заболевания следует уделять особое внимание строгому соблюдению практик противотуберкулезной инфекции.
Рассмотреть возможность вакцинации БЦЖ медицинских работников в регионах с высоким уровнем передачи ТБ
Рассмотреть возможность вакцинации медицинских работников из стран с низким уровнем риска, осуществляющих уход за пациентами или беженцами в эндемичных по ТБ странах
Рекомендации по иммунизации БЦЖ зависят на распространенность туберкулезной инфекции. [22][23] Иммунизация детей БЦЖ должна быть рутинной в странах с высокой распространенностью туберкулеза. В странах с низкой и средней заболеваемостью ТБ (<5/100 000 случаев с положительным мазком в год) иммунизацию БЦЖ следует проводить детям, подвергающимся особому риску заражения ТБ [23] (т. е. детям, подверженным заболеваниям с множественной лекарственной устойчивостью).
[22][23] Иммунизация детей БЦЖ должна быть рутинной в странах с высокой распространенностью туберкулеза. В странах с низкой и средней заболеваемостью ТБ (<5/100 000 случаев с положительным мазком в год) иммунизацию БЦЖ следует проводить детям, подвергающимся особому риску заражения ТБ [23] (т. е. детям, подверженным заболеваниям с множественной лекарственной устойчивостью).
Политика вакцинации БЦЖ определяется региональной распространенностью туберкулезной инфекции. Рутинная неонатальная вакцинация рекомендована ВОЗ в странах с умеренной и тяжелой распространенностью туберкулеза. Тесные контакты больных туберкулезной инфекцией и медицинских работников, контактировавших с больными полирезистентными туберкулезными инфекциями с отрицательными туберкулиновыми тестами, должны быть вакцинированы БЦЖ. Рутинная вакцинация БЦЖ не рекомендуется в странах с низкой распространенностью туберкулеза. Рутинная вакцинация БЦЖ никогда не рекомендовалась в Соединенных Штатах из-за низкой распространенности туберкулезной инфекции. Плановая вакцинация БЦЖ детей в возрасте 13 лет и всех новорожденных в группах высокого риска проводилась в возрасте от 19 до 19 лет.53 и 2005 в Соединенном Королевстве. Плановая вакцинация была позже прекращена в 2005 году из-за снижения заболеваемости туберкулезом.
Плановая вакцинация БЦЖ детей в возрасте 13 лет и всех новорожденных в группах высокого риска проводилась в возрасте от 19 до 19 лет.53 и 2005 в Соединенном Королевстве. Плановая вакцинация была позже прекращена в 2005 году из-за снижения заболеваемости туберкулезом.
Лечение рака мочевого пузыря
Однократная доза иммунотерапии M. bovis бациллой Кальметта-Герена имеет большой терапевтический эффект при лечении неинвазивных форм рака мочевого пузыря. Его вводят внутрипузырно, и доказанные преимущества включают задержку и предотвращение прогрессирования злокачественного новообразования.[24][25][26]
Противопоказания
Пациенты с ослабленным иммунитетом
БЦЖ является живой вакциной и не должна вводиться:
Лицам с ослабленным иммунитетом с врожденным иммунодефицитом, ВИЧ-инфекцией, злокачественными новообразованиями или тем, кто принимает иммунодепрессанты, такие как блокаторы фактора некроза опухоли-альфа и кортикостероиды
Взрослые с ВИЧ-инфицированные, проживающие в районах с низкой распространенностью туберкулеза
Осложнения
Наиболее частым осложнением является реакция в месте инъекции.
 Реакция в месте инъекции включает гранулематозные поражения, лимфаденопатию регионарных лимфатических узлов, а также узелки или язвы в месте вакцинации с дренированием свищевых ходов или свищей или без них. Mycobacterium bovis является положительным при получении посева из раны.
Реакция в месте инъекции включает гранулематозные поражения, лимфаденопатию регионарных лимфатических узлов, а также узелки или язвы в месте вакцинации с дренированием свищевых ходов или свищей или без них. Mycobacterium bovis является положительным при получении посева из раны.Одним из побочных эффектов БЦЖ является гнойный лимфаденит, у детей с первичными иммунодефицитами более высокий риск распространенного гнойного лимфаденита, и его следует избегать.[27][28] Другие осложнения включают:
Остеит
Остеомиелит
Диссеминированная инфекция может возникать на фоне иммуносупрессии, включая ВИЧ-инфекцию.
Клиническое значение
Вакцинация БЦЖ в младенческом возрасте оказывает существенное влияние на реактивность туберкулиновой кожной пробы (ТКП). Испытание БЦЖ в Соединенных Штатах показало, что у лиц, получивших БЦЖ в младенчестве, реакция туберкулиновой кожной пробы ≥10 мм в течение 55 лет после иммунизации [29]. ]
]
Предыдущая вакцинация БЦЖ не должна влиять на интерпретацию результатов ТКП у лиц, вакцинированных при рождении более десяти лет назад, учитывая, что большинство лиц, получающих вакцину БЦЖ, являются выходцами из районов с высокой заболеваемостью туберкулезом. Анализ высвобождения гамма-интерферона (IGRA) следует использовать для интерпретации положительных ТКП у лиц с иммунизацией БЦЖ в анамнезе, поскольку на этот тест не влияет введение БЦЖ. У лиц, подвергшихся серийному тестированию на туберкулин, предыдущая вакцинация БЦЖ может быть увеличена, что приведет к положительному кожному тесту у человека с предшествующим отрицательным кожным тестом. Сообщалось, что более чем у 50 процентов пациентов, которым внутрипузырно вводили БЦЖ по поводу рака мочевого пузыря, отмечалась конверсия в положительную туберкулиновую кожную пробу. Такое внутрипузырное введение БЦЖ не должно приводить к положительному результату IGRA.[30][31]
Обоснование разработки бустерной вакцины связано со снижением иммунитета примерно через 15-20 лет после начальной иммунизации в младенчестве [32]. Однако исследования, проведенные в Бразилии и Малави, показали, что бустерная доза вакцины БЦЖ не очень эффективна против туберкулеза [33][34][35]. Вакцина БЦЖ может обеспечить защиту от инфекций, вызванных нетуберкулезными микобактериями.[36]
Однако исследования, проведенные в Бразилии и Малави, показали, что бустерная доза вакцины БЦЖ не очень эффективна против туберкулеза [33][34][35]. Вакцина БЦЖ может обеспечить защиту от инфекций, вызванных нетуберкулезными микобактериями.[36]
Исследования показали, что вакцина БЦЖ снижает риск заболевания, вызванного Mycobacterium leprae на 50–80 процентов, и этот эффект усиливается при бустерных дозах БЦЖ.[34][37] Предыдущие исследования показали, что вакцина также на 50 процентов эффективна в предотвращении язвенной болезни Бурули, вызванной M. , , но более поздние ретроспективные исследования не показали доказательств того, что БЦЖ защищает от язвенной болезни Бурули.[38]
Вакцинация БЦЖ также защищает от детского лимфаденита из-за комплекса M. avium [39] было увеличение детского аденита из-за нетуберкулезных микобактерий после прекращения детской иммунизации БЦЖ.
Реакция на туберкулиновую кожную пробу (ТКП) размером от 3 до 19 мм ожидается у большинства лиц, получивших иммунизацию БЦЖ, через два-три месяца после вакцинации. В исследовании 5952 человек, которым была сделана прививка БЦЖ и впоследствии через 10–25 лет проведена туберкулиновая кожная проба, только у 8% были положительные результаты кожной пробы.[31]
В исследовании 5952 человек, которым была сделана прививка БЦЖ и впоследствии через 10–25 лет проведена туберкулиновая кожная проба, только у 8% были положительные результаты кожной пробы.[31]
Улучшение результатов медицинского персонала
Политика вакцинации БЦЖ определяется региональной распространенностью туберкулезной инфекции. Рутинная неонатальная вакцинация рекомендована ВОЗ в странах со средней и тяжелой заболеваемостью туберкулезом. Преобразование туберкулиновой кожной пробы не следует использовать для определения эффективности вакцины БЦЖ среди реципиентов.[34][35][42]
Рутинная вакцинация БЦЖ обычно не рекомендуется в Соединенных Штатах из-за низкой заболеваемости туберкулезом, а также из-за того, что иммунизация мешает тесту PPD. Вакцинация БЦЖ не рекомендуется для медицинских работников в районах с низким уровнем риска. Вакцинация также противопоказана пациентам с ослабленным иммунитетом.
Вакцинация БЦЖ может рассматриваться в ситуациях, когда высокий процент пациентов инфицирован штаммами туберкулеза, устойчивыми к изониазиду и рифампину. [42] Вакцинацию также можно найти в случаях неудачного выполнения общих мер предосторожности в отношении инфекций и при передаче штамма 9 с множественной лекарственной устойчивостью.0035 Вероятен Mycobacterium tuberculosis .[42] Практикующие медсестры, помощники врачей и врачи, которые вводят БЦЖ, должны работать вместе в межпрофессиональной команде, чтобы обеспечить безопасное и эффективное введение, последующее наблюдение и обучение пациента. [Уровень 5]
[42] Вакцинацию также можно найти в случаях неудачного выполнения общих мер предосторожности в отношении инфекций и при передаче штамма 9 с множественной лекарственной устойчивостью.0035 Вероятен Mycobacterium tuberculosis .[42] Практикующие медсестры, помощники врачей и врачи, которые вводят БЦЖ, должны работать вместе в межпрофессиональной команде, чтобы обеспечить безопасное и эффективное введение, последующее наблюдение и обучение пациента. [Уровень 5]
Контрольные вопросы
Доступ к бесплатным вопросам с несколькими вариантами ответов по этой теме.
Комментарий к этой статье.
Каталожные номера
- 1.
фон Рейн С.Ф., Вуола Дж.М. Новые вакцины для профилактики туберкулеза. Клин Инфекция Дис. 2002 г., 15 августа; 35 (4): 465–74. [PubMed: 12145732]
- 2.
Эдвардс Л.Б., Палмер К.Э. Биология микобактериозов. Выявление туберкулезно-инфицированных кожными пробами. Энн Н.
 Ю. Академия наук. 1968 г., 05 сентября; 154 (1): 140-8. [PubMed: 5266317]
Ю. Академия наук. 1968 г., 05 сентября; 154 (1): 140-8. [PubMed: 5266317]- 3.
Мелкий полиэтилен. Изменение защиты БЦЖ: последствия гетерологичного иммунитета и для него. Ланцет. 1995 18 ноября; 346(8986):1339-45. [PubMed: 7475776]
- 4.
Эндрюс Дж. Р., Нубари Ф., Валенский Р. П., Серда Р., Лосина Э., Хорсбург К.Р. Риск прогрессирования активного туберкулеза после повторного заражения микобактериями туберкулеза. Клин Инфекция Дис. 2012 март; 54(6):784-91. [Бесплатная статья PMC: PMC3284215] [PubMed: 22267721]
- 5.
Бьяртвейт К. Олаф Шил и Йоханнес Хаймбек: их вклад в понимание патогенеза и профилактики туберкулеза. Int J Tuberc Lung Dis. 2003 Апрель; 7 (4): 306-11. [В паблике: 12729334]
- 6.
HEIMBECK J. Вакцинация медсестер БЦЖ. бугорок. 1948 апр; 29 (4): 84-8. [PubMed: 18
- 4]
- 7.
Verver S, Warren RM, Beyers N, Richardson M, van der Spuy GD, Borgdorff MW, Enarson DA, Behr MA, van Helden PD.
 Частота повторного заражения туберкулезом после успешного лечения выше, чем частота нового туберкулеза. Am J Respir Crit Care Med. 2005 15 июня; 171 (12): 1430-5. [PubMed: 15831840]
Частота повторного заражения туберкулезом после успешного лечения выше, чем частота нового туберкулеза. Am J Respir Crit Care Med. 2005 15 июня; 171 (12): 1430-5. [PubMed: 15831840]- 8.
фон Рейн CF, Horsburgh CR. Реинфекция микобактериями туберкулеза. Am J Respir Crit Care Med. 2006 01 января; 173 (1): 133-4; ответ автора 134-5. [PubMed: 16368796]
- 9.
Лахи Т., Маккензи Т., Арбайт Р.Д., Бакари М., Мтей Л., Мати М., Маро И., Хорсбург К.Р., Паллангио К., фон Рейн С.Ф. Риск рецидивирующего туберкулеза среди ВИЧ-инфицированных взрослых в Танзании с предшествующим активным туберкулезом. Клин Инфекция Дис. 2013 Январь; 56 (1): 151-8. [Бесплатная статья PMC: PMC3518880] [PubMed: 22972862]
- 10.
Зумла А., Равильоне М., Хафнер Р., фон Рейн С.Ф. Туберкулез. N Engl J Med. 2013 21 февраля; 368 (8): 745-55. [PubMed: 23425167]
- 11.
Roth AE, Stensballe LG, Garly ML, Aaby P. Благоприятные нецелевые эффекты БЦЖ — этические последствия для предстоящего внедрения новых противотуберкулезных вакцин.
 Туберкулез (Эдинб). 2006 ноябрь; 86 (6): 397-403. [PubMed: 165]
Туберкулез (Эдинб). 2006 ноябрь; 86 (6): 397-403. [PubMed: 165]- 12.
Рот А., Дженсен Х., Гарли М.Л., Джана К., Мартинс С.Л., Содеманн М., Родригес А., Ааби П. Младенцы с низкой массой тела при рождении и вакцинация против палочки Кальметта-Герена при рождении: исследование сообщества из Гвинеи-Бисау. Pediatr Infect Dis J. 2004 Jun;23(6):544-50. [Пубмед: 15194836]
- 13.
Кристенсен И., Ааби П., Дженсен Х. Обычные прививки и выживание детей: последующее исследование в Гвинее-Бисау, Западная Африка. БМЖ. 2000 г., 09 декабря; 321 (7274): 1435-8. [Бесплатная статья PMC: PMC27544] [PubMed: 11110734]
- 14.
Kleinnijenhuis J, Quintin J, Preijers F, Joosten LA, Ifrim DC, Saeed S, Jacobs C, van Loenhout J, de Jong D, Stunnenberg Х.Г., Ксавье Р.Дж., ван дер Меер Дж.В., ван Кревел Р., Нетеа М.Г. Бацилла Кальметта-Герена индуцирует NOD2-зависимую неспецифическую защиту от повторного заражения путем эпигенетического перепрограммирования моноцитов.
 Proc Natl Acad Sci U S A. 2012 23 октября; 109(43):17537-42. [Бесплатная статья PMC: PMC3491454] [PubMed: 22988082]
Proc Natl Acad Sci U S A. 2012 23 октября; 109(43):17537-42. [Бесплатная статья PMC: PMC3491454] [PubMed: 22988082]- 15.
Джейнатан М., Гериазон А., Син З. Просветные Т-клетки дыхательных путей: новинка на этапе стратегий вакцинации против туберкулеза. Тренды Иммунол. 2010 июль; 31 (7): 247-52. [PubMed: 20542470]
- 16.
Horvath CN, Shaler CR, Jeyanathan M, Zganiacz A, Xing Z. Механизмы отсроченной противотуберкулезной защиты в легких хозяев, вакцинированных парентерально БЦЖ: решающая роль дыхательных путей Люминальные Т-клетки. Иммунол слизистых оболочек. 2012 июль; 5 (4): 420-31. [В паблике: 22453678]
- 17.
Лутвама Ф., Кагина Б.М., Ваджа А., Вайсва Ф., Мансур Н., Киримунда С., Хьюз Э.Дж., Киванука Н., Джолоба М.Л., Мусоке П., Скриба Т.Дж., Майянджа-Кицца Х., Дэй С.Л., Ханеком ВА. Отчетливые ответы Т-клеток, когда вакцинация БЦЖ откладывается от рождения до 6-недельного возраста у младенцев Уганды. J заразить Dis.
 2014 март; 209(6):887-97. [Бесплатная статья PMC: PMC6392474] [PubMed: 24179111]
2014 март; 209(6):887-97. [Бесплатная статья PMC: PMC6392474] [PubMed: 24179111]- 18.
Перейра С.М., Баррето М.Л., Пилгер Д., Круз А.А., Сант-Анна С., Хиджар М.А., Ичихара М.Ю., Сантос А.С., Генсер Б., Родригес ЛК. Эффективность и экономическая эффективность первой вакцинации БЦЖ против туберкулеза у детей школьного возраста без туберкулиновой пробы в анамнезе (исследование БЦЖ-REVAC): кластерное рандомизированное исследование. Ланцет Infect Dis. 2012 апр;12(4):300-6. [В паблике: 22071248]
- 19.
Роль вакцины БЦЖ в профилактике и борьбе с туберкулезом в США. Совместное заявление Консультативного совета по ликвидации туберкулеза и Консультативного комитета по практике иммунизации. MMWR Recomm Rep. 1996 Apr 26;45(RR-4):1-18. [PubMed: 8602127]
- 20.
Dara M, Acosta CD, Rusovich V, Zellweger JP, Centis R, Migliori GB., Члены рабочей группы ВОЗ по вопросам детства. Вакцинация против бациллы Кальметта-Герена: текущая ситуация в Европе.
 Eur Respir J. 2014 янв; 43(1):24-35. [В паблике: 24381321]
Eur Respir J. 2014 янв; 43(1):24-35. [В паблике: 24381321]- 21.
Брюэр Т.Ф., Кольдиц Г.А. Вакцинация бациллой Кальметта-Герена для профилактики туберкулеза у медицинских работников. Клин Инфекция Дис. 1995 янв; 20 (1): 136-42. [PubMed: 7727639]
- 22.
Критерии прекращения программ вакцинации с использованием бациллы Кальметта-Герена (БЦЖ) в странах с низкой распространенностью туберкулеза. Заявление Международного союза по борьбе с туберкулезом и болезнями легких. Tuber Lung Dis. 1994 июня; 75(3):179-80. [PubMed: 7919307]
- 23.
Fine P. Прекращение плановой вакцинации против туберкулеза в школах. БМЖ. 2005 г., 24 сентября; 331 (7518): 647-8. [Статья бесплатно PMC: PMC1226231] [PubMed: 16179677]
- 24.
Miyazaki J, Onozawa M, Takaoka E, Yano I. Различия штаммов Bacillus Calmette-Guérin как основа иммунотерапии против рака мочевого пузыря. Int J Урол. 2018 май; 25(5):405-413. [PubMed: 29506322]
- 25.

Hameed A, Sezian N, Thwaini A. Контрактура мочевого пузыря: обзор осложнений внутрипузырной бациллы Кальметта-Герена. Может Джей Урол. 2007 Декабрь; 14 (6): 3745-9. [PubMed: 18163926]
- 26.
DeGeorge KC, Holt HR, Hodges SC. Рак мочевого пузыря: диагностика и лечение. Ам семейный врач. 2017 15 октября; 96 (8): 507-514. [PubMed: 288]
- 27.
Болурсаз М.Р., Лотфиан Ф., Велаяти А.А. Осложнения вакцины Bacillus Calmette-Guérin у иранских детей в университетской больнице. Аллергол Иммунопатол (Мадр). 2017 июль — август; 45 (4): 356-361. [В паблике: 28161281]
- 28.
Аль-Хаммади С., Алсувайди А.Р., Альшамси Э.Т., Гаташе Г.А., Суид А.К. Диссеминированная инфекция бациллой Кальметта-Герена (БЦЖ) у детей раннего возраста с иммунодефицитом. Примечания BMC Res. 2017 05 мая; 10 (1): 177. [Бесплатная статья PMC: PMC5420150] [PubMed: 28476145]
- 29.
Mancuso JD, Mody RM, Olsen CH, Harrison LH, Santosham M, Aronson NE.
 Долгосрочное влияние вакцинации бациллой Кальметта-Герена на туберкулиновые кожные пробы: 55-летнее последующее исследование. Грудь. 2017 авг; 152 (2): 282-294. [PubMed: 28087302]
Долгосрочное влияние вакцинации бациллой Кальметта-Герена на туберкулиновые кожные пробы: 55-летнее последующее исследование. Грудь. 2017 авг; 152 (2): 282-294. [PubMed: 28087302]- 30.
Ламм Д.Л. Иммунотерапия бациллами Кальметта-Герена при раке мочевого пузыря. Дж Урол. 1985 г., июль; 134 (1): 40–7. [PubMed: 3892050]
- 31.
Сильверман М.С., Рейнольдс Д., Кавсак П.А., Гарай Дж., Дали А., Дэвис И. Использование интерферон-гамма-анализа для оценки пациентов с раком мочевого пузыря, получавших внутрипузырное введение БЦЖ и подвергшихся воздействию к туберкулёзу. Клин Биохим. 2007 авг; 40 (12): 913-5. [PubMed: 17512514]
- 32.
фон Рейн CF. Исправление записи о БЦЖ, прежде чем мы лицензируем новые вакцины против туберкулеза. JR Soc Med. 2017 ноябрь;110(11):428-433. [Бесплатная статья PMC: PMC5728619] [PubMed: 28949270]
- 33.
Black GF, Weir RE, Floyd S, Bliss L, Warndorff DK, Crampin AC, Ngwira B, Sichali L, Nazareth B, Blackwell JM, Брэнсон К.
 , Чагулука С.Д., Донован Л., Джарман Э., Кинг Э., Файн ЧП, Докрелл Х.М. Индуцированное БЦЖ усиление интерферон-гамма-ответа на микобактериальные антигены и эффективность вакцинации БЦЖ в Малави и Великобритании: два рандомизированных контролируемых исследования. Ланцет. 2002 20 апреля; 359(9315):1393-401. [PubMed: 11978337]
, Чагулука С.Д., Донован Л., Джарман Э., Кинг Э., Файн ЧП, Докрелл Х.М. Индуцированное БЦЖ усиление интерферон-гамма-ответа на микобактериальные антигены и эффективность вакцинации БЦЖ в Малави и Великобритании: два рандомизированных контролируемых исследования. Ланцет. 2002 20 апреля; 359(9315):1393-401. [PubMed: 11978337]- 34.
Рандомизированное контролируемое исследование однократной БЦЖ, повторной БЦЖ или комбинированной вакцины БЦЖ и убитой микобактерии лепры для профилактики лепры и туберкулеза в Малави. Пробная группа по профилактике каронга. Ланцет. 1996 06 июля; 348 (9019): 17-24. [PubMed: 8691924]
- 35.
Родригес Л.С., Перейра С.М., Кунья С.С., Генсер Б., Ичихара М.Ю., де Брито С.К., Хиджар М.А., Дорадо И., Круз А.А., Сант-Анна С., Бирренбах А.Л., Баррето мл. Влияние ревакцинации БЦЖ на заболеваемость туберкулезом среди детей школьного возраста в Бразилии: кластерное рандомизированное исследование БЦЖ-REVAC. Ланцет. 2005 08 октября; 366(9)493):1290-5.
 [PubMed: 16214599]
[PubMed: 16214599]- 36.
Циммерманн П., Финн А., Кертис Н. Защищает ли вакцинация БЦЖ от нетуберкулезной микобактериальной инфекции? Систематический обзор и метаанализ. J заразить Dis. 2018 24 июля; 218 (5): 679-687. [PubMed: 29635431]
- 37.
Merle CS, Cunha SS, Rodrigues LC. Вакцинация БЦЖ и защита от проказы: обзор текущих данных и статуса БЦЖ в борьбе с проказой. Эксперт Rev Вакцины. 2010 Февраль;9(2):209-22. [PubMed: 20109030]
- 38.
Phillips RO, Phanzu DM, Beissner M, Badziklou K, Luzolo EK, Sarfo FS, Halatoko WA, Amoako Y, Frimpong M, Kabiru AM, Piten E, Maman I, Bidjada Б., Коба А., Авусси К.С., Кобара Б., Ничке Дж., Видеманн Ф.Х., Кере А.Б., Аджей О., Лешер Т., Флейшер Б., Бретцель Г., Хербингер К.Х. Эффективность плановой вакцинации БЦЖ при язвенной болезни бурули: исследование случай-контроль в Демократической Республике Конго, Гане и Того. PLoS Negl Trop Dis. 2015 янв;9(1):e3457. [Бесплатная статья PMC: PMC4287572] [PubMed: 25569674]
- 39.

Katila ML, Brander E, Backman A. Неонатальная вакцинация БЦЖ и микобактериальный аденит шейки матки в детстве. бугорок. 1987 декабрь; 68 (4): 291-6. [PubMed: 3138802]
- 40.
Romanus V, Hallander HO, Wåhlén P, Olinder-Nielsen AM, Magnusson PH, Juhlin I. Атипичные микобактерии при внелегочных заболеваниях у детей. Заболеваемость в Швеции с 1969 по 1990 год, связанная с изменением охвата вакцинацией БЦЖ. Tuber Lung Dis. 1995 августа; 76(4):300-10. [PubMed: 7579311]
- 41.
Конттури А., Сойни Х., Оллгрен Дж., Сало Э. Увеличение числа нетуберкулезных микобактериальных инфекций у детей после падения охвата бациллой Кальметта-Герена: общенациональное популяционное ретроспективное исследование, Финляндия, 1995-2016 гг. Клин Инфекция Дис. 2018 28 сентября; 67 (8): 1256-1261. [PubMed: 29584893]
- 42.
Люн К.С., Тэм К.М., Чан С.Л., Чан-Юнг М., Чан К.К., Чанг К.К. Эффективность программы ревакцинации БЦЖ в когорте, получившей прививку БЦЖ при рождении в Гонконге.
 Int J Tuberc Lung Dis. 2001 авг; 5 (8): 717-23. [В паблике: 11495262]
Int J Tuberc Lung Dis. 2001 авг; 5 (8): 717-23. [В паблике: 11495262]
Вакцинация БЦЖ: 90 лет прошло, а еще так много предстоит узнать…
Текст статьи
Меню статьи
- Статья
Текст - Артикул
информация - Цитата
Инструменты - Поделиться
- Быстрое реагирование
- Артикул
метрика - Оповещения
Редакция
Вакцинация БЦЖ: 90 лет спустя, а еще так много предстоит узнать…
Бесплатно
- Ajit Lalvani,
- Saranya Sridhar
- Tuberculosis Research Unit, Department of Respiratory Medicine, National Heart and Lung Institute, Imperial College London, London, UK
- Correspondence to Ajit Lalvani, Tuberculosis Research Подразделение, Департамент респираторной медицины, Национальный институт сердца и легких, Имперский колледж Лондона, Норфолк-плейс, Лондон, W2 1PG, Великобритания; a.
 lalvani{at}imperial.ac.uk
lalvani{at}imperial.ac.uk
http://dx.doi.org/10.1136/thx.2010.140996
Статистика с сайта Altmetric.com
Запрос разрешений
вас к службе RightsLink Центра защиты авторских прав. Вы сможете получить быструю цену и мгновенное разрешение на повторное использование контента различными способами.
История вакцинации против туберкулеза изобилует случаями научных открытий и повторных открытий. В конце 19В начале XX века, после объявления Робертом Кохом об открытии им Mycobacterium tuberculosis в 1882 году, ученые всего мира, в том числе и сам Кох, приступили к созданию вакцины против туберкулеза. В 1908 году Леон Кальметт, бактериолог, и Камиль Герен, ветеринар из Института Пастера, Лилль, начали эксперимент по разработке вакцины путем ослабления штамма Mycobacterium bovis до тех пор, пока он не потерял свою вирулентность. Тринадцать лет и 230 пассажей спустя они смогли показать, что штамм обладал защитным действием на животных моделях и больше не вызывал болезни, которая, как впоследствии было обнаружено, в первую очередь связана с потерей генов в области различия 1 (RD1) области M bovis genome. 1 В том же году ребенку, контактировавшему с туберкулезом, была введена первая доза этой живой аттенуированной вакцины, M bovis Bacille Calmette-Geurin (БЦЖ). Теперь, когда ввели более 3 миллиардов доз, БЦЖ является наиболее широко используемой вакциной во всем мире.
1 В том же году ребенку, контактировавшему с туберкулезом, была введена первая доза этой живой аттенуированной вакцины, M bovis Bacille Calmette-Geurin (БЦЖ). Теперь, когда ввели более 3 миллиардов доз, БЦЖ является наиболее широко используемой вакциной во всем мире.
С момента своего первого применения 90 лет назад БЦЖ была рекомендована в качестве вакцины из-за ее частичного защитного действия против активного туберкулеза и смерти, хотя и с большей эффективностью против диссеминированных и менингеальных заболеваний у детей, чем против легочных заболеваний у подростков и взрослых.2 3 Это, вместе с исследованиями вскрытия, предполагает, что БЦЖ уменьшает размер очагов туберкулеза в легких, тем самым ограничивая бациллярное размножение и распространение4, и модели животных, где вакцинация БЦЖ снижает бактериальную нагрузку через 9 лет.0525 Mtuberculosis вызов, но не защищает от инфекции, привел к давней догме, согласно которой БЦЖ защищает от распространения и заболевания, но не от инфекции. Всего 5 лет назад первое сообщение5 о способности БЦЖ защищать от инфекции изменило наше представление о том, как действует БЦЖ. Вывод о том, что БЦЖ может действовать на ранней стадии пути передачи инфекции от туберкулеза к заболеванию (рис. 1), впоследствии был подтвержден исследованиями контактов взрослых и детей в сообществе в Гамбурге6 и двумя исследованиями школьных вспышек туберкулеза в Великобритании. 7 последний из которых опубликован в текущем выпуске Thorax ( , см. стр. 1067 ).8 Исследуя вспышку точечного туберкулеза в детском саду, Эриксен и его коллеги обнаружили, что дети, вакцинированные БЦЖ, имели значительно меньшую вероятность заражения, судя по высвобождению гамма-интерферона. -анализа (IGRA), чем у непривитых детей. Эффективность вакцины против инфекции оценивалась в 66%, но, учитывая небольшой размер исследования, доверительные интервалы достаточно широки, чтобы перекрываться со снижением ОР на 38%7 и 24%5, наблюдавшимся в предыдущих более крупных исследованиях.
Всего 5 лет назад первое сообщение5 о способности БЦЖ защищать от инфекции изменило наше представление о том, как действует БЦЖ. Вывод о том, что БЦЖ может действовать на ранней стадии пути передачи инфекции от туберкулеза к заболеванию (рис. 1), впоследствии был подтвержден исследованиями контактов взрослых и детей в сообществе в Гамбурге6 и двумя исследованиями школьных вспышек туберкулеза в Великобритании. 7 последний из которых опубликован в текущем выпуске Thorax ( , см. стр. 1067 ).8 Исследуя вспышку точечного туберкулеза в детском саду, Эриксен и его коллеги обнаружили, что дети, вакцинированные БЦЖ, имели значительно меньшую вероятность заражения, судя по высвобождению гамма-интерферона. -анализа (IGRA), чем у непривитых детей. Эффективность вакцины против инфекции оценивалась в 66%, но, учитывая небольшой размер исследования, доверительные интервалы достаточно широки, чтобы перекрываться со снижением ОР на 38%7 и 24%5, наблюдавшимся в предыдущих более крупных исследованиях. В совокупности эти данные убедительно свидетельствуют о том, что по крайней мере часть защитного эффекта БЦЖ связана с защитой от инфекции, что имеет существенное значение для разработки и оценки новых противотуберкулезных вакцин, а также роли БЦЖ в программах борьбы с ТБ. Действительно, Эриксен и его коллеги обсуждают вопрос о пересмотре порога вакцинации БЦЖ в регионах с разным уровнем заболеваемости туберкулезом. Тем не менее, к выводам о причинной роли БЦЖ в защите от инфекции следует относиться с осторожностью, учитывая нерандомизированный характер обсервационных исследований на сегодняшний день, хотя совокупные данные из множества эпидемиологически различных условий делают доводы в пользу причинной роли БЦЖ все более частыми. неотразимый.
В совокупности эти данные убедительно свидетельствуют о том, что по крайней мере часть защитного эффекта БЦЖ связана с защитой от инфекции, что имеет существенное значение для разработки и оценки новых противотуберкулезных вакцин, а также роли БЦЖ в программах борьбы с ТБ. Действительно, Эриксен и его коллеги обсуждают вопрос о пересмотре порога вакцинации БЦЖ в регионах с разным уровнем заболеваемости туберкулезом. Тем не менее, к выводам о причинной роли БЦЖ в защите от инфекции следует относиться с осторожностью, учитывая нерандомизированный характер обсервационных исследований на сегодняшний день, хотя совокупные данные из множества эпидемиологически различных условий делают доводы в пользу причинной роли БЦЖ все более частыми. неотразимый.
Рисунок 1
Схема защитного действия БЦЖ на различных стадиях естественного течения туберкулеза. Серые стрелки представляют эффекты БЦЖ, обнаруженные за последние 5 лет, а черные стрелки представляют исторически известные эффекты.
В этом выпуске Thorax мы также узнаем о другом до сих пор неизвестном эффекте БЦЖ, который, по-видимому, заключается в ее способности способствовать разрешению лечения у пациентов с активным заболеванием. Jeremiah и его коллеги сообщают о результатах лонгитюдного исследования 546 взрослых пациентов с обычно высоким исходным бактериальным обсеменением мокроты, проходящих лечение от туберкулеза легких в Танзании (9).0489 см. стр. 1072 )9; 5,5% результатов посева мокроты не стали отрицательными через 2 месяцев лечения, что является общепризнанным маркером риска рецидива после завершения лечения. При многофакторном анализе отсутствие рубца после введения БЦЖ было связано с весьма значимым трехкратным увеличением риска неудачной конверсии посева мокроты. Пациенты с самой высокой начальной бактериальной нагрузкой мокроты имели пятикратно повышенный риск неудачной конверсии мокроты в течение 2 месяцев, как и ожидалось, в то время как ВИЧ-статус, количество CD4 и индекс массы тела не были значимо связаны с неудачной конверсией мокроты. Эти результаты намекают на возможную роль БЦЖ в содействии клиренсу большой бациллярной нагрузки во время лечения. Учитывая, что БЦЖ не защищает от развития туберкулеза легких в условиях высокой нагрузки, ее связь с микробиологической реакцией на лечение является неожиданной и удивительной. Однако возможно, что противотуберкулезные антибиотики и иммунный ответ хозяина каким-то образом взаимодействуют, чтобы уменьшить микобактериальную нагрузку in vivo, но вклад иммунного ответа хозяина сам по себе трудно установить наряду с мощным эффектом противотуберкулезного лечения при лекарственно-чувствительных заболеваниях. болезнь. Тем не менее, значительные показатели спонтанного выздоровления больных туберкулезом в доантибиотическую эру в санаториях10 и недавние данные на животных моделях11 предполагают значительную роль реакции хозяина в микробиологическом излечении. Таким образом, по крайней мере вероятно, что иммунитет хозяина играет роль в бактериальном клиренсе мокроты, но неизвестно, как этот иммунитет позитивно и долговременно модулируется вакцинацией БЦЖ много лет назад.
Эти результаты намекают на возможную роль БЦЖ в содействии клиренсу большой бациллярной нагрузки во время лечения. Учитывая, что БЦЖ не защищает от развития туберкулеза легких в условиях высокой нагрузки, ее связь с микробиологической реакцией на лечение является неожиданной и удивительной. Однако возможно, что противотуберкулезные антибиотики и иммунный ответ хозяина каким-то образом взаимодействуют, чтобы уменьшить микобактериальную нагрузку in vivo, но вклад иммунного ответа хозяина сам по себе трудно установить наряду с мощным эффектом противотуберкулезного лечения при лекарственно-чувствительных заболеваниях. болезнь. Тем не менее, значительные показатели спонтанного выздоровления больных туберкулезом в доантибиотическую эру в санаториях10 и недавние данные на животных моделях11 предполагают значительную роль реакции хозяина в микробиологическом излечении. Таким образом, по крайней мере вероятно, что иммунитет хозяина играет роль в бактериальном клиренсе мокроты, но неизвестно, как этот иммунитет позитивно и долговременно модулируется вакцинацией БЦЖ много лет назад. Кроме того, вызывает недоумение тот факт, что предположительно иммунологически опосредованные эффекты БЦЖ на микробиологический ответ на лечение могли быть настолько сильными, когда ВИЧ-статус и количество CD4 не оказывали существенного влияния на скорость конверсии мокроты. Бумага Иеремии et al не содержит информации о чувствительности инфекционных штаммов к антибиотикам, которая является основным фактором, определяющим время конверсии мазка мокроты и посева, но, учитывая сообщения о низкой распространенности туберкулеза с множественной лекарственной устойчивостью в Танзании,12 результаты. К этому замечательному первому сообщению о связи вакцинации БЦЖ с выздоровлением следует относиться с осторожностью, пока дальнейшие исследования не подтвердят это наблюдение; тем не менее, результаты должны стимулировать дальнейшие исследования в том же духе, расширенные на детей, внелегочные заболевания и устойчивые к лекарствам организмы. Интересно, что этот отчет расширил данные о защитном действии БЦЖ, идентифицировав другой гораздо более поздний момент в естественном течении туберкулезной инфекции, когда БЦЖ, по-видимому, действует (рис.
Кроме того, вызывает недоумение тот факт, что предположительно иммунологически опосредованные эффекты БЦЖ на микробиологический ответ на лечение могли быть настолько сильными, когда ВИЧ-статус и количество CD4 не оказывали существенного влияния на скорость конверсии мокроты. Бумага Иеремии et al не содержит информации о чувствительности инфекционных штаммов к антибиотикам, которая является основным фактором, определяющим время конверсии мазка мокроты и посева, но, учитывая сообщения о низкой распространенности туберкулеза с множественной лекарственной устойчивостью в Танзании,12 результаты. К этому замечательному первому сообщению о связи вакцинации БЦЖ с выздоровлением следует относиться с осторожностью, пока дальнейшие исследования не подтвердят это наблюдение; тем не менее, результаты должны стимулировать дальнейшие исследования в том же духе, расширенные на детей, внелегочные заболевания и устойчивые к лекарствам организмы. Интересно, что этот отчет расширил данные о защитном действии БЦЖ, идентифицировав другой гораздо более поздний момент в естественном течении туберкулезной инфекции, когда БЦЖ, по-видимому, действует (рис. 1).
1).
Наряду с растущим количеством свидетельств того, что БЦЖ влияет на несколько отдельных моментов в естественном течении туберкулеза, все больше данных указывают на положительное влияние БЦЖ на другие заболевания, помимо туберкулеза, включая проказу13, астму14, детскую пневмонию15 и младенческую смертность от всех причин16. 17 Таким образом, несмотря на то, что мы используем БЦЖ уже почти столетие, только совсем недавно база эпидемиологических данных постепенно раскрывает плейотропные эффекты БЦЖ на туберкулез и другие серьезные заболевания. Несмотря на этот недавний прогресс в распознавании множественных эффектов БЦЖ, ее иммунологические механизмы действия, а также причины ее неспособности последовательно предотвращать туберкулез легких у взрослых остаются неясными.18 Это серьезный недостаток, учитывая исключительную важность такого понимания для разработка и оценка новых и улучшенных противотуберкулезных вакцин с большей защитной эффективностью. Более того, в клинических испытаниях находится не менее двенадцати экспериментальных вакцин-кандидатов, большинство из которых оцениваются на предмет их способности усиливать иммунный ответ, первоначально вызванный БЦЖ. Проблема в том, что мы до сих пор не знаем, какой из иммунных ответов, индуцированных БЦЖ, опосредует или коррелирует с защитой от туберкулезной инфекции или заболевания. Хотя полифункциональные CD4 и CD8 Т-клетки, специфичные для Антигены М.tuberculosis все чаще рассматриваются как потенциальные корреляты или медиаторы защитного иммунитета в испытаниях вакцин и индуцируются новыми вакцинами,19 20 БЦЖ-специфические полифункциональные Т-клетки не коррелируют с защитой от туберкулеза.21
Проблема в том, что мы до сих пор не знаем, какой из иммунных ответов, индуцированных БЦЖ, опосредует или коррелирует с защитой от туберкулезной инфекции или заболевания. Хотя полифункциональные CD4 и CD8 Т-клетки, специфичные для Антигены М.tuberculosis все чаще рассматриваются как потенциальные корреляты или медиаторы защитного иммунитета в испытаниях вакцин и индуцируются новыми вакцинами,19 20 БЦЖ-специфические полифункциональные Т-клетки не коррелируют с защитой от туберкулеза.21
Значительная трудность в интерпретация результатов обеих статей, опубликованных в этом выпуске Thorax , и, действительно, всех обсервационных исследований, изучающих защитные эффекты и основные механизмы БЦЖ, основывается на формировании рубцов как суррогатном маркере вакцинации БЦЖ. Зависимость от образования рубца при выводе о прививке осложняется высокой распространенностью (20–50%) реципиентов, неспособных сформировать рубец22–24, и влиянием метода вакцинации на развитие рубца.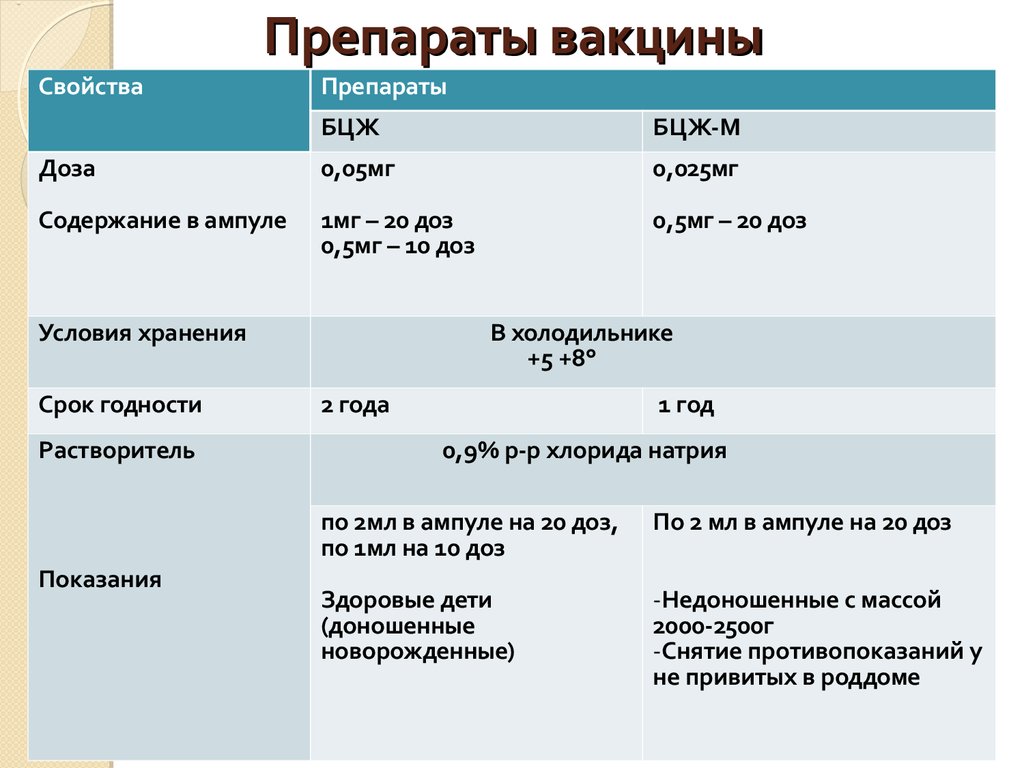 16 Более того, образование рубца не коррелирует с БЦЖ-индуцированное развитие адаптивных клеточных иммунных ответов.25, 26 Эта нерешенная связь между образованием рубца и вакцинацией БЦЖ затрудняет оценку истинного защитного эффекта вакцины, независимо от рубца, в эпоху, когда рандомизированные испытания БЦЖ по сравнению с плацебо являются неэтичными. Таким образом, вопрос заключается в том, опосредована ли частичная защита от различных стадий пути от воздействия туберкулеза до болезни, вызванной вакцинацией БЦЖ, иммунными реакциями, которые не зависят от реакции, необходимой для рубцевания, или иммунными реакциями, которые также вызывают рубцевание. Третья возможность заключается в том, что рубцовая реакция на внутрикожное введение БЦЖ является суррогатным маркером людей, у которых уже есть врожденный защитный иммунитет к туберкулезу, который не индуцируется вакцинацией БЦЖ. Продольные иммуноэпидемиологические исследования с клиническими конечными точками, которые наблюдают за лицами, вакцинированными БЦЖ, у которых есть и у которых нет рубцов, необходимы, чтобы распутать иммунологические отношения между триадой вакцинации, образованием рубцов и защитой.
16 Более того, образование рубца не коррелирует с БЦЖ-индуцированное развитие адаптивных клеточных иммунных ответов.25, 26 Эта нерешенная связь между образованием рубца и вакцинацией БЦЖ затрудняет оценку истинного защитного эффекта вакцины, независимо от рубца, в эпоху, когда рандомизированные испытания БЦЖ по сравнению с плацебо являются неэтичными. Таким образом, вопрос заключается в том, опосредована ли частичная защита от различных стадий пути от воздействия туберкулеза до болезни, вызванной вакцинацией БЦЖ, иммунными реакциями, которые не зависят от реакции, необходимой для рубцевания, или иммунными реакциями, которые также вызывают рубцевание. Третья возможность заключается в том, что рубцовая реакция на внутрикожное введение БЦЖ является суррогатным маркером людей, у которых уже есть врожденный защитный иммунитет к туберкулезу, который не индуцируется вакцинацией БЦЖ. Продольные иммуноэпидемиологические исследования с клиническими конечными точками, которые наблюдают за лицами, вакцинированными БЦЖ, у которых есть и у которых нет рубцов, необходимы, чтобы распутать иммунологические отношения между триадой вакцинации, образованием рубцов и защитой. Примечательно, что крупные клинические испытания вакцины с конечной точкой, предназначенные для усиления БЦЖ новыми вакцинами, могут предоставить возможность решить этот сложный вопрос и выявить истинные корреляты защитного иммунитета, вызванные вакцинами.
Примечательно, что крупные клинические испытания вакцины с конечной точкой, предназначенные для усиления БЦЖ новыми вакцинами, могут предоставить возможность решить этот сложный вопрос и выявить истинные корреляты защитного иммунитета, вызванные вакцинами.
Подобно прекрасному вину, которое с возрастом становится только лучше, через 90 лет после первой прививки людям мы все еще изучаем различные аспекты применения БЦЖ при туберкулезе и не только. По иронии судьбы, масштабы глобальной пандемии туберкулеза, сами по себе частично являющиеся результатом неспособности БЦЖ полностью защитить от туберкулеза, вынуждают нас настойчиво пытаться разгадать механизмы, ответственные за частичную эффективность БЦЖ, одновременно продвигаясь вперед с клиническими испытаниями вакцины. новые экспериментальные вакцины. Таким образом, прививка от туберкулеза, по-видимому, имеет много общего с самой жизнью, как предполагал Серен Кьеркегор:0525 Жизнь можно понять только задом наперёд, а прожить её надо вперёд ’.
Ссылки
- ↵
- Хсу Т.,
- Хингли-Уилсон С.М.,
- Чен Б.,
- и др.
28 90. Первичный механизм аттенуации бациллы Кальметта-Герена заключается в потере секреторной литической функции, необходимой для инвазии в интерстициальную ткань легких. Proc Natl Acad Sci U S A 2003;100:12420–5.
- ↵
- Trunz BB,
- Fine P,
- Краситель C
. Влияние вакцинации БЦЖ на детский туберкулезный менингит и милиарный туберкулез во всем мире: метаанализ и оценка экономической эффективности. Ланцет 2006; 367:1173–80.
- ↵
- Colditz GA,
- Brewer TF,
- Berkey CS,
- и др.
. Эффективность вакцины БЦЖ в профилактике туберкулеза. Метаанализ опубликованной литературы. JAMA 1994; 271:698–702.
- ↵
- Сазерленд I,
- Линдгрен I
.
 Защитный эффект вакцинации БЦЖ на основании патологоанатомических исследований. Бугорок 1979; 60: 225–31.
Защитный эффект вакцинации БЦЖ на основании патологоанатомических исследований. Бугорок 1979; 60: 225–31. - ↵
- Сойсал А.,
- Миллингтон К.А.,
- Бакир М.,
- и др.
. Влияние вакцинации БЦЖ на риск инфицирования микобактериями туберкулеза у детей с бытовым контактом с туберкулезом: проспективное исследование на базе местных сообществ. Ланцет 2005; 366:1443–51.
- ↵
- Diel R,
- Loddenkemper R,
- Niemann S,
- и др.
. Значение IGRA цельной крови для развития активного туберкулеза — обновление. Am J Respir Crit Care Med . Впервые опубликовано в сети: 27 августа 2010 г. doi:10.1164/rccm.201006-0974OC.
- ↵
- Эйзенхут М,
- Паранджоти С,
- Абубакар I,
- и др.
.
 Вакцинация БЦЖ снижает риск инфицирования микобактериями туберкулеза, выявляемыми с помощью анализа высвобождения гамма-интерферона. Вакцина 2009;27:6116–20.
Вакцинация БЦЖ снижает риск инфицирования микобактериями туберкулеза, выявляемыми с помощью анализа высвобождения гамма-интерферона. Вакцина 2009;27:6116–20. - ↵
- Эриксен Дж.,
- Чоу Дж.Ю.,
- Меллис В.,
- и др.
. Защитный эффект вакцинации БЦЖ при вспышке питомников в 2009 г.: пора пересмотреть порог вакцинации? Thorax 2010;65:1067–71.
- ↵
- Jeremiah K,
- PrayGod G,
- Faurholt-Jepsen D,
- и др.
. Статус прививки БЦЖ может предсказать конверсию мокроты у пациентов с туберкулезом легких: новый взгляд на старую вакцину? Грудная клетка 2010;65:1072–6.
- ↵
- Миллингтон К.А.,
- Гудинг С.,
- Хинкс Т.С.,
- и др.
. Специфические клеточные иммунные профили Mycobacterium tuberculosis предполагают бактериальную персистенцию спустя десятилетия после спонтанного излечения при нелеченном самоизлеченном туберкулезе.
 J Infect Dis 2010;202:10.
J Infect Dis 2010;202:10. - ↵
- Сада-Овалле I,
- Скольд М.,
- Тиан Т,
- и др.
. Альфа-галактозилцерамид как терапевтическое средство при легочной микобактериальной туберкулезной инфекции. Am J Respir Crit Care Med 2010;182:841–7.
- ↵
- Chonde TM,
- Basra D,
- Mfinanga SG,
- и др.
. Национальное исследование устойчивости к противотуберкулезным препаратам в Танзании. Int J Tuberc Lung Dis 2010;14:967–72.
- ↵
- Setia MS,
- Steinmaus C,
- Ho CS,
- и др.
. Роль БЦЖ в профилактике лепры: метаанализ. Lancet Infect Dis 2006; 6:162–70.
- ↵
- Эль-Зейн М.,
- Родитель М.Е.,
- Бенедетти А.
 ,
, - и др.
. Защищает ли вакцинация БЦЖ от развития детской астмы? Систематический обзор и метаанализ эпидемиологических исследований. Int J Epidemiol 2010; 39:469–86.
- ↵
- Niobey FM,
- Duchiade MP,
- Vasconcelos AG,
- и др.
. [Факторы риска смерти от пневмонии у детей в возрасте до 1 года в столичном регионе на юго-востоке Бразилии. Исследование случай-контроль]. Rev Saude Publica 1992; 26: 229–38.
- ↵
- Рот А,
- Густафсон П,
- Нхага А,
- и др.
. Шрам от вакцинации БЦЖ связан с лучшей выживаемостью детей в Гвинее-Бисау. Int J Epidemiol 2005;34:540–7.
- ↵
- Garly ML,
- Martins CL,
- Bale C,
- и др.
.
 Рубец БЦЖ и положительная туберкулиновая реакция связаны со снижением детской смертности в Западной Африке. Неспецифический положительный эффект БЦЖ? Вакцина 2003;21:2782–90.
Рубец БЦЖ и положительная туберкулиновая реакция связаны со снижением детской смертности в Западной Африке. Неспецифический положительный эффект БЦЖ? Вакцина 2003;21:2782–90. - ↵
- Orme IM
. Ахиллесова пята BCG. Туберкулез (Эдинб) . Впервые опубликовано в Интернете: 24 июля 2010 г. doi: 10.1016 / j.tube.2010.06.002.
- ↵
- Абель Б.,
- Тамерис М.,
- Мансур Н.,
- и др.
. Новая противотуберкулезная вакцина AERAS-402 индуцирует устойчивые и полифункциональные CD4+ и CD8+ Т-клетки у взрослых. Am J Respir Crit Care Med 2010;181:1407–17.
- ↵
- Beveridge NE,
- Price DA,
- Casazza JP,
- и др.
. Иммунизация БЦЖ и рекомбинантным MVA85A индуцирует долгоживущие полифункциональные популяции Т-лимфоцитов памяти CD4+, специфичные для Mycobacterium tuberculosis.
 Eur J Immunol 2007; 37:3089–100.
Eur J Immunol 2007; 37:3089–100. - ↵
- Кагина Б.М.,
- Абель Б.,
- Скриба Т.Ж.,
- и др.
. Специфическая частота Т-клеток и профиль экспрессии цитокинов не коррелируют с защитой от туберкулеза после вакцинации новорожденных БЦЖ. Am J Respir Crit Care Med 2010;182:1073–9.
- ↵
- Fjallbrant H,
- Ridell M,
- Larsson LO
. Рубец БЦЖ и туберкулиновая реактивность у детей и взрослых. Scand J Infect Dis 2008;40:387–92.
- ↵
- Friedland IR
. Бустерный эффект повторного туберкулинового тестирования у детей и его связь с вакцинацией БЦЖ. S Afr Med J 1990;77:387–9.
- ↵
- Фариди М.М.,
- Каур С.,
- Кришнамурти С.
 ,
, - и др.
. Тест торможения туберкулиновой конверсии и миграции лейкоцитов после вакцинации БЦЖ у новорожденных. Hum Вакцина 2009;5:690–5.
- ↵
- Джейсон Дж.,
- Арчибальд Л.К.,
- Нваньянву О.К.,
- и др.
. Клинические и иммунные последствия рубцевания прививки Mycobacterium bovis БЦЖ. Infect Immun 2002;70:6188–95.
- ↵
- Рани С.Х.,
- Виджаялакшми В.,
- Сунил К.,
- и др.
. Клеточный иммунитет у детей с рубцовой недостаточностью после вакцинации БЦЖ. Indian Pediatr 1998; 35: 123–7.
Посмотреть реферат
Сноски
Связанные статьи 140186, 134767. ESAT-6/CFP-10 IFN-gamma ELISpot был коммерциализирован дочерней компанией Оксфордского университета (T-SPOT.
 TB, Oxford Immunotec Ltd, Абингдон, Великобритания), в которой Оксфордский университет и AL имеют миноритарные доли капитала и прав к роялти. У СС нет конфликта интересов.
TB, Oxford Immunotec Ltd, Абингдон, Великобритания), в которой Оксфордский университет и AL имеют миноритарные доли капитала и прав к роялти. У СС нет конфликта интересов.Происхождение и экспертная оценка Введено в эксплуатацию; не рецензируемых внешними экспертами.
Статьи по ссылкам
- Туберкулез
Защитный эффект вакцинации БЦЖ при вспышке питомников в 2009 г.: пора пересмотреть порог вакцинации?
Дж Эриксен
Джей И Чоу
В. Меллис
Б Уипп
С Уолтерс
Э. Абрахамсон
I АбубакарГрудная клетка 2010; 65 1067-1071 Впервые опубликовано в сети: 28 октября 2010 г. doi: 10.1136/thx.2010.140186
- Туберкулез
Статус прививки БЦЖ может предсказать конверсию мокроты у пациентов с туберкулезом легких: новый подход к старой вакцине?
Кидола Иеремия
Джордж ПрейГод
Даниэль Форхольт-Джепсен
Хребет Нягося
Аасе Б. Андерсен
Харлин М.С. Гревал
Хенрик ФриисThorax 2010; 65 1072-1076 Впервые опубликовано в сети: 01 октября 2010 г.



 д/в/к введения 500 мкг/20 доз: амп. 5 шт. в компл. с растворителем
д/в/к введения 500 мкг/20 доз: амп. 5 шт. в компл. с растворителем
 Реакция в месте инъекции включает гранулематозные поражения, лимфаденопатию регионарных лимфатических узлов, а также узелки или язвы в месте вакцинации с дренированием свищевых ходов или свищей или без них. Mycobacterium bovis является положительным при получении посева из раны.
Реакция в месте инъекции включает гранулематозные поражения, лимфаденопатию регионарных лимфатических узлов, а также узелки или язвы в месте вакцинации с дренированием свищевых ходов или свищей или без них. Mycobacterium bovis является положительным при получении посева из раны. Ю. Академия наук. 1968 г., 05 сентября; 154 (1): 140-8. [PubMed: 5266317]
Ю. Академия наук. 1968 г., 05 сентября; 154 (1): 140-8. [PubMed: 5266317] Частота повторного заражения туберкулезом после успешного лечения выше, чем частота нового туберкулеза. Am J Respir Crit Care Med. 2005 15 июня; 171 (12): 1430-5. [PubMed: 15831840]
Частота повторного заражения туберкулезом после успешного лечения выше, чем частота нового туберкулеза. Am J Respir Crit Care Med. 2005 15 июня; 171 (12): 1430-5. [PubMed: 15831840] Туберкулез (Эдинб). 2006 ноябрь; 86 (6): 397-403. [PubMed: 165]
Туберкулез (Эдинб). 2006 ноябрь; 86 (6): 397-403. [PubMed: 165] 2014 март; 209(6):887-97. [Бесплатная статья PMC: PMC6392474] [PubMed: 24179111]
2014 март; 209(6):887-97. [Бесплатная статья PMC: PMC6392474] [PubMed: 24179111] Eur Respir J. 2014 янв; 43(1):24-35. [В паблике: 24381321]
Eur Respir J. 2014 янв; 43(1):24-35. [В паблике: 24381321]
 Долгосрочное влияние вакцинации бациллой Кальметта-Герена на туберкулиновые кожные пробы: 55-летнее последующее исследование. Грудь. 2017 авг; 152 (2): 282-294. [PubMed: 28087302]
Долгосрочное влияние вакцинации бациллой Кальметта-Герена на туберкулиновые кожные пробы: 55-летнее последующее исследование. Грудь. 2017 авг; 152 (2): 282-294. [PubMed: 28087302] , Чагулука С.Д., Донован Л., Джарман Э., Кинг Э., Файн ЧП, Докрелл Х.М. Индуцированное БЦЖ усиление интерферон-гамма-ответа на микобактериальные антигены и эффективность вакцинации БЦЖ в Малави и Великобритании: два рандомизированных контролируемых исследования. Ланцет. 2002 20 апреля; 359(9315):1393-401. [PubMed: 11978337]
, Чагулука С.Д., Донован Л., Джарман Э., Кинг Э., Файн ЧП, Докрелл Х.М. Индуцированное БЦЖ усиление интерферон-гамма-ответа на микобактериальные антигены и эффективность вакцинации БЦЖ в Малави и Великобритании: два рандомизированных контролируемых исследования. Ланцет. 2002 20 апреля; 359(9315):1393-401. [PubMed: 11978337] [PubMed: 16214599]
[PubMed: 16214599]
 Int J Tuberc Lung Dis. 2001 авг; 5 (8): 717-23. [В паблике: 11495262]
Int J Tuberc Lung Dis. 2001 авг; 5 (8): 717-23. [В паблике: 11495262]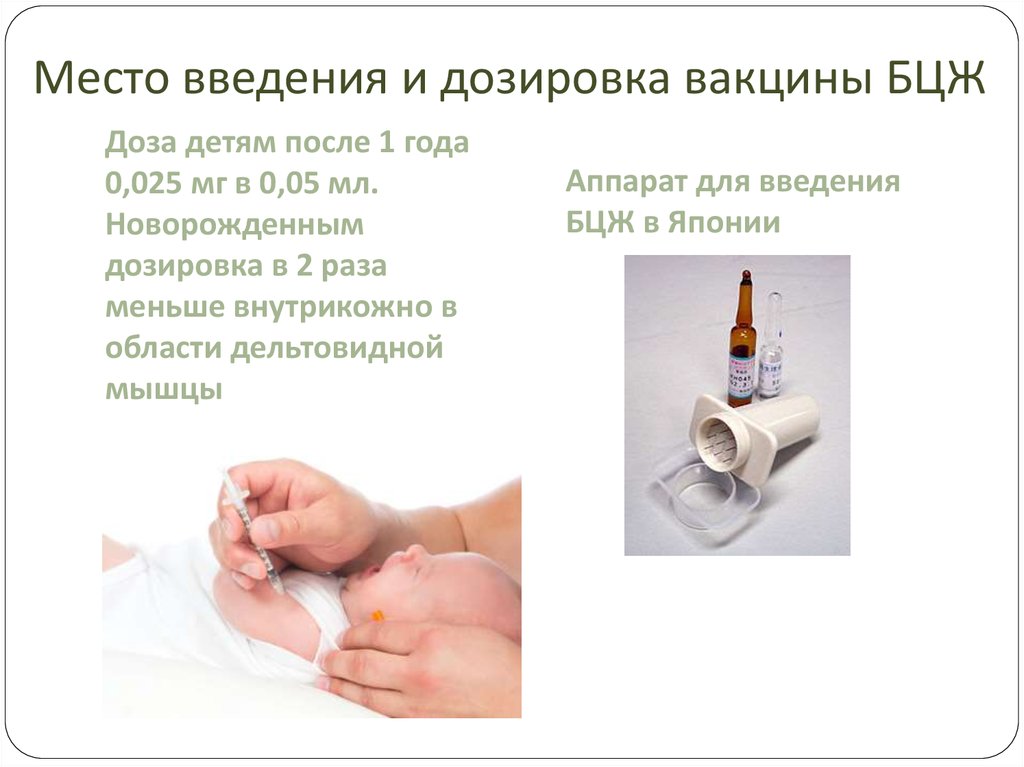 lalvani{at}imperial.ac.uk
lalvani{at}imperial.ac.uk Защитный эффект вакцинации БЦЖ на основании патологоанатомических исследований. Бугорок 1979; 60: 225–31.
Защитный эффект вакцинации БЦЖ на основании патологоанатомических исследований. Бугорок 1979; 60: 225–31.  Вакцинация БЦЖ снижает риск инфицирования микобактериями туберкулеза, выявляемыми с помощью анализа высвобождения гамма-интерферона. Вакцина 2009;27:6116–20.
Вакцинация БЦЖ снижает риск инфицирования микобактериями туберкулеза, выявляемыми с помощью анализа высвобождения гамма-интерферона. Вакцина 2009;27:6116–20.  J Infect Dis 2010;202:10.
J Infect Dis 2010;202:10.  ,
, Рубец БЦЖ и положительная туберкулиновая реакция связаны со снижением детской смертности в Западной Африке. Неспецифический положительный эффект БЦЖ? Вакцина 2003;21:2782–90.
Рубец БЦЖ и положительная туберкулиновая реакция связаны со снижением детской смертности в Западной Африке. Неспецифический положительный эффект БЦЖ? Вакцина 2003;21:2782–90.  Eur J Immunol 2007; 37:3089–100.
Eur J Immunol 2007; 37:3089–100.  ,
, TB, Oxford Immunotec Ltd, Абингдон, Великобритания), в которой Оксфордский университет и AL имеют миноритарные доли капитала и прав к роялти. У СС нет конфликта интересов.
TB, Oxford Immunotec Ltd, Абингдон, Великобритания), в которой Оксфордский университет и AL имеют миноритарные доли капитала и прав к роялти. У СС нет конфликта интересов.