Содержание
Контроль за производством вакцин . Для любознательных. Инфекционные заболевания. Специалисты о прививках
Вакцины и схемы введения
Рекомендуемые материалы
Прививки для детей: к вопросу о безопасности
Существующая в Российской Федерации система надзора за качеством вакцин основана не только на контроле конечной продукции, но, прежде всего, на контроле производства, гарантирующего выпуск безопасных вакцин.
Государственный контроль
В соответствии с рекомендациями ВОЗ, каждое государство, даже не производящее вакцины, должно иметь национальный орган контроля МИБП.
Постановлением Правительства России функции национального органа контроля, отвечающего за качество вакцин, возложены на ФГБУ «Научный центр экспертизы средств медицинского применения» Минздрава России.
Центр оценивает разрабатываемые препараты и сертифицирует серии выпущенных продуктов. За качество вакцин отвечает разработчик и производитель. Качество вакцин, находящихся в обороте, мониторит Росздравнадзор.
Соответствие условий производства требованиям GMP (лицензирование предприятий) под эгидой Минпромторга осуществляет ФГУ «Государственный институт лекарственных средств и надлежащих практик».
Система оценки безопасности вакцин включает 5 уровней контроля:
- испытание новых вакцин разработчиком и национальным органом контроля
- контроль вакцин на производстве
- сертификация серий вакцин ФГБУ «Научный центр экспертизы средств медицинского применения» Минздрава России
- инспектирование предприятий
- госконтроль соответствия качества вакцин на местах их применения.
В отличие от многих стран в России существует система государственных испытаний, которые проводятся под руководством контрольного института с применением препаратов сравнения, двойного слепого метода и других принципов контролируемых испытаний без участия разработчиков.
Национальный орган контроля МИБП имеет право запрещать применение вакцины при несоответствии ее качества установленным требованиям, переводить контроль вакцины с выборочного на сплошной, приостанавливать действие ранее выданного сертификата на право производства вакцины, представлять Минздраву России материалы для решения вопроса о прекращении производства устаревших вакцин или вакцин, не соответствующих по качеству установленным требованиям.
Испытания
Вакцины оценивают сначала на взрослых людях, а затем — на детях. При этом используется принцип информированного согласия лиц, участвующих в испытаниях вакцин.
Основные требования к проведению испытаний вакцин:
Доклинические
- процесс тщательного и всестороннего изучения препарата на экспериментальном уровне, в результате которого подтверждается максимальная безопасность при использовании вакцин для людей.
Клинические
- проводятся с участием людей, по их результатам решается вопрос о целесообразности применения препарата в практике здравоохранения.
В РФ принят закон о лекарственных средствах, в котором определены этические и правовые аспекты проведения клинических испытаний. Протокол клинических испытаний проходит экспертную оценку различными учреждениями и специалистами и на конечном этапе одобряется Комитетом по этике при Минздраве России.
При экспертизе протоколов клинических испытаний этическими комитетами на первом месте стоят интересы участников испытаний (пациентов и врачей), а не цель испытаний.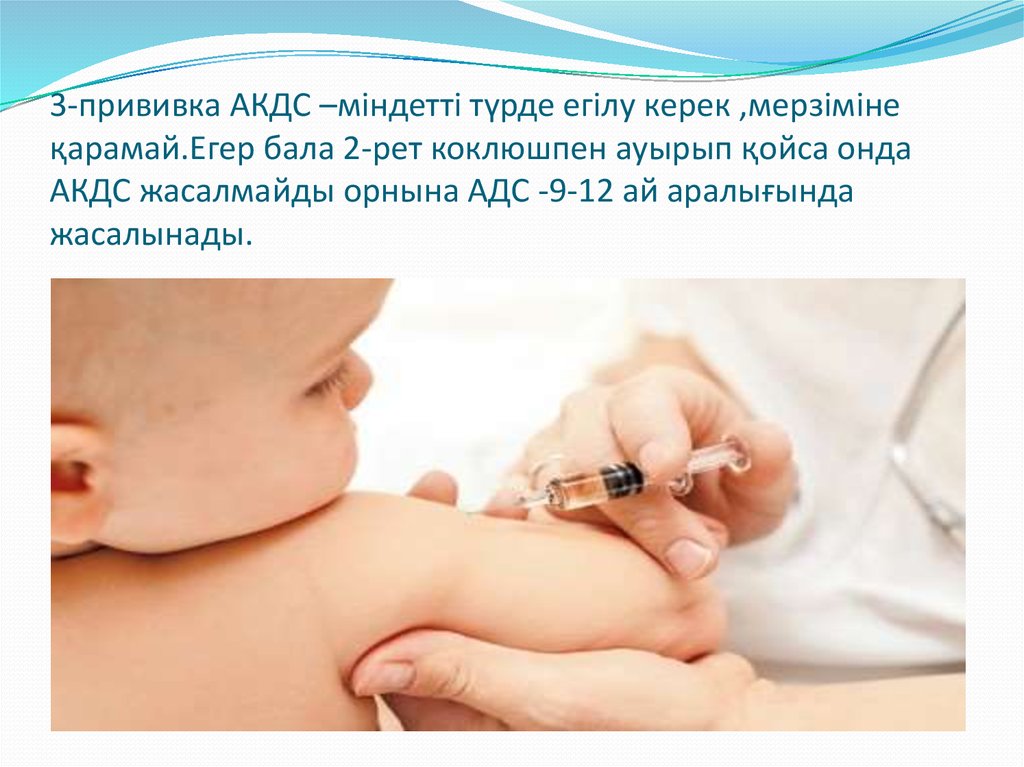
Каждый этап проводится очень тщательно. В зависимости от заболевания процесс от открытия до клинического широкомасштабного испытания вакцин может длиться 10 и более лет. Число испытуемых составляет тысячи человек, а длительность наблюдения определяется, исходя из результатов, полученных на предыдущих этапах испытаний, и обычно ограничивается 1-2 годами (но не менее 6 месяцев).
Транспортировка
При транспортировании и хранении вакцин необходимо соблюдать условия, обеспечивающие их сохранность от механических повреждений и неблагоприятного воздействия температуры окружающей среды.
Транспортирование вакцин должно осуществляться в специальных контейнерах с термоиндикаторами или авторефрижераторным транспортом при температуре от +2 до +8 C.
Рекомендуемые материалы
Прививки для детей: к вопросу о безопасности
Gel-Pac® позволяет проводить инкубаторную вакцинацию против ИБК и кокцидиоза в сочетании
- Во-первых, природные неорганические минералы в воде, например железо, повреждают пальцеобразную внешнюю поверхность вакцины, делая ее неспособной генерировать эффективную иммунитет.

- Во-вторых, некоторые органические соединения, такие как нитраты в природных источниках воды, могут окислять вакцину, инактивируя ее.
- В-третьих, некоторые элементы, добавленные для улучшения качества воды, разрушат живую вакцину. К ним относятся хлор, перекись и озон.
«Gel-Pac меняет будущее инкубаторной вакцинации».
«Больше не нужно замачивать птенцов».
Помимо удобства и экономии труда, распыление съедобной кокковой вакцины признано за более сильную и однородную защиту от кокков, чем аэрозольные спреи, которые не так легко и эффективно потребляются вылупившимися птенцами. Ооцисты кокковой вакцины, как и другие пероральные активные вещества, лучше всего действуют, когда они находятся в птице, а не на птице.
Тестирование на совместимость
Чтобы профилировать стабильность вакцины против ИБ в сочетании с вакциной кокков, Lasher Associates 1 измерила остаточные титры вакцины против ИБ в суспензиях вакцины кокков, смешанных в соответствии с концентрацией, указанной на этикетке, для распыления в инкубаторе. Используемое титрование IB было тем, которое Министерство сельского хозяйства США требует от производителей вакцин в Разделе 9 Свода федеральных правил §113.329. Титрование проводилось с использованием яиц-эмбрионов, свободных от специфических патогенов (SPF) 2 , в трехкратной повторности с отдельными разведениями для каждого титрования. Метод Спирмена-Карбера был использован для расчета EID 50 на дозу вакцины 0,2 мл.
Используемое титрование IB было тем, которое Министерство сельского хозяйства США требует от производителей вакцин в Разделе 9 Свода федеральных правил §113.329. Титрование проводилось с использованием яиц-эмбрионов, свободных от специфических патогенов (SPF) 2 , в трехкратной повторности с отдельными разведениями для каждого титрования. Метод Спирмена-Карбера был использован для расчета EID 50 на дозу вакцины 0,2 мл.
Одну ампулу имеющейся в продаже живой вакцины против ИБ, MILDVAC ® – ARK 3 (10 000 доз), разводили в 10 мл воды, а затем разбавляли до концентрации 5 доз на мл в стерильном дистиллированном (DI ) воды, в деионизированной воде, содержащей 5 доз LIVACOX ® T4 на мл, и в растворе Gel-Pac, содержащем 5 доз LIVACOX T на мл. Вакцину в воде немедленно титровали для количественного определения исходной активности ИБ в качестве положительного контроля. Вакцину в двух других препаратах титровали через 15 минут, чтобы сравнить краткосрочную стабильность, а суспензию Gel-Pac снова титровали через 30 и 60 минут, чтобы оценить сохранение активности ИБ в течение типичного времени пребывания в суспензии (см. рисунок). .
рисунок). .
Результаты и обсуждение
Стремясь повысить эффективность работы инкубатория, многие компании пытаются комбинировать две или более вакцины для распыления после вывода. Комбинируя вакцины, вылупившиеся детеныши не подвергаются многократному распылению, а количество распылительных шкафов с сопутствующими требованиями к обслуживанию сокращается. Двумя широко применяемыми распыляемыми вакцинами являются ИБ и кокцидиоз. Некоторые вакцины от кокцидиоза сохраняются в растворе сильнодействующего консерванта. Когда любой из них комбинируют с живой вакциной против ИБ, титр последней снижается (предыдущие неопубликованные результаты). Цель этого исследования состояла в том, чтобы определить, можно ли использовать Gel-Pac для противодействия эффекту вакцины против кокцидиоза и поддержания активности вакцины против ИБ.
Как и ожидалось на основании предыдущих титрований с комбинированными вакцинами, воздействие только одной кокцидиозной вакцины уничтожило вакцинный вирус ИБ до того, как был титрован самый ранний образец. Менее чем за 15 минут вакцина против ИБ значительно разлагалась, снижая титр по крайней мере на 2,8 log в присутствии кокковой вакцины, если только она не стабилизировалась с помощью Gel-Pac. Титр ИБ снизился с 10 3,3 EID 50 /доза 0,2 мл в начале до 10 0,5 EID 50 в растворе с нестабилизированной кокковой вакциной (более 9потеря 9%). В тот же 15-минутный момент времени Gel-Pac защитил вакцину против ИБК от этой инактивации, сохранив титр на уровне 10 3,1 EID 50 мл и продлив защитную активность после окончания 60-минутного интервала, дольше чем обычно требуется птицам для потребления гелевых капель вакцины .
Менее чем за 15 минут вакцина против ИБ значительно разлагалась, снижая титр по крайней мере на 2,8 log в присутствии кокковой вакцины, если только она не стабилизировалась с помощью Gel-Pac. Титр ИБ снизился с 10 3,3 EID 50 /доза 0,2 мл в начале до 10 0,5 EID 50 в растворе с нестабилизированной кокковой вакциной (более 9потеря 9%). В тот же 15-минутный момент времени Gel-Pac защитил вакцину против ИБК от этой инактивации, сохранив титр на уровне 10 3,1 EID 50 мл и продлив защитную активность после окончания 60-минутного интервала, дольше чем обычно требуется птицам для потребления гелевых капель вакцины .
Изменение формы
Птицеводческая промышленность во всем мире наблюдает, как ее интегрированные компании возлагают больше ответственности за здоровье птицы на свои инкубаторы. Это проявляется в таких методах, как вакцинация in ovo, раннее введение пробиотиков перед посадкой и брудерное выращивание в инкубаторе. Инкубаторы работают над поддержанием эффективности операций, выполняя эти все более сложные обязанности. Увеличение количества прививок и пероральных добавок, вводимых в инкубатории, естественно, побудило ветеринаров искать способы объединить их в одно применение. Распыленные аэрозольные спреи, содержащие эти орально-активные ингредиенты, не идеальны, потому что, кроме охлаждения птиц с помощью нескольких спреев, птицы не могут полностью потреблять добавки, пропитанные их влажными перьями. Gel-Pac объединяет пероральные добавки и вакцины в одном удобном съедобном гелевом спрее . Стабилизаторы позволяют безопасно приготовить гелевую суспензию из водопроводной воды инкубатория или колодезной воды, не рискуя инактивировать кокковые вакцины, а однородно суспендированные вакцины не требуют постоянного перемешивания, как это делают жидкие спреи. Gel-Pac меняет систему распыления в инкубаториях. Теперь открывается больше возможностей для пероральных активных веществ благодаря более удобным и эффективным комбинациям, которые теперь действительно лучше сочетаются друг с другом.
Инкубаторы работают над поддержанием эффективности операций, выполняя эти все более сложные обязанности. Увеличение количества прививок и пероральных добавок, вводимых в инкубатории, естественно, побудило ветеринаров искать способы объединить их в одно применение. Распыленные аэрозольные спреи, содержащие эти орально-активные ингредиенты, не идеальны, потому что, кроме охлаждения птиц с помощью нескольких спреев, птицы не могут полностью потреблять добавки, пропитанные их влажными перьями. Gel-Pac объединяет пероральные добавки и вакцины в одном удобном съедобном гелевом спрее . Стабилизаторы позволяют безопасно приготовить гелевую суспензию из водопроводной воды инкубатория или колодезной воды, не рискуя инактивировать кокковые вакцины, а однородно суспендированные вакцины не требуют постоянного перемешивания, как это делают жидкие спреи. Gel-Pac меняет систему распыления в инкубаториях. Теперь открывается больше возможностей для пероральных активных веществ благодаря более удобным и эффективным комбинациям, которые теперь действительно лучше сочетаются друг с другом.
Каталожные номера
1 В.С. Дэвис, Lasher Associates, Inc., Миллсборо, Делавэр, США.
2 Чарльз-Ривер, Северный Франклин, Коннектикут, США.
3 MILDVAC ® – ARK, 10 000 доз на 10 мл флакон, зарегистрированный товарный знак Merck Animal Health. Штаб-квартира корпорации в США: 2 Gerald Farms, Мэдисон, Нью-Джерси, США.
4 ЛИВАКОКС ® Т, 5000 доз во флаконе 50 мл в 1,0 % растворе хлорамина Б, зарегистрированная торговая марка БИОФАРМ, НИИ биофармацевтики и ветеринарных препаратов, Похори-Чотун 90, 254 49 Йилове-у-Праги, Чехия.
Gel-Pac ® is a registered trademark of Animal Science Products, Inc., Nacogdoches, Texas, USA
Package Inserts and Manufacturers for some US Licensed Vaccines and Immunoglobulins
| VACCINE ▼ | ANTIGENS ▼ | ПРОИЗВОДИТЕЛЬ ▼ | ПОСЛЕДНИЙ ИП ▼ | ||||||
|---|---|---|---|---|---|---|---|---|---|
| BioThrax | Вакцина против сибирской язвы адсорбированная | Emergent BioSolutions | 2015 – 11 | ||||||
| BCG Vaccine | Bacillus of Calmette and Guerin (BCG) | Merck | 2021 – 05 | ||||||
| Hiberix | Tetanus Toxoid Conjugate | GlaxoSmithKline | 2019 – 05 | ||||||
| Фиолетовый/серый колпачок Comirnaty | COVID-19, мРНК | BioNTech Manufacturing GmbH | 2021 – 12 | ||||||
| SPIKEVAX | COVID-19, мРНК | 2022- 01 | |||||||
| DT | Diphtheria and Tetanus Toxoids | Sanofi Pasteur | 2019 – 03 | ||||||
| KINRIX | Diphtheria and Tetanus Toxoids and Acellular Pertussis Adsorbed and Inactivated Poliovirus | GlaxoSmithKline | 2019 – 11 | ||||||
| Quadracel | Дифтерийно-столбнячный анатоксин и бесклеточный коклюш Адсорбированный и инактивированный полиовирус | Sanofi Pasteur | 2021 – 02 | ||||||
| Vaxelis | Diphtheria and Tetanus Toxoids and Acellular Pertussis Adsorbed, Inactivated Poliovirus, Haemophilus b Conjugate [Meningococcal Protein Conjugate] and Hepatitis B [Recombinant] Vaccine | Merck/Sanofi Pasteur | 2021 – 11 | ||||||
| Даптацел | Дифтерия, столбняк, коклюш | Санофи Пастер | 2020 – 02 | ||||||
| Инф0123 | Diphtheria, Tetanus, (acellular) Pertussis | GlaxoSmithKline | 2019 – 11 | ||||||
| Pediarix | Diphtheria, Tetanus, Pertussis, Hepatitis B and Poliovirus | GlaxoSmithKline | 2019 – 11 | ||||||
| Pentacel | Дифтерия, столбняк, коклюш, полиомиелит и Haemophilus influenzae типа b | Санофи Пастер | 2021 – 02 | ||||||
| PedvaxHIB | Haemophilus influenzae type b (PRP-OMP) | Merck | 2020 – 02 | ||||||
| ActHIB | Haemophilus influenzae type b (PRP-T) | Sanofi Pasteur | 2019 – 06 | ||||||
| Havrix | Hepatitis A | GlaxoSmithKline | 2021 – 12 | ||||||
| Vaqta | Hepatitis A (inactivated) | Merck | 2020 – 10 | ||||||
| Twinrix | Hepatitis A and B | GlaxoSmithKline | Dec 2018 | ||||||
| Engerix-B | Hepatitis B | GlaxoSmithKline | Jun 2021 | ||||||
| Heplisav-B | Hepatitis B | Dynavax | May 2020 | ||||||
| PREHEVBRIO | Гепатит В (рекомбинантный) | VBI Vaccines (Делавэр) Инк. 0123 0123 | Feb 2020 | ||||||
| Gardasil | Human Papillomavirus (Types 6, 11, 16, and 18) | Merck | Apr 2015 | ||||||
| Gardasil 9 | Human Papillomavirus (Types 6, 11, 16, and 18) | Merck | август 2021 | ||||||
| Флузона внутридермальный квадроцик-20 Formula) | Seqirus | Mar 2019 | |||||||
| Fluzone Quad | Influenza (2019-20 Formula) | Sanofi Pasteur | Jul 2019 | ||||||
| Fluad Quad | Influenza (2021-22 Formula) | Seqirus | Jul 2021 | ||||||
| Fluarix Quad | Influenza (2021-22 Formula) | GlaxoSmithKline | Jul 2021 | ||||||
| Flublok Quad | Influenza (2021-22 Formula) | Protein Sciences | Jul 2021 | ||||||
| Flucelvax Quad | Influenza (2021-22 Formula) | Seqirus | Oct 2021 | ||||||
| FluLaval Quad | Influenza (2021-22 Formula) | ID Biomedical | Jul 2021 | ||||||
| FluMist Quad | Influenza (2021-22 Formula) | AstraZeneca | Aug 2021 | ||||||
| Fluzone High-Dose Quad | Influenza (2021-22 Formula) | Sanofi Pasteur | Jul 2021 | ||||||
| Ixiaro | Japanese Encephalitis | Valneva | Sep 2018 | ||||||
| M-M-R II | Measles, Mumps, Rubella (live) | Merck | Dec 2020 | ||||||
| Priorix | Корь, эпидемический паротит, краснуха (живой) | GlaxoSmithKline | июнь 2022 г. | ||||||
| ProQuad | Корь, эпидемический паротит, краснуха и варикоз | Apr 2021 | |||||||
| Menveo | Meningococcal (Groups A,C,Y and W-135) | GlaxoSmithKline | Jul 2020 | ||||||
| MenQuadfi | Meningococcal (Groups A,C,Y,W ) Conjugate | Sanofi Pasteur | Oct 2021 | ||||||
| Menactra | Meningococcal (Groups A,C,Y,W-135) Conjugate | Sanofi Pasteur | Jul 2019 | ||||||
| Menactra | Meningococcal (Groups A ,C,Y,W-135) Полисахаридный конъюгат дифтерийного анатоксина | Sanofi Pasteur | июля 2019 | ||||||
| Menomune-A/C/Y/W-135 | Meningococcal (Polysachcharid | ||||||||
| Trumenba | Meningococcal Group B | Wyeth/Pfizer | Nov 2021 | ||||||
| Bexsero | Meningococcal Group B | GlaxoSmithKline | Jan 2022 | ||||||
| Pneumovax 23 | Pneumococcal (polysaccharide) | Merck | Apr 2021 | ||||||
| Prevnar 13 | Pneumococcal 13-valent Conjugate Vaccine | Wyeth/Pfizer | Jul 2019 | ||||||
| Vaxneuvance | Pneumococcal 15-valent Conjugate Vaccine | Merck | 2021 | ||||||
| Prevnar 20 | Пневмококковая 20-валентная конъюгированная вакцина | Wyeth/Pfizer | Июнь 2021 | IPOL | Polio (inactivated) | Sanofi Pasteur | May 2020 | ||
| RabAvert | Rabies (PCEC) | GlaxoSmithKline | Sep 2019 | ||||||
| Imogam Rabies-HT | Rabies Immune Globulin | Санофи Пастер | декабрь 2020 г. | ||||||
| Имовакс против бешенства | Вакцина против бешенства (HDCV) | Санофи Пастер | декабрь 2019 г. | 0123 | Rotavirus Vaccine, Live, Oral, | GlaxoSmithKline | Nov 2019 | ||
| RotaTeq | Rotavirus Vaccine, Live, Oral, Pentavalent | Merck | Aug 2020 | ||||||
| ACAM2000 | Smallpox (Vaccinia) | Emergent Product Development | Март 2018 г. | ||||||
| JYNNEOS | Оспа и оспа обезьян | Bavarian Nordic A/S | Июнь 2021 г. | 3 | 3 | 20122 TDVAX | Tetanus and Diphtheria Toxoids Adsorbed | Mass Biol Labs | Sep 2018 |
| Tenivac | Tetanus and Diptheria Toxoids Adsorbed | Sanofi Pasteur | Dec 2019 | ||||||
| Adacel | Tetanus toxoid, reduced Diphtheria Токсоид, бесклеточная коклюшная вакцина, адсорбированная | Санофи Пастер | Декабрь 2020 г.
|

